Nonlogam

Ekstrak tabel periodik yang menunjukkan seberapa sering setiap unsur diklasifikasikan sebagai nonlogam:
14 secara efektif selalu[n 1] 3 sering[n 2] 6 kadang-kadang (metaloid)[n 3]
Logam terdekat ditampilkan dalam fon abu-abu.[n 4]
Tidak ada definisi yang tepat dari nonlogam; unsur mana yang dihitung seperti ini bervariasi.
Hidrogen biasanya berada di golongan 1 (sesuai tabel lengkap di bawah) tetapi bisa juga di golongan 17 (seperti ekstrak di atas).[n 5]
| ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ |
| ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ ▉ |
Dalam kimia, nonlogam adalah sebuah unsur kimia yang umumnya tidak memiliki sifat logam yang dominan; mereka berkisar dari gas tak berwarna (seperti hidrogen) hingga padatan mengkilap dengan titik lebur yang tinggi (seperti boron). Elektron pada nonlogam berperilaku berbeda dari elektron pada logam. Dengan beberapa pengecualian, nonlogam tetap pada tempatnya, sehingga nonlogam biasanya menjadi konduktor panas dan listrik yang buruk serta rapuh saat berbentuk padat. Elektron dalam logam umumnya bergerak bebas dan inilah mengapa logam adalah konduktor yang baik dan sebagian besar mudah diratakan menjadi lembaran dan ditarik menjadi kabel. Atom nonlogam memiliki keelektronegatifan sedang hingga tinggi; mereka cenderung menarik elektron dalam reaksi kimia dan membentuk senyawa asam.
Dua nonlogam, hidrogen dan helium, menyusun sekitar 99% materi biasa di alam semesta teramati berdasarkan massa. Lima unsur nonlogam, hidrogen, karbon, nitrogen, oksigen, dan silikon, secara besar membentuk kerak Bumi, atmosfer, samudra, dan biosfer.
Sebagian besar nonlogam memiliki peran atau kegunaan biologis, teknologi, atau domestik. Organisme hidup hampir seluruhnya terdiri dari hidrogen, oksigen, karbon, dan nitrogen. Hampir semua nonlogam memiliki kegunaan tersendiri dalam pengobatan dan farmasi; pencahayaan dan laser; serta barang-barang rumah tangga.
Walaupun istilah nonlogam berasal dari setidaknya tahun 1566, tidak ada definisi pasti yang disepakati secara luas mengenai nonlogam. Beberapa unsur memiliki campuran yang ditandai dari sifat logam dan nonlogam; mana dari kasus batas ini yang dihitung sebagai nonlogam dapat bervariasi tergantung pada kriteria klasifikasinya. Empat belas unsur secara efektif selalu dikenali sebagai nonlogam, dan hingga sekitar sembilan unsur lagi kadang-kadang ditambahkan, seperti yang ditunjukkan pada ekstrak tabel periodik terlampir.
Definisi dan unsur yang berlaku[sunting | sunting sumber]

Nonlogam adalah sebuah unsur kimia yang memiliki, di antara sifat-sifat lainnya, massa jenis yang relatif rendah dan keelektronegatifan sedang hingga tinggi. Secara umum, mereka tidak memiliki atribut logan lebih banyak, seperti kilau, deformabilitas, konduktivitas termal dan listrik yang baik, serta keelektronegatifan rendah.[11] Karena tidak ada definisi yang tepat mengenai nonlogam,[10][12][13] beberapa variasi mungkin ditemukan di antara sumber-sumber tentang unsur mana yang diklasifikasikan sebagai nonlogam. Keputusan yang terlibat tergantung pada properti atau properti mana yang dianggap paling menunjukkan karakter nonlogam atau logam.[14]
Meskipun Steudel,[15] pada tahun 2020, mengakui dua puluh tiga unsur sebagai nonlogam, daftar semacam ini terbuka untuk ditantang.[1] Empat belas unsur yang secara efektif selalu diakui sebagai nonlogam adalah hidrogen, oksigen, nitrogen, dan belerang; halogen yang korosif fluorin, klorin, bromin, dan iodin; dan gas mulia helium, neon, argon, kripton, xenon, dan radon; lihat e.g. Larrañaga dkk.[1] Meskipun penulis yang sama mengakui karbon, fosforus dan selenium sebagai nonlogam, Vernon[2] sebelumnya telah melaporkan bahwa ketiga unsur ini kadang-kadang dihitung sebagai metaloid. Unsur-unsur yang biasa dikenal sebagai metaloid yaitu boron; silikon dan germanium; arsen dan antimon; serta telurium kadang-kadang dihitung sebagai kelas perantara antara logam dan nonlogam ketika kriteria yang digunakan untuk membedakan antara logam dan nonlogam tidak dapat disimpulkan.[16] Di lain waktu mereka dihitung sebagai nonlogam berdasarkan sifat kimia nonlogamnya.[4]
Dari 118 unsur yang telah diketahui,[17] 23 unsur yang dapat dianggap sebagai nonlogam beberapa kali kalah jumlah dengan logam.[18] Astatin, halogen kelima, sering diabaikan karena kelangkaannya dan radioaktivitasnya yang intens;[19] teori dan bukti eksperimental menunjukkan bahwa ia adalah logam.[20] Unsur superberat kopernisium (Z = 112), flerovium (114), dan oganeson (118) dapat berubah menjadi nonlogam; status mereka yang sebenarnya belum dikonfirmasi.[21]
Sifat umum[sunting | sunting sumber]
Fisik[sunting | sunting sumber]
dari beberapa unsur nonlogam
Secara lahiriah, sekitar setengah dari unsur nonlogam adalah gas berwarna atau tidak berwarna; sebagian besar sisanya adalah padatan mengkilap. Bromin, satu-satunya cairan, sangat mudah menguap sehingga biasanya ditutupi oleh lapisan asapnya; belerang adalah satu-satunya nonlogam padat berwarna. Fluida nonlogam memiliki massa jenis, titik lebur dan titik didih yang sangat rendah, dan merupakan penghantar panas dan listrik yang buruk.[22] Unsur nonlogam padat memiliki massa jenis rendah, rapuh dengan kekuatan mekanik dan struktural yang rendah,[23] dan konduktor yang buruk hingga baik.[n 8]
Struktur internal yang bervariasi dan susunan ikatan nonlogam menjelaskan perbedaan bentuk mereka. Mereka yang ada sebagai atom diskrit (misalnya xenon) atau molekul (misalnya oksigen, belerang, bromin) cenderung memiliki titik lebur dan titik didih yang rendah karena mereka disatukan oleh gaya dispersi London yang lemah yang bekerja di antara atom atau molekulnya.[27] Banyak nonlogam yang berbentuk gas pada suhu kamar. Nonlogam yang membentuk struktur raksasa, seperti rantai hingga 1.000 atom (misalnya selenium),[28] lembaran (misalnya karbon), atau kisi 3D (misalnya silikon), memiliki titik lebur dan titik didih yang lebih tinggi, karena dibutuhkan lebih banyak energi untuk mengalahkan ikatan kovalen yang lebih kuat; mereka semua padat. Mereka yang lebih dekat ke sisi kiri tabel periodik, atau lebih jauh ke bawah kolom, sering memiliki beberapa interaksi logam yang lemah antara molekul, rantai, atau lapisan mereka, konsisten dengan kedekatannya dengan logam; ini terjadi pada boron,[29] karbon,[30] fosforus,[31] arsen,[32] selenium,[33] antimon,[34] telurium,[35] dan iodin.[36]
Konduktivitas listrik dan termal nonlogam serta sifat rapuh dari nonlogam padat juga terkait dengan pengaturan internal mereka. Sedangkan konduktivitas dan plastisitas (kelenturan, keuletan) yang baik biasanya dikaitkan dengan keberadaan elektron yang bergerak bebas dan terdistribusi secara merata dalam logam[37] elektron dalam nonlogam biasanya tidak memiliki mobilitas seperti itu.[38] Di antara unsur-unsur nonlogam, konduktivitas listrik dan termal yang baik hanya terjadi pada karbon, arsen, dan antimon.[n 9] Konduktivitas termal yang baik sebaliknya hanya terjadi pada boron, silikon, fosforus, dan germanium;[24] konduktivitas tersebut ditransmisikan melalui getaran kristal kisi dari unsur-unsur ini.[39] Konduktivitas listrik sedang terjadi pada boron, silikon, fosforus, germanium, selenium, telurium, dan iodin.[n 10] Plastisitas terjadi dalam keadaan terbatas hanya pada karbon, fosforus, belerang, dan selenium.[n 11]
Perbedaan fisik antara logam dan nonlogam muncul dari kekuatan atom internal dan eksternal. Secara internal, muatan positif yang timbul dari proton dalam inti atom bertindak untuk menahan elektron terluar atom pada tempatnya. Secara eksternal, elektron yang sama tunduk pada gaya tarik menarik dari proton di atom terdekat. Ketika gaya eksternal lebih besar dari, atau sama dengan, gaya internal, elektron terluar diperkirakan menjadi bebas untuk bergerak di antara atom, dan sifat logam diprediksi muncul. Jika tidak, maka sifat nonlogamlah yang diperkirakan muncul.[47]
Kimia[sunting | sunting sumber]
| Aspek | Logam | Nonlogam |
|---|---|---|
| Elektro- negativitas |
Lebih rendah dari nonlogam, dengan beberapa pengecualian[49] |
Sedang hingga sangat tinggi |
| Ikatan kimia | ||
| Jarang terbentuk ikatan kovalen | Sering membentuk ikatan kovalen | |
| Ikatan logam (paduan) antar logam | Ikatan kovalen antara nonlogam | |
| Ikatan ionik antara nonlogam dan logam | ||
| Bilangan oksidasi |
Positif | Negatif atau positif |
| Oksida | Basa dalam oksida yang lebih rendah; semakin asam dalam oksida yang lebih tinggi | Asam; tidak pernah basa[50] |
| Dalam larutan berair[51] |
Eksis sebagai kation | Eksis sebagai anion atau oksianion |
Nonlogam memiliki nilai elektronegativitas sedang hingga tinggi[52] dan, dalam reaksi kimia, cenderung membentuk senyawa asam. Misalnya, nonlogam padat (termasuk metaloid) bereaksi dengan asam nitrat untuk membentuk antara asam, atau oksida yang bersifat asam atau memiliki sifat asam yang mendominasi.[n 12]
Mereka cenderung mendapatkan atau berbagi elektron ketika mereka bereaksi, tidak seperti logam yang cenderung menyumbangkan elektron. Lebih khusus, mengingat stabilitas konfigurasi elektron dari gas mulia (yang telah mengisi kulit terluar), nonlogam umumnya memperoleh sejumlah elektron yang cukup untuk memberi mereka konfigurasi elektron dari gas mulia berikutnya sedangkan logam cenderung kehilangan elektron yang cukup untuk meninggalkan mereka dengan konfigurasi elektron dari gas mulia sebelumnya. Untuk unsur nonlogam kecenderungan ini diringkas dalam kaidah duet dan oktet (dan untuk logam ada kaidah 18 elektron yang diikuti dengan kurang ketat).[55]
Secara kuantitatif, nonlogam sebagian besar memiliki energi ionisasi, afinitas elektron, nilai keelektronegatifan, dan potensial reduksi standar yang lebih tinggi daripada logam. Secara umum, semakin tinggi nilai-nilai ini, semakin banyak sifat nonlogam dalam suatu unsur.[56]
Perbedaan kimia antara logam dan nonlogam sebagian besar timbul dari gaya tarik menarik antara muatan inti positif dari atom individu dan elektron terluarnya yang bermuatan negatif. Dari kiri ke kanan melintasi setiap periode tabel periodik, muatan inti meningkat seiring dengan bertambahnya jumlah proton dalam inti atom.[57] Ada reduksi terkait dalam jari-jari atom[58] karena muatan inti yang meningkat menarik elektron terluar lebih dekat ke inti.[59] Dalam logam, efek muatan inti umumnya lebih lemah daripada unsur nonlogam. Dalam ikatan kimia, logam cenderung kehilangan elektron, dan membentuk atom atau ion bermuatan positif atau terpolarisasi sedangkan nonlogam cenderung mendapatkan elektron yang sama karena muatan nuklirnya yang lebih kuat, dan membentuk ion bermuatan negatif atau atom terpolarisasi.[60]
Jumlah senyawa yang dibentuk oleh nonlogam sangatlah banyak.[61] Sepuluh tempat pertama dalam tabel "20 teratas" unsur yang paling sering ditemui dalam 895.501.834 senyawa, sebagaimana tercantum dalam daftar Chemical Abstracts Service untuk 2 November 2021, ditempati oleh nonlogam. Hidrogen, karbon, oksigen, dan nitrogen secara kolektif ditemukan di sebagian besar (80%) senyawa. Silikon, sebuah metaloid, berada di urutan ke-11. Logam dengan nilai tertinggi, dengan frekuensi kemunculan 0,14%, adalah besi, di tempat ke-12.[62] Beberapa contoh senyawa nonlogam adalah: asam borat (H3BO3), digunakan dalam glasir keramik; selenosistein (C3H7NO2Se), asam amino kehidupan ke-21;[63] fosforus sesquisulfida (P4S3), dalam korek api; dan teflon ((C2F4)n),[64] seperti yang digunakan dalam (misalnya) pelapis antilengket untuk panci dan peralatan masak lainnya.
Komplikasi[sunting | sunting sumber]

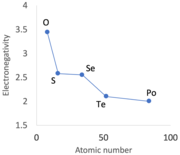
Rumitnya kimia nonlogam adalah anomali yang terlihat pada baris pertama setiap blok tabel periodik. Anomali ini menonjol dalam hidrogen, boron (baik sebagai nonlogam atau metaloid), karbon, nitrogen, oksigen dan fluorin. Di baris selanjutnya, mereka bermanifestasi sebagai periodisitas sekunder atau tren periodik yang tidak seragam yang menuruni sebagian besar gugus blok-p,[65] dan bilangan oksidasi yang tidak biasa pada nonlogam yang lebih berat.
Anomali baris pertama[sunting | sunting sumber]
Dimulai dengan hidrogen, anomali baris pertama sebagian besar muncul dari konfigurasi elektron unsur-unsur yang bersangkutan. Hidrogen terkenal karena berbagai caranya membentuk ikatan. Ia paling sering membentuk ikatan kovalen. Ia dapat kehilangan satu elektronnya dalam larutan berair, meninggalkan proton kosong dengan kekuatan polarisasi yang luar biasa.[66] Ini akibatnya menempel pada pasangan elektron bebas dari atom oksigen dalam molekul air, sehingga membentuk dasar kimia asam-basa.[67] Atom hidrogen dalam suatu molekul dapat membentuk ikatan kedua yang lebih lemah dengan atom atau kelompok atom dalam molekul lain. Ikatan tersebut, "membantu memberikan kepingan salju simetri heksagon mereka, mengikat DNA menjadi heliks ganda; membentuk protein tiga dimensi; dan bahkan menaikkan titik didih air cukup tinggi untuk membuat secangkir teh yang layak."[68]
Hidrogen dan helium, dan boron hingga neon memiliki jari-jari atom yang sangat kecil. Hal ini terjadi karena subkulit 1s dan 2p tidak memiliki analog dalam (yaitu, tidak ada kulit nol dan tidak ada subkulit 1p) dan karena itu mereka tidak mengalami efek tolakan elektron, tidak seperti subkulit 3p, 4p dan 5p dari unsur yang lebih berat.[69] Energi ionisasi dan elektronegativitas di antara unsur-unsur ini akibatnya lebih tinggi daripada yang diperkirakan, dengan memperhatikan tren periodik. Jari-jari atom karbon, nitrogen, dan oksigen yang kecil memfasilitasi pembentukan ikatan rangkap atau rangkap tiga.[70]
Meskipun biasanya diharapkan bahwa hidrogen dan helium, atas dasar konsistensi konfigurasi elektron, akan ditempatkan di atas unsur blok-s, anomali baris pertama dalam dua unsur ini cukup kuat untuk menjamin penempatan alternatif. Hidrogen kadang-kadang ditempatkan di atas fluorin, di golongan 17 dan bukan di atas litium di golongan 1. Helium secara teratur ditempatkan di atas neon, di golongan 18, dan bukan di atas berilium, di golongan 2.[71]
Periodisitas sekunder[sunting | sunting sumber]
Segera setelah baris pertama logam blok-d, skandium hingga seng, elektron 3d dalam unsur blok-p yaitu galium (logam), germanium, arsen, selenium, dan bromin, tidak efektif dalam melindungi peningkatan muatan inti positif. Efek serupa menyertai penampilan empat belas logam blok-f antara barium dan lutesium, yang pada akhirnya menghasilkan jari-jari atom yang lebih kecil dari yang diperkirakan untuk unsur-unsur mulai dari hafnium (Hf) dan seterusnya.[72] Hasil akhirnya, terutama untuk unsur golongan 13–15, adalah bahwa ada pergantian dalam beberapa tren periodik yang turun ke golongan 13 hingga 17.[73]
Bilangan oksidasi yang tidak biasa[sunting | sunting sumber]
Jari-jari atom yang lebih besar dari nonlogam golongan 15–18 yang lebih berat memungkinkan bilangan koordinasi massal yang lebih tinggi, dan menghasilkan nilai elektronegativitas yang lebih rendah yang lebih baik menoleransi muatan positif yang lebih tinggi. Unsur-unsur yang terlibat dengan demikian dapat menunjukkan bilangan oksidasi selain yang terendah untuk golongan mereka (yaitu, 3, 2, 1, atau 0) misalnya dalam fosforus pentaklorida (PCl5), belerang heksafluorida (SF6), iodin heptafluorida (IF7), dan xenon difluorida (XeF2).[74]
Subkelas [sunting | sunting sumber]
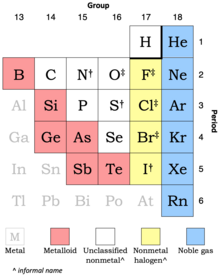
† Zat pengoksidasi cukup kuat ‡ Zat pengoksidasi kuat[n 15]
Pendekatan untuk mengklasifikasikan nonlogam mungkin melibatkan sedikitnya dua subkelas hingga enam atau tujuh. Misalnya, tabel periodik Encyclopædia Britannica mengakui gas mulia, halogen, dan nonlogam lainnya, dan membagi unsur-unsur yang umumnya dikenal sebagai metaloid antara "logam lain" dan "nonlogam lainnya".[86] Tabel periodik Royal Society of Chemistry malah menggunakan warna yang berbeda untuk masing-masing dari delapan golongan utamanya, dan nonlogam dapat ditemukan di tujuh di antaranya.[87]
Dari kanan ke kiri dalam tabel periodik, tiga atau empat jenis nonlogam kurang lebih umum dibedakan. Mereka adalah:
- gas mulia yang relatif lengai;
- satu set unsur halogen yang kuat secara kimiawi—fluorin, klorin, bromin, dan iodin—kadang-kadang disebut sebagai halogen nonlogam[88] (istilah yang digunakan di sini) atau halogen stabil;[89]
- satu set nonlogam yang tidak diklasifikasikan, termasuk unsur-unsur seperti hidrogen, karbon, nitrogen, dan oksigen, tanpa nama kolektif yang dikenal luas; dan
- metaloid nonlogam yang lemah secara kimiawi[90] terkadang dianggap bukan logam dan terkadang tidak.[n 16]
Karena metaloid menempati "wilayah perbatasan",[92] di mana logam bertemu dengan nonlogam, perlakuannya bervariasi dari penulis ke penulis. Beberapa menganggapnya terpisah dari logam dan nonlogam; beberapa menganggapnya sebagai nonlogam[93] atau sebagai subkelas nonlogam.[94] Penulis lain menghitung beberapa nonlogam sebagai logam, misalnya arsen dan antimon, karena kesamaan mereka dengan logam berat.[95][n 17] Metaloid di sini diperlakukan sebagai nonlogam berdasarkan perilaku kimianya, dan untuk tujuan perbandingan.
Selain metaloid, beberapa ketidakjelasan batas dan tumpang tindih (seperti yang terjadi dengan skema klasifikasi pada umumnya)[96] dapat dilihat di antara subkelas nonlogam lainnya. Karbon, fosforus, selenium, dan iodin membatasi metaloid dan menunjukkan beberapa karakter logam, seperti halnya hidrogen. Di antara gas mulia, radon adalah yang paling seperti logam dan mulai menunjukkan beberapa perilaku kationik, yang tidak biasa untuk nonlogam.[97]
Gas mulia[sunting | sunting sumber]

Enam nonlogam diklasifikasikan sebagai gas mulia: helium, neon, argon, kripton, xenon, dan radon radioaktif yang radioaktif. Dalam tabel periodik konvensional mereka menempati kolom paling kanan. Mereka disebut gas mulia karena reaktivitas kimia mereka yang sangat rendah.[98]
Mereka memiliki sifat yang sangat mirip, semuanya tidak berwarna, tidak berbau, dan tidak mudah terbakar. Dengan kulit elektron terluar yang tertutup, gas mulia memiliki gaya tarik menarik antar atom yang lemah sehingga menghasilkan titik lebur dan titik didih yang sangat rendah.[99] Itulah sebabnya mereka semua berbentuk gas dalam kondisi standar, bahkan mereka memiliki massa atom lebih besar daripada banyak unsur yang biasanya padat.[100]
Secara kimia, gas mulia memiliki energi ionisasi yang relatif tinggi, afinitas elektron nol atau negatif, dan keelektronegatifan yang relatif tinggi. Senyawa gas mulia berjumlah ratusan meskipun daftarnya terus bertambah,[101] dengan sebagian besar melibatkan oksigen atau fluorin yang bergabung dengan kripton, xenon, atau radon.[102]
Dalam tabel periodik, analogi dapat ditarik antara gas mulia dan logam mulia seperti platina dan emas, dengan emas juga enggan untuk masuk ke dalam kombinasi kimia.[103] Sebagai contoh lebih lanjut, xenon, dalam bilangan oksidasi +8, membentuk oksida eksplosif berwarna kuning pucat, XeO4, sedangkan osmium, logam mulia lainnya, membentuk oksida pengoksidasi kuat berwarna kuning, OsO4. Ada persamaan juga dalam rumus oksifluorida: XeO2F4 dan OsO2F4, serta XeO3F2 dan OsO3F2.[104]
Sekitar 1015 ton gas mulia hadir di atmosfer Bumi.[105] Helium juga ditemukan dalam gas alam sebanyak 7%.[106] Radon berdifusi keluar dari batuan, di mana ia terbentuk selama urutan peluruhan alami uranium dan torium.[107] Pada tahun 2014, dilaporkan bahwa inti Bumi mungkin mengandung sekitar 1013 ton xenon, dalam bentuk senyawa antarlogam XeFe3 dan XeNi3 yang stabil. Ini mungkin menjelaskan mengapa "studi mengenai atmosfer bumi telah menunjukkan bahwa lebih dari 90% dari jumlah Xe yang diperkirakan terdeplesi."[108]
Halogen nonlogam[sunting | sunting sumber]

Walaupun halogen nonlogam merupakan unsur-unsur yang sangat reaktif dan korosif, mereka dapat ditemukan dalam senyawa biasa seperti pasta gigi (NaF); garam meja biasa (NaCl); disinfektan kolam renang (NaBr); atau suplemen makanan (KI). Kata "halogen" memiliki arti "pembentuk garam".[109]
Secara fisik, fluorin dan klorin merupakan gas berwarna kuning pucat dan hijau kekuningan; bromin merupakan cairan coklat kemerahan (biasanya ditutupi oleh lapisan asapnya); dan iodin, di bawah cahaya putih, merupakan padatan yang tampak seperti logam[75]. Secara elektrik, tiga yang pertama merupakan insulator sedangkan iodin merupakan semikonduktor (sepanjang bidangnya).[110]
Secara kimia, mereka memiliki energi ionisasi, afinitas elektron, dan nilai keelektronegatifan yang tinggi, dan sebagian besar merupakan zat pengoksidasi yang relatif kuat.[111] Manifestasi dari status ini termasuk sifat korosif mereka.[112] Keempatnya menunjukkan kecenderungan untuk membentuk senyawa ionik yang dominan dengan logam[113] sedangkan nonlogam yang tersisa, oksigen batang, cenderung membentuk senyawa kovalen dengan logam.[n 18] Sifat reaktif dan sangat elektronegatif dari halogen nonlogam mewakili lambang karakter nonlogam.[117]
Dalam tabel periodik, lawan dari halogen yang sangat nonlogam dalam golongan 17 adalah logam alkali yang sangat reaktif, seperti natrium dan kalium, dalam golongan 1.[118] Sebagian besar logam alkali, seolah-olah meniru halogen nonlogam, diketahui diketahui membentuk anion –1 (sesuatu yang jarang terjadi di antara logam).[119]
Halogen nonlogam ditemukan dalam mineral yang berhubungan dengan garam. Fluorin terdapat dalam fluorit (CaF2), sebuah mineral yang tersebar luas. Klorin, bromin, dan iodin ditemukan dalam air garam. Secara luar biasa, sebuah studi tahun 2012 melaporkan adanya 0,04% fluorin asli (F2) menurut beratnya dalam antozonit, yang menghubungkan inklusi ini sebagai akibat radiasi dari keberadaan sejumlah kecil uranium.[120]
Nonlogam yang tak terklasifikasi[sunting | sunting sumber]

Setelah unsur nonlogam diklasifikasikan sebagai gas mulia, halogen atau metaloid (berikut), tujuh nonlogam sisanya adalah hidrogen, karbon, nitrogen, oksigen, fosforus, belerang, dan selenium. Dalam bentuk mereka yang paling stabil, tiga merupakan gas tidak berwarna (H, N, O); tiga memiliki penampilan seperti logam (C, P, Se); dan satu berwarna kuning (S). Secara elektrik, karbon grafit adalah semilogam sepanjang bidangnya[122] dan semikonduktor dalam arah tegak lurus bidangnya;[123] fosforus dan selenium adalah semikonduktor;[124] serta hidrogen, nitrogen, oksigen, dan belerang adalah insulator.[n 19]
Mereka umumnya dianggap terlalu beragam untuk mendapatkan pemeriksaan kolektif,[126] dan telah disebut sebagai nonlogam lainnya,[127] atau lebih jelas sebagai nonlogam, terletak di antara metaloid dan halogen.[128] Akibatnya, kimia mereka cenderung diajarkan secara berbeda, menurut empat golongan tabel periodik masing-masing,[129] misalnya: hidrogen dalam golongan 1; nonlogam golongan 14 (karbon, dan mungkin silikon dan germanium); nonlogam golongan 15 (nitrogen, fosfor, dan mungkin arsen serta antimon); serta nonlogam golongan 16 (oksigen, belerang, selenium, dan mungkin telurium). Subdivisi lain dimungkinkan sesuai dengan preferensi individu penulis.[n 20]
Hidrogen, khususnya, dalam beberapa hal berperilaku seperti logam dan dalam hal lain seperti nonlogam.[131] Seperti logam, (pertama-tama) ia dapat kehilangan satu elektronnya;[132] ia dapat menggantikan logam alkali dalam struktur logam alkali yang khas;[133] dan mampu membentuk hidrida seperti paduan, menampilkan ikatan logam, dengan beberapa logam transisi.[134] Di sisi lain, ia merupakan gas diatomik penginsulasi, seperti nonlogam yang khas, dan dalam reaksi kimia memiliki kecenderungan untuk mencapai konfigurasi elektron helium.[135] Ia melakukannya dengan cara membentuk ikatan kovalen atau ionik[134] atau, jika kehilangan elektronnya, mengikatkan dirinya pada pasangan elektron bebas.[136]
Beberapa atau semua nonlogam ini memiliki beberapa sifat bersama. Kebanyakan dari mereka, karena kurang reaktif dibandingkan halogen,[137] dapat terjadi secara alami di lingkungan.[138] Mereka memiliki peran biologis[139][140] dan geokimia yang menonjol.[126] Walaupun karakter fisik dan kimia mereka "cukup non-logam", secara bersih,[126] semuanya memiliki aspek korosif. Hidrogen dapat menimbulkan korosi pada logam. Korosi karbon dapat terjadi pada sel bahan bakar.[141] Hujan asam disebabkan oleh nitrogen terlarut atau belerang. Oksigen menimbulkan korosi besi melalui karat. Fosforus putih, bentuk yang paling tidak stabil, menyala di udara dan menghasilkan residu asam fosfat.[142] Selenium yang tidak diolah dalam tanah dapat menimbulkan gas hidrogen selenida yang korosif.[143] Ketika dikombinasikan dengan logam, nonlogam yang tidak terklasifikasi dapat membentuk senyawa dengan kekerasan (interstisi atau refraktori) yang tinggi,[144] karena jari-jari atom mereka yang relatif kecil dan nilai energi ionisasi yang cukup rendah.[126] Mereka menunjukkan kecenderungan untuk mengikat diri mereka sendiri, terutama dalam senyawa padat.[126][145] Hubungan tabel periodik diagonal di antara nonlogam-nonlogam ini menggemakan hubungan serupa di antara metaloid.[146][147]
Dalam tabel periodik, analogi geografis terlihat antara nonlogam yang tak terklasifikasi dan logam transisi. Nonlogam yang tak terklasifikasi menempati wilayah antara halogen nonlogam kuat di sebelah kanan dan metaloid nonlogam lemah di sebelah kiri. Logam transisi menempati wilayah, "antara logam ganas di sebelah kiri tabel periodik, dan logam tenang dan berisi di sebelah kanan ... [dan] ... membentuk jembatan transisi di antara keduanya".[148]
Nonlogam yang tak terklasifikasi biasanya terdapat dalam bentuk elemental (oksigen, belerang) atau ditemukan berasosiasi dengan salah satu dari dua unsur ini:[149]
- Hidrogen terjadi di lautan dunia sebagai komponen air, dan dalam gas alam sebagai komponen metana dan hidrogen sulfida.[150]
- Karbon terdapat pada batu gamping, dolomit, dan marmer, sebagai karbonat.[151] Yang kurang dikenal adalah karbon sebagai grafit, yang terutama terjadi pada batuan silikat metamorf[152] sebagai akibat dari kompresi dan pemanasan senyawa karbon sedimen.[153]
- Oksigen ditemukan di atmosfer; di lautan sebagai komponen air; dan di kerak sebagai mineral oksida.
- Mineral fosfor tersebar luas, biasanya sebagai fosfat fosforus-oksigen.[154]
- Belerang elemental dapat ditemukan di atau dekat sumber air panas dan daerah vulkanik di banyak bagian dunia; mineral belerang tersebar luas, biasanya sebagai sulfida atau sulfat oksigen-belerang.[155]
- Selenium terjadi pada bijih logam sulfida, di mana ia sebagian menggantikan belerang; selenium elemental kadang-kadang ditemukan.[156]
Metaloid[sunting | sunting sumber]

Enam unsur yang lebih umum dikenal sebagai metaloid adalah boron, silikon, germanium, arsen, antimon, dan telurium, masing-masing memiliki penampilan logam. Pada tabel periodik standar, mereka menempati area diagonal di blok-p yang membentang dari boron di kiri atas hingga telurium di kanan bawah, di sepanjang garis pemisah antara logam dan nonlogam yang ditunjukkan pada beberapa tabel.[2]
Mereka rapuh dan buruk sebagai konduktor panas dan listrik yang baik. Boron, silikon, germanium, dan telurium adalah semikonduktor. Arsen dan antimon memiliki struktur elektronik semilogam meskipun keduanya memiliki bentuk semikonduktor yang kurang stabil.[2]
Secara kimia, metaloid umumnya berperilaku seperti nonlogam (lemah). Di antara unsur-unsur nonlogam, mereka cenderung memiliki energi ionisasi, afinitas elektron, dan nilai keelektronegatifan terendah, dan merupakan zat pengoksidasi yang relatif lemah. Mereka lebih lanjut menunjukkan kecenderungan untuk membentuk paduan dengan logam.[2]
Dalam tabel periodik, di sebelah kiri metaloid nonlogam lemah adalah himpunan tak tentu dari logam yang memiliki sifat logam lemah (seperti timah, timbal dan bismut)[157] kadang-kadang disebut sebagai logam pascatransisi.[158] Dingle menjelaskan situasinya seperti ini:
- ... dengan logam 'tidak diragukan lagi' di paling kiri tabel, dan tidak diragukan lagi nonlogam di paling kanan ... celah antara dua ekstrem dijembatani pertama oleh logam miskin (pascatransisi), dan kemudian oleh metaloid—yang, mungkin dengan cara yang sama, mungkin secara kolektif dinamai 'nonlogam yang buruk'.[159]
Metaloid cenderung ditemukan dalam bentuk yang dikombinasikan dengan oksigen atau belerang atau (dalam kasus telurium) emas atau perak.[149] Boron ditemukan dalam mineral boron-oksigen borat termasuk di mata air vulkanik. Silikon terjadi pada mineral silikon-oksigen silika (pasir). Germanium, arsen, dan antimon ditemukan terutama sebagai komponen bijih sulfida. Telurium terjadi pada mineral telurida dari emas atau perak. Bentuk asli arsen, antimon dan telurium telah dilaporkan.[160]
Alotrop[sunting | sunting sumber]

Sebagian besar unsur nonlogam ada dalam bentuk alotropik. Karbon, misalnya, terjadi sebagai grafit dan sebagai intan. Alotrop tersebut mungkin menunjukkan sifat fisik yang lebih logam atau kurang nonlogam.[161]
Di antara halogen nonlogam, dan nonlogam yang tak terklasifikasi:
- Iodin dikenal dalam bentuk amorf semikonduktor.[162]
- Grafit, keadaan standar karbon, adalah konduktor listrik yang cukup baik. Berlian, sebuah alotrop karbon, jelas nonlogam, tembus cahaya dan merupakan konduktor listrik yang sangat buruk.[163] Karbon dikenal dalam beberapa bentuk alotropik lainnya, termasuk bukminsterfulerena yang semikonduktor,[164] dan varietas amorf[165] serta parakristalin (campuran amorf dan kristal)[166].
- Nitrogen dapat membentuk gas tetranitrogen (N4), sebuah molekul poliatomik yang tidak stabil dengan masa hidup sekitar satu mikrodetik.[167]
- Oksigen adalah molekul diatomik dalam keadaan standar; ia juga eksis sebagai ozon (O3), sebuah alotrop nonlogam yang tidak stabil dengan waktu paruh "di dalam ruangan" sekitar setengah jam, dibandingkan dengan sekitar tiga hari di udara sekitar pada suhu 20 °C.[168]
- Fosforus, secara unik, ada dalam beberapa bentuk alotropik yang lebih stabil daripada keadaan standarnya sebagai fosforus putih (P4). Alotrop fosforus putih, merah, dan hitam mungkin yang paling terkenal; yang pertama merupakan insulator; dua yang terakhir merupakan semikonduktor.[169] Fosforus juga eksis sebagai difosforus (P2), sebuah alotrop diatomik yang tidak stabil.[170]
- Sulfur memiliki lebih banyak alotrop daripada unsur lainnya.[171] Belerang amorf, campuran metastabil dari alotrop semacam ini, terkenal karena elastisitasnya.[172]
- Selenium memiliki beberapa alotrop nonlogam, yang semuanya jauh lebih sedikit menghantarkan listrik daripada keadaan standar selenium "metalik" abu-abu.[173]
Semua unsur yang paling umum dikenal sebagai metaloid membentuk alotrop:
- Boron dikenal dalam beberapa bentuk kristal dan amorf.[174]
- Silikon dapat membentuk kristal (seperti berlian); amorf; dan alotrop ortorombik Si24.[175]
- Pada tekanan sekitar 10–11 GPa, germanium berubah menjadi fase logam dengan struktur tetragonal yang sama seperti timah. Ketika didekompresi—dan bergantung pada kecepatan pelepasan tekanan—germanium metalik membentuk serangkaian alotrop yang metastabil dalam kondisi sekitar.[176]
- Arsen dan antimon membentuk beberapa alotrop terkenal (kuning, abu-abu, dan hitam).[177]
- Telurium dikenal dalam bentuk kristal dan amorf.[178]
Bentuk alotropik lain dari unsur nonlogam telah diketahui, baik di bawah tekanan atau dalam lapisan tunggal. Di bawah tekanan yang cukup tinggi, setidaknya setengah dari unsur nonlogam yang merupakan semikonduktor atau insulator,[n 21] dimulai dengan fosforus pada 1,7 GPa, telah diamati membentuk alotrop logam.[180][n 22] Bentuk dua dimensi lapisan tunggal nonlogam termasuk borofena (boron), grafena (karbon), silisena (silikon), fosforena (fosforus), germanena (germanium), arsenena (arsen), antimonena (antimon), dan telurena (telurium), secara kolektif disebut sebagai xenes.[182]
Prevalensi dan akses[sunting | sunting sumber]
Kelimpahan[sunting | sunting sumber]
| Domain | Komponen utama | Paling melimpah berikutnya |
|---|---|---|
| Kerak | O 61%, Si 20% | H 2,9% |
| Atmosfer | N 78%, O 21% | Ar 0,5% |
| Hidrosfer | O 66,2%, H 33,2% | Cl 0,3% |
| Biomassa | O 63%, C 20%, H 10% | N 3,0% |
Hidrogen dan helium diperkirakan membentuk sekitar 99% dari semua materi biasa di alam semesta dan lebih dari 99,9% atomnya.[184] Oksigen dianggap sebagai unsur paling melimpah berikutnya, sekitar 0,1%.[185] Kurang dari lima persen alam semesta diyakini terbuat dari materi biasa, yang diwakili oleh bintang, planet, dan makhluk hidup. Keseimbangannya terbuat dari energi gelap dan materi gelap, yang keduanya saat ini kurang dipahami.[186]
Lima nonlogam yaitu hidrogen, karbon, nitrogen, oksigen, dan silikon merupakan bagian terbesar dari kerak, atmosfer, hidrosfer, dan biomassa Bumi, dalam jumlah yang ditunjukkan pada tabel.
Ekstraksi[sunting | sunting sumber]

Nonlogam, dan metaloid, diekstraksi dalam bentuk mentahnya dari:[138]
- air garam—klorin, bromin, iodin;
- udara cair—nitrogen, oksigen, neon, argon, kripton, xenon;
- mineral—boron (mineral borat); karbon (batubara; intan; grafit); fluorin (fluorit); silikon (silika); fosforus (fosfat); antimon (stibnit, tetrahedrit); iodin (dalam natrium iodat dan natrium iodida);
- gas alam—hidrogen, helium, belerang; dan
- bijih, sebagai produk sampingan pengolahan—germanium (bijih seng); arsen (bijih tembaga dan timbal); selenium, telurium (bijih tembaga); dan radon (bijih yang mengandung uranium).
Biaya[sunting | sunting sumber]
Biaya harian akan bervariasi tergantung pada kemurnian, kuantitas, kondisi pasar, dan biaya tambahan pemasok.[189]
Berdasarkan literatur yang tersedia pada Agustus 2022, walaupun biaya yang dikutip dari sebagian besar nonlogam kurang dari AS$0,80 per gram biaya perak,[190] boron, fosforus, germanium, xenon, dan radon (secara umum) adalah pengecualian:
- Boron berharga sekitar AS$25 per gram untuk 99,7% bongkahan polikristalin murni dengan ukuran partikel sekitar 1 cm.[191] Sebelumnya, pada tahun 1997, boron dikutip dengan harga AS$280 per gram untuk batang polikristalin berdiameter 4 hingga 6 mm dengan kemurnian 99,999%,[192] sekitar sepuluh kali lipat biaya emas saat itu ($28,35 per gram).[193]
- Pada tahun 2020, fosforus dalam bentuk hitamnya yang paling stabil dapat "berharga hingga AS$1.000 per gram",[194] more than 15 times the cost of gold, lebih dari 15 kali lipat biaya emas, sedangkan fosforus merah biasa, pada tahun 2017, dihargai sekitar AS$3,40 per kilogram.[195] Para peneliti berharap dapat mengurangi biaya fosforus hitam hingga AS$1 per gram.[194]
- Germanium dan xenon berharga sekitar AS$1,20 dan AS$7,60 per gram.[196]
- Hingga tahun 2013, radon tersedia dari National Institute of Standards and Technology dengan harga $1.636 per unit 0,2 ml, setara dengan sekitar $86.000.000 per gram, tanpa indikasi diskon untuk jumlah massal.[197]
Penggunaan[sunting | sunting sumber]
Hampir semua nonlogam memiliki kegunaan yang bervariasi dalam barang-barang rumah tangga; pencahayaan dan laser; serta obat-obatan dan farmasi. Nitrogen, misalnya, ditemukan di beberapa perawatan taman; laser; dan obat diabetes. Germanium, arsen, dan radon masing-masing memiliki kegunaan dalam satu atau dua bidang ini tetapi tidak ketiganya.[138] Selain gas mulia, sebagian besar nonlogam yang tersisa telah, atau pernah, digunakan dalam agrokimia dan bahan pewarna.[138] Sejauh metaloid menunjukkan karakter logam, mereka memiliki kegunaan khusus yang meluas ke (misalnya) gelas oksida, komponen pemaduan, dan semikonduktor.[198]
Penggunaan lebih lanjut dari subset yang berbeda dari nonlogam terjadi di atau sebagai pengganti udara; kriogenik dan refrigeran; pupuk; penghambat nyala atau pemadam api; asam mineral; kendaraan hibrida plug-in; gas pengelasan; dan ponsel pintar.[138]
Sejarah, latar belakang, dan taksonomi[sunting | sunting sumber]
Penemuan[sunting | sunting sumber]

Mayoritas nonlogam ditemukan pada abad ke-18 dan ke-19. Sebelum itu, karbon, belerang, dan antimon dikenal di zaman kuno; arsen ditemukan selama Abad Pertengahan (oleh Albertus Agung); dan Hennig Brand mengisolasi fosforus dari urine pada tahun 1669. Helium (1868) memiliki perbedaan sebagai satu-satunya unsur nonlogam yang tidak pertama kali ditemukan di Bumi.[n 23] Radon adalah nonlogam yang paling baru ditemukan. Ia ditemukan pada akhir abad ke-19.[138]
Teknik berbasis kimia atau fisika yang digunakan dalam upaya isolasi adalah spektroskopi, distilasi fraksional, deteksi radiasi, elektrolisis, pengasaman bijih, reaksi perpindahan, pembakaran dan pemanasan; beberapa nonlogam terjadi secara alami sebagai unsur bebas.
Di antara gas mulia, helium terdeteksi melalui garis kuningnya di spektrum koronal matahari, dan kemudian dengan mengamati gelembung yang keluar dari uranit (UO2) yang dilarutkan dalam asam. Neon hingga xenon diperoleh melalui distilasi fraksional udara. Radon pertama kali teramati berasal dari senyawa torium, tiga tahun setelah penemuan radiasi Henri Becquerel pada tahun 1896.[200]
Halogen nonlogam diperoleh dari halida mereka melalui elektrolisis, penambahan asam, atau perpindahan. Beberapa ahli kimia meninggal akibat percobaan mereka dalam mencoba mengisolasi fluorin.[201]
Di antara nonlogam tak terklasifikasi, karbon dikenal (atau diproduksi) sebagai arang, jelaga, grafit dan intan; nitrogen teramati di udara dari mana oksigen telah dihilangkan; oksigen diperoleh dengan memanaskan raksa oksida; fosforus dibebaskan dengan memanaskan amonium natrium hidrogen fosfat (Na(NH4)HPO4), seperti yang ditemukan dalam urine;[202] belerang terjadi secara alami sebagai unsur bebas; dan selenium[n 24] terdeteksi sebagai residu dalam asam sulfat.[204]
Sebagian besar unsur yang umumnya dikenal sebagai metaloid diisolasi dengan memanaskan sulfida (germanium) atau oksida mereka (boron, silikon, arsen, telurium).[138] Antimon dikenal dalam bentuk aslinya serta dapat dicapai dengan memanaskan sulfidanya.[205]
Asal usul konsep ini[sunting | sunting sumber]
Perbedaan antara logam dan nonlogam muncul, secara berbelit-belit, dari pengenalan kasar berbagai jenis materi yaitu zat murni, campuran, senyawa dan unsur. Dengan demikian, materi dapat dibagi menjadi zat murni (seperti garam, soda bikarbonat, atau belerang) dan campuran (misalnya air raja, bubuk mesiu, atau perunggu) dan zat murni akhirnya dapat dibedakan sebagai senyawa dan unsur.[206] Unsur-unsur "logam" kemudian tampaknya memiliki atribut yang dapat dibedakan secara luas yang tidak dimiliki oleh unsur-unsur lain, seperti kemampuan mereka untuk menghantarkan panas atau karena "tanah" (oksida) mereka untuk membentuk larutan basa dalam air, misalnya seperti yang terjadi pada kapur tohor (CaO).[207]
Penggunaan istilah[sunting | sunting sumber]
Istilah nonlogam berasal dari tahun 1566. Dalam risalah medis yang diterbitkan tahun itu, Loys de L’Aunay (seorang dokter Prancis) menyebutkan sifat-sifat zat tanaman dari tanah logam dan "nonlogam".[208]
Dalam kimia awal, Wilhelm Homberg (seorang filsuf alam Jerman) mengacu pada belerang "nonlogam" dalam Des Essais de Chimie (1708).[209] Dia mempertanyakan pembagian lima kali lipat dari semua materi menjadi belerang, raksa, garam, air, dan tanah, seperti yang didalilkan oleh Étienne de Clave (1641) dalam New Philosophical Light of True Principles and Elements of Nature.[210] Pendekatan Homberg mewakili "sebuah langkah penting menuju konsep modern dari sebuah unsur".[211]
Lavoisier, dalam karya tahun 1789-nya yang "revolusioner"[212] Traité Élémentaire de Chimie, menerbitkan daftar modern pertama dari unsur-unsur kimia di mana ia membedakan antara gas, logam, nonlogam, dan tanah (oksida tahan panas).[213] Dalam tujuh belas tahun pertamanya, karya Lavoisier diterbitkan ulang dalam dua puluh tiga edisi dalam enam bahasa, dan "membawa ... kimia baru[nya] ke seluruh Eropa dan Amerika."[214]
Kriteria pembeda yang disarankan[sunting | sunting sumber]
|
Terkait elektron
|
Pada tahun 1809, penemuan natrium dan kalium oleh Humphry Davy "memusnahkan"[235] garis demarkasi antara logam dan nonlogam. Sebelum itu, logam telah dibedakan berdasarkan bobot atau massa jenisnya yang relatif tinggi.[236] Natrium dan kalium, di sisi lain, mengapung di atas air namun jelas merupakan logam berdasarkan perilaku kimianya.[237]
Sejak tahun 1811, sifat-sifat yang berbeda—fisik, kimia, dan terkait elektron—telah digunakan dalam upaya untuk memperhalus perbedaan antara logam dan nonlogam. Tabel terlampir menetapkan 22 sifat tersebut, menurut jenis dan urutan tanggal.
Mungkin sifat yang paling terkenal adalah bahwa konduktivitas listrik logam meningkat ketika suhu turun sedangkan nonlogam naik.[227] Namun skema ini tidak bekerja untuk plutonium, karbon, arsen, dan antimon. Plutonium, yang merupakan logam, meningkatkan konduktivitas listriknya ketika dipanaskan dalam kisaran suhu sekitar –175 hingga +125 °C.[238] Karbon, meskipun secara luas dianggap sebagai nonlogam, juga meningkatkan konduktivitasnya saat dipanaskan.[239] Arsen dan antimon kadang-kadang diklasifikasikan sebagai nonlogam namun bertindak mirip dengan karbon.[240]
Emsley mencatat bahwa, "Tidak ada sifat tunggal ... dapat digunakan untuk mengklasifikasikan semua unsur baik sebagai logam atau nonlogam."[241] Kneen dkk. menyarankan bahwa nonlogam dapat dilihat setelah kriteria [tunggal] untuk metalisitas telah dipilih, adding that, "menambahkan bahwa, "banyak klasifikasi sewenang-wenang yang mungkin, yang sebagian besar, jika dipilih secara wajar, akan serupa tetapi tidak harus identik."[14] Jones, sebaliknya, mengamati bahwa "kelas biasanya didefinisikan oleh lebih dari dua atribut".[242]
Johnson memperkirakan bahwa sifat fisik dapat menunjukkan sifat logam atau nonlogam terbaik dari suatu unsur, dengan ketentuan bahwa sifat lain akan diperlukan dalam kasus yang ambigu. Lebih khusus lagi, dia mengamati bahwa semua elemen gas atau nonkonduktor adalah nonlogam; logam nonlogam padat keras dan rapuh atau lunak dan rapuh sedangkan logam biasanya dapat ditempa dan ulet; dan oksida nonlogam bersifat asam.[243]
Setelah dasar untuk membedakan antara "dua kelas besar unsur"[244] ditetapkan, ternyata nonlogam adalah mereka yang tidak memiliki sifat logam,[245] hingga derajat yang lebih besar atau lebih kecil.[246] Beberapa penulis selanjutnya membagi unsur-unsur menjadi logam, metaloid, dan nonlogam meskipun Odberg berpendapat bahwa apa pun yang bukan logam berdasarkan kategorisasi, adalah nonlogam.[247]
Pengembangan subkelas[sunting | sunting sumber]
Sebuah taksonomi dasar nonlogam ditetapkan pada tahun 1844, oleh Alphonse Dupasquier, seorang dokter, apoteker, dan kimiawan Prancis.[248] Untuk memudahkan studi nonlogam, ia menulis:[249]
- Mereka akan dibagi menjadi empat kelompok atau bagian, seperti berikut ini:
- Organogen O, N, H, C
- Sulfuroid S, Se, P
- Kloroid F, Cl, Br, I
- Boroid B, Si.
Gema klasifikasi empat kali lipat Dupasquier terlihat di subkelas modern. Organogen dan belerang mewakili himpunan nonlogam yang tak terklasifikasi. Variasi konfigurasi dari tujuh nonlogam ini telah disebut sebagai, misalnya, nonlogam dasar;[250] biogen;[251] nonlogam pusat;[252] CHNOPS;[253] unsur esensial;[254] "nonlogam";[255][n 26] nonlogam yatim piatu;[256] atau nonlogam redoks.[257] Nonlogam kloroid kemudian secara independen disebut sebagai halogen.[258] Nonlogam boroid berkembang menjadi metaloid, mulai dari tahun 1864.[259] Gas mulia, sebagai pengelompokan diskrit, dihitung di antara nonlogam sejak 1900.[260]
Perbandingan[sunting | sunting sumber]
Beberapa sifat logam, metaloid, nonlogam yang tak terklasifikasi, halogen nonlogam, dan gas mulia dirangkum dalam tabel.[n 27] Sifat fisik berlaku untuk unsur dalam bentuknya yang paling stabil dalam kondisi sekitar, dan dicantumkan dalam urutan yang mudah. Sifat kimia terdaftar dari umum ke deskriptif, dan kemudian ke khusus. Garis putus-putus di sekitar metaloid menunjukkan bahwa, tergantung pada pembuatnya, unsur-unsur yang terlibat mungkin atau mungkin tidak dikenali sebagai kelas atau subkelas unsur yang berbeda. Logam dimasukkan sebagai titik referensi.
Sebagian besar sifat menunjukkan perkembangan kiri-ke-kanan dalam karakter logam ke nonlogam atau nilai rata-rata. Tabel periodik dengan demikian dapat secara indikatif dibagi menjadi logam dan nonlogam, dengan gradasi yang kurang lebih berbeda terlihat di antara nonlogam.[261]
| Sifat fisik | Logam alkali, alkali tanah, lantanida, aktinida, transisi, pascatransisi |
Metaloid boron, silikon, germanium, arsen, antimon, telurium |
Nonlogam tak terklasifikasi hidrogen, karbon, nitrogen, oksigen, fosforus, belerang, selenium |
Halogen nonlogam fluorin, klorin, bromin, iodin |
Gas mulia helium, neon, argon, kripton, xenon, radon |
|---|---|---|---|---|---|
| Bentuk dan berat[262] |
|
|
|
|
|
| Penampilan | berkilau[22] | berkilau[265] | tak berwarna[270] | ||
| Elastisitas | sebagian besar lunak dan ulet[22] (Hg adalah cairan) | rapuh[265] | C, hitam P, S, Se rapuh; keempatnya memiliki bentuk tak rapuh yang kurang stabil[271][n 28] | iodin rapuh[273] | tak dapat diterapkan |
| Konduktivitas listrik | baik[n 29] |
|
|
|
buruk[n 33] |
| Struktur elektronik[179] | metalik (Bi adalah semilogam) | semilogam (As, Sb) atau semikonduktor |
|
semikonduktor (I) atau insulator | insulator |
| Sifat kimia | Logam alkali, alkali tanah, lantanida, aktinida, transisi, pascatransisi |
Metaloid boron, silikon, germanium, arsen, antimon, telurium |
Nonlogam tak terklasifikasi hidrogen, karbon, nitrogen, oksigen, fosforus, belerang, selenium |
Halogen nonlogam fluorin, klorin, bromin, iodin |
Gas mulia helium, neon, argon, kripton, xenon, radon |
| Perilaku kimia umum |
|
nonmetalik lemah[n 34] | nonmetalik sedang[279] | nonmetalik kuat[280] | |
| Oksida | |||||
| Senyawa dengan logam | paduan[22] atau senyawa antarlogam[298] | cenderung membentuk paduan atau senyawa antarlogam[299] | terutama ionik[113] | senyawa sederhana dalam kondisi sekitar tidak diketahui[n 37] | |
| Energi ionisasi (kJ mol−1)‡ (halaman data) |
|
|
|
|
|
| Elektronegativitas (Pauling)[n 38]‡ (halaman data) |
|
|
|
|
|
| † Hidrogen juga dapat membentuk hidrida seperti-paduan[303] ‡ Label rendah, sedang, tinggi, dan sangat tinggi secara sewenang-wenang berdasarkan rentang nilai yang tercantum dalam tabel | |||||
Lihat pula[sunting | sunting sumber]
- CHON (karbon, hidrogen, oksigen, nitrogen)
- Daftar monografi nonlogam
- Tekanan metalisasi
- Unsur periode 1 (hidrogen dan helium)
- Sifat nonlogam (dan metaloid) menurut golongan
Catatan[sunting | sunting sumber]
- ^ H; N; O, S; F, Cl, Br, I; He, Ne, Ar, Kr, Xe, Rn[1]
- ^ C; P; Se.[1] Di sisi lain, ketiga unsur ini dihitung sebagai metaloid dalam survei terhadap 194 daftar metaloid, masing-masing 16, 10, dan 46 kali.[2]
- ^ B; Si, Ge; As, Sb; Te[3][4]
- ^ Al, Ga, In, Tl; Sn, Pb; Bi; Po; At
- ^ Hidrogen secara historis ditempatkan di atas satu atau lebih litium, boron,[5] karbon, atau fluorin;[6] atau tidak di atas suatu golongan sama sekali; atau di atas semua golongan utama secara bersamaan, dan karena itu mungkin atau mungkin tidak berdekatan dengan nonlogam lainnya.[7]
- ^ Jumlah tertimbang dari unsur-unsur yang sangat radioaktif, At (unsur 85), Fr (87), dan unsur-unsur dengan nomor atom lebih tinggi dari Es (99), belum disiapkan;[9] nilai massa jenis yang digunakan untuk At dan Fr adalah perkiraan teoretis.
- ^ Yang pertama dari dua sumber ini mengatakan bahwa ahli kimia tidak lagi menggunakan istilah metaloid dan bahwa unsur-unsur yang terlibat adalah nonlogam. Sumber kedua mengatakan bahwa unsur-unsur tabel periodik "setiap saat" dibagi menjadi logam, metaloid, dan nonlogam.
- ^ Nonlogam padat memiliki nilai konduktivitas termal dari 0,27 W m–1 K–1 untuk belerang hingga 2.000 untuk karbon vs. 6,3 untuk neptunium hingga 429 untuk perak, keduanya logam;[24] nilai konduktivitas listrik berkisar dari 10−18 S•cm−1 untuk belerang[24] hingga 3 × 104 dalam grafit[25] atau 3,9 × 104 untuk arsen[26] vs. 0,69 × 104 untuk mangan hingga 63 × 104 untuk perak, keduanya logam.[24]
- ^ Nilai konduktivitas termal untuk logam berkisar dari 6,3 W m–1 K–1 untuk neptunium hingga 429 untuk perak; vs. antimon 24,3, arsen 50, dan karbon 2000;[24] nilai konduktivitas listrik logam berkisar dari 0,69 S•cm−1 × 104 untuk mangan to 63 × 104 untuk perak; vs. karbon 3 × 104,[25] arsen 3,9 × 104 dan antimon 2,3 × 104[24]
- ^ Unsur-unsur ini menjadi semikonduktor[40]
- ^ Misalnya, C sebagai grafit terkelupas (diperluas),[41] dan sebagai kawat tabung nano karbon sepanjang satu meter;[42][43] P sebagai fosforus putih (lunak seperti lilin, lentur dan dapat dipotong dengan pisau, pada suhu kamar);[44] S sebagai belerang plastik;[45] dan Se sebagai kawat selenium, diambil dari bentuk cair[46]
- ^ Asam dibentuk oleh boron, fosforus, selenium, arsen, iodin;[53] oksida oleh karbon, silikon, germanium, belerang, antimon, dan telurium.[54]
- ^ Unsur-unsur ini adalah hidrogen dan helium di blok-s; boron hingga neon di blok-p; skandium hingga seng di blok-d; dan lantanum hingga iterbium di blok-f.
- ^ Gas mulia: He, Ne, Ar, Kr, Xe, Rn; Halogen nonlogam: F, Cl, Br, I; Nonlogam tak terklasifikasi: H, C, N, P, O, S, Se; Metaloid: B, Si, Ge, As, Sb, Te. Logam terdekat adalah Al, Ga, In, Tl; Sn, Pb; Bi; Po; dan At.
- ^ Tujuh nonlogam ditandai dengan belati tunggal atau ganda masing-masing memiliki penampilan loyo dan struktur molekul diskrit, tetapi untuk I memiliki penampilan logam di bawah cahaya putih.[75] Unsur nonlogam reaktif yang tersisa memiliki struktur kovalen raksasa, tetapi untuk H merupakan gas diatomik.[76]
Nonlogam belati tunggal N, S dan iodin agak tertatih-tatih sebagai nonlogam "kuat".
Walaupun N memiliki keelektronegatifan tinggi, N merupakan pembentuk anion yang enggan,[77] dan zat pengoksidasi pedestrian kecuali jika digabungkan dengan nonlogam yang lebih aktif seperti O atau F.[78]
S bereaksi dalam dingin dengan alkali dan logam pascatransisi, serta Cu, Ag dan Hg,[79] tetapi sebaliknya memiliki nilai energi ionisasi, afinitas elektron, dan keelektronegatifan yang rendah dibandingkan dengan rata-rata nonlogam lainnya; ia dianggap bukan zat pengoksidasi yang sangat baik.[80]
Iodin cukup korosif untuk menyebabkan lesi yang menyerupai luka bakar termal, jika ditangani tanpa perlindungan yang sesuai,[81] dan tingtur iodin akan melarutkan Au dengan lancar.[82] Yang mengatakan, walaupun "F, Cl dan Br semuanya akan mengoksidasi Fe2+ (aq) menjadi Fe3+(aq) ... iodin ... merupakan agen pengoksidasi yang [relatif] lemah sehingga tidak dapat melepaskan elektron dari ion Fe(II) dan membentuk ion Fe(III)."[83] Jadi, untuk reaksi X2 + 2e− → 2X−(aq) potensial reduksinya adalah F +2,87 V; Cl +1,36; Br +1,09; I +0,54. Di sini Fe3+ + e− → Fe3+ +0,77.[84] Dengan demikian F2, Cl2 dan Br2 akan mengoksidasi Fe2+ menjadi Fe3+ tetapi Fe3+ akan mengoksidasi I− menjadi I2. Iodin sebelumnya telah disebut sebagai zat pengoksidasi yang cukup kuat.[85] - ^ Tshitoyan dkk. (2019) melakukan analisis berbasis mesin tentang kedekatan nama unsur berdasarkan 3,3 juta abstrak yang diterbitkan antara tahun 1922 dan 2018 di lebih dari 1.000 jurnal. Peta yang dihasilkan menunjukkan bahwa "unsur yang mirip secara kimiawi terlihat mengelompok bersama dan distribusi keseluruhan menunjukkan topologi yang mengingatkan pada tabel periodik itu sendiri".[91]
- ^ Jones mengambil pandangan filosofis atau pragmatis untuk pertanyaan-pertanyaan ini. Dia menulis: "Meskipun klasifikasi adalah fitur penting dari semua cabang ilmu pengetahuan, selalu ada kasus sulit di perbatasan. Batas dari sebuah kelas jarang tajam ... Ilmuwan tidak boleh kehilangan tidur atas kasus-kasus sulit. Selama klasifikasi sistem bermanfaat untuk ekonomi deskripsi, untuk menyusun pengetahuan dan pemahaman kita, dan kasus-kasus sulit merupakan minoritas kecil, kemudian hapus dan ganti dengan sistem berdasarkan karakteristik bersama yang berbeda".[96]
- ^ Oksida logam biasanya ionik.[114] Di sisi lain, oksida logam dengan bilangan oksidasi tinggi biasanya berupa polimer atau kovalen.[115] Sebuah oksida polimer memiliki struktur terkait yang terdiri dari beberapa unit berulang.[116]
- ^ Belerang, sebuah insulator, dan selenium, sebuah semikonduktor, masing-masing merupakan fotokonduktor—konduktivitas listrik mereka meningkat hingga enam kali lipat saat terkena cahaya.[125]
- ^ Misalnya, Wulfsberg membagi nonlogam, termasuk B, Si, Ge, As, Sb, Te, Xe, menjadi nonlogam yang sangat elektronegatif (keelektronegatifan Pauling lebih dari 2,8) dan nonlogam elektronegatif (1,9 hingga 2,8). Hal ini menyebabkan N dan O menjadi nonlogam yang sangat elektronegatif, bersama dengan halogen; dan H, C, P, S dan Se adalah nonlogam elektronegatif. Se selanjutnya dikenal sebagai metaloid semikonduktor.[130]
- ^ B; Si, Ge; N, P; O, S, Se, Te; halogen nonlogam; dan gas mulia[179]
- ^ Pada tahun 2020, studi dan eksperimen bertekanan tinggi dikatakan mewakili "bidang penelitian yang sangat aktif dan kuat".[181]
- ^ Bagaimana helium memperoleh akhiran -ium dijelaskan dalam bagian berikut oleh penemunya, William Lockyer: "Saya mengambil tanggung jawab untuk menciptakan kata helium ... Saya tidak tahu apakah zat itu ... adalah logam seperti kalsium atau gas seperti hidrogen, tetapi saya tahu bahwa ia berperilaku seperti hidrogen [ditemukan di matahari] dan bahwa hidrogen, seperti yang dikatakan Dumas, berperilaku sebagai logam".[199]
- ^ Berzelius, yang menemukan selenium, mengira ia memiliki sifat logam, dikombinasikan dengan belerang.[203]
- ^ Rasio Goldhammer-Herzfeld kira-kira sama dengan pangkat tiga jari-jari atom dibagi dengan volume molar.[218] Lebih khusus lagi, ini adalah rasio gaya yang menahan elektron terluar atom individu pada tempatnya dengan gaya pada elektron yang sama dari interaksi antara atom-atom dalam unsur padat atau cair. Ketika gaya antar atom lebih besar dari, atau sama dengan, gaya atom, perjalanan elektron terluar ditunjukkan dan perilaku logam diprediksi. Jika tidak, perilaku nonlogam diantisipasi.[219]
- ^ Tanda kutip tidak ditemukan di sumber; mereka digunakan di sini untuk memperjelas bahwa sumbernya menggunakan kata nonlogam sebagai istilah formal untuk subset unsur kimia yang bersangkutan, daripada berlaku untuk nonlogam secara umum.
- ^ Lihat pula Sifat logam, metaloid dan nonlogam, yang memperlakukan metaloid sebagai kelasnya sendiri
- ^ Karbon sebagai grafit terkelupas (diperluas),[272] dan sebagai kawat tabung nano karbon;[42] fosforus sebagai fosforus putih (lunak seperti lilin, lentur dan dapat dipotong dengan pisau, pada suhu kamar);[44] belerang sebagai belerang plastik;[45] dan selenium sebagai kawat selenium[46]
- ^ Logam memiliki nilai konduktivitas listrik mulai dari 6,9×103 S•cm−1 untuk mangan hingga 6,3×105 untuk perak.[274]
- ^ Metaloid memiliki nilai konduktivitas listrik mulai dari 1,5×10−6 S•cm−1 untuk boron hingga 3,9×104 untuk arsen.[275]
- ^ Nonlogam yang tak terklasifikasi memiliki nilai konduktivitas listrik mulai dari sekitar 1×10−18 S•cm−1 untuk gas elemental hingga 3±4 dalam grafit.[276]
- ^ Halogen nonlogam memiliki nilai konduktivitas listrik mulai dari sekitar 1×10−18 S•cm−1 untuk F dan Cl hingga 1,7×10−8 S•cm−1 untuk iodin.[110][276]
- ^ Gas-gas elemental tersebut memiliki nilai konduktivitas listrik sekitar 1×10−18 S•cm−1.[276]
- ^ Mereka selalu memberikan "senyawa yang sifatnya kurang asam daripada senyawa yang sesuai dari nonlogam [khas]"[265]
- ^ Arsen trioksida bereaksi dengan belerang trioksida, membentuk arsen "sulfat" As2(SO4)3.[287]
- ^ CO dan N2O adalah "secara resmi anhidrida asam format dan hiponitrit, berturut-turut: CO + H2O → H2CO2 (HCOOH, asam format); N2O + H2O → H2N2O2 (asam hiponitrit)".[292]
- ^ Dinatrium helida (Na2He) adalah senyawa helium dan natrium yang stabil pada tekanan tinggi di atas 113 GPa. Argon membentuk paduan dengan nikel, pada 140 GPa dan mendekati 1.500 K namun pada tekanan ini argon bukan lagi gas mulia.[301]
- ^ Nilai untuk gas mulia berasal dari Rahm, Zeng dan Hoffmann.[302]
Referensi[sunting | sunting sumber]
Rujukan[sunting | sunting sumber]
- ^ a b c d e Larrañaga, Lewis & Lewis 2016, hlm. 988
- ^ a b c d e f Vernon 2013
- ^ Hérold 2006, hlm. 149–50
- ^ a b c Vernon 2020, hlm. 220
- ^ Luchinskii & Trifonov 1981, hlm. 200–220
- ^ Jolly 1966, inside cover
- ^ Rayner-Canham 2020, hlm. 212
- ^ Aylward & Findlay 2008, hlm. 6–13; 126: Nilai massa jenis dan keelektronegatifan
- ^ Edelstein & Morrs 2009, hlm. 123
- ^ a b Godovikov & Nenasheva 2020, hlm. 4
- ^ Glinka 1959, hlm. 77; Oxtoby, Gillis & Butler 2015, hlm. I.23
- ^ a b Sanderson 1957, hlm. 229
- ^ Morely & Muir 1892, hlm. 241
- ^ a b Kneen, Rogers & Simpson 1972, hlm. 218–219
- ^ Steudel 2020, hlm. 43
- ^ a b Hill, Holman & Hulme 2017, hlm. 182: Konduktansi atom adalah konduktivitas listrik satu mol zat. Itu sama dengan konduktivitas listrik dibagi dengan volume molar.
- ^ Tabel Periodik Unsur IUPAC
- ^ Johnson 2007, hlm. 13
- ^ Bodner & Pardue 1993, hlm. 354; Cherim 1971, hlm. 98
- ^ Restrepo dkk. 2006, hlm. 411; Thornton & Burdette 2010, hlm. 86; Hermann, Hoffmann & Ashcroft 2013, hlm. 11604‒1‒11604‒5
- ^ Mewes dkk. 2019; Smits dkk. 2020; Florez dkk. 2022
- ^ a b c d Kneen, Rogers & Simpson 1972, hlm. 261–264
- ^ Phillips 1973, hlm. 7
- ^ a b c d e f Aylward & Findlay 2008, hlm. 6–12
- ^ a b Jenkins & Kawamura 1976, hlm. 88
- ^ Carapella 1968, hlm. 30
- ^ Zumdahl & DeCoste 2010, hlm. 455, 456, 469, A40
- ^ Still 2016, hlm. 120
- ^ Siekierski & Burgess 2002, hlm. 86
- ^ Charlier, Gonze & Michenaud 1994
- ^ Taniguchi dkk. 1984, hlm. 867: "... fosforus hitam ... [dicirikan] oleh pita valensi lebar dengan sifat yang agak terdelokalisasi."; Morita 1986, hlm. 230; Carmalt & Norman 1998, hlm. 7: "Fosforus ... oleh karena itu diperkirakan memiliki beberapa sifat metaloid."; Du dkk. 2010. Interaksi antar lapisan dalam fosforus hitam, yang dikaitkan dengan gaya van der Waals-Keesom, dianggap berkontribusi pada sela pita yang lebih kecil dari bahan curah (dihitung 0,19 eV; diamati 0,3 eV) sebagai berlawanan dengan celah pita yang lebih besar dari satu lapisan (dihitung ~0,75 eV).
- ^ Wiberg 2001, hlm. 742
- ^ Evans 1966, hlm. 124–25
- ^ Wiberg 2001, hlm. 758
- ^ Stuke 1974, hlm. 178; Donohue 1982, hlm. 386–87; Cotton dkk. 1999, hlm. 501
- ^ Steudel 1977, hlm. 240: "... tumpang tindih orbital yang cukup besar harus ada, untuk membentuk ikatan antarmolekul, banyak pusat ... [sigma], menyebar melalui lapisan dan diisi dengan elektron terdelokalisasi, tercermin dalam sifat iodin (kilau, warna, konduktivitas listrik sedang)."; Segal 1989, hlm. 481: "Iodin menunjukkan beberapa sifat logam ..."
- ^ Kneen, Rogers & Simpson 1972, hlm. 85–86, 237
- ^ Salinas 2019, hlm. 379
- ^ Yang 2004, hlm. 9
- ^ Wiberg 2001, hlm. 416, 574, 681, 824, 895, 930; Siekierski & Burgess 2002, hlm. 129
- ^ Chung 1987; Godfrin & Lauter 1995
- ^ a b Janas, Cabrero-Vilatela & Bulmer 2013
- ^ Cambridge Enterprise 2013
- ^ a b Faraday 1853, hlm. 42; Holderness & Berry 1979, hlm. 255
- ^ a b Partington 1944, hlm. 405
- ^ a b Regnault 1853, hlm. 208
- ^ Herzfeld 1927, hlm. 701–705; Edwards 2000, hlm. 100–103
- ^ Kneen, Rogers & Simpson 1972, hlm. 263‒264
- ^ Langley & Hattori 2014, hlm. 214
- ^ a b Abbott 1966, hlm. 18
- ^ Brown et al. 2014, hlm. 237
- ^ Ebbing & Wrighton 2007 hlm. 868
- ^ Lidin 1996, hlm. 22, 29; 322, 165; 381, 173–174; 12, 147; 157 [B; P; Se; As; I]; Housecroft & Sharpe 2008, hlm. 472 [I]
- ^ Lidin 1996, hlm. 52, 58; 386; 140; 361, 365; 372, 376; 403 [C; Si; Ge; S; Sb; Te]; Rochow 1973, hlm. 1338 [Si]; Sanderson 1967, hlm. 172 [Ge]; Shkol'nikov 2010, hlm. 2127 [Sb]; Wiberg 2001, hlm. 592 [Te]
- ^ Matson & Orbaek 2013, hlm. 85
- ^ Yoder, Suydam & Snavely 1975, hlm. 58
- ^ Young dkk. 2018, hlm. 753
- ^ Brown dkk. 2014, hlm. 227
- ^ Siekierski & Burgess 2002, hlm. 21, 133, 177
- ^ Moore 2016; Burford, Passmore & Sanders 1989, hlm. 54
- ^ King & Caldwell 1954, hlm. 17; Brady & Senese 2009, hlm. 69
- ^ Chemical Abstracts Service 2021
- ^ Cockell 2019, hlm. 210
- ^ Emsley 2011, hlm. 81, 181; Scott 2014, hlm. 3
- ^ Kneen, Rogers & Simpson 1972, hlm. 226, 360
- ^ Lee 1996, hlm. 240
- ^ Greenwood & Earnshaw 2002, hlm. 43
- ^ Cressey 2010
- ^ Siekierski & Burgess 2002, hlm. 24–25
- ^ Siekierski & Burgess 2002, hlm. 23
- ^ Petruševski & Cvetković 2018; Grochala 2018
- ^ Greenwood & Earnshaw 2002, hlm. 27, 1232, 1234
- ^ Siekierski & Burgess 2002, hlm. 52, 101, 111, 124, 194
- ^ Cox 2004, hlm. 146
- ^ a b Vernon 2013, hlm. 1706
- ^ Wiberg 2001, passim
- ^ Vernon 2020, hlm. 222
- ^ Atkins & Overton 2010, hlm. 377, 389
- ^ Moody 1991, hlm. 391
- ^ Rodgers 2012, hlm. 504; Wulfsberg 2000, hlm. 726
- ^ Stellman 1998, bab 104–211
- ^ Nakao 1992, hlm. 426–427
- ^ Hill & Holman 2000, hlm. 196
- ^ Wiberg 2001, hlm. 1761–1762
- ^ Young 2006, hlm. 1285
- ^ Encyclopædia Britannica 2021
- ^ Royal Society of Chemistry 2021
- ^ Chambers & Holliday 1982, hlm. 273–274; Bohlmann 1992, hlm. 213; Jentzsch 2015, hlm. 247
- ^ Vassilakis, Kalemos & Mavridis 2014, hlm. 1; Hanley & Koga 2018, hlm. 24; Kaiho 2017, bab 2, hlm. 1
- ^ Bailar dkk. 1989, hlm. 742
- ^ Tshitoyan dkk. 2019, hlm. 95–98
- ^ Russell & Lee 2005, hlm. 419
- ^ Hampel & Hawley 1976, hlm. 174;
- ^ Goodrich 1844, hlm. 264; The Chemical News 1897, hlm. 189; Hampel & Hawley 1976, hlm. 191; Lewis 1993, hlm. 835; Hérold 2006, hlm. 149–50
- ^ Tyler 1948, hlm. 105; Reilly 2002, hlm. 5–6
- ^ a b Jones 2010, hlm. 169–71
- ^ Stein 1983, hlm. 165
- ^ Matson & Orbaek 2013, hlm. 203
- ^ Jolly 1966, hlm. 20
- ^ Clugston & Flemming 2000, hlm. 100–101, 104–105, 302
- ^ Maosheng 2020, hlm. 962
- ^ Mazej 2020
- ^ Wiberg 2001, hlm. 1131
- ^ Vernon 2020, hlm. 229
- ^ Cox 2000, hlm. 258–259; Möller 2003, hlm. 173; Trenberth & Smith 2005, hlm. 864
- ^ Emsley 2011, hlm. 220
- ^ Emsley 2011, hlm. 440
- ^ Zhu dkk. 2014, hlm. 644–648
- ^ Wiberg 2001, hlm. 4022
- ^ a b Greenwood & Earnshaw 2002, hlm. 804
- ^ Rudolph 1973, plhln. 133: "Oksigen dan halogen khususnya ... merupakan zat pengoksidasi kuat."
- ^ Daniel & Rapp 1976, hlm. 55
- ^ a b Cotton dkk. 1999, hlm. 554
- ^ Woodward dkk. 1999, hlm. 133–194
- ^ Phillips & Williams 1965, hlm. 478–479
- ^ Moeller dkk. 2012, hlm. 314
- ^ Lanford 1959, hlm. 176
- ^ Rayner-Canham 2020, hlm. 92, 139
- ^ Massey 2000, hlm. 113
- ^ Schmedt, Mangstl & Kraus 2012, hlm. 7847‒7849
- ^ Emsley 2011, hlm. 478
- ^ Greenwood & Earnshaw 2002, hlm. 277
- ^ Atkins dkk. 2006, hlm. 320
- ^ Greenwood & Earnshaw 2002, hlm. 482; Berger 1997, hlm. 86
- ^ Moss 1952, hlm. 180, 202
- ^ a b c d e Cao dkk. 2021, hlm. 20–21
- ^ Challoner 2014, hlm. 5; Government of Canada 2015; Gargaud dkk. 2006, hlm. 447
- ^ Crichton 2012, hlm. 6; Scerri 2013; Laboratorium Nasional Los Alamos 2021
- ^ Vernon 2020, hlm. 218
- ^ Wulfsberg 2000, hlm. 273–274, 620
- ^ Seese & Daub 1985, hlm. 65
- ^ MacKay, MacKay & Henderson 2002, hlm. 209
- ^ Cousins, Davidson & García-Vivó 2013, hlm. 11809–11811
- ^ a b Wiberg 2001, hlm. 255–257
- ^ Liptrot 1983, hlm. 161
- ^ Scott & Kanda 1962, hlm. 153
- ^ Taylor 1960, hlm. 316
- ^ a b c d e f g Emsley 2011, passim
- ^ Crawford 1968, hlm. 540
- ^ Benner, Ricardo & Carrigan 2018, hlm. 167—168: "Stabilitas ikatan karbon—karbon ... telah menjadikannya sebagai unsur pilihan pertama untuk menopang biomolekul. Hidrogen dibutuhkan karena berbagai alasan; setidaknya, ia mengakhiri rantai C–C. Heteroatom (atom yang bukan karbon atau hidrogen) menentukan reaktivitas biomolekul karbon. Dalam ... kehidupan, mereka adalah oksigen, nitrogen dan, pada tingkat lebih rendah, belerang, fosforus, selenium, dan halogen sesekali."
- ^ Zhao, Tu & Chan 2021
- ^ Kosanke dkk. 2012, hlm. 841
- ^ Wasewar 2021, hlm. 322–323
- ^ Messler 2011 hlm. 10
- ^ King dkk. 1994, hlm. 1344; Powell & Tims 1974, hlm. 189–191
- ^ Vernon 2020, hlm. 221–223
- ^ Rayner-Canham 2020, hlm. 216
- ^ Atkins 2001, hlm. 24–25
- ^ a b Cox 1997, hlm. 130–132; Emsley 2011, passim
- ^ National Center for Biotechnology Information 2021
- ^ Emsley 2011, hlm. 113
- ^ Greenwood & Earnshaw 2002, hlm. 270–271
- ^ Khan 2001, hlm. 59
- ^ Cox 1997, hlm. 130; Emsley 2011, hlm. 393
- ^ Cox 1997, hlm. 130; Emsley 2011, hlm. 515–516, 518
- ^ Boyd 2011, hlm. 570
- ^ Masterton, Hurley & Neth 2011, hlm. 38
- ^ McCue 1963, hlm. 264
- ^ Dingle 2017, hlm. 101
- ^ Hurlbut 1961, hlm. 132
- ^ Barton 2021, hlm. 200
- ^ Shanabrook, Lannin & Hisatsune 1981, hlm. 130‒133
- ^ Borg & Dienes 1992, hlm. 26
- ^ Wiberg 2001, hlm. 796
- ^ Shang dkk. 2021
- ^ Tang dkk. 2021
- ^ Cacace, de Petris & Troiani 2002, hlm. 480‒481
- ^ Koziel 2002, hlm. 18
- ^ Gusmão, Sofer & Pumera 2017, hlm. 8052–8053; Berger 1997, hlm. 84; Vernon 2013, hlm. 1704‒1705
- ^ Piro dkk. 2006, hlm. 1276‒1279
- ^ Steudel & Eckert 2003, hlm. 1
- ^ Greenwood & Earnshaw 2002, hlm. 659–660
- ^ Moss 1952, hlm. 192; Greenwood & Earnshaw 2002, hlm. 751
- ^ Donohue 1982, hlm. 48–81
- ^ Shiell dkk. 2021
- ^ Zhao et al. 2017
- ^ Donohue 1982, hlm. 302–310
- ^ Brodsky dkk. 1972, hlm. 609–614
- ^ a b Keeler & Wothers 2013, hlm. 293
- ^ Yousuf 1998, hlm. 425; Elatresh & Bonev 2020
- ^ Errandonea 2020, hlm. 595
- ^ Su dkk. 2020, hlm. 1621–1649
- ^ Nelson 1987, hlm. 732: crust, atmosphere, hydrosphere; Fortescue 2012, hlm. 56, 65: biomass
- ^ MacKay, MacKay & Henderson 2002, hlm. 200
- ^ Cox 1997, hlm. 17, 19
- ^ Ostriker & Steinhardt 2001, hlm. 46‒53
- ^ Höll dkk. 2007
- ^ Mineral Commodity Summaries 2022 (PDF). U.S. Geological Survey. 2022. hlm. 70–71.
- ^ Mineral Commodity Summaries 2022 (PDF). U.S. Geological Survey. 2022. hlm. 25, 64, 78.
- ^ Mineral Commodity Summaries 2022 (PDF). U.S. Geological Survey. 2022. hlm. 24, 25, 26, 70, 74, 78, 82, 148, 150, 152, 160, 169.; Kopteva, A; Kalimullin, L; Tcvetkov, P (2021). "Prospects and obstacles for green hydrogen production in Russia". Energies. 14 (3): 1–21(1). doi:10.3390/en14030718.; Oztemel, BH; Salt, I; Salt, Y (2022). "Carbon dioxide utilization: Process simulation of synthetic fuel production from flue gases". Chemical Industry and Chemical Engineering Quarterly. doi:10.2298/CICEQ211025005B.; "Editorial: Xenon anaesthesia for all, or only a select few?". Anaesthesia. 71 (11): 1259–1272 (1268). 2016. doi:10.1111/anae.13569.; Howe-Grant, M, ed. (1995). Fluorine Chemistry: A Comprehensive Treatment. New York: John Wiley and Sons. hlm. 17. ISBN 978-0-471-12031-5.; Dalakov, P; Neuber, E; Herzog, R (2020). "Innovative neon refrigeration unit operating down to 30 K". MATEC Web of Conferences. 324. doi:10.1051/matecconf/20203240.; Boysen, B; Cristóbal, J; Hilbig, J (2020). "Economic and environmental assessment of water reuse in industrial parks: case study based on a Model Industrial Park". Journal of Water Reuse and Desalination. 10 (4): 475–489. doi:10.2166/wrd.2020.034.; Gardner, AJ; Menon, DK (2018). "Moving to human trials for argon neuroprotection in neurological injury: A narrative review". British Journal of Anaesthesia. 120 (4): 453–468 (455). doi:10.1016/j.bja.2017.10.017.; Rajarathnam, GP; assallo, AM. The Zinc/bromine Flow Battery: Materials Challenges and Practical Solutions for Technology Advancement. Singapore: Springer. hlm. 3. ISBN 978-981-287-645-4.; Xia, G-J; Ning, Z-X; Zhu, X-M (2020). "Effect of low-frequency oscillation on plasma focusing in krypton hall thruster". Journal of Propulsion and Power. 36 (1): 25–32. doi:10.2514/1.B37599.;
- ^ Chand, H; Kumar, A; Bhumla, P (2022). "Scalable production of ultrathin boron nanosheets from a low-cost precursor". Advanced Materials Interfaces. 9: 22058 (2 of 11). doi:10.1002/admi.202200508.
- ^ Berger, LI (1997). Semiconductor Materials. Boca Raton: CRC Press. hlm. 42. ISBN 978-0-8493-8912-2.
- ^ "Mineral Commodity Summaries 1998" (PDF). U.S. Geological Survey. 1998. Diakses tanggal 4 September 2022.
- ^ a b Boise State University 2020
- ^ Hu, Z; Shen, Z; Yu, JC (2017). "Phosphorus containing materials for photocatalytic hydrogen evolution". Green Chemistry. 19: 588–613 (595). doi:10.1039/C6GC02825J.
- ^ Gardner, AJ; Menon, DK (2018). "Moving to human trials for argon neuroprotection in neurological injury: A narrative review". British Journal of Anaesthesia. 120 (4): 453–468 (454). doi:10.1016/j.bja.2017.10.017.; Mineral Commodity Summaries 2022 (PDF). U.S. Geological Survey. 2022. hlm. 25.
- ^ National Institute of Standards and Technology 2013
- ^ Gaffney & Marley 2017, hlm. 27
- ^ Labinger 2019, hlm. 305
- ^ Emsley 2011, hlm. 42–43, 219–220, 263–264, 341, 441–442, 596, 609
- ^ Emsley 2011, hlm. 84, 128, 180–181, 247
- ^ Cook 1923, hlm. 124
- ^ Weeks 1945, hlm. 161
- ^ Emsley 2011, hlm. 113, 363, 378, 477, 514–515
- ^ Weeks 1945, hlm. 22; Emsley 2011, hlm. 40
- ^ Klein 1994, hlm. 168
- ^ Lidin 1996, hlm. 64‒65
- ^ de L'Aunay 1566, hlm. 7
- ^ Homberg 1708, hlm. 350; vide Kim 2000
- ^ de Clave 1641
- ^ Schlager & Lauer 2000, hlm. 370
- ^ Strathern 2000, hlm. 239
- ^ Criswell hlm. 1140
- ^ Salzberg 1991, hlm. 204
- ^ Kendall 1811, hlm. 298–303
- ^ Brande 1821, hlm. 5
- ^ Edwards & Sienko 1983, hlm. 691–96
- ^ Edwards & Sienko 1983, hlm. 693
- ^ Herzfeld 1927; Edwards 2000, hlm. 100–03
- ^ Kubaschewski 1949, hlm. 931–940
- ^ Remy 1956, hlm. 9
- ^ White 1962, hlm. 106: Ia membuat suara dering ketika dipukul.
- ^ Johnson 1966, hlm. 3–4
- ^ Horvath 1973, hlm. 335–336
- ^ Rao & Ganguly 1986
- ^ Smith & Dwyer 1991, hlm. 65: Perbedaan titik lebur dan titik didih.
- ^ a b Herman 1999, hlm. 702
- ^ Suresh & Koga 2001, hlm. 5940–5944
- ^ Johnson 2007, hlm. 15–16
- ^ a b Edwards 2010, hlm. 941–965
- ^ Povh & Rosin 2017, hlm. 131
- ^ Beach 1911
- ^ Stott 1956, hlm. 100–102
- ^ Parish 1977, hlm. 178
- ^ Hare & Bache 1836, hlm. 310
- ^ Chambers 1743: "Yang membedakan logam dari semua benda lain ... adalah beratnya ..."
- ^ Edwards 2000, hlm. 85
- ^ Russell & Lee 2005, hlm. 466
- ^ Atkins dkk. 2006, hlm. 320–21
- ^ Zhigal'skii & Jones 2003, hlm. 66
- ^ Emsley 1971, hlm. 1
- ^ Jones 2010, hlm. 169
- ^ Johnson 1966, hlm. 3–5, 15
- ^ Leach & Ewing 1966, hlm. 47
- ^ Brady & Senese 2009, hlm. 52
- ^ Zumdahl & DeCoste 2010, hlm. 92
- ^ Oderberg 2007, hlm. 97
- ^ Bertomeu-Sánchez, Garcia-Belmar & Bensaude-Vincent 2002, hlm. 248–249
- ^ Dupasquier 1844, hlm. 66–67
- ^ Williams 2007, hlm. 1550–1561
- ^ Wächtershäuser 2014
- ^ Hengeveld & Fedonkin, hlm. 181–226
- ^ Wakeman 1899, hlm. 562
- ^ Fraps 1913, hlm. 11
- ^ Parameswaran dkk. 2020, hlm. 210
- ^ Knight 2002, hlm. 148
- ^ Fraústo da Silva & Williams 2001, hlm. 500
- ^ Berzelius 1832, hlm. 248–276
- ^ The Chemical News 1864, hlm. 22
- ^ Renouf 1901, hlm. 268
- ^ Vernon 2020, hlm. 217–225
- ^ Tregarthen 2003, hlm. 10
- ^ Lewis 1993, hlm. 28, 827
- ^ Lewis 1993, hlm. 28, 813
- ^ a b c d Rochow 1966, hlm. 4
- ^ Wiberg 2001, hlm. 780; Emsley 2011, hlm. 397; Rochow 1966, hlm. 23, 84
- ^ Kneen, Rogers & Simpson 1972, hlm. 321, 404, 436
- ^ Kneen, Rogers & Simpson 1972, hlm. 439
- ^ Kneen, Rogers & Simpson 1972, hlm. 465
- ^ Kneen, Rogers & Simpson 1972, hlm. 308
- ^ Wiberg 2001, hlm. 505, 681, 781; Glinka 1958, hlm. 355
- ^ Chung 1987, hlm. 4190‒4198; Godfrin & Lauter 1995, hlm. 216‒218
- ^ Wiberg 2001, hlm. 416
- ^ Desai, James & Ho 1984, hlm. 1160; Matula 1979, hlm. 1260
- ^ Schaefer 1968, hlm. 76; Carapella 1968, hlm. 29‒32
- ^ a b c Bogoroditskii & Pasynkov 1967, hlm. 77; Jenkins & Kawamura 1976, hlm. 88
- ^ Kneen, Rogers & Simpson 1972, hlm. 264
- ^ Rayner-Canham 2018, hlm. 203
- ^ Welcher 2001, hlm. 3–32: "Unsur-unsur berubah dari ... menjadi nonlogam yang cukup aktif, menjadi nonlogam yang sangat aktif, dan menjadi gas mulia."
- ^ Mackin 2014, hlm. 80
- ^ Johnson 1966, hlm. 105–108
- ^ Stein 1969, hlm. 5396‒5397; Pitzer 1975, hlm. 760‒761
- ^ Porterfield 1993, hlm. 336
- ^ a b Rao 2002, hlm. 22
- ^ Wells 1984, hlm. 534
- ^ Atkins dkk. 2006, hlm. 8, 122–123
- ^ Wiberg 2001, hlm. 750
- ^ Sidorov 1960, hlm. 599‒603
- ^ a b c d Puddephatt & Monaghan 1989, hlm. 59
- ^ a b Sanderson 1967, hlm. 172
- ^ a b Mingos 2019, hlm. 27
- ^ House 2008, hlm. 441
- ^ McMillan 2006, hlm. 823
- ^ King 1995, hlm. 182
- ^ Wiberg 2001, hlm. 399
- ^ Kläning & Appelman 1988, hlm. 3760
- ^ Ritter 2011, hlm. 10
- ^ Yamaguchi & Shirai 1996, hlm. 3
- ^ Vernon 2020, hlm. 223
- ^ Woodward dkk. 1999, hlm. 134
- ^ Dalton 2019
- ^ Rahm, Zeng & Hoffmann 2019, hlm. 345
- ^ Steudel 1977, hlm. 176
Bibliografi[sunting | sunting sumber]
- Abbott D 1966, An Introduction to the Periodic Table, J. M. Dent & Sons, London
- Atkins PA 2001, The Periodic Kingdom: A Journey Into the Land of the Chemical Elements, Phoenix, London, ISBN 978-1-85799-449-0
- Atkins PA dkk. 2006, Shriver & Atkins' Inorganic Chemistry, ed. ke-4., Oxford University Press, Oxford, ISBN 978-0-7167-4878-6
- Atkins PA & Overton T 2010, Shriver & Atkins' Inorganic Chemistry, ed. ke-5, Oxford University Press, Oxford, ISBN 978-0-19-923617-6
- Aylward G dan Findlay T 2008, SI Chemical Data, ed. ke-6, John Wiley & Sons Australia, Milton, ISBN 978-0-470-81638-7
- Bailar JC dkk. 1989, Chemistry, ed. ke-3, Harcourt Brace Jovanovich, San Diego, ISBN 978-0-15-506456-0
- Barton AFM 2021, States of Matter, States of Mind, CRC Press, Boca Raton, ISBN 978-0-7503-0418-4
- Beach FC (ed.) 1911, The Americana: A universal reference library, vol. XIII, Mel–New, Metalloid, Scientific American Compiling Department, New York
- Benner SA, Ricardo A & Carrigan MA 2018, "Is there a common chemical model for life in the universe?", dalam Cleland CE & Bedau MA (eds.), The Nature of Life: Classical and Contemporary Perspectives from Philosophy and Science, Cambridge University Press, Cambridge, ISBN 978-1-108-72206-3
- Berger LI 1997, Semiconductor Materials, CRC Press, Boca Raton, ISBN 978-0-8493-8912-2
- Bertomeu-Sánchez JR, Garcia-Belmar A & Bensaude-Vincent B 2002, "Looking for an order of things: Textbooks and chemical classifications in nineteenth century France", Ambix, vol. 49, no. 3, DOI:10.1179/amb.2002.49.3.227
- Berzelius JJ & Bache AD 1832, "An essay on chemical nomenclature, prefixed to the treatise on chemistry", The American Journal of Science and Arts, vol. 22
- Bodner GM & Pardue HL 1993, Chemistry, An Experimental Science, John Wiley & Sons, New York, ISBN 0-471-59386-9
- Bogoroditskii NP & Pasynkov VV 1967, Radio and Electronic Materials, Iliffe Books, London
- Bohlmann R 1992, "Synthesis of halides", dalam (ed.) Winterfeldt E, Heteroatom manipulation, Pergamon Press, Oxford, ISBN 978-0-08-091249-3
- Boise State University 2020, "Cost-effective manufacturing methods breathe new life into black phosphorus research", Micron School of Materials Science and Engineering, diakses tanggal 5 September 2022
- Borg RG & Dienes GJ 1992, The Physical Chemistry of Solids, Academic Press, Boston, ISBN 978-0-12-118420-9
- Boyd R 2011, "Selenium stories", Nature Chemistry, vol. 3, DOI:10.1038/nchem.1076
- Brady JE & Senese F 2009, Chemistry: The study of Matter and its Changes, ed. ke-5, John Wiley & Sons, New York, ISBN 978-0-470-57642-7
- Brande WT 1821, A Manual of Chemistry, vol. II, John Murray, London
- Brodsky MH, Gambino RJ, Smith JE Jr & Yacoby Y 1972, "The Raman spectrum of amorphous tellurium", Physica Status Solidi (b), vol. 52, DOI:10.1002/pssb.2220520229
- Brown TL dkk. 2014, Chemistry: The Central Science, ed. ke-3, Pearson Australia: Sydney, ISBN 978-1-4425-5460-3
- Burford N, Passmore J & Sanders JCP 1989, "The preparation, structure, and energetics of homopolyatomic cations of groups 16 (the chalcogens) and 17 (the halogens)", dalam Liebman JF & Greenberg A, From atoms to polymers : isoelectronic analogies, VCH: New York, ISBN 978-0-89573-711-3
- Cacace F, de Petris G & Troiani A 2002, "Experimental detection of tetranitrogen", Science, vol. 295, no. 5554, DOI:10.1126/science.1067681
- Cao C et al. 2021, "Understanding periodic and non-periodic chemistry in periodic tables", Frontiers in Chemistry, vol. 8, no. 813, DOI:10.3389/fchem.2020.00813
- Carapella SC 1968, "Arsenic" dalam (ed.) Hampel CA, The Encyclopedia of the Chemical Elements, Reinhold, New York
- Carmalt CJ & Norman NC 1998, 'Arsenic, Antimony and Bismuth: Some General Properties and Aspects of Periodicity', dalam (ed.) NC Norman, Chemistry of Arsenic, Antimony and Bismuth, Blackie Academic & Professional, London, pp. 1–38, ISBN 0-7514-0389-X
- Challoner J 2014, The Elements: The New Guide to the Building Blocks of our Universe, Carlton Publishing Group, ISBN 978-0-233-00436-5
- Chambers E 1743, dalam "Metal", Cyclopedia: Or an Universal Dictionary of Arts and Sciences (etc.), vol. 2, D Midwinter, London
- Chambers C & Holliday AK 1982, Inorganic Chemistry, Butterworth & Co., London, ISBN 978-0-408-10822-5
- Charlier J-C, Gonze X, Michenaud J-P 1994, First-principles Study of the Stacking Effect on the Electronic Properties of Graphite(s), Carbon, vol. 32, no. 2, hlm. 289–99, DOI:10.1016/0008-6223(94)90192-9
- Chemical Abstracts Service 2021, CAS REGISTRY database sejak 2 November
- Cherim SM 1971, Chemistry for Laboratory Technicians, Saunders, Philadelphia, ISBN 978-0-7216-2515-7
- Chung DD 1987, "Review of exfoliated graphite", Journal of Materials Science, vol. 22, DOI:10.1007/BF01132008
- Clugston MJ & Flemming R 2000, Advanced Chemistry, Oxford University Press, Oxford, ISBN 978-0-19-914633-8
- Cockell C 2019, The Equations of Life: How Physics Shapes Evolution, Atlantic Books, London, ISBN 978-1-78649-304-0
- Cook CG 1923, Chemistry in Everyday Life: With Laboratory Manual, D Appleton, New York
- Cotton A dkk. 1999, Advanced Inorganic Chemistry, ed. ke-6, Wiley, New York, ISBN 978-0-471-19957-1
- Cousins DM, Davidson MG & García-Vivó D 2013, "Unprecedented participation of a four-coordinate hydrogen atom in the cubane core of lithium and sodium phenolates", Chemical Communications, vol. 49, DOI:10.1039/C3CC47393G
- Cox (ed.) AN 2000, Allen's Astrophysical Quantities, ed. ke-4, AIP Press, New York, ISBN 978-0-387-98746-0
- Cox PA 1997, The Elements: Their Origins, Abundance, and Distribution, Oxford University Press, Oxford, ISBN 978-0-19-855298-7
- Cox T 2004, Inorganic Chemistry, ed. ke-2, BIOS Scientific Publishers, London, ISBN 978-1-85996-289-3
- Crawford FH 1968, Introduction to the Science of Physics, Harcourt, Brace & World, New York
- Crichton R 2012, Biological Inorganic Chemistry: A New Introduction to Molecular Structure and Function, ed. ke-2, Elsevier, Amsterdam, ISBN 978-0-444-53783-6
- Cressey D 2010, "Chemists re-define hydrogen bond Diarsipkan 2019-01-24 di Wayback Machine.", Nature newsblog, diakses tanggal 5 September 2022
- Criswell B 2007, "Mistake of having students be Mendeleev for just a day", Journal of Chemical Education, vol. 84, no. 7, hlm. 1140—1144, DOI:10.1021/ed084p1140
- Dalton L 2019, "Argon reacts with nickel under pressure-cooker conditions", Chemical & Engineering News, diakses tanggal 5 September 2022
- Daniel PL & Rapp RA 1976, "Halogen corrosion of metals", dalam (ed.) Fontana MG & Staehle RW, Advances in Corrosion Science and Technology, Springer, Boston, DOI:10.1007/978-1-4615-9062-0_2
- de Clave E 1641, New Philosophical Light of True Principles and Elements of Nature, Olivier Devarennes, Paris, diakses tanggal 5 September 2022
- de L'Aunay L 1566, Responce au discours de maistre Iacques Grevin, docteur de Paris, qu'il a escript contre le livre de maistre Loys de l'Aunay, medecin en la Rochelle, touchant la faculté de l'antimoine (Tanggapan terhadap Pidato Master Jacques Grévin,... Yang Dia Tulis Terhadap Buku Master Loys de L'Aunay,... Menyentuh Fakultas Antimon), De l'Imprimerie de Barthelemi Berton, La Rochelle
- Desai PD, James HM & Ho CY 1984, "Electrical Resistivity of Aluminum and Manganese", Journal of Physical and Chemical Reference Data, vol. 13, no. 4, DOI:10.1063/1.555725
- Dingle A 2017, The Elements: An Encyclopedic Tour of the Periodic Table, Quad Books, Brighton, ISBN 978-0-85762-505-2
- Donohue J 1982, The Structures of the Elements, Robert E. Krieger, Malabar, Florida, ISBN 978-0-89874-230-5
- Du Y, Ouyang C, Shi S & Lei M 2010, 'Ab Initio Studies on Atomic and Electronic Structures of Black Phosphorus', Journal of Applied Physics, vol. 107, no. 9, hlm. 093718–1–4, DOI:10.1063/1.3386509
- Dupasquier A 1844, Traité élémentaire de chimie industrielle, Charles Savy Juene, Lyon.
- Ebbing DD & Gammon SD 2007, General Chemistry, ed. ke-9, Houghton Miffllin, Boston, ISBN 978-0-618-85748-7
- Edelstein NM & Morrs LR 2009, "Chemistry of the Actinide elements", dalam (ed.) Nagy S, Radiochemistry and Nuclear Chemistry: Volume II, Encyclopedia of Life Support Systems, EOLSS Publishers, Oxford, hlm. 118–176, ISBN 978-1-84826-577-6
- Edwards PP 2000, "What, why and when is a metal?", dalam (ed.) Hall N, The New Chemistry, Cambridge University, Cambridge, hlm. 85–114, ISBN 978-0-521-45224-3
- Edwards PP dkk. 2010, "... logam menghantarkan dan nonlogam tidak", Philosophical Transactions of the Royal Society A, 2010, vol, 368, no. 1914, DOI:10.1098/rsta.2009.0282
- Edwards PP & Sienko MJ 1983, "On the occurrence of metallic character in the periodic table of the elements", Journal of Chemical Education, vol. 60, no. 9, DOI:10.1021/ed060p691, PMID 25666074
- Elatresh SF & Bonev SA 2020, "Stability and metallization of solid oxygen at high pressure", Physical Chemistry Chemical Physics, vol. 22, no. 22, DOI:10.1039/C9CP05267D
- Emsley J 1971, The Inorganic Chemistry of the Non-metals, Methuen Educational, London, ISBN 978-0-423-86120-4
- Emsley J 2011, Nature's Building Blocks: An A–Z Guide to the Elements, Oxford University Press, Oxford, ISBN 978-0-19-850341-5
- Encyclopædia Britannica 2021, Periodic table, diakses tanggal 5 September 2022
- Errandonea D 2020, "Pressure-induced phase transformations," Crystals, vol. 10, DOI:10.3390/cryst10070595
- Evans RC 1966, An Introduction to Crystal Chemistry, ed. ke-2, Cambridge University, Cambridge
- Faraday M 1853, The Subject Matter of a Course of Six Lectures on the Non-metallic Elements, (disusun oleh John Scoffern), Longman, Brown, Green, dan Longmans, London
- Florez dkk. 2022, From the gas phase to the solid state: The chemical bonding in the superheavy element flerovium, The Journal of Chemical Physics, vol. 157, 064304, DOI:10.1063/5.0097642
- Fortescue JAC 2012, Environmental Geochemistry: A Holistic Approach, Springer-Verlag, New York, ISBN 978-1-4612-6047-9
- Fraps GS 1913, Principles of Agricultural Chemistry, The Chemical Publishing Company, Easton, PA
- Fraústo da Silva JJR & Williams RJP 2001, The Biological Chemistry of the Elements: The Inorganic Chemistry of Life, ed. ke-2, Oxford University Press, Oxford, ISBN 978-0-19-850848-9
- Gaffney J & Marley N 2017, General Chemistry for Engineers, Elsevier, Amsterdam, ISBN 978-0-12-810444-6
- (Ed.) Gargaud M dkk. 2006, Lectures in Astrobiology, vol. 1, part 1: The Early Earth and Other Cosmic Habitats for Life, Springer, Berlin, ISBN 978-3-540-29005-6
- Glinka N 1958, General chemistry, Sobolev D (trans.), Foreign Languages Publishing House, Moscow
- Godfrin H & Lauter HJ 1995, "Experimental properties of 3He adsorbed on graphite", dalam (ed.) Halperin WP, Progress in Low Temperature Physics, volume 14, Elsevier Science B.V., Amsterdam, ISBN 978-0-08-053993-5
- Godovikov AA & Nenasheva N 2020, Structural-chemical Systematics of Minerals, ed. ke-3, Springer, Cham, Swiss, ISBN 978-3-319-72877-3
- Goodrich BG 1844, A Glance at the Physical Sciences, Bradbury, Soden & Co., Boston
- Government of Canada 2015, Periodic table of the elements, diakses tanggal 5 September 2022
- Greenwood NN & Earnshaw A 2002, Chemistry of the Elements, ed. ke-2, Butterworth-Heinemann, ISBN 978-0-7506-3365-9
- Grochala W 2018, "On the position of helium and neon in the Periodic Table of Elements", Foundations of Chemistry, vol. 20, hlm. 191–207, DOI:10.1007/s10698-017-9302-7
- Gusmão R, Sofer Z & Pumera M 2017, "Black phosphorus rediscovered: From bulk material to monolayers", Angewandte Chemie International Edition, vol. 56, no. 28, DOI:10.1002/anie.201610512
- Hampel CA & Hawley GG 1976, Glossary of Chemical Terms, Van Nostrand Reinhold, New York, ISBN 978-0-442-23238-2
- Hanley JJ & Koga KT 2018, "Halogens in terrestrial and cosmic geochemical systems: Abundances, geochemical behaviours, and analytical methods" dalam The Role of Halogens in Terrestrial and Extraterrestrial Geochemical Processes: Surface, Crust, and Mantle, (ed.) Harlov DE & Aranovich L, Springer, Cham, ISBN 978-3-319-61667-4
- Hare RA & Bache F 1836, Compendium of the Course of Chemical Instruction in the Medical Department of the University of Pennsylvania, ed. ke-3, JG Auner, Philadelphia
- Hengeveld R & Fedonkin MA 2007, "Bootstrapping the energy flow in the beginning of life", Acta Biotheoretica, vol. 55, DOI:10.1007/s10441-007-9019-4
- Herman ZS 1999, "The nature of the chemical bond in metals, alloys, and intermetallic compounds, according to Linus Pauling", dalam (ed.) Maksić, ZB, Orville-Thomas WJ, 1999, Pauling's Legacy: Modern Modelling of the Chemical Bond, Elsevier, Amsterdam, DOI:10.1016/S1380-7323(99)80030-2
- Hermann A, Hoffmann R & Ashcroft NW 2013, "Condensed Astatine: Monatomic and metallic", Physical Review Letters, vol. 111, DOI:10.1103/PhysRevLett.111.116404
- Hérold A 2006, "An arrangement of the chemical elements in several classes inside the periodic table according to their common properties", Comptes Rendus Chimie, vol. 9, no. 1, DOI:10.1016/j.crci.2005.10.002
- Herzfeld K 1927, "On atomic properties which make an element a metal", Physical Review, vol. 29, no. 5, DOI:10.1103PhysRev.29.701
- Hill G & Holman J 2000, Chemistry in Context, ed. ke-5, Nelson Thornes, Cheltenham, ISBN 0-17-448307-4
- Hill G, Holman J & Hulme PG 2017, Chemistry in Context, ed. ke-7, Oxford University Press, Oxford, ISBN 978-0-19-839618-5
- Holderness A & Berry M 1979, Advanced Level Inorganic Chemistry, ed. ke-3, Heinemann Educational Books, London, ISBN 978-0-435-65435-1
- Höll, Kling & Schroll E 2007, "Metallogenesis of germanium—A review", Ore Geology Reviews, vol. 30, nos. 3–4, hlm. 145–180, DOI:10.1016/j.oregeorev.2005.07.034
- Homberg W 1708, "Des Essais de Chimie", dalam Histoire De L'Academie Royale Des Sciences: Avec les Memoires de Mathematique & de Physique, L'Académie, Paris
- Horvath AL 1973, "Critical temperature of elements and the periodic system", Journal of Chemical Education, vol. 50, no. 5, DOI:10.1021/ed050p335
- House JE 2008, Inorganic Chemistry, Elsevier, Amsterdam, ISBN 978-0-12-356786-4
- Housecroft CE & Sharpe AG 2008, Inorganic Chemistry, ed. ke-3, Prentice-Hall, Harlow, ISBN 978-0-13-175553-6
- Hurlbut Jr CS 1961, Manual of Mineralogy, ed. ke-15, John Wiley & Sons, New York
- IUPAC Periodic Table of the Elements, diakses tanggal 5 September 2022
- Janas D, Cabrero-Vilatela, A & Bulmer J 2013, "Carbon nanotube wires for high-temperature performance", Carbon, vol. 64, hlm. 305-314, DOI:10.1016/j.carbon.2013.07.067
- Jenkins GM & Kawamura K 1976, Polymeric Carbons—Carbon Fibre, Glass and Char, Cambridge University Press, Cambridge, ISBN 978-0-521-20693-8
- Jentzsch AV & Matile S 2015, "Anion transport with halogen bonds", dalam (ed.) Metrangolo P & Resnati G, Halogen Bonding I: Impact on Materials Chemistry and Life Sciences, Springer, Cham, ISBN 978-3-319-14057-5
- (Ed.) Johnson D 2007, Metals and Chemical Change, RSC Publishing, Cambridge, ISBN 978-0-85404-665-2
- Johnson RC 1966, Introductory Descriptive Chemistry, WA Benjamin, New York
- Jolly WL 1966, The Chemistry of the Non-metals, Prentice-Hall, Englewood Cliffs, New Jersey
- Jones BW 2010, Pluto: Sentinel of the Outer Solar System, Cambridge University, Cambridge, ISBN 978-0-521-19436-5
- Kaiho T 2017, Iodine Made Simple, CRC Press, e-book, DOI:10.1201/9781315158310
- Keeler J & Wothers P 2013, Chemical Structure and Reactivity: An Integrated Approach, Oxford University Press, Oxford, ISBN 978-0-19-960413-5
- Kendall EA 1811, Pocket encyclopædia, ed. ke-2, vol. III, Longman, Hurst, Rees, Orme, dan Co., London
- Khan N 2001, An Introduction to Physical Geography, Concept Publishing, New Delhi, ISBN 978-81-7022-898-1
- Kim MG 2000, "Chemical analysis and the domains of reality: Wilhelm Homberg's Essais de chimie, 1702–1709", Studies in History and Philosophy of Science Part A, vol. 31, no. 1, hlm. 37–69, DOI:10.1016/S0039-3681(99)00033-3
- King RB 1994, Encyclopedia of Inorganic Chemistry, vol. 3, John Wiley & Sons, New York, ISBN 978-0-471-93620-6
- King RB 1995, Inorganic Chemistry of Main Group Elements, VCH, New York, ISBN 978-1-56081-679-9
- King GB & Caldwell WE 1954, The Fundamentals of College Chemistry, American Book Company, New York
- Kläning UK & Appelman EH 1988, "Protolytic properties of perxenic acid", Inorganic Chemistry, vol. 27, no. 21, DOI:10.1021/ic00294a018
- Klein U 1994, "Origin of the concept of chemical compound", Science in Context, no. 7, vol. 2, hlm. 163–204, DOI:10.1017/s0269889700001666
- Kneen WR, Rogers MJW & Simpson P 1972, Chemistry: Facts, Patterns, and Principles, Addison-Wesley, London, ISBN 978-0-201-03779-1
- Knight J 2002, Science of Everyday Things: Real-life chemistry, Gale Group, Detroit, ISBN 9780787656324
- Kosanke dkk. 2012, Encyclopedic Dictionary of Pyrotechnics (and Related Subject), Part 3 – P hingga Z, Pyrotechnic Reference Series No. 5, Journal of Pyrotechnics, Whitewater, Colorado, ISBN 978-1-889526-21-8
- Koziel JA 2002, "Sampling and sample preparation for indoor air analysis", dalam (ed.) Pawliszyn J, Comprehensive Analytical Chemistry, vol. 37, Elsevier Science B.V., Amsterdam, ISBN 978-0-444-50510-1
- Kubaschewski O 1949, "The change of entropy, volume and binding state of the elements on melting", Transactions of the Faraday Society, vol. 45, DOI:10.1039/TF9494500931
- Labinger JA 2019, "The history (and pre-history) of the discovery and chemistry of the noble gases", dalam (ed.) Giunta CJ, Mainz VV & Girolami GS, 150 Years of the Periodic Table: A Commemorative Symposium, Springer Nature, Cham, Switzerland, ISBN 978-3-030-67910-1
- Lanford OE 1959, Using Chemistry, McGraw-Hill, New York
- Langley RH & Hattori H 2014, 1,001 Practice Problems: Chemistry For Dummies, John Wiley & Sons, Hoboken, NJ, ISBN 978-1-118-54932-2
- Larrañaga MD, Lewis RJ & Lewis RA 2016, Hawley's Condensed Chemical Dictionary, ed. ke-16, Wiley, Hoboken, New York, ISBN 978-1-118-13515-0
- Leach RB & Ewing GW 1966, Chemistry, Doubleday, New York
- Lee JD 1996, Concise Inorganic Chemistry, ed. ke-5, Blackwell Science, Oxford, ISBN 978-0-632-05293-6
- Lewis RJ 1993, Hawley's Condensed Chemical Dictionary, ed. ke-12, Van Nostrand Reinhold, New York, ISBN 978-0-442-01131-4
- Lidin RA 1996, Inorganic Substances Handbook, Begell House, New York, ISBN 978-0-8493-0485-9
- Liptrot GF 1983, Modern Inorganic Chemistry, ed. ke-4, Bell & Hyman, ISBN 978-0-7135-1357-8
- Los Alamos National Laboratory 2021, Periodic Table of Elements: A Resource for Elementary, Middle School, and High School Students, diakses tanggal 5 September 2022
- Luchinskii GP & Trifonov DN 1981, "Some problems of chemical elements classification and the structure of the periodic system", in Uchenie o Periodichnosti. Istoriya i Sovremennoct, (Russian) Nauka, Moscow
- MacKay KM, MacKay RA & Henderson W 2002, Introduction to Modern Inorganic Chemistry, ed. ke-6, Nelson Thornes, Cheltenham, ISBN 978-0-7487-6420-4
- Mackin M 2014, Study Guide to Accompany Basics for Chemistry, Elsevier Science, Saint Louis, ISBN 978-0-323-14652-4
- Maosheng M 2020, "Noble gases in solid compounds show a rich display of chemistry with enough pressure", Frontiers in Chemistry, vol. 8, DOI:10.3389/fchem.2020.570492
- Massey AG 2000, Main group chemistry, ed. ke-2, John Wiley & Sons, Chichester, ISBN 978-0-471-49039-5
- Masterton W, Hurley C & Neth E 2011, Chemistry: Principles and Reactions, ed. ke-7, Brooks/Cole, Belmont, California, ISBN 978-1-111-42710-8
- Matson M & Orbaek AW 2013, Inorganic Chemistry for Dummies, John Wiley & Sons: Hoboken, ISBN 978-1-118-21794-8
- Matula RA 1979, "Electrical resistivity of copper, gold, palladium, and silver", Journal of Physical and Chemical Reference Data, vol. 8, no. 4, DOI:10.1063/1.555614
- Mazej Z 2020, "Noble-gas chemistry more than half a century after the first report of the noble-gas compound", Molecules, vol. 25, no. 13, DOI:10.3390/molecules25133014, PMID 32630333, PMC 7412050
- McCue JJ 1963, World of Atoms: An Introduction to Physical Science, Ronald Press, New York
- McMillan P 2006, "A glass of carbon dioxide", Nature, vol. 441, DOI:10.1038/441823a
- Messler Jr RW 2011, The Essence of Materials for Engineers, Jones and Bartlett Learning, Sudbury, Massachusetts, ISBN 978-0-7637-7833-0
- Mewes dkk. 2019, Copernicium: A relativistic noble liquid, Angewandte Chemie International Edition, vol. 58, pp. 17964–17968, DOI:10.1002/anie.201906966
- Mingos DMP 2019, "The discovery of the elements in the Periodic Table", dalam (ed.) Mingos DMP, The Periodic Table I. Structure and Bonding, Springer Nature, Cham, DOI:10.1007/978-3-030-40025-5
- Moeller T dkk. 2012, Chemistry: With Inorganic Qualitative Analysis, Academic Press, New York, ISBN 978-0-12-503350-3
- Möller D 2003, Luft: Chemie, Physik, Biologie, Reinhaltung, Recht, Walter de Gruyter, Berlin, ISBN 978-3-11-016431-2
- Moody B 1991, Comparative Inorganic Chemistry, ed. ke-3, Edward Arnold, London, ISBN 978-0-7131-3679-1
- Moore JT 2016, Chemistry for Dummies, ed. ke-2, bab 16, Tracking periodic trends, John Wiley & Sons: Hoboken, ISBN 978-1-119-29728-4
- Morita A 1986, 'Semiconducting Black Phosphorus', Journal of Applied Physics A, vol. 39, no. 4, pp. 227–42, DOI:10.1007/BF00617267
- Morely HF & Muir MM 1892, Watt's Dictionary of Chemistry, vol. 3, Longman's Green, dan Co., London
- Moss, TS 1952, Photoconductivity in the Elements, Butterworths Scientific, London
- Nakao Y 1992, "Dissolution of noble metals in halogen–halide–polar organic solvent systems", Journal of the Chemical Society, Chemical Communications, no. 5, DOI:10.1039/C39920000426
- National Center for Biotechnology Information 2021, "PubChem compound summary for CID 402, Hydrogen sulfide", diakses tanggal 5 September 2022
- National Institute of Standards and Technology 2013, SRM 4972 – Radon-222 Emanation Standard, diakses tanggal 5 September 2022
- Nelson PG 1987, "Important elements", Journal of Chemical Education, vol. 68, no. 9, DOI:10.1021/ed068p732
- Oderberg DS 2007, Real Essentialism, Routledge, New York, ISBN 978-1-134-34885-5
- Ostriker JP & Steinhardt PJ 2001, "The quintessential universe", Scientific American, vol. 284, no. 1, hlm. 46–53 PMID 11132422, doi:10.1038/scientificamerican0101-46 10.1038/scientificamerican0101-46
- Oxtoby DW, Gillis HP & Butler LJ 2015, Principles of Modern Chemistry, ed. ke-8, Cengage Learning, Boston, ISBN 978-1-305-07911-3
- Parameswaran P dkk. 2020, "Phase evolution and characterization of mechanically alloyed hexanary Al16.6Mg16.6Ni16.6Cr16.6Ti16.6Mn16.6 high entropy alloy", Metal Powder Report, vol. 75, no. 4, DOI:10.1016/j.mprp.2019.08.001
- Parish RV 1977, The Metallic Elements, Longman, London, ISBN 978-0-582-44278-8
- Partington JR 1944, A Text-book of Inorganic Chemistry, ed. ke-5, Macmillan & Co., London
- Petruševski VM & Cvetković J 2018, "On the 'true position' of hydrogen in the Periodic Table", Foundations of Chemistry, vol. 20, hlm. 251–260, DOI:10.1007/s10698-018-9306-y
- Phillips CSG & Williams RJP 1965, Inorganic Chemistry, vol. 1, Principles and non-metals, Clarendon Press, Oxford
- Phillips JC 1973, "The chemical structure of solids," dalam (ed.) Hannay NB, Treatise on Solid State Chemistry, vol. 1, Plenum Press, New York, hlm. 1–42, ISBN 978-1-4684-2663-2
- Piro NA dkk. 2006, "Triple-bond reactivity of diphosphorus molecules", Science, vol. 313, no. 5791, DOI:10.1126/science.1129630, PMID 16946068
- Pitzer K 1975, "Fluorides of radon and elements 118", Journal of the Chemical Society, Chemical Communications, no. 18, doi:10.1039/C3975000760B
- Porterfield WW 1993, Inorganic chemistry, Academic Press, San Diego, ISBN 978-0-12-562980-5
- Povh B & Rosina M 2017, Scattering and Structures: Essentials and Analogies in Quantum Physics, ed. ke-2, Springer, Berlin, DOI:10.1007/978-3-662-54515-7
- Powell P & Timms P 1974, The Chemistry of the Non-Metals, Chapman and Hall, London, ISBN 978-0-412-12200-2
- Puddephatt RJ & Monaghan PK 1989, The Periodic Table of the Elements, ed. ke-2, Clarendon Press, Oxford, ISBN 978-0-19-855516-2
- Rahm M, Zeng T & Hoffmann R 2019, "Electronegativity seen as the ground-state average valence electron binding energy", Journal of the American Chemical Society, vol. 141, no. 1, hlm. 342−351, DOI:10.1021/jacs.8b10246
- Rao KY 2002, Structural Chemistry of Glasses, Elsevier, Oxford, ISBN 978-0-08-043958-7
- Rao CNR & Ganguly PA 1986, "New criterion for the metallicity of elements", Solid State Communications, vol. 57, no. 1, hlm. 5–6, DOI:10.1016/0038-1098(86)90659-9
- Rayner-Canham G 2018, "Organizing the transition metals", in Scerri E & Restrepo G, Mendeleev to Oganesson: A multidisciplinary perspective on the periodic table, Oxford University, New York, ISBN 978-0-190-668532
- Rayner-Canham G 2020, The Periodic Table: Past, Present and Future, World Scientific, New Jersey, ISBN 978-981-121-850-7
- Regnault MV 1853, Elements of Chemistry, vol. 1, ed. ke-2, Clark & Hesser, Philadelphia
- Reilly C 2002, Metal Contamination of Food, Blackwell Science, Oxford, ISBN 978-0-632-05927-0
- Remy H 1956, Treatise on Inorganic Chemistry, Anderson JS (trans.), (ed.) Kleinberg J, vol. II, Elsevier, Amsterdam
- Renouf E 1901, "Lehrbuch der anorganischen Chemie", Science, vol. 13, no. 320, DOI:10.1126/science.13.320.268
- Restrepo G, Llanos EJ & Mesa H 2006, "Topological space of the chemical elements and its properties", Journal of Mathematical Chemistry, vol. 39, DOI:10.1007/s10910-005-9041-1
- Ritter SK 2011, "The case of the missing xenon", Chemical & Engineering News, vol. 89, no. 9, ISSN 0009-2347
- Rochow EG 1966, The Metalloids, DC Heath and Company, Boston
- Rochow EG 1973, "Silicon", dalam (ed.) Bailar JC dkk., Comprehensive Inorganic Chemistry, vol. 1, Pergamon Press, Oxford, ISBN 978-0-08-015655-2
- Rodgers GE 2012, Descriptive Inorganic, Coordination, and Solid State Chemistry, ed. ke-3, Brooks/Cole, Belmont, California, ISBN 978-0-8400-6846-0
- Royal Society of Chemistry 2021, Periodic Table: Non-metal, accessed September 3, 2021
- Rudolph J 1973, Chemistry for the Modern Mind, Macmillan, New York
- Russell AM & Lee KL 2005, Structure-Property Relations in Nonferrous Metals, Wiley-Interscience, New York, ISBN 0-471-64952-X
- Salinas JT 2019 Exploring Physical Science in the Laboratory, Moreton Publishing, Englewood, Colorado, ISBN 978-1-61731-753-8
- Salzberg HW 1991, From Caveman to Chemist: Circumstances and Achievements, American Chemical Society, Washington, DC, ISBN 0-8412-1786-6
- Sanderson RT 1957, "An electronic distinction between metals and nonmetals", Journal of Chemical Education, vol. 34, no. 5, DOI:10.1021/ed034p229
- Sanderson RT 1967, Inorganic Chemistry, Reinhold, New York
- (Ed.) Scerri E 2013, 30-Second Elements: The 50 Most Significant Elements, Each Explained In Half a Minute, Ivy Press, London, ISBN 978-1-84831-616-4
- Schaefer JC 1968, "Boron" dalam (ed.) Hampel CA, The Encyclopedia of the Chemical Elements, Reinhold, New York
- (Ed.)
Schlager N & Lauer J 2000, Science and Its Times: 1700–1799, volume 4 of Science and its times: Understanding the social significance of scientific discovery, Gale Group, ISBN 978-0-7876-3932-7
- Schmedt auf der Günne J, Mangstl M & Kraus F 2012, "Occurrence of difluorine F2 in nature—In situ proof and quantification by NMR spectroscopy", Angewandte Chemie International Edition, vol. 51, no. 31, DOI:10.1002/anie.201203515
- Scott D 2014, Around the World in 18 Elements, Royal Society of Chemistry, e-book, ISBN 978-1-78262-509-4
- Scott EC & Kanda FA 1962, The Nature of Atoms and Molecules: A General Chemistry, Harper & Row, New York
- Seese WS & Daub GH 1985, Basic Chemistry, ed. ke-4, Prentice-Hall, Englewood Cliffs, NJ, ISBN 978-0-13-057811-2
- Segal BG 1989, Chemistry: Experiment and Theory, ed. ke-2, John Wiley & Sons, New York, ISBN 0-471-84929-4
- Shanabrook BV, Lannin JS & Hisatsune IC 1981, "Inelastic light scattering in a onefold-coordinated amorphous semiconductor", Physical Review Letters, vol. 46, no. 2, 12 Januari, DOI:10.1103/PhysRevLett.46.130
- Shang dkk. 2021, "Ultrahard bulk amorphous carbon from collapsed fullerene", Nature, vol. 599, hlm. 599–604, DOI:10.1038/s41586-021-03882-9
- Sherwin E & Weston GJ 1966, Chemistry of the Non-metallic Elements, Pergamon Press, Oxford
- Shiell dkk. 2021, "Bulk crystalline 4H-silicon through a metastable allotropic transition", Physical Review Letters, vol. 26, p 215701, DOI:10.1103/PhysRevLett.126.215701
- Shkol’nikov EV 2010, "Thermodynamic characterization of the amphoterism of oxides M2O3 (M = As, Sb, Bi) and their hydrates in aqueous media, Russian Journal of Applied Chemistry, vol. 83, no. 12, pp. 2121–2127, DOI:10.1134/S1070427210120104
- Sidorov TA 1960, "The connection between structural oxides and their tendency to glass formation", Glass and Ceramics, vol. 17, no. 11, doi:10.1007BF00670116
- Siekierski S & Burgess J 2002, Concise Chemistry of the Elements, Horwood Press, Chichester, ISBN 978-1-898563-71-6
- Smith A & Dwyer C 1991, Key Chemistry: Investigating Chemistry in the Contemporary World: Book 1: Materials and Everyday Life, Melbourne University Press, Carlton, Victoria, ISBN 978-0-522-84450-4
- Smits dkk. 2020, Oganesson: A noble gas element that is neither noble nor a gas, Angewandte Chemie International Edition, vol. 59, hlm. 23636–23640, DOI:10.1002/anie.202011976
- Stein L 1969, "Oxidized radon in halogen fluoride solutions", Journal of the American Chemical Society, vol. 19, no. 19, doi:10.1021/ja01047a042
- Stein L 1983, "The chemistry of radon", Radiochimica Acta, vol. 32, DOI:10.1524/ract.1983.32.13.163
- (Ed.) Stellman JM 1998, Encyclopaedia of Occupational Health and Safety, vol. 4, ed. ke-4, International Labour Office, Geneva, ISBN 978-92-2-109817-1
- Steudel R 1977, Chemistry of the Non-metals: With an Introduction to atomic Structure and Chemical Bonding, Walter de Gruyter, Berlin, ISBN 978-3-11-004882-7
- Steudel R & Eckert B 2003, "Solid sulfur allotropes", in Steudel R (ed.), Elemental Sulfur and Sulfur-rich Compounds I, Springer-Verlag, Berlin, ISBN 978-3-540-40191-9
- Steudel R 2020, Chemistry of the Non-metals: Syntheses - Structures - Bonding - Applications, in collaboration with D Scheschkewitz, Berlin, Walter de Gruyter, DOI:10.1515/9783110578065
- Still B 2016 The secret life of the periodic table, Cassell, London, ISBN 978-1-84403-885-5
- Stott RWA 1956, Companion to Physical and Inorganic Chemistry, Longmans, Green and Co, London
- Stuke J 1974, 'Optical and electrical properties of selenium', dalam (ed.) RA Zingaro & WC Cooper, Selenium, Van Nostrand Reinhold, New York, hlm. 174
- Strathern P 2000, Mendeleyev's dream: The Quest for the Elements, Hamish Hamilton, London, ISBN 978-0-8412-1786-7
- Su et al. 2020, "Advances in photonics of recently developed Xenes", Nanophotonics, vol. 9, no. 7, DOI:10.1515/nanoph-2019-0561
- Suresh CH & Koga NA 2001, "A consistent approach toward atomic radii”, Journal of Physical Chemistry A, vol. 105, no. 24. DOI:10.1021/jp010432b
- Tang dkk. 2021, "Synthesis of paracrystalline diamond", Nature, vol. 599, hlm. 605–610, DOI:10.1038/s41586-021-04122-w
- Taniguchi M, Suga S, Seki M, Sakamoto H, Kanzaki H, Akahama Y, Endo S, Terada S & Narita S 1984, 'Core-exciton induced resonant photoemission in the covalent semiconductor black phosphorus', Solid State Communications, vo1. 49, no. 9, hlm. 867–7, DOI:10.1016/0038-1098(84)90441-1
- Taylor MD 1960, First Principles of Chemistry, Van Nostrand, Princeton
- The Chemical News and Journal of Physical Science 1864, "Notices of books: Manual of the Metalloids", vol. 9, hlm. 22
- The Chemical News and Journal of Physical Science 1897, "Notices of books: A Manual of Chemistry, Theoretical and Practical", by WA Tilden", vol. 75, hlm. 188–189
- Thornton BF & Burdette SC 2010, "Finding eka-iodine: Discovery priority in modern times", Bulletin for the history of chemistry, vol. 35, no. 2, diakses tanggal 5 September 2022
- Tregarthen L 2003, Preliminary Chemistry, Macmillan Education: Melbourne, ISBN 978-0-7329-9011-4
- Trenberth KE & Smith L 2005, "The mass of the atmosphere: A constraint on global analyses", Journal of Climate, vol. 18, no. 6, DOI:10.1175/JCLI-3299.1
- Tshitoyan dkk. 2019, "Unsupervised word embeddings capture latent knowledge from materials science literature", Nature, vol. 571, DOI:10.1038/s41586-019-1335-8
- Tyler PM 1948, From the Ground Up: Facts and Figures of the Mineral Industries of the United States, McGraw-Hill, New York
- Vassilakis AA, Kalemos A & Mavridis A 2014, "Accurate first principles calculations on chlorine fluoride ClF and its ions ClF±", Theoretical Chemistry Accounts, vol. 133, no. 1436, DOI:10.1007/s00214-013-1436-7
- Vernon R 2013, "Which elements are metalloids?", Journal of Chemical Education, vol. 90, no. 12, 1703‒1707, DOI:10.1021/ed3008457
- Vernon R 2020, "Organising the metals and nonmetals", Foundations of Chemistry, vol. 22, DOI:10.1007/s10698-020-09356-6 (akses terbuka)
- Wächtershäuser G 2014, "From chemical invariance to genetic variability", dalam (ed.) Weigand W and Schollhammer P, Bioinspired Catalysis: Metal Sulfur Complexes, Wiley-VCH, Weinheim, DOI:10.1002/9783527664160.ch1
- Wakeman TH 1899, "Free thought—Past, present and future", Free Thought Magazine, vol. 17
- Wasewar KL 2021, "Intensifying approaches for removal of selenium", dalam (ed.) Devi dkk., Selenium contamination in water, John Wiley & Sons, Hoboken, hlm. 319–355, ISBN 978-1-119-69354-3
- Weeks ME 1945, Discovery of the Elements, ed. ke-5, Journal of Chemical Education, Easton, Pennsylvania
- Welcher SH 2001, High marks: Regents Chemistry Made Easy, ed. ke-2, High Marks Made Easy, New York, ISBN 978-0-9714662-4-1
- Wells AF 1984, Structural Inorganic Chemistry, ed. ke-5, Clarendon Press, Oxford, ISBN 978-0-19-855370-0
- White JH 1962, Inorganic Chemistry: Advanced and Scholarship Levels, University of London Press, London
- Wiberg N 2001, Inorganic Chemistry, Academic Press, San Diego, ISBN 978-0-12-352651-9
- Williams RPJ 2007, "Life, the environment and our ecosystem", Journal of Inorganic Biochemistry, vol. 101, no. 11–12, DOI:10.1016/j.jinorgbio.2007.07.006
- Woodward dkk. 1999, "The electronic structure of metal oxides", dalam (ed.) Fierro JLG, Metal Oxides: Chemistry and Applications, CRC Press, Boca Raton, ISBN 1-4200-2812-X
- Wulfsberg G 1987, Principles of Descriptive Chemistry, Brooks/Cole, Belmont CA, ISBN 978-0-534-07494-4
- Wulfsberg G 2000, Inorganic Chemistry, University Science Books, Sausalito, California, ISBN 978-1-891389-01-6
- Yamaguchi M & Shirai Y 1996, "Defect structures", dalam (ed.) Stoloff NS & Sikka VK, Physical Metallurgy and Processing of Intermetallic Compounds, Chapman & Hall, New York, ISBN 978-1-4613-1215-4
- Yang J 2004, 'Theory of thermal conductivity', dalam (ed.) Tritt TM, Thermal Conductivity: Theory, Properties, and Applications, Kluwer Academic/Plenum Publishers, New York, hlm. 1–20, ISBN 978-0-306-48327-1,
- Yoder CH, Suydam FH & Snavely FA 1975, Chemistry, ed. ke-2, Harcourt Brace Jovanovich, New York, ISBN 978-0-15-506470-6
- Young JA 2006, "Iodine", Journal of Chemical Education, vol. 83, no. 9, DOI:10.1021/ed083p1285
- Young dkk. 2018, General Chemistry: Atoms First, Cengage Learning: Boston, ISBN 978-1-337-61229-6
- Yousuf M 1998, "Diamond anvil cells in high-pressure studies of semiconductors", dalam (ed.) Suski T & Paul W, High Pressure in Semiconductor Physics II, Semiconductors and Semimetals, vol. 55, Academic Press, San Diego, ISBN 978-0-08-086453-2
- Zhao J, Tu Z & Chan SH 2021, Carbon corrosion mechanism and mitigation strategies in a proton exchange membrane fuel cell (PEMFC): A review, Journal of Power Sources, vol. 488, #229434, DOI:10.1016/j.jpowsour.2020.229434
- Zhao Z, Zhang H, Kim D. dkk. 2017, "Properties of the exotic metastable ST12 germanium allotrope", Nature Communications, vol. 8, artikel no. 13909, DOI:10.1038/ncomms13909, PMID 28045027, (Palumata)
- Zhigal'skii GP & Jones BK 2003, The Physical Properties of Thin Metal Films, Taylor & Francis, London, ISBN 978-0-415-28390-8
- Zhu dkk. 2014, "Reactions of xenon with iron and nickel are predicted in the Earth's inner core", Nature Chemistry, vol. 6, DOI:10.1038/nchem.1925, PMID 24950336
- Zumdahl SS & DeCoste DJ 2010, Introductory Chemistry: A Foundation, ed. ke-7, Cengage Learning, Mason, Ohio, ISBN 978-1-111-29601-8
Pranala luar[sunting | sunting sumber]
 Media terkait Nonmetals di Wikimedia Commons
Media terkait Nonmetals di Wikimedia Commons
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||








