Sulfida
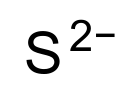
| |
| Nama | |
|---|---|
| Nama IUPAC (sistematis) | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| |
| |
| Sifat | |
| S2- | |
| Senyawa terkait | |
Anion lain
|
Telurida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Sulfida (nama sistematisnya sulfanediida, dan sulfida(2−)) adalah suatu anion anorganik dari belerang (atau sulfur) dengan rumus kimia S. Ia tidak memberi warna pada garam sulfida. Oleh karena diklasifikasikan sebagai basa kuat, larutan encer garamnya seperti natrium sulfida (Na) bersifat korosif dan dapat menyerang kulit. Sulfida adalah anion belerang yang paling sederhana.
Tata nama
[sunting | sunting sumber]Nama sistematisnya sulfanediida dan sulfida(2−), nama IUPAC yang valid, ditentukan menurut tata nama substitutif dan aditif. Namun, nama sulfida juga digunakan dalam tata nama IUPAC komposisional tanpa mempedulikan sifat ikatan yang terlibat. Contoh penamaan tersebut adalah selenium disulfida dan titanium sulfida, yang tidak mengandung ion sulfida sama sekali.
Sulfida juga digunakan secara non-sistematik, untuk menggambarkan senyawa yang melepaskan hidrogen sulfida pada pengasaman, atau senyawa yang mengandung belerang dalam beberapa bentuk, seperti dimetil sulfida. "Hidrogen sulfida" sendiri merupakan contoh nama non-sistematis dari sifat ini. Namun, ini juga merupakan nama trivial, dan nama yang lebih disukai IUPAC untuk sulfana.
Sifat kimia
[sunting | sunting sumber]Sulfida tidak ada dalam konsentrasi yang cukup, bahkan dalam air yang sangat alkalis, tidak terdeteksi pada pH < ~15 (8 M NaOH).[2]
Alkalinitas
[sunting | sunting sumber]Anion sulfida dapat mengasimilasi proton dengan rekombinasi:
- S2− + H+ → SH−
Karena penangkapan proton (H+), sulfida memiliki karakter basa. Dalam larutan akuatik, ia memiliki nilai pKb kurang dari 0. Asam konjugatnya adalah bisulfida (SH−). Dalam larutan akuatik, sebagian besar ion sulfida dinetralkan.
- S + H SH− + OH−
Reaksi kimia
[sunting | sunting sumber]Setelah diberi perlakuan dengan asam standar, sulfida berubah menjadi hidrogen sulfida (H2S) dan garam logam. Oksidasi sulfida menghasilkan belerang atau sulfat. Logam sulfida bereaksi dengan nonlogam termasuk iodium, brom, dan klor membentuk belerang dan garam logam.
- 8 MgS + 8 I2 → S8 + 8 MgI2
Belerang juga bisa dibuat dari sulfida dan oksidator yang tepat:
- 16 HNO3 + 24 H → 16 NO + 3 S8 + 32 H2O
Sulfida adalah basa kuat, sehingga larutan sulfida dalam air bersifat basa, karena mengalami hidrolisis. Larutan sulfida mengeluarkan bau telur busuk yang khas H sebagai hasil hidrolisis.[3]
- S2–(aq) + H(l)
 HS–(aq) + OH–(aq) (Kb = 8,3)
HS–(aq) + OH–(aq) (Kb = 8,3) - HS–(aq) + H(l)
 H(aq) + OH–(aq) (Kb = 1×10−7)
H(aq) + OH–(aq) (Kb = 1×10−7)
Derivat logam
[sunting | sunting sumber]Larutan kation logam transisi dalam air bereaksi dengan sumber sulfida (H2S, NaHS, Na2S) membentuk endapan sulfida padat. Sulfida anorganik tertentu biasanya memiliki kelarutan dalam air yang sangat rendah, dan banyak terkait dengan mineral dengan komposisi yang sama (lihat di bawah). Salah satu contoh yang terkenal adalah spesies kuning terang CdS atau "kadmium kuning". Noda hitam yang terbentuk pada perak murni adalah Ag2S. Spesies semacam itu terkadang disebut sebagai garam. Sebenarnya, ikatan dalam sulfida logam transisi adalah kovalen, yang menyebabkan sifat semikonduktor mereka, yang pada gilirannya terkait dengan kecerahan warnanya. Beberapa sulfida memiliki aplikasi praktis seperti pigmen, sel surya, dan sebagai katalis. Aspergillus niger berperan dalam pelarutan sulfida logam berat.[4]
Geologi
[sunting | sunting sumber]Banyak bijih logam penting adalah sulfida.[5] Contoh penting meliputi: argentit (perak sulfida), cinnabar (raksa), galena (timbal sulfida), molibdenit (molibdenum sulfida), pentlandit (nikel sulfida]), realgar (arsenik sulfida), dan stibnit (antimon), sfalerit (seng sulfida), dan pirit (besi disulfida), serta kalkopirit (besi-tembaga sulfida).
Korosi yang diinduksi oleh sulfida
[sunting | sunting sumber]Sulfida bebas terlarut (H2S, HS− dan S2−) adalah spesies yang sangat agresif dalam korosi banyak logam seperti baja, baja nirkarat, dan tembaga. Sulfida yang terdapat dalam larutan akuatik bertanggung jawab terhadap retak stress korosi (bahasa Inggris: stress corrosion cracking (SCC)) pada baja, yang dikenal juga sebagai retak stress sulfida. Korosi merupakan hal yang menjadi perhatian besar dalam banyak instalasi industri pemrosesan sulfida: pabrik bijih sulfida, sumur minyak dalam, pipa penyalur minyak curah, pabrik kertas Kraft.
Korosi yang diinduksi mikrob (Microbially-induced corrosion, MIC) atau korosi sulfida biogenik juga disebabkan oleh bakteri pereduksi sulfat, menghasilkan sulfida, yang disebarkan di udara dan teroksidasi dalam asam sulfat oleh bakteri pengoksidasi belerang. Asam sulfat biogenik bereaksi dengan bahan selokan sanitasi dan umumnya mengakibatkan kehilangan massa, keretakan pada pipa saluran air kotor, dan puncaknya, kerusakan struktur. Deteriorasi jenis ini adalah proses utama yang mempengaruhi sistem air kotor di seluruh dunia dan memicu biaya rehabilitasi yang sangat tinggi.
Oksidasi sulfida dapat membentuk tiosulfat (S), suatu spesies antara yang bertanggung jawab pada masalah berat korosi ceruk baja dan baja nirkarat yang mediumnya juga diasamkan oleh produksi asam sulfat jika diperlukan oksidasi lanjutan.
Kimia organik
[sunting | sunting sumber]Dalam kimia organik, "sulfida" biasanya merujuk pada ikatan C–S–C, meskipun istilah tioeter lebih sesuai. Misalnya, tioeter dimetil sulfida adalah H. Polifenilena sulfida (lihat di bawah) mempunyai rumus empiris C. Terkadang, istilah sulfida mengacu pada molekul yang mengandung gugus fungsi –SH. Sebagai contoh, metil sulfida dapat berarti H3C–SH. Deskripsi yang lebih disukai untuk senyawa yang mengandung SH tersebut adalah tiol atau merkaptan, yaitu metanatiol, atau metil merkaptan.
Disulfida
[sunting | sunting sumber]Kerancuan muncul dari perbedaan makna istilah "disulfida". Molibdenum disulfida (MoS2) terdiri dari pusat sulfida yang terpisah, yang terikat dengan molibdenum pada tingkat oksidasi formal +4 (Mo4+). Besi disulfida (pirit, FeS2) sebaliknya, terdiri dari S2−2, atau dianion −S−S−, yang terikat pada besi divalen dengan tingkat oksidasi formal +2 (ion ferro: Fe2+). Dimetildisulfida memiliki ikatan kimia H3C–S–S–CH3, sementara karbon disulfida tidak mempunyai ikatan S–S, melainkan S=C=S (molekul linier yang analog dengan CO2). Paling sering dalam kimia sulfur dan biokimia, istilah disulfida umum diasosiasikan untuk sulfur yang analog dengan ikatan –O–O– peroksida. Ikatan disulfida (–S–S–) memainkan peran penting dalam konformasi protein dan aktivitas katalitik enzim.
Contoh
[sunting | sunting sumber]| Rumus | Titik lebur (°C) | Titik didih (°C) | Nomor CAS | |
|---|---|---|---|---|
| H2S | Hidrogen sulfida adalah gas yang sangat beracun dan korosif yang dapat ditandai dengan bau "telur busuk" yang khas. | −85,7 | −60,20 | 7783-06-4 |
| CdS | Kadmium sulfida dapat digunakan dalam fotosel. | 1750 | 1306-23-6 | |
| Kalsium polisulfida ("belerang kapur") adalah fungisida tradisional dalam pertamanan. | ||||
| CS2 | Karbon disulfida kadang-kadang digunakan sebagai pelarut dalam kimia industri. | −111,6 | 46 | 75-15-0 |
| PbS | Timbal sulfida digunakan dalam sensor inframerah. | 1114 | 1314-87-0 | |
| MoS2 | Molibdenum disulfida, mineral molibdenit, digunakan sebagai katalis untuk menghilangkan belerang dari bahan bakar fosil; juga sebagai pelumas untuk aplikasi bersuhu tinggi dan dan bertekanan tinggi. | 1317-33-5 | ||
| Cl− CH |
Sulfur mustard (gas mustard) adalah suatu organosulfida (tioeter) yang digunakan sebagai senjata kimia dalam Perang Dunia I, klorida dalam molekul bertindak sebagai gugus pergi jika terkena air dan membentuk tioeter-alkohol dan HCl. | 13–14 | 217 | 505-60-2 |
| Ag2S | Perak sulfida terbentuk pada kontak listrik perak yang beroperasi pada atmosfer kaya hidrogen sulfida. | 21548-73-2 | ||
| Na2S | Natrium sulfida adalah bahan kimia industri penting, digunakan dalam manufaktur kertas kraft, pewarna, penyamakan kulit, pengolahan minyak mentah, pengolahan polusi logam berat, dan lain-lain. | 920 | 1180 | 1313-82-2 |
| ZnS | Seng sulfida digunakan untuk lensa dan peralatan optik lainnya pada bagian spektrum inframerah. Seng sulfida yang didoping dengan perak digunakan dalam detektor alfa, sementara seng sulfida dengan sekelumit tembaga memiliki aplikasi dalam garis fotoluminesensi untuk lampu darurat dan tombol pemutar arloji yang berpendar. | 1185 | 1314-98-3 | |
| MeS | Beberapa logam sulfida digunakan sebagai pigmen dalam seni, meskipun penggunaannya mengundang penolakan karena toksisitasnya. Pigmen sulfida meliputi kadmium, raksa, dan arsenik. | |||
| C | Polifenilena sulfida adalah suatu polimer yang umum disebut "Sulfar". Unit berulangnya terikat satu sama lain melalui tautan sulfida (tioeter). | 26125-40-6 25212-74-2 | ||
| SeS2 | Selenium disulfida adalah suatu antijamur yang digunakan dalam preparat anti-ketombe, seperti Selsun Blue. Adanya selenium yang sangat beracun dalam produk kesehatan dan kosmetika merupakan masalah kesehatan dan lingkungan yang umum. | <100 | 7488-56-4 | |
| FeS2 | Kisi kristal pirit tersusun dari besi disulfida, yang mana besi berbentuk divalen dan hadir sebagai ion ferro (Fe2+). | 600 | 1317-66-4 |
Preparasi
[sunting | sunting sumber]Senyawa sulfida dapat disiapkan dengan beragam cara:[6]
- Kombinasi langsung unsur-unsurnya:
- Contoh: Fe(s) + S(s) → FeS(s)
- Reduksi sulfat:
- Contoh: MgSO(s) + 4 C(s) → MgS(s) + 4 CO(g)
- Presipitasi sulfida tak larut:
- Contoh: M2+ + H(g) → MS(s) + 2 H+(aq)
Keselamatan
[sunting | sunting sumber]Banyak sulfida logam sangat tidak larut dalam air sehingga mereka mungkin tidak terlalu beracun. Beberapa sulfida logam, ketika terpapar asam mineral kuat, termasuk asam lambung, akan membebaskan hidrogen sulfida yang beracun.
Sulfida organik sangat mudah terbakar. Ketika sulfida terbakar, akan membebaskan gas belerang dioksida (SO2).
Hidrogen sulfida, beberapa logamnya, dan hampir semua senyawa sulfida organik mempunyai bau busuk dan menyengat yang dihasilkan dari pembusukan biomassa.
Lihat juga
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ a b "sulfide(2−) (CHEBI:15138)". Chemical Entities of Biological Interest (ChEBI). UK: European Bioinformatics Institute.
- ^ Meyer, B; Ward, K; Koshlap, K; Peter, L (1983). "Second dissociation constant of hydrogen sulfide". Inorganic Chemistry. 22: 2345. doi:10.1021/ic00158a027.
- ^ "Sulfide Ion, S2-", public.asu.edu, diakses tanggal 2017-05-23
- ^ Harbhajan Singh. Mycoremediation: Fungal Bioremediation. hlm. 509.
- ^ Vaughan, D.J.; Craig, J.R. (1978), Mineral chemistry of metal sulfides, Cambridge: Cambridge University Press, ISBN 0-521-21489-0
- ^ Atkins; Shriver (2010). Inorganic Chemistry (edisi ke-5th). New York: W. H. Freeman & Co. hlm. 413.

