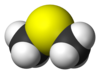
Dimetil sulfida
| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
(Metilsulfanil)metana | |
| Nama lain
(Metiltio)metana
Dimetil sulfida | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Referensi Beilstein | 1696847 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
| MeSH | dimethyl+sulfide |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 1164 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C2H6S | |
| Massa molar | 62,13 g·mol−1 |
| Penampilan | Cairan tak berwarna |
| Bau | Kubis, belerang |
| Densitas | 0.846 g cm−3 |
| Titik lebur | −98 °C; −145 °F; 175 K |
| Titik didih | [convert: unit tak dikenal] |
| log P | 0.977 |
| Tekanan uap | 53.7 kPa (pada 20 °C) |
| -44.9·10−6 cm3/mol | |
| Indeks bias (nD) | 1.435 |
| Termokimia | |
| Entalpi pembentukan standar (ΔfH |
-66.9--63.9 kJ mol−1 |
| Entalpi pembakaran standar ΔcH |
-2.1818--2.1812 MJ mol−1 |
| Bahaya | |
| Lembar data keselamatan | osha.gov |
| Piktogram GHS |   
|
| Keterangan bahaya GHS | {{{value}}} |
| H225, H315, H318, H335 | |
| P210, P261, P280, P305+351+338 | |
| Titik nyala | −36 °C (−33 °F; 237 K) |
| 206 °C (403 °F; 479 K) | |
| Ambang ledakan | 19.7% |
| Senyawa terkait | |
Related kalkogenida
|
Dimetil eter (dimetil oksida) |
Senyawa terkait
|
Dimetil sulfoksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Dimetil sulfida (DMS) atau metiltiometana adalah suatu senyawa organosulfur dengan rumus kimia (CH3)2S. Dimetil sulfida adalah cairan mudah terbakar yang mendidih pada suhu 37 °C (99 °F) dan memiliki bau khas yang tidak menyenangkan. Senyawa ini adalah komponen bau yang dihasilkan dari masakan sayuran tertentu, terutama jagung, kol, bit, dan makanan laut. Senyawa ini juga merupakan indikasi adanya kontaminasi bakteri dalam produksi malt dan pembuatan bir. Senyawa ini adalah produk pemecahan dimetilsulfoniopropionat (DMSP), dan juga diproduksi oleh metabolisme bakteri metanatiol.
Keberadaan di alam[sunting | sunting sumber]
DMS utamanya berasal dari DMSP, suatu metabolit sekunder utama pada alga laut.[1] DMS adalah senyawa belerang biologis paling melimpah yang dipancarkan ke atmosfer.[2][3] Emisi terjadi di atas lautan oleh fitoplankton. DMS juga diproduksi secara alami oleh transformasi bakteri dari limbah dimetil sulfoksida (DMSO) yang dibuang ke selokan, di mana dapat menyebabkan masalah bau lingkungan.[4]
DMS dioksidasi dalam atmosfer laut ke berbagai senyawa yang mengandung belerang, seperti belerang dioksida, dimetil sulfoksida (DMSO), dimetil sulfon, asam metanasulfonat, dan hidrogen sulfida.[5] Di antara senyawa ini, asam sulfat memiliki potensi untuk menciptakan aerosol baru yang bertindak sebagai inti kondensasi awan. Melalui interaksi ini dengan formasi awan, produksi besar-besaran DMS atmosfer di atas lautan mungkin memiliki dampak signifikan pada iklim bumi.[6][7] Hipotesis CLAW menunjukkan bahwa dengan cara ini DMS dapat berperan dalam homeostasis planet.[8]
Fitoplankton laut juga memproduksi dimetil sulfida,[9] dan DMS juga diproduksi oleh bakteri pembelahan DMSP ekstraselular.[10] DMS telah dikarakterisasi sebagai "bau laut",[11] meskipun akan lebih akurat untuk mengatakan bahwa DMS adalah komponen dari bau laut, yang lainnya adalah turunan kimia dari DMS, seperti oksida, namun ada pula yang menjadi feromon alga seperti diktiopterena.[12]
Dimetil sulfida juga merupakan bau yang dipancarkan oleh pabrik pulp kraft, dan senyawa ini adalah produk samping dari oksidasi Swern.
Dimetil sulfida, dimetil disulfida, dan dimetil trisulfida telah ditemukan di antara zat volatil yang dilepaskan oleh tanaman yang menarik lalat yang dikenal sebagai Helicodiceros muscivorus. Senyawa tersebut adalah komponen dari bau seperti daging busuk, yang menarik berbagai penyerbuk yang memakan bangkai, seperti banyak spesies lalat.[13]
Preparasi[sunting | sunting sumber]
Dalam industri dimetil sulfida diproduksi dengan memperlakukan hidrogen sulfida dengan kelebihan metanol di atas katalis aluminium oksida.[14]
Penggunaan[sunting | sunting sumber]
Industri[sunting | sunting sumber]
Dimetil sulfida telah digunakan dalam petroleum untuk memperbaiki katalis pra-hidrodesulfurisasi sulfida, walaupun disulfida atau polisulfida lain lebih disukai dan lebih mudah ditangani. Senyawa ini digunakan sebagai agen prasulfida untuk mengendalikan pembentukan kokas dan karbon monoksida dalam produksi etilena. DMS juga digunakan dalam sintesis kimia, termasuk sebagai agen pereduksi dalam reaksi ozonolisis.[15][16][17] Senyawa ini juga memiliki penggunaan sebagai komponen penyedap makanan. Hal ini juga dapat dioksidasi menjadi dimetil sulfoksida, (DMSO), yang merupakan pelarut industri yang penting.
Produsen DMS komersial terbesar di dunia adalah Gaylord Chemical Corporation, yang sampai pertengahan 2010 merupakan komponen ekonomi penting bagi industri kertas di Bogalusa, Louisiana. Pabrik DMS Bogalusa beroperasi terus-menerus sampai saat ini, sejak diluncurkan pada tahun 1961 oleh Crown Zellerbach Corporation yang sekarang sudah tidak berfungsi lagi. Teknologi pemrosesan yang dipraktikkan di pabrik Bogalusa (alkilasi sulfur menggunakan Kraft lignin) tidak lagi beroperasi di mana pun di dunia. Semua produsen DMS saat ini menggunakan bahan baku berbasis hidrokarbon. Gaylord tidak memproduksi apa pun di Louisiana lama setelah membuka operasi DMS/Dimetil sulfoksida yang diperluas di Tuscaloosa, Alabama pada tahun 2010.[18]
ChevronPhillips Chemical Company merupakan produsen utama DMS lainnya. CP Chem material ini di pabriknya di Borger, Texas, Amerika Serikat dan Tessenderlo, Belgia.
Kegunaan lain[sunting | sunting sumber]
Dimetil sulfida dapat digunakan sebagai ligan yang dapat dipindahkan dalam kloro(dimetil sulfida)emas(I) dan senyawa koordinasi lainnya. Dimetil sulfida juga digunakan dalam ozonolisis alkena, mereduksi zat antara trioksolana dan mengoksidasi menjadi DMSO.[19][20][21]
alkena + ozon + DMS → aldehida(1) + aldehida(2) + DMSO
Contohnya adalah ozonolisis dari eugenol, mengubah alkena terminal menjadi aldehida:[22]
![Ozonolisis eugenol[22]](//upload.wikimedia.org/wikipedia/commons/thumb/f/fd/EugenolOzonolysis.svg/700px-EugenolOzonolysis.svg.png)
Ozonolisis eugenol[22]
Keamanan[sunting | sunting sumber]
Dimetil sulfida sangat mudah terbakar dan menghasilkan bekas iritan pada mata dan kulit. Senyawa ini berbahaya jika tertelan dan memiliki bau tidak menyenangkan pada konsentrasi yang sangat rendah sekali pun. Suhu nyalanya adalah 205 °C.
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ Stefels, J.; Steinke, M.; Turner, S.; Malin, S.; Belviso, A. (2007). "Environmental constraints on the production and removal of the climatically active gas dimethylsulphide (DMS) and implications for ecosystem modelling". Biogeochemistry. 83 (1–3): 245–275. doi:10.1007/s10533-007-9091-5.
- ^ Kappler, Ulrike; Schäfer, Hendrik (2014). "Chapter 11. Transformations of Dimethylsulfide". Dalam Peter M.H. Kroneck and Martha E. Sosa Torres. The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. 14. Springer. hlm. 279–313. doi:10.1007/978-94-017-9269-1_11.
- ^ Simpson, D.; Winiwarter, W.; Börjesson, G.; Cinderby, S.; Ferreiro, A.; Guenther, A.; Hewitt, C. N.; Janson, R.; Khalil, M. A. K.; Owen, S.; Pierce, T. E.; Puxbaum, H.; Shearer, M.; Skiba, U.; Steinbrecher, R.; Tarrasón, L.; Öquist, M. G. (1999). "Inventorying emissions from nature in Europe". Journal of Geophysical Research. 104 (D7): 8113–8152. Bibcode:1999JGR...104.8113S. doi:10.1029/98JD02747.
- ^ Glindemann, D.; Novak, J.; Witherspoon, J. (2006). "Dimethyl Sulfoxide (DMSO) Waste Residues and Municipal Waste Water Odor by Dimethyl Sulfide (DMS): the North-East WPCP Plant of Philadelphia". Environmental Science and Technology. 40 (1): 202–207. Bibcode:2006EnST...40..202G. doi:10.1021/es051312a. PMID 16433352.
- ^ Lucas, D. D.; Prinn, R. G. (2005). "Parametric sensitivity and uncertainty analysis of dimethylsulfide oxidation in the clear-sky remote marine boundary layer". Atmospheric Chemistry and Physics. 5 (6): 1505–1525. doi:10.5194/acp-5-1505-2005.
- ^ Malin, G.; Turner, S. M.; Liss, P. S. (1992). "Sulfur: The plankton/climate connection". Journal of Phycology. 28 (5): 590–597. doi:10.1111/j.0022-3646.1992.00590.x.
- ^ Gunson, J.R.; Spall, S.A.; Anderson, T.R.; Jones, A.; Totterdell, I.J.; Woodage, M.J. (1 April 2006). "Climate sensitivity to ocean dimethylsulphide emissions". Geophys. Res. Lett. 33, L07701. 33. Bibcode:2006GeoRL..33.7701G. doi:10.1029/2005GL024982.
- ^ Charlson, R. J.; Lovelock, J. E.; Andreae, M. O.; Warren, S. G. (1987). "Oceanic phytoplankton, atmospheric sulphur, cloud albedo and climate". Nature. 326 (6114): 655–661. Bibcode:1987Natur.326..655C. doi:10.1038/326655a0.
- ^ "The Climate Gas You've Never Heard Of". Oceanus Magazine.
- ^ "Dimethylsulfide production from dimethylsulfoniopropionate by a marine bacterium". Marine Ecology Progress Series. 110: 95–103. 1994. doi:10.3354/meps110095.
- ^ "Cloning the smell of the seaside". University of East Anglia. February 2, 2007. Diarsipkan dari versi asli tanggal 2013-11-12. Diakses tanggal 2017-06-13.
- ^ Itoh, T.; Inoue, H.; Emoto, S. (2000). "Synthesis of Dictyopterene A: Optically Active Tributylstannylcyclopropane as a Chiral Synthon". Bulletin of the Chemical Society of Japan. 73 (2): 409–416. doi:10.1246/bcsj.73.409. ISSN 1348-0634.
- ^ Stensmyr, M. C.; Urru, I.; Collu, I.; Celander, M.; Hansson, B. S.; Angioy, A.-M. (2002). "Rotting Smell of Dead-Horse Arum Florets". Nature. 420 (6916): 625–626. Bibcode:2002Natur.420..625S. doi:10.1038/420625a. PMID 12478279.
- ^ Roy, Kathrin-Maria (15 June 2000). "Thiols and Organic Sulfides". Ullmann's Encyclopedia of Industrial Chemistry: 8. doi:10.1002/14356007.a26_767. ISBN 3-527-30673-0. Diakses tanggal 2 June 2017.
- ^ Mordecai B. Rubin (2003). "The History of Ozone Part III, C. D. Harries and the Introduction of Ozone into Organic Chemistry". Helv. Chim. Acta. 86 (4): 930–940. doi:10.1002/hlca.200390111.
- ^ Ikan, Raphael (1991). Natural Products: A Laboratory Guide (edisi ke-2nd). San Diego, CA: Academic Press. hlm. 35. ISBN 0123705517.
- ^ Veysoglu, Tarik; Mitscher, Lester A.; Swayze, John K. (1980). "A Convenient Method for the Control of Selective Ozonizations of Olefins". Synthesis: 807–810. doi:10.1055/s-1980-29214.
- ^ "Locations". Gaylord Chemicals.[pranala nonaktif permanen]
- ^ Bailey, P. S. (1973). "Diphenaldehyde". Org. Synth.; Coll. Vol. 5: 489.
- ^ Tietze, L. F. (1998). "Dialkyl Mesoxalates by Ozonolysis of Dialkyl Benzalmalonates". Org. Synth.; Coll. Vol. 9: 314.
- ^ Harwood, Laurence M.; Moody, Christopher J. (1989). Experimental Organic Chemistry: Principles and Practice (edisi ke-Illustrated). Wiley-Blackwell. hlm. 55–57. ISBN 978-0632020171.
- ^ a b Branan, Bruce M.; Butcher, Joshua T.; Olsen, Lawrence R. (2007). "Using Ozone in Organic Chemistry Lab: The Ozonolysis of Eugenol". J. Chem. Educ. 84 (12): 1979. Bibcode:2007JChEd..84.1979B. doi:10.1021/ed084p1979.

![Ozonolisis eugenol[22]](http://upload.wikimedia.org/wikipedia/commons/thumb/f/fd/EugenolOzonolysis.svg/700px-EugenolOzonolysis.svg.png)