Kalsium sulfat
| |

| |
| Nama | |
|---|---|
| Nama lain | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| CaSO4 | |
| Massa molar | 136.14 g/mol (anhidrat) 145.15 g/mol (hemihidrat) 172.172 g/mol (dihidrat) |
| Penampilan | padat putih |
| Bau | tidak berbau |
| Densitas | 2.96 g/cm3 (anhidrat) 2.32 g/cm3 (dihidrat) |
| Titik lebur | 1.460 °C (2.660 °F; 1.730 K) (anhidrat) |
| 0.21g/100ml pada suhu 20 °C (anhidrat)[1] 0.24 g/100ml at 20 °C (dihydrate)[2] | |
| Hasil kali kelarutan, Ksp | 4.93 × 10−5 mol2L−2 (anhidrat) 3.14 × 10−5 (dihidrat) [3] |
| Kelarutan dalam gliserol | Agak dapat larut (dihidrat) |
| Keasaman (pKa) | 10.4 (anhidrat) 7.3 (dihidrat) |
| -49.7·10−6 cm3/mol | |
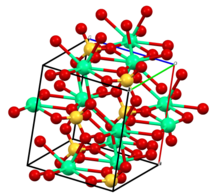
| Struktur | |
| Ortorombik | |
| Termokimia | |
| Entropi molar standar (S |
107 J·mol−1·K−1[4] |
| Entalpi pembentukan standar (ΔfH |
-1433 kJ/mol[4] |
| Bahaya | |
| Lembar data keselamatan | ICSC 1589 |
| Titik nyala | Tidak mudah terbakar |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp) [for anhydrous form only][5] |
REL (yang direkomendasikan)
|
TWA 10 mg/m3 (total) TWA 5 mg/m3 (resp) [anhydrous only][5] |
IDLH (langsung berbahaya)
|
N.D.[5] |
| Senyawa terkait | |
Kation lainnya
|
Magnesium sulfat Stronsium sulfat Barium sulfat |
Related
|
Kalsium klorida Magnesium sulfat |
Senyawa terkait
|
Plaster Paris Gipsum |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Kalsium sulfat adalah senyawa anorganik dengan rumus kimia CaSO4. Dalam bentuk anhidratnya, senyawa ini digunakan sebagai bahan pengering. Salah satu hidrat kalsium sulfat dikenal dengan sebutan Plaster Paris, sementara jenis hidrat yang lain dikenal sebagai mineral gipsum yang dapat ditemui di alam.
Semua jenis kalsium sulfat merupakan senyawa padat berwarna putih yang sulit larut dalam air.[6] Kalsium sulfat dapat mengakibatkan kesadahan permanen pada air.
Hidrasi[sunting | sunting sumber]
Terdapat tiga jenis senyawa kalsium sulfat berdasarkan tingkat hidrasi:
- CaSO4 (anhidrit): keadaan anhidrat.[7]
- CaSO4 · 2 H2O (gipsum): dihidrat.[8]
- CaSO4 · 0.5 H2O (basanit): hemihidrat, juga dikenal dengan nama Plaster Paris.[9]
Referensi[sunting | sunting sumber]
- ^ S. Gangolli (1999). The Dictionary of Substances and Their Effects: C. Royal Society of Chemistry. hlm. 71. ISBN 0-85404-813-8.
- ^ American Chemical Society (2006). Reagent chemicals: specifications and procedures : American Chemical Society specifications, official from January 1, 2006. Oxford University Press. hlm. 242. ISBN 0-8412-3945-2.
- ^ D.R. Linde (ed.) "CRC Handbook of Chemistry and Physics", 83rd Edition, CRC Press, 2002
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. hlm. A21. ISBN 0-618-94690-X.
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0095". National Institute for Occupational Safety and Health (NIOSH).
- ^ Franz Wirsching "Calcium Sulfate" in Ullmann's Encyclopedia of Industrial Chemistry, 2012 Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_555
- ^ Morikawa, H.; Minato, I.; Tomita, T.; Iwai, S. (1975). "Anhydrite: A refinement". Acta Crystallographica Section B. 31 (8): 2164. doi:10.1107/S0567740875007145.
- ^ Cole, W.F.; Lancucki, C.J. (1974). "A refinement of the crystal structure of gypsum CaSO4·2H2O". Acta Crystallographica Section B. 30 (4): 921. doi:10.1107/S0567740874004055.
- ^ Taylor H.F.W. (1990) Cement Chemistry. Academic Press, ISBN 0-12-683900-X, hlm. 186-187.
Wikimedia Commons memiliki media mengenai Calcium sulfate.
