Plutonium
94Pu Plutonium | ||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
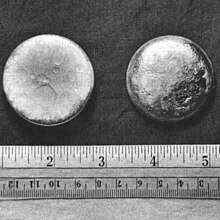 Sampel plutonium berdiameter ~44 mm | ||||||||||||||||||||||||||||||||||||||||||||||||
Garis spektrum plutonium | ||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | ||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /plutonium/[1] | |||||||||||||||||||||||||||||||||||||||||||||||
| Alotrop | lihat alotrop plutonium | |||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | putih keperakan, teroksidasi menjadi abu-abu gelap ketika terpapar dengan udara | |||||||||||||||||||||||||||||||||||||||||||||||
| Plutonium dalam tabel periodik | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 94 | |||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan n/a | |||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 7 | |||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-f | |||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | aktinida | |||||||||||||||||||||||||||||||||||||||||||||||
| Nomor massa | [244] | |||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Rn] 5f6 7s2 | |||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 32, 24, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | ||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | |||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 912,5 K (639,4 °C, 1182,9 °F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 3505 K (3228 °C, 5842 °F) | |||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 19,85 g/cm3 (239Pu)[2] | |||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 16,63 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 2,82 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 333,5 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 35,5 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| ||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | ||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | +2, +3, +4, +5, +6, +7, +8 (oksida amfoter) | |||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,28 | |||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 584,7 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 159 pm | |||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 187±1 pm | |||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | ||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | dari peluruhan | |||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | monoklin | |||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara | 2260 m/s | |||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 46,7 µm/(m·K) (suhu 25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 6,74 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 1,460 µΩ·m (suhu 0 °C) | |||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | paramagnetik | |||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 96 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 43 GPa | |||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,21 | |||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-07-5 | |||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | ||||||||||||||||||||||||||||||||||||||||||||||||
| Penamaan | dari planet katai Pluto, ia sendiri dinamai dari dewa dunia bawah klasik Pluto | |||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan | Glenn T. Seaborg, A. Wahl, Joseph W. Kennedy, E. McMillan (1940–1941) | |||||||||||||||||||||||||||||||||||||||||||||||
| Isotop plutonium yang utama | ||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||
Plutonium adalah sebuah unsur kimia radioaktif dengan lambang Pu dan nomor atom 94. Ia adalah sebuah logam aktinida berwarna abu-abu keperakan yang mengusam saat terkena udara, dan membentuk lapisan kusam saat teroksidasi. Unsur ini pada dasarnya memiliki enam alotrop dan empat keadaan oksidasi. Ia dapat bereaksi dengan karbon, halogen, nitrogen, silikon, dan hidrogen. Ketika terpapar oleh kelembapan udara, ia akan membentuk oksida dan hidrida yang dapat memperluas sampel hingga 70% volume, yang pada gilirannya mengelupas sebagai bubuk yang bersifat piroforik. Ia bersifat radioaktif dan dapat terakumulasi dalam tulang, yang membuat penanganan plutonium menjadi berbahaya, walaupun tingkat toksisitas keseluruhan logam ini terkadang dibesar-besarkan.
Plutonium pertama kali diproduksi dan diisolasi secara sintetis pada akhir 1940 dan awal 1941, melalui pemborbardiran sebuah deuteron uranium-238 dalam siklotron 1,5-meter (60 in) di Universitas California, Berkeley. Pertama, neptunium-238 (waktu paruh 2,1 hari) disintesis, yang kemudian mengalami peluruhan beta untuk membentuk unsur baru dengan nomor atom 94 dan berat atom 238 (waktu paruh 88 tahun). Karena uranium dinamai dari planet Uranus dan neptunium dari planet Neptunus, unsur 94 dinamai dari Pluto, yang pada saat itu masih dianggap sebagai sebuah planet. Kerahasiaan masa perang mencegah tim Universitas California menerbitkan penemuannya hingga tahun 1948.
Plutonium adalah unsur dengan nomor atom tertinggi yang terjadi di alam. Jumlah jejak plutonium muncul dalam endapan uranium-238 alami ketika uranium-238 menangkap neutron yang dipancarkan oleh peluruhan atom uranium-238 lainnya.
Baik plutonium-239 maupun plutonium-241 bersifat fisil, yang berarti bahwa mereka dapat mempertahankan reaksi rantai nuklir, yang mengarah pada aplikasi senjata nuklir dan reaktor nuklir. Plutonium-240 menunjukkan laju fisi spontan yang tinggi, meningkatkan fluks neutron dari setiap sampel yang mengandungnya. Kehadiran plutonium-240 membatasi kegunaan sampel plutonium untuk senjata atau kualitasnya sebagai bahan bakar reaktor, dan persentase plutonium-240 akan menentukan tingkatnya (tingkat senjata, tingkat bahan bakar, atau tingkat reaktor). Plutonium-238 memiliki waktu paruh 87,7 tahun dan memancarkan partikel alfa. Ia adalah sumber panas dalam generator termoelektrik radioisotop, yang digunakan untuk memberi daya pada beberapa wahana antariksa. Isotop plutonium berharga mahal dan tidak mudah untuk dipisahkan, sehingga isotop plutonium tertentu biasanya diproduksi dalam reaktor khusus.
Produksi plutonium dalam jumlah yang berguna untuk pertama kalinya merupakan bagian utama dari Proyek Manhattan selama Perang Dunia II yang mengembangkan bom atom pertama. Bomb Fat Man yang digunakan dalam uji coba nuklir Trinity pada Juli 1945, dan pengeboman Nagasaki pada Agustus 1945, memiliki inti plutonium. Eksperimen radiasi manusia yang mempelajari plutonium dilakukan tanpa persetujuan, dan beberapa kecelakaan kritis, beberapa mematikan, terjadi setelah perang. Pembuangan limbah plutonium dari pembangkit listrik tenaga nuklir dan pembongkaran senjata nuklir yang dibangun selama Perang Dingin adalah sebuah bentuk proliferasi nuklir dan kekhawatiran lingkungan. Sumber plutonium di lingkungan lainnya adalah hasil dari berbagai uji coba nuklir di atas tanah, yang sekarang telah dilarang.
Karakteristik
[sunting | sunting sumber]Sifat fisik
[sunting | sunting sumber]Plutonium, seperti kebanyakan logam lainnya, pada awalnya berwarna keperakan cerah, seperti nikel, tetapi ia teroksidasi dengan sangat cepat menjadi abu-abu kusam, meskipun kuning dan hijau zaitun juga pernah dilaporkan.[3][4] Pada suhu kamar, plutonium berada dalam fase-α (alfa)-nya. Bentuk ini, bentuk struktur unsur ini (alotrop) yang paling umum, sama keras dan rapuhnya dengan besi tuang kelabu kecuali jika ia dipadukan dengan logam lain untuk membuatnya lunak dan ulet. Berbeda dengan kebanyakan jenis logam, ia bukanlah konduktor panas atau listrik yang baik. Ia memiliki titik lebur yang rendah (640 °C, 1.184 °F) dan titik didih yang sangat tinggi (3.228 °C, 5.842 °F).[3] Ini memberikan kisaran suhu yang besar (lebarnya lebih dari 2.500 K) di mana plutonium berbentuk cair, tetapi kisaran ini bukanlah yang terbesar di antara semua aktinida maupun di antara semua logam.[5] Titik lebur yang rendah serta reaktivitas logam asli dibandingkan dengan oksida menyebabkan oksida plutonium menjadi bentuk yang lebih disukai untuk aplikasi seperti bahan bakar reaktor fisi nuklir (bahan bakar MOX).
Peluruhan alfa, pelepasan inti helium berenergi tinggi, adalah bentuk paling umum dari peluruhan plutonium.[6] 239Pu dengan massa 5 kg mengandung sekitar 12,5×1024 atom. Dengan waktu paruh 24.100 tahun, sekitar 11,5×1012 atomnya meluruh setiap detik dengan memancarkan partikel alfa 5,157 MeV. Nilai ini setara dengan 9,68 watt daya. Panas yang dihasilkan oleh perlambatan partikel alfa ini membuatnya hangat saat disentuh.[7][8] Karena waktu paruhnya yang jauh lebih pendek, 238Pu memanas hingga suhu yang jauh lebih tinggi dan bersinar merah panas dengan radiasi benda hitam jika dibiarkan tanpa pemanasan atau pendinginan eksternal. Panas ini telah digunakan dalam generator termoelektrik radioisotop (lihat di bawah).
Resistivitas adalah ukuran seberapa kuat suatu material melawan aliran arus listrik. Resistivitas plutonium pada suhu kamar sangatlah tinggi jika dibandingkan dengan logam lain dan ia akan semakin tinggi ketika suhu diturunkan, yang tidak biasa untuk logam.[9] Tren peningkatan resistivitas ini akan diteruskan hingga suhu 100 K. Di bawah suhu ini, resistivitas akan menurun drastis untuk sampel baru.[9] Resistivitas kemudian mulai meningkat kembali dengan waktu sekitar suhu 20 K karena kerusakan radiasi, dengan laju peningkatan ditentukan oleh komposisi isotop sampel.[9]
Karena adanya swairadiasi (self-irradiation), sampel plutonium akan mengalami kelelahan (fatigue) pada keseluruhan struktur kristalnya, yang berarti susunan atomnya yang teratur akan dikacaukan oleh radiasi tersebut dari waktu ke waktu.[10] Swairadiasi juga dapat menyebabkan penganilan yang dapat menetralkan beberapa efek kelelahan saat suhu meningkat di atas 100 K.[11]
Tidak seperti kebanyakan bahan, kepadatan plutonium meningkat ketika melebur, sebesar 2,5%, tetapi logam plutonium cair menunjukkan penurunan kepadatan linear dengan suhu.[9] Di dekat titik lebur, plutonium cair memiliki viskositas dan tegangan permukaan yang sangat tinggi dibandingkan dengan logam lainnya.[10]
Alotrop
[sunting | sunting sumber]
Plutonium biasanya memiliki enam alotrop dan membentuk alotrop ketujuh (zeta, ζ) pada suhu tinggi dalam kisaran tekanan terbatas.[12] Alotrop-alotrop ini, yang merupakan modifikasi struktural atau bentuk suatu unsur yang berbeda, memiliki energi internal yang sangat mirip tetapi kepadatan dan struktur kristal yang berbeda secara signifikan. Hal ini membuat plutonium sangat sensitif terhadap perubahan suhu, tekanan, atau kimia, dan memungkinkan perubahan volume yang dramatis mengikuti transisi fase dari satu bentuk alotropik ke bentuk lainnya.[10] Kepadatan berbagai alotrop plutonium bervariasi, mulai dari 16,00 g/cm3 hingga 19,86 g/cm3.[13]
Keberadaan banyak alotrop ini membuat pemesinan plutonium menjadi sangat sulit, karena ia sangat mudah berubah keadaan. Misalnya, fase-α eksis pada suhu kamar dalam plutonium murni. Ia memiliki karakteristik pemesinan yang mirip dengan besi tuang tetapi berubah menjadi fase-β (beta) plastik dan lunak pada suhu yang sedikit lebih tinggi.[14] Alasan mengapa plutonium memiliki diagram fase yang rumit belumlah sepenuhnya dipahami. Bentuk α memiliki struktur monoklinik dengan simetri rendah, sehingga ia rapuh, kuat, kompresibilitas, dan konduktivitas termal yang buruk.[12]
Plutonium dalam fase-δ (delta) umumnya terbentuk pada rentang suhu 310 °C hingga 452 °C, tetapi ia stabil pada suhu kamar saat dipadukan dengan galium, aluminium, atau cerium dalam persentase kecil, meningkatkan kemampuan kerjanya dan memungkinkannya untuk dilas.[14] Bentuk δ memiliki karakter logam yang lebih khas, dan kira-kira sama kuat dan lunaknya dengan aluminium.[12] Dalam senjata fisi, gelombang kejut eksplosif yang digunakan untuk menekan inti plutonium juga akan menyebabkan transisi dari plutonium fase-δ biasa ke fase-α yang lebih padat, yang secara signifikan membantunya mencapai superkritisitas.[butuh rujukan] Fase-ε (epsilon), alotrop padat suhu tertinggi, menunjukkan swadifusi atomik yang sangat tinggi dibandingkan dengan unsur lain.[10]
Fisi nuklir
[sunting | sunting sumber]
Plutonium adalah sebuah logam aktinida radioaktif yang isotopnya, plutonium-239, merupakan salah satu dari tiga isotop fisil utama (sisanya adalah uranium-233 dan uranium-235); plutonium-241 juga bersifat sangat fisil. Agar dapat dianggap fisil, inti atom dari suatu isotop harus dapat memecah (fisi) ketika ditembakkan dengan sebuah neutron yang bergerak lambat dan melepaskan sejumlah neutron tambahan yang cukup untuk mempertahankan reaksi rantai nuklir dengan memecahkan inti selanjutnya.[15]
Plutonium-239 murni dapat memiliki faktor penggandaan (keff) lebih besar dari satu, yang berarti bahwa jika logam tersebut tersedia dalam jumlah yang cukup dan dengan geometri yang sesuai (misalnya bola dengan ukuran yang cukup), ia dapat membentuk massa kritis.[16] Selama fisi, sebagian kecil dari energi pengikatan nuklir, yang mengikat inti agar tetap bersama, dilepaskan sebagai energi elektromagnetik dan kinetik dalam jumlah besar (sebagian besar energi kinetik diubah dengan cepat menjadi energi panas). Fisi satu kilogram plutonium-239 dapat menghasilkan ledakan yang setara dengan 21.000 ton TNT (88.000 GJ). Jumlah energi yang sangat besar inilah yang membuat plutonium-239 berguna dalam senjata dan reaktor nuklir.[7]
Keberadaan isotop plutonium-240 dalam suatu sampel akan membatasi potensi bom nuklir plutonium, karena plutonium-240 memiliki laju fisi spontan yang relatif tinggi (~440 fisi per detik per gram—lebih dari 1.000 neutron per detik per gram),[17] sehingga meningkatkan tingkat neutron latar, yang pada akhirnya akan meningkatkan risiko pradetonasi.[18] Plutonium dapat dikategorikan ke dalam berbagai tingkatan, yaitu tingkat senjata, tingkat bahan bakar, atau tingkat reaktor, bergantung pada persentase plutonium-240 yang dikandungnya. Plutonium tingkat senjata memiliki kadar plutonium-240 kurang dari 7%. Plutonium tingkat bahan bakar memiliki kadar plutonium-240 dari 7% hingga kurang dari 19%, dan tingkat reaktor daya memiliki kadar plutonium-240 sebesar 19% atau lebih. Plutonium tingkat super, dengan kadar plutonium-240 kurang dari 4%, digunakan dalam senjata Angkatan Laut A.S. yang disimpan di dekat awak kapal dan kapal selam, karena radioaktivitasnya yang lebih rendah.[19] Isotop plutonium-238 tidak bersifat fisil tetapi dapat mengalami fisi nuklir dengan mudah dengan neutron cepat serta dapat mengalami peluruhan alfa.[7] Semua isotop plutonium dapat "dibiakkan" menjadi bahan fisil dengan satu atau lebih absorpsi neutron, baik diikuti peluruhan beta atau tidak. Hal ini membuat isotop plutonium nonfisil menjadi bahan yang subur.
Isotop dan nukleosintesis
[sunting | sunting sumber]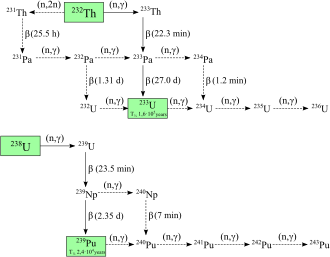
Terdapat setidaknya dua puluh isotop radioaktif plutonium yang telah dikarakterisasi. Isotop yang berumur paling panjang adalah plutonium-244, dengan waktu paruh 80,8 juta tahun, plutonium-242, dengan waktu paruh 373.300 tahun, dan plutonium-239, dengan waktu paruh 24.110 tahun. Semua isotop radioaktif yang tersisa memiliki waktu paruh kurang dari 7.000 tahun. Unsur ini juga memiliki delapan keadaan metastabil, meskipun semuanya memiliki waktu paruh kurang dari satu detik.[6] Plutonium-244 telah ditemukan di ruang antarbintang[20] dan ia memiliki waktu paruh terpanjang dari semua radioisotop nonprimordial.
Isotop plutonium yang diketahui memiliki nomor massa yang berkisar mulai dari 228 hingga 247. Mode peluruhan utama isotop dengan nomor massa lebih rendah dari isotop paling stabil, plutonium-244, adalah fisi spontan dan emisi alfa, sebagian besar membentuk isotop uranium (92 proton) dan neptunium (93 proton) sebagai produk peluruhan (dengan mengabaikan berbagai inti anak yang dihasilkan oleh proses fisi). Mode peluruhan utama untuk isotop dengan nomor massa lebih tinggi dari plutonium-244 adalah emisi beta, sebagian besar membentuk isotop amerisium (95 proton) sebagai produk peluruhan. Plutonium-241 merupakan isotop induk dari deret peluruhan neptunium, meluruh menjadi amerisium-241 melalui emisi beta.[6][21]
Plutonium-238 dan -239 adalah isotop yang paling sering disintesis.[7] Plutonium-239 disintesis melalui reaksi berikut yang menggunakan uranium (U) dan neutron (n) melalui peluruhan beta (β−) dengan neptunium (Np) sebagai perantara:[22]
Neutron yang berasal dari fisi uranium-235 ditangkap oleh inti uranium-238 untuk membentuk uranium-239; sebuah peluruhan beta akan mengubah neutron menjadi proton untuk membentuk neptunium-239 (waktu paruh 2,36 hari) dan peluruhan beta lebih lanjut akan membentuk plutonium-239.[23] Egon Bretscher yang mengerjakan proyek Tube Alloys Britania Raya memprediksikan reaksi ini secara teoretis pada tahun 1940.[24]
Plutonium-238 disintesis dengan membombardir uranium-238 dengan deuteron (D, inti hidrogen berat) dalam reaksi berikut:[25]
Dalam proses ini, deuteron yang menabrak uranium-238 menghasilkan dua neutron beserta neptunium-238, yang secara spontan meluruh dengan memancarkan partikel beta negatif untuk membentuk plutonium-238.[26] Plutonium-238 juga dapat diproduksi melalui penyinaran neutron dari neptunium-237.[27]
Panas peluruhan dan sifat fisi
[sunting | sunting sumber]Isotop plutonium mengalami peluruhan radioaktif dan menghasilkan panas peluruhan. Isotop yang berbeda menghasilkan jumlah panas per massa yang berbeda. Panas peluruhan biasanya dinyatakan dengan satuan watt/kilogram, atau miliwatt/gram. Pada potongan plutonium yang lebih besar (misalnya lubang senjata) dan pembuangan panas yang tidak memadai, pemanasan sendiri yang dihasilkan dapat berdampak signifikan.
| Isotop | Mode peluruhan | Waktu paruh (tahun) | Panas peluruhan (W/kg) | Neutron fisi spontan (1/(g·s)) | Komentar |
|---|---|---|---|---|---|
| 238Pu | alfa menjadi 234U | 87,74 | 560 | 2600 | Panas peluruhan sangat tinggi. Dalam jumlah kecilpun berdampak signifikan. Digunakan pada generator termoelektrik radioisotop. |
| 239Pu | alfa menjadi 235U | 24100 | 1,9 | 0,022 | Isotop fisil utama yang banyak digunakan. |
| 240Pu | alfa menjadi 236U, fisi spontan | 6560 | 6,8 | 910 | Pengotor utama dalam sampel isotop 239Pu. Tingkat plutonium biasanya dinyatakan dalam persentase 240Pu. Fisi spontan yang tinggi menghalangi penggunaan pada senjata nuklir. |
| 241Pu | beta-minus, menjadi 241Am | 14,4 | 4,2 | 0,049 | Meluruh menjadi amerisium-241; penumpukannya menghadirkan bahaya radiasi pada sampel yang lebih tua. |
| 242Pu | alfa menjadi 238U | 376000 | 0,1 | 1700 | 242Pu meluruh menjadi 238U melalui peluruhan alfa; ia juga akan meluruh melalui fisi spontan. |
Sifat kimia dan senyawa
[sunting | sunting sumber]
Pada suhu kamar, plutonium murni berwarna keperakan tetapi berubah menjadi kusam saat teroksidasi.[29] Unsur ini menunjukkan empat keadaan oksidasi ionik yang umum dalam larutan berair dan satu yang langka:[13]
- Pu(III), sebagai Pu3+ (biru lavender)
- Pu(IV), sebagai Pu4+ (kuning cokelat)
- Pu(V), sebagai PuO+2 (pink muda)[note 1]
- Pu(VI), sebagai PuO2+2 (pink oranye)
- Pu(VII), sebagai PuO3−5 (hijau)—ion heptavalen yang jarang terjadi.
Warna yang ditunjukkan oleh larutan plutonium bergantung pada keadaan oksidasi dan sifat-sifat anion asam.[31] Anion asamlah yang memengaruhi derajat pengompleksan—bagaimana atom terhubung ke atom pusat—spesies plutonium. Selain itu, keadaan oksidasi plutonium formal +2 diketahui dalam kompleks [K(2.2.2-kriptan)] [PuIICp″3], Cp″ = C5H3(SiMe3)2.[32]
Keadaan oksidasi +8 juga dimungkinkan dalam plutonium tetroksida PuO4 yang volatil.[33] Meskipun ia mudah terurai melalui mekanisme reduksi yang mirip dengan FeO4, PuO4 dapat distabilkan dalam larutan basa dan kloroform.[33][34]
Logam plutonium diproduksi dengan mereaksikan plutonium(IV) fluorida dengan barium, kalsium atau litium pada suhu 1200 °C.[35] Logam plutonium akan diserang oleh asam, oksigen, dan uap, tetapi tidak oleh alkali dan mudah larut dalam asam klorida, iodida, dan perklorat pekat.[36] Leburan logam plutonium harus disimpan dalam ruang hampa atau atmosfer lengai untuk menghindari terjadinya reaksi dengan udara.[14] Pada suhu 135 °C logam plutonium akan menyala di udara dan akan meledak jika diletakkan dalam karbon tetraklorida.[37]

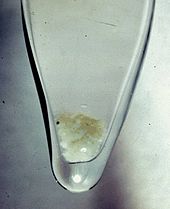
Plutonium merupakan logam yang reaktif. Di udara lembap atau argon lembap, logam ini akan teroksidasi dengan cepat, menghasilkan campuran oksida dan hidrida.[3] Jika logam ini terpapar cukup lama dengan sejumlah uap air dalam jumlah terbatas, lapisan permukaan PuO2 berbentuk bubuk yang membungkus logam akan terbentuk.[3] Selain itu, juga terbentuk plutonium hidrida. Apabila terpapar dengan uap air yang berlebihan, hanya akan terbentuk PuO2.[36]
Plutonium menunjukkan laju reaksi yang sangat besar dan dapat dibalik dengan hidrogen murni, membentuk plutonium hidrida.[10] Ia juga mudah bereaksi dengan oksigen, membentuk PuO dan PuO2 serta oksida intermediat; plutonium oksida mengisi volume 40% lebih banyak daripada logam plutonium. Logam ini bereaksi dengan halogen, menghasilkan senyawa dengan rumus umum PuX3 di mana X dapat berupa F, Cl, Br atau I dan PuF4 juga telah terlihat. Oksihalida berikut telah teramati: PuOCl, PuOBr dan PuOI. Ia akan bereaksi dengan karbon untuk membentuk PuC, nitrogen untuk membentuk PuN dan silikon untuk membentuk PuSi2.[13][37]
Kimia organologam kompleks plutonium sangat khas untuk spesies organoaktinida; contoh karakteristik senyawa organoplutonium adalah plutonosena.[23][38] Metode kimia komputasi menunjukkan karakter kovalen yang ditingkatkan dalam ikatan plutonium–ligan.[10][38]
Serbuk plutonium, hidridanya, dan oksida tertentunya seperti Pu2O3 bersifat piroforik, artinya mereka dapat menyala secara spontan pada suhu sekitar sehingga harus ditangani dalam atmosfer nitrogen atau argon yang lengai dan kering. Plutonium curah hanya menyala ketika dipanaskan di atas suhu 400 °C. Pu2O3 secara spontan memanas dan berubah menjadi PuO2, yang stabil di udara kering, tetapi bereaksi dengan uap air saat dipanaskan.[39]
Krus yang digunakan untuk mengandung plutonium haruslah tahan terhadap lingkungan reduksi yang kuat. Logam tahan api seperti tantalum dan wolfram beserta dengan oksida, borida, karbida, nitrida, dan silisida yang lebih stabil dapat menoleransi lingkungan seperti ini. Peleburan dalam tanur busur listrik dapat digunakan untuk menghasilkan batangan logam kecil tanpa memerlukan krus.[14]
Serium digunakan sebagai tiruan kimia plutonium untuk pengembangan penahanan, ekstraksi, dan teknologi lainnya.[40]
Struktur elektronik
[sunting | sunting sumber]Plutonium adalah sebuah unsur di mana elektron 5f adalah batas transisi antara terdelokalisasi dan terlokalisasi; oleh karena itu, ia dianggap sebagai salah satu unsur yang paling kompleks.[41] Perilaku anomali plutonium disebabkan oleh struktur elektroniknya. Perbedaan energi antara subkulit 6d dan 5f sangatlah rendah. Ukuran kulit 5f cukup untuk memungkinkan elektron membentuk ikatan di dalam kisi, pada batas antara perilaku terlokalisasi dan pengikatan. Kedekatan tingkat energi menyebabkan adanya beberapa konfigurasi elektron berenergi rendah dengan tingkat energi yang hampir sama. Hal ini menyebabkan konfigurasi 5fn7s2 dan 5fn−16d17s2 bersaing, yang menyebabkan kompleksitas perilaku kimianya. Sifat orbital 5f yang sangat terarah bertanggung jawab atas ikatan kovalen terarah dalam molekul dan kompleks plutonium.[10]
Paduan
[sunting | sunting sumber]Plutonium dapat membentuk paduan dan senyawa intermediat dengan sebagian besar logam lainnya. Pengecualiannya meliputi litium, natrium, kalium, rubidium, dan sesium dari logam alkali; magnesium, kalsium, stronsium, dan barium dari logam alkali tanah; serta europium dan iterbium dari logam tanah jarang.[36] Pengecualian sebagian meliputi logam tahan api kromium, molibdenum, niobium, tantalum, dan wolfram, yang larut dalam plutonium cair, tetapi tidak larut atau hanya sedikit larut dalam plutonium padat.[36] Galium, aluminium, amerisium, skandium dan serium dapat menstabilkan fase-δ plutonium dalam suhu kamar. Silikon, indium, seng, dan zirkonium memungkinkan pembentukan keadaan-δ metastabil ketika didinginkan dengan cepat. Jumlah hafnium, holmium, dan talium yang tinggi juga dapat mempertahankan fase-δ pada suhu kamar. Neptunium adalah satu-satunya unsur yang dapat menstabilkan fase-α pada suhu yang lebih tinggi.[10]
Paduan plutonium dapat diproduksi dengan menambahkan sebuah logam ke plutonium cair. Jika logam pemadu cukup reduktif, plutonium dapat ditambahkan dalam bentuk oksida atau halida. Paduan plutonium–galium dan plutonium–aluminium fase-δ diproduksi dengan menambahkan plutonium(III) fluorida pada galium atau aluminium cair, yang memiliki keuntungan untuk menghindari kontak langsung dengan logam plutonium yang sangat reaktif.[42]
- Paduan plutonium–galium digunakan untuk menstabilkan fase-δ plutonium, menghindari masalah terkait fase-α dan α–δ. Penggunaan utamanya adalah pada biji senjata nuklir delakan.[43]
- Paduan plutonium–aluminium adalah alternatif paduan Pu–Ga. Ia adalah unsur asli yang dipertimbangkan untuk stabilisasi fase-δ, tetapi kecenderungannya untuk bereaksi dengan partikel alfa dan melepaskan neutron mengurangi kegunaannya untuk biji senjata nuklir. Paduan plutonium–aluminium juga dapat digunakan sebagai komponen bahan bakar nuklir.[44]
- Paduan plutonium–galium–kobalt (PuCoGa5) adalah superkonduktor yang tidak konvensional, menunjukkan superkonduktivitas di bawah 18,5 K, satu urutan besar lebih tinggi dari yang tertinggi di antara sistem fermion berat, dan memiliki arus kritis yang besar.[41][45]
- Paduan plutonium–zirkonium dapat digunakan sebagai bahan bakar nuklir.[46]
- Paduan plutonium–serium dan plutonium–serium–kobalt digunakan sebagai bahan bakar nuklir.[47]
- Paduan plutonium–uranium, dengan kandungan plutonium sekitar 15–30 mol.%, dapat digunakan sebagai bahan bakar nuklir untuk reaktor pembiak cepat. Sifatnya yang piroforik dan kerentanannya yang tinggi terhadap korosi hingga dapat menyala sendiri atau swadisintegrasi setelah terpapar udara membutuhkan paduan dengan komponen lain. Penambahan aluminium, karbon atau tembaga tidak meningkatkan laju disintegrasi secara nyata, paduan zirkonium dan besi memiliki ketahanan korosi yang lebih baik tetapi juga terdisintegrasi dalam beberapa bulan di udara. Penambahan titanium dan/atau zirkonium akan meningkatkan titik lebur paduan secara signifikan.[48]
- Paduan plutonium–uranium–titanium dan plutonium–uranium–zirkonium telah diteliti untuk digunakan sebagai bahan bakar nuklir. Penambahan unsur ketiga meningkatkan ketahanan korosi, mengurangi sifat mudah terbakar, dan meningkatkan keuletan, fabrikabilitas, kekuatan, dan ekspansi termal. Paduan plutonium–uranium–molibdenum memiliki ketahanan korosi terbaik, membentuk lapisan pelindung oksida, tetapi titanium dan zirkonium lebih disukai karena alasan fisika.[48]
- Paduan torium–uranium–plutonium telah diteliti sebagai bahan bakar nuklir untuk reaktor pembiak cepat.[48]
Keterjadian
[sunting | sunting sumber]
Sejumlah kecil isotop plutonium-238, plutonium-239, plutonium-240, dan plutonium-dapat ditemukan di alam. Jumlah plutonium-239 yang lebih kecil lagi, beberapa bagian per triliun, dan produk peluruhannya secara alami ditemukan di beberapa bijih uranium terkonsentrasi,[49] seperti reaktor fisi nuklir alami di Oklo, Gabon.[50] Rasio plutonium-239 terhadap uranium di deposit uranium Tambang Cigar Lake berkisar antara 2,4×10−12 hingga 44×10−12.[51] Jumlah kecil 239Pu ini berasal dari cara berikut: pada kesempatan langka, 238U mengalami fisi spontan, dan dalam prosesnya, ia memancarkan satu atau dua neutron bebas dengan sejumlah energi kinetik. Ketika salah satu neutron ini menumbuk inti atom 238U lainnya, ia diserap oleh atom itu, yang menjadi 239U. Dengan waktu paruh yang relatif singkat, 239U meluruh menjadi 239Np, yang kemudian meluruh menjadi 239Pu.[52][53] Akhirnya, sejumlah kecil plutonium-238, dikaitkan dengan peluruhan beta ganda uranium-238 yang sangat langka, telah ditemukan dalam sampel uranium alami.[54]
Karena waktu paruhnya yang relatif panjang, yaitu sekitar 80 juta tahun, diperkirakan bahwa plutonium-244 terjadi secara alami sebagai nuklida primordial, tetapi laporan awal pendeteksiannya tidak dapat dikonfirmasikan.[55] Namun, waktu paruhnya yang panjang memastikan peredarannya melintasi Tata Surya sebelum kepunahannya,[56] dan memang, bukti fisi spontan dari 244Pu yang telah punah telah ditemukan pada beberapa meteorit.[57] Kehadiran 244Pu sebelumnya di Tata Surya awal telah dikonfirmasi, karena ia memanifestasikan dirinya sekarang sebagai surplus dari produk peluruhannya, baik 232Th (dari jalur peluruhan alfa) ataupun isotop xenon (dari fisi spontannya). Yang terakhir umumnya lebih berguna, karena sifat kimia torium dan plutonium agak mirip (keduanya utamanya tetravalen) sehingga surplus torium tidak akan menjadi bukti kuat bahwa beberapa di antaranya terbentuk sebagai produk peluruhan plutonium.[58] 244Pu memiliki waktu paruh terpanjang dari semua nuklida transuranium dan hanya diproduksi dalam proses-r pada supernova dan bintang neutron yang bertabrakan; ketika inti dikeluarkan dari peristiwa ini dengan kecepatan tinggi untuk mencapai Bumi, hanya 244Pu di antara seluruh nuklida transuranium yang memiliki waktu paruh yang cukup lama untuk bertahan dalam perjalanan, sehingga jejak kecil 244Pu antarbintang telah ditemukan di dasar laut dalam. Karena 240Pu juga terjadi dalam rantai peluruhan 244Pu, ia juga harus hadir dalam kesetimbangan sekuler, meskipun dalam jumlah yang lebih kecil.[59]
Sejumlah kecil plutonium biasanya ditemukan pada tubuh manusia akibat dari 550 uji coba nuklir di atmosfer dan bawah air serta beberapa kecelakaan nuklir besar yang pernah terjadi.[37] Sebagian besar pengujian nuklir atmosfer dan bawah air dihentikan oleh Traktat Pelarangan Uji Nuklir Sebagian pada tahun 1963, yang mana kekuatan nuklir ditandatangani dan diratifikasi oleh Amerika Serikat, Britania Raya, dan Uni Soviet. Prancis melanjutkan uji coba nuklir atmosfer hingga 1974 dan Tiongkok melanjutkan uji coba nuklir atmosfer hingga 1980. Semua uji coba nuklir selanjutnya dilakukan di bawah tanah.[60]
Sejarah
[sunting | sunting sumber]Penemuan
[sunting | sunting sumber]Pada tahun 1934, Enrico Fermi dan sekelompok ilmuwan Universitas Roma melaporkan bahwa mereka telah menemukan unsur 94.[61] Fermi menyebut unsur ini sebagai hesperium dan menyebutkannya dalam Kuliah Nobelnya pada tahun 1938.[62] Sampel tersebut sebenarnya mengandung produk fisi nuklir, terutama barium dan kripton.[63] Fisi nuklir, ditemukan di Jerman pada tahun 1938 oleh Otto Hahn dan Fritz Strassmann, belum diketahui pada saat itu.[64]

Plutonium (khususnya, plutonium-238) pertama kali diproduksi, diisolasi dan kemudian diidentifikasi secara kimiawi antara Desember 1940 dan Februari 1941 oleh Glenn T. Seaborg, Edwin McMillan, Emilio Segrè, Joseph W. Kennedy, dan Arthur Wahl melalui pemborbardiran deuteron terhadap uranium dalam siklotron 60-inci (150 cm) di Laboratorium Radiasi Berkeley di Universitas California, Berkeley.[65][66][67] Neptunium-238 diciptakan langsung oleh pemborbardiran itu tetapi meluruh melalui emisi beta dengan waktu paruh lebih dari dua hari, yang menunjukkan pembentukan unsur 94.[37] Pemborbardiran pertama terjadi pada 14 Desember 1940, dan unsur baru itu pertama kali diidentifikasi melalui oksidasi pada malam tanggal 23–24 Februari 1941.[66]
Sebuah makalah yang mendokumentasikan penemuan tersebut disiapkan oleh tim dan dikirim ke jurnal Physical Review pada Maret 1941,[37] namun publikasi ditunda hingga setahun setelah berakhirnya Perang Dunia II karena masalah keamanan.[68] Di Laboratorium Cavendish di Cambridge, Egon Bretscher dan Norman Feather menyadari bahwa reaktor neutron lambat berbahan bakar uranium secara teoretis akan menghasilkan sejumlah besar plutonium-239 sebagai produk sampingan. Mereka menghitung bahwa unsur 94 akan bersifat fisil, dan memiliki keuntungan tambahan karena secara kimiawi berbeda dari uranium, dan dapat dengan mudah dipisahkan darinya.[24]
Edwin McMillan yang sebelumnya telah menamai unsur transuranium pertama dengan nama neptunium (berasal dari nama planet Neptunus) mengajukan bahwa unsur 94, sebagai unsur transuranium kedua, dinamai dari planet Pluto.[7][note 2] Nicholas Kemmer dari tim Cambridge secara independen mengusulkan nama yang sama, berdasarkan alasan yang sama dengan tim Berkeley.[24] Seaborg pada awalnya mempertimbangkan nama "plutium", namun kemudian merasa bahwa nama tersebut tidak sebagus "plutonium".[70] Dia memilih lambang "Pu" pada awalnya hanyalah sebagai lelucon, mengacu pada kata seru "P U" (Pee-yoo) untuk menunjukkan bau yang sangat menjijikkan, namun ternyata lambang tersebut kemudian tanpa disadari telah terdaftar ke dalam tabel periodik.[note 3] Nama alternatif yang dipertimbangkan oleh Seaborg dan lainnya adalah "ultimium" atau "extremium" karena terdapat kepercayaan bahwa mereka telah menemukan kemungkinan unsur terakhir pada tabel periodik.[72]
Hahn dan Strassmann, dan secara terpisah Kurt Starke, pada saat itu juga mengerjakan unsur transuranium di Berlin. Tampaknya Hahn dan Strassmann menyadari bahwa plutonium-239 seharusnya bersifat fisil. Namun, mereka tidak memiliki sumber neutron yang kuat. Unsur 93 dilaporkan oleh Hahn dan Strassmann, serta Starke, pada tahun 1942. Tim Hahn tidak mengejar unsur 94, mungkin karena mereka patah semangat karena McMillan dan Abelson tidak berhasil mengisolasinya ketika mereka pertama kali menemukan unsur 93. Namun, karena tim Hahn memiliki akses ke siklotron yang lebih kuat di Paris pada saat itu, mereka kemungkinan besar dapat mendeteksi plutonium seandainya mereka mencobanya, meskipun dalam jumlah kecil (beberapa becquerel).[73]
Penelitian awal
[sunting | sunting sumber]
Sifat-sifat kimia plutonium ditemukan menyerupai uranium setelah dilakukan kajian awal selama beberapa bulan.[37] Penelitian awal dilanjutkan di Met Lab rahasia Universitas Chicago. Pada tanggal 20 Agustus 1942, sejumlah kecil unsur ini diisolasi dan diukur untuk pertama kalinya. Sekitar 50 mikrogram plutonium-239 yang dikombinasikan dengan uranium dan produk fisi dihasilkan, namun hanya sekitar 1 mikrogram yang berhasil diisolasi.[49][74] Prosedur ini memungkinkan para kimiawan untuk menentukan berat atom unsur baru ini.[75][note 4] Pada tanggal 2 Desember 1942, di lapangan raket di bawah tribun barat di Lapangan Stagg Universitas Chicago, para peneliti yang dipimpin oleh Enrico Fermi mencapai reaksi rantai mandiri pertama dalam tumpukan grafit dan uranium yang dikenal sebagai CP-1. Menggunakan informasi teoretis yang dikumpulkan dari pengoperasian CP-1, DuPont membangun reaktor produksi eksperimental berpendingin udara, yang dikenal sebagai X-10, dan fasilitas pemisahan bahan kimia percontohan di Oak Ridge. Fasilitas pemisahan, menggunakan metode yang dikembangkan oleh Glenn T. Seaborg dan tim peneliti di Met Lab, menghilangkan plutonium dari uranium yang disinari dalam reaktor X-10. Informasi dari CP-1 juga berguna bagi ilmuwan Met Lab yang merancang reaktor produksi plutonium berpendingin air untuk Hanford. Konstruksi di tempat tersebut dimulai pada pertengahan 1943.[76]
Pada bulan November 1943, beberapa plutonium trifluorida direduksi untuk membuat sampel logam plutonium pertama: beberapa mikrogram manik-manik logam.[49] Plutonium yang dihasilkan cukup banyak untuk membuatnya menjadi unsur sintetis pertama yang terlihat dengan mata telanjang.[77]
Sifat-sifat nuklir plutonium-239 juga dikaji; para peneliti menemukan bahwa ketika dihantam oleh neutron, ia akan memecah (fisi) dengan melepaskan lebih banyak neutron dan energi. Neutron ini kemudian dapat menghantam atom plutonium-239 lainnya, dan mengakibatkan reaksi rantai yang meningkat secara eksponensial. Reaksi rantai ini dapat mengakibatkan ledakan yang cukup besar untuk menghancurkan sebuah kota jika cukup banyak isotop yang terkonsentrasi untuk mencapai massa kritis.[37]
Selama tahap awal penelitian, beberapa hewan digunakan untuk mempelajari efek zat radioaktif terhadap kesehatan. Studi ini dimulai pada tahun 1944 di Universitas California di Laboratorium Radiasi Berkeley dan dilakukan oleh Joseph G. Hamilton. Hamilton ingin menjawab pertanyaan mengenai bagaimana plutonium akan bervariasi dalam tubuh tergantung pada mode paparan (ingesti oral, inhalasi, absorpsi melalui kulit), tingkat retensi, dan bagaimana plutonium akan diperbaiki dalam jaringan dan didistribusikan di antara berbagai organ. Hamilton mulai memberikan bagian mikrogram terlarut dari senyawa plutonium-239 kepada tikus menggunakan keadaan valensi yang berbeda dan metode yang berbeda untuk memasukkan plutonium (secara oral, intravena, dll.). Akhirnya, laboratorium di Chicago juga melakukan eksperimen injeksi plutoniumnya sendiri dengan menggunakan berbagai hewan seperti tikus, kelinci, ikan, dan bahkan anjing. Hasil penelitian di Berkeley dan Chicago menunjukkan bahwa perilaku fisiologis plutonium berbeda secara signifikan dengan radium. Hasil yang paling mengkhawatirkan adalah adanya pengendapan plutonium yang signifikan di hati dan di bagian tulang yang "bermetabolisme aktif". Selain itu, laju eliminasi plutonium dalam ekskreta berbeda di antara spesies hewan sebanyak lima kali lipat. Variasi seperti itu membuat sangat sulit untuk memperkirakan berapa lajunya bagi manusia.[78]
Produksi semasa Proyek Manhattan
[sunting | sunting sumber]Semasa Perang Dunia II, pemerintah AS mencanangkan Proyek Manhattan yang ditugaskan untuk mengembangkan bom atom. Tiga tempat penelitian dan produksi utama dari proyek ini adalah fasilitas produksi plutonium di tempat yang sekarang menjadi Situs Hanford, fasilitas pengayaan uranium di Oak Ridge, Tennessee, dan laboratorium penelitian dan desain senjata yang sekarang ini dikenal sebagai Laboratorium Nasional Los Alamos.[79]


Reaktor produksi pertama yang memproduksi plutonium-239 adalah Reaktor Grafit X-10. Ia mulai bekerja pada tahun 1943 dan dibangun di sebuah fasilitas di Oak Ridge yang kemudian menjadi Laboratorium Nasional Oak Ridge.[37][note 5]
Pada bulan Januari 1944, para pekerja meletakkan fondasi untuk gedung pemisahan bahan kimia pertama, Pabrik T yang berlokasi di 200-West. Pabrik T dan fasilitas saudaranya di 200-West, Pabrik U, selesai pada bulan Oktober. (Pabrik U hanya digunakan untuk pelatihan selama Proyek Manhattan.) Gedung pemisahan di 200-East, Pabrik B, selesai pada Februari 1945. Fasilitas kedua yang direncanakan untuk 200-East dibatalkan. Dijuluki Queen Marys oleh para pekerja yang membangunnya, bangunan pemisah itu adalah struktur seperti ngarai yang mengagumkan dengan panjang 800 kaki, lebar 65 kaki, dan tinggi 80 kaki yang berisi empat puluh kolam proses. Interiornya memiliki kualitas yang menakutkan karena operator di balik pelindung beton setinggi tujuh kaki memanipulasi peralatan kendali jarak jauh dengan melihat melalui monitor televisi dan periskop dari galeri atas. Bahkan dengan penutup beton masif pada kolam proses, tindakan pencegahan terhadap paparan radiasi diperlukan dan memengaruhi semua aspek desain pabrik.[76]
Pada 5 April 1944, Emilio Segrè yang berada di Los Alamos menerima sampel pertama plutonium yang dihasilkan oleh reaktor dari Oak Ridge.[81] Dalam waktu sepuluh hari, dia menemukan bahwa plutonium yang dihasilkan itu memiliki konsentrasi isotop plutonium-240 yang lebih tinggi daripada plutonium yang dihasilkan dari siklotron. Plutonium-240 memiliki laju fisi spontan yang tinggi dan akan meningkatkan tingkat neutron latar sampel plutonium.[82] Senjata plutonium jenis bedil asli, dengan nama kode "Thin Man", terpaksa dibatalkan karena peningkatan jumlah neutron spontan akan meningkatkan probabilitas terjadinya pradetonasi nuklir.[83]
Desain senjata plutonium yang dikerjakan di Los Alamos kemudian diubah menjadi bentuk delakan yang lebih rumit, diberi nama kode "Fat Man". Dengan senjata delakan, plutonium dikompresi hingga kepadatan tinggi dengan lensa ledak—tugas yang secara teknis lebih menakutkan daripada desain jenis bedil sederhana, tetapi perlu menggunakan plutonium untuk keperluan senjata. Sebaliknya, uranium yang diperkaya dapat digunakan dengan kedua metode tersebut.[83]
Konstruksi Reaktor B Hanford, reaktor nuklir berskala industri yang pertama untuk keperluan produksi bahan, diselesaikan pada Maret 1945. Reaktor B memroduksi bahan fisil yang digunakan untuk senjata plutonium yang digunakan semasa Perang Dunia II.[note 6] B, D dan F adalah reaktor awal yang dibangun di Hanford, dan enam reaktor penghasil plutonium tambahan dibangun kemudian di lokasi tersebut.[86]
Pada akhir Januari 1945, plutonium yang sangat murni menjalani konsentrasi lebih lanjut di gedung isolasi kimia yang telah selesai, di mana pengotor yang tersisa berhasil dihilangkan. Los Alamos menerima plutonium pertamanya dari Hanford pada tanggal 2 Februari. Meskipun masih belum jelas bahwa plutonium yang cukup dapat diproduksi untuk digunakan dalam bom pada akhir perang, Hanford beroperasi pada awal 1945. Hanya dua tahun telah berlalu sejak Kolonel Franklin Matthias pertama kali mendirikan markas sementaranya di tepi Sungai Columbia.[76]
Menurut Kate Brown, pabrik produksi plutonium di Hanford dan Mayak di Rusia, selama empat dekade, "keduanya telah melepaskan lebih dari 200 juta curie isotop radioaktif ke lingkungan sekitarnya—dua kali jumlah yang dikeluarkan dalam bencana Chernobyl di setiap kejadian".[87] Sebagian besar kontaminasi radioaktif ini selama bertahun-tahun merupakan bagian dari operasi normal, tetapi kecelakaan tak terduga memang terjadi dan manajemen pabrik merahasiakan hal ini, karena polusi terus berlanjut.[87]
Pada tahun 2004, sebuah brankas ditemukan selama penggalian parit pemakaman di situs nuklir Hanford. Di dalam brankas tersebut terdapat berbagai barang, termasuk botol kaca besar berisi bubur keputihan yang kemudian diidentifikasi sebagai sampel plutonium tingkat senjata tertua yang diketahui ada. Analisis isotop yang dilakukan oleh Laboratorium Nasional Pacific Northwest menunjukkan bahwa plutonium dalam botol tersebut diproduksi di Reaktor Grafit X-10 di Oak Ridge pada tahun 1944.[88][89][90]
Bom atom Trinity dan Fat Man
[sunting | sunting sumber]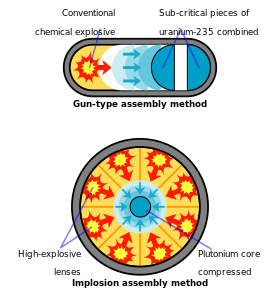
Uji bom atom pertama, diberi nama kode "Trinity" dan didetonasi pada 16 Juli 1945 dekat Alamogordo, New Mexico, menggunakan plutonium sebagai bahan fisilnya.[49] Desain delakan "gawai", sebagaimana perangkat Trinity diberi nama kode, menggunakan lensa-lensa ledak yang digunakan untuk mengompres bola plutonium agar mencapai massa superkritis, yang secara bersamaan dihujani dengan neutron dari "Urchin", sebuah inisiator yang terbuat dari polonium dan berilium (sumber neutron: reaksi (α, n)).[37] Dengan demikian, ia akan menjamin terjadinya reaksi berantai dan ledakan. Keseluruhan senjata ini memiliki berat lebih dari 4 ton, walaupun plutonium yang digunakan pada inti senjata hanyalah seberat 6,2 kg.[91] Sekitar 20% plutonium yang digunakan dalam senjata Trinity mengalami fisi, menghasilkan ledakan dengan energi yang setara dengan kira-kira 20.000 ton TNT.[92][note 7]
Desain identik yang digunakan pada bom atom "Fat Man" yang dijatuhkan di Nagasaki, Jepang, pada 9 Agustus 1945, menewaskan 35.000–40.000 orang dan menghancurkan 68%–80% produksi perang di Nagasaki.[94] Hanya setelah pengumuman bom atom pertama inilah keberadaan dan nama plutonium diketahui publik oleh Laporan Smyth milik Proyek Manhattan.[95]
Penggunaan pada Perang Dingin dan limbah
[sunting | sunting sumber]Sejumlah besar timbunan plutonium tingkat senjata diproduksi oleh Uni Soviet dan Amerika Serikat selama Perang Dingin. Reaktor-reaktor milik Amerika Serikat di Hanford dan Situs Sungai Savannah di Carolina Selatan memroduksi 103 ton plutonium,[96] dan diperkirakan 170 ton plutonium tingkat militer diproduksi di Uni Soviet.[97][note 8] Setiap tahun, sekitar 20 ton unsur ini masih diproduksi sebagai produk sampingan industri tenaga nuklir.[13] Sebanyak 1000 ton plutonium masih berada dalam penyimpanan, dengan 200 ton di antaranya berada di dalam atau diekstraksi dari senjata nuklir.[37] SIPRI memperkirakan stok plutonium dunia pada tahun 2007 sekitar 500 ton, dibagi rata antara stok senjata dan sipil.[99]

Kontaminasi radioaktif di Pabrik Rocky Flats terutama dihasilkan dari dua kebakaran plutonium besar pada tahun 1957 dan 1969. Konsentrasi isotop radioaktif yang jauh lebih rendah dilepaskan selama masa operasional pabrik dari tahun 1952 hingga 1992. Angin yang bertiup dari pabrik membawa kontaminasi udara ke selatan dan timur, ke daerah berpenduduk di barat laut Denver. Kontaminasi wilayah Denver oleh plutonium dari kebakaran dan sumber lainnya tidak dilaporkan secara terbuka hingga tahun 1970-an. Menurut sebuah studi tahun 1972 yang ditulis bersama oleh Edward Martell, "Di daerah yang lebih padat penduduknya di Denver, tingkat kontaminasi Pu di permukaan tanah beberapa kali lipat", dan kontaminasi plutonium "tepat di sebelah timur pabrik Rocky Flats berkisar hingga ratusan kali lipat dari uji coba nuklir".[100] Seperti yang dicatat oleh Carl Johnson dalam Ambio, "Paparan populasi besar di wilayah Denver terhadap plutonium dan radionuklida lainnya dalam asap buangan dari pabrik berasal dari tahun 1953."[101] Produksi senjata di pabrik Rocky Flats dihentikan setelah serangan gabungan FBI dan EPA pada tahun 1989 dan protes selama bertahun-tahun. Pabrik tersebut telah ditutup, dengan bangunannya sepenuhnya dihancurkan dari lokasi tersebut.[102]
Di A.S., beberapa plutonium yang diekstrak dari senjata nuklir yang dibongkar dileburkan untuk membentuk gelondongan kaca plutonium oksida seberat dua ton.[37] Kaca tersebut terbuat dari borosilikat yang dicampur dengan kadmium dan gadolinium.[note 9] Gelondongan-gelodongan ini direncanakan ditutup dengan baja nirkarat dan disimpan sejauh 4 km (2 mi) di bawah tanah dalam lubang bor yang akan ditimbun kembali dengan beton.[37] A.S. berencana untuk menyimpan plutonium dengan cara ini di repositori limbah nuklir Gunung Yucca, yang berjarak sekitar 100 mil (160 km) sebelah timur laut Las Vegas, Nevada.[103]
Pada tanggal 5 Maret 2009, Menteri Energi A.S. Steven Chu mengatakan pada sidang Senat "situs Gunung Yucca tidak lagi dipandang sebagai pilihan untuk menyimpan limbah reaktor".[104] Mulai tahun 1999, limbah nuklir yang dihasilkan militer dikubur di Pabrik Percontohan Isolasi Limbah di New Mexico.
Dalam Memorandum Presiden tertanggal 29 Januari 2010, Presiden Obama membentuk Komisi Pita Biru untuk Masa Depan Nuklir Amerika.[105] Dalam laporan akhir mereka, Komisi tersebut menyampaikan rekomendasi untuk mengembangkan strategi komprehensif yang harus dilakukan, termasuk:[106]
- "Rekomendasi #1: Amerika Serikat harus melakukan program pengelolaan limbah nuklir terpadu yang mengarah pada pengembangan tepat waktu dari satu atau lebih fasilitas geologi dalam permanen untuk pembuangan bahan bakar bekas dan limbah nuklir tingkat tinggi secara aman".[106]
Eksperimen medis
[sunting | sunting sumber]Semasa dan setelah berakhirnya Perang Dunia II, para ilmuwan yang terlibat dalam Proyek Manhattan dan proyek-proyek penelitian senjata nuklir lainnya melakukan berbagai kajian pada efek plutonium terhadap hewan dan manusia.[107] Pada kajian hewan, ditemukan bahwa beberapa miligram plutonium per kilogram jaringan tubuh merupakan dosis yang mematikan.[108]
Sedangkan pada kasus percobaan pada manusia, disuntikkan larutan yang (biasanya) mengandung lima mikrogram plutonium ke tubuh pasien rumah sakit yang telah menderita sakit parah ataupun yang memiliki tingkat harapan hidup yang lebih kecil dari sepuluh tahun baik oleh karena usia maupun kondisi penyakit yang kronis.[107] Kadar suntikan ini diturunkan menjadi satu mikrogram pada Juli 1945 setelah dari data percobaan hewan, ditemukan bahwa cara plutonium mendistribusikan dirinya pada tulang ternyata lebih berbahaya daripada radium.[108] Sebagian besar subjek, ujar Eileen Welsome, adalah orang miskin, tidak berdaya, dan sakit.[109]
Dari tahun 1945 hingga 1947, delapan belas subjek uji manusia disuntik dengan plutonium tanpa persetujuan mereka. Percobaan ini dilakukan untuk mengembangkan alat diagnostik yang dapat menentukan kadar penyerapan plutonium dalam tubuh, sehingga dapat dikembangkan sebuah standar keamanan pekerjaan yang melibatkan plutonium.[107] Ebb Cade adalah peserta yang tidak bersedia dalam eksperimen medis yang melibatkan injeksi 4,7 mikrogram plutonium pada 10 April 1945 di Oak Ridge, Tennessee.[110][111] Eksperimen ini berada di bawah pengawasan Harold Hodge.[112] Eksperimen lain yang diarahkan oleh Komisi Energi Atom Amerika Serikat dan Proyek Manhattan berlanjut hingga tahun 1970-an. The Plutonium Files mengisahkan kehidupan para subjek program rahasia dengan menyebutkan nama setiap orang yang terlibat dan mendiskusikan penelitian etis dan medis yang dilakukan secara rahasia oleh para ilmuwan dan dokter. Eksperimen tersebut sekarang dianggap sebagai pelanggaran serius terhadap kode etik kedokteran dan Sumpah Hippokrates.[113]
Pemerintah menutupi sebagian besar kecelakaan radiasi ini sampai tahun 1993, ketika Presiden Bill Clinton memerintahkan perubahan kebijakan, dan kemudian lembaga federal menyediakan catatan yang relevan. Investigasi yang dihasilkan dilakukan oleh Komite Penasihat Presiden untuk Eksperimen Radiasi Manusia, dan mengungkap banyak materi tentang penelitian plutonium pada manusia. Komite tersebut mengeluarkan laporan tahun 1995 yang kontroversial yang mengatakan bahwa "kesalahan telah dilakukan" tetapi tidak mengutuk mereka yang melakukannya.[109]
Aplikasi
[sunting | sunting sumber]Bahan peledak
[sunting | sunting sumber]
Isotop plutonium-239 adalah komponen fisil utama dalam senjata nuklir, karena kemudahannya menjalani fisi dan ketersediaannya. Dengan membungkus bola plutonium padat dengan pemadat (lapisan tambahan yang dibuat dari bahan-bahan padat) akan menurunkan jumlah plutonium yang diperlukan untuk mencapai massa kritis dengan memantulkan kembali neutron yang lolos kembali ke inti plutonium. Hal ini akan menurunkan jumlah plutonium yang diperlukan untuk mencapai kekritisan dari 16 kg menjadi 10 kg, yang berupa bola dengan diameter sekitar 10 sentimeter (4 in).[114] Massa kritis ini adalah sekitar sepertiga dari massa kritis uranium-235.[7]
Bom plutonium Fat Man yang diproduksi semasa Proyek Manhattan menggunakan kompresi eksplosif plutonium untuk mendapatkan tingkat kepadatan plutonium yang lebih besar daripada biasanya dan menggabungkannya dengan sumber neutron untuk memulai reaksi dan meningkatkan efisiensi. Sehingga, hanya diperlukan 6,2 kg plutonium untuk mendapatkan daya ledak yang setara dengan 20 kiloton TNT.[92][115] Secara hipotetis, hanya diperlukan 4 kg plutonium—dan bahkan mungkin kurang—untuk membuat satu bom atom dengan menggunakan desain perakitan yang sangat canggih.[115]
Bahan bakar oksida campuran
[sunting | sunting sumber]Bahan bakar nuklir bekas dari reaktor air ringan biasa mengandung plutonium, tetapi biasanya merupakan campuran plutonium-242, -240, -239 dan -238. Campuran tersebut tidak cukup diperkaya untuk senjata nuklir yang efisien, tetapi dapat digunakan sekali sebagai bahan bakar MOX.[116] Penangkapan neutron yang tidak disengaja menyebabkan jumlah plutonium-242 dan -240 bertambah setiap kali plutonium disinari dalam reaktor dengan neutron "termal" kecepatan rendah, sehingga setelah siklus kedua, plutonium hanya dapat dikonsumsi oleh reaktor neutron cepat. Jika reaktor neutron cepat tidak tersedia (kasus normal), surplus plutonium biasanya dibuang, dan membentuk salah satu komponen limbah nuklir yang berumur panjang. Keinginan untuk mengonsumsi plutonium ini dan bahan bakar transuranium lainnya dan mengurangi radiotoksisitas limbah adalah alasan yang biasa diberikan oleh para insinyur nuklir untuk membuat reaktor neutron cepat.[117]
Proses kimia yang paling umum, PUREX (Plutonium–URanium EXtraction), memroses ulang bahan bakar nuklir bekas untuk mengekstraksi uranium dan plutonium dalam bentuk bahan bakar oksida campuran (MOX) untuk digunakan kembali dalam reaktor nuklir. Plutonium tingkat senjata dapat ditambahkan ke campuran bahan bakar tersebut. Bahan bakar MOX digunakan pada reaktor air ringan dan terdiri dari 60 kg plutonium per ton bahan bakar; setelah empat tahun, tiga per empat plutonium tersebut akan habis digunakan (berubah menjadi unsur lain).[37] Reaktor pembiak secara spesifik dirancang untuk mendapatkan bahan fisil dengan laju yang lebih cepat daripada laju konsumsi bahan tersebut.[118]
Bahan bakar MOX telah digunakan sejak tahun 1980-an dan secara luas digunakan di Eropa.[116] Pada bulan September 2000, Amerika Serikat dan Federasi Rusia menandatangani Perjanjian Pengelolaan dan Disposisi Plutonium yang mana masing-masing pihak setuju untuk membuang 34 ton plutonium tingkat senjata.[119] Departemen Energi A.S. berencana membuang 34 ton plutonium tingkat senjata di Amerika Serikat sebelum akhir 2019 dengan mengubahnya menjadi bahan bakar MOX yang dapat digunakan pada reaktor nuklir komersial.[119]
Bahan bakar MOX dapat meningkatkan pembakaran total. Sebuah batang bahan bakar diproses ulang setelah tiga tahun digunakan untuk menghilangkan produk limbah, yang pada saat itu mencapai 3% dari total berat batang.[37] Isotop uranium dan plutonoum apapun yang dihasilkan selama tiga tahun tersebut ditinggalkan dan batang tersebut kembali digunakan.[note 10] Namun, keberadaan hingga 1% galium per massa dalam paduan plutonium tingkat senjata berpotensi mengganggu operasi jangka panjang reaktor air ringan.[120]
Plutonium yang diperoleh kembali dari bahan bakar reaktor bekas menimbulkan sedikit bahaya proliferasi, karena kontaminasi yang berlebihan dengan plutonium-240 dan plutonium-242 yang nonfisil. Pemisahan isotop tidak dapat dilakukan. Reaktor khusus yang beroperasi dengan pembakaran sangat rendah (sehingga meminimalkan paparan plutonium-239 yang baru terbentuk terhadap neutron tambahan yang menyebabkannya diubah menjadi isotop plutonium yang lebih berat) umumnya diperlukan untuk menghasilkan bahan yang cocok untuk digunakan dalam senjata nuklir yang efisien. Walaupun plutonium "tingkat senjata" didefinisikan mengandung setidaknya 92% plutonium-239 (dari total plutonium), Amerika Serikat telah berhasil meledakkan sebuah perangkat di bawah 20 kt menggunakan plutonium yang diyakini hanya mengandung sekitar 85% plutonium-239, disebut plutonium "tingkat bahan bakar".[121] Plutonium "tingkat reaktor" yang diproduksi oleh siklus pembakaran LWR reguler biasanya mengandung kurang dari 60% Pu-239, dengan hingga 30% Pu-240/Pu-242 yang merupakan parasit, dan 10–15% Pu-241 yang fisil.[121] Tidak diketahui apakah perangkat yang menggunakan plutonium yang diperoleh dari limbah nuklir sipil yang diproses ulang dapat diledakkan, namun perangkat semacam itu secara hipotetis dapat gagal dan menyebarkan bahan radioaktif ke area perkotaan yang luas. IAEA secara konservatif mengklasifikasikan plutonium dari semua vektor isotop sebagai bahan "penggunaan langsung", yaitu, "bahan nuklir yang dapat digunakan untuk pembuatan komponen bahan peledak nuklir tanpa transmutasi atau pengayaan lebih lanjut".[121]
Sumber tenaga dan panas
[sunting | sunting sumber]

Isotop plutonium-238 memiliki waktu paruh 87,74 tahun.[122] Ia memancarkan energi termal dalam jumlah besar dengan tingkat sinar gama/foton dan sinar/partikel neutron spontan yang rendah.[123] Sebagai pemancar partikel alfa, ia memancarkan radiasi berenergi tinggi dengan tingkat penetrasi yang rendah, sehingga hanya diperlukan pemerisaian yang minimal. Selembar kertas dapat digunakan untuk memerisai partikel alfa yang dipancarkan oleh plutonium-238. Satu kilogram isotop ini dapat menghasilkan 570 watt panas.[7][123]
Karakteristik ini membuatnya sangat cocok untuk pembangkit tenaga listrik untuk perangkat yang harus berfungsi tanpa pemeliharaan secara langsung selama seumur hayat manusia. Oleh karena itu, ia digunakan dalam generator termoelektrik radioisotop dan unit pemanas radioisotop seperti yang digunakan pada prob antariksa Cassini,[124] Voyager, Galileo, dan New Horizons[125], serta wahana penjelajah Mars Curiosity[126] dan Perseverance (Mars 2020).
Wahana antariksa kembar Voyager diluncurkan pada tahun 1977, masing-masing berisi sumber daya plutonium 500 watt. Lebih dari 30 tahun kemudian, masing-masing sumber masih menghasilkan sekitar 300 watt yang memungkinkan pengoperasian terbatas untuk masing-masing wahana antariksa.[127] Versi sebelumnya dari teknologi yang sama mendukung lima Paket Eksperimen Permukaan Bulan Apollo, dimulai dengan Apollo 12 pada tahun 1969.[37]
Plutonium-238 juga telah sukses digunakan untuk menenagai alat pacu jantung buatan, sehingga mengurangi risiko pembedahan ulang.[128][129] Ia umumnya telah digantikan dengan sel primer berbasis litium, namun hingga 2003[update] masih terdapat sekitar 50 hingga 100 alat pacu jantung yang ditenagai plutonium yang masih ditanam dan berfungsi pada pasien yang masih hidup di Amerika Serikat.[130] Pada akhir tahun 2007, jumlah alat pacu jantung bertenaga plutonium dilaporkan turun menjadi hanya sembilan.[131] Plutonium-238 dipelajari sebagai cara untuk memberikan panas tambahan untuk selam skuba.[132] Plutonium-238 yang dicampur dengan berilium digunakan untuk menghasilkan neutron untuk tujuan penelitian.[37]
Pencegahan
[sunting | sunting sumber]Toksisitas
[sunting | sunting sumber]Terdapat dua aspek terhadap efek berbahaya dari plutonium: radioaktivitas dan efek racun logam berat. Isotop dan senyawa plutonium bersifat radioaktif dan terakumulasi dalam sumsum tulang. Kontaminasi oleh plutonium oksida dihasilkan dari bencana nuklir dan insiden radioaktif, termasuk kecelakaan nuklir militer di mana senjata nuklir telah terbakar.[133] Studi mengenai efek dari beberapa pelepasan yang lebih kecil ini, serta penyakit keracunan radiasi dan kematian yang meluas setelah serangan bom atom Hiroshima dan Nagasaki, telah memberikan banyak informasi mengenai bahaya, gejala dan prognosis dari keracunan radiasi, di mana dalam kasus para penyintas di Jepang sebagian besar dari mereka tidak terkait dengan paparan plutonium langsung.[134]
Selama peluruhan plutonium, tiga jenis radiasi pengion dilepaskan, yaitu alfa, beta, dan gama. Paparan akut atau jangka panjang membawa bahaya kesehatan yang serius, meliputi penyakit radiasi, kerusakan genetik, kanker, dan kematian. Bahaya ini meningkat dengan jumlah paparan.[37] Radiasi alfa hanya dapat menempuh jarak pendek dan tidak dapat menembus lapisan luar kulit mati manusia. Radiasi beta dapat menembus kulit manusia, tetapi tidak dapat menembus seluruh tubuh. Radiasi gama dapat menyebar ke seluruh tubuh.[135] Meskipun radiasi alfa tidak dapat menembus kulit, plutonium yang tertelan atau terhirup dapat menyinari organ dalam.[37] Partikel alfa yang dihasilkan oleh plutonium yang dihirup telah ditemukan menyebabkan kanker paru-paru pada sekelompok pekerja nuklir Eropa.[136] Kerangka, tempat plutonium terakumulasi, dan hati, tempat ia terkumpul dan terkonsentrasi, memiliki risiko paling tinggi.[36] Plutonium tidak akan diserap ke dalam tubuh secara efisien saat dicerna; hanya sekitar 0,04% plutonium oksida yang diserap setelah tertelan.[37] Ketika plutonium diserap ke dalam tubuh, ia akan diekskresikan dengan sangat lambat, dengan waktu paruh biologis selama 200 tahun.[137] Plutonium hanya bergerak perlahan melalui membran sel dan batas usus, sehingga penyerapan melalui penelanan dan penggabungan ke dalam struktur tulang berlangsung sangat lambat.[138][139] Donald Mastick secara tidak sengaja menelan sejumlah kecil plutonium(III) klorida, yang dapat terdeteksi selama tiga puluh tahun berikutnya dalam hidupnya, tetapi tampaknya tidak menimbulkan efek buruk.[140]
Plutonium lebih berbahaya ketika terhirup daripada tertelan. Risiko kanker paru-paru akan meningkat setelah total dosis radiasi plutonium yang terhirup melebihi 400 mSv.[141] Departemen Energi A.S. memperkirakan bahwa risiko kanker seumur hidup akibat menghirup 5.000 partikel plutonium, masing-masing selebar 3 µm, adalah 1% di atas rata-rata A.S.[142] Penelanan atau penghirupan plutonium dalam jumlah besar dapat menyebabkan keracunan radiasi akut dan kemungkinan kematian. Namun, sampai sekarang tidak ada satupun manusia yang diketahui meninggal oleh karena menghirup ataupun menelan plutonium, dan banyak orang mempunyai sejumlah kecil plutonium yang dapat dideteksi dalam tubuh mereka.[121]
Teori "partikel panas" di mana partikel debu plutonium menyinari titik jaringan paru-paru yang terlokalisir tidak didukung oleh penelitian arus utama—partikel semacam itu lebih bebas bergerak daripada yang diperkirakan semula dan toksisitasnya tidak meningkat secara terukur karena bentuk partikulat.[138] Saat terhirup, plutonium dapat masuk ke aliran darah. Begitu berada di aliran darah, plutonium bergerak ke seluruh tubuh dan masuk ke tulang, hati, atau organ tubuh lainnya. Plutonium yang mencapai organ tubuh umumnya tetap berada di dalam tubuh selama beberapa dekade dan terus memaparkan jaringan di sekitarnya terhadap radiasi sehingga dapat menyebabkan kanker.[143]
Kutipan yang sering dikutip oleh Ralph Nader menyatakan bahwa satu pon debu plutonium yang menyebar ke atmosfer akan cukup untuk membunuh 8 miliar orang.[144] Pernyataan ini dibantah oleh Bernard Cohen, seorang penentang model tanpa ambang linear dari toksisitas radiasi yang diterima secara umum. Cohen memperkirakan bahwa satu pon plutonium dapat membunuh tidak lebih dari 2 juta orang jika terhirup, sehingga toksisitas plutonium kira-kira setara dengan gas saraf.[145]
Beberapa populasi orang yang terpapar debu plutonium (misalnya orang-orang yang tinggal di lokasi uji coba Nevada, para penyintas serangan bom Hiroshima dan Nagasaki, pekerja fasilitas nuklir, dan pasien "sakit parah" yang disuntik dengan plutonium pada tahun 1945–46 untuk mempelajari metabolisme plutonium) telah diikuti dan dianalisis dengan cermat. Cohen menemukan studi ini tidak konsisten dengan perkiraan tinggi toksisitas plutonium, mengutip kasus seperti Albert Stevens yang bertahan sampai usia tua setelah disuntik dengan plutonium.[138] "Ada sekitar 25 pekerja dari Laboratorium Nasional Los Alamos yang menghirup sejumlah besar debu plutonium selama tahun 1940-an; menurut teori partikel panas, masing-masing dari mereka memiliki kemungkinan 99,5% meninggal akibat kanker paru-paru saat ini, tetapi belum ada satu pun dari mereka yang mengidap kanker paru-paru."[145][146]
Toksisitas laut
[sunting | sunting sumber]Penyelidikan toksisitas plutonium pada fauna di sistem laut sama pentingnya dengan melihat efeknya pada manusia. Plutonium diketahui memasuki lingkungan laut dengan pembuangan limbah atau kebocoran yang tidak disengaja dari pembangkit nuklir. Meskipun konsentrasi plutonium tertinggi di lingkungan laut ditemukan pada sedimen, siklus biogeokimia plutonium yang kompleks mengartikan bahwa plutonium juga ditemukan pada semua kompartemen lainnya.[147] Misalnya, berbagai spesies zooplankton yang membantu siklus nutrien akan mengonsumsi unsur tersebut setiap hari. Ekskresi lengkap plutonium yang tertelan oleh zooplankton menjadikan defekasi mereka sebagai mekanisme yang sangat penting dalam pemungutan plutonium dari air permukaan.[148] Namun, zooplankton yang mati karena dimangsa oleh organisme yang lebih besar dapat menjadi sarana transmisi plutonium ke ikan.
Selain dikonsumsi, ikan juga dapat terpapar plutonium karena distribusi geografisnya di seluruh dunia. Satu studi menyelidiki efek dari beberapa unsur transuranium (plutonium-238, plutonium-239, plutonium-240) pada berbagai ikan yang hidup di Zona Eksklusi Chernobyl (CEZ). Hasil penyelidikan tersebut menunjukkan bahwa proporsi ikan perca betina di CEZ menunjukkan kegagalan atau keterlambatan pematangan gonad.[149] Studi serupa menemukan akumulasi besar plutonium pada organ pernapasan dan pencernaan ikan kod, sebelah (flounder), dan haring.[147]
Toksisitas plutonium sama merugikannya terhadap larva ikan di area limbah nuklir. Telur yang tidak berkembang memiliki risiko lebih tinggi daripada ikan dewasa yang terpapar unsur di area limbah ini. Laboratorium Nasional Oak Ridge menunjukkan bahwa embrio ikan karper dan minnow yang dibesarkan dalam larutan yang mengandung isotop plutonium tidak menetas; telur yang menetas menunjukkan kelainan yang signifikan jika dibandingkan dengan embrio kontrol yang dikembangkan.[150] Terungkap bahwa konsentrasi plutonium yang lebih tinggi telah ditemukan menyebabkan masalah pada fauna laut yang terpapar unsur tersebut.
Potensi kekritisan
[sunting | sunting sumber]
Selain permasalahan pada toksisitas plutonium, akumulasi sejumlah plutonium yang mencapai massa kritis juga harus dihindari, terutama karena massa kritis plutonium hanyalah sepertiga dari massa kritis uranium-235.[7] Plutonium yang mencapai massa kritis akan memancarkan sejumlah neutron dan sinar gama dalam kadar yang mematikan.[151] Plutonium dalam larutan lebih berkemungkinan membentuk massa kritis daripada plutonium dalam bentuk padatan karena moderasi oleh hidrogen dalam air.[diragukan][13]
Kecelakaan kekritisan telah terjadi di masa lalu, beberapa di antaranya memiliki konsekuensi yang mematikan. Penanganan yang tidak hati-hati pada bata wolfram karbida yang diletakkan di sekitar bola plutonium berbobot 6,2 kg menyebabkan radiasi dengan dosis fatal pada tanggal 21 Agustus 1945 di Los Alamos, yang mana ilmuwan Harry Daghlian menerima dosis yang diperkirakan setara dengan 5,1 Sievert (510 rem) dan meninggal 25 hari sesudahnya.[152][153] Sembilan bulan kemudian, ilmuwan Los Alamos lainnya, Louis Slotin, juga meninggal dalam kecelakaan yang melibatkan reflektor berilium dan inti plutonium yang sama (yang disebut "inti setan") yang sebelumnya telah merenggut nyawa Daghlian.[154] Insiden ini kemudian diangkat ke dalam film tahun 1989 berjudul Fat Man and Little Boy.
Pada bulan Desember 1958, selama proses pemurnian plutonium di Los Alamos, massa kritis terbentuk di dalam tabung pencampuran, menyebabkan kematian seorang operator derek bernama Cecil Kelley. Selain itu, kecelakaan nuklir lainnya juga pernah terjadi di Uni Soviet, Jepang, Amerika Serikat, dan negara-negara lainnya.[155]
Flamabilitas
[sunting | sunting sumber]Logam plutonium juga merupakan bahan yang mudah terbakar, terutama jika ia terbelah dengan halus. Di lingkungan lembap, plutonium akan membentuk hidrida pada permukaannya, yang bersifat piroforik dan dapat menyala di udara pada suhu kamar. Plutonium akan mengembang hingga 70% volumenya saat teroksidasi, sehingga dapat merusak wadah penampungnya.[39] Radioaktivitas bahan yang terbakar merupakan bahaya tambahan. Pasir magnesium oksida merupakan bahan yang paling efektif dalam memadamkan api plutonium. Ia mendinginkan bahan yang terbakar, bekerja sebagai pembuang panas, dan juga mengeblok oksigen. Tindakan pencegahan khusus diperlukan untuk menyimpan atau menangani plutonium dalam bentuk apa pun; umumnya atmosfer lengai yang kering diperlukan.[39][note 11]
Transportasi
[sunting | sunting sumber]Darat dan laut
[sunting | sunting sumber]Transportasi plutonium yang biasa adalah melalui plutonium oksida yang lebih stabil dalam kemasan tertutup. Pengangkutan tipikal terdiri dari satu truk yang membawa satu peti kemas terlindung, menampung sejumlah paket dengan berat total bervariasi mulai dari 80 hingga 200 kg plutonium oksida. Kiriman laut dapat terdiri dari beberapa peti kemas, masing-masing berisi bungkusan tertutup.[157] Komisi Regulasi Nuklir Amerika Serikat menyatakan bahwa plutonium harus dalam bentuk padat, bukan bubuk, jika isinya melebihi 0,74 TBq (20 Curie) aktivitas radioaktif.[158] Pada tahun 2016, kapal Pacific Egret[159] dan Pacific Heron milik Pacific Nuclear Transport Ltd. mengangkut 331 kg (730 lbs) plutonium ke fasilitas pemerintah Amerika Serikat di Sungai Savannah, Carolina Selatan.[160][161]
Udara
[sunting | sunting sumber]Peraturan angkutan udara Pemerintah A.S. mengizinkan pengangkutan plutonium melalui udara, tunduk pada pembatasan bahan berbahaya lainnya yang dibawa dalam penerbangan yang sama, persyaratan pengemasan, dan penyimpanan di bagian paling belakang pesawat.[162]
Pada tahun 2012, media mengungkapkan bahwa plutonium telah diterbangkan dari Norwegia oleh maskapai penumpang komersial—sekitar dua tahun sekali—termasuk satu kali pada tahun 2011.[163] Peraturan mengizinkan sebuah pesawat untuk mengangkut 15 gram bahan yang dapat difisi.[163] Transportasi plutonium semacam itu dinilai tidak memiliki masalah, menurut penasihat senior (seniorrådgiver) di Statens strålevern.[163]
Dalam budaya populer
[sunting | sunting sumber]Plutonium disebutkan dalam beberapa film. Ia disebutkan dalam film-film berikut:[164]
Catatan
[sunting | sunting sumber]Catatan kaki
[sunting | sunting sumber]- ^ Ion PuO+2 tidak stabil dalam larutan dan akan berdisproporsionasi menjadi Pu4+ dan PuO2+2; Pu4+ kemudian akan mengoksidasi PuO+2 yang tersisa menjadi PuO2+2, dan ia sendiri akan tereduksi menjadi Pu3+. Oleh karena itu, larutan berair PuO+2 cenderung berubah menjadi campuran Pu3+ dan PuO2+2 dari waktu ke waktu. UO+2 tidak stabil karena alasan yang sama.[30]
- ^ Ini bukan pertama kalinya seseorang menyarankan agar suatu unsur diberi nama "plutonium". Satu dekade setelah barium ditemukan, seorang profesor Universitas Cambridge menyarankan untuk mengganti nama barium menjadi "plutonium" karena unsur tersebut tidak termasuk unsur berat (karena barium memiliki akar kata dari bahasa Yunani, barys, yang berarti "berat"). Dia beralasan, karena barium diproduksi dengan teknik elektrolisis yang relatif baru, namanya harus mengacu pada api. Karena itu dia menyarankan nama "plutonium" dari dewa Romawi dunia bawah, Pluto.[69]
- ^ Seperti yang dikatakan salah satu artikel, mengacu pada informasi yang diberikan Seaborg dalam sebuah ceramah: "Pilihan yang jelas untuk lambang tersebut adalah Pl, tetapi dengan jenaka, Seaborg menyarankan Pu, seperti kata-kata yang akan diserukan seorang anak, 'Pee-yoo!' ketika mencium sesuatu yang tidak enak Seaborg berpikir bahwa dia akan menerima banyak kritik atas saran itu, tetapi komite penamaan menerima lambang itu tanpa sepatah kata pun."[71]
- ^ Ruang 405 di Laboratorium George Herbert Jones, tempat isolasi plutonium pertama berlangsung, dinobatkan sebagai Mercu Tanda Sejarah Nasional pada Mei 1967.
- ^ Semasa Proyek Manhattan, plutonium sering dirujuk sebagai "49": angka 4 adalah digit terakhir dalam 94 (nomor atom plutonium), dan 9 adalah digit terakhir dalam plutonium-239, isotop fisil tingkat senjata yang digunakan dalam bom nuklir.[80]
- ^ Perhimpunan Insinyur Mekanik Amerika (ASME) mendirikan Reaktor B sebagai Mercu Teknik Mesin Bersejarah Nasional pada September 1976.[84] Pada Agustus 2008, Reaktor B ditetapkan sebagai Mercu Tanda Sejarah Nasional A.S..[85]
- ^ Perhitungan efisiensi ini didasarkan pada fakta bahwa 1 kg fisi plutonium-239 (atau uranium-235) menghasilkan pelepasan energi sekitar 17 kt, yang mengarah pada perkiraan bulat sebesar 1,2 kg plutonium yang sebenarnya difisi untuk menghasilkan hasil 20 kt.[93]
- ^ Sebagian besar plutonium ini digunakan untuk membuat inti yang dapat dibelah dari jenis senjata termonuklir yang menggunakan desain Teller–Ulam. Senjata yang disebut sebagai 'bom hidrogen' ini merupakan varian senjata nuklir yang menggunakan bom fisi untuk memicu fusi nuklir isotop hidrogen berat. Kerusakan yang disebabkan oleh senjata ini umumnya setara dengan jutaan ton TNT, bandingkan dengan senjata nuklir yang hanya menggunakan fisi nuklir dan menghasilkan kerusakan setara dengan ribuan ton TNT.[98]
- ^ Gadolinium zirkonium oksida (Gd2Zr2O7) juga telah dikaji karena ia dapat menampung plutonium selama 30 juta tahun.[98]
- ^ Komposisi plutonium pada batang bahan bakar nuklir bekas: plutonium-239 (~58%), -240 (24%), -241 (11%), -242 (5%), dan -238 (2%).[98]
- ^ Terdapat sebuah kebakaran besar yang dipicu oleh plutonium di Pabrik Rocky Flats dekat Boulder, Colorado pada tahun 1969.[156]
Rujukan
[sunting | sunting sumber]- ^ (Indonesia) "Plutonium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Dihitung dari berat atom dan volume atomnya. Sel satuan, yang mengandung 16 atom, memiliki volume 319,96 kubik Å, menurut Siegfried S. Hecker (2000). "Plutonium and its alloys: from atoms to microstructure" (PDF). Los Alamos Science. 26: 331.. Ini memberikan kerapatan untuk 239Pu sebesar (1,66053906660×10−24g/dalton×239,0521634 dalton/atom×16 atom/sel satuan)/(319.96 Å3/sel satuan×10−24cc/Å3) atau 19,85 g/cc.
- ^ a b c d "Plutonium, Radioactive". Wireless Information System for Emergency Responders (WISER). Bethesda (MD): U.S. National Library of Medicine, National Institutes of Health. Diarsipkan dari versi asli tanggal 22 Agustus 2011. Diakses tanggal 15 Juni 2023. (public domain text)
- ^ "Nitric acid processing". Actinide Research Quarterly. Los Alamos (NM): Laboratorium Nasional Los Alamos (kuartal ke-3). 2008. Diarsipkan dari versi asli tanggal 18 September 2016. Diakses tanggal 15 Juni 2023.
Walaupun plutonium dioksida biasanya berwarna hijau zaitun, sampel dapat memiliki berbagai warna. Secara umum diyakini bahwa warna merupakan fungsi dari kemurnian kimia, stoikiometri, ukuran partikel, dan metode pembuatan, walaupun warna yang dihasilkan dari metode pembuatan tertentu tidak selalu dapat direproduksi.
- ^ "Liquid Range". webelements.com. Diarsipkan dari versi asli tanggal 27 Februari 2022. Diakses tanggal 15 Juni 2023.
- ^ a b c Sonzogni, Alejandro A. (2008). "Chart of Nuclides". Upton: Pusat Data Nuklir Nasional, Laboratorium Nasional Brookhaven. Diarsipkan dari versi asli tanggal 21 Juli 2011. Diakses tanggal 15 Juni 2023.
- ^ a b c d e f g h Heiserman 1992, hlm. 338
- ^ Rhodes 1986, hlm. 659–660 Leona Marshall: "Saat Anda memegang segumpal di tangan Anda, rasanya hangat, seperti seekor kelinci hidup"
- ^ a b c d Miner 1968, hlm. 544
- ^ a b c d e f g h Hecker, Siegfried S. (2000). "Plutonium and its alloys: from atoms to microstructure" (PDF). Los Alamos Science. 26: 290–335. Diarsipkan dari versi asli (PDF) tanggal 24 Februari 2009. Diakses tanggal 15 Juni 2023.
- ^ Hecker, Siegfried S.; Martz, Joseph C. (2000). "Aging of Plutonium and Its Alloys" (PDF). Los Alamos Science. Los Alamos, New Mexico: Laboratorium Nasional Los Alamos (26): 242. Diarsipkan dari versi asli (PDF) tanggal 28 April 2021. Diakses tanggal 15 Juni 2023.
- ^ a b c d Baker, Richard D.; Hecker, Siegfried S.; Harbur, Delbert R. (1983). "Plutonium: A Wartime Nightmare but a Metallurgist's Dream" (PDF). Los Alamos Science. Laboratorium Nasional Los Alamos: 148, 150–151. Diarsipkan dari versi asli (PDF) tanggal 17 Oktober 2011. Diakses tanggal 15 Juni 2023.
- ^ a b c d e Lide 2006, hlm. 4–27
- ^ a b c d Miner 1968, hlm. 542
- ^ "Glossary – Fissile material". United States Nuclear Regulatory Commission. 20 November 2014. Diarsipkan dari versi asli tanggal 4 Februari 2015. Diakses tanggal 15 Juni 2023.
- ^ Asimov 1988, hlm. 905
- ^ Glasstone, Samuel; Redman, Leslie M. (Juni 1972). "An Introduction to Nuclear Weapons" (PDF). Atomic Energy Commission Division of Military Applications. hlm. 12. WASH-1038. Diarsipkan dari versi asli (PDF) tanggal 27 Agustus 2009.
- ^ Gosling 1999, hlm. 40
- ^ "Plutonium: The First 50 Years" (PDF). U.S. Department of Energy. 1996. DOE/DP-1037. Diarsipkan dari versi asli (PDF) tanggal 18 Februari 2013.
- ^ Wallner, A.; Faestermann, T.; Feige, J.; Feldstein, C.; Knie, K.; Korschinek, G.; Kutschera, W.; Ofan, A.; Paul, M.; Quinto, F.; Rugel, G.; Steier, P. (2015). "Abundance of live 244Pu in deep-sea reservoirs on Earth points to rarity of actinide nucleosynthesis". Nature Communications. 6: 5956. arXiv:1509.08054
 . Bibcode:2015NatCo...6.5956W. doi:10.1038/ncomms6956. ISSN 2041-1723. PMC 4309418
. Bibcode:2015NatCo...6.5956W. doi:10.1038/ncomms6956. ISSN 2041-1723. PMC 4309418  . PMID 25601158.
. PMID 25601158.
- ^ Heiserman 1992, hlm. 340
- ^ Kennedy, J. W.; Seaborg, G. T.; Segrè, E.; Wahl, A. C. (1946). "Properties of Element 94". Physical Review. 70 (7–8): 555–556. Bibcode:1946PhRv...70..555K. doi:10.1103/PhysRev.70.555
 .
.
- ^ a b Greenwood 1997, hlm. 1259
- ^ a b c Clark 1961, hlm. 124–125.
- ^ Seaborg, Glenn T.; McMillan, E.; Kennedy, J. W.; Wahl, A. C. (1946). "Radioactive Element 94 from Deuterons on Uranium". Physical Review. 69 (7–8): 366. Bibcode:1946PhRv...69..366S. doi:10.1103/PhysRev.69.366.
- ^ Bernstein 2007, hlm. 76–77.
- ^ Miotla, Dennis (21 April 2008). "Assessment of Plutonium-238 Production of Alternatives: Briefing for Nuclear Energy Advisory Committee" (PDF). Energy.gov. Diarsipkan dari versi asli (PDF) tanggal 16 Maret 2022. Diakses tanggal 15 Juni 2023.
- ^ "Can Reactor Grade Plutonium Produce Nuclear Fission Weapons?". Council for Nuclear Fuel Cycle Institute for Energy Economics, Japan. Mei 2001. Diarsipkan dari versi asli tanggal 24 Februari 2021. Diakses tanggal 15 Juni 2023.
- ^ Heiserman 1992, hlm. 339
- ^ Crooks, William J. (2002). "Nuclear Criticality Safety Engineering Training Module 10 – Criticality Safety in Material Processing Operations, Part 1" (PDF). Diarsipkan dari versi asli (PDF) tanggal 20 Maret 2006. Diakses tanggal 15 Juni 2023.
- ^ Matlack, George (2002). A Plutonium Primer: An Introduction to Plutonium Chemistry and its Radioactivity. Los Alamos National Laboratory. LA-UR-02-6594.
- ^ Windorff, Cory J.; Chen, Guo P; Cross, Justin N; Evans, William J.; Furche, Filipp; Gaunt, Andrew J.; Janicke, Michael T.; Kozimor, Stosh A.; Scott, Brian L. (2017). "Identification of the Formal +2 Oxidation State of Plutonium: Synthesis and Characterization of {PuII[C5H3(SiMe3)2]3}−". J. Am. Chem. Soc. 139 (11): 3970–3973. doi:10.1021/jacs.7b00706. PMID 28235179.
- ^ a b Zaitsevskii, Andréi; Mosyagin, Nikolai S.; Titov, Anatoly V.; Kiselev, Yuri M. (21 Juli 2013). "Relativistic density functional theory modeling of plutonium and americium higher oxide molecules". The Journal of Chemical Physics. 139 (3): 034307. Bibcode:2013JChPh.139c4307Z. doi:10.1063/1.4813284. PMID 23883027.
- ^ Kiselev, Yu. M.; Nikonov, M. V.; Dolzhenko, V. D.; Ermilov, A. Yu.; Tananaev, I. G.; Myasoedov, B. F. (17 January 2014). "On existence and properties of plutonium(VIII) derivatives". Radiochimica Acta. 102 (3): 227–237. doi:10.1515/ract-2014-2146.
- ^ Eagleson 1994, hlm. 840
- ^ a b c d e Miner 1968, hlm. 545
- ^ a b c d e f g h i j k l m n o p q r s Emsley 2001, hlm. 324–329
- ^ a b Apostolidis, Christos; Walter, Olaf; Vogt, Jochen; Liebing, Phil; Maron, Laurent; Edelmann, Frank T. (2017). "A Structurally Characterized Organometallic Plutonium(IV) Complex". Angewandte Chemie International Edition (dalam bahasa Inggris). 56 (18): 5066–5070. doi:10.1002/anie.201701858. ISSN 1521-3773. PMC 5485009
 . PMID 28371148.
. PMID 28371148.
- ^ a b c "Primer on Spontaneous Heating and Pyrophoricity – Pyrophoric Metals – Plutonium". Washington (DC): U.S. Department of Energy, Office of Nuclear Safety, Quality Assurance and Environment. 1994. Diarsipkan dari versi asli tanggal 28 April 2007.
- ^ Crooks, W. J.; et al. (2002). "Low Temperature Reaction of ReillexTM HPQ and Nitric Acid". Solvent Extraction and Ion Exchange. 20 (4–5): 543–559. doi:10.1081/SEI-120014371. Diarsipkan dari versi asli tanggal 14 Juni 2011. Diakses tanggal 15 Juni 2023.
- ^ a b Dumé, Belle (20 November 2002). "Plutonium is also a superconductor". PhysicsWeb.org. Diarsipkan dari versi asli tanggal 12 Januari 2012. Diakses tanggal 15 Juni 2023.
- ^ Moody, Hutcheon & Grant 2005, hlm. 169
- ^ Kolman, D. G.; Colletti, L. P. (2009). "The aqueous corrosion behavior of plutonium metal and plutonium–gallium alloys exposed to aqueous nitrate and chloride solutions". ECS Transactions. Electrochemical Society. 16 (52): 71. Bibcode:2009ECSTr..16Z..71K. doi:10.1149/1.3229956. ISBN 978-1-56677-751-3. Diarsipkan dari versi asli tanggal 16 Maret 2022. Diakses tanggal 15 Juni 2023.
- ^ Hurst & Ward 1956
- ^ Curro, N. J. (Spring 2006). "Unconventional superconductivity in PuCoGa5" (PDF). Laboratorium Nasional Los Alamos. Diarsipkan dari versi asli (PDF) tanggal 22 Juli 2011. Diakses tanggal 15 Juni 2023.
- ^ McCuaig, Franklin D. "Pu–Zr alloy for high-temperature foil-type fuel" U.S. Patent 4.059.439, Dikeluarkan pada 22 November 1977
- ^ Jha 2004, hlm. 73
- ^ a b c Kay 1965, hlm. 456
- ^ a b c d Miner 1968, hlm. 541
- ^ "Oklo: Natural Nuclear Reactors". U.S. Department of Energy, Office of Civilian Radioactive Waste Management. 2004. Diarsipkan dari versi asli tanggal 20 Oktober 2008. Diakses tanggal 15 Juni 2023.
- ^ Curtis, David; Fabryka-Martin, June; Paul, Dixon; Cramer, Jan (1999). "Nature's uncommon elements: plutonium and technetium". Geochimica et Cosmochimica Acta. 63 (2): 275–285. Bibcode:1999GeCoA..63..275C. doi:10.1016/S0016-7037(98)00282-8. Diarsipkan dari versi asli tanggal 27 Juni 2021. Diakses tanggal 15 Juni 2023.
- ^ Bernstein 2007, hlm. 75–77.
- ^ Hoffman, D. C.; Lawrence, F. O.; Mewherter, J. L.; Rourke, F. M. (1971). "Detection of Plutonium-244 in Nature". Nature. 234 (5325): 132–134. Bibcode:1971Natur.234..132H. doi:10.1038/234132a0.
- ^ Peterson, Ivars (7 Desember 1991). "Uranium displays rare type of radioactivity". Science News. Wiley-Blackwell. 140 (23): 373. doi:10.2307/3976137. JSTOR 3976137.
- ^ Hoffman, D. C.; Lawrence, F. O.; Mewherter, J. L.; Rourke, F. M. (1971). "Detection of Plutonium-244 in Nature". Nature. 234 (5325): 132–134. Bibcode:1971Natur.234..132H. doi:10.1038/234132a0. Nr. 34.
- ^ Turner, Grenville; Harrison, T. Mark; Holland, Greg; Mojzsis, Stephen J.; Gilmour, Jamie (2004-01-01). "Extinct 244Pu in Ancient Zircons" (PDF). Science. 306 (5693): 89–91. Bibcode:2004Sci...306...89T. doi:10.1126/science.1101014. JSTOR 3839259. PMID 15459384. Diarsipkan dari versi asli (PDF) tanggal 11 Februari 2020.
- ^ Hutcheon, I. D.; Price, P. B. (1972-01-01). "Plutonium-244 Fission Tracks: Evidence in a Lunar Rock 3.95 Billion Years Old". Science. 176 (4037): 909–911. Bibcode:1972Sci...176..909H. doi:10.1126/science.176.4037.909. JSTOR 1733798. PMID 17829301.
- ^ Kunz, Joachim; Staudacher, Thomas; Allègre, Claude J. (1998-01-01). "Plutonium-Fission Xenon Found in Earth's Mantle". Science. 280 (5365): 877–880. Bibcode:1998Sci...280..877K. doi:10.1126/science.280.5365.877. JSTOR 2896480. PMID 9572726.
- ^ Wallner, A.; Faestermann, T.; Feige, J.; Feldstein, C.; Knie, K.; Korschinek, G.; Kutschera, W.; Ofan, A.; Paul, M.; Quinto, F.; Rugel, G.; Steiner, P. (30 Maret 2014). "Abundance of live 244Pu in deep-sea reservoirs on Earth points to rarity of actinide nucleosynthesis". Nature Communications. 6: 5956. arXiv:1509.08054
 . Bibcode:2015NatCo...6.5956W. doi:10.1038/ncomms6956. PMC 4309418
. Bibcode:2015NatCo...6.5956W. doi:10.1038/ncomms6956. PMC 4309418  . PMID 25601158.
. PMID 25601158.
- ^ "Nuclear Testing 1945 - today". Comprehensive Test Ban Treaty Organization. Diarsipkan dari versi asli tanggal 7 Februari 2022. Diakses tanggal 15 Juni 2023.
- ^ Holden, Norman E. (2001). "A Short History of Nuclear Data and Its Evaluation". 51st Meeting of the USDOE Cross Section Evaluation Working Group. Upton (NY): National Nuclear Data Center, Brookhaven National Laboratory. Diarsipkan dari versi asli tanggal 22 Agustus 2011. Diakses tanggal 15 Juni 2023.
- ^ Fermi, Enrico (12 Desember 1938). "Artificial radioactivity produced by neutron bombardment: Nobel Lecture" (PDF). Royal Swedish Academy of Sciences. Diarsipkan dari versi asli (PDF) tanggal 5 Agustus 2011. Diakses tanggal 15 Juni 2023.
- ^ Darden, Lindley (1998). "The Nature of Scientific Inquiry". College Park: Department of Philosophy, University of Maryland. Diarsipkan dari versi asli tanggal 17 Agustus 2012. Diakses tanggal 15 Juni 2023.
- ^ Bernstein 2007, hlm. 44–52.
- ^ Seaborg, Glenn T. "An Early History of LBNL: Elements 93 and 94". Advanced Computing for Science Department, Lawrence Berkeley National Laboratory. Diarsipkan dari versi asli tanggal 5 November 2014. Diakses tanggal 15 Juni 2023.
- ^ a b Glenn T. Seaborg (September 1981). "The plutonium story". Lawrence Berkeley Laboratory, University of California. LBL-13492, DE82 004551. Diarsipkan dari versi asli tanggal 16 Mei 2013. Diakses tanggal 15 Juni 2023.
- ^ E. Segrè, A Mind Always in Motion, University of California Press, 1993, hlm. 162-169
- ^ Seaborg & Seaborg 2001, hlm. 71–72.
- ^ Heiserman 1992, hlm. 338.
- ^ Clark, David L.; Hobart, David E. (2000). "Reflections on the Legacy of a Legend: Glenn T. Seaborg, 1912–1999" (PDF). Los Alamos Science. 26: 56–61, pada 57. Diarsipkan dari versi asli (PDF) tanggal 3 Juni 2016. Diakses tanggal 15 Juni 2023.
- ^ Clark, David L.; Hobart, David E. (2000). "Reflections on the Legacy of a Legend: Glenn T. Seaborg, 1912–1999" (PDF). Los Alamos Science. 26: 56–61, pada 57. Diarsipkan dari versi asli (PDF) tanggal 3 Juni 2016. Diakses tanggal 15 Juni 2023.
- ^ "Frontline interview with Seaborg". Frontline. Public Broadcasting Service. 1997. Diarsipkan dari versi asli tanggal 29 Juni 2018. Diakses tanggal 15 Juni 2023.
- ^ Winterberg, Friedwardt; Herrmann, Günter; Fodor, Igor; Wolfenstein, Lincoln; Singer, Mark E. (1996). "More on How Nazi Germany Failed to Develop the Atomic Bomb". Physics Today. 49 (1): 11–15, 83. Bibcode:1996PhT....49a..11W. doi:10.1063/1.2807455.
- ^ Glenn T. Seaborg (1977). "History of MET Lab Section C-I, April 1942 – April 1943". Office of Scientific & Technical Information Technical Reports. California Univ., Berkeley (USA). Lawrence Berkeley Lab. doi:10.2172/7110621. Diarsipkan dari versi asli tanggal 15 Maret 2020. Diakses tanggal 15 Juni 2023.
- ^ "Room 405, George Herbert Jones Laboratory". National Park Service. Diarsipkan dari versi asli tanggal February 8, 2008. Diakses tanggal 15 Juni 2023.
- ^ a b c "Periodic Table of Elements". Los Alamos National Laboratory. Diarsipkan dari versi asli tanggal 12 Februari 2019. Diakses tanggal 15 Juni 2023.
- ^ Miner 1968, hlm. 540
- ^ "Plutonium". Atomic Heritage Foundation. Diarsipkan dari versi asli tanggal 6 Mei 2019. Diakses tanggal 15 Juni 2023.
- ^ "Site Selection". LANL History. Los Alamos, New Mexico: Laboratorium Nasional Los Alamos. Diarsipkan dari versi asli tanggal 13 September 2011. Diakses tanggal 15 Juni 2023.
- ^ Hammel, E. F. (2000). "The taming of "49" – Big Science in little time. Recollections of Edward F. Hammel, In: Cooper N.G. Ed. Challenges in Plutonium Science" (PDF). Los Alamos Science. 26 (1): 2–9. Diarsipkan dari versi asli (PDF) tanggal 20 Januari 2017. Diakses tanggal 15 Juni 2023.
- Hecker, S. S. (2000). "Plutonium: an historical overview. In: Challenges in Plutonium Science". Los Alamos Science. 26 (1): 1–2. Diarsipkan dari versi asli tanggal 18 Januari 2017. Diakses tanggal 15 Juni 2023.
- ^ Sublette, Carey. "Atomic History Timeline 1942–1944". Washington (DC): Atomic Heritage Foundation. Diarsipkan dari versi asli tanggal 4 Januari 2009. Diakses tanggal 15 Juni 2023.
- ^ Hoddeson et al. 1993, hlm. 235–239.
- ^ a b Hoddeson et al. 1993, hlm. 240–242.
- ^ Wahlen 1989, hlm. 1.
- ^ "Weekly List Actions". National Park Service. 29 Agustus 2008. Diarsipkan dari versi asli tanggal 31 Oktober 2008. Diakses tanggal 15 Juni 2023.
- ^ Wahlen 1989, hlm. iv, 1
- ^ a b Lindley, Robert (2013). "Kate Brown: Nuclear "Plutopias" the Largest Welfare Program in American History". History News Network. Diarsipkan dari versi asli tanggal 3 Mei 2019. Diakses tanggal 15 Juni 2023.
- ^ Rincon, Paul (2 Maret 2009). "BBC NEWS – Science & Environment – US nuclear relic found in bottle". BBC News. Diarsipkan dari versi asli tanggal 2 Maret 2009. Diakses tanggal 15 Juni 2023.
- ^ Gebel, Erika (2009). "Old plutonium, new tricks". Analytical Chemistry. 81 (5): 1724. doi:10.1021/ac900093b
 .
.
- ^ Schwantes, Jon M.; Matthew Douglas; Steven E. Bonde; James D. Briggs; et al. (2009). "Nuclear archeology in a bottle: Evidence of pre-Trinity U.S. weapons activities from a waste burial site". Analytical Chemistry. 81 (4): 1297–1306. doi:10.1021/ac802286a. PMID 19152306.
- ^ Sublette, Carey (3 Juli 2007). "8.1.1 The Design of Gadget, Fat Man, and "Joe 1" (RDS-1)". Nuclear Weapons Frequently Asked Questions, edition 2.18. The Nuclear Weapon Archive. Diakses tanggal 15 Juni 2023.
- ^ a b Malik, John (September 1985). "The Yields of the Hiroshima and Nagasaki Explosions" (PDF). Los Alamos. hlm. Table VI. LA-8819. Diarsipkan dari versi asli (PDF) tanggal 24 Februari 2009. Diakses tanggal 15 Juni 2023.
- ^ On the figure of 1 kg = 17 kt, see Garwin, Richard (4 Oktober 2002). "Proliferation of Nuclear Weapons and Materials to State and Non-State Actors: What It Means for the Future of Nuclear Power" (PDF). University of Michigan Symposium. Federation of American Scientists. Diarsipkan dari versi asli (PDF) tanggal 24 Februari 2009. Diakses tanggal 15 Juni 2023.
- ^ Sklar 1984, hlm. 22–29.
- ^ Bernstein 2007, hlm. 70.
- ^ "Historic American Engineering Record: B Reactor (105-B Building)". Richland: U.S. Department of Energy. 2001. hlm. 110. DOE/RL-2001-16. Diarsipkan dari versi asli tanggal 26 Desember 2008. Diakses tanggal 15 Juni 2023.
- ^ Cochran, Thomas B. (1997). Safeguarding nuclear weapons-usable materials in Russia (PDF). International Forum on Illegal Nuclear Traffic. Washington (DC): Natural Resources Defense Council, Inc. Diarsipkan dari versi asli (PDF) tanggal 5 Juli 2013. Diakses tanggal 15 Juni 2023.
- ^ a b c Emsley 2001.
- ^ Stockholm International Peace Research Institute 2007, hlm. 567.
- ^ Poet, S. E.; Martell, EA (Oktober 1972). "Plutonium-239 and americium-241 contamination in the Denver area". Health Physics. 23 (4): 537–48. doi:10.1097/00004032-197210000-00012. PMID 4634934.
- ^ Johnson, C. J. (October 1981). "Cancer Incidence in an area contaminated with radionuclides near a nuclear installation". Ambio. 10 (4): 176–182. JSTOR 4312671. PMID 7348208. Reprinted in Johnson, C. J (Oktober 1981). "Cancer Incidence in an area contaminated with radionuclides near a nuclear installation". Colo Med. 78 (10): 385–92. PMID 7348208.
- ^ "Rocky Flats National Wildlife Refuge". U.S. Fish & Wildlife Service. Diarsipkan dari versi asli tanggal 9 April 2020. Diakses tanggal 15 Juni 2023.
- ^ Press Secretary (23 Juli 2002). "President Signs Yucca Mountain Bill". Washington (DC): Office of the Press Secretary, White House. Diarsipkan dari versi asli tanggal 6 Maret 2008. Diakses tanggal 15 Juni 2023.
- ^ Hebert, H. Josef (6 Maret 2009). "Nuclear waste won't be going to Nevada's Yucca Mountain, Obama official says". Chicago Tribune. hlm. 4. Diarsipkan dari versi asli tanggal 24 Maret 2011. Diakses tanggal 15 Juni 2023.
- ^ "About the Commission". Diarsipkan dari versi asli tanggal 21 Juni 2011.
- ^ a b Blue Ribbon Commission on America’s Nuclear Future. "Disposal Subcommittee Report to the Full Commission" (PDF). Diarsipkan dari versi asli (PDF) tanggal 25 Januari 2017. Diakses tanggal 15 Juni 2023.
- ^ a b c Moss, William; Eckhardt, Roger (1995). "The Human Plutonium Injection Experiments" (PDF). Los Alamos Science. Laboratorium Nasional Los Alamos. 23: 188, 205, 208, 214. Diarsipkan dari versi asli (PDF) tanggal 14 Januari 2009. Diakses tanggal 15 Juni 2023.
- ^ a b Voelz, George L. (2000). "Plutonium and Health: How great is the risk?". Los Alamos Science. Los Alamos (NM): Laboratorium Nasional Los Alamos (26): 78–79.
- ^ a b Longworth, R. C. (November–Desember 1999). "Injected! Book review: The Plutonium Files: America's Secret Medical Experiments in the Cold War". The Bulletin of the Atomic Scientists. 55 (6): 58–61. doi:10.2968/055006016. Diarsipkan dari versi asli tanggal 5 Januari 2013.
- ^ Moss, William, dan Roger Eckhardt. (1995). "The human plutonium injection experiments." Los Alamos Science. 23: 177–233.
- ^ Openness, DOE. (June 1998). Human Radiation Experiments: ACHRE Report. Chapter 5: The Manhattan district Experiments; the first injection. Washington, DC. Superintendent of Documents US Government Printing Office.
- ^ AEC no. UR-38, 1948 Quarterly Technical Report
- ^ Yesley, Michael S. (1995). "'Ethical Harm' and the Plutonium Injection Experiments" (PDF). Los Alamos Science. 23: 280–283. Diarsipkan dari versi asli (PDF) tanggal 24 Februari 2009. Diakses tanggal 15 Juni 2023.
- ^ Martin 2000, hlm. 532.
- ^ a b "Nuclear Weapon Design". Federation of American Scientists. 1998. Diarsipkan dari versi asli tanggal 26 Desember 2008. Diakses tanggal 15 Juni 2023.
- ^ a b "Mixed Oxide (MOX) Fuel". London (UK): World Nuclear Association. 2006. Diarsipkan dari versi asli tanggal 1 Maret 2013. Diakses tanggal 15 Juni 2023.
- ^ Till & Chang 2011, hlm. 254–256.
- ^ Till & Chang 2011, hlm. 15.
- ^ a b "Plutonium Storage at the Department of Energy's Savannah River Site: First Annual Report to Congress" (PDF). Defense Nuclear Facilities Safety Board. 2004. hlm. A–1. Diarsipkan dari versi asli (PDF) tanggal 17 Februari 2017. Diakses tanggal 15 Juni 2023.
- ^ Besmann, Theodore M. (2005). "Thermochemical Behavior of Gallium in Weapons-Material-Derived Mixed-Oxide Light Water Reactor (LWR) Fuel". Journal of the American Ceramic Society. 81 (12): 3071–3076. doi:10.1111/j.1151-2916.1998.tb02740.x. Diarsipkan dari versi asli tanggal 17 Maret 2020. Diakses tanggal 15 Juni 2023.
- ^ a b c d "Plutonium". World Nuclear Association. Maret 2009. Diarsipkan dari versi asli tanggal 30 Maret 2010. Diakses tanggal 15 Juni 2023.
- ^ "Science for the Critical Masses: How Plutonium Changes with Time". Institute for Energy and Environmental Research. Diarsipkan dari versi asli tanggal 14 Februari 2012. Diakses tanggal 15 Juni 2023.
- ^ a b "From heat sources to heart sources: Los Alamos made material for plutonium-powered pumper". Actinide Research Quarterly. Los Alamos: Laboratorium Nasional Los Alamos (1). 2005. Diarsipkan dari versi asli tanggal 16 Februari 2013. Diakses tanggal 15 Juni 2023.
- ^ "Why the Cassini Mission Cannot Use Solar Arrays" (PDF). NASA/JPL. 6 Desember 1996. Diarsipkan dari versi asli (PDF) tanggal 26 Februari 2015. Diakses tanggal 15 Juni 2023.
- ^ St. Fleur, Nicholas, "The Radioactive Heart of the New Horizons Spacecraft to Pluto" Diarsipkan 9 Januari 2017 di Wayback Machine., New York Times, 7 Agustus 2015. Generator seberat 125 pon pesawat itu [disebut] Generator Termoelektrik Radioisotop Sumber Panas Tujuan Umum. [Ia] diisi dengan 24 pon plutonium yang menghasilkan sekitar 240 watt listrik ketika meninggalkan Bumi pada tahun 2006, menurut Ryan Bechtel, seorang insinyur dari Departemen Energi A.S. yang bekerja pada tenaga nuklir luar angkasa. Selama terbang melintasi Pluto, baterai itu menghasilkan 202 watt, ujar Mr. Bechtel. Dayanya akan terus berkurang saat logam meluruh, tetapi jumlahnya cukup untuk memerintahkan prob itu selama 20 tahun lagi, menurut Curt Niebur, seorang ilmuwan program NASA di misi New Horizons." Diakses tanggal 15 Juni 2023.
- ^ Mosher, Dave (19 September 2013). "NASA's Plutonium Problem Could End Deep-Space Exploration". Wired. Diarsipkan dari versi asli tanggal 8 Februari 2015. Diakses tanggal 15 Juni 2023.
- ^ "Voyager-Spacecraft Lifetime". Jet Propulsion Laboratory. 11 Juni 2014. Diarsipkan dari versi asli tanggal 27 Oktober 2007. Diakses tanggal 15 Juni 2023.
- ^
Venkateswara Sarma Mallela; V. Ilankumaran; N.Srinivasa Rao (2004). "Trends in Cardiac Pacemaker Batteries". Indian Pacing Electrophysiol. 4 (4): 201–212. PMC 1502062
 . PMID 16943934.
. PMID 16943934.
- ^ "Plutonium Powered Pacemaker (1974)". Oak Ridge Associated Universities. Diarsipkan dari versi asli tanggal 29 Oktober 2021. Diakses tanggal 15 Juni 2023.
- ^ "Plutonium Powered Pacemaker (1974)". Oak Ridge: Orau.org. 2021. Diarsipkan dari versi asli tanggal 29 Oktober 2021. Diakses tanggal 15 Juni 2023.
- ^ "Nuclear pacemaker still energized after 34 years". 19 Desember 2007. Diarsipkan dari versi asli tanggal 9 Januari 2018. Diakses tanggal 15 Juni 2023.
- ^ Bayles, John J.; Taylor, Douglas (1970). SEALAB III – Diver's Isotopic Swimsuit-Heater System (Laporan). Port Hueneme: Naval Civil Engineering Lab. AD0708680. Diarsipkan dari versi asli tanggal 12 Maret 2020.
- ^ "Toxicological Profile for Plutonium" (PDF). U.S. Department of Health and Human Services, Agency for Toxic Substances and Disease Registry (ATSDR). November 2010. Diarsipkan dari versi asli (PDF) tanggal 28 Mei 2012. Diakses tanggal 16 Juni 2023.
- ^ Little, M. P. (Juni 2009). "Cancer and non-cancer effects in Japanese atomic bomb survivors". J Radiol Prot. 29 (2A): A43–59. Bibcode:2009JRP....29...43L. doi:10.1088/0952-4746/29/2A/S04. PMID 19454804.
- ^ "Plutonium, CAS ID #: 7440-07-5". Centers for Disease Control and Prevention (CDC) Agency for Toxic Substances and Disease Registry. Diarsipkan dari versi asli tanggal 5 Februari 2015. Diakses tanggal 16 Juni 2023.
- ^ Grellier, James; Atkinson, Will; Bérard, Philippe; Bingham, Derek; Birchall, Alan; Blanchardon, Eric; Bull, Richard; Guseva Canu, Irina; Challeton-de Vathaire, Cécile; Cockerill, Rupert; Do, Minh T; Engels, Hilde; Figuerola, Jordi; Foster, Adrian; Holmstock, Luc; Hurtgen, Christian; Laurier, Dominique; Puncher, Matthew; Riddell, Tony; Samson, Eric; Thierry-Chef, Isabelle; Tirmarche, Margot; Vrijheid, Martine; Cardis, Elisabeth (2017). "Risk of lung cancer mortality in nuclear workers from internal exposure to alpha particle-emitting radionuclides". Epidemiology. 28 (5): 675–684. doi:10.1097/EDE.0000000000000684. PMC 5540354
 . PMID 28520643.
. PMID 28520643.
- ^ "Radiological control technical training" (PDF). U.S. Department of Energy. Diarsipkan dari versi asli (PDF) tanggal 30 Juni 2007. Diakses tanggal 16 Juni 2023.
- ^ a b c Cohen, Bernard L. "The Myth of Plutonium Toxicity". Diarsipkan dari versi asli tanggal 26 Agustus 2011.
- ^ Cohen, Bernard L. (Mei 1977). "Hazards from Plutonium Toxicity". The Radiation Safety Journal: Health Physics. 32 (5): 359–379. doi:10.1097/00004032-197705000-00003. PMID 881333. Diarsipkan dari versi asli tanggal 16 Maret 2022. Diakses tanggal 16 Juni 2023.
- ^ Welsome, Eileen (1999). The Plutonium Files: America's Secret Medical Experiments in the Cold War. New York: The Dial Press. hlm. 15–19. ISBN 0-385-31402-7. OCLC 537755781.
- ^ Brown, Shannon C.; Margaret F. Schonbeck; David McClure; et al. (Juli 2004). "Lung cancer and internal lung doses among plutonium workers at the Rocky Flats Plant: a case-control study". American Journal of Epidemiology. Oxford Journals. 160 (2): 163–172. doi:10.1093/aje/kwh192
 . PMID 15234938.
. PMID 15234938.
- ^ "ANL human health fact sheet—plutonium" (PDF). Laboratorium Nasional Argonne. 2001. Diarsipkan dari versi asli (PDF) tanggal 16 Februari 2013. Diakses tanggal 16 Juni 2023.
- ^ "Radiation Protection, Plutonium: What does plutonium do once it gets into the body?". U.S. Environmental Protection Agency. Diarsipkan dari versi asli tanggal 16 Maret 2011. Diakses tanggal 16 Juni 2023.
- ^ "Did Ralph Nader say that a pound of plutonium could cause 8 billion cancers?". Diarsipkan dari versi asli tanggal 3 November 2013. Diakses tanggal 16 Juni 2023.
- ^ a b Bernard L. Cohen. "The Nuclear Energy Option, Chapter 13, Plutonium and Bombs". Diarsipkan dari versi asli tanggal 21 Juli 2013. Diakses tanggal 16 Juni 2023. (Online version of Cohen's book The Nuclear Energy Option (Plenum Press, 1990) ISBN 0-306-43567-5).
- ^ Voelz, G. L. (1975). "What We Have Learned About Plutonium from Human Data". The Radiation Safety Journal Health Physics. 29 (4): 551–561. doi:10.1097/00004032-197510000-00011. PMID 1205858. Diarsipkan dari versi asli tanggal 16 Agustus 2017. Diakses tanggal 16 Juni 2023.
- ^ a b Skwarzec, B; Struminska, D; Borylo, A (2001). "Bioaccumulation and distribution of plutonium in fish from Gdansk Bay". Journal of Environmental Radioactivity. 55 (2): 167–178. doi:10.1016/s0265-931x(00)00190-9. PMID 11398376.
- ^ Baxter, M; Fowler, S; Povined, P (1995). "Observations on plutonium in the oceans". Applied Radiation and Isotopes. 46 (11): 1213–1223. doi:10.1016/0969-8043(95)00163-8.
- ^ Lerebours, A; Gudkov, D; Nagorskaya, L; Kaglyan, A; Rizewski, V; Leshchenko, A (2018). "Impact of Environmental Radiation on the Health and Reproductive Status of Fish from Chernobyl". Environmental Science & Technology. 52 (16): 9442–9450. Bibcode:2018EnST...52.9442L. doi:10.1021/acs.est.8b02378
 . PMID 30028950.
. PMID 30028950.
- ^ Till, John E.; Kaye, S. V.; Trabalka, J. R. (1976). "The Toxicity of Uranium and Plutonium to the Developing Embryos of Fish". Laboratorium Nasional Oak Ridge: 187. doi:10.2172/7344946. Diarsipkan dari versi asli tanggal 16 Maret 2022. Diakses tanggal 16 Juni 2023.
- ^ Miner 1968, hlm. 546
- ^ Roark, Kevin N. (2000). "Criticality accidents report issued". Los Alamos (NM): Laboratorium Nasional Los Alamos. Diarsipkan dari versi asli tanggal 8 Oktober 2008. Diakses tanggal 16 Juni 2023.
- ^ Hunner 2004, hlm. 85.
- ^ "Raemer Schreiber". Staff Biographies. Los Alamos, NM: Laboratorium Nasional Los Alamos. Diarsipkan dari versi asli tanggal 3 Januari 2013. Diakses tanggal 16 Juni 202.
- ^ McLaughlin, Monahan & Pruvost 2000, hlm. 17.
- ^ Albright, David; O'Neill, Kevin (1999). "The Lessons of Nuclear Secrecy at Rocky Flats". ISIS Issue Brief. Institute for Science and International Security (ISIS). Diarsipkan dari versi asli tanggal 8 Juli 2008. Diakses tanggal 16 Juni 2023.
- ^ "Transport of Radioactive Materials". World Nuclear Association. Diarsipkan dari versi asli tanggal 5 Februari 2015. Diakses tanggal 16 Juni 2023.
- ^ "§ 71.63 Special requirement for plutonium shipments". Komisi Regulasi Nuklir Amerika Serikat. Diarsipkan dari versi asli tanggal 5 Februari 2015. Diakses tanggal 16 Juni 2023.
- ^ "Pacific Egret". Diarsipkan dari versi asli tanggal 20 April 2016. Diakses tanggal 16 Juni 2023.
- ^ Yamaguchi, Mari. "Two British ships arrive in Japan to carry plutonium to US". Diarsipkan dari versi asli tanggal 23 Maret 2016. Diakses tanggal 16 Juni 2023.
- ^ "Two British ships arrive in Japan to transport plutonium for storage in U.S." Diarsipkan dari versi asli tanggal 24 Maret 2016. Diakses tanggal 16 Juni 2023.
- ^ "Part 175.704 Plutonium shipments". Code of Federal Regulations 49 — Transportation. Diarsipkan dari versi asli tanggal 27 April 2012. Diakses tanggal 16 Juni 2023.
- ^ a b c Av Ida Søraunet Wangberg og Anne Kari Hinna. "Klassekampen : Flyr plutonium med rutefly". Klassekampen.no. Diarsipkan dari versi asli tanggal 2 Agustus 2012. Diakses tanggal 16 Juni 2023.
- ^ "Plutonium movies and TV shows". BestSimilar.com. BestSimilar.com. Diakses tanggal 16 Juni 2023.
Referensi
[sunting | sunting sumber]- Asimov, Isaac (1988). "Nuclear Reactors". Understanding Physics. New York: Barnes & Noble Publishing. ISBN 0-88029-251-2.
- Bernstein, Jeremy (2007). Plutonium: a History of the World's most Dangerous Element
 . Washington, D.C.: Joseph Henry Press. ISBN 978-0-309-10296-4. OCLC 76481517.
. Washington, D.C.: Joseph Henry Press. ISBN 978-0-309-10296-4. OCLC 76481517. - Clark, Ronald (1961). The Birth of the Bomb: The Untold Story of Britain's Part in the Weapon That Changed the World. London: Phoenix House. OCLC 824335.
- Eagleson, Mary (1994). Concise Encyclopedia Chemistry
 . Berlin: Walter de Gruyter. ISBN 978-3-11-011451-5.
. Berlin: Walter de Gruyter. ISBN 978-3-11-011451-5. - Emsley, John (2001). "Plutonium". Nature's Building Blocks: An A–Z Guide to the Elements. Oxford (UK): Oxford University Press. ISBN 0-19-850340-7.
- Gosling, F. G. (1999). The Manhattan Project: Making the Atomic Bomb (PDF). Oak Ridge: Departemen Energi Amerika Serikat. ISBN 0-7881-7880-6. DOE/MA-0001-01/99. Diarsipkan dari versi asli (PDF) tanggal 24 Februari 2009. Diakses tanggal 16 Juni 2023.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (edisi ke-2). Oxford (UK): Butterworth-Heinemann. ISBN 0-7506-3365-4.
- Heiserman, David L. (1992). "Element 94: Plutonium"
 . Exploring Chemical Elements and their Compounds. New York (NY): TAB Books. hlm. 337–340. ISBN 0-8306-3018-X.
. Exploring Chemical Elements and their Compounds. New York (NY): TAB Books. hlm. 337–340. ISBN 0-8306-3018-X. - Hoddeson, Lillian; Henriksen, Paul W.; Meade, Roger A.; Westfall, Catherine L. (1993). Critical Assembly: A Technical History of Los Alamos During the Oppenheimer Years, 1943–1945. New York: Cambridge University Press. ISBN 0-521-44132-3. OCLC 26764320.
- Hunner, Jon (2004). Inventing Los Alamos. ISBN 978-0-8061-3891-6.
- Hurst, D. G.; Ward, A. G. (1956). Canadian Research Reactors (PDF). Ottawa: Atomic Energy of Canada Limited. OCLC 719819357. Diarsipkan dari versi asli (PDF) tanggal 5 Februari 2015. Diakses tanggal 16 Juni 2023.
- Jha, D. K. (2004). Nuclear Energy. Discovery Publishing House. ISBN 81-7141-884-8. Diarsipkan dari versi asli tanggal 6 Januari 2022. Diakses tanggal 16 Juni 2023.
- Kaku, Michio; Trainer, Jennifer (1983). Nuclear Power, Both Sides: The Best Arguments for and Against the Most Controversial Technology. W. W. Norton & Company. ISBN 9780393301281. Diarsipkan dari versi asli tanggal 6 Januari 2022. Diakses tanggal 16 Juni 2023.
- Kay, A. E. (1965). plutonium 1965. Taylor & Francis. Diarsipkan dari versi asli tanggal 6 Januari 2022. Diakses tanggal 16 Juni 2023.
- Lide, David R., ed. (2006). Handbook of Chemistry and Physics (edisi ke-87). Boca Raton: CRC Press, Taylor & Francis Group. ISBN 0-8493-0487-3.
- Magurno, B. A.; Pearlstein, S., ed. (1981). Proceedings of the conference on nuclear data evaluation methods and procedures. BNL-NCS 51363 (PDF). II. Upton: Laboratorium Nasional Brookhaven. Diarsipkan dari versi asli (PDF) tanggal 8 Maret 2021. Diakses tanggal 16 Juni 2023.
- Martin, James E. (2000). Physics for Radiation Protection. Wiley-Interscience. ISBN 0-471-35373-6.
- McLaughlin, Thomas P.; Monahan, Shean P.; Pruvost, Norman L. (2000). A Review of Criticality Accidents (PDF). Los Alamos, NM: Laboratorium Nasional Los Alamos. LA-13638. Diarsipkan dari versi asli (PDF) tanggal 18 Januari 2017. Diakses tanggal 16 Juni 2023.
- Miner, William N.; Schonfeld, Fred W. (1968). "Plutonium"
 . Dalam Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York (NY): Reinhold Book Corporation. hlm. 540–546. LCCN 68029938.
. Dalam Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York (NY): Reinhold Book Corporation. hlm. 540–546. LCCN 68029938. - Moody, Kenton James; Hutcheon, Ian D.; Grant, Patrick M. (2005). Nuclear forensic analysis. CRC Press. ISBN 0-8493-1513-1. Diarsipkan dari versi asli tanggal 6 Januari 2022. Diakses tanggal 16 Juni 2023.
- Rhodes, Richard (1986). The Making of the Atomic Bomb. New York: Simon & Schuster. ISBN 0-671-65719-4.
- Seaborg, G. T.; Seaborg, E. (2001). Adventures in the Atomic Age: From Watts to Washington
 . Farrar, Straus and Giroux. ISBN 0-374-29991-9.
. Farrar, Straus and Giroux. ISBN 0-374-29991-9. - Sklar, Morty (1984). Nuke-Rebuke: Writers & Artists Against Nuclear Energy & Weapons. The Contemporary anthology series. The Spirit That Moves Us Press.
- Stockholm International Peace Research Institute (2007). SIPRI Yearbook 2007: Armaments, Disarmament, and International Security. Oxford University Press. ISBN 978-0-19-923021-1. Diarsipkan dari versi asli tanggal 6 Januari 2022. Diakses tanggal 16 Juni 2023.
- Till, C. E.; Chang, Y. I. (2011). Plentiful Energy: The Story of the Integral Fast Reactor, the Complex History of a Simple Reactor Technology, with Emphasis on Its Scientific Basis for Non-specialists. Charles E. Till and Yoon Il Chang. ISBN 978-1-4663-8460-6.
- Wahlen, R. K. (1989). History of 100-B Area (PDF). Richland, Washington: Westinghouse Hanford Company. WHC-EP-0273. Diarsipkan dari versi asli (PDF) tanggal 27 Maret 2009. Diakses tanggal 16 Juni 2023.
- Welsome, Eileen (2000). The Plutonium Files: America's Secret Medical Experiments in the Cold War. New York: Random House. ISBN 0-385-31954-1.
Pranala luar
[sunting | sunting sumber]- (Inggris) "Alsos Digital Library for Nuclear Issues – Plutonium". Washington and Lee University. Diarsipkan dari versi asli tanggal 3 Februari 2009. Diakses tanggal 16 Juni 2023.
- (Inggris) Sutcliffe, W. G.; et al. (1995). "A Perspective on the Dangers of Plutonium". Laboratorium Nasional Lawrence Livermore. Diarsipkan dari versi asli tanggal 29 September 2006.
- (Inggris) "Physical, Nuclear, and Chemical, Properties of Plutonium". IEER. 2005. Diakses tanggal 16 Juni 2023.
- (Inggris) Bhadeshia, H. "Plutonium crystallography".
- (Inggris) Samuels, D. (2005). "End of the Plutonium Age". Discover Magazine. 26 (11).
- (Inggris) Pike, J.; Sherman, R. (2000). "Plutonium production". Federation of American Scientists. Diarsipkan dari versi asli tanggal 3 Februari 2009. Diakses tanggal 16 Juni 2023.
- (Inggris) "Plutonium Manufacture and Fabrication".
- (Inggris) Ong, C. (1999). "World Plutonium Inventories". Nuclear Files.org. Diarsipkan dari versi asli tanggal 5 Agustus 2014. Diakses tanggal 16 Juni 2023.
- (Inggris) "Challenges in Plutonium Science". Los Alamos Science. I & II (26). 2000. Diakses tanggal 16 Juni 2023.
- (Inggris) "Plutonium". Royal Society of Chemistry. Diakses tanggal 16 Juni 2023.
- (Inggris) "Plutonium". The Periodic Table of Videos. Universitas Nottingham. Diakses tanggal 16 Juni 2023.
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


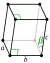
![{\displaystyle {\ce {{^{238}_{92}U}+{^{1}_{0}n}->{^{239}_{92}U}->[\beta ^{-}][23,5\ {\ce {mnt}}]{^{239}_{93}Np}->[\beta ^{-}][2,3565\ {\ce {hri}}]{^{239}_{94}Pu}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4098f26d73ffd83e8cba005e7be94976b62e6741)
![{\displaystyle {\begin{aligned}{\ce {{^{238}_{92}U}+{^{2}_{1}D}->}}&{\ce {{^{238}_{93}Np}+2_{0}^{1}n}}\\&{\ce {^{238}_{93}Np->[\beta ^{-}][2,117\ {\ce {hri}}]{^{238}_{94}Pu}}}\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/804b7f7e8b0e838418503580ba22e6040b7ab702)
