Lambang unsur
Lambang unsur adalah singkatan yang digunakan dalam kimia untuk unsur kimia, gugus fungsi, dan senyawa kimia. Lambang unsur untuk sebuah unsur kimia biasanya terdiri dari satu atau dua huruf dari huruf Latin dan huruf pertama ditulis dengan huruf kapital. Dalam bahasa Tionghoa, setiap unsur kimia memiliki karakter khusus, biasanya dibuat untuk tujuan tertentu. Namun, lambang Latin juga tetap digunakan, terutama dalam rumus.
Lambang yang lebih awal untuk unsur kimia berasal dari kosakata Latin dan Yunani klasik. Untuk beberapa unsur, ini karena bahannya sudah dikenal di zaman kuno, sedangkan untuk yang lain, namanya adalah penemuan yang lebih baru. Misalnya, Pb adalah lambang untuk timbal (plumbum dalam bahasa Latin); Hg adalah lambang untuk raksa (hydrargyrum dalam bahasa Yunani); dan He adalah lambang untuk helium (nama Latin baru) karena helium tidak dikenal di zaman Romawi kuno. Beberapa simbol berasal dari sumber lain, seperti W untuk tungsten (wolfram dalam bahasa Jerman) yang tidak dikenal pada zaman Romawi.
Lambang sementara tiga huruf dapat diberikan pada unsur yang baru disintesis (atau belum disintesis). Misalnya, "Uno" adalah lambang sementara untuk hasium (unsur ke-108) yang memiliki nama sementara unniloktium, berdasarkan angka nomor atomnya. Ada juga beberapa lambang lama yang tidak lagi digunakan secara resmi.
Selain huruf untuk unsur itu sendiri, detail tambahan dapat ditambahkan pada lambang sebagai subskrip (tulisan yang berada di bawah) atau superskrip (tulisan yang berada di atas) bagi isotop, ionisasi, atau bilangan oksidasi, atau detail atom tertentu lainnya.[1] Beberapa isotop memiliki lambang spesifiknya sendiri, bukan hanya detail isotop yang ditambahkan ke lambang elemennya.
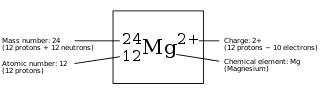
Subskrip atau superskrip terlampir yang menentukan nuklida atau molekul memiliki arti dan posisi sebagai berikut:
- Nomor nukleon (nomor massa) ditampilkan dengan superskrip di sebelah kiri (misalnya, 14N). Nomor ini mendefinisikan isotop spesifik. Berbagai huruf, seperti "m" dan "f" juga dapat digunakan di sini untuk menunjukkan isomer nuklir (misalnya, 99mTc). Sebagai alternatif, angka di sini dapat mewakili keadaan spin tertentu (misalnya, 1O2). Detail ini dapat dihilangkan jika tidak relevan dalam konteks tertentu.
- Nomor proton (nomor atom) ditampilkan dengan subskrip di sebelah kiri (misalnya, 69Tm). Nomor atom terlihat kurang berguna jika ditulis untuk unsur kimia, tetapi kadang-kadang digunakan untuk menekankan perubahan jumlah nukleon dalam reaksi nuklir.
- Jika perlu, keadaan ionisasi atau keadaan tereksitasi dapat ditunjukkan dengan superskrip di sebelah kanan (misalnya, bilangan ionisasi Ca2+).
- Jumlah atom suatu unsur dalam molekul atau senyawa kimia ditunjukkan dengan subskrip di sebelah kanan (misalnya, H2O atau Fe2O3). Jika angkanya satu, biasanya dihilangkan - angka satu secara implisit dipahami jika tidak ditentukan.
- Sebuah radikal ditunjukkan dengan titik di sebelah kanan (misalnya, Cl• untuk atom klorin netral). Ini sering dihilangkan kecuali relevan dengan konteks tertentu karena sudah dapat dikurangkan dari muatan dan nomor atom, seperti umumnya berlaku untuk elektron valensi tidak terikat dalam rumus kerangka.
Banyak gugus fungsi juga memiliki lambang kimianya sendiri, misalnya Ph untuk gugus fenil, dan Me untuk gugus metil.

Daftar tanda dan lambang saat ini, yang kuno, juga yang diusulkan serta yang secara historis disertakan di sini dengan artinya. Juga diberikan nomor atom setiap unsur, berat atom atau massa atom dari isotop paling stabil, nomor golongan dan periode pada tabel periodik, dan juga etimologi lambang.
Piktograf bahaya adalah jenis lambang lain yang digunakan dalam kimia.
Lambang unsur kimia
[sunting | sunting sumber]| Z[I] | Lambang | Nama | Asal nama[2][3] | Golongan | Periode | Berat atom[4][5] (u (±)) |
|---|---|---|---|---|---|---|
| 1 | H | Hidrogen | Yunani hydro- dan -gen, 'pembentuk air' | 1 | 1 | 1,008[II][III][IV][V] |
| 2 | He | Helium | Yunani hḗlios, 'Matahari' | 18 | 1 | 4,002602(2)[II][IV] |
| 3 | Li | Litium | Yunani líthos, 'batu' | 1 | 2 | 6,94[II][III][IV][VI][V] |
| 4 | Be | Berilium | beril, sebuah mineral (akhirnya dari nama Belur di India selatan) | 2 | 2 | 9,0121831(5) |
| 5 | B | Boron | boraks, sebuah mineral (dari Arab bawraq) | 13 | 2 | 10,81[II][III][IV][V] |
| 6 | C | Karbon | Latin carbo, 'batu bara' | 14 | 2 | 12,011[II][IV][V] |
| 7 | N | Nitrogen | Yunani nítron dan -gen, 'pembentuk niter' | 15 | 2 | 14,007[II][IV][V] |
| 8 | O | Oksigen | Yunani oxy- dan -gen, 'pembentuk asam' | 16 | 2 | 15,999[II][IV][V] |
| 9 | F | Fluorin | Latin fluere, 'mengalir' | 17 | 2 | 18,998403163(6) |
| 10 | Ne | Neon | Yunani néon, 'baru' | 18 | 2 | 20,1797(6)[II][III] |
| 11 | Na | Natrium | Latin baru natrium, berasal dari Jerman Natron, 'natron' | 1 | 3 | 22,98976928(2) |
| 12 | Mg | Magnesium | Magnesia, sebuah distrik di Thessalia Timur di Yunani | 2 | 3 | 24,305[V] |
| 13 | Al | Aluminium | alumina, dari Latin alumen (gen. alumni), 'garam pahit, tawas' | 13 | 3 | 26,9815384(3) |
| 14 | Si | Silikon | Latin silex, 'rijang' (semula silicium) | 14 | 3 | 28,085[IV][V] |
| 15 | P | Fosforus | Yunani phōsphóros, 'penghantar cahaya' | 15 | 3 | 30,973761998(5) |
| 16 | S | Belerang | Latin sulphur, 'batu belerang' | 16 | 3 | 32,06[II][IV][V] |
| 17 | Cl | Klorin | Yunani chlōrós, 'kuning kehijauan' | 17 | 3 | 35,45[II][III][IV][V] |
| 18 | Ar | Argon | Yunani argós, 'diam' (karena kelembamannya) | 18 | 3 | 39,948[II][IV][V] |
| 19 | K | Kalium | Latin kalium | 1 | 4 | 39,0983(1) |
| 20 | Ca | Kalsium | Latin calx, 'kapur' | 2 | 4 | 40,078(4)[II] |
| 21 | Sc | Skandium | Latin Scandia, 'Skandinavia' | 3 | 4 | 44,955908(5) |
| 22 | Ti | Titanium | Titans, putra dewi Bumi dari mitologi Yunani | 4 | 4 | 47,867(1) |
| 23 | V | Vanadium | Vanadis, nama Nordik Kuno untuk dewi Skandinavia Freyja | 5 | 4 | 50,9415(1) |
| 24 | Cr | Kromium | Yunani chróma, 'warna' | 6 | 4 | 51,9961(6) |
| 25 | Mn | Mangan | magnesia negra; lihat Magnesium | 7 | 4 | 54,938043(2) |
| 26 | Fe | Besi | Latin ferrum | 8 | 4 | 55,845(2) |
| 27 | Co | Kobalt | Jerman Kobold, 'goblin' | 9 | 4 | 58,933194(3) |
| 28 | Ni | Nikel | Nickel, sprite nakal dari mitologi penambang Jerman | 10 | 4 | 58,6934(4) |
| 29 | Cu | Tembaga | Latin cuprum, dari Yunani Kuno Kýpros, 'Siprus' | 11 | 4 | 63,546(3)[IV] |
| 30 | Zn | Seng | kemungkinan besar dari Jerman Zinke, 'cabang' atau 'gigi', meskipun beberapa memperkirakan dari Farsi sang, 'batu' | 12 | 4 | 65,38(2) |
| 31 | Ga | Galium | Latin Galia, 'Prancis' | 13 | 4 | 69,723(1) |
| 32 | Ge | Germanium | Latin Germania, 'Jerman' | 14 | 4 | 72,630(8) |
| 33 | As | Arsen | Prancis arsenic, dari Yunani arsenikón 'arsen kuning' (dipengaruhi oleh arsenikós, 'maskulin' atau 'jantan'), dari sebuah wanderwort Asia Barat yang pada akhirnya berasal dari Persia Kuno *zarniya-ka, 'seperti emas' | 15 | 4 | 74,921595(6) |
| 34 | Se | Selenium | Yunani selḗnē, 'Bulan' | 16 | 4 | 78,971(8)[IV] |
| 35 | Br | Bromin | Yunani brômos, 'bau' | 17 | 4 | 79,904[V] |
| 36 | Kr | Kripton | Yunani kryptós, 'tersembunyi' | 18 | 4 | 83,798(2)[II][III] |
| 37 | Rb | Rubidium | Latin rubidus, 'merah tua' | 1 | 5 | 85,4678(3)[II] |
| 38 | Sr | Stronsium | Strontian, sebuah desa di Skotlandia | 2 | 5 | 87,62(1)[II][IV] |
| 39 | Y | Itrium | Ytterby, sebuah desa di Swedia | 3 | 5 | 88,90584(1) |
| 40 | Zr | Zirkonium | zirkon, sebuah mineral | 4 | 5 | 91,224(2)[II] |
| 41 | Nb | Niobium | Niobe, putri raja Tantalos dari mitologi Yunani | 5 | 5 | 92,90637(1) |
| 42 | Mo | Molibdenum | Yunani molýbdaina, 'sepotong timbal', dari mólybdos, 'timbal' | 6 | 5 | 95,95(1)[II] |
| 43 | Tc | Teknesium | Yunani tekhnētós, 'buatan' | 7 | 5 | [97][VII] |
| 44 | Ru | Rutenium | Latin baru Rutenia, 'Rusia' | 8 | 5 | 101,07(2)[II] |
| 45 | Rh | Rodium | Yunani rhodóeis, 'berwarna mawar', dari rhódon, 'mawar' | 9 | 5 | 102,90549(2) |
| 46 | Pd | Paladium | asteroid Pallas, dianggap sebagai planet pada saat itu | 10 | 5 | 106,42(1)[II] |
| 47 | Ag | Perak | Latin argentum | 11 | 5 | 107,8682(2)[II] |
| 48 | Cd | Kadmium | Latin baru cadmia, dari Raja Kadmos | 12 | 5 | 112,414(4)[II] |
| 49 | In | Indium | Latin indicum, 'indigo' (warna yang ditemukan dalam spektrumnya) | 13 | 5 | 114,818(1) |
| 50 | Sn | Timah | Latin stannum | 14 | 5 | 118,710(7)[II] |
| 51 | Sb | Antimon | Latin stibium 'stibnit' | 15 | 5 | 121,760(1)[II] |
| 52 | Te | Telurium | Latin tellus, 'tanah, Bumi' | 16 | 5 | 127,60(3)[II] |
| 53 | I | Iodin | Prancis iode, dari Yunani ioeidḗs, 'violet' | 17 | 5 | 126,90447(3) |
| 54 | Xe | Xenon | Yunani xénon, bentuk netral dari xénos 'aneh' | 18 | 5 | 131,293(6)[II][III] |
| 55 | Cs | Sesium | Latin caesius, 'biru langit' | 1 | 6 | 132,90545196(6) |
| 56 | Ba | Barium | Yunani barýs, 'berat' | 2 | 6 | 137,327(7) |
| 57 | La | Lantanum | Yunani lanthánein, 'bersembunyi' | 6 | 138,90547(7)[II] | |
| 58 | Ce | Serium | planet katai Ceres, dianggap sebagai planet pada saat itu | 6 | 140,116(1)[II] | |
| 59 | Pr | Praseodimium | Yunani prásios dídymos, 'kembar hijau' | 6 | 140,90766(1) | |
| 60 | Nd | Neodimium | Yunani néos dídymos, 'kembar baru' | 6 | 144,242(3)[II] | |
| 61 | Pm | Prometium | Prometheus dari mitologi Yunani | 6 | [145][VII] | |
| 62 | Sm | Samarium | samarskit, sebuah mineral yang dinamai dari Kolonel Vasili Samarsky-Bykhovets, pejabat tambang Rusia | 6 | 150,36(2)[II] | |
| 63 | Eu | Europium | Eropa | 6 | 151,964(1)[II] | |
| 64 | Gd | Gadolinium | gadolinit, sebuah mineral yang dinamai dari Johan Gadolin, ahli kimia, fisikawan, dan ahli mineral Finlandia | 6 | 157,25(3)[II] | |
| 65 | Tb | Terbium | Ytterby, sebuah desa di Swedia | 6 | 158,925354(8) | |
| 66 | Dy | Disprosium | Yunani dysprósitos, 'sulit didapatkan' | 6 | 162,500(1)[II] | |
| 67 | Ho | Holmium | Latin baru Holmia, 'Stockholm' | 6 | 164,930328(7) | |
| 68 | Er | Erbium | Ytterby, sebuah desa di Swedia | 6 | 167,259(3)[II] | |
| 69 | Tm | Tulium | Thule, nama kuno untuk lokasi di utara Bumi yang tidak jelas | 6 | 168,934218(6) | |
| 70 | Yb | Iterbium | Ytterby, sebuah desa di Swedia | 6 | 173,045(10)[II] | |
| 71 | Lu | Lutesium | Latin Lutetia, 'Paris' | 3 | 6 | 174,9668(1)[II] |
| 72 | Hf | Hafnium | Latin baru Hafnia, 'Kopenhagen' (dari Denmark havn) | 4 | 6 | 178,49(2) |
| 73 | Ta | Tantalum | Raja Tantalos, ayah Niobe dari mitologi Yunani | 5 | 6 | 180,94788(2) |
| 74 | W | Wolfram | nama lama dari mineral wolfram wolframit | 6 | 6 | 183,84(1) |
| 75 | Re | Renium | Latin Rhenus, 'Rhein' | 7 | 6 | 186,207(1) |
| 76 | Os | Osmium | Yunani osmḗ, 'bau' | 8 | 6 | 190,23(3)[II] |
| 77 | Ir | Iridium | Iris, dewi pelangi Yunani | 9 | 6 | 192,217(2) |
| 78 | Pt | Platina | Spanyol platina, 'perak kecil', dari plata 'perak' | 10 | 6 | 195,084(9) |
| 79 | Au | Emas | Latin aurum | 11 | 6 | 196,966570(4) |
| 80 | Hg | Raksa | Latin hydrargyrum, berasal dari Yunani hydrárgyros, 'air-perak') | 12 | 6 | 200,592(3) |
| 81 | Tl | Talium | Yunani thallós, 'pucuk atau ranting hijau' | 13 | 6 | 204,38[V] |
| 82 | Pb | Timbal | Latin plumbum | 14 | 6 | 207,2(1)[II][IV] |
| 83 | Bi | Bismut | Jerman Wismut, dari weiß Masse 'massa putih', kecuali dari Arab | 15 | 6 | 208,98040(1)[VII] |
| 84 | Po | Polonium | Latin Polonia, 'Polandia' (negara asal Marie Curie) | 16 | 6 | [209][VII] |
| 85 | At | Astatin | Yunani ástatos, 'tidak stabil' | 17 | 6 | [210][VII] |
| 86 | Rn | Radon | radium | 18 | 6 | [222][VII] |
| 87 | Fr | Fransium | Prancis | 1 | 7 | [223][VII] |
| 88 | Ra | Radium | Prancis radium, dari Latin radius, 'sinar' | 2 | 7 | [226][VII] |
| 89 | Ac | Aktinium | Yunani aktís, 'sinar' | 7 | [227][VII] | |
| 90 | Th | Torium | Thor, dewa guntur Skandinavia | 7 | 232,0377(4)[VII][II] | |
| 91 | Pa | Protaktinium | proto- (dari Yunani prôtos, 'pertama, sebelum') + aktinium, yang dihasilkan melalui peluruhan radioaktif protaktinium | 7 | 231,03588(1)[VII] | |
| 92 | U | Uranium | Uranus, planet ke-7 di Tata Surya | 7 | 238,02891(3)[VII] | |
| 93 | Np | Neptunium | Neptunus, planet ke-8 di Tata Surya | 7 | [237][VII] | |
| 94 | Pu | Plutonium | planet katai Pluto, dianggap sebagai planet ke-9 di Tata Surya pada saat itu | 7 | [244][VII] | |
| 95 | Am | Amerisium | Amerika, sebagai unsur pertama yang disintesis di benua itu, mirip seperti europium | 7 | [243][VII] | |
| 96 | Cm | Kurium | Pierre Curie dan Marie Curie, fisikawan dan kimiawan Prancis | 7 | [247][VII] | |
| 97 | Bk | Berkelium | Berkeley, Kalifornia, tempat di mana unsur ini pertama kali disintesis, mirip seperti terbium | 7 | [247][VII] | |
| 98 | Cf | Kalifornium | California, tempat di mana unsur ini pertama kali disintesis | 7 | [251][VII] | |
| 99 | Es | Einsteinium | Albert Einstein, fisikawan Jerman | 7 | [252][VII] | |
| 100 | Fm | Fermium | Enrico Fermi, fisikawan Italia | 7 | [257][VII] | |
| 101 | Md | Mendelevium | Dmitri Mendeleev, ahli kimia dan penemu asal Rusia yang mengusulkan tabel periodik | 7 | [258][VII] | |
| 102 | No | Nobelium | Alfred Nobel, ahli kimia dan insinyur Swedia | 7 | [259][VII] | |
| 103 | Lr | Lawrensium | Ernest O. Lawrence, fisikawan Amerika | 3 | 7 | [266][VII] |
| 104 | Rf | Ruterfordium | Ernest Rutherford, ahli kimia dan fisikawan Inggris | 4 | 7 | [267][VII] |
| 105 | Db | Dubnium | Dubna, Rusia, tempat di mana Joint Institute for Nuclear Research berada | 5 | 7 | [268][VII] |
| 106 | Sg | Seaborgium | Glenn T. Seaborg, ahli kimia Amerika | 6 | 7 | [269][VII] |
| 107 | Bh | Bohrium | Niels Bohr, fisikawan Denmark | 7 | 7 | [270][VII] |
| 108 | Hs | Hasium | Latin baru Hassia, 'Hessen' (sebuah negara bagian di Jerman) | 8 | 7 | [270][VII] |
| 109 | Mt | Meitnerium | Lise Meitner, fisikawan Austria | 9 | 7 | [278][VII] |
| 110 | Ds | Darmstadtium | Darmstadt, Jerman, tempat di mana unsur ini pertama kali disintesis | 10 | 7 | [281][VII] |
| 111 | Rg | Roentgenium | Wilhelm Conrad Röntgen, fisikawan Jerman | 11 | 7 | [282][VII] |
| 112 | Cn | Kopernisium | Nicolaus Copernicus, astronom Polandia | 12 | 7 | [285][VII] |
| 113 | Nh | Nihonium | Jepang Nihon, 'Jepang' (tempat di mana unsur ini pertama kali disintesis) | 13 | 7 | [286][VII] |
| 114 | Fl | Flerovium | Flerov Laboratory of Nuclear Reactions, bagian dari JINR, tempat di mana unsur tersebut disintesis; dinamai dari Georgy Flyorov, fisikawan Rusia | 14 | 7 | [289][VII] |
| 115 | Mc | Moskovium | Oblast Moskwa, Rusia, tempat di mana unsur ini pertama kali disintesis | 15 | 7 | [290][VII] |
| 116 | Lv | Livermorium | Laboratorium Nasional Lawrence Livermore di Livermore, California, yang berkolaborasi dengan JINR dalam penyintetisannya | 16 | 7 | [293][VII] |
| 117 | Ts | Tenesin | Tennessee, Amerika Serikat | 17 | 7 | [294][VII] |
| 118 | Og | Oganeson | Yuri Oganessian, fisikawan Rusia | 18 | 7 | [294][VII] |
Catatan
[sunting | sunting sumber]- ^ Z adalah lambang standar untuk nomor atom
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al Komposisi isotop unsur ini bervariasi di beberapa spesimen geologi, dan variasinya dapat melebihi ketidakpastian yang dinyatakan dalam tabel.
- ^ a b c d e f g Komposisi isotop unsur ini dapat bervariasi dalam bahan komersial, yang dapat menyebabkan massa atomnya menyimpang secara signifikan dari nilai yang diberikan.
- ^ a b c d e f g h i j k l m n o Komposisi isotop unsur ini bervariasi dalam bahan terestrial sehingga massa atom yang lebih tepat tidak dapat diberikan.
- ^ a b c d e f g h i j k l m Nilai berikut yang tercantum adalah nilai massa atom konvensional yang sesuai untuk perdagangan dan niaga. Nilai ini sebenarnya mungkin berbeda tergantung pada komposisi isotop sampel. Sejak 2009, IUPAC memberikan nilai massa atom standar untuk unsur-unsur ini menggunakan notasi interval. Massa atom standar yang sesuai adalah:
- Hidrogen: [1,00784, 1,00811]
- Litium: [6,938, 6,997]
- Boron: [10,806, 10,821]
- Karbon: [12,0096, 12,0116]
- Nitrogen: [14,00643, 14,00728]
- Oksigen: [15,99903, 15,99977]
- Magnesium: [24,304, 24,307]
- Silikon: [28,084, 28,086]
- Belerang: [32,059, 32,076]
- Klorin: [35,446, 35,457]
- Argon: [39,792, 39,963]
- Bromin: [79,901, 79,907]
- Talium: [204,382, 204,385]
- ^ Massa atom litium komersial dapat bervariasi antara 6,939 dan 6,996—analisis bahan spesifik diperlukan untuk menemukan nilai yang lebih akurat.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al Unsur ini tidak memiliki nuklida stabil, dan nilai dalam tanda kurung siku, misalnya [209], menunjukkan nomor massa dari isotop unsur yang berumur paling lama. Namun, empat unsur, bismut, torium, protaktinium, dan uranium, memiliki komposisi isotop terestrial yang khas, dan dengan demikian bobot atom standarnya diberikan.
Atom antimateri dilambangkan dengan garis di atas lambung pasangan materinya, jadi misalnya H adalah lambang untuk antihidrogen.
Lambang dan nama yang saat ini tidak digunakan
[sunting | sunting sumber]Berikut ini adalah daftar lambung dan nama yang sebelumnya digunakan atau disarankan untuk elemen, termasuk lambang untuk nama placeholder dan nama yang diberikan oleh pengklaim yang didiskreditkan atas penemuannya.
| Lambang | Nama | Nomor atom |
Catatan | Kenapa tidak digunakan |
Ref |
|---|---|---|---|---|---|
| A | Argon | 18 | A digunakan untuk Argon sampai tahun 1957. Saat ini lambangnya adalah Ar. | [nb 1] | [6] |
| Ab | Alabamin | 85 | Klaim yang didiskreditkan atas penemuan astatin. | [nb 2] | [7][8] |
| Ad | Aldebaranium | 70 | Nama sebelumnya dari iterbium. | [nb 2] | |
| Ah | Anglohelvetium | 85 | Klaim yang didiskreditkan atas penemuan astatin. | [nb 2] | [9] |
| Ak | Alkalinium | 87 | Klaim yang didiskreditkan atas penemuan fransium. | [nb 2] | [7] |
| Am | Alabamin | 85 | Klaim yang didiskreditkan atas penemuan astatin. Lambang Am sekarang digunakan untuk amerisium. | [nb 2] | [7][8] |
| An | Atenium | 99 | Nama yang diusulkan untuk einsteinium. | [nb 3] | |
| Ao | Ausonium | 93 | Klaim yang didiskreditkan atas penemuan neptunium. | [nb 2] | [7] |
| At | Austriakum | 84 | Klaim yang didiskreditkan atas penemuan polonium. Lambang At sekarang digunakan untuk astatin. | [nb 2] | |
| Az | Azote | 7 | Nama sebelumnya dari nitrogen. | [nb 1] | |
| Bo | Bohemium | 93 | Klaim yang didiskreditkan atas penemuan neptunium. | [nb 2] | |
| Bo | Boron | 5 | Saat ini lambangnya adalah B. | [nb 1] | |
| Bv | Brevium | 91 | Nama sebelumnya dari protaktinium. | [nb 1] | |
| Bz | Berzelium | 90 | Charles Baskerville salah mengira jika berzelium merupakan unsur baru. Yang sebenarnya adalah torium. | [9] | |
| Cb | Kolumbium | 41 | Nama sebelumnya dari niobium. | [nb 1] | [7][9] |
| Ch | Kromium | 24 | Saat ini lambangnya adalah Cr. | [nb 1] | |
| Cl | Kolumbium | 41 | Nama sebelumnya dari niobium. Lambang Cl sekarang digunakan untuk klorin. | [nb 1] | |
| Cm | Katium | 87 | Nama yang diusulkan untuk fransium. Lambang Cm sekarang digunakan untuk kurium. | [nb 3] | |
| Cn | Karolinium | 90 | Charles Baskerville salah mengira jika kparolinium merupakan unsur baru. Yang sebenarnya adalah torium. Lambang Cn sekarang digunakan untuk kopernisium. | [9] | |
| Cp | Kassiopeium | 71 | Nama sebelumnya dari lutesium. | [nb 1] | |
| Cp | Kopernisium | 112 | Saat ini lambangnya adalah Cn. | [nb 1] | |
| Ct | Seltium | 72 | Klaim yang didiskreditkan atas penemuan hafnium. | [nb 2] | |
| Ct | Senturium | 100 | Nama yang diusulkan untuk fermium. | [nb 3] | |
| Cy | Cyclonium | 61 | Nama yang diusulkan untuk prometium. | [nb 3] | |
| D | Didymium | 59/60 | Campuran unsur praseodimium dan neodimium. Carl Gustaf Mosander salah mengira jika didymium merupakan sebuah unsur. | [10] | |
| Da | Davyum | 43 | Klaim yang didiskreditkan atas penemuan teknesium. | [nb 2] | [7] |
| Db | Dubhium | 69 | Josef Maria Eder salah mengira jika dubhium merupakan unsur baru. Yang sebenarnya adalah tulium. Lambang Db sekarang digunakan untuk dubnium. | ||
| Db | Dubnium | 104 | Nama yang diusulkan untuk ruterfordium. Lambang dan nama ini kemudian digunakan untuk unsur 105. | [nb 1][nb 3] | [7] |
| Dc | Desipium | 62 | Marc Delafontaine salah mengira jika desipium merupakan unsur baru. Yang sebenarnya adalah samarium. | ||
| Dc | Dvisesium | 87 | Nama yang diberikan oleh Dmitri Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, fransium sangat cocok dengan prediksinya. | [nb 3][nb 4] | |
| De | Denebium | 69 | Josef Maria Eder salah mengira jika denebium merupakan unsur baru. Yang sebenarnya adalah tulium. | ||
| Di | Didymium | 59/60 | Campuran unsur praseodimium dan neodimium. Carl Gustaf Mosander salah mengira jika didymium merupakan sebuah unsur. | [10] | |
| Do | Dor | 85 | Klaim yang didiskreditkan atas penemuan astatin. | [nb 2] | [9] |
| Dn | Dubnadium | 118 | Nama yang diusulkan untuk oganeson. | [nb 3] | |
| Dp | Desipium | 62 | Marc Delafontaine salah mengira jika decipium merupakan unsur baru. Yang sebenarnya adalah samarium. | ||
| Ds | Disprosium | 66 | Saat ini lambangnya adalah Dy. Lambang Ds sekarang digunakan untuk darmstadtium. | [nb 1] | |
| Dt | Dvitelurium | 84 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, polonium sangat cocok dengan prediksinya. | [nb 3][nb 4] | |
| E | Einsteinium | 99 | Saat ini lambangnya adalah Es. | [nb 1] | |
| E | Erbium | 68 | Saat ini lambangnya adalah Er. | [nb 1] | |
| Ea | Ekaaluminium | 31 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, galium sangat cocok dengan prediksinya. | [nb 3][nb 4] | |
| Eb | Ekaboron | 21 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, skandium sangat cocok dengan prediksinya. | [nb 3][nb 4] | [7] |
| Eb | Erebodium | 42 | Alexander Pringle salah mengira jika erebodium merupakan unsur baru. Yang sebenarnya adalah molibdenum. | ||
| El | Ekaaluminium | 31 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, galium sangat cocok dengan prediksinya. | [nb 3][nb 4] | [7] |
| Em | Ekamangan | 43 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, teknesium sangat cocok dengan prediksinya. | [nb 3][nb 4] | [7] |
| Em | Emanasi | 86 | Juga disebut "emanasi radium", nama ini awalnya diberikan oleh Friedrich Ernst Dorn pada tahun 1900. Pada tahun 1923, unsur ini secara resmi menjadi radon (nama yang diberikan pada suatu waktu menjadi 222Rn, sebuah isotop yang teridentifikasi dalam deret peluruhan radioaktif radium). |
[nb 1] | [7] |
| Em | Emanium | 89 | Nama alternatif yang sebelumnya diusulkan untuk aktinium. | [nb 3] | |
| Es | Ekasilikon | 32 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, germanium sangat cocok dengan prediksinya. Lambang Es sekarang digunakan untuk einsteinium. |
[nb 3][nb 4] | [7] |
| Es | Esperium | 94 | Klaim yang didiskreditkan atas penemuan plutonium. Lambang Es sekarang digunakan untuk einsteinium. | [nb 2] | [7] |
| Et | Ekatantalum | 91 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, protaktinium sangat cocok dengan prediksinya. | [nb 3][nb 4] | |
| Ex | Euksenium | 72 | Klaim yang didiskreditkan atas penemuan hafnium. | [nb 2] | |
| Fa | Fransium | 87 | Saat ini lambangnya adalah Fr. | [nb 1] | |
| Fl | Florentium | 61 | Klaim yang didiskreditkan atas penemuan prometium. Lambang Fl sekarang digunakan untuk flerovium. | [nb 2] | |
| Fl | Fluorin | 9 | Saat ini lambangnya adalah F. Lambang Fl sekarang digunakan untuk flerovium. | [nb 1] | |
| Fr | Florentium | 61 | Klaim yang didiskreditkan atas penemuan prometium. Lambang Fr sekarang digunakan untuk fransium. | [nb 2] | [7] |
| G | Glusinium | 4 | Nama sebelumnya dari berilium. | [nb 1] | |
| Gh | Ghiorsium | 118 | Klaim yang didiskreditkan atas penemuan oganeson. | [nb 2] | |
| Gl | Glusinium | 4 | Nama sebelumnya dari berilium. | [nb 1] | [7] |
| Ha | Hahnium | 105 | Nama yang diusulkan untuk dubnium. | [nb 3] | |
| Hn | Hahnium | 108 | Nama yang diusulkan untuk hasium. | [nb 3] | [7] |
| Hv | Helvetium | 85 | Klaim yang didiskreditkan atas penemuan astatin. | [nb 2] | [9] |
| Hy | Raksa | 80 | Hy dari Yunani hydrargyrum untuk "perak cair". Saat ini lambangnya adalah Hg. | [nb 1] | [6] |
| I | Iridium | 77 | Saat ini lambangnya adalah Ir. Lambang I sekarang digunakan untuk iodin. | [nb 1] | |
| Ic | Incognitium | 65 | Eugène-Anatole Demarçay salah mengira jika incognitium merupakan unsur baru. Yang sebenarnya adalah terbium. | ||
| Il | Illinium | 61 | Klaim yang didiskreditkan atas penemuan prometium. | [nb 2] | [7] |
| Il | Ilmenium | 41/73 | Campuran unsur niobium dan tantalum. R. Hermann salah mengira jika ilmenium merupakan sebuah unsur. | ||
| Io | Ionium | 65 | Eugène-Anatole Demarçay salah mengira jika ionium merupakan unsur baru. Yang sebenarnya adalah terbium. | ||
| J | Jodium | 53 | Nama sebelumnya dari iodin. | [nb 1] | |
| Jg | Jargonium | 72 | Klaim yang didiskreditkan atas penemuan hafnium. | [nb 2] | [7] |
| Jl | Joliotium | 105 | Nama yang diusulkan untuk dubnium. | [nb 3] | [7] |
| Jp | Japonium | 113 | Nama yang diusulkan untuk nihonium. | [nb 3] | |
| Ka | Kalium | 19 | Saat ini lambangnya adalah K. | [nb 1] | |
| Ku | Kurchatovium | 104 | Nama yang diusulkan untuk ruterfordium. | [nb 3] | [7] |
| L | Litium | 3 | Saat ini lambangnya adalah Li. | [nb 1] | |
| Lw | Lawrensium | 103 | Saat ini lambangnya adalah Lr. | [nb 1] | |
| M | Muriatikum | 17 | Nama sebelumnya dari klorin. | [nb 1] | |
| Ma | Mangan | 25 | Saat ini lambangnya adalah Mn. | [nb 1] | |
| Ma | Masurium | 43 | Klaim yang disengketakan atas penemuan teknesium. | [nb 2] | [7] |
| Md | Mendelevium | 97 | Nama yang diusulkan untuk berkelium. Lambang dan nama ini kemudian digunakan untuk unsur 101. | [nb 1][nb 3] | |
| Ml | Moldavium | 87 | Klaim yang didiskreditkan atas penemuan fransium. | [nb 2] | [9] |
| Ms | Magnesium | 12 | Saat ini lambangnya adalah Mg. | [nb 1] | |
| Ms | Masrium | 88 | Klaim yang didiskreditkan atas penemuan radium. | [nb 2] | |
| Ms | Masurium | 43 | Klaim yang disengketakan atas penemuan teknesium. | [nb 2] | |
| Ms | Mosandrium | 65 | J. Lawrence Smith salah mengira jika mosandrium merupakan unsur baru. Yang sebenarnya adalah terbium. | ||
| Mv | Mendelevium | 101 | Saat ini lambangnya adalah Md. | [nb 1] | |
| Ng | Norwegium | 72 | Klaim yang didiskreditkan atas penemuan hafnium. | [nb 2] | |
| No | Norium | 72 | Klaim yang didiskreditkan atas penemuan hafnium. Lambang No sekarang digunakan untuk nobelium. | [nb 2] | |
| Np | Neptunium | 91 | Klaim yang didiskreditkan atas penemuan protaktinium. Lambang dan nama ini kemudian digunakan untuk unsur 93. | [nb 2] | [11] |
| Np | Nipponium | 43 | Klaim yang didiskreditkan atas penemuan teknesium. Lambang Np sekarang digunakan untuk neptunium. | [nb 2] | [7] |
| Ns | Nielsbohrium | 105 | Nama yang diusulkan untuk dubnium. | [nb 3] | [7] |
| Ns | Nielsbohrium | 107 | Nama yang diusulkan untuk bohrium. | [nb 3] | [7] |
| Nt | Niton | 86 | Nama sebelumnya dari radon. | [nb 1] | [7] |
| Ny | Neoiterbium | 70 | Nama sebelumnya dari iterbium. | [nb 1] | |
| P | Timbal | 82 | Saat ini lambangnya adalah Pb. Lambang P sekarang digunakan untuk fosforus. | [nb 1] | |
| Pa | Paladium | 46 | Saat ini lambangnya adalah Pd. Lambang Pa sekarang digunakan untuk protaktinium. | [nb 1] | |
| Pe | Pelopium | 41 | Nama sebelumnya dari niobium. | [nb 1] | |
| Ph | Fosforus | 15 | Saat ini lambangnya adalah P. | [nb 1] | |
| Pl | Paladium | 46 | Saat ini lambangnya adalah Pd. | [nb 1] | |
| Pm | Polimnestum | 33 | Alexander Pringle salah mengira jika polimnestum merupakan unsur baru. Yang sebenarnya adalah arsen. Lambang Pm sekarang digunakan untuk prometium. | ||
| Po | Kalium | 19 | Saat ini lambangnya adalah K. Lambang Po sekarang digunakan untuk polonium. | [nb 1] | |
| Pp | Filippium | 67 | Marc Delafontaine salah mengira jika filippium merupakan unsur baru. Yang sebenarnya adalah holmium. | ||
| R | Rodium | 45 | Saat ini lambangnya adalah Rh (Lambang ini sekarang kadang-kadang digunakan untuk golongan alkil). | [nb 1] | |
| Rd | Radium | 88 | Saat ini lambangnya adalah Ra. | [nb 1] | |
| Rf | Ruterfordium | 106 | Nama yang diusulkan untuk seaborgium. Lambang dan nama ini kemudian digunakan untuk unsur 104. | [nb 1][nb 3] | [7] |
| Ro | Rodium | 45 | Saat ini lambangnya adalah Rh. | [nb 1] | |
| Sa | Samarium | 62 | Saat ini lambangnya adalah Sm. | [nb 1] | [7] |
| So | Natrium | 11 | Saat ini lambangnya adalah Na. | [nb 1] | |
| Sq | Sequanium | 93 | Klaim yang didiskreditkan atas penemuan neptunium. | [nb 2] | |
| St | Antimon | 51 | Saat ini lambangnya adalah Sb. | [nb 1] | |
| St | Timah | 50 | Saat ini lambangnya adalah Sn. | [nb 1] | |
| Tm | Trimangan | 75 | Nama yang diberikan oleh Mendeleev untuk unsur yang saat itu belum ditemukan. Ketika ditemukan, renium sangat cocok dengan prediksinya. Lambang Tm sekarang digunakan untuk tulium. | [nb 3][nb 4] | |
| Tn | Wolfram | 74 | Saat ini lambangnya adalah W. | [nb 1] | |
| Tr | Terbium | 65 | Saat ini lambangnya adalah Tb. | [nb 1] | |
| Tu | Tulium | 69 | Saat ini lambangnya adalah Tm. | [nb 1] | |
| Tu | Wolfram | 74 | Saat ini lambangnya adalah W. | [nb 1] | |
| Unb | Unnilbium | 102 | Nama sementara yang diberikan untuk nobelium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Une | Unnilennium | 109 | Nama sementara yang diberikan untuk meitnerium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Unh | Unnilheksium | 106 | Nama sementara yang diberikan untuk seaborgium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uno | Unniloktium | 108 | Nama sementara yang diberikan untuk hasium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Unp | Unnilpentium | 105 | Nama sementara yang diberikan untuk dubnium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Unq | Unnilquadium | 104 | Nama sementara yang diberikan untuk ruterfordium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uns | Unnilseptium | 107 | Nama sementara yang diberikan untuk bohrium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Unt | Unniltrium | 103 | Nama sementara yang diberikan untuk lawrensium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Unu | Unnilunium | 101 | Nama sementara yang diberikan untuk mendelevium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uub | Ununbium | 112 | Nama sementara yang diberikan untuk kopernisium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uuh | Ununheksium | 116 | Nama sementara yang diberikan untuk livermorium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uun | Ununnilium | 110 | Nama sementara yang diberikan untuk darmstadtium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uuo | Ununoktium | 118 | Nama sementara yang diberikan untuk oganeson hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uup | Ununpentium | 115 | Nama sementara yang diberikan untuk moskovium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uuq | Ununquadium | 114 | Nama sementara yang diberikan untuk flerovium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uus | Ununseptium | 117 | Nama sementara yang diberikan untuk tenesin hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uut | Ununtrium | 113 | Nama sementara yang diberikan untuk nihonium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Uuu | Unununium | 111 | Nama sementara yang diberikan untuk roentgenium hingga diberi nama permanen oleh IUPAC. | [nb 4] | |
| Ur | Uralium | 75 | Klaim yang didiskreditkan atas penemuan renium. | [nb 2] | |
| Ur | Uranium | 92 | Saat ini lambangnya adalah U. | [nb 1] | |
| Vc | Viktorium | 64 | William Crookes salah mengira jika viktorium merupakan unsur baru. Yang sebenarnya adalah gadolinium. | ||
| Vi | Viktorium | 64 | William Crookes salah mengira jika viktorium merupakan unsur baru. Yang sebenarnya adalah gadolinium. | ||
| Vi | Virginium | 87 | Klaim yang didiskreditkan atas penemuan fransium. | [nb 2] | [7] |
| Vm | Virginium | 87 | Klaim yang didiskreditkan atas penemuan francium. | [nb 2] | [7] |
| Va | Vanadium | 23 | Saat ini lambangnya adalah V. | [nb 1] | |
| Wo | Wolfram | 74 | Saat ini lambangnya adalah W. | [nb 1] | |
| X | Xenon | 54 | Saat ini lambangnya adalah Xe. Lambang X sekarang digunakan untuk semua halogen. | [nb 1] | |
| Yt | Itrium | 39 | Saat ini lambangnya adalah Y. | [nb 1] | [7] |
Lambang alkimia
[sunting | sunting sumber]Lambang ideografik berikut digunakan dalam alkimia untuk melambangkan elemen yang dikenal sejak zaman kuno. Tidak termasuk dalam daftar ini adalah unsur palsu, seperti unsur klasik api dan air, dan zat yang sekarang dikenal sebagai senyawa. Banyak lagi lambang yang setidaknya digunakan secara sporadis: satu manuskrip alkimia awal abad ke-17 mencantumkan 22 lambang hanya untuk raksa saja.[12]
Nama dan lambang planet untuk logam – tujuh planet dan tujuh logam yang dikenal sejak zaman Klasik di Eropa dan Timur Tengah – ada di mana-mana dalam alkimia. Asosiasi dari apa yang anakronistik kenal sebagai logam planet mulai rusak dengan ditemukannya antimon, bismut, dan seng pada abad ke-16. Alkemis biasanya akan menyebut logam dengan nama planet mereka, misalnya "Saturnus" untuk timah dan "Mars" untuk besi; senyawa timah, besi dan perak terus disebut "jovial", "martial" dan "lunar"; atau "dari Jupiter", "dari Mars" dan "dari Bulan", selama abad ke-17. Tradisi tetap hari ini dengan nama unsur merkuri, di mana ahli kimia memutuskan nama planet lebih disukai daripada nama-nama umum seperti "quicksilver", dan dalam beberapa istilah kuno seperti lunar caustic (perak nitrat) dan saturnism (keracunan timbal).[12]
| Lambang | Unsur | Nomor atom |
Catatan | |
|---|---|---|---|---|
| 🜍 | Belerang | 16 | ||
| ♂ | Besi | 26 | logam planet untuk Mars | |
| Nikel | 28 | (varian posisi lama arsen) | ||
| ♀ | Tembaga | 29 | logam planet untuk Venus | |
| 🜺 | Arsen | 33 | ||
| ☾ | Perak | 47 | logam planet untuk Bulan | |
| 🜛 | ||||
| ♃ | Timah | 50 | logam planet untuk Jupiter | |
| ♁ | Antimon | 51 | "logam ke-8" diberi lambang Bumi, yang diakui sebagai planet pada saat itu | |
| Platina | 78 | Senyawa ☉ emas dan ☾ perak | ||
| ⛢ | lambang diciptakan untuk planet baru Uranus | |||
| ☉ | Emas | 79 | logam planet untuk Matahari | |
| 🜚 | lambang klasik | |||
| ☿ | Raksa | 80 | logam planet untuk Merkurius | |
| ♄ | Timbal | 82 | logam planet untuk Saturnus | |
| ♉︎ | Bismut | 83 | digunakan oleh Torbern Bergman (1775) | |
Lambang Dalton
[sunting | sunting sumber]
Simbol-simbol berikut digunakan oleh John Dalton pada awal 1800-an ketika tabel periodik unsur sedang dirumuskan. Tidak termasuk dalam daftar ini adalah zat yang sekarang dikenal sebagai senyawa, seperti campuran mineral tanah jarang. Notasi alfabet modern diperkenalkan pada tahun 1814 oleh Jöns Jakob Berzelius; pendahulunya dapat dilihat dalam huruf-huruf yang dilingkari Dalton untuk logam-logam tersebut, terutama dalam tabelnya yang diperbesar dari tahun 1810.[13] Jejak konvensi Dalton juga bertahan dalam model molekul bola dan tongkat, di mana bola untuk karbon berwarna hitam dan untuk oksigen berwarna merah.
| Lambang | Nama Dalton | Nama modern (dalam bahasa Indonesia) |
Nomor atom |
Catatan | Ref | |
|---|---|---|---|---|---|---|
| gmbr. | kar. | |||||
| ☉ | hydrogen | hidrogen | 1 | atau ⊙ | [14] | |
| glucine | berilium | 4 | lambang alkimia untuk 'gula' | [15] | ||
| ● | carbone | karbon | 6 | [14] | ||
| ⦶ | azote | nitrogen | 7 | lambang alkimia untuk niter | [14] | |
| ○ | oxygen | oksigen | 8 | atau ◯ | [14] | |
| ⦷ | soda | natrium | 11 | [14] | ||
| ⊛ | magnesia | magnesium | 12 | lambang alkimia untuk magnesia | [14] | |
| alumine | aluminium | 13 | (4 titik) | [14] | ||
| 🟕 | silex | silikon | 14 | [15] | ||
| phosphorus | fosforus | 15 | (3 jari-jari) | [14] | ||
| 🜨 | sulfur | belerang | 16 | [14] | ||
| potash | kalium | 19 | (3 garis vertikal) | [14] | ||
| ⦾ | lime | kalsium | 20 | atau ◎ | [14] | |
| titanium | 22 | (lingkaran penutup) Tit⃝ | [15] | |||
| manganese | mangan | 25 | (lingkaran penutup) Ma⃝ | [15] | ||
| Ⓘ | iron | besi | 26 | [14] | ||
| Ⓝ | nickel | nikel | 28 | [14] | ||
| cobalt | kobalt | 27 | (lingkaran penutup) Cob⃝ | [15] | ||
| Ⓒ | copper | tembaga | 29 | (huruf hitam dalam lingkaran merah) | [14] | |
| Ⓩ | zinc | seng | 30 | [14] | ||
| arsenic | arsen | 33 | (lingkaran penutup) Ar⃝ | [15] | ||
| strontian | stronsium | 38 | (4 garis pendek) | [14] | ||
| ⊕︀︀ | yttria | itrium | 39 | (tanda plus tidak menyentuh lingkaran) | [15] | |
| zircone | zirkonium | 40 | (zig-zag vertical) | [15] | ||
| Ⓢ | silver | perak | 47 | [14] | ||
| Ⓣ | tin | timah | 50 | [15] | ||
| antimony | antimon | 51 | (lingkaran penutup) An⃝ | [15] | ||
| barytes | barium | 56 | (6 garis pendek) | [14] | ||
| cerium | serium | 58 | (lingkaran penutup) Ce⃝ | [15] | ||
| tungsten | wolfram | 74 | (lingkaran penutup) Tu⃝ | [15] | ||
| Ⓟ | platina | 78 | (huruf hitam dalam lingkaran merah) | [14] | ||
| Ⓖ | gold | emas | 79 | [14] | ||
| mercury | raksa | 80 | (titik-titik dalam lingkaran) | [14] | ||
| Ⓛ | lead | timbal | 82 | [14] | ||
| Ⓑ | bismuth | bismut | 83 | [15] | ||
| Ⓤ | uranium | 92 | [15] | |||
Lambang untuk isotop bernama
[sunting | sunting sumber]Berikut ini adalah daftar isotop unsur yang diberikan dalam tabel sebelumnya yang telah ditetapkan sebagai lambang unik. Dengan ini berarti bahwa daftar lengkap lambang sistematis saat ini (dalam bentuk uAtom) tidak termasuk dalam daftar dan sebaliknya dapat ditemukan di grafik indeks Isotop. Lambang untuk nama isotop hidrogen, deuterium (D), dan tritium (T) masih digunakan sampai sekarang, seperti halnya toron (Tn) untuk radon-220 (meskipun bukan aktinon; An biasanya digunakan sebagai pengganti aktinida umum). Air berat dan pelarut terdeuterasi lainnya biasanya digunakan dalam kimia, dan lebih mudah menggunakan satu karakter daripada lambang dengan subskrip dalam kasus ini. Praktek juga berlanjut dengan senyawa tritium. Ketika nama pelarut diberikan, huruf kecil d kadang-kadang digunakan. Misalnya, d6-benzena dan C6D6 dapat digunakan sebagai pengganti C6[2H6].[16]
Lambang untuk isotop unsur selain hidrogen dan radon tidak lagi digunakan dalam komunitas ilmiah. Banyak dari simbol-simbol ini ditunjuk selama tahun-tahun awal radiokimia, dan beberapa isotop (yaitu yang ada dalam rantai peluruhan aktinium, radium, dan torium) menyandang nama placeholder menggunakan sistem penamaan awal yang dirancang oleh Ernest Rutherford.[17]
| Lambang | Nama | Nomor atom |
Asal lambang |
|---|---|---|---|
| Ac | Aktinium | 89 | Dari Yunani aktinos. Nama dibatasi pada satu waktu menjadi 227Ac, sebuah isotop aktinium. Isotop bernama ini kemudian menjadi nama resmi untuk unsur 89. |
| AcA | Aktinium A | 84 | Dari aktinium dan A. Nama placeholder diberikan pada satu waktu menjadi 215Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcB | Aktinium B | 82 | Dari aktinium dan B. Nama placeholder diberikan pada satu waktu menjadi 211Pb, sebuah isotop timbal yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcC | Aktinium C | 83 | Dari aktinium dan C. Nama placeholder diberikan pada satu waktu menjadi 211Bi, sebuah isotop bismut yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcC' | Aktinium C' | 84 | Dari aktinium dan C'. Nama placeholder diberikan pada satu waktu menjadi 211Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcC" | Aktinium C" | 81 | Dari aktinium dan C". Nama placeholder diberikan pada satu waktu menjadi 207Tl, sebuah isotop talium yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcK | Aktinium K | 87 | Nama diberikan pada satu waktu menjadi 223Fr, sebuah isotop fransium yang teridentifikasi dalam rantai peluruhan aktinium. |
| AcU | Aktino-uranium | 92 | Nama diberikan pada satu waktu menjadi 235U, sebuah isotop uranium. |
| AcX | Aktinium X | 88 | Nama diberikan pada satu waktu menjadi 223Ra, sebuah isotop radium yang teridentifikasi dalam rantai peluruhan aktinium. |
| An | Aktinon | 86 | Dari aktinium dan emanation. Nama diberikan pada satu waktu menjadi 219Rn, sebuah isotop radon yang teridentifikasi dalam rantai peluruhan aktinium. |
| D | Deuterium | 1 | Dari Yunani deuteros. Nama diberikan menjadi 2H. |
| Io | Ionium | 90 | Nama diberikan menjadi 230Th, sebuah isotop torium yang teridentifikasi dalam rantai peluruhan uranium. |
| MsTh1 | Mesotorium 1 | 88 | Nama diberikan pada satu waktu menjadi 228Ra, sebuah isotop radium. |
| MsTh2 | Mesotorium 2 | 89 | Nama diberikan pada satu waktu menjadi 228Ac, sebuah isotop aktinium. |
| Pa | Protaktinium | 91 | Dari Yunani protos dan aktinium. Nama dibatasi pada satu waktu menjadi 231Pa, sebuah isotop protaktinium. Isotop bernama ini kemudian menjadi nama resmi untuk unsur 91. |
| Ra | Radium | 88 | Dari Latin radius. Nama dibatasi pada satu waktu menjadi 226Ra, sebuah isotop radium. Isotop bernama ini kemudian menjadi nama resmi untuk unsur 88. |
| RaA | Radium A | 84 | Dari radium dan A. Nama placeholder diberikan pada satu waktu menjadi 218Po, sebuah isotop torium yang teridentifikasi dalam rantai peluruhan radium. |
| RaB | Radium B | 82 | Dari radium dan B. Nama placeholder diberikan pada satu waktu menjadi 214Pb, sebuah isotop timbal yang teridentifikasi dalam rantai peluruhan radium. |
| RaC | Radium C | 83 | Dari radium dan C. Nama placeholder diberikan pada satu waktu menjadi 214Bi, sebuah isotop bismut yang teridentifikasi dalam rantai peluruhan radium. |
| RaC' | Radium C' | 84 | Dari radium dan C'. Nama placeholder diberikan pada satu waktu menjadi 214Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan radium. |
| RaC" | Radium C" | 81 | Dari radium dan C". Nama placeholder diberikan pada satu waktu menjadi 210Tl, sebuah isotop talium yang teridentifikasi dalam rantai peluruhan radium. |
| RaD | Radium D | 82 | Dari radium dan D. Nama placeholder diberikan pada satu waktu menjadi 210Pb, sebuah isotop timbal yang teridentifikasi dalam rantai peluruhan radium. |
| RaE | Radium E | 83 | Dari radium dan E. Nama placeholder diberikan pada satu waktu menjadi 210Bi, sebuah isotop bismut yang teridentifikasi dalam rantai peluruhan radium. |
| RaE" | Radium E" | 81 | Dari radium dan E". Nama placeholder diberikan pada satu waktu menjadi 206Tl, sebuah isotop talium yang teridentifikasi dalam rantai peluruhan radium. |
| RaF | Radium F | 84 | Dari radium dan F. Nama placeholder diberikan pada satu waktu menjadi 210Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan radium. |
| RdAc | Radioaktinium | 90 | Nama diberikan pada satu waktu menjadi 227Th, sebuah isotop torium. |
| RdTh | Radiotorium | 90 | Nama diberikan pada satu waktu menjadi 228Th, sebuah isotop torium. |
| Rn | Radon | 86 | Dari radium dan emanation. Nama dibatasi pada satu waktu menjadi 222Rn, sebuah isotop radon yang teridentifikasi dalam rantai peluruhan uranium. Isotop bernama ini kemudian menjadi nama resmi untuk unsur 86 pada 1923. |
| T | Tritium | 1 | Dari Yunani tritos. Nama diberikan menjadi 3H. |
| Th | Torium | 90 | Dari kata Thor. Nama dibatasi pada satu waktu menjadi 232Th, sebuah isotop torium yang teridentifikasi dalam rantai peluruhan uranium. Isotop bernama ini kemudian menjadi nama resmi untuk unsur 90. |
| ThA | Torium A | 84 | Dari torium dan A. Nama placeholder diberikan pada satu waktu menjadi 216Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan torium. |
| ThB | Torium B | 82 | Dari torium dan B. Nama placeholder diberikan pada satu waktu menjadi 212Pb, sebuah isotop timbal yang teridentifikasi dalam rantai peluruhan torium. |
| ThC | Torium C | 83 | Dari torium dan C. Nama placeholder diberikan pada satu waktu menjadi 212Bi, sebuah isotop bismut yang teridentifikasi dalam rantai peluruhan torium. |
| ThC' | Torium C' | 84 | Dari torium dan C'. Nama placeholder diberikan pada satu waktu menjadi 212Po, sebuah isotop polonium yang teridentifikasi dalam rantai peluruhan torium. |
| ThC" | Thorium C" | 81 | Dari torium dan C". Nama placeholder diberikan pada satu waktu menjadi 208Tl, sebuah isotop talium yang teridentifikasi dalam rantai peluruhan torium. |
| ThX | Torium X | 88 | Nama diberikan pada satu waktu menjadi 224Ra, sebuah isotop radium yang teridentifikasi dalam rantai peluruhan torium. |
| Tn | Toron | 86 | Dari torium dan emanation. Nama diberikan pada satu waktu menjadi 220Rn, sebuah isotop radon yang teridentifikasi dalam rantai peluruhan torium. |
| UI | Uranium I | 92 | Nama diberikan pada satu waktu menjadi 238U, sebuah isotop uranium. |
| UII | Uranium II | 92 | Nama diberikan pada satu waktu menjadi 234U, sebuah isotop uranium. |
| UX1 | Uranium X1 | 90 | Nama diberikan pada satu waktu menjadi 234Th, sebuah isotop torium yang teridentifikasi dalam rantai peluruhan uranium. |
| UX2 | Uranium X2 | 91 | Nama diberikan pada satu waktu menjadi 234mPa, sebuah isotop protaktinium yang teridentifikasi dalam rantai peluruhan uranium. |
| UY | Uranium Y | 90 | Nama diberikan pada satu waktu menjadi 231Th, sebuah isotop torium yang teridentifikasi dalam rantai peluruhan uranium. |
| UZ | Uranium Z | 91 | Nama diberikan pada satu waktu menjadi 234Pa, sebuah isotop protaktinium yang teridentifikasi dalam rantai peluruhan uranium. |
Lambang lainnya
[sunting | sunting sumber]Umum:
- A: asam terdeprotonasi atau anion
- An: aktinida apa saja
- B: basa, sering dalam konteks teori asam-basa Lewis atau teori asam-basa Brønsted–Lowry
- E: unsur atau elektrofil apa saja
- L: ligan apa saja
- Ln: lantanida apa saja
- M: logam apa saja
- Mm: mischmetal (kadang-kadang digunakan)[18]
- Ng: gas mulia apa saja (Rg kadang-kadang digunakan, tetapi lambang Rg digunakan untuk unsur roentgenium)
- Nu: nukleofil apa saja
- R: radikal (moitas) apa saja yang tidak penting dalam pembahasan
- St: baja (kadang-kadang digunakan)
- X: halogen apa saja (atau terkadang pseudohalogen)
Dari kimia organik:
- Ac: asetil–(juga digunakan untuk unsur aktinium)
- Ad: 1-adamantil
- All: alil
- Am: amil (pentil)–(juga digunakan untuk unsur amerisium)
- Ar: aril–(juga digunakan untuk unsur argon)
- Bn: benzil
- Bs: brosil atau benzenasulfonil (kedaluwarsa)
- Bu: butil (awalan i-, s-, or t- dapat digunakan untuk menunjukkan iso-, sec-, atau tert-isomer)
- Bz: benzoil
- Cp: cyclopentadienil
- Cp*: pentametilcyclopentadienil
- Cy: cycloheksil
- Cyp: cyclopentil
- Et: etil
- Me: metil
- Mes: mesitil (2,4,6-trimetilfenil)
- Ms: mesil (metilsulfonil)
- Np: neopentil–(juga digunakan untuk unsur neptunium)
- Ns: nosil
- Pent: pentil
- Ph, Φ: fenil
- Pr: propil–(awalan i- dapat digunakan untuk menunjukkan isopropil. Juga digunakan untuk unsur praseodimium)
- R: dalam konteks kimia organik, "R" yang tidak ditentukan sering dipahami sebagai gugus alkil
- Tf: triflil (trifluorometaneulfonil)
- Tr, Trt: tritil (trifenilmetil)
- Ts, Tos: tosil (para-toluensulfonil)–(Ts juga digunakan untuk unsur tenesin)
- Vi: vinil
- Mu: muonium
- Pn: protonium
- Ps: positronium
Lihat pula
[sunting | sunting sumber]- Unsur kimia
- Daftar unsur kimia
- Daftar unsur kimia menurut nama
- Daftar unsur kimia menurut nomor atom
- Nomor atom
- Notasi nuklir
- Perang Transfermium
Catatan
[sunting | sunting sumber]- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb Nama diubah karena standarisasi, modernisasi, atau pembaruan pada lambang lama yang digunakan sebelumnya.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae Nama yang ditunjuk oleh pengklaim yang didiskreditkan/disengketakan.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y Nama yang diusulkan sebelum penemuan/pembuatan unsur atau sebelum penggantian nama resmi dari nama placeholder.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa Nama placeholder sementara.
Referensi
[sunting | sunting sumber]- ^ IUPAC Provisional Recommendations: IR-3: Elements and Groups of Elements (PDF) (Laporan). IUPAC. Maret 2004.
- ^ "Periodic Table–Royal Society of Chemistry". www.rsc.org (dalam bahasa Inggris).
- ^ "Online Etymology Dictionary". etymonline.com (dalam bahasa Inggris).
- ^ Wieser, Michael E.; et al. (2013). Atomic weights of the elements 2011 (IUPAC Technical Report). Pure Appl. Chem. (Laporan). 85. hlm. 1047–1078. doi:10.1351/PAC-REP-13-03-02
 . (untuk berat atom standar unsur)
. (untuk berat atom standar unsur)
- ^ Sonzogni, Alejandro. "Interactive Chart of Nuclides". National Nuclear Data Center: Brookhaven National Laboratory. Diakses tanggal 13 Juni 2022. (untuk berat atom unsur dengan nomor atom 103–118)
- ^ a b Holden, N. E. (12 Maret 2004). "History of the Origin of the Chemical Elements and Their Discoverers". National Nuclear Data Center.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad Leal, João P. (2013). "The Forgotten Names of Chemical Elements". Foundations of Science. 19 (2): 175–183. doi:10.1007/s10699-013-9326-y.
- ^ a b "Fred Allison". Encyclopedia of Alabama.
- ^ a b c d e f g Fontani, Marco; Costa, Mariagrazia; Orna, Mary Virginia (2014). The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. ISBN 9780199383344.
- ^ a b Praseodymium Diarsipkan 2018-10-08 di Wayback Machine. di was.chemistryexplained.com.
- ^ Rang, F. (1895). "The Period-Table". The Chemical News and Journal of Physical Science. 72: 200–201.
- ^ a b Maurice Crosland (2004) Historical Studies in the Language of Chemistry
- ^ Berzelius, Jöns Jakob. "Essay on the Cause of Chemical Proportions, and on Some Circumstances Relating to Them: Together with a Short and Easy Method of Expressing Them." Annals of Philosophy 2, Pp.443–454 (1813); 3, Pp.51–52, 93–106, 244–255, 353–364 (1814); (Selanjutnya diterbitkan ulang dalam "A Source Book in Chemistry, 1400-1900", eds. Leicester, Henry M. & Herbert S. Klickstein. 1952.)
- ^ a b c d e f g h i j k l m n o p q r s t u v Dalton, John (1808). "III: On Chemical Synthesis - Section 1: Explanation of the Plates - Plate 4: Elements". A New System of Chemical Philosophy. Part I. Manchester: Printed by S. Russell for R. Bickerstaff, Strand, London. hlm. 217-220.
- ^ a b c d e f g h i j k l m n Dalton, John (1810). "V: Compounds of two Elements - Section 12: Earths - Explanation of Plates - Plate 5: Elements". A New System of Chemical Philosophy. Part II. Manchester: Printed by Russell & Allen for R. Bickerstaff, Strand, London. hlm. 546–548.
- ^ IUPAC. "Isotopically Modified Compounds". IUPAC. Diakses tanggal 14 Juni 2022.
- ^ Morgan, G. T., ed. (1905). "Annual Reports on the Progress of Chemistry for 1904". Journal of the Chemical Society. Gurney & Jackson. 1: 268.
Mengingat sifat yang luar biasa kompleks dari perubahan selanjutnya yang terjadi pada Radium, Rutherford telah mengusulkan sistem nomenklatur yang baru dan nyaman. Produk pertama dari perubahan emanasi radium diberi nama radium A, berikutnya radium B, dan seterusnya.
- ^ Jurczyk, M.; Rajewski, W.; Majchrzycki, W.; Wójcik, G. (1999-08-30). "Mechanically alloyed MmNi5-type materials for metal hydride electrodes". Journal of Alloys and Compounds. 290 (1–2): 262–266. doi:10.1016/S0925-8388(99)00202-9.
- Elementymology & Elements Multidict, etimologi nama unsur. Diakses tanggal 14 Juni 2022.
- Massa Atom Unsur 2001, Pure Appl. Chem. 75(8), 1107–1122, 2003. Diakses tanggal 14 Juni 2022. Massa atom unsur dengan nomor atom 1-109 diambil dari sumber ini.
- Massa Atom Standar IUPAC, Direvisi Diarsipkan 2008-03-05 di Wayback Machine. (2005).
- WebElements Periodic Table. Diakses tanggal 14 Juni 2022. Massa atom unsur dengan nomor atom 110-116 diambil dari sumber ini.
- Leighton, Robert B. Principles of Modern Physics. New York: McGraw-Hill. 1959.
- Scerri, E.R. "The Periodic Table, Its Story and Its Significance". New York, Oxford University Press. 2007.
