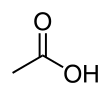
Asam asetat
| |||
| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC | |||
| Nama IUPAC (sistematis)
Asam etanoat[5] | |||
| Nama lain | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| Singkatan | AcOH | ||
| Referensi Beilstein | 506007 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| Nomor EC | |||
| Referensi Gmelin | 1380 | ||
| KEGG | |||
| MeSH | Acetic+acid | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 2789 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C2H4O2 | |||
| Massa molar | 60,05 g·mol−1 | ||
| Penampilan | Cairan tak berwarna atau kristal | ||
| Bau | Menyengat/Seperti cuka | ||
| Densitas | 1,049 g cm−3 | ||
| Titik lebur | 289 sampai 290 K | ||
| Titik didih | 391 sampai 392 K | ||
| Dapat campur | |||
| log P | -0,322 | ||
| Tekanan uap | 1,5 kPa (20 °C)[6] | ||
| Keasaman (pKa) | 4,76[7] | ||
| Kebasaan (pKb) | 9,24 (kebasaan ion asetat) | ||
| Indeks bias (nD) | 1,371 | ||
| Viskositas | 1,22 mPa s | ||
| 1,74 D | |||
| Termokimia | |||
| Kapasitas kalor (C) | 123,1 J·K−1·mol−1 | ||
| Entropi molar standar (S |
158,0 J·K−1·mol−1 | ||
| Entalpi pembentukan standar (ΔfH |
-483,88--483,16 kJ·mol−1 | ||
| Entalpi pembakaran standar ΔcH |
-875,50--874.82 kJ·mol−1 | ||
| Bahaya | |||
| Piktogram GHS |  
| ||
| Keterangan bahaya GHS | {{{value}}} | ||
| H226, H314 | |||
| P280, P305+351+338, P310 | |||
| Titik nyala | 39 °C (closed cup)[6] | ||
| 485 °C[6] | |||
| Ambang ledakan | 4-16% | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (dosis median)
|
3,31 g·kg−1, oral (mencit) | ||
LC50 (konsentrasi median)
|
5.620 ppm (tikus, 1 jam) 16.000 ppm (tikus, 4 hr)[9] | ||
| Batas imbas kesehatan AS (NIOSH): | |||
PEL (yang diperbolehkan)
|
TWA 10 ppm (25 mg/m3)[8] | ||
REL (yang direkomendasikan)
|
TWA 10 ppm (25 mg/m3) ST 15 ppm (37 mg/m3)[8] | ||
IDLH (langsung berbahaya)
|
50 ppm[8] | ||
| Senyawa terkait | |||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Asam asetat atau asam cuka (Inggris: ethanoic acid) adalah salah satu senyawa organik yang berada dalam golongan asam alkanoat.[10] Asam asetat pekat (disebut asam asetat glasial) adalah cairan higroskopis tak berwarna, dan memiliki titik beku 16,7°C. Asam asetat adalah komponen utama cuka (3–9%) selain air. Asam asetat berasa asam dan berbau menyengat. Selain diproduksi untuk cuka konsumsi rumah tangga, asam asetat juga diproduksi sebagai prekursor untuk senyawa lain seperti polivinil asetat dan selulosa asetat. Meskipun digolongkan sebagai asam lemah, asam asetat pekat bersifat korosif dan dapat menyebabkan iritasi pada kulit.
Asam asetat merupakan salah satu asam karboksilat paling sederhana, setelah asam format. Larutan asam asetat dalam air merupakan sebuah asam lemah, artinya hanya terdisosiasi sebagian menjadi ion H+ dan CH–. Asam asetat merupakan pereaksi kimia dan bahan baku industri yang penting. Asam asetat digunakan dalam produksi polimer seperti polietilena tereftalat, selulosa asetat, dan polivinil asetat, maupun berbagai macam serat dan kain. Dalam industri makanan, asam asetat, dengan kode aditif makanan E260, digunakan sebagai pengatur keasaman. Di rumah tangga, asam asetat encer juga sering digunakan sebagai pelunak air. Sebagai aditif makanan, asam asetat disetujui penggunaannya di banyak negara, termasuk Kanada,[11] Uni Eropa,[12] Amerika Serikat,[13] Australia dan Selandia Baru.[14]
Dalam setahun, kebutuhan dunia akan asam asetat mencapai 6,5 juta ton per tahun. 1,5 juta ton per tahun diperoleh dari hasil daur ulang, sisanya diperoleh dari industri petrokimia, terutama dengan bahan baku metanol.[15] Cuka adalah asam asetat encer, sering kali diproduksi melalui fermentasi dan oksidasi lanjutan etanol.
Tata nama[sunting | sunting sumber]
Asam asetat merupakan nama trivial dari senyawa ini atau nama yang dianjurkan IUPAC yang berasal dari kata dalam bahasa Latin: acetum, yang berarti cuka.[16] Akan tetapi, dalam penggunaan untuk tata nama IUPAC secara umum, senyawa ini memiliki nama asam etanoat.[17] Asam asetat glasial merupakan nama trivial yang merujuk pada asam asetat yang tidak memiliki kandungan air (anhidrat). Penamaan ini disebabkan oleh sifat asam asetat anhidrat yang membentuk kristal mirip es pada suhu 16,6 °C (61,9 °F) yang merupakan suhu sedikit di bawah suhu ruang.[18]
Singkatan nama senyawa yang paling sering digunakan dan menjadi singkatan resmi bagi asam asetat adalah AcOH atau HOAc. Ac mempresentasikan gugus asetil, (CH3–C(=O)–), sedangkan asetat (CH) yang berfungsi sebagai basa konjungat disingkat sebagai AcO−. Ac jangan disalahartikan dengan lambang unsur aktinium (Ac).[19] Untuk mendapatkan gambaran struktur yang lebih baik, asam asetat sering kali ditulis sebagai CH3–C(O)OH, CH3–C(=O)OH, CH, dan CH. Dalam konteks reaksi asam-basa, singkatan HAc sering digunakan untuk simbol asam basa, dengan Ac merupakan singkatan dari asetat.[20] Asetat adalah ion yang dihasilkan dari lepasnya H+ dari asam asetat.[21] Nama asetat dapat pula merujuk pada garam dan ester yang dihasilkan dari interaksi asam asetat dengan senyawa lain.[22]
Sejarah[sunting | sunting sumber]

Cuka merupakan jenis asam asetat yang telah dikenal manusia sejak dahulu kala dan pertama kali ditemukan pada 5000 SM saat seorang pelayan istana dari Babilonia menemukan anggur berubah menjadi minuman anggur ketika dibiarkan di ruang terbuka .[23] Penggunaan cuka dilakukan pertama kali untuk alkimia pada abad ke-3 Sebelum Masehi. Saat itu, Filsuf Yunani Kuno Theophrastus menjelaskan bahwa cuka bereaksi dengan logam-logam dan membentuk berbagai pigmen, misalnya timbal putih (timbal karbonat), dan verdigris, yaitu zat warna hijau yang merupakan campuran garam-garam tembaga, seperti tembaga (II) asetat.[24] Bangsa Romawi Kuno menghasilkan sapa, sebuah sirup yang sangat manis, dengan mendidihkan anggur yang sudah diasamkan. Sapa yang direbus di sebuah panci berbahan timbal memiliki kandungan timbal(II) asetat yang tinggi. Sapa yang merupakan suatu zat manis disebut juga dengan nama gula timbal atau garam Saturnus. Konsumsi terhadap zat ini menyebabkan keracunan timbal yang terjadi pada kaum bangsawan Romawi Kuno.[25]
Pada tahun 750 M, ilmuwan Persia Jabir ibn Hayyan merupakan ilmuwan pertama yang bisa menghasilkan asam asetat dari proses distilasi pada cuka.[26] Pada masa renaisans, asam asetat glasial dihasilkan dari distilasi kering tembaga asetat atau logam berat sejenis. Pada abad ke-16 ahli alkimia Jerman Andreas Libavius menjelaskan prosedur tersebut, dan membandingkan asam asetat glasial yang dihasilkan terhadap cuka. Ternyata asam asetat glasial memiliki banyak perbedaan sifat dengan larutan asam asetat dalam air sehingga kimiawan, seperti Antoine Lavoisier mencoba untuk membedakan kedua zat tersebut, tetapi tidak berhasil. Akhirnya, kimiawan Prancis Pierre Adet membuktikan bahwa kedua zat ini sebenarnya sama dan asam asetat glasial merupakan bentuk monohidrat dari senyawa asam asetat.[27]
Pada 1847, kimiawan Jerman Hermann Kolbe berhasil mensintesis asam asetat dari zat anorganik untuk pertama kalinya. Reaksi kimia yang dilakukan adalah klorinasi karbon disulfida menjadi karbon tetraklorida, diikuti dengan pirolisis menjadi tetrakloroetilena dan klorinasi dalam air menjadi asam trikloroasetat, dan akhirnya reduksi elektrolisis menjadi asam asetat.[28]
Sejak 1910 kebanyakan asam asetat glasial dihasilkan dari cuka kayu yang diperoleh dari distilasi kayu. Cairan ini direaksikan dengan kalsium hidroksida dan menghasilkan kalsium asetat yang kemudian diasamkan dengan asam sulfat untuk menghasilkan asam asetat. Pada saat itu, Jerman memproduksi 10.000 ton asam asetat glasial, sekitar 30% dari yang digunakan untuk produksi zat warna indigo.[29][30]
Karena metanol dan karbon monoksida merupakan bahan baku yang diperdagangkan secara umum, teknik karbonilasi metanol cukup lama menjadi prekursor yang menarik untuk memproduksi asam asetat. Pada awal tahun 1925, Henry Dreyfus mengembangkan rencara pabrik rintisan menggunakan teknik karbonilasi metanol di perusahaan British Celanese. Namun, kurangnya bahan logam yang berfungsi sebagai wadah campuran reaksi korosif ini menyebabkan komersialisasi teknik produksi proses ini tertunda.[31] Proses karbonilasi metanol komersial pertama, menggunakan kobalt sebagai katalis. Teknik ini dikembangkan oleh perusahaan kimia Jerman BASF, pada tahun 1963. Pada tahun 1968, katalis berbasis rodium (cis−[Rh(CO)2I2]−) ditemukan yang dapat beroperasi secara efisien pada tekanan rendah dengan hampir tanpa produk sampingan. Perusahaan kimia Amerika Serikat Monsanto Company membangun pabrik pertamanya menggunakan katalis ini pada tahun 1970, dan karbonilasi metanol dengan katalis rodium menjadi metode dominan pada produksi asam asetat (lihat proses Monsanto).[32] Pada tahun 1990-an, perusahaan kimia BP Chemicals mengembangkan teknik menggunakan katalisator ([Ir(CO)2I2]−) yang mengandung iridium sebagai promotor. Teknik ini diberi nama Cativa , untuk efisiensi yang lebih besar dan mengomersialkannya pada tahun 1995.[33] Proses Cativa berkatalis iridium dinilai lebih ramah lingkungan dan lebih efisien sehingga menggantikan proses Monsato.[34]
Sifat-sifat kimia[sunting | sunting sumber]
Keasaman[sunting | sunting sumber]
Atom hidrogen (H) yang menjadi pusat pada gugus karboksil (−COOH) dalam asam karboksilat seperti asam asetat dapat dilepaskan sebagai ion H+ (proton), melalui proses ionisasi sebagai berikut:
Karena ion H+ yang telah dilepaskan hanya satu , maka asam asetat merupakan asam lemah monoprotik yang bila berada dalam larutan air memiliki nilai pKa=4,76.[35][36] Basa konjugasinya adalah asetat (CH3COO−). Basa konjugatnya adalah asetat (CH3COO−). 1 M asam asetat (kira-kira sama dengan konsentrasi pada cuka rumah) memiliki pH sekitar 2.4 yang menandakan bahwa hanya sekitar 0.4% molekul asam asetat saja yang terdisosiasi.[n 1]
Struktur[sunting | sunting sumber]
Asam asetat dalam bentuk padat menunjukkan bahwa molekul-molekul pada asam asetat membentuk rantai yang disatukan oleh ikatan hidrogen.[37] Pada saat asam asetat berada dalam bentuk gas, senyawa ini diketahui terdiri dari dimer siklik yang mengikat dua atom hidrogen.[38] Bentuk dimer ini juga dapat dideteksi hanya ketika dilarutkan oleh pelarut yang tidak memiliki ikatan hidrogen dalam konsentrasi yang kecil.[39] Karena keberadaan dimer dapat dideteksi ketika dilarutkan dalam pelarut berikatan hidrogen (misalnya air).[40] Entalpi disosiasi standar dimer tersebut diperkirakan 65,0–66,0 kJ/mol, entropi disosiasi sekitar 154–157 J mol−1 K−1.[41] Sifat dimerisasi ini juga dimiliki oleh asam karboksilat sederhana lainnya.[42]

Sifat pelarut[sunting | sunting sumber]
Asam asetat merupakan pelarut protik hidrofilik (polar) seperti air dan etanol. Asam asetat memiliki konstanta dielektrik yang sedang yaitu 6,2 sehingga ia bisa melarutkan baik senyawa polar seperti garam anorganik dan gula maupun senyawa non-polar seperti minyak dan unsur-unsur seperti sulfur dan iodin. Asam asetat bercampur dengan mudah dengan pelarut polar atau nonpolar lainnya seperti air, kloroform dan heksana. Ketika larut dalam senyawa alkana yang lebih tinggi (dimulai dari oktana), asam asetat tidak lagi bercampur sempurna dan kebercampurannya terus menurun berbanding lurus dengan panjang rantai n-alkana.[43] Sifat kelarutan dan ketercampuran dari asam asetat ini membuatnya digunakan secara luas dalam industri kimia, misalnya sebagai pelarut dalam produksi dimetil tereftalat dan asam tereftalat.[44]
Reaksi kimia[sunting | sunting sumber]
Reaksi dengan senyawa anorganik[sunting | sunting sumber]
Asam asetat bersifat korosif terhadap banyak logam seperti besi, magnesium, dan seng, membentuk gas hidrogen dan garam-garam asetat (disebut logam asetat). Logam asetat juga dapat diperoleh dengan reaksi asam asetat dengan suatu basa yang cocok. Contoh yang terkenal adalah reaksi soda kue (Natrium bikarbonat) bereaksi dengan cuka. Hampir semua garam asetat larut dengan baik dalam air. Salah satu pengecualian adalah kromium (II) asetat. Contoh reaksi pembentukan garam asetat:
Karena aluminium membentuk suatu film aluminium oksida yang tahan asam sehingga melindungi permukaannya, tangki aluminium digunakan untuk menampung dan mengangkut asam asetat. Asetat logam dapat juga diperoleh dari asam asetat dan basa yang sesuai, seperti dalam reaksi populer "baking soda + cuka":
Kimia organik[sunting | sunting sumber]

Asam asetat mengalami reaksi-reaksi asam karboksilat, misalnya menghasilkan garam asetat bila bereaksi dengan alkali, menghasilkan logam etanoat bila bereaksi dengan logam, dan menghasilkan logam etanoat, air dan karbondioksida bila bereaksi dengan garam karbonat atau bikarbonat. Dengan basa kuat (misalnya pereaksi organolitium), asam asetat mengalami deprotonasi menghasilkan LiCH2CO2Li. Reaksi organik yang paling terkenal dari asam asetat adalah pembentukan etanol melalui reduksi, pembentukan turunan asam karboksilat seperti asetil klorida atau anhidrida asetat melalui substitusi nukleofilik. Anhidrida asetat dibentuk melalui kondensasi dua molekul asam asetat. Ester dari asam asetat dapat diperoleh melalui reaksi esterifikasi Fischer, dan juga pembentukan amida. Pada suhu 440 °C, asam asetat terurai menjadi metana dan karbon dioksida, atau ketena dan air.
Deteksi[sunting | sunting sumber]
Asam asetat dapat dikenali dengan baunya yang khas. Selain itu, garam-garam dari asam asetat bereaksi dengan larutan besi(III) klorida, yang menghasilkan warna merah pekat yang hilang bila larutan diasamkan.[45] Garam-garam asetat bila dipanaskan dengan arsenik trioksida (AsO3) membentuk kakodil oksida ((CH3)2As-O-As(CH3)2), yang mudah dikenali dengan bau uapnya yang tidak menyenangkan.[46]
Turunan lain[sunting | sunting sumber]
Garam organik atau anorganik yang dihasilkan dari asam asetat antara lain:
- Natrium asetat, digunakan dalam industri tekstil dan sebagai pengawet makanan (E262).
- Tembaga(II) asetat, digunakan sebagai pigmen dan fungisida.
- Aluminium asetat dan besi(II) asetat—sebagai mordan untuk pewarna.
- Paladium(II) asetat, digunakan sebagai katalis untuk reaksi penjodohan organik seperti reaksi Heck.
- Perak asetat, digunakan sebagai pestisida.
Produk-produk asam asetat tersubstitusi mencakup:
- Asam kloroasetat (monochloroacetic acid, MCA), asam dikloroasetat (ditengarai sebagai produk sampingan), dan asam trikloroasetat. MCA digunakan dalam fabrikasi pewarna indigo.
- Asam bromoasetat, yang jika diesterifikasi menghasilkan pereaksi etil bromoasetat.
- Asam trifluoroasetat, merupakan pereaksi umum dalam sintesis organik.
Jumlah asam asetat yang digunakan dalam aplikasi lain ini (tidak termasuk TPA) meliputi 5–10% dari penggunaan asam asetat dunia. Namun aplikasi-aplikasi ini diperkirakan tidak tumbuh sepesat produksi TPA.[47]
Biokimia[sunting | sunting sumber]
Pada pH fisiologis, asam asetat biasanya terionisasi sempurna membentuk asetat. Gugus asetil yang terdapat pada asam asetat merupakan gugus yang penting bagi reaksi biokimia pada hampir seluruh makhluk hidup, seperti gugus asetil yang berikatan pada koenzim A menjadi senyawa yang disebut Asetil-KoA,. Senyawa ini merupakan koenzim penting bagi metabolisme karbohidrat dan lemak. Namun, asam asetat bebas memiliki konsentrasi yang kecil dalam sel, karena asam asetat bebas dapat menyebabkan gangguan pada mekanisme pengaturan pH sel. Berbeda dengan asam karboksilat berantai panjang lainnya (asam lemak), asam asetat tidak ditemukan pada trigliserida dalam tubuh makhluk hidup. Sekalipun demikian, trigliserida buatan yang memiliki gugus asetat, triasetin (trigliserin asetat), adalah zat aditif yang umum pada makanan, dan juga digunakan dalam kosmetika dan obat-obatan.[48]
Asam asetat diproduksi dan diekskresikan oleh bakteri-bakteri tertentu, misalnya dari genus Acetobacter dan spesies Clostridium acetobutylicum. Bakteri-bakteri ini terdapat pada makanan, air, dan juga tanah, sehingga asam asetat secara alami diproduksi pada buah-buahan/makanan yang telah basi. Asam asetat juga terdapat pelumas vagina manusia dan primata lainnya, berperan sebagai agen anti-bakteri.[49]
Biosintesis asam asetat[sunting | sunting sumber]
Asam asetat merupakan produk katabolisme aerob dalam jalur glikolisis atau perombakan glukosa. Asam piruvat sebagai produk oksidasi glukosa dioksidasi oleh NAD+ terion lalu segera diikat oleh Koenzim-A. Pada prokariota proses ini terjadi di sitoplasma sementara pada eukariota berlangsung pada mitokondria.
Pembuatan[sunting | sunting sumber]

Asam asetat diproduksi secara sintetis maupun secara alami melalui fermentasi bakteri. Sekitar 75% asam asetat yang dibuat untuk digunakan dalam industri kimia diproduksi melalui karbonilasi metanol, yang dijelaskan di bawah.[15] Sisanya dihasilkan melalui metode-metode alternatif. Sekarang hanya 10% dari produksi asam asetat dihasilkan melalui jalur alami, namun kebanyakan hukum yang mengatur bahwa asam asetat yang terdapat dalam cuka haruslah berasal dari proses biologis.[50] Sepanjang tahun 2003–2005, produksi total asam asetat dunia diperkirakan 5 Mt/a (juta ton per tahun), setengahnya diproduksi di Amerika Serikat. Eropa memproduksi sekitar 1 Mt/a dan terus menurun, sedangkan Jepang memproduksi sekitar 0,7 Mt/a. Sebanyak 1,51 Mt/a dihasilkan melalui daur ulang, sehingga total pasar asam asetat mencapai 6,51 Mt/a.[47][51] Sejak saat itu produksi global telah meningkat menjadi 10,7 Mt/a (in 2010), namun selanjutnya, diperkirakan terdapat perlambatan kenaikan produksi.[52] Dua perusahan produsen asam asetat terbesar adalah Celanese dan BP Chemicals. Produsen besar lainnya adalah Millenium Chemicals, Sterling Chemicals, Samsung, Eastman, dan Svensk Etanolkemi.[53]
Karbonilasi metanol[sunting | sunting sumber]
Kebanyakan asam asetat murni dihasilkan melalui karbonilasi. Dalam reaksi ini, metanol dan karbon monoksida bereaksi menghasilkan asam asetat sesuai persamaan:
Proses ini melibatkan iodometana sebagai zat antara, di mana reaksi itu sendiri terjadi dalam tiga tahap. Diperlukan suatu katalis karbonil logam untuk karbonilasi (tahap 2).[50]
Dua proses terkait dengan karbonilasi metanol adalah: proses Monsanto dengan katalis rodium, dan proses Cativa dengan katalis iridium. Proses Cativa lebih ramah lingkungan dan lebih efisien[54] dan telah banyak menggantikan proses sebelumnya. Jumlah katalisis air yang digunakan dalam kedua proses cukup banyak, tetapi proses Cativa memerlukan lebih sedikit air, sehingga reaksi pergeseran air-gas dapat ditekan dan produk sampingan yang dihasilkan juga lebih sedikit.
Dengan mengubah kondisi reaksi, anhidrida asetat dapat juga diproduksi pada kilang yang sama menggunakan katalis rodium.[55]
Oksidasi asetaldehida[sunting | sunting sumber]
Sebelum komersialisasi proses Monsanto, kebanyakan asam asetat diproduksi melalui oksidasi asetaldehida. Sekarang oksidasi asetaldehida merupakan metode produksi asam asetat terpenting kedua, sekalipun tidak kompetitif bila dibandingkan dengan metode karbonilasi metanol.
Asetaldehida yang digunakan dihasilkan melalui oksidasi butana atau nafta ringan, atau hidrasi dari etilena. Saat butena atau nafta ringan dipanaskan bersama udara disertai dengan beberapa ion logam, termasuk ion mangan, kobalt dan kromium, terbentuk peroksida yang selanjutnya terurai menjadi asam asetat sesuai dengan persamaan reaksi di bawah ini.
Umumnya reaksi ini dijalankan pada temperatur dan tekanan sedemikian rupa sehingga tercapai suhu setinggi mungkin namun butana masih berwujud cair. Kondisi reaksi pada umumnya sekitar 150 °C (302 °F) dan 55 atm. Produk sampingan seperti butanon, etil asetat, asam format dan asam propionat juga mungkin terbentuk. Produk sampingan ini juga bernilai komersial dan jika diinginkan kondisi reaksi dapat diubah untuk menghasilkan lebih banyak produk samping, namun pemisahannya dari asam asetat menjadi kendala karena membutuhkan biaya lebih banyak lagi.[56]
Melalui kondisi dan katalis yang sama seperti yang digunakan dalam oksidasi butana, oksigen di udara yang menghasilkan asam asetat dapat mengoksidasi asetaldehida.[56]
- Di mana reaksi sampingnya :
Dengan menggunakan katalis modern, reaksi ini dapat memiliki rendemen (yield) lebih besar dari 95%. Produk samping utamanya adalah etil asetat, asam format, dan formaldehida yang memiliki titik didih lebih rendah daripada asam asetat sehingga dapat dipisahkan dengan mudah melalui distilasi.[56]
Oksidasi etilena[sunting | sunting sumber]
Asetaldehida dapat dibuat dari etilena melalui proses Wacker, dan kemudian dioksidasi seperti di atas. Beberapa waktu terakhir, perusahaan kimia Showa Denko, yang membuka kilang oksidasi etilena di Ōita, Jepang, pada tahun 1997, mengkomersialkan konversi etilena menjadi asam asetat tahap-tunggal yang lebih murah.[56] Proses ini menggunakan katalis logam paladium yang didukung dengan asam heteropoli seperti asam tungstosilikat. Sulit untuk lebih kompetitif daripada karbonilasi metanol untuk kilang yang lebih kecil (100–250 kt/a), bergantung pada harga etilena lokal. Pendekatannya akan berbasis penggunaan teknologi oksidasi fotokatalitik untuk oksidasi selektif etilena dan etana menjadi asam asetat. Tidak seperti katalis oksidasi tradisional, proses oksidasi selektif akan menggunakan radiasi ultraviolet untuk memproduksi asam asetat pada temperatur dan tekanan kamar.
Fermentasi oksidatif[sunting | sunting sumber]
Dalam sejarah manusia, bakteri asam asetat dari genus Acetobacter telah membuat asam asetat dalam bentuk cuka. Dengan adanya oksigen yang cukup, bakteri ini dapat memproduksi cuka dari berbagai bahan makanan beralkohol. Bahan baku yang umum digunakan antara lain sari apel, anggur, dan biji-bijian terfermentasi, malt, beras, atau tepung kentang. Reaksi kimia keseluruhan yang difasilitasi oleh bakteri ini adalah:
Larutan alkohol encer diinokulasi dengan Acetobacter dan disimpan di tempat yang hangat dan cukup udara akan menjadi cuka setelah beberapa bulan. Metode pembuatan cuka industri mempercepat proses ini dengan meningkatkan pasokan oksigen kepada bakteri.[57]
Batch pertama dari cuka yang dihasilkan oleh fermentasi mungkin mengandung kesalahan dalam proses pembuatan anggur. Jika cendawan difermentasi pada suhu terlalu tinggi, acetobacter akan merusak ragi alami pada buah anggur. Karena permintaan cuka untuk keperluan memasak, kesehatan, dan sanitasi meningkat, pengrajin anggur cepat belajar untuk menggunakan bahan-bahan organik lain untuk menghasilkan cuka pada bulan-bulan musim panas sebelum tersedia buah anggur matang dan siap untuk diproses menjadi anggur. Metode ini lambat, namun, dan tidak selalu berhasil, sebagian pengrajin anggur tidak memahami proses.[58]
Salah satu proses komersial modern pertama adalah "metode cepat" atau "metode Jerman", pertama kali dipraktikkan di Jerman pada tahun 1823. Dalam proses ini, fermentasi berlangsung dalam suatu menara yang dikemas dengan serutan kayu atau arang. Umpan yang mengandung alkohol diteteskan di atas menara, dan udara segar dipasok dari bawah baik secara alami atau konveksi. Peningkatan pasokan udara dalam proses ini mempersingkat waktu produksi cuka dari bulan ke minggu.[59]
Saat ini, sebagian besar cuka dibuat dalam tangki budidaya terendam, pertama kali dijelaskan pada 1949 oleh Otto Hromatka dan Heinrich Ebner.[60] Dalam metode ini, alkohol difermentasi menjadi cuka dalam tangki sambil terus diaduk, dan oksigen disuplai dengan menggelegakkan udara melalui larutan. Dengan menggunakan aplikasi modern dari metode ini, cuka dengan 15% asam asetat dapat dibuat hanya dalam waktu 24 jam dalam proses batch, bahkan 20% dalam 60 jam proses kontinu.[58]
Fermentasi anaerobik[sunting | sunting sumber]
Spesies bakteri anaerob, termasuk anggota dari genus Clostridium atau Acetobacterium dapat mengkonversi gula menjadi asam asetat langsung, tanpa menggunakan etanol sebagai perantara. Reaksi kimia keseluruhan yang dilakukan oleh bakteri ini dapat direpresentasikan sebagai:
Bakteri asetogenik menghasilkan asam asetat dari senyawa satu-karbon, termasuk metanol, karbon monoksida, atau campuran karbon dioksida dan hidrogen:
Kemampuan Clostridium ini untuk memanfaatkan gula secara langsung, atau untuk menghasilkan asam asetat dari bahan yang lebih murah, berarti bahwa bakteri ini berpotensi menghasilkan asam asetat lebih efisien daripada oksidator etanol seperti Acetobacter. Namun, bakteri Clostridium lebih peka terhadap asam daripada Acetobacter. Bahkan strain Clostridium yang paling toleran terhadap asam dapat menghasilkan cuka dengan persentase asam asetat yang sangat sedikit, dibandingkan dengan strain Acetobacter yang dapat menghasilkan cuka hingga 20% asam asetat. Saat ini, masih lebih efisien memproduksi cuka menggunakan Acetobacter daripada menggunakan Clostridium dan kemudian dipekatkan. Akibatnya, meskipun bakteri asetogenik telah dikenal sejak tahun 1940, penggunaan industri mereka tetap terbatas pada beberapa aplikasi ceruk.[61]
Penggunaan[sunting | sunting sumber]

Asam asetat digunakan sebagai pereaksi kimia untuk menghasilkan berbagai senyawa kimia. Sebagian besar (40-45%) dari asam asetat dunia digunakan sebagai bahan untuk memproduksi monomer vinil asetat (vinyl acetate monomer, VAM). Selain itu asam asetat juga digunakan dalam produksi anhidrida asetat dan juga ester. Penggunaan asam asetat lainnya, termasuk penggunaan dalam cuka relatif kecil.[15][47]
Monomer vinil asetat[sunting | sunting sumber]
Penggunaan utama dari asam asetat adalah untuk produksi monomer vinil asetat (VAM). Pada tahun 2008, aplikasi ini diperkirakan mengkonsumsi sepertiga dari produksi asam asetat dunia.[15] Reaksinya adalah etilena dan asam asetat dengan oksigen melalui katalis paladium, yang dilakukan dalam fase gas.[62]
- 2 H3C–COOH + 2 C + O2 → 2 H3C–CO–O–CH=CH2 + 2 H
Vinil asetat dapat dipolimerisasi menjadi polivinil asetat atau polimer lain, yang merupakan komponen dalam cat dan perekat.[62]
Produksi ester[sunting | sunting sumber]
Ester utama dari asam asetat biasanya digunakan sebagai pelarut untuk tinta, cat dan pelapis. Ester ini termasuk etil asetat, n-butil asetat, isobutil asetat, dan propil asetat. Mereka biasanya diproduksi dari asam asetat dan alkohol yang sesuai melalui reaksi yang dikatalisis:
- H3C–COOH + HO–R → H3C–CO–O–R + H2O, (R = gugus alkil umum)
Kebanyakan ester asetat, yang dihasilkan dari asetaldehida menggunakan reaksi Tishchenko. Selain itu, eter asetat digunakan sebagai pelarut untuk nitroselulosa, lak akrilik, penghilang pernis, dan noda kayu. Pertama, glikol monoeter diproduksi dari etilena oksida atau propilena oksida dengan alkohol, yang kemudian diesterifikasi dengan asam asetat. Tiga produk utama adalah etilena glikol monoetil eter asetat (EEA), etilena glikol monobutil eter asetat (EBA), dan propilena glikol monometil eter asetat (PMA, lebih dikenal sebagai PGMEA dalam proses manufaktur semikonduktor, tempat ia digunakan sebagai pelarut penahan). Aplikasi ini mengkonsumsi sekitar 15% sampai 20% dari asam asetat di seluruh dunia. Eter asetat, misalnya EEA, telah terbukti berbahaya bagi reproduksi manusia.[47]
Anhidrida asetat[sunting | sunting sumber]
Produk dari kondensasi dua molekul asam asetat adalah anhidrida asetat. Produksi anhidrida asetat seluruh dunia adalah aplikasi utama, dan menggunakan sekitar 25% sampai 30% dari produksi asam asetat global. Proses utama melibatkan dehidrasi asam asetat untuk menghasilkan ketena pada 700–750 °C. Ketena kemudian direaksikan dengan asam asetat untuk mendapatkan anhidrida dengan:[63]
CH3CO2H → CH2=C=O + H2O
CH3CO2H + CH2=C=O → (CH3CO)2O
Anhidrida asetat adalah asetilator. Dengan demikian, aplikasi utama adalah pada pembuatan selulosa asetat, tekstil sintetis yang juga digunakan untuk film fotografi. Anhidrida asetat juga merupakan pereaksi pada produksi heroin dan senyawa lainnya.[63]
Sebagai pelarut[sunting | sunting sumber]
Asam asetat glasial adalah pelarut protik polar yang baik, seperti disebutkan di atas. Ia sering digunakan sebagai pelarut pada rekristalisasi untuk memurnikan senyawa organik. Asam asetat digunakan sebagai pelarut dalam produksi asam tereftalat (TPA), bahan baku untuk polietilena tereftalat (PET). Pada tahun 2006, sekitar 20% dari asam asetat digunakan untuk produksi TPA.[47]
Asam asetat sering digunakan sebagai pelarut untuk reaksi yang melibatkan karbokation, seperti alkilasi Friedel-Crafts. Sebagai contoh, satu tahap dalam pembuatan kamper sintetis komersial melibatkan penataulangan Wagner-Meerwein dari kamfena menjadi isobornil asetat; di sini asam asetat bertindak sebagai pelarut dan nukleofil sekaligus untuk menjebak karbokation yang sudah mengalami penataulangan.[64]
Asam asetat glasial digunakan dalam kimia analitik untuk menentukan kadar basa lemah seperti amida organik. Asam asetat glasial merupakan basa yang jauh lebih lemah daripada air, sehingga amida berperilaku sebagai basa kuat dalam media ini. Ia kemudian dapat dititrasi menggunakan asam yang sangat kuat, seperti asam perklorat, yang dilarutkan dalam asam asetat glasial.[65]
Manfaat medis[sunting | sunting sumber]
Asam asetat encer digunakan dalam terapi fisik menggunakan iontoforesis.[66]
Cuka[sunting | sunting sumber]
Cuka biasanya mengandung 4-18% massa asam asetat. Cuka digunakan langsung sebagai bumbu, dan dalam pengawetan sayuran dan makanan lain. Cuka meja cenderung lebih encer (4% sampai 8% asam asetat), sementara makanan acar komersial menggunakan larutan yang lebih pekat. Jumlah asam asetat yang digunakan sebagai cuka pada skala dunia tidak besar, tetapi merupakan aplikasi tertua dan paling terkenal.[67]
Dampak kesehatan dan keselamatan[sunting | sunting sumber]
Asam asetat pekat bersifat korosif terhadap kulit dan karena itu harus digunakan dengan hati-hati, karena dapat menyebabkan luka bakar, kerusakan mata permanen, serta iritasi pada membran mukosa.[68][69] Luka bakar atau lepuhan bisa jadi tidak terlihat hingga beberapa jam setelah kontak. Sarung tangan lateks tidak melindungi dari asam asetat, sehingga dalam menangani senyawa ini perlu digunakan sarung tangan berbahan karet nitril. Asam asetat sulit terbakar di laboratorium. Ia menjadi mudah terbakar jika suhu ruang melebihi 39 °C (102 °F), dan dapat membentuk campuran yang mudah meledak dengan udara di atas suhu ini (ambang ledakan: 5,4%–16%).

Asam asetat adalah iritan keras untuk mata, kulit, dan membran mukosa. Kontak kulit yang berkepanjangan dengan asam asetat glasial dapat mengakibatkan kerusakan jaringan. Paparan inhalasi (delapan jam) dengan uap asam asetat pada 10 ppm bisa mengakibatkan iritasi mata, hidung, dan tenggorokan; pada 100 ppm ditandai iritasi paru-paru dan kemungkinan kerusakan paru-paru, mata, dan kulit. Konsentrasi uap 1.000 ppm menyebabkan iritasi mata, hidung dan saluran pernapasan bagian atas dan tidak dapat ditoleransi. Prediksi ini didasarkan pada hewan percobaan dan paparan industri. Sensitisasi kulit terhadap asam asetat adalah jarang, tetapi telah terjadi.
Telah dilaporkan bahwa, untuk 12 pekerja yang terpapar selama dua tahun atau lebih pada rata-rata asam asetat di udara dengan konsentrasi 51 ppm, ada gejala iritasi mata, iritasi saluran pernapasan bagian atas, dan dermatitis hiperkeratosis. Paparan 50 ppm atau lebih tak dapat ditoleransi bagi kebanyakan orang dan menghasilkan lakrimasi intensif dan iritasi mata, hidung, serta tenggorokan, disertai edema faring dan bronkitis kronis. Iritasi mata dan hidung yang hebat pada konsentrasi lebih dari 25 ppm, dan konjungtivitis dari konsentrasi di bawah 10 ppm telah dilaporkan. Dalam sebuah studi dari lima pekerja yang terpapar selama 7 sampai 12 tahun untuk konsentrasi puncak 80-200 ppm, temuan utama adalah penghitaman dan hiperkeratosis kulit tangan, konjungtivitis (tapi tidak ada kerusakan kornea), bronkitis dan faringitis, dan erosi gigi yang terpapar (gigi seri dan taring).[70]
Bahaya larutan asam asetat tergantung pada konsentrasi. Tabel berikut mencantumkan klasifikasi Uni Eropa larutan asam asetat:[71]
| Konsentrasi berdasar berat |
Molaritas | Klasifikasi | Frase-R |
|---|---|---|---|
| 10%–25% | 1.67–4.16 mol/L | Iritan (Xi) | R36/38 |
| 25%–90% | 4.16–14.99 mol/L | Korosif (C) | R34 |
| >90% | >14.99 mol/L | Korosif (C) | R10, R35 |
Larutan asam asetat dengan konsentrasi lebih dari 25% harus ditangani di sungkup asap (fume hood) karena uapnya yang korosif dan berbau menyengat. Asam asetat encer, seperti pada cuka, tidak berbahaya. Namun konsumsi asam asetat yang lebih pekat adalah berbahaya bagi manusia maupun hewan. Hal itu dapat menyebabkan kerusakan pada sistem pencernaan, dan perubahan yang mematikan pada keasaman darah.
Oleh karena ketidakcocokannya, sangat disarankan agar asam asetat dijauhkan dari asam kromat, etilena glikol, asam nitrat, asam perklorat, permanganat, peroksida, dan hidroksil.[72]
Lihat pula[sunting | sunting sumber]
Catatan kaki[sunting | sunting sumber]
- ^ [H3O+] = 10−2,4 = 0,4 %
Referensi[sunting | sunting sumber]
- ^ Scientific literature reviews on generally recognized as safe (GRAS) food ingredients (dalam bahasa Inggris). National Technical Information Service. 1974. hlm. 1.
- ^ "Chemistry", volume 5, Encyclopedia Britannica, 1961, hlm. 374
- ^ IUPAC, Commission on Nomenclature of Organic Chemistry (1993). "Table 28(a) Carboxylic acids and related groups. Unsubstituted parent structures". A Guide to IUPAC Nomenclature of Organic Compounds (Recommendations 1993) (dalam bahasa Inggris). Blackwell Scientific publications. ISBN 0-632-03488-2. Diarsipkan dari versi asli tanggal 2012-04-25. Diakses tanggal 2015-09-20.
- ^ "Acetic Acid - PubChem Public Chemical Database". The PubChem Project (dalam bahasa Inggris). USA: National Center for Biotechnology Information. Diarsipkan dari versi asli tanggal 2018-12-25. Diakses tanggal 2015-09-20.
- ^ IUPAC Provisional Recommendations 2004 Chapter P-12.1; hlm. 4 Diarsipkan 2017-08-29 di Wayback Machine.
- ^ a b c Acetic acid (dalam bahasa Inggris), International Programme on Chemical Safety, diarsipkan dari versi asli tanggal 2016-03-06, diakses tanggal 16 Februari 2016
- ^ Ripin, D. H.; Evans, D. A. (4 November 2005). "pKa Table" (PDF) (dalam bahasa Inggris). Diarsipkan dari versi asli (PDF) tanggal 2015-07-22. Diakses tanggal 19 Juli 2015.
- ^ a b c "NIOSH Pocket Guide to Chemical Hazards #0002". National Institute for Occupational Safety and Health (NIOSH).
- ^ "Acetic acid". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ Modul Bahan Ajar Cetak Farmasi. Jakarta: Kementerian Kesehatan Republik Indonesia. 2016. hlm. 20.
- ^ "Food and Drug Regulations (C.R.C., c. 870)", Consolidated Regulations (dalam bahasa Inggris), Canadian Department of Justice, 31 Mei 2013, diarsipkan dari versi asli tanggal 2013-06-30, diakses tanggal 2016-01-18
- ^ UK Food Standards Agency: "Current EU approved additives and their E Numbers" Diarsipkan 2010-10-07 di Wayback Machine.
- ^ US Food and Drug Administration: "Listing of Food Additives Status Part I"
- ^ Australia New Zealand Food Standards Code: "Standard 1.2.4 – Labeling of ingredients" Diarsipkan 2013-09-02 di Wayback Machine.
- ^ a b c d Hosea Cheung; Robin S. Tanke; G. Paul Torrence (2005), "Acetic Acid", Ullmann's Encyclopedia of Industrial Chemistry (dalam bahasa Inggris), Weinheim: Wiley-VCH, doi:10.1002/14356007.a01_045.pub2
- ^ "acetic (adj.)". www.etymonline.com (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 2021-05-20. Diakses tanggal 20 Mei 2021.
- ^ "1". Preferred IUPAC Names (PDF). IUPAC. 2004. hlm. 4. Diarsipkan (PDF) dari versi asli tanggal 2017-08-29. Diakses tanggal 2015-09-20.
- ^ Doles, William; Wilkerson, Garrett; Morrison, Samantha; Richmond, Rodney G. (1 April 2015). "Glacial Acetic Acid Adverse Events: Case Reports and Review of the Literature". Hospital Pharmacy (dalam bahasa Inggris). 50 (4): 304–309. doi:10.1310/hpj5004-304. ISSN 0018-5787. PMC 4589881
 . PMID 26448660.
. PMID 26448660.
- ^ Cooper, Caroline (2010). Organic Chemist's Desk Reference (edisi ke-2). CRC Press. hlm. 102–104. ISBN 1-4398-1166-0.
- ^ Desousa, Luis R (1995). Common medical abbreviations. Albany: Delmar Publishers. hlm. 97. ISBN 978-0-8273-6643-5.
- ^ "Compound Summary Acetate". www.ebi.ac.uk (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 2021-08-30. Diakses tanggal 30 Agustus 2021.
- ^ Guerra, R (2005). "Industrial Effluents". Dalam Worsfold, Paul; Townshend, Alan; Poolen, Collin. Encyclopedia of Analytical Science (edisi ke-2). Amsterdam: Elsevier. hlm. 288-289. doi:10.1016/B0-12-369397-7/00111-4. ISBN 978-0-12-369397-6.
- ^ Johnston, Carol S.; Gaas, Cindy A. (30 Mei 2006). "Vinegar: medicinal uses and antiglycemic effect". MedGenMed: Medscape General Medicine. 8 (2): 61. ISSN 1531-0132. PMC 1785201
 . PMID 16926800. Diarsipkan dari versi asli tanggal 2021-05-26. Diakses tanggal 2021-05-26.
. PMID 16926800. Diarsipkan dari versi asli tanggal 2021-05-26. Diakses tanggal 2021-05-26.
- ^ Photos-Jones, E.; Bots, P.; Oikonomou, E.; Hamilton, A.; Knapp, C. W. (26 September 2020). "On metal and 'spoiled' wine: analysing psimythion (synthetic cerussite) pellets (5th–3rd centuries BCE) and hypothesising gas-metal reactions over a fermenting liquid within a Greek pot". Archaeological and Anthropological Sciences (dalam bahasa Inggris). 12 (10): 243. doi:10.1007/s12520-020-01184-1. ISSN 1866-9565. PMC 7560938
 . PMID 33088349 Periksa nilai
. PMID 33088349 Periksa nilai |pmid=(bantuan). - ^ Mingren, Wu (4 Desember 2019). "Savoring the Danger: Romans Loved Toxic 'Sugar of Lead' Wine". www.ancient-origins.net (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 2021-05-26. Diakses tanggal 26 Mei 2021.
- ^ Rezende, Lisa (2006). Chronology of Science (dalam bahasa Inggris). Infobase Publishing. hlm. 60–61. ISBN 978-1-4381-2980-8.
- ^ Wagner, Frank S. (2000). Kirk-Othmer Encyclopedia of Chemical Technology (dalam bahasa Inggris). American Cancer Society. doi:10.1002/0471238961.0103052023010714.a01. ISBN 978-0-471-23896-6. Diarsipkan dari versi asli tanggal 2021-11-09. Diakses tanggal 2021-05-27.
- ^ Goldwhite, Harold (September 2003). "This month in chemical history" (PDF). New Haven Section Bulletin American Chemical Society. 20 (3): 4. Diarsipkan dari versi asli (PDF) tanggal 4 Maret 2009.
- ^ Martin, Geoffrey (1917). Industrial and Manufacturing Chemistry (dalam bahasa Inggris) (edisi ke-Part 1, Organic). London: Crosby Lockwood. hlm. 330–331.
- ^ Schweppe, Helmut (1979). "Identification of Dyes on Old Textiles". Journal of the American Institute for Conservation. 19 (1): 14–23. doi:10.2307/3179569. ISSN 0197-1360. JSTOR 3179569. Diarsipkan dari versi asli tanggal 2021-04-14. Diakses tanggal 2021-05-28.
- ^ Murphy, Mark A. (2018-07-01). "Early Industrial Roots of Green Chemistry and the history of the BHC Ibuprofen process invention and its Quality connection". Foundations of Chemistry (dalam bahasa Inggris). 20 (2): 121–165. doi:10.1007/s10698-017-9300-9. ISSN 1572-8463.
- ^ Kalck, Philippe; Le Berre, Carole; Serp, Philippe (2020). "Recent advances in the methanol carbonylation reaction into acetic acid". Coordination Chemistry Reviews (dalam bahasa Inggris). 402: 213078. doi:10.1016/j.ccr.2019.213078. ISSN 0010-8545. Diarsipkan dari versi asli tanggal 2021-06-02. Diakses tanggal 2021-05-30.
- ^ Jones, Jane H (2000). "The Cativa™ Process for the Manufacture of Acetic AcidIridium Catalyst Improves Productivity in an Established Industrial Process". Platinum Metals Rev 94. 44 (3): 94–105. Diarsipkan dari versi asli tanggal 2021-06-02. Diakses tanggal 2021-05-30.
- ^ Lancaster, Mike (2002). Green Chemistry, an Introductory Text
 . Cambridge: Royal Society of Chemistry. hlm. 262–266. ISBN 978-0-85404-620-1.
. Cambridge: Royal Society of Chemistry. hlm. 262–266. ISBN 978-0-85404-620-1.
- ^ Goldberg, R.; Kishore, N.; Lennen, R. (2002). "Thermodynamic Quantities for the Ionization Reactions of Buffers" (PDF). Journal of Physical and Chemical Reference Data. 31 (2): 231–370. Bibcode:2002JPCRD..31..231G. doi:10.1063/1.1416902. Diarsipkan dari versi asli (PDF) tanggal 6 Oktober 2008.
- ^ "Comparison of the influence of citric acid and acetic acid as simulant for acidic food on the release of alloy constituents from stainless steel AISI 201". Journal of Food Engineering (dalam bahasa Inggris). 145: 51–63. 2015-01-01. doi:10.1016/j.jfoodeng.2014.08.006. ISSN 0260-8774. Diarsipkan dari versi asli tanggal 2021-05-31. Diakses tanggal 2021-06-01.
- ^ Jones, R. E.; Templeton, D. H. (1958). "The crystal structure of acetic acid". Acta Crystallographica (dalam bahasa Inggris). 11 (7): 484–487. doi:10.1107/S0365110X58001341. ISSN 0365-110X. Diarsipkan dari versi asli tanggal 2021-08-21. Diakses tanggal 2021-08-21.
- ^ Socha, Ondřej; Dračínský, Martin (2020). "Dimerization of Acetic Acid in the Gas Phase—NMR Experiments and Quantum-Chemical Calculations". Molecules (dalam bahasa Inggris). 25 (9): 2150. doi:10.3390/molecules25092150. PMC 7248931
 . PMID 32375390. Diarsipkan dari versi asli tanggal 2022-03-10. Diakses tanggal 2021-08-22.
. PMID 32375390. Diarsipkan dari versi asli tanggal 2022-03-10. Diakses tanggal 2021-08-22.
- ^ Briggs, James M.; Nguyen, Toan B.; Jorgensen, William L. (1991-04-01). "Monte Carlo simulations of liquid acetic acid and methyl acetate with the OPLS potential functions". The Journal of Physical Chemistry. 95 (8): 3315–3322. doi:10.1021/j100161a065. ISSN 0022-3654. Diarsipkan dari versi asli tanggal 2021-08-22. Diakses tanggal 2021-08-22.
- ^ Chocholoušová, Jana; Vacek, Jaroslav; Hobza, Pavel (2003-05-01). "Acetic Acid Dimer in the Gas Phase, Nonpolar Solvent, Microhydrated Environment, and Dilute and Concentrated Acetic Acid: Ab Initio Quantum Chemical and Molecular Dynamics Simulations". The Journal of Physical Chemistry A. 107 (17): 3086–3092. doi:10.1021/jp027637k. ISSN 1089-5639.
- ^ James B. Togeas. Acetic Acid Vapor: 2. A Statistical Mechanical Critique of Vapor Density Experiments. J. Phys. Chem. A 2005, 109, 5438-5444. DOI:10.1021/jp058004j
- ^ McMurry, John (2000), Organic Chemistry (dalam bahasa Inggris) (edisi ke-5), Brooks/Cole, hlm. 818, ISBN 0-534-37366-6
- ^ Zieborak, K.; Olszewski, K. (1958), Bulletin de L'Academie Polonaise des Sciences-Serie des Sciences Chimiques Geologiques et Geographiques (dalam bahasa Inggris), 6 (2), hlm. 3315–3322
- ^ Berre, Carole Le; Serp, Philippe; Kalck, Philippe; Torrence, G. Paull (2014). Acetic Acid (dalam bahasa Inggris). American Cancer Society. hlm. 1–34. doi:10.1002/14356007.a01_045.pub3. ISBN 978-3-527-30673-2. Diarsipkan dari versi asli tanggal 2021-08-31. Diakses tanggal 2021-08-31.
- ^ Charlot, G.; Murray, R.G. (1954), Qualitative Inorganic Analysis (edisi ke-4th), CUP Archive, hlm. 110
- ^ Brantley, L.R.; T.M. Cromwell; J.F. Mead (1947), "Detection of acetate ion by the reaction with arsenious oxide to form cacodyl oxide", Journal of Chemical Education (dalam bahasa Inggris), 24 (7): 353, Bibcode:1947JChEd..24..353B, doi:10.1021/ed024p353, ISSN 0021-9584
- ^ a b c d e Suresh, Bala (2003). "Acetic Acid" Diarsipkan 2010-12-20 di Wayback Machine.. CEH Report 602.5000, SRI International.
- ^ Fiume, Monice Zondlo; Cosmetic Ingredients Review Expert Panel (2003). "Final report on the safety assessment of triacetin". International Journal of Toxicology. 22 (Suppl 2): 1–10. doi:10.1080/10915810390204845. ISSN 1091-5818. PMID 14555416. Diarsipkan dari versi asli tanggal 2021-08-31. Diakses tanggal 2021-08-31.
- ^ Edisi eksekutif: J. Buckingham (1996), Dictionary of Organic Compounds (dalam bahasa Inggris), 1 (edisi ke-6), London: Chapman & Hall, ISBN 0-412-54090-8
- ^ a b Yoneda, Noriyki; Kusano, Satoru; Yasui, Makoto; Pujado, Peter; Wilcher, Steve (2001). Appl. Catal. A: Gen. 221, 253–265.
- ^ "Production report". Chem. Eng. News (11 Juli 2005), 67–76.
- ^ Acetic Acid :: Petrochemicals :: World Petrochemicals :: SRI Consulting. http://chemical.ihs.com/WP/Public/Reports/acetic_acid/ Diarsipkan 2012-01-19 di Wayback Machine.
- ^ "Reportlinker Adds Global Acetic Acid Market Analysis and Forecasts Diarsipkan 2016-03-03 di Wayback Machine.". Market Research Database. Maret 2009. p. contents.
- ^ Lancaster, Mike (2002) Green Chemistry, an Introductory Text, Cambridge: Royal Society of Chemistry, pp. 262–266. ISBN 0-85404-620-8.
- ^ Zoeller, J.R.; Agreda, V.H.; Cook, S.L.; Lafferty, N.L.; Polichnowski, S.W.; Pond, D.M. (1992), "Eastman Chemical Company Acetic Anhydride Process", Catalysis Today (dalam bahasa Inggris), 13 (1): 73–91, doi:10.1016/0920-5861(92)80188-S
- ^ a b c d Sano, Ken‐ichi; Hiroshi Uchida; Syoichirou Wakabayashi (1999), "A new process for acetic acid production by direct oxidation of ethylene", Catalysis Surveys from Japan (dalam bahasa Inggris), 3 (1): 55–60, doi:10.1023/A:1019003230537, ISSN 1384-6574
- ^ Chotani, Gopal K.; Gaertner, Alfred L.; Arbige, Michael V.; Timothy C. Dodge (2007), "Industrial Biotechnology: Discovery to Delivery", Kent and Riegel's Handbook of Industrial Chemistry and Biotechnology (dalam bahasa Inggris), Springer: 32–34, ISBN 978-0-387-27842-1
- ^ a b Otto Hromatka; Heinrich Ebner (1959), "Vinegar by Submerged Oxidative Fermentation", Industrial & Engineering Chemistry (dalam bahasa Inggris), 51 (10): 1279–1280, doi:10.1021/ie50598a033
- ^ Everett P. Partridge (1931), "Acetic Acid and Cellulose Acetate in the United States A General Survey of Economic and Technical Developments", Industrial & Engineering Chemistry (dalam bahasa Inggris), 23 (5): 482–498, doi:10.1021/ie50257a005
- ^ O Hromatka; H Ebner (1949), "Investigations on vinegar fermentation: Generator for vinegar fermentation and aeration procedures", Enzymologia (dalam bahasa Inggris), 13: 369
- ^ Jia Huey Sim; Azlina Harun Kamaruddin; Wei Sing Long; Ghasem Najafpour (2007), "Clostridium aceticum—A potential organism in catalyzing carbon monoxide to acetic acid: Application of response surface methodology", Enzyme and Microbial Technology, 40 (5): 1234–1243, doi:10.1016/j.enzmictec.2006.09.017
- ^ a b Günter Roscher (2005), "VInyl Esters", Ullmann's Encyclopedia of Industrial Chemistry (dalam bahasa Inggris), Weinheim: Wiley-VCH, doi:10.1002/14356007.a27_419
- ^ a b Heimo Held; Alfred Rengstl; Dieter Mayer (2005), "Acetic Anhydride and Mixed Fatty Acid Anhydrides", Ullmann's Encyclopedia of Industrial Chemistry (dalam bahasa Inggris), Weinheim: Wiley-VCH, doi:10.1002/14356007.a01_065
- ^ Sell, Charles S. (2006), "4.2.15 Bicyclic Monoterpenoids", The Chemistry of Fragrances: From Perfumer to Consumer. RSC Paperbacks Series (dalam bahasa Inggris), 38 (edisi ke-2), Great Britain: Royal Society of Chemistry, hlm. 80, ISBN 0-85404-824-3
- ^ Felgner, Andrea, Titration in Non-Aqueous Media (dalam bahasa Inggris), Sigma-Aldrich
- ^ Kolt, Gregory S.; Snyder-Mackler, Lynn (2007), Physical Therapies in Sport and Exercise (dalam bahasa Inggris), Elsevier Health Sciences, hlm. 223, ISBN 978-0-443-10351-3
- ^ Bernthsen, A.; Sudborough, J.J. (1922), Organic Chemistry, London: Blackie and Son, hlm. 155
- ^ "ICSC 0363 – ACETIC ACID" Diarsipkan 2016-03-03 di Wayback Machine.. International Programme on Chemical Safety. 5 June 2010.
- ^ "Occupational Safety and Health Guideline for Acetic Acid" Diarsipkan 2016-03-04 di Wayback Machine. (PDF). Centers for Disease Control and Prevention.
- ^ Sherertz, Peter C. (1 June 1994), Acetic Acid Diarsipkan 2016-03-04 di Wayback Machine. (PDF), Virginia Department of Health Division of Health Hazards Control
- ^ Yee, Allan (10 May 2013). "HSIS Consolidated List – Alphabetical Index" Diarsipkan 2016-03-03 di Wayback Machine.. Safe Work Australia.
- ^ "Acetic acid MSDS" Diarsipkan 2016-01-11 di Wayback Machine.. 21 Mei 2013
Pranala luar[sunting | sunting sumber]
- (Inggris) Acetic Acid dari Encyclopædia Britannica
- (Inggris) Halaman data asam asetat
- (Inggris) International Chemical Safety Card 0363
- (Inggris) National Pollutant Inventory – Acetic acid fact sheet
- (Inggris) NIOSH Pocket Guide to Chemical Hazard
- (Inggris) Method for sampling and analysis
- (Inggris) ChemSub Online: Acetic acid
- (Inggris) Perhitungan tekanan uap, rapat jenis cairan, viskositas cairan dinamis, dan tegangan permukaan asam asetat
- (Inggris) National Center for Biotechnology Information. PubChem Compound Database; CID=176 (diakses tanggal 27 Februari 2016).