Dimetil tereftalat

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Dimetil benzena-1,4-dikarboksilat | |
| Nama lain
Dimetil tereftalat
Dimetil ester asam 1,4-Benzenadikarboksilat Dimethyl 4-ftalat Dimetil p-ftalat Di-Me tereftalat Metil 4-karbometoksibenzoat Metil-p-(metoksikarbonil)benzoat Metil tereftalat Metil ester asam tereftalat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Singkatan | DMT |
| Referensi Beilstein | 1107185 |
| ChemSpider | |
| Nomor EC | |
| MeSH | Dimethyl+4-phthalate |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C10H10O4 | |
| Massa molar | 194,19 g·mol−1 |
| Penampilan | padatan putih |
| Densitas | 1.2 g/cm3, ? |
| Titik lebur | 142[1] °C (288 °F; 415 K) |
| Titik didih | 288 °C (550 °F; 561 K) |
| Keasaman (pKa) | -7.21 |
| Kebasaan (pKb) | -6.60 |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Dimetil tereftalat (DMT) adalah suatu senyawa organik dengan rumus C6H4(CO2CH3)2. Senyawa ini merupakan diester yang terbentuk dari asam tereftalat dan metanol. Senyawa ini merupakan padatan putih yang meleleh untuk menghasilkan cairan tak berwarna yang dapat didistilasi.[2]
Produksi[sunting | sunting sumber]
Dimetil tereftalat (DMT) telah diproduksi dalam beberapa cara. Secara konvensional dan masih bernilai komersial adalah esterifikasi langsung dari asam tereftalat. Atau, dapat dibuat dengan tahap oksidasi dan esterifikasi metil secara bergantian dari p-xilena melalui metil p-toluat.[2]
Proses Witten[sunting | sunting sumber]
Dimetil tereftalat adalah ester dari asam tereftalat dan metanol dan disintesis oleh urutan reaksi. Jalur yang paling umum adalah proses Witten yang dinamai kota Witten di Ruhr.[3] Metode yang umum untuk produksi DMT dari para-xilena (PX) dan metanol tersebut terdiri dari empat tahap utama: oksidasi, esterifikasi, distilasi, dan kristalisasi.
Campuran p-xilena (PX) dan ester p-toluat (PT) dioksidasi dengan udara dengan adanya katalis logam berat (Co/Mn). Campuran asam yang dihasilkan dari oksidasi diesterifikasi dengan metanol (MeOH, CH3OH) untuk menghasilkan campuran ester. Campuran ester mentah disuling untuk membuang semua boiler berat dan residu yang dihasilkan; ester ringan akan didaur ulang pada bagian oksidasi. DMT mentah kemudian dikirim ke bagian kristalisasi untuk membuang isomer DMT, asam residual dan aldehida aromatik.[4]

|
| Sintesis Dimetil tereftalat |
|---|
Esterifikasi asam yang dihasilkan dengan metanol menghasilkan metil p-toluat pada 250⁰C dan 2500 kPa dan oksidasi berikutnya serta esterifikasi metil p-toluat menghasilkan Dimetil tereftalat (DMT) seperti yang ditunjukkan pada reaksi di bawah ini:[2]
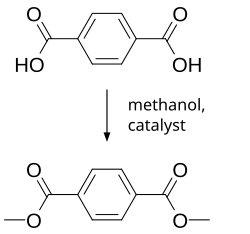
|
| Esterifikasi asam yang dihasilkan dengan metanol |
|---|
Metode alternatif dari reaksi ini dimulai dengan oksidasi p-xilena dengan asam tereftalat,[5] yang kemudian diesterifikasi dengan metanol. Metode ini disebut sebagai "proses SD".
Esterifikasi langsung[sunting | sunting sumber]
Jika asam tereftalat yang sangat murni tersedia, DMT dapat dibuat dalam proses yang terpisah melalui esterifikasi dengan metanol untuk dimetil tereftalat yang kemudian dimurnikan dengan distilasi:
- C8H6O4 (TPA) + 2CH3OH (Methanol) → C10H10O4 (DMT) + 2 H2O
dengan kehadiran o-xilena pada suhu 250–300 ⁰C.
Aplikasi[sunting | sunting sumber]
DMT digunakan dalam produksi poliester,[6] termasuk polietilena tereftalat (PET), politrimetilena tereftalat (PTT), dan polibutilena tereftalat (PBT). Senyawa ini terdiri dari benzena tersubstitusi dengan gugus karboksimetil (CO2CH3) pada posisi 1 dan 4. Karena DMT bersifat volatil, ia merupakan zat antara dalam beberapa skema untuk daur ulang PET, misalnya dari botol plastik.
 |

|
| Sintesis PET melalui transesterifikasi dimetil tereftalat dan etilen glikol | |
|---|---|
Hidrogenasi DMT menghasilkan diol sikloheksanadimetanol, yang merupakan monomer yang berguna.
Referensi[sunting | sunting sumber]
- ^ Record of Dimethylterephthalate dalam GESTIS Substance Database dari IFA, diakses tanggal 9 March 2008.
- ^ a b c Richard J. Sheehan "Terephthalic Acid, Dimethyl Terephthalate, and Isophthalic Acid" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.doi:10.1002/14356007.a26_193
- ^ Lihat GB Patent 727989, "Improvements in or relating to the production of Benzene Polycarboxylic Acids or Derivatives thereof" untuk Imhausen & Co dari Witten (Jerman), diterbitkan pada 13 April 1955
- ^ http://www.gtctech.com/technology-licensing/polyester-technologies/dimethyl-terephthalate-technology/[pranala nonaktif permanen]
- ^ U.S. Patent 2833816, "Preparation of aromatic polycarboxylic acids", 6 Mei 1958, Mid-Century Corporation
- ^ Bertram Philipp, Peter Stevens: Grundzüge der Industriellen Chemie, VCH Verlagsgesellschaft mbH, 1987, S. 308–309, ISBN 3-527-25991-0.
