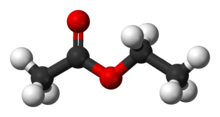
Etil asetat

| |
| |
| Nama | |
|---|---|
| Nama IUPAC
Etil asetat
| |
| Nama IUPAC (sistematis)
Etil etanoat | |
| Nama lain
Ester asetat, Eter asetat, Etil ester dari asam asetat
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C4H8O2 | |
| Massa molar | 88,11 g·mol−1 |
| Penampilan | Cairan tak berwarns |
| Bau | seperti eter, aroma buah[1] |
| Densitas | 0,902 g/cm3 |
| Titik lebur | −83,6 °C (−118,5 °F; 189,6 K) |
| Titik didih | 77,1 °C (170,8 °F; 350,2 K) |
| 8,3 g/100 mL (20 °C) | |
| Kelarutan dalam etanol, aseton, dietil eter, benzena |
Dapat campur |
| Tekanan uap | 73 mmHg (20 °C)[1] |
| Keasaman (pKa) | 25 |
| Indeks bias (nD) | 1,3720 |
| Viskositas | 426 μPa s (0,426 cP) pada 25 °C |
| Struktur | |
| 1,78 D | |
| Bahaya | |
| Bahaya utama | Mudah terbakar (F), Iritan (Xi) |
| Frasa-R | R11, R36, R66, R67 |
| Frasa-S | S16, S26, S33 |
| Titik nyala | −4 °C (25 °F; 269 K) |
| Ambang ledakan | 2,0%-11,5%[1] |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
11,3 g/kg, mencit |
LC50 (konsentrasi median)
|
16000 ppm (mencit, 6 jam) 12295 ppm (tikus, 2 jam) 1600 ppm (mencit, 8 jam)[2] |
LCLo (terendah tercatat)
|
21 ppm (marmot, 1 jam) 12330 ppm (tikus, 3 jam)[2] |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
TWA 400 ppm (1400 mg/m3)[1] |
REL (yang direkomendasikan)
|
TWA 400 ppm (1400 mg/m3)[1] |
IDLH (langsung berbahaya)
|
2000 ppm[1] |
| Senyawa terkait | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Etil asetat adalah senyawa organik dengan rumus CH3CH2OC(O)CH3. Senyawa ini merupakan ester dari etanol dan asam asetat. Senyawa ini berwujud cairan tak berwarna, memiliki aroma khas dan digunakan sebagai perekat[3]. Senyawa ini sering disingkat EtOAc, dengan Et mewakili gugus etil dan OAc mewakili asetat. Etil asetat diproduksi dalam skala besar sebagai pelarut.
Sifat kimia dan fisika
[sunting | sunting sumber]Etil asetat adalah pelarut polar menengah yang volatil (mudah menguap), tidak beracun, dan tidak higroskopis. Etil asetat merupakan penerima ikatan hidrogen yang lemah, dan bukan suatu donor ikatan hidrogen karena tidak adanya proton yang bersifat asam (yaitu hidrogen yang terikat pada atom elektronegatif seperti fluor, oksigen, dan nitrogen. Etil asetat dapat melarutkan air hingga 3%, dan larut dalam air hingga kelarutan 8% pada suhu kamar. Kelarutannya meningkat pada suhu yang lebih tinggi. Namun, senyawa ini tidak stabil dalam air yang mengandung basa atau asam.
Sintesis
[sunting | sunting sumber]Etil asetat disintesis melalui reaksi esterifikasi Fischer dari asam asetat dan etanol dan hasilnya beraroma jeruk (perisa sintesis), biasanya dalam sintesis disertai katalis asam seperti asam sulfat.
- CH3CH2OH + CH3COOH → CH3COOCH2CH3 + H2O
Reaksi di atas merupakan reaksi reversibel dan menghasilkan suatu kesetimbangan kimia. Karena itu, rasio hasil dari reaksi di atas menjadi rendah jika air yang terbentuk tidak dipisahkan. Di laboratorium, produk etil asetat yang terbentuk dapat dipisahkan dari air dengan menggunakan aparatus Dean-Stark.
Reaksi
[sunting | sunting sumber]Etil asetat dapat dihidrolisis pada keadaan asam atau basa menghasilkan asam asetat dan etanol kembali. Katalis asam seperti asam sulfat dapat menghambat hidrolisis karena berlangsungnya reaksi kebalikan hidrolisis yaitu esterifikasi Fischer.
Untuk memperoleh rasio hasil yang tinggi, biasanya digunakan basa kuat dengan proporsi stoikiometris, misalnya natrium hidroksida. Reaksi ini menghasilkan etanol dan natrium asetat, yang tidak dapat bereaksi lagi dengan etanol:
- CH3CO2C2H5 + NaOH → C2H5OH + CH3CO2Na
Referensi
[sunting | sunting sumber]- ^ a b c d e f "NIOSH Pocket Guide to Chemical Hazards #0260". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b "Ethyl acetate". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ Praja, Denny Indra (2015-09-01). Zat Aditif Makanan: Manfaat dan Bahayanya. Garudhawaca. ISBN 978-602-7949-55-3.
Pranala luar
[sunting | sunting sumber]- (Inggris) Material safety data (MSDS) for ethyl acetate
- (Inggris) National Pollutant Inventory - Ethyl acetate fact sheet Diarsipkan 2006-01-12 di Wayback Machine.
- (Inggris) Ethyl Acetate: Molecule of the Month
- (Inggris) Purpose of Using Concentrated Sulfuric Acid in Esterification for Catalysis Diarsipkan 2007-05-28 di Wayback Machine.
