Tembaga
| Tembaga | ||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Tembaga asli (berukuran ~4 cm) | ||||||||||||||||||||||||||||
Garis spektrum tembaga | ||||||||||||||||||||||||||||
| Sifat umum | ||||||||||||||||||||||||||||
| Nama, lambang | tembaga, Cu | |||||||||||||||||||||||||||
| Pengucapan | /têmbaga/[1] | |||||||||||||||||||||||||||
| Penampilan | metalik merah-jingga | |||||||||||||||||||||||||||
| Tembaga dalam tabel periodik | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Nomor atom (Z) | 29 | |||||||||||||||||||||||||||
| Golongan | golongan 11 | |||||||||||||||||||||||||||
| Periode | periode 4 | |||||||||||||||||||||||||||
| Blok | blok-d | |||||||||||||||||||||||||||
| Kategori unsur | logam transisi | |||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| |||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 3d10 4s1 | |||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 1 | |||||||||||||||||||||||||||
| Sifat fisik | ||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | |||||||||||||||||||||||||||
| Titik lebur | 1357,77 K (1084,62 °C, 1984,32 °F) | |||||||||||||||||||||||||||
| Titik didih | 2835 K (2562 °C, 4643 °F) | |||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 8,96 g/cm3 | |||||||||||||||||||||||||||
| saat cair, pada t.l. | 8,02 g/cm3 | |||||||||||||||||||||||||||
| Kalor peleburan | 13,26 kJ/mol | |||||||||||||||||||||||||||
| Kalor penguapan | 300,4 kJ/mol | |||||||||||||||||||||||||||
| Kapasitas kalor molar | 24,440 J/(mol·K) | |||||||||||||||||||||||||||
Tekanan uap
| ||||||||||||||||||||||||||||
| Sifat atom | ||||||||||||||||||||||||||||
| Bilangan oksidasi | −2, 0,[2] +1, +2, +3, +4 (oksida agak basa) | |||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,90 | |||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 745,5 kJ/mol ke-2: 1957,9 kJ/mol ke-3: 3555 kJ/mol (artikel) | |||||||||||||||||||||||||||
| Jari-jari atom | empiris: 128 pm | |||||||||||||||||||||||||||
| Jari-jari kovalen | 132±4 pm | |||||||||||||||||||||||||||
| Jari-jari van der Waals | 140 pm | |||||||||||||||||||||||||||
| Lain-lain | ||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | |||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | |||||||||||||||||||||||||||
| Kecepatan suara batang ringan | (teranil) 3810 m/s (pada s.k.) | |||||||||||||||||||||||||||
| Ekspansi kalor | 16,5 µm/(m·K) (suhu 25 °C) | |||||||||||||||||||||||||||
| Konduktivitas termal | 401 W/(m·K) | |||||||||||||||||||||||||||
| Resistivitas listrik | 16,78 nΩ·m (suhu 20 °C) | |||||||||||||||||||||||||||
| Arah magnet | diamagnetik[3] | |||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | −5,46×10−6 cm3/mol[4] | |||||||||||||||||||||||||||
| Modulus Young | 110–128 GPa | |||||||||||||||||||||||||||
| Modulus Shear | 48 GPa | |||||||||||||||||||||||||||
| Modulus curah | 140 GPa | |||||||||||||||||||||||||||
| Rasio Poisson | 0,34 | |||||||||||||||||||||||||||
| Skala Mohs | 3,0 | |||||||||||||||||||||||||||
| Skala Vickers | 343–369 MPa | |||||||||||||||||||||||||||
| Skala Brinell | 235–878 MPa | |||||||||||||||||||||||||||
| Nomor CAS | 7440-50-8 | |||||||||||||||||||||||||||
| Sejarah | ||||||||||||||||||||||||||||
| Penamaan | dari Siprus, tempat penambangan utama di era Romawi (Cyprium) | |||||||||||||||||||||||||||
| Penemuan | Timur Tengah (9000 SM) | |||||||||||||||||||||||||||
| Simbol | "Cu": dari Latin cuprum | |||||||||||||||||||||||||||
| Isotop tembaga yang utama | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Tembaga adalah sebuah unsur kimia dengan lambang Cu (dari bahasa Latin: cuprum) dan nomor atom 29. Ia adalah logam yang lunak, mudah ditempa, dan ulet dengan konduktivitas termal dan listrik yang sangat tinggi. Permukaan tembaga murni yang baru diekspos memiliki warna oranye merah muda. Tembaga digunakan sebagai konduktor panas dan listrik, sebagai building material, bahan bangunan, dan sebagai konstituen dari berbagai paduan logam, seperti perak sterling yang digunakan dalam perhiasan, kupronikel yang digunakan untuk membuat perangkat keras laut dan koin, serta konstantan yang digunakan dalam pengukur regangan dan termokopel untuk pengukuran suhu.
Tembaga adalah salah satu dari sedikit logam yang dapat terjadi di alam dalam bentuk logam yang dapat digunakan secara langsung (logam asli). Hal ini menyebabkan penggunaan tembaga oleh manusia sangat awal di beberapa daerah, dari c. 8000 SM. Ribuan tahun kemudian, ia adalah logam pertama yang dilebur dari bijih sulfida, c. 5000 SM; logam pertama yang dicetak menjadi sebuah bentuk dalam cetakan, c. 4000 SM; dan logam pertama yang sengaja dipadukan dengan logam lain, timah, untuk membuat perunggu, c. 500 SM.[5]
Pada zaman Romawi, tembaga ditambang terutama di Siprus, yang menjadi asal nama logam ini, dari aes cyprium (logam Siprus), kemudian berubah menjadi cuprum (bahasa Latin). Coper (bahasa Inggris Kuno) dan copper (bahasa Inggris) berasal dari kata tersebut, dan ejaan selanjutnya pertama kali digunakan sekitar tahun 1530.[6]
Senyawa yang biasa ditemui adalah garam tembaga(II), yang sering memberi warna biru atau hijau pada mineral seperti azurit, malasit, dan pirus, dan telah digunakan secara luas dan historis sebagai pigmen.
Tembaga yang digunakan dalam bangunan, biasanya untuk atap, teroksidasi membentuk patina hijau dari senyawa yang disebut verdigris. Tembaga kadang-kadang digunakan dalam seni dekoratif, baik dalam bentuk logam elemental maupun dalam senyawa sebagai pigmen. Senyawa tembaga digunakan sebagai agen bakteriostatik, fungisida, dan pengawet kayu.
Tembaga sangat penting untuk semua organisme hidup sebagai mineral diet karena ia merupakan konstituen kunci dari sitokrom c oksidase. Pada moluska dan krustasea, tembaga merupakan konstituen dari pigmen hemosianin darah, digantikan oleh hemoglobin kompleks besi pada ikan dan vertebrata lainnya. Pada manusia, tembaga ditemukan terutama di hati, otot, dan tulang.[7] Tubuh orang dewasa mengandung antara 1,4 dan 2,1 mg tembaga per kilogram berat badan.[8]
Karakteristik[sunting | sunting sumber]
Sifat fisik[sunting | sunting sumber]


Tembaga, perak, dan emas berada di golongan 11 pada tabel periodik; ketiga logam ini memiliki satu elektron orbital-s di atas sebuah kulit elektron-d yang terisi dan dicirikan oleh keuletan, serta konduktivitas listrik dan termal yang tinggi. Kulit-d yang terisi pada ketiga unsur ini berkontribusi sedikit pada interaksi antaratom, yang didominasi oleh elektron-s melalui ikatan logam. Tidak seperti logam dengan kulit-d yang tidak lengkap, ikatan logam pada tembaga tidak memiliki karakter kovalen dan relatif lemah. Pengamatan ini menjelaskan kekerasan yang rendah dan keuletan yang tinggi dari monokristalin tembaga.[9] Pada skala makroskopis, kemunculan cacat yang diperluas ke kisi kristal, menghambat aliran material di bawah tekanan yang diterapkan, sehingga meningkatkan kekerasannya. Untuk alasan ini, tembaga biasanya dipasok dalam bentuk polikristalin berbutir halus, yang memiliki kekuatan lebih besar daripada bentuk monokristalin.[10]
Kelunakan tembaga sebagian menjelaskan konduktivitas listriknya yang tinggi dan (59,6×106 S/m) dan konduktivitas termalnya yang tinggi, tertinggi kedua (kedua setelah perak) di antara logam murni pada suhu kamar.[11] Hal ini dikarenakan resistivitas transpor elektron dalam logam pada suhu kamar terutama berasal dari hamburan elektron pada getaran termal kisi, yang relatif lemah pada logam lunak.[9] Kerapatan arus tembaga maksimum yang diperbolehkan di udara terbuka kira-kira sebesar 3,1×106 A/m2 luas penampang, dan di atasnya ia mulai memanas secara berlebihan.[12]
Tembaga adalah salah satu dari sedikit unsur logam dengan warna alami selain abu-abu atau perak.[13] Tembaga murni berwarna oranye-merah dan memperoleh noda kemerahan saat terkena udara. Hal ini disebabkan oleh frekuensi plasma tembaga yang rendah, yang terletak di bagian merah dari spektrum tampak, menyebabkannya menyerap warna hijau dan biru dengan frekuensi lebih tinggi.[14]
Seperti logam lainnya, jika tembaga bersentuhan dengan logam lain, korosi galvanik akan terjadi.[15]
Sifat kimia[sunting | sunting sumber]


Tembaga tidak bereaksi dengan air, tetapi bereaksi perlahan dengan oksigen dari udara untuk membentuk lapisan tembaga oksida cokelat-hitam yang, tidak seperti karat yang terbentuk pada besi di udara lembap, akan melindungi logam di bawahnya dari korosi lebih lanjut (pasivasi). Lapisan hijau verdigris (tembaga karbonat) sering terlihat pada struktur tembaga tua, seperti atap dari banyak bangunan tua[16] dan Patung Liberty.[17] Tembaga akan ternoda bila terkena beberapa senyawa belerang, di mana ia akan bereaksi membentuk berbagai tembaga sulfida.[18]
Isotop[sunting | sunting sumber]
Terdapat 29 isotop tembaga. 63Cu dan 65Cu bersifat stabil, dengan 63Cu membentuk sekitar 69% tembaga alami; keduanya memiliki spin 3⁄2.[19] Isotop lainnya bersifat radioaktif, dengan yang paling stabil adalah 67Cu dengan waktu paruh 61,83 jam.[19] Tujuh isotop metastabil telah dikarakterisasi; 68mCu adalah yang berumur paling panjang dengan waktu paruh 3,8 menit. Isotop dengan nomor massa di atas 64 mengalami β−, sedangkan isotop dengan nomor massa di bawah 64 mengalami β+. 64Cu, yang memiliki waktu paruh 12,7 jam, meluruh melalui dua cara tersebut.[20]
62Cu dan 64Cu memiliki aplikasi yang signifikan. 62Cu digunakan dalam 62CuCu-PTSM sebagai pelacak radioaktif untuk tomografi emisi positron.[21]
Keterjadian[sunting | sunting sumber]

Tembaga diproduksi di dalam bintang masif[22] dan terdapat di kerak Bumi dengan proporsi sekitar 50 bagian per juta (ppm).[23] Di alam, tembaga terjadi dalam berbagai mineral, meliputi tembaga asli, tembaga sulfida seperti kalkopirit, bornit, digenit, kovelit, dan kalkosit, tembaga sulfosalt seperti tetrahedit-tenantit dan enargit, tembaga karbonat seperti azurit dan malasit, serta sebagai tembaga(I) atau tembaga(II) oksida seperti kuprit dan tenorit, masing-masing.[11] Massa tembaga elemental terbesar yang ditemukan memiliki berat 420 ton dan ditemukan pada tahun 1857 di Semenanjung Keweenaw di Michigan, Amerika Serikat.[23] Tembaga asli adalah sebuah polikristal, dengan kristal tunggal terbesar yang pernah dijelaskan berukuran 4,4 × 3,2 × 3,2 cm.[24] Tembaga adalah unsur paling melimpah ke-25 di kerak Bumi, membentuk sekitar 50 ppm, dibandingkan dengan 75 ppm untuk seng dan 14 ppm untuk timbal.[25]
Konsentrasi latar belakang khas tembaga tidak melebihi 1 ng/m3 di atmosfer; 150 mg/kg di dalam tanah; 30 mg/kg pada tumbuh-tumbuhan; 2 μg/L dalam air tawar dan 0,5 μg/L dalam air laut.[26]
Produksi[sunting | sunting sumber]


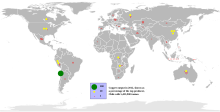

Sebagian besar tembaga ditambang atau diekstraksi sebagai tembaga sulfida dari tambang terbuka besar dalam deposit tembaga porfiri yang mengandung 0,4 hingga 1,0% tembaga. Contoh tambang yang ada antara lain Chuquicamata, di Chili, Tambang Kanyon Bingham, di Utah, Amerika Serikat, dan Tambang El Chino, di New Mexico, Amerika Serikat. Menurut Survei Geologi Britania Raya, pada tahun 2005, Chili adalah produsen tembaga terbesar dan menguasai sepertiga pasar dunia, diikuti oleh Amerika Serikat, Indonesia, dan Peru.[11] Tembaga juga dapat diperoleh kembali melalui proses pelindian in-situ. Beberapa lokasi di negara bagian Arizona dianggap sebagai kandidat utama untuk metode ini.[27] Jumlah tembaga yang digunakan terus meningkat dan kuantitas yang tersedia hampir tidak cukup untuk memungkinkan semua negara mencapai tingkat penggunaan dunia maju.[28] Sumber tembaga alternatif untuk pengumpulan yang saat ini sedang diteliti adalah nodul polimetalik, yang terletak di Samudra Pasifik pada kedalaman sekitar 3000–6500 meter di bawah permukaan laut. Nodul ini mengandung logam berharga lainnya seperti kobalt dan nikel.[29]
Cadangan dan harga[sunting | sunting sumber]

Tembaga telah digunakan setidaknya selama 10.000 tahun, tetapi lebih dari 95% dari semua tembaga yang pernah ditambang dan dilebur telah diekstraksi sejak tahun 1900.[30] Seperti banyak sumber daya alam lainnya, jumlah total tembaga di Bumi sangat besar, dengan sekitar 1014 ton dalam kilometer teratas kerak Bumi, yang bernilai sekitar 5 juta tahun pada tingkat ekstraksi saat ini. Namun, hanya sebagian kecil dari cadangan ini yang layak secara ekonomi dengan harga dan teknologi saat ini. Estimasi cadangan tembaga yang tersedia untuk pertambangan bervariasi dari 25 hingga 60 tahun, tergantung pada asumsi inti seperti tingkat pertumbuhan.[31] Daur ulang adalah sumber utama tembaga di dunia modern.[30] Karena faktor-faktor ini dan faktor lainnya, masa depan produksi dan pasokan tembaga menjadi bahan perdebatan, termasuk konsep tembaga puncak, analog dengan minyak puncak.[butuh rujukan]
Harga tembaga secara historis tidak stabil,[32] dan harganya meningkat dari level terendah dalam 60 tahun terakhir sebesar AS$0,60/lb (AS$1,32/kg) pada Juni 1999 menjadi $3,75/lb ($8,27/kg) pada Mei 2006. Harga tersebut turun menjadi $2,40/lb ($5,29/kg) pada Februari 2007, kemudian naik kembali menjadi $3,50/lb ($7,71/kg) pada April 2007.[33][butuh sumber yang lebih baik] Pada Februari 2009, melemahnya permintaan global dan penurunan tajam harga komoditas sejak harga tertinggi tahun sebelumnya membuat harga tembaga berada di angka $1,51/lb ($3,32/kg).[34] Antara September 2010 dan Februari 2011, harga tembaga naik dari £5.000 per metrik ton menjadi £6.250 per metrik ton.[35]
Metode[sunting | sunting sumber]

Konsentrasi tembaga pada bijih-bijih yang ada rata-rata hanya 0,6%, dan sebagian besar bijih komersial yang ada adalah sulfida, terutama kalkopirit (CuFeS2), bornit (Cu5FeS4) dan, pada tingkat yang lebih rendah, kovelit (CuS) dan kalkosit (Cu2S).[36] Sebaliknya, konsentrasi rata-rata tembaga dalam nodul polimetalik diperkirakan 1,3%. Metode ekstraksi tembaga serta logam lain yang ditemukan dalam nodul ini meliputi pelindian belerang, peleburan, dan penerapan proses Cuprion.[37][38] Untuk mineral yang ditemukan dalam bijih tanah, mereka dipekatkan dari bijih yang dihancurkan hingga kadar tembaga 10–15% melalui flotasi buih atau pelindian biologis.[39] Pemanasan bahan ini dengan silika dalam peleburan kilat menghilangkan sebagian besar besi sebagai terak. Proses ini memanfaatkan kemudahan yang lebih besar untuk mengubah besi sulfida menjadi oksida, yang pada gilirannya bereaksi dengan silika untuk membentuk terak silikat yang mengapung di atas massa yang dipanaskan. Matte tembaga tembaga yang dihasilkan, terdiri dari Cu2S, dipanggang untuk mengubah tembaga sulfida menjadi oksida:[40]
- 2 Cu2S + 3 O2 → 2 Cu2O + 2 SO2
Kuproksida bereaksi dengan kuprosulfida untuk diubah menjadi tembaga melepuh saat dipanaskan:
- 2 Cu2O + Cu2S → 6 Cu + 2 SO2
Proses matte Sudbury hanya mengubah setengah sulfida tersebut menjadi oksida dan kemudian menggunakan oksida ini untuk menghilangkan sisa belerang sebagai oksida. Ia kemudian disempurnakan secara elektrolitik dan lumpur anoda dieksploitasi untuk platina dan emas yang dikandungnya. Langkah ini memanfaatkan reduksi tembaga oksida menjadi logam tembaga yang relatif mudah. Gas alam kemudian dialirkan ke seluruh lepuh untuk menghilangkan sebagian besar oksigen yang tersisa dan pengekstrakan elektrolisis dilakukan pada bahan yang dihasilkan untuk menghasilkan tembaga murni:[41]
- Cu2+ + 2 e− → Cu
- Tembaga melepuh
- Peleburan
- Tanur pantulan
- Penghapusan terak
- Pengecoran tembaga terhadap anoda
- Roda pengecoran
- Mesin pelepas anoda
- Lepas landas anoda
- Kereta rel
- Transportasi ke rumah tangki

Daur ulang[sunting | sunting sumber]
Seperti aluminium, tembaga dapat didaur ulang tanpa mengurangi kualitasnya, baik dari keadaan mentah maupun dari produk manufaktur.[42] Dilihat dari volumenya, tembaga adalah logam yang paling banyak didaur ulang ketiga setelah besi dan aluminium.[43] Diperkirakan 80% dari semua tembaga yang pernah ditambang masih digunakan hingga saat ini.[44] Menurut laporan Persediaan Logam dalam Masyarakat dari International Resource Panel, pemakaian tembaga per kapita global adalah sekitar 35–55 kg. Sebagian besar pemakaiannya terjadi di negara-negara yang lebih maju (140–300 kg per kapita) daripada negara-negara kurang berkembang (30–40 kg per capita).
Proses daur ulang tembaga kira-kira sama dengan yang digunakan untuk mengekstraksi tembaga tetapi membutuhkan langkah yang lebih sedikit. Tembaga bekas dengan kemurnian tinggi dilebur dalam sebuah tanur dan kemudian direduksi dan dicetak menjadi bilet dan ingot; tembaga bekas dengan kemurnian lebih rendah dimurnikan melalui penyepuhan dalam bak asam sulfat.[45]
Paduan[sunting | sunting sumber]

Terdapat banyak paduan tembaga yang telah diformulasikan, banyak di antaranya memiliki kegunaan penting. Kuningan adalah paduan tembaga dan seng. Perunggu biasanya mengacu pada paduan tembaga-timah, tetapi dapat merujuk pada paduan tembaga apa pun seperti perunggu aluminium. Tembaga adalah salah satu konstituen terpenting dari solder perak dan emas karat yang digunakan dalam industri perhiasan, mengubah warna, kekerasan, dan titik lebur paduan yang dihasilkan.[48] Beberapa solder bebas timbal terdiri dari paduan timah dengan sebagian kecil tembaga dan logam lainnya.[49]
Paduan tembaga dan nikel, disebut kupronikel, digunakan dalam koin berdenominasi rendah, seringkali untuk kelongsong luar. Koin lima sen A.S. (saat ini disebut nikel) terdiri dari 75% tembaga dan 25% nikel dalam komposisi homogen. Sebelum pengenalan kupronikel, yang diadopsi secara luas oleh banyak negara pada paruh kedua abad ke-20,[50] paduan tembaga dan perak juga digunakan, dengan Amerika Serikat menggunakan paduan 90% perak dan 10% tembaga hingga tahun 1965, ketika perak yang beredar telah dihapus dari semua koin dengan pengecualian Setengah dolar - mereka diturunkan menjadi paduan 40% perak dan 60% tembaga antara tahun 1965 dan 1970.[51] Paduan 90% tembaga dan 10% nikel tidaklah biasa karena ketahanannya terhadap korosi, digunakan untuk berbagai benda yang terpapar air laut, meskipun rentan terhadap sulfida yang terkadang ditemukan di pelabuhan dan muara yang tercemar.[52] Paduan tembaga dengan aluminium (sekitar 7%) memiliki warna keemasan dan digunakan dalam dekorasi.[23] Shakudō adalah paduan tembaga dekoratif Jepang yang mengandung persentase emas yang rendah, biasanya 4–10%, yang dapat dipatinakan menjadi warna biru tua atau hitam.[53]
Komposisi[sunting | sunting sumber]
Kemiripan tampilan luar dari berbagai paduan, bersama dengan kombinasi unsur yang berbeda yang digunakan saat membuat setiap paduan, dapat menimbulkan kebingungan saat mengkategorikan komposisi yang berbeda. Ada sebanyak 400 komposisi tembaga dan paduan tembaga berbeda yang dikelompokkan secara longgar ke dalam kategori: tembaga, paduan tembaga tinggi, kuningan, perunggu, nikel tembaga, tembaga-nikel-seng (perak nikel), tembaga bertimbal, dan paduan khusus. Tabel berikut mencantumkan elemen paduan utama untuk empat jenis yang lebih umum digunakan dalam industri modern, bersama dengan nama untuk setiap jenis. Jenis sejarah, seperti yang menjadi ciri Zaman Perunggu, lebih kabur karena campuran umumnya bervariasi.
| Keluarga | Unsur paduan utama | nomor UN |
|---|---|---|
| Paduan tembaga, kuningan | Seng (Zn) | C1xxxx–C4xxxx,C66400–C69800 |
| Perunggu fosfor | Timah (Sn) | C5xxxx |
| Perunggu aluminium | Aluminium (Al) | C60600–C64200 |
| Perunggu silikon | Silikon (Si) | C64700–C66100 |
| Kupronikel, perak nikel | Nikel (Ni) | C7xxxx |
Tabel berikut menguraikan komposisi kimia dari berbagai tingkat paduan tembaga.
| Keluarga | CDA | AMS | UNS | Cu [%] | Sn [%] | Pb [%] | Zn [%] | Ni [%] | Fe [%] | Al [%] | Lainnya [%] |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Kuningan merah | 833 | C83300 | 93 | 1.5 | 1.5 | 4 | |||||
| C83400[55] | 90 | 10 | |||||||||
| 836 | 4855B | C83600 | 85 | 5 | 5 | 5 | |||||
| 838 | C83800 | 83 | 4 | 6 | 7 | ||||||
| Kuningan setengah merah | 844 | C84400 | 81 | 3 | 7 | 9 | |||||
| 845 | C84500 | 78 | 3 | 7 | 12 | ||||||
| 848 | C84800 | 76 | 3 | 6 | 15 | ||||||
| Perunggu mangan | C86100[56] | 67 | 0,5 | 21 | 3 | 5 | Mn 4 | ||||
| 862† | C86200 | 64 | 26 | 3 | 4 | Mn 3 | |||||
| 863† | 4862B | C86300 | 63 | 25 | 3 | 6 | Mn 3 | ||||
| 865 | 4860A | C86500 | 58 | 0,5 | 39,5 | 1 | 1 | Mn 0,25 | |||
| Perunggu timah | 903 | C90300 | 88 | 8 | 4 | ||||||
| 905 | 4845D | C90500 | 88 | 10 | 0,3 maks | 2 | |||||
| 907 | C90700 | 89 | 11 | 0,5 maks | 0,5 maks | ||||||
| Perunggu timah bertimbal | 922 | C92200 | 88 | 6 | 1,5 | 4,5 | |||||
| 923 | C92300 | 87 | 8 | 1 maks | 4 | ||||||
| 926 | 4846A | C92600 | 87 | 10 | 1 | 2 | |||||
| 927 | C92700 | 88 | 10 | 2 | 0,7 maks | ||||||
| Perunggu timah bertimbal tinggi | 932 | C93200 | 83 | 7 | 7 | 3 | |||||
| 934 | C93400 | 84 | 8 | 8 | 0,7 maks | ||||||
| 935 | C93500 | 85 | 5 | 9 | 1 | 0,5 maks | |||||
| 937 | 4842A | C93700 | 80 | 10 | 10 | 0,7 maks | |||||
| 938 | C93800 | 78 | 7 | 15 | 0,75 maks | ||||||
| 943 | 4840A | C94300 | 70 | 5 | 25 | 0,7 maks | |||||
| Perunggu aluminium | 952 | C95200 | 88 | 3 | 9 | ||||||
| 953 | C95200 | 89 | 1 | 10 | |||||||
| 954 | 4870B 4872B |
C95400 | 85 | 4 | 11 | ||||||
| C95410[57] | 85 | 4 | 11 | Ni 2 | |||||||
| 955 | C95500 | 81 | 4 | 4 | 11 | ||||||
| C95600[58] | 91 | 7 | Si 2 | ||||||||
| C95700[59] | 75 | 2 | 3 | 8 | Mn 12 | ||||||
| 958 | C95800 | 81 | 5 | 4 | 9 | Mn 1 | |||||
| Perunggu silikon | C87200[60] | 89 | Si 4 | ||||||||
| C87400[61] | 83 | 14 | Si 3 | ||||||||
| C87500[62] | 82 | 14 | Si 4 | ||||||||
| C87600[63] | 90 | 5,5 | Si 4,5 | ||||||||
| 878 | C87800[64] | 80 | 14 | Si 4 | |||||||
| C87900[65] | 65 | 34 | Si 1 | ||||||||
| † Komposisi kimia dapat bervariasi untuk menghasilkan sifat mekanik | |||||||||||
Senyawa[sunting | sunting sumber]

Tembaga membentuk berbagai macam senyawa, biasanya dengan keadaan oksidasi +1 dan +2, yang masing-masing sering disebut kupro dan kupri.[66] Senyawa tembaga, baik kompleks organik maupun organologam, mempromosikan atau mengatalisasi berbagai proses kimia dan biologi.[67]
Senyawa biner[sunting | sunting sumber]
Seperti unsur lainnya, senyawa tembaga yang paling sederhana adalah senyawa biner, yaitu senyawa yang hanya mengandung dua unsur, contoh utamanya adalah oksida, sulfida, dan halida. Kupro- dan kuprioksida telah diketahui. Di antara banyak tembaga sulfida,[68] contoh pentingnya ialah tembaga(I) sulfida (Cu
2S) dan tembaga monosulfida (CuS).[69]
Kuprohalida dengan fluorin, klorin, bromin, dan iodin telah dikenal, sama seperti kuprihalida dengan fluorin, klorin, dan bromin. Percobaan untuk membuat tembaga(II) iodida hanya menghasilkan tembaga(I) iodida dan iodin.[66]
- 2 Cu2+ + 4 I− → 2 CuI + I2
Kimia koordinasi[sunting | sunting sumber]

Tembaga membentuk kompleks koordinasi dengan beberapa ligan. Dalam larutan berair, tembaga(II) eksis sebagai [Cu(H2O)6]2+. Kompleks ini menunjukkan nilai tukar air tercepat (kecepatan pengikatan dan pelepasan ligan air) untuk setiap kompleks akuo logam transisi. Menambahkan larutan natrium hidroksida akan menyebabkan pengendapan tembaga(II) hidroksida padat berwarna biru muda. Persamaan yang disederhanakan adalah:

- Cu2+ + 2 OH− → Cu(OH)2
Amonia berair menghasilkan endapan yang sama. Setelah menambahkan amonia berlebih, endapan tersebut akan larut, membentuk tetraamminatembaga(II):
- Cu(H2O)4(OH)2 + 4 NH3 → [Cu(H2O)2(NH3)4]2+ + 2 H2O + 2 OH−
Banyak oksianion lainnya membentuk kompleks; mereka meliputi tembaga(II) asetat, tembaga(II) nitrat, dan tembaga(II) karbonat. Tembaga(II) sulfat membentuk pentahidrat kristalin biru, senyawa tembaga yang paling dikenal di laboratorium. Ia digunakan dalam fungisida yang disebut campuran Bordeaux.[70]

Poliol, senyawa yang mengandung lebih dari satu gugus fungsi alkohol, umumnya berinteraksi dengan garam tembaga. Misalnya, garam tembaga digunakan untuk menguji gula pereduksi. Secara khusus, dengan menggunakan reagen Benedict dan larutan Fehling, adanya gula tersebut ditandai dengan perubahan warna dari tembaga(II) biru menjadi tembaga(I) oksida kemerahan.[71] Reagen Schweizer dan kompleks terkait dengan etilenadiamina dan amina lainnya melarutkan selulosa.[72] Asam amino seperti sistina membentuk kompleks kelat yang sangat stabil dengan tembaga(II)[73][74][75] termasuk dalam bentuk biohibrida logam–organik (MOBs). Ada banyak uji kimia basah untuk ion tembaga, salah satunya melibatkan kalium ferisianida, yang menghasilkan endapan biru cemerlang dengan garam tembaga(II).[76]
Kimia organotembaga[sunting | sunting sumber]
Senyawa yang mengandung ikatan karbon–tembaga dikenal sebagai senyawa organotembaga. Mereka sangat reaktif terhadap oksigen untuk membentuk tembaga(I) oksida dan memiliki banyak kegunaan dalam kimia. Mereka disintesis dengan mereaksikan senyawa tembaga(I) dengan reagen Grignard, alkuna terminal atau reagen organolitium;[77] khususnya, reaksi terakhir yang dijelaskan menghasilkan reagen Gilman. Mereka dapat mengalami substitusi dengan alkil halida untuk membentuk produk penggandengan; dengan demikian, mereka dinilai penting dalam bidang sintesis organik. Tembaga(I) asetilida sangat peka terhadap kejutan tetapi merupakan perantara dalam reaksi seperti penggandengan Cadiot–Chodkiewicz[78] dan penggandengan Sonogashira.[79] Adisi konjugat pada enona[80] dan karbokuprasi alkuna[81] juga dapat dicapai dengan senyawa organotembaga. Tembaga(I) membentuk berbagai kompleks lemah dengan alkena dan karbon monoksida, terutama dengan adanya ligan amina.[82]
Tembaga(III) dan tembaga(IV)[sunting | sunting sumber]
Tembaga(III) paling sering ditemukan dalam oksida. Contoh sederhananya adalah kalium kuprat, KCuO2, padatan berwarna biru kehitaman.[83] Senyawa tembaga(III) yang paling banyak dipelajari adalah superkonduktor kuprat. Itrium barium tembaga oksida (YBa2Cu3O7) terdiri dari pusat Cu(II) dan Cu(III). Seperti oksida, fluorida adalah anion yang sangat basa[84] dan diketahui dapat menstabilkan ion logam dalam keadaan oksidasi tinggi. Baik tembaga(III) dan bahkan tembaga(IV) fluorida telah diketahui, masing-masing K3CuF6 dan Cs2CuF6.[66]
Beberapa protein tembaga membentuk kompleks okso, yang juga mengandung tembaga(III).[85] Dengan tetrapeptida, kompleks tembaga(III) berwarna ungu akan distabilkan oleh ligan amida yang terdeprotonasi.[86]
Kompleks tembaga(III) juga ditemukan sebagai perantara dalam reaksi senyawa organotembaga,[87][88][89] misalnya dalam reaksi Kharasch–Sosnovsky.
Sejarah[sunting | sunting sumber]
Garis waktu tembaga menggambarkan bagaimana logam ini telah memajukan peradaban manusia selama 11.000 tahun terakhir.[90]
Prasejarah[sunting | sunting sumber]
Zaman Tembaga[sunting | sunting sumber]



Tembaga terjadi secara alami sebagai tembaga metalik asli dan diketahui oleh beberapa peradaban tertua yang pernah tercatat. Sejarah penggunaan tembaga dimulai pada 9000 SM di Timur Tengah;[91] sebuah liontin tembaga ditemukan di Irak utara yang berasal dari tahun 8700 SM.[92] Bukti menunjukkan bahwa emas dan besi meteorik (tetapi bukan besi yang dilebur) adalah dua logam pertama yang digunakan manusia sebelum tembaga.[93] Sejarah metalurgi tembaga dianggap mengikuti urutan ini: Pertama, pengerjaan dingin tembaga asli, kemudian penganilan, peleburan, dan, akhirnya, pengecoran lilin yang hilang. Di Anatolia tenggara, keempat teknik ini muncul kurang lebih secara bersamaan pada permulaan zaman Neolitikum sekitar 7500 SM.[94]
Peleburan tembaga ditemukan secara independen di berbagai tempat. Teknik ini mungkin ditemukan di Tiongkok sebelum 2800 SM, di Amerika Tengah sekitar 600 M, dan di Afrika Barat sekitar abad ke-9 atau ke-10 M.[95] Bukti paling awal dari tembaga pengecoran lilin yang hilang berasal dari jimat yang ditemukan di Mehrgarh, Pakistan dan bertanggal 4000 SM.[96] Pengecoran investasi ditemukan pada 4500–4000 SM di Asia Tenggara[91] dan penanggalan karbon telah mendirikan penambangan di Alderley Edge di Cheshire, Inggris, pada tahun 2280 hingga 1890 SM.[97]
Ötzi si Manusia Es, seorang pria dari tahun 3300 hingga 3200 SM, ditemukan bersama kapak dengan kepala tembaga 99,7% murni; kadar arsen yang tinggi di rambutnya menunjukkan keterlibatan dalam peleburan tembaga.[98] Pengalaman dengan tembaga telah membantu pengembangan logam lain; khususnya, peleburan tembaga menyebabkan penemuan peleburan besi.[98]

Produksi di Kompleks Tembaga Tua di Michigan dan Wisconsin bertanggal antara 6500 dan 3000 SM.[99][100][101] Sebuah tombak tembaga yang ditemukan di Wisconsin bertanggal 6500 SM.[99] Penggunaan tembaga oleh penduduk asli Kompleks Tembaga Tua dari wilayah Danau-Danau Besar di Amerika Utara telah ditentukan secara radiometrik sejak 7500 SM.[99][102][103] Penduduk asli Amerika Utara di sekitar Danau-Danau Besar mungkin juga telah menambang tembaga semasa itu, menjadikannya sebagai salah satu contoh ekstraksi tembaga tertua di dunia.[104] Terdapat bukti dari pencemaran timbal prasejarah dari danau di Michigan bahwa orang-orang di wilayah tersebut mulai menambang tembaga c. 6000 SM.[99][104] Bukti menunjukkan bahwa benda-benda tembaga utilitarian semakin tidak digunakan di Kompleks Tembaga Tua di Amerika Utara selama Zaman Perunggu dan terjadi pergeseran ke arah peningkatan produksi benda-benda tembaga hias.[105]
Zaman Perunggu[sunting | sunting sumber]

Perunggu alami, sejenis tembaga yang terbuat dari bijih yang kaya akan silikon, arsen, dan timah (jarang), mulai digunakan secara umum di Balkan sekitar 5500 SM.[106] Pemaduan tembaga dengan timah untuk membuat perunggu pertama kali dilakukan sekitar 4000 tahun setelah penemuan peleburan tembaga, dan sekitar 2000 tahun setelah "perunggu alami" mulai digunakan secara umum.[107] Artefak perunggu dari kebudayaan Vinča berasal dari tahun 4500 SM.[108] Artefak paduan tembaga dan perunggu Sumeria dan Mesir berasal dari tahun 3000 SM.[109] Biru Mesir, atau kuprorivait (kalsium tembaga silikat) adalah pigmen sintetis yang mengandung tembaga dan mulai digunakan di Mesir kuno sekitar 3250 SM.[110] Proses pembuatan biru Mesir diketahui oleh orang Romawi, tetapi pada abad keempat Masehi pigmen tersebut tidak lagi digunakan dan rahasia proses pembuatannya menjadi hilang. Bangsa Romawi mengatakan bahwa pigmen biru tersebut terbuat dari tembaga, silika, kapur, dan natron, dan dikenal sebagai caeruleum oleh mereka.
Zaman Perunggu dimulai di Eropa Tenggara sekitar 3700–3300 SM, di Eropa Barat Laut sekitar 2500 SM. Zaman tersebut berakhir dengan dimulainya Zaman Besi, 2000–1000 SM di Timur Dekat, dan 600 SM di Eropa Utara. Transisi antara periode Neolitikum dan Zaman Perunggu dulunya disebut periode Kalkolitik (batu tembaga), ketika perkakas tembaga digunakan dengan perkakas batu. Istilah ini berangsur-angsur tidak digunakan karena di beberapa bagian dunia, Kalkolitik dan Neolitikum saling berdekatan di kedua akhirnya. Kuningan, paduan tembaga dan seng, ditemukan lebih baru. Ia dikenal oleh bangsa Yunani, tetapi menjadi tambahan yang signifikan untuk perunggu selama Kekaisaran Romawi.[109]
Kuno dan pasca-klasik[sunting | sunting sumber]


Di Yunani, tembaga dikenal dengan nama chalkos (χαλκός). Ia adalah sumber daya penting bagi orang Romawi, Yunani, dan orang kuno lainnya. Di zaman Romawi, ia dikenal sebagai aes Cyprium, aes menjadi istilah Latin umum untuk paduan tembaga dan Cyprium dari Siprus, tempat banyak tembaga ditambang. Ungkapan itu disederhanakan menjadi cuprum, yang menjadi asal kata copper dalam bahasa Inggris. Afrodit (Venus di Roma) mewakili tembaga dalam mitologi dan alkimia karena keindahannya yang berkilau dan penggunaannya yang kuno dalam pembuatan cermin; Siprus, sumber tembaga, disakralkan oleh sang dewi. Tujuh benda langit yang diketahui orang-orang kuno dikaitkan dengan tujuh logam yang dikenal di zaman kuno, dan Venus dikaitkan dengan tembaga, baik karena hubungannya dengan sang dewi maupun karena Venus adalah benda langit paling terang setelah Matahari dan Bulan sehingga berhubungan dengan logam yang paling berkilau dan diinginkan setelah emas dan perak.[111]
Tembaga pertama kali ditambang di Inggris kuno pada awal 2100 SM. Penambangan di tambang terbesar ini, Great Orme, berlanjut hingga akhir Zaman Perunggu. Penambangan tampaknya sebagian besar terbatas pada bijih supergene, yang lebih mudah dilebur. Deposit tembaga yang kaya di Cornwall tampaknya sebagian besar belum tersentuh, terlepas dari penambangan timah yang ekstensif di wilayah tersebut, karena alasan yang lebih bersifat sosial dan politik daripada teknologi.[112]
Di Amerika Utara, tembaga asli diketahui telah diekstraksi dari situs di Isle Royale dengan alat batu primitif antara tahun 800 dan 1600 M.[113] Penganilan tembaga dilakukan di kota Cahokia di Amerika Utara sekitar tahun 1000–1300 M.[114] Terdapat beberapa pelat tembaga yang sangat indah, yang dikenal sebagai pelat tembaga Mississippi yang ditemukan di Amerika Utara di daerah sekitar Cahokia yang berasal dari periode ini (1000-1300 M).[114] Pelat tembaga ini diperkirakan telah diproduksi di Cahokia sebelum berakhir di tempat lain di Amerika Serikat bagian Barat Tengah dan Tenggara seperti pelat Malden dan pelat Etowah.

Di Amerika Selatan, topeng tembaga bertanggal 1000 SM yang ditemukan di Andes Argentina adalah artefak tembaga tertua yang ditemukan di Andes.[115] Peru telah dianggap sebagai asal metalurgi tembaga awal di Amerika Pra-Kolumbus, tetapi topeng tembaga dari Argentina menunjukkan bahwa lembah Cajon di Andes selatan adalah pusat penting lainnya untuk pengerjaan tembaga awal di Amerika Selatan.[115] Metalurgi tembaga berkembang pesat di Amerika Selatan, khususnya di Peru sekitar tahun 1000 Masehi. Ornamen penguburan tembaga dari abad ke-15 telah ditemukan, tetapi produksi komersial logam tersebut baru dimulai pada awal abad ke-20.[butuh rujukan]
Peran tembaga terhadap budaya sangatlah penting, terutama dalam mata uang. Bangsa Romawi pada abad ke-6 hingga ke-3 SM menggunakan bongkahan tembaga sebagai uang. Pada awalnya, tembaga itu sendiri yang dihargai, namun lambat laun bentuk dan tampilan tembaga menjadi lebih penting. Julius Caesar memiliki koin sendiri yang terbuat dari kuningan, sedangkan koin Octavianus Augustus Caesar terbuat dari paduan Cu-Pb-Sn. Dengan perkiraan hasil tahunan sekitar 15.000 t, aktivitas penambangan dan peleburan tembaga Romawi mencapai skala yang tak tertandingi hingga masa Revolusi Industri; provinsi yang paling banyak ditambang adalah provinsi Hispania, Siprus, dan di Eropa Tengah.[116][117]
Gerbang Kuil Yerusalem menggunakan perunggu Korintus yang diolah melalui pelapisan emas terdeplesi.[butuh klarifikasi][butuh rujukan] Proses ini paling lazim dilakukan di Aleksandria, tempat di mana alkimia dianggap telah dimulai.[118] Di India kuno, tembaga digunakan dalam ilmu kedokteran holistik Ayurweda untuk peralatan bedah dan peralatan medis lainnya. Orang Mesir Kuno (~2400 SM) menggunakan tembaga untuk mensterilkan luka dan air minum, dan kemudian untuk mengobati sakit kepala, luka bakar, dan gatal-gatal.[119]
Modern[sunting | sunting sumber]


Great Copper Mountain adalah sebuah tambang di Falun, Swedia, yang beroperasi dari abad ke-10 hingga 1992. Ia memenuhi dua pertiga konsumsi tembaga Eropa pada abad ke-17 dan membantu mendanai banyak perang Swedia selama waktu itu.[120] Ia disebut sebagai perbendaharaan negara; Swedia memiliki mata uang yang didukung tembaga.[121]

Tembaga digunakan untuk atap,[16] mata uang, dan untuk teknologi fotografi yang dikenal sebagai daguerreotype. Tembaga digunakan dalam patung Renaisans, dan digunakan untuk membangun Patung Liberty; tembaga terus digunakan dalam berbagai jenis konstruksi. Penyepuhan tembaga dan pelapisan tembaga banyak digunakan untuk melindungi lambung kapal di bawah air, sebuah teknik yang dipelopori oleh Angkatan Laut Inggris pada abad ke-18.[122] Norddeutsche Affinerie di Hamburg adalah pabrik penyepuhan modern pertama, mulai berproduksi pada tahun 1876.[123] Ilmuwan Jerman Gottfried Osann menemukan metalurgi bubuk pada tahun 1830 saat menentukan massa atom logam tersebut; sekitar saat itu ditemukan bahwa jumlah dan jenis unsur pemadu (misalnya timah) tembaga akan mempengaruhi nada lonceng.[butuh rujukan]
Selama peningkatan permintaan tembaga pada Zaman Listrik, dari tahun 1880-an hingga Depresi Besar tahun 1930-an, Amerika Serikat memproduksi sepertiga hingga setengah dari tembaga dunia yang baru ditambang.[124] Distrik-distrik penambangan utama meliputi distrik Keweenaw di Michigan utara, terutama endapan tembaga asli, yang dikalahkan oleh endapan sulfida yang luas di Butte, Montana pada akhir tahun 1880-an, yang dikalahkan oleh endapan porfiri di Amerika Serikat Barat Daya, khususnya di Ngarai Bingham, Utah dan Morenci, Arizona. Pengenalan penambangan sekop uap lubang terbuka dan inovasi dalam peleburan, pemurnian, pemusatan pengapungan, dan langkah pemrosesan lainnya menghasilkan produksi massal. Di awal abad ke-20, Arizona menduduki peringkat pertama, diikuti oleh Montana, kemudian Utah dan Michigan.[125]
Peleburan kilat dikembangkan oleh Outokumpu di Finlandia dan pertama kali diterapkan di Harjavalta in 1949; pada tahun 1949; proses hemat energi ini menyumbang 50% dari produksi tembaga primer dunia.[126]
Dewan Antarpemerintah Negara Pengekspor Tembaga, dibentuk pada tahun 1967 oleh Chili, Peru, Zaire, dan Zambia, beroperasi di pasar tembaga seperti yang dilakukan OPEC dalam minyak, meskipun tidak pernah mencapai pengaruh yang sama, terutama karena produsen terbesar kedua, Amerika Serikat, tidak pernah menjadi anggota; organisasi itu dibubarkan pada tahun 1988.[127]
Aplikasi[sunting | sunting sumber]

Aplikasi utama tembaga adalah kabel listrik (60%), atap dan pipa ledeng (20%), dan mesin industri (15%). Tembaga sebagian besar digunakan sebagai logam murni, tetapi jika diperlukan kekerasan yang lebih besar, tembaga dimasukkan ke dalam paduan seperti kuningan dan perunggu (5% dari total penggunaan).[23] Selama lebih dari dua abad, cat tembaga telah digunakan pada lambung kapal untuk mengontrol pertumbuhan tumbuhan dan kerang.[128] Sebagian kecil pasokan tembaga digunakan untuk suplemen nutrisi dan fungisida di bidang pertanian.[70][129] Pemesinan tembaga dimungkinkan, meskipun paduannya lebih disukai karena kemampuan mesinnya yang baik dalam membuat bagian yang rumit.
Kawat dan kabel[sunting | sunting sumber]
Terlepas dari persaingan dari bahan lain, tembaga tetap menjadi konduktor listrik yang disukai di hampir semua kategori kabel listrik kecuali transmisi tenaga listrik di mana aluminium lebih disukai.[130][131] Kawat tembaga digunakan dalam pembangkit daya, transmisi daya, distribusi daya, telekomunikasi, sirkuit elektronika, dan jenis peralatan listrik yang tak terhitung jumlahnya.[132] Kabel listrik adalah pasar terpenting bagi industri tembaga.[133] Ini meliputi kawat daya struktural, kabel distribusi daya, kawat alat, kabel komunikasi, kawat dan kabel otomotif, dan kawat magnet. Kira-kira setengah dari semua tembaga yang ditambang digunakan untuk kawat listrik dan konduktor kabel.[134] Banyak perangkat listrik mengandalkan kawat tembaga karena banyaknya sifat menguntungkan yang melekat, seperti konduktivitas listrik, kekuatan tarik, keuletan, ketahanan rangkak (deformasi), dan ketahanan korosi yang tinggi, ekspansi termal yang rendah, konduktivitas termal yang tinggi, kemudahan penyolderan, kelenturan, dan kemudahan pemasangan.
Untuk waktu yang singkat dari akhir 1960-an hingga akhir 1970-an, kabel tembaga digantikan oleh kabel aluminium di banyak proyek pembangunan perumahan di Amerika. Kabel baru ini terlibat dalam sejumlah kebakaran rumah dan industri akhirnya kembali ke tembaga.[135]
Elektronika dan perangkat terkait[sunting | sunting sumber]

Sirkuit terpadu dan papan sirkuit cetak semakin menonjolkan tembaga sebagai pengganti aluminium karena konduktivitas listriknya yang unggul; pembuang panas dan penukar panas menggunakan tembaga karena sifat pembuangan panasnya yang unggul. Elektromagnet, tabung vakum, tabung sinar katoda, dan magnetron dalam oven gelombang mikro menggunakan tembaga, seperti halnya pandu gelombang untuk radiasi gelombang mikro.[136]
Motor listrik[sunting | sunting sumber]
Konduktivitas tembaga yang unggul akan meningkatkan efisiensi motor listrik.[137] Hal ini penting karena motor dan sistem yang digerakkan motor menyumbang 43%–46% dari seluruh konsumsi listrik global dan 69% dari seluruh listrik yang digunakan oleh industri.[138] Meningkatkan massa dan penampang lintang tembaga dalam koil akan meningkatkan efisiensi motor. Rotor motor tembaga, teknologi baru yang dirancang untuk aplikasi motor di mana penghematan energi adalah tujuan desain utama,[139][140] memungkinkan motor induksi serba guna untuk memenuhi dan melampaui standar efisiensi premium Asosiasi Produsen Listrik Nasional (NEMA).[141]
Produksi energi terbarukan[sunting | sunting sumber]
Sumber energi terbarukan seperti matahari, angin, pasang surut, air, biomassa, dan panas bumi telah menjadi sektor penting dalam pasar energi.[142][143] Pesatnya pertumbuhan sumber-sumber ini di abad ke-21 telah didorong oleh meningkatnya biaya bahan bakar fosil serta masalah dampak lingkungan yang secara signifikan menurunkan penggunaannya.
Tembaga memainkan peran penting dalam sistem energi terbarukan ini.[144][145][146][147][148] Penggunaan tembaga memiliki rata-rata hingga lima kali lebih banyak dalam sistem energi terbarukan daripada pembangkit listrik tradisional, seperti bahan bakar fosil dan pembangkit listrik tenaga nuklir.[149] Karena tembaga adalah konduktor termal dan listrik yang sangat baik di antara logam teknik (kedua setelah perak),[150] sistem kelistrikan yang memanfaatkan tembaga dapat menghasilkan dan mentransmisikan energi dengan efisiensi tinggi dan dengan dampak lingkungan yang minimal.
Saat memilih konduktor listrik, perencana dan insinyur fasilitas memperhitungkan biaya investasi modal bahan terhadap penghematan operasional karena efisiensi energi listrik selama masa manfaatnya, ditambah biaya pemeliharaan. Tembaga sering berhasil dengan baik dalam perhitungan ini. Faktor yang disebut "intensitas penggunaan tembaga", adalah ukuran kuantitas tembaga yang diperlukan untuk memasang satu megawatt kapasitas pembangkit listrik baru.

Saat merencanakan fasilitas daya terbarukan yang baru, para insinyur dan penentu produk berupaya menghindari kekurangan pasokan bahan pilihan. Menurut Survei Geologi Amerika Serikat, cadangan tembaga di dalam tanah telah meningkat lebih dari 700% sejak tahun 1950, dari hampir 100 juta ton menjadi 720 juta ton pada tahun 2017, terlepas dari fakta bahwa penggunaan olahan dunia meningkat lebih dari tiga kali lipat dalam 50 tahun terakhir.[151] Sumber daya tembaga diperkirakan melebihi 5 miliar ton.[152][153]
Memperkuat pasokan dari ekstraksi tembaga adalah fakta bahwa lebih dari 30 persen tembaga yang dipasang selama dekade terakhir berasal dari sumber daur ulang.[154] Laju daur ulangnya lebih tinggi daripada logam lainnya.[155]
Arsitektur[sunting | sunting sumber]



Tembaga telah digunakan sejak zaman kuno sebagai bahan arsitektur yang tahan lama, tahan korosi, dan tahan cuaca.[156][157][158][159] Atap, talang air hujan, talang tegak, kubah, puncak menara, dan pintu telah dibuat dari tembaga selama ratusan atau ribuan tahun. Penggunaan arsitektur tembaga telah diperluas di zaman modern untuk mencakup pelapis dinding interior dan eksterior, sambungan ekspansi bangunan, pelindung frekuensi radio, dan produk dalam ruangan antimikroba dan dekoratif seperti pegangan tangan yang menarik, perlengkapan kamar mandi, dan meja dapur. Beberapa manfaat penting tembaga lainnya sebagai bahan arsitektur meliputi pergerakan termal yang rendah, ringan, proteksi petir, dan dapat didaur ulang
Patina hijau alami yang khas dari logam ini telah lama didambakan oleh para arsitek dan desainer. Patina akhir adalah lapisan yang sangat tahan lama dan sangat tahan terhadap korosi atmosfer, sehingga melindungi logam di bawahnya dari pelapukan lebih lanjut.[160][161][162] Ia dapat berupa campuran senyawa karbonat dan sulfat dalam berbagai jumlah, tergantung pada kondisi lingkungan seperti hujan asam yang mengandung belerang.[163][164][165][166] Tembaga arsitektur dan paduannya juga dapat 'diselesaikan' untuk mendapatkan tampilan, rasa, atau warna tertentu. Penyelesaian ini meliputi perawatan permukaan mekanis, pewarnaan kimia, dan pelapisan.[167]
Tembaga memiliki sifat mematri dan menyolder yang sangat baik dan dapat dilas; hasil terbaik diperoleh dengan las busur logam gas.[168]
Perlawanan terhadap penumpukan biologis[sunting | sunting sumber]
Tembaga bersifat biostatik, artinya bakteri dan banyak bentuk kehidupan lainnya tidak akan tumbuh di atasnya. Karena alasan ini, ia telah lama digunakan untuk melapisi bagian kapal sebagai perlindungan dari teritip dan remis. Ia awalnya digunakan dalam bentuk murni, tetapi telah digantikan oleh logam Muntz dan cat berbasis tembaga. Demikian pula, seperti yang dibahas dalam paduan tembaga dalam budi daya perairan, paduan tembaga telah menjadi bahan jaring yang penting dalam industri budi daya perairan karena mereka bersifat antimikroba dan mencegah penumpukan biologis, bahkan dalam kondisi ekstrem[169] serta memiliki sifat struktural dan ketahanan korosi yang kuat[170] di lingkungan laut.
Antimikroba[sunting | sunting sumber]
Permukaan sentuh paduan tembaga memiliki sifat alami yang menghancurkan berbagai mikroorganisme (misalnya, E. coli O157:H7, Staphylococcus aureus resisten-metisilin (MRSA), Staphylococcus, Clostridium difficile, virus influenza A, adenovirus, SARS-Cov-2, dan jamur).[171][172] Orang India telah menggunakan bejana tembaga sejak zaman kuno untuk menyimpan air, bahkan sebelum ilmu pengetahuan modern menyadari sifat antimikrobanya.[173] Beberapa paduan tembaga terbukti membunuh lebih dari 99,9% bakteri penyebab penyakit hanya dalam waktu dua jam bila dibersihkan secara teratur.[174] Badan Perlindungan Lingkungan Amerika Serikat (EPA) telah menyetujui pendaftaran paduan tembaga ini sebagai "bahan antimikroba dengan manfaat kesehatan masyarakat";[174] persetujuan itu memungkinkan produsen untuk membuat klaim hukum atas manfaat kesehatan masyarakat dari produk yang terbuat dari paduan terdaftar. Selain itu, EPA telah menyetujui daftar panjang produk tembaga antimikroba yang terbuat dari paduan ini, seperti pegangan tempat tidur, pegangan tangan, meja di atas tempat tidur, wastafel, keran, gagang pintu, perangkat keras toilet, papan tombol komputer, peralatan pusat kebugaran, dan pegangan keranjang belanja (untuk daftar lengkap, lihat: Permukaan sentuh paduan tembaga antimikroba#Produk tembaga antimikroba). Kenop pintu tembaga digunakan oleh rumah sakit untuk mengurangi perpindahan penyakit, dan penyakit Legionella ditekan oleh pipa tembaga dalam sistem perpipaan.[175] Produk paduan tembaga antimikroba sekarang dipasang di fasilitas kesehatan di Britania Raya, Irlandia, Jepang, Korea, Prancis, Denmark, dan Brasil, serta diminta di Amerika Serikat,[176] dan di sistem transit kereta bawah tanah di Santiago, Chili, di mana pegangan tangan paduan tembaga-seng dipasang di sekitar 30 stasiun antara tahun 2011 dan 2014.[177][178][179] Serat tekstil dapat dicampur dengan tembaga untuk membuat kain pelindung antimikroba.[180][tepercaya?]
Investasi spekulatif[sunting | sunting sumber]
Tembaga dapat digunakan sebagai investasi spekulatif karena perkiraan peningkatan penggunaannya dari pertumbuhan infrastruktur di seluruh dunia, dan peran pentingnya dalam memproduksi turbin angin, panel surya, dan sumber energi terbarukan lainnya.[181][182] Alasan lain yang memprediksi peningkatan permintaan adalah fakta bahwa mobil listrik rata-rata mengandung tembaga 3,6 kali lebih banyak daripada mobil konvensional, meskipun pengaruh mobil listrik terhadap permintaan tembaga masih diperdebatkan.[183][184] Beberapa orang berinvestasi dalam tembaga melalui saham pertambangan tembaga, ETF, dan kontrak berjangka. Yang lainnya menyimpan tembaga fisik dalam bentuk batangan atau bulatan tembaga meskipun keduanya cenderung memiliki harga premium yang lebih tinggi dibandingkan dengan logam mulia.[185] Mereka yang ingin menghindari harga premium dari bulion tembaga dapat menyimpan kawat tembaga dan tabung tembaga tua, atau penny Amerika yang dibuat sebelum tahun 1982 sebagai alternatifnya.[186]
Pengobatan tradisional[sunting | sunting sumber]
Tembaga umumnya digunakan dalam perhiasan, dan menurut beberapa cerita rakyat, gelang tembaga dapat meredakan gejala artritis.[187] Dalam satu percobaan untuk osteoartritis dan satu percobaan untuk artritis reumatoid, tidak ada perbedaan yang ditemukan antara gelang tembaga dan gelang (non-tembaga) kontrol.[188][189] Tidak ada bukti yang menunjukkan bahwa tembaga dapat diserap melalui kulit. Jika iya, maka ia dapat menyebabkan keracunan tembaga.[190]
Pakaian kompresi[sunting | sunting sumber]
Baru-baru ini, beberapa pakaian kompresi dengan jalinan tembaga telah dipasarkan dengan klaim kesehatan yang mirip dengan klaim pengobatan tradisional. Karena pakaian kompresi adalah pengobatan yang valid untuk beberapa penyakit, pakaian tersebut mungkin memiliki manfaat itu, tetapi tembaga tambahan mungkin tidak memiliki manfaat selain efek plasebo.[191]
Degradasi[sunting | sunting sumber]
Chromobacterium violaceum dan Pseudomonas fluorescens dapat memobilisasi tembaga padat sebagai senyawa sianida.[192] Jamur mikoriza erikoid yang berasosiasi dengan Calluna, Erica dan Vaccinium dapat tumbuh di tanah logam yang mengandung tembaga.[192] Jamur ektomikoriza Suillus luteus melindungi pohon pinus muda dari toksisitas tembaga. Sampel jamur Aspergillus niger ditemukan tumbuh dari larutan tambang emas dan ditemukan mengandung kompleks siano dari beberapa logam seperti emas, perak, tembaga, besi, dan seng. Jamur tersebut juga berperan dalam pelarutan sulfida logam berat.[193]
Peran biologis[sunting | sunting sumber]

Biokimia[sunting | sunting sumber]
Protein tembaga memiliki peran yang beragam dalam transpor elektron dan transportasi oksigen biologis, proses yang memanfaatkan interkonversi mudah dari Cu(I) dan Cu(II).[194] Tembaga sangat penting dalam respirasi aerobik semua eukariota. Pada mitokondria, ia ditemukan dalam sitokrom c oksidase, yang merupakan protein terakhir dalam fosforilasi oksidatif. Sitokrom c oksidase adalah protein yang mengikat O2 antara tembaga dan besi; protein tersebut mentransfer 8 elektron ke molekul O2 untuk mereduksinya menjadi dua molekul air. Tembaga juga ditemukan di banyak superoksida dismutase, protein yang mengatalisis dekomposisi superoksida dengan mengubahnya (melalui disproporsionasi) menjadi oksigen dan hidrogen peroksida:
- Cu2+-SOD + O2− → Cu+-SOD + O2 (reduksi tembaga; oksidasi superoksida)
- Cu+-SOD + O2− + 2H+ → Cu2+-SOD + H2O2 (oksidasi tembaga; reduksi superoksida)
Protein hemosianin adalah pembawa oksigen pada sebagian besar moluska dan beberapa artropoda seperti kepiting tapal kuda (Limulus polyphemus).[195] Karena hemosianin berwarna biru, organisme ini memiliki darah biru alih-alih darah merah hemoglobin berbasis besi. Yang terkait dengan hemosianin secara struktural adalah lakase dan tirosinase. Alih-alih mengikat oksigen secara reversibel, protein ini menghidroksilat substrat, diilustrasikan oleh perannya dalam pembentukan lakuer.[196] Peran biologis tembaga dimulai dengan munculnya oksigen di atmosfer bumi.[197] Beberapa protein tembaga, seperti "protein tembaga biru", tidak berinteraksi langsung dengan substrat; karenanya mereka bukan enzim. Protein ini menyampaikan elektron melalui proses yang disebut transfer elektron.[196]
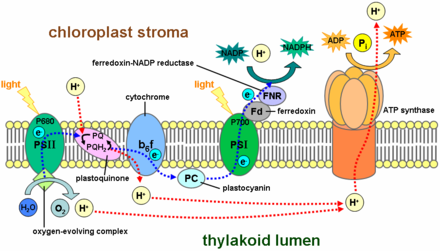
Sebuah pusat tembaga berinti 4 yang unik telah ditemukan dalam dinitrogen monoksida reduktase.[198]
Senyawa kimia yang dikembangkan untuk pengobatan penyakit Wilson telah diteliti untuk digunakan dalam terapi kanker.[199]
Nutrisi[sunting | sunting sumber]
Tembaga adalah sebuah unsur renik penting pada tumbuhan dan hewan, tetapi tidak semua mikroorganisme. Tubuh manusia mengandung tembaga pada tingkat sekitar 1,4 hingga 2,1 mg per kg massa tubuh.[200]
Penyerapan[sunting | sunting sumber]
Tembaga diserap di usus, kemudian diangkut ke hati dengan terikat albumin.[201] Setelah diproses di hati, tembaga didistribusikan ke jaringan lain pada fase kedua, yang melibatkan protein seruloplasmin, yang membawa sebagian besar tembaga dalam darah. Seruloplasmin juga membawa tembaga yang diekskresikan dalam susu, dan diserap dengan baik sebagai sumber tembaga.[202] Tembaga dalam tubuh biasanya mengalami sirkulasi enterohepatik (sekitar 5 mg per hari, vs. sekitar 1 mg per hari yang diserap dalam makanan dan dikeluarkan dari tubuh), dan tubuh dapat mengeluarkan beberapa kelebihan tembaga, jika diperlukan, melalui empedu, yang membawa beberapa tembaga keluar dari hati yang tidak diserap kembali oleh usus.[203][204]
Rekomendasi diet[sunting | sunting sumber]
Institut Kedokteran A.S. (IOM) memperbarui Kebutuhan Perkiraan Rata-rata (EAR) dan Angka Kecukupan Gizi (AKG) untuk tembaga pada tahun 2001. Jika tidak ada informasi yang cukup untuk menetapkan EAR dan AKG, digunakan perkiraan Asupan Adekuat (AI) sebagai gantinya. AI untuk tembaga adalah: 200 μg tembaga untuk laki-laki dan perempuan berusia 0–6 bulan, dan 220 μg tembaga untuk laki-laki dan perempuan berusia 7–12 bulan. Untuk kedua jenis kelamin, AKG untuk tembaga adalah: 340 μg tembaga untuk usia 1–3 tahun, 440 μg tembaga untuk usia 4–8 tahun, 700 μg tembaga untuk usia 9–13 tahun, 890 μg tembaga untuk usia 14–18 tahun, dan 900 μg tembaga untuk usia 19 tahun ke atas. Untuk ibu hamil, 1.000 μg. Untuk ibu menyusui, 1.300 μg.[205] Mengenai keamanan, IOM juga menetapkan Batas Atas Asupan (UL) yang dapat ditoleransi untuk vitamin dan mineral bila bukti cukup. Dalam kasus tembaga, UL ditetapkan pada 10 mg/hari. Secara kolektif EAR, AKG, AI, dan UL disebut sebagai Asupan Referensi Diet.[206]
Otoritas Keamanan Makanan Eropa (EFSA) menyebut kumpulan informasi kolektif tersebut sebagai Nilai Referensi Diet, dengan Asupan Referensi Populasi (PRI) alih-alih AKG, dan Kebutuhan Rata-rata alih-alih EAR. AI dan UL didefinisikan sama seperti di Amerika Serikat. Untuk wanita dan pria berusia 18 tahun ke atas, AI ditetapkan masing-masing sebesar 1,3 dan 1,6 mg/hari. AI untuk ibu hamil dan menyusui adalah 1,5 mg/hari. Untuk anak usia 1–17 tahun, AI meningkat seiring bertambahnya usia dari 0,7 menjadi 1,3 mg/hari. AI ini lebih tinggi dari AKG Amerika Serikat.[207] Otoritas Keamanan Makanan Eropa meninjau pertanyaan keamanan yang sama dan menetapkan UL pada 5 mg/hari, yang merupakan setengah dari nilai Amerika Serikat.[208]
Untuk tujuan pelabelan makanan dan suplemen makanan A.S., jumlah dalam satu porsi dinyatakan sebagai persentase dari Nilai Harian (%DV). Untuk tujuan pelabelan tembaga, 100% Nilai Harian adalah 2,0 mg, tetapi pada 27 Mei 2016 direvisi menjadi 0,9 mg agar sesuai dengan AKG.[209][210] Tabel nilai harian dewasa lama dan baru disediakan di Asupan Harian Referensi.
Kekurangan tembaga[sunting | sunting sumber]
Karena perannya dalam memfasilitasi penyerapan zat besi, kekurangan tembaga dapat menghasilkan gejala seperti-anemia, neutropenia, kelainan tulang, hipopigmentasi, gangguan pertumbuhan, peningkatan insiden infeksi, osteoporosis, hipertiroidisme, dan kelainan metabolisme glukosa dan kolesterol. Sebaliknya, penyakit Wilson menyebabkan penumpukan tembaga di jaringan tubuh.
Defisiensi yang parah dapat ditemukan dengan menguji kadar tembaga plasma atau serum yang rendah, seruloplasmin yang rendah, dan kadar superoksida dismutase sel darah merah yang rendah; mereka tidak sensitif terhadap status tembaga marjinal. "Aktivitas sitokrom c oksidase leukosit dan trombosit" telah dinyatakan sebagai faktor lain dalam kekurangan tembaga, tetapi hasilnya belum dikonfirmasi melalui replikasi.[211]
Toksisitas[sunting | sunting sumber]
Jumlah gram dari berbagai garam tembaga telah diambil dalam upaya bunuh diri dan menghasilkan toksisitas tembaga akut pada manusia, kemungkinan karena siklus redoks dan pembentukan spesies oksigen reaktif yang merusak DNA.[212][213] Jumlah garam tembaga yang sesuai (30 mg/kg) bersifat racun bagi hewan.[214] Nilai makanan minimum untuk pertumbuhan yang sehat pada kelinci telah dilaporkan setidaknya 3 ppm dalam makanan.[215] Namun, konsentrasi tembaga yang lebih tinggi (100 ppm, 200 ppm, atau 500 ppm) dalam makanan kelinci dapat memengaruhi efisiensi konversi pakan, tingkat pertumbuhan, dan persentase ganti karkas.[216]
Toksisitas tembaga kronis biasanya tidak terjadi pada manusia karena sistem transportasi yang mengatur penyerapan dan ekskresi. Mutasi resesif autosomal pada protein transpor tembaga dapat menonaktifkan sistem ini, menyebabkan penyakit Wilson dengan akumulasi tembaga dan sirosis hati pada orang yang mewarisi dua gen yang rusak.[200]
Peningkatan kadar tembaga juga dikaitkan dengan memburuknya gejala penyakit Alzheimer.[217][218]
Paparan manusia[sunting | sunting sumber]
Di Amerika Serikat, Administrasi Keselamatan dan Kesehatan Kerja (OSHA) telah menetapkan batas paparan yang diizinkan (PEL) untuk debu dan asap tembaga di tempat kerja sebagai rata-rata tertimbang waktu (TWA) sebesar 1 mg/m3.[219] Institut Nasional untuk Keselamatan dan Kesehatan Kerja (NIOSH) telah menetapkan batas paparan yang direkomendasikan (REL) sebesar 1 mg/m3, rata-rata tertimbang waktu. Nilai IDLH (langsung berbahaya bagi kehidupan dan kesehatan) tembaga adalah 100 mg/m3.[220]
Tembaga adalah komponen dalam asap tembakau.[221][222] Tumbuhan tembakau dapat dengan mudah menyerap dan mengakumulasi logam berat, seperti tembaga dari tanah di sekitarnya ke dalam daunnya. Ia mudah diserap ke dalam tubuh pengguna setelah menghirup asap.[223] Implikasi kesehatannya tidak jelas.[224]
Lihat pula[sunting | sunting sumber]
- Tembaga dalam energi terbarukan
- Nanopartikel tembaga
- Korosi erosi tabung air tembaga
- Daftar negara menurut produksi tembaga
- Pencurian logam
- Anaconda Copper
- Antofagasta PLC
- Codelco
- Tambang El Boleo
- Tambang Grasberg
Referensi[sunting | sunting sumber]
- ^ (Indonesia) "Tembaga". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Moret, Marc-Etienne; Zhang, Limei; Peters, Jonas C. (2013). "A Polar Copper–Boron One-Electron σ-Bond". J. Am. Chem. Soc. 135 (10): 3792–3795. doi:10.1021/ja4006578. PMID 23418750.
- ^ Lide, D. R., ed. (2005). "Magnetic susceptibility of the elements and inorganic compounds". CRC Handbook of Chemistry and Physics (PDF) (edisi ke-86th). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5. Diarsipkan dari versi asli (PDF) tanggal 19 Juli 2022.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ Templat:Cite EB15
- ^ "Copper". Merriam-Webster Dictionary. 2018. Diakses tanggal 3 Juli 2023.
- ^ Johnson, MD PhD, Larry E., ed. (2008). "Copper". Merck Manual Home Health Handbook. Merck Sharp & Dohme Corp., a subsidiary of Merck & Co., Inc. Diarsipkan dari versi asli tanggal 7 Maret 2016. Diakses tanggal 3 Juli 2023.
- ^ "Copper in human health".
- ^ a b Trigg, George L.; Immergut, Edmund H. (1992). Encyclopedia of Applied Physics. 4: Combustion to Diamagnetism. VCH. hlm. 267–272. ISBN 978-3-527-28126-8. Diakses tanggal 3 Juli 2023.
- ^ Smith, William F.; Hashemi, Javad (2003). Foundations of Materials Science and Engineering. McGraw-Hill Professional. hlm. 223. ISBN 978-0-07-292194-6.
- ^ a b c Hammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics (edisi ke-81). CRC Press. ISBN 978-0-8493-0485-9.
- ^ Resistance Welding Manufacturing Alliance (2003). Resistance Welding Manual (edisi ke-4). Resistance Welding Manufacturing Alliance. hlm. 18–12. ISBN 978-0-9624382-0-2.
- ^ Chambers, William; Chambers, Robert (1884). Chambers's Information for the People. L (edisi ke-5). W. & R. Chambers. hlm. 312. ISBN 978-0-665-46912-1.
- ^ Ramachandran, Harishankar (14 Maret 2007). "Why is Copper Red?" (PDF). IIT Madras. Diakses tanggal 3 Juli 2023.
- ^ "Galvanic Corrosion". Corrosion Doctors. Diakses tanggal 3 Juli 2023.
- ^ a b Grieken, Rene van; Janssens, Koen (2005). Cultural Heritage Conservation and Environmental Impact Assessment by Non-Destructive Testing and Micro-Analysis (dalam bahasa Inggris). CRC Press. hlm. 197. ISBN 978-0-203-97078-2.
- ^ "Copper.org: Education: Statue of Liberty: Reclothing the First Lady of Metals – Repair Concerns". Copper.org. Diakses tanggal 3 Juli 2023.
- ^ Rickett, B. I.; Payer, J. H. (1995). "Composition of Copper Tarnish Products Formed in Moist Air with Trace Levels of Pollutant Gas: Hydrogen Sulfide and Sulfur Dioxide/Hydrogen Sulfide". Journal of the Electrochemical Society. 142 (11): 3723–3728. Bibcode:1995JElS..142.3723R. doi:10.1149/1.2048404.
- ^ a b Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ "Interactive Chart of Nuclides". National Nuclear Data Center. Diarsipkan dari versi asli tanggal 25 Agustus 2013. Diakses tanggal 3 Juli 2023.
- ^ Okazawad, Hidehiko; Yonekura, Yoshiharu; Fujibayashi, Yasuhisa; Nishizawa, Sadahiko; Magata, Yasuhiro; Ishizu, Koichi; Tanaka, Fumiko; Tsuchida, Tatsuro; Tamaki, Nagara; Konishi, Junji (1994). "Clinical Application and Quantitative Evaluation of Generator-Produced Copper-62-PTSM as a Brain Perfusion Tracer for PET" (PDF). Journal of Nuclear Medicine. 35 (12): 1910–1915. PMID 7989968.
- ^ Romano, Donatella; Matteucci, Fransesca (2007). "Contrasting copper evolution in ω Centauri and the Milky Way". Monthly Notices of the Royal Astronomical Society: Letters. 378 (1): L59–L63. arXiv:astro-ph/0703760
 . Bibcode:2007MNRAS.378L..59R. doi:10.1111/j.1745-3933.2007.00320.x.
. Bibcode:2007MNRAS.378L..59R. doi:10.1111/j.1745-3933.2007.00320.x.
- ^ a b c d Emsley, John (2003). Nature's building blocks: an A–Z guide to the elements
 . Oxford University Press. hlm. 121–125. ISBN 978-0-19-850340-8. Diakses tanggal 3 Juli 2023.
. Oxford University Press. hlm. 121–125. ISBN 978-0-19-850340-8. Diakses tanggal 3 Juli 2023.
- ^ Rickwood, P. C. (1981). "The largest crystals" (PDF). American Mineralogist. 66: 885.
- ^ Emsley, John (2003). Nature's building blocks: an A–Z guide to the elements
 . Oxford University Press. hlm. 124, 231, 449, 503. ISBN 978-0-19-850340-8. Diakses tanggal 3 Juli 2023.
. Oxford University Press. hlm. 124, 231, 449, 503. ISBN 978-0-19-850340-8. Diakses tanggal 3 Juli 2023.
- ^ Rieuwerts, John (2015). The Elements of Environmental Pollution. London and New York: Earthscan Routledge. hlm. 207. ISBN 978-0-415-85919-6. OCLC 886492996.
- ^ Randazzo, Ryan (19 Juni 2011). "A new method to harvest copper". Azcentral.com. Diakses tanggal 3 Juli 2023.
- ^ Gordon, R.B.; Bertram, M.; Graedel, T.E. (2006). "Metal stocks and sustainability". Proceedings of the National Academy of Sciences. 103 (5): 1209–1214. Bibcode:2006PNAS..103.1209G. doi:10.1073/pnas.0509498103
 . PMC 1360560
. PMC 1360560  . PMID 16432205.
. PMID 16432205.
- ^ Beaudoin, Yannick C.; Baker, Elaine (Desember 2013). Deep Sea Minerals: Manganese Nodules, a physical, biological, environmental and technical review. Secretariat of the Pacific Community. hlm. 7–18. ISBN 978-82-7701-119-6. Diakses tanggal 3 Juli 2023.
- ^ a b Leonard, Andrew (3 Maret 2006). "Peak copper?". Salon (dalam bahasa Inggris). Diakses tanggal 3 Juli 2023.
- ^ Brown, Lester (2006). Plan B 2.0: Rescuing a Planet Under Stress and a Civilization in Trouble
 . New York: W.W. Norton. hlm. 109. ISBN 978-0-393-32831-8.
. New York: W.W. Norton. hlm. 109. ISBN 978-0-393-32831-8.
- ^ Schmitz, Christopher (1986). "The Rise of Big Business in the World, Copper Industry 1870–1930". Economic History Review. 2. 39 (3): 392–410. doi:10.1111/j.1468-0289.1986.tb00411.x. JSTOR 2596347.
- ^ "Copper Trends: Live Metal Spot Prices". Diarsipkan dari versi asli tanggal 1 Mei 2012.
- ^ Ackerman, R. (2 April 2009). "A Bottom in Sight For Copper". Forbes. Diarsipkan dari versi asli tanggal 8 Desember 2012.
- ^ Employment Appeal Tribunal, AEI Cables Ltd. v GMB and others, 5 April 2013. Diakses tanggal 3 Juli 2023.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ Su, Kun; Ma, Xiaodong; Parianos, John; Zhao, Baojun (2020). "Thermodynamic and Experimental Study on Efficient Extraction of Valuable Metals from Polymetallic Nodules". Minerals. 10 (4): 360. Bibcode:2020Mine...10..360S. doi:10.3390/min10040360
 .
.
- ^ International Seabed Authority. "Polymetallic Nodules" (PDF). International Seabed Authority. Diakses tanggal 3 Juli 2023.
- ^ Watling, H.R. (2006). "The bioleaching of sulphide minerals with emphasis on copper sulphides – A review" (PDF). Hydrometallurgy. 84 (1): 81–108. Bibcode:2006HydMe..84...81W. doi:10.1016/j.hydromet.2006.05.001. Diarsipkan dari versi asli (PDF) tanggal 18 Agustus 2011.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 1174–1175, ISBN 0-7506-3365-4
- ^ Samans, Carl (1949). Engineering metals and their alloys. New York: Macmillan. OCLC 716492542.
- ^ Bahadir, Ali Mufit; Duca, Gheorghe (2009). The Role of Ecological Chemistry in Pollution Research and Sustainable Development (dalam bahasa Inggris). Springer. ISBN 978-90-481-2903-4.
- ^ Green, Dan (2016). The Periodic Table in Minutes (dalam bahasa Inggris). Quercus. ISBN 978-1-68144-329-4.
- ^ "International Copper Association". Diarsipkan dari versi asli tanggal 5 Maret 2012. Diakses tanggal 3 Juli 2023.
- ^ "Overview of Recycled Copper" Copper.org. (25 Agustus 2010). Diakses tanggal 3 Juli 2023.
- ^ "Dime". US Mint. Diakses tanggal 3 Juli 2023.[pranala nonaktif permanen]
- ^ "Pride and skill – the 10-cent coin". Royal Canadian Mint. Diakses tanggal 3 Juli 2023.
- ^ "Gold Jewellery Alloys". World Gold Council. Diarsipkan dari versi asli tanggal 14 April 2009. Diakses tanggal 3 Juli 2023.
- ^ Balver Zinn Solder Sn97Cu3 Diarsipkan 7 Juli 2011 di Wayback Machine.. (PDF) . balverzinn.com. Diakses tanggal 3 Juli 2023.
- ^ Deane, D. V. "Modern Coinage Systems" (PDF). British Numismatic Society. Diakses tanggal 3 Juli 2023.
- ^ "What is 90% Silver?". American Precious Metals Exchange (APMEX). Diarsipkan dari versi asli tanggal 28 Juli 2020. Diakses tanggal 3 Juli 2023.
- ^ Corrosion Tests and Standards (dalam bahasa Inggris). ASTM International. 2005. hlm. 368.
- ^ Oguchi, Hachiro (1983). "Japanese Shakudō: its history, properties and production from gold-containing alloys". Gold Bulletin. 16 (4): 125–132. doi:10.1007/BF03214636
 .
.
- ^ Brass and Bronze Alloys, diarsipkan dari versi asli tanggal 25 Agustus 2009, diakses tanggal 3 Juli 2023 .
- ^ UNS C83400, diakses tanggal 3 Juli 2023.
- ^ UNS C86100, diakses tanggal 3 Juli 2023.
- ^ UNS C95410, diakses tanggal 3 Juli 2023.
- ^ UNS C95600, diakses tanggal 3 Juli 2023.
- ^ UNS C95700, diakses tanggal 3 Juli 2023.
- ^ UNS C87200, diakses tanggal 3 Juli 2023.
- ^ UNS C87400, diakses tanggal 3 Juli 2023.
- ^ UNS C87500, diakses tanggal 3 Juli 2023.
- ^ UNS C87600, diakses tanggal 3 Juli 2023.
- ^ UNS C87800, diakses tanggal 3 Juli 2023.
- ^ UNS C87900, diakses tanggal 3 Juli 2023.
- ^ a b c Holleman, A.F.; Wiberg, N. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 978-0-12-352651-9.
- ^ Trammell, Rachel; Rajabimoghadam, Khashayar; Garcia-Bosch, Isaac (30 Januari 2019). "Copper-Promoted Functionalization of Organic Molecules: from Biologically Relevant Cu/O2 Model Systems to Organometallic Transformations". Chemical Reviews. 119 (4): 2954–3031. doi:10.1021/acs.chemrev.8b00368. PMC 6571019
 . PMID 30698952.
. PMID 30698952.
- ^ Wells, A. F. (1984). Structural Inorganic Chemistry (edisi ke-5). Oxford University Press. hlm. 1142–1145. ISBN 978-0-19-965763-6.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 1181, ISBN 0-7506-3365-4
- ^ a b Wiley-Vch (2 April 2007). "Nonsystematic (Contact) Fungicides". Ullmann's Agrochemicals. hlm. 623. ISBN 978-3-527-31604-5.
- ^ Ralph L. Shriner, Christine K.F. Hermann, Terence C. Morrill, David Y. Curtin, Reynold C. Fuson "The Systematic Identification of Organic Compounds" edisi ke-8, J. Wiley, Hoboken. ISBN 0-471-21503-1
- ^ Saalwächter, Kay; Burchard, Walther; Klüfers, Peter; Kettenbach, G.; Mayer, Peter; Klemm, Dieter; Dugarmaa, Saran (2000). "Cellulose Solutions in Water Containing Metal Complexes". Macromolecules. 33 (11): 4094–4107. Bibcode:2000MaMol..33.4094S. CiteSeerX 10.1.1.951.5219
 . doi:10.1021/ma991893m.
. doi:10.1021/ma991893m.
- ^ Deodhar, S., Huckaby, J., Delahoussaye, M. dan DeCoster, M.A., Agustus 2014. High-aspect ratio bio-metallic nanocomposites for cellular interactions. In IOP Conference Series: Materials Science and Engineering (Vol. 64, No. 1, hlm. 012014). https://iopscience.iop.org/article/10.1088/1757-899X/64/1/012014/meta.
- ^ Kelly, K.C., Wasserman, J.R., Deodhar, S., Huckaby, J. dan DeCoster, M.A., 2015. Generation of scalable, metallic high-aspect ratio nanocomposites in a biological liquid medium. Journal of Visualized Experiments, (101), hlm.e52901. https://www.jove.com/t/52901/generation-scalable-metallic-high-aspect-ratio-nanocomposites.
- ^ Karan, A., Darder, M., Kansakar, U., Norcross, Z. dan DeCoster, M.A., 2018. Integration of a Copper-Containing Biohybrid (CuHARS) with Cellulose for Subsequent Degradation and Biomedical Control. International journal of environmental research and public health, 15(5), hlm.844. https://www.mdpi.com/1660-4601/15/5/844
- ^ Birk, James (3 April 2018). "Characteristic Reactions of Iron (Fe³⁺)". LibreText Chemistry. LibreText. Diakses tanggal 3 Juli 2023.
- ^ "Modern Organocopper Chemistry" Norbert Krause, Ed., Wiley-VCH, Weinheim, 2002. ISBN 978-3-527-29773-3.
- ^ Berná, José; Goldup, Stephen; Lee, Ai-Lan; Leigh, David; Symes, Mark; Teobaldi, Gilberto; Zerbetto, Fransesco (26 Mei 2008). "Cadiot–Chodkiewicz Active Template Synthesis of Rotaxanes and Switchable Molecular Shuttles with Weak Intercomponent Interactions". Angewandte Chemie. 120 (23): 4464–4468. Bibcode:2008AngCh.120.4464B. doi:10.1002/ange.200800891.
- ^ Rafael Chinchilla; Carmen Nájera (2007). "The Sonogashira Reaction: A Booming Methodology in Synthetic Organic Chemistry". Chemical Reviews. 107 (3): 874–922. doi:10.1021/cr050992x. PMID 17305399.
- ^ "An Addition of an Ethylcopper Complex to 1-Octyne: (E)-5-Ethyl-1,4-Undecadiene" (PDF). Organic Syntheses. 64: 1. 1986. doi:10.15227/orgsyn.064.0001. Diarsipkan dari versi asli (PDF) tanggal 19 Juni 2012.
- ^ Kharasch, M.S.; Tawney, P.O. (1941). "Factors Determining the Course and Mechanisms of Grignard Reactions. II. The Effect of Metallic Compounds on the Reaction between Isophorone and Methylmagnesium Bromide". Journal of the American Chemical Society. 63 (9): 2308–2316. doi:10.1021/ja01854a005.
- ^ Imai, Sadako; Fujisawa, Kiyoshi; Kobayashi, Takako; Shirasawa, Nobuhiko; Fujii, Hiroshi; Yoshimura, Tetsuhiko; Kitajima, Nobumasa; Moro-oka, Yoshihiko (1998). "63Cu NMR Study of Copper(I) Carbonyl Complexes with Various Hydrotris(pyrazolyl)borates: Correlation between 63Cu Chemical Shifts and CO Stretching Vibrations". Inorganic Chemistry. 37 (12): 3066–3070. doi:10.1021/ic970138r.
- ^ G. Brauer, ed. (1963). "Potassium Cuprate (III)". Handbook of Preparative Inorganic Chemistry. 1 (edisi ke-2). NY: Academic Press. hlm. 1015.
- ^ Schwesinger, Reinhard; Link, Reinhard; Wenzl, Peter; Kossek, Sebastian (2006). "Anhydrous phosphazenium fluorides as sources for extremely reactive fluoride ions in solution". Chemistry: A European Journal. 12 (2): 438–45. doi:10.1002/chem.200500838. PMID 16196062.
- ^ Lewis, E.A.; Tolman, W.B. (2004). "Reactivity of Dioxygen-Copper Systems". Chemical Reviews. 104 (2): 1047–1076. doi:10.1021/cr020633r. PMID 14871149.
- ^ McDonald, M.R.; Fredericks, F.C.; Margerum, D.W. (1997). "Characterization of Copper(III)–Tetrapeptide Complexes with Histidine as the Third Residue". Inorganic Chemistry. 36 (14): 3119–3124. doi:10.1021/ic9608713. PMID 11669966.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 1187, ISBN 0-7506-3365-4
- ^ Hickman, A.; Sanford, M. (2012). "High-valent organometallic copper and palladium in catalysis". Nature. 484 (7393): 177–185. Bibcode:2012Natur.484..177H. doi:10.1038/nature11008. PMC 4384170
 . PMID 22498623.
. PMID 22498623.
- ^ Liu, He; Shen, Qilong (2021). "Well-defined organometallic Copper(III) complexes: Preparation, characterization and reactivity". Coord. Chem. Rev. 442: 213923. doi:10.1016/j.ccr.2021.213923.
- ^ A Timeline of Copper Technologies, Copper Development Association, https://www.copper.org/education/history/timeline/
- ^ a b "CSA – Discovery Guides, A Brief History of Copper". Csa.com. Diarsipkan dari versi asli tanggal 3 Februari 2015. Diakses tanggal 3 Juli 2023.
- ^ Rayner W. Hesse (2007). Jewelrymaking through History: an Encyclopedia. Greenwood Publishing Group. hlm. 56. ISBN 978-0-313-33507-5.Tidak ada sumber utama yang diberikan dalam buku itu.
- ^ "Copper". Elements.vanderkrogt.net. Diakses tanggal 3 Juli 2023.
- ^ Renfrew, Colin (1990). Before civilization: the radiocarbon revolution and prehistoric Europe. Penguin. ISBN 978-0-14-013642-5. Diakses tanggal 3 Juli 2023.
- ^ Cowen, R. "Essays on Geology, History, and People: Chapter 3: Fire and Metals". Diakses tanggal 3 Juli 2023.
- ^ Thoury, M.; Mille, B.; Séverin-Fabiani, T.; Robbiola, L.; Réfrégiers, M.; Jarrige, J.-F.; Bertrand, L. (15 November 2016). "High spatial dynamics-photoluminescence imaging reveals the metallurgy of the earliest lost-wax cast object". Nature Communications. 7: 13356. Bibcode:2016NatCo...713356T. doi:10.1038/ncomms13356. ISSN 2041-1723. PMC 5116070
 . PMID 27843139.
. PMID 27843139.
- ^ Timberlake, S.; Prag A.J.N.W. (2005). The Archaeology of Alderley Edge: Survey, excavation and experiment in an ancient mining landscape. Oxford: John and Erica Hedges Ltd. hlm. 396. doi:10.30861/9781841717159. ISBN 9781841717159.
- ^ a b "CSA – Discovery Guides, A Brief History of Copper". CSA Discovery Guides. Diarsipkan dari versi asli tanggal 3 Februari 2015. Diakses tanggal 3 Juli 2023.
- ^ a b c d Pompeani, David P; Steinman, Byron A; Abbott, Mark B; Pompeani, Katherine M; Reardon, William; DePasqual, Seth; Mueller, Robin H (April 2021). "On the Timing of the Old Copper Complex in North America: A Comparison of Radiocarbon Dates from Different Archaeological Contexts". Radiocarbon (dalam bahasa Inggris). 63 (2): 513–531. Bibcode:2021Radcb..63..513P. doi:10.1017/RDC.2021.7. ISSN 0033-8222.
- ^ Pleger, Thomas C. "A Brief Introduction to the Old Copper Complex of the Western Great Lakes: 4000–1000 BC", Proceedings of the Twenty-Seventh Annual Meeting of the Forest History Association of Wisconsin, Oconto, Wisconsin, 5 Oktober 2002, hlm. 10–18.
- ^ Emerson, Thomas E. dan McElrath, Dale L. Archaic Societies: Diversity and Complexity Across the Midcontinent, SUNY Press, 2009 ISBN 1-4384-2701-8.
- ^ Bebber, Michelle R.; Buchanan, Briggs; Holland-Lulewicz, Jacob (26 April 2022). "Refining the chronology of North America's copper using traditions: A macroscalar approach via Bayesian modeling". PLOS ONE (dalam bahasa Inggris). 17 (4): e0266908. Bibcode:2022PLoSO..1766908B. doi:10.1371/journal.pone.0266908
 . ISSN 1932-6203. PMC 9041870
. ISSN 1932-6203. PMC 9041870  Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 35472064 Periksa nilai|pmid=(bantuan). - ^ Malakoff, David (19 Maret 2021). "Ancient Native Americans were among the world's first coppersmiths". Science. doi:10.1126/science.abi6135. ISSN 0036-8075.
- ^ a b Pompeani, David P.; Abbott, Mark B.; Steinman, Byron A.; Bain, Daniel J. (14 Mei 2013). "Lake Sediments Record Prehistoric Lead Pollution Related to Early Copper Production in North America". Environmental Science & Technology. 47 (11): 5545–5552. Bibcode:2013EnST...47.5545P. doi:10.1021/es304499c. ISSN 0013-936X. PMID 23621800.
- ^ Bebber, Michelle R.; Eren, Metin I. (1 Oktober 2018). "Toward a functional understanding of the North American Old Copper Culture "technomic devolution"". Journal of Archaeological Science (dalam bahasa Inggris). 98: 34–44. Bibcode:2018JArSc..98...34B. doi:10.1016/j.jas.2018.08.001. ISSN 0305-4403.
- ^ Dainian, Fan. Chinese Studies in the History and Philosophy of Science and Technology. hlm. 228.
- ^ Wallach, Joel. Epigenetics: The Death of the Genetic Theory of Disease Transmission.
- ^ Radivojević, Miljana; Rehren, Thilo (Desember 2013). "Tainted ores and the rise of tin bronzes in Eurasia, c. 6500 years ago". Antiquity Publications Ltd.
- ^ a b McNeil, Ian (2002). Encyclopaedia of the History of Technology. London; New York: Routledge. hlm. 13, 48–66. ISBN 978-0-203-19211-5.
- ^ Eastaugh, Nicholas; Walsh, Valentine; Chaplin, Tracey; Siddall, Ruth (17 Juni 2013). Pigment Compendium: Optical Microscopy of Historical Pigments. doi:10.4324/9780080454573. ISBN 9781136373794.
- ^ Rickard, T.A. (1932). "The Nomenclature of Copper and its Alloys". Journal of the Royal Anthropological Institute. 62: 281–290. doi:10.2307/2843960. JSTOR 2843960.
- ^ Timberlake, Simon (11 Juni 2017). "New ideas on the exploitation of copper, tin, gold, and lead ores in Bronze Age Britain: The mining, smelting, and movement of metal". Materials and Manufacturing Processes. 32 (7–8): 709–727. doi:10.1080/10426914.2016.1221113.
- ^ Martin, Susan R. (1995). "The State of Our Knowledge About Ancient Copper Mining in Michigan". The Michigan Archaeologist. 41 (2–3): 119. Diarsipkan dari versi asli tanggal 7 Februari 2016.
- ^ a b Chastain, Matthew L.; Deymier-Black, Alix C.; Kelly, John E.; Brown, James A.; Dunand, David C. (1 Juli 2011). "Metallurgical analysis of copper artifacts from Cahokia". Journal of Archaeological Science (dalam bahasa Inggris). 38 (7): 1727–1736. Bibcode:2011JArSc..38.1727C. doi:10.1016/j.jas.2011.03.004. ISSN 0305-4403.
- ^ a b Cortés, Leticia Inés; Scattolin, María Cristina (Juni 2017). "Ancient metalworking in South America: a 3000-year-old copper mask from the Argentinian Andes". Antiquity (dalam bahasa Inggris). 91 (357): 688–700. doi:10.15184/aqy.2017.28. ISSN 0003-598X.
- ^ Hong, S.; Candelone, J.-P.; Patterson, C.C.; Boutron, C.F. (1996). "History of Ancient Copper Smelting Pollution During Roman and Medieval Times Recorded in Greenland Ice". Science. 272 (5259): 246–249 (247f.). Bibcode:1996Sci...272..246H. doi:10.1126/science.272.5259.246.
- ^ de Callataÿ, François (2005). "The Graeco-Roman Economy in the Super Long-Run: Lead, Copper, and Shipwrecks". Journal of Roman Archaeology. 18: 361–372 (366–369). doi:10.1017/S104775940000742X.
- ^ Savenije, Tom J.; Warman, John M.; Barentsen, Helma M.; van Dijk, Marinus; Zuilhof, Han; Sudhölter, Ernst J.R. (2000). "Corinthian Bronze and the Gold of the Alchemists" (PDF). Macromolecules. 33 (2): 60–66. Bibcode:2000MaMol..33...60S. doi:10.1021/ma9904870. Diarsipkan dari versi asli (PDF) tanggal 29 September 2007.
- ^ Yuniastuti, Ari (2014). Nutrisi Mikromineral dan Kesehatan (PDF). Semarang: UNNES PRESS. ISBN 9786022850144.
- ^ Lynch, Martin (2004). Mining in World History. hlm. 60. ISBN 978-1-86189-173-0.
- ^ "Gold: prices, facts, figures and research: A brief history of money". Diakses tanggal 3 Juli 2023.
- ^ "Copper and Brass in Ships". Diakses tanggal 3 Juli 2023.
- ^ Stelter, M.; Bombach, H. (2004). "Process Optimization in Copper Electrorefining". Advanced Engineering Materials. 6 (7): 558–562. doi:10.1002/adem.200400403.
- ^ Gardner, E. D.; et al. (1938). Copper Mining in North America. Washington, D. C.: U. S. Bureau of Mines. Diakses tanggal 3 Juli 2023.
- ^ Hyde, Charles (1998). Copper for America, the United States Copper Industry from Colonial Times to the 1990s. Tucson, Arizona: University of Arizona Press. hlm. passim. ISBN 0-8165-1817-3.
- ^ "Outokumpu Flash Smelting" (PDF). Outokumpu. hlm. 2. Diarsipkan dari versi asli (PDF) tanggal 24 Juli 2011.
- ^ Karen A. Mingst (1976). "Cooperation or illusion: an examination of the intergovernmental council of copper exporting countries". International Organization. 30 (2): 263–287. doi:10.1017/S0020818300018270.
- ^ Ryck Lydecker. "Is Copper Bottom Paint Sinking?". BoatUS Magazine. Diakses tanggal 3 Juli 2023.
- ^ "Copper". American Elements. 2008. Diarsipkan dari versi asli tanggal 8 Juni 2008. Diakses tanggal 3 Juli 2023.
- ^ Pops, Horace, 2008, "Processing of wire from antiquity to the future", Wire Journal International, June, hlm. 58–66
- ^ The Metallurgy of Copper Wire, http://www.litz-wire.com/pdf%20files/Metallurgy_Copper_Wire.pdf Diarsipkan 1 September 2013 di Wayback Machine.
- ^ Joseph, Günter, 1999, Copper: Its Trade, Manufacture, Use, and Environmental Status, edited by Kundig, Konrad J.A., ASM International, hlm. 141–192 dan hlm. 331–375.
- ^ "Copper, Chemical Element – Overview, Discovery and naming, Physical properties, Chemical properties, Occurrence in nature, Isotopes". Chemistryexplained.com. Diakses tanggal 3 Juli 2023.
- ^ Joseph, Günter, 1999, Copper: Its Trade, Manufacture, Use, and Environmental Status, disunting oleh Kundig, Konrad J.A., ASM International, hlm.348
- ^ "Aluminum Wiring Hazards and Pre-Purchase Inspections". www.heimer.com. Diarsipkan dari versi asli tanggal 28 Mei 2016. Diakses tanggal 3 Juli 2023.
- ^ "Accelerator: Waveguides (SLAC VVC)". SLAC Virtual Visitor Center. Diakses tanggal 3 Juli 2023.
- ^ IE3 energy-saving motors, Engineer Live, http://www.engineerlive.com/Design-Engineer/Motors_and_Drives/IE3_energy-saving_motors/22687/
- ^ Energy‐efficiency policy opportunities for electric motor‐driven systems, International Energy Agency, 2011 Working Paper in the Energy Efficiency Series, by Paul Waide and Conrad U. Brunner, OECD/IEA 2011
- ^ Fuchsloch, J. dan E.F. Brush, (2007), "Systematic Design Approach for a New Series of Ultra‐NEMA Premium Copper Rotor Motors", in EEMODS 2007 Conference Proceedings, 10–15 Juni, Beijing.
- ^ Copper motor rotor project; Copper Development Association; "Copper.org: Copper Motor Rotor Project". Diarsipkan dari versi asli tanggal 13 Maret 2012. Diakses tanggal 3 Juli 2023.
- ^ NEMA Premium Motors, The Association of Electrical Equipment and Medical Imaging Manufacturers; "NEMA - NEMA Premium Motors". Diarsipkan dari versi asli tanggal 2 April 2010. Diakses tanggal 3 Juli 2023.
- ^ IEA (2022), Renewables 2022, IEA, Paris https://www.iea.org/reports/renewables-2022, License: CC BY 4.0
- ^ Global trends in renewable energy investment 2012, by REN21 (Renewable Energy Policy Network for the 21st Century); http://www.ren21.net/gsr
- ^ Will the Transition to Renewable Energy Be Paved in Copper?, Renewable Energy World; 15 Januari 2016; https://www.renewableenergyworld.com/articles/2016/01/will-the-transition-to-renewable-energy-be-paved-in-copper.html Diarsipkan 22 Juni 2018 di Wayback Machine.
- ^ García-Olivares, Antonio, Joaquim Ballabrera-Poy, Emili García-Ladona, and Antonio Turiel. A global renewable mix with proven technologies and common materials, Energy Policy, 41 (2012): 561-57, http://imedea.uib-csic.es/master/cambioglobal/Modulo_I_cod101601/Ballabrera_Diciembre_2011/Articulos/Garcia-Olivares.2011.pdf
- ^ A kilo more of copper increases environmental performance by 100 to 1,000 times; Renewable Energy Magazine; 14 April 2011; http://www.renewableenergymagazine.com/article/a-kilo-more-of-copper-increases-environmental
- ^ Copper at the core of renewable energies; European Copper Institute; European Copper Institute; 18 halaman; http://www.eurocopper.org/files/presskit/press_kit_copper_in_renewables_final_29_10_2008.pdf Diarsipkan 23 Mei 2012 di Wayback Machine.
- ^ Copper in energy systems; Copper Development Association Inc.; http://www.copper.org/environment/green/energy.html
- ^ The Rise Of Solar: A Unique Opportunity For Copper; Solar Industry Magazine; April 2017; Zolaika Strong; https://issues.solarindustrymag.com/article/rise-solar-unique-opportunity-copper
- ^ Pops, Horace, 1995. Physical Metallurgy of Electrical Conductors, in Nonferrous Wire Handbook, Volume 3: Principles and Practice, The Wire Association International
- ^ The World Copper Factbook, 2017; http://www.icsg.org/index.php/component/jdownloads/finish/170/2462
- ^ Copper Mineral Commodity Summary (USGS, 2017) https://minerals.usgs.gov/minerals/pubs/commodity/copper/ mcs-2017-coppe.pdf
- ^ Global Mineral Resource Assessment (USGS, 2014) http://pubs.usgs.gov/fs/2014/3004/pdf/fs2014-3004.pdf
- ^ Long-Term Availability of Copper; International Copper Association; http://copperalliance.org/wordpress/wp-content/uploads/2018/02/ICA-long-term-availability-201802-A4-HR.pdf Diarsipkan 29 Juni 2018 di Wayback Machine.
- ^ Will the Transition to Renewable Energy Be Paved in Copper?, Renewable Energy World; 15 Januari 2016; oleh Zolaikha Strong; https://www.renewableenergyworld.com/articles/2016/01/will-the-transition-to-renewable-energy-be-paved-in-copper.html Diarsipkan 22 Juni 2018 di Wayback Machine.
- ^ Seale, Wayne (2007). The role of copper, brass, and bronze in architecture and design; Metal Architecture, Mei 2007
- ^ Copper roofing in detail; Copper in Architecture; Copper Development Association, U.K., www.cda.org.uk/arch
- ^ Architecture, European Copper Institute; http://eurocopper.org/copper/copper-architecture.html Diarsipkan 9 Oktober 2012 di Wayback Machine.
- ^ Kronborg completed; Agency for Palaces and Cultural Properties, København, "Kronborg completed - Agency for Palaces and Cultural Properties". Diarsipkan dari versi asli tanggal 24 Oktober 2012. Diakses tanggal 3 Juli 2023.
- ^ Berg, Jan. "Why did we paint the library's roof?". Diarsipkan dari versi asli tanggal 25 Juni 2007. Diakses tanggal 3 Juli 2023.
- ^ Architectural considerations; Copper in Architecture Design Handbook, http://www.copper.org/applications/architecture/arch_dhb/fundamentals/arch_considerations.htm[pranala nonaktif permanen]
- ^ Peters, Larry E. (2004). Preventing corrosion on copper roofing systems; Professional Roofing, October 2004, http://www.professionalroofing.net
- ^ Wu, Chun. "Oxidation reaction: Why is the Statue of Liberty blue-green? How does rust work?" (PDF). wepanknowledgecenter.org. Engage Engineering. Diarsipkan dari versi asli (PDF) tanggal 25 Oktober 2013. Diakses tanggal 3 Juli 2023.
- ^ Fitzgerald, K.P.; Nairn, J.; Atrens, A. (1998). "The chemistry of copper patination". Corrosion Science. 40 (12): 2029–50. doi:10.1016/S0010-938X(98)00093-6.
- ^ Application Areas: Architecture – Finishes – patina; http://www.copper.org/applications/architecture/finishes.html
- ^ Glossary of copper terms, Copper Development Association (UK): "Glossary of copper terms". Diarsipkan dari versi asli tanggal 20 Agustus 2012. Diakses tanggal 3 Juli 2023.
- ^ Finishes – natural weathering; Copper in Architecture Design Handbook, Copper Development Association Inc., "Copper.org: Architecture Design Handbook: Finishes". Diarsipkan dari versi asli tanggal 16 Oktober 2012. Diakses tanggal 3 Juli 2023.
- ^ Davis, Joseph R. (2001). Copper and Copper Alloys. ASM International. hlm. 3–6, 266. ISBN 978-0-87170-726-0.
- ^ Edding, Mario E., Flores, Hector, and Miranda, Claudio, (1995), Experimental Usage of Copper-Nickel Alloy Mesh in Mariculture. Part 1: Feasibility of usage in a temperate zone; Part 2: Demonstration of usage in a cold zone; Final report to the International Copper Association Ltd.
- ^ Corrosion Behaviour of Copper Alloys used in Marine Aquaculture Diarsipkan 24 September 2013 di Wayback Machine.. (PDF) . copper.org. Diakses tanggal 3 Juli 2023.
- ^ Copper Touch Surfaces Diarsipkan 23 Juli 2012 di Wayback Machine.. Copper Touch Surfaces. Diakses tanggal 3 Juli 2023.
- ^ "EPA Registers Copper Surfaces for Residual Use Against Coronavirus". United States Environmental Protection Agency. 10 Februari 2021. Diakses tanggal 3 Juli 2023.
- ^ Montero, David A.; Arellano, Carolina; Pardo, Mirka; Vera, Rosa; Gálvez, Ricardo; Cifuentes, Marcela; Berasain, María A.; Gómez, Marisol; Ramírez, Claudio; Vidal, Roberto M. (2019-01-05). "Antimicrobial properties of a novel copper-based composite coating with potential for use in healthcare facilities". Antimicrobial Resistance and Infection Control. 8 (1): 3. doi:10.1186/s13756-018-0456-4. ISSN 2047-2994. PMC 6321648
 . PMID 30627427.
. PMID 30627427.
- ^ a b "EPA registers copper-containing alloy products". United States Environmental Protection Agency. Mei 2008. Diarsipkan dari versi asli tanggal 29 September 2015.
- ^ Biurrun, Amaya; Caballero, Luis; Pelaz, Carmen; León, Elena; Gago, Alberto (1999). "Treatment of a Legionella pneumophila‐Colonized Water Distribution System Using Copper‐Silver Ionization and Continuous Chlorination" (PDF). Infection Control and Hospital Epidemiology. 20 (6): 426–428. doi:10.1086/501645. JSTOR 30141645. PMID 10395146. Diarsipkan dari versi asli (PDF) tanggal 17 Februari 2019.
- ^ Zaleski, Andrew, As hospitals look to prevent infections, a chorus of researchers make a case for copper surfaces, STAT, 24 September 2020
- ^ Chilean subway protected with Antimicrobial Copper – Rail News from Diarsipkan 24 July 2012 di Wayback Machine. rail.co. Diakses tanggal 3 Juli 2023.
- ^ Codelco to provide antimicrobial copper for new metro lines (Chile) [pranala nonaktif]. Construpages.com.ve. Diakses tanggal 3 Juli 2023.
- ^ PR 811 Chilean Subway Installs Antimicrobial Copper Diarsipkan 23 November 2011 di Wayback Machine.. (PDF). antimicrobialcopper.com. Diakses tanggal 3 Juli 2023.
- ^ "Copper and Cupron". Cupron.
- ^ "Global copper market under supplied, demand on the rise – report". Mining.com (dalam bahasa Inggris). 6 Januari 2019. Diakses tanggal 3 Juli 2023.
- ^ "Will the Transition to Renewable Energy Be Paved in Copper?". www.renewableenergyworld.com. 15 Januari 2015. Diarsipkan dari versi asli tanggal 22 Juni 2018. Diakses tanggal 3 Juli 2023.
- ^ "Copper and cars: Boom goes beyond electric vehicles". MINING.com (dalam bahasa Inggris). 18 Juni 2018. Diakses tanggal 3 Juli 2023.
- ^ "Impact of electric cars in medium-term copper demand 'overrated', experts say". MINING.com (dalam bahasa Inggris). 12 April 2018. Diakses tanggal 3 Juli 2023.
- ^ "Why are Premiums for Copper Bullion So High?". Provident Metals. 20 Agustus 2012. Diakses tanggal 3 Juli 2023.
- ^ Chace, Zoe. "Penny Hoarders Hope for the Day The Penny Dies". NPR.org. NPR. Diakses tanggal 3 Juli 2023.
- ^ Walker, W.R.; Keats, D.M. (1976). "An investigation of the therapeutic value of the 'copper bracelet'-dermal assimilation of copper in arthritic/rheumatoid conditions". Agents and Actions. 6 (4): 454–459. PMID 961545.
- ^ Richmond SJ, Gunadasa S, Bland M, Macpherson H (2013). "Copper bracelets and magnetic wrist straps for rheumatoid arthritis – analgesic and anti-inflammatory effects: a randomised double-blind placebo controlled crossover trial". PLOS ONE. 8 (9): e71529. Bibcode:2013PLoSO...871529R. doi:10.1371/journal.pone.0071529
 . PMC 3774818
. PMC 3774818  . PMID 24066023.
. PMID 24066023.
- ^ Richmond, Stewart J.; Brown, Sally R.; Campion, Peter D.; Porter, Amanda J.L.; Moffett, Jennifer A. Klaber; Jackson, David A.; Featherstone, Valerie A.; Taylor, Andrew J. (2009). "Therapeutic effects of magnetic and copper bracelets in osteoarthritis: A randomised placebo-controlled crossover trial". Complementary Therapies in Medicine. 17 (5–6): 249–256. doi:10.1016/j.ctim.2009.07.002. ISSN 0965-2299. PMID 19942103.
- ^ University of Arkansas for Medical Sciences:
Find the Truth Behind Medical Myths Diarsipkan 6 Januari 2014 di Wayback Machine.
Meskipun tidak pernah terbukti bahwa tembaga dapat diserap melalui kulit dengan memakai gelang, penelitian menunjukkan bahwa tembaga yang berlebihan dapat menyebabkan keracunan, menyebabkan muntah dan, dalam kasus yang parah, kerusakan hati. - ^
Truth in Advertising
Tommie Copper - ^ a b Geoffrey Michael Gadd (March 2010). "Metals, minerals and microbes: geomicrobiology and bioremediation". Microbiology. 156 (3): 609–643. doi:10.1099/mic.0.037143-0
 . PMID 20019082.
. PMID 20019082.
- ^ Harbhajan Singh (2006). Mycoremediation: Fungal Bioremediation. hlm. 509. ISBN 978-0-470-05058-3.
- ^ Vest, Katherine E.; Hashemi, Hayaa F.; Cobine, Paul A. (2013). "Chapter 13 The Copper Metallome in Eukaryotic Cells". Dalam Banci, Lucia. Metallomics and the Cell. Metal Ions in Life Sciences. 12. Springer. hlm. 451–78. doi:10.1007/978-94-007-5561-1_13. ISBN 978-94-007-5560-4. PMID 23595680. electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 electronic-ISSN 1868-0402
- ^ "Fun facts". Horseshoe crab. University of Delaware. Diarsipkan dari versi asli tanggal 22 Oktober 2008. Diakses tanggal 3 Juli 2023.
- ^ a b S.J. Lippard, J.M. Berg "Principles of bioinorganic chemistry" University Science Books: Mill Valley, CA; 1994. ISBN 0-935702-73-3.
- ^ Decker, H.; Terwilliger, N. (2000). "COPs and Robbers: Putative evolution of copper oxygen-binding proteins". Journal of Experimental Biology. 203 (Pt 12): 1777–1782. doi:10.1242/jeb.203.12.1777
 . PMID 10821735.
. PMID 10821735.
- ^ Schneider, Lisa K.; Wüst, Anja; Pomowski, Anja; Zhang, Lin; Einsle, Oliver (2014). "Chapter 8. No Laughing Matter: The Unmaking of the Greenhouse Gas Dinitrogen Monoxide by Nitrous Oxide Reductase". Dalam Peter M.H. Kroneck; Martha E. Sosa Torres. The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences. 14. Springer. hlm. 177–210. doi:10.1007/978-94-017-9269-1_8. ISBN 978-94-017-9268-4. PMID 25416395.
- ^ Denoyer, Delphine; Clatworthy, Sharnel A.S.; Cater, Michael A. (2018). "Chapter 16. Copper Complexes in Cancer Therapy". Dalam Sigel, Astrid; Sigel, Helmut; Freisinger, Eva; Sigel, Roland K.O. Metallo-Drugs: Development and Action of Anticancer Agents. Metal Ions in Life Sciences. 18. Berlin: de Gruyter GmbH. hlm. 469–506. doi:10.1515/9783110470734-022. ISBN 978-3-11-047073-4. PMID 29394035.
- ^ a b "Amount of copper in the normal human body, and other nutritional copper facts". Diarsipkan dari versi asli tanggal 10 April 2009. Diakses tanggal 3 Juli 2023.
- ^ Adelstein, S. J.; Vallee, B. L. (1961). "Copper metabolism in man". New England Journal of Medicine. 265 (18): 892–897. doi:10.1056/NEJM196111022651806. PMID 13859394.
- ^ M.C. Linder; Wooten, L.; Cerveza, P.; Cotton, S.; Shulze, R.; Lomeli, N. (1 Mei 1998). "Copper transport". The American Journal of Clinical Nutrition. 67 (5): 965S–971S. doi:10.1093/ajcn/67.5.965S
 . PMID 9587137.
. PMID 9587137.
- ^ Frieden, E.; Hsieh, H.S. (1976). Ceruloplasmin: The copper transport protein with essential oxidase activity. Advances in Enzymology – and Related Areas of Molecular Biology. 44. hlm. 187–236. doi:10.1002/9780470122891.ch6. ISBN 978-0-470-12289-1. JSTOR 20170553. PMID 775938.
- ^ S.S. Percival; Harris, E.D. (1 Januari 1990). "Copper transport from ceruloplasmin: Characterization of the cellular uptake mechanism". American Journal of Physiology. Cell Physiology. 258 (1): C140–C146. doi:10.1152/ajpcell.1990.258.1.c140. PMID 2301561.
- ^ Dietary Reference Intakes: RDA and AI for Vitamins and Elements Diarsipkan 13 November 2018 di Wayback Machine. Food and Nutrition Board, Institute of Medicine, National Academies Press, 2011. Diakses tanggal 3 Juli 2023.
- ^ Copper. IN: Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Copper, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Copper. National Academy Press. 2001, hlm. 224–257.
- ^ "Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies" (PDF). 2017.
- ^ Tolerable Upper Intake Levels For Vitamins And Minerals (PDF), European Food Safety Authority, 2006
- ^ "Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR p. 33982" (PDF).
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Diarsipkan dari versi asli tanggal 7 April 2020. Diakses tanggal 4 Juli 2023.
- ^ Bonham, Maxine; O'Connor, Jacqueline M.; Hannigan, Bernadette M.; Strain, J.J. (2002). "The immune system as a physiological indicator of marginal copper status?". British Journal of Nutrition. 87 (5): 393–403. doi:10.1079/BJN2002558
 . PMID 12010579.
. PMID 12010579.
- ^ Li, Yunbo; Trush, Michael; Yager, James (1994). "DNA damage caused by reactive oxygen species originating from a copper-dependent oxidation of the 2-hydroxy catechol of estradiol". Carcinogenesis. 15 (7): 1421–1427. doi:10.1093/carcin/15.7.1421. PMID 8033320.
- ^ Gordon, Starkebaum; John, M. Harlan (April 1986). "Endothelial cell injury due to copper-catalyzed hydrogen peroxide generation from homocysteine". J. Clin. Invest. 77 (4): 1370–6. doi:10.1172/JCI112442. PMC 424498
 . PMID 3514679.
. PMID 3514679.
- ^ "Pesticide Information Profile for Copper Sulfate". Cornell University. Diakses tanggal 4 Juli 2023.
- ^ Hunt, Charles E.; William W. Carlton (1965). "Cardiovascular Lesions Associated with Experimental Copper Deficiency in the Rabbit". Journal of Nutrition. 87 (4): 385–394. doi:10.1093/jn/87.4.385. PMID 5841854.
- ^ Ayyat M.S.; Marai I.F.M.; Alazab A.M. (1995). "Copper-Protein Nutrition of New Zealand White Rabbits under Egyptian Conditions". World Rabbit Science. 3 (3): 113–118. doi:10.4995/wrs.1995.249
 .
.
- ^ Brewer GJ (Maret 2012). "Copper excess, zinc deficiency, and cognition loss in Alzheimer's disease". BioFactors (Review). 38 (2): 107–113. doi:10.1002/biof.1005. hdl:2027.42/90519
 . PMID 22438177.
. PMID 22438177.
- ^ "Copper: Alzheimer's Disease". Examine.com. Diakses tanggal 4 Juli 2023.
- ^ "NIOSH Pocket Guide to Chemical Hazards #0151". National Institute for Occupational Safety and Health (NIOSH).
- ^ "NIOSH Pocket Guide to Chemical Hazards #0150". National Institute for Occupational Safety and Health (NIOSH).
- ^ OEHHA Copper
- ^ Talhout, Reinskje; Schulz, Thomas; Florek, Ewa; Van Benthem, Jan; Wester, Piet; Opperhuizen, Antoon (2011). "Hazardous Compounds in Tobacco Smoke". International Journal of Environmental Research and Public Health. 8 (12): 613–628. doi:10.3390/ijerph8020613
 . ISSN 1660-4601. PMC 3084482
. ISSN 1660-4601. PMC 3084482  . PMID 21556207.
. PMID 21556207.
- ^ Pourkhabbaz, A.; Pourkhabbaz, H. (2012). "Investigation of Toxic Metals in the Tobacco of Different Iranian Cigarette Brands and Related Health Issues". Iranian Journal of Basic Medical Sciences. 15 (1): 636–644. PMC 3586865
 . PMID 23493960.
. PMID 23493960.
- ^ Bernhard, David; Rossmann, Andrea; Wick, Georg (2005). "Metals in cigarette smoke". IUBMB Life. 57 (12): 805–809. doi:10.1080/15216540500459667
 . PMID 16393783.
. PMID 16393783.
Catatan[sunting | sunting sumber]
 |
 |
 |
 |
| dalam air murni, atau kondisi asam atau alkali. Tembaga dalam air netral lebih mulia daripada hidrogen. | dalam air yang mengandung sulfida | dalam larutan amonia 10 M | dalam larutan klorida |
Bacaan lebih lanjut[sunting | sunting sumber]
- Massaro, Edward J., ed. (2002). Handbook of Copper Pharmacology and Toxicology. Humana Press. ISBN 978-0-89603-943-8.
- "Copper: Technology & Competitiveness (Summary) Chapter 6: Copper Production Technology" (PDF). Office of Technology Assessment. 2005.
- Current Medicinal Chemistry, Volume 12, Number 10, Mei 2005, hlm. 1161–1208(48) Metals, Toxicity and Oxidative Stress
- William D. Callister (2003). Materials Science and Engineering: an Introduction
 (edisi ke-6). Wiley, New York. Table 6.1, hlm. 137. ISBN 978-0-471-73696-7.
(edisi ke-6). Wiley, New York. Table 6.1, hlm. 137. ISBN 978-0-471-73696-7. - Material: Copper (Cu), bulk, MEMS and Nanotechnology Clearinghouse.
- Kim BE; Nevitt T; Thiele DJ (2008). "Mechanisms for copper acquisition, distribution and regulation". Nat. Chem. Biol. 4 (3): 176–85. doi:10.1038/nchembio.72. PMID 18277979.
Pranala luar[sunting | sunting sumber]
- (Inggris) Copper di The Periodic Table of Videos (Universitas Nottingham)
- (Inggris) Lembar fakta tembaga dan senyawanya dari National Pollutant Inventory Australia
- (Inggris) Copper.org – situs web resmi Copper Development Association dengan situs luas mengenai sifat dan penggunaan tembaga
- (Inggris) Sejarah harga tembaga, menurut IMF
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


