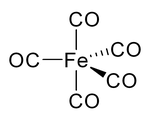
Karbon monoksida
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Karbon monoksida
| |||
| Nama lain
Karbonat oksida
| |||
| Penanda | |||
| 3DMet | {{{3DMet}}} | ||
| Nomor EC | |||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| Sifat | |||
| CO | |||
| Massa molar | 28,0101 g/mol | ||
| Penampilan | tak berwarna, gas tak berbau | ||
| Densitas | 0,789 g/cm³, liquid 1,250 g/L at 0 °C, 1 atm. 1,145 g/L pada 25 °C, 1 atm. (lebih ringan dari udara) | ||
| Titik lebur | -205 °C (68 K) | ||
| Titik didih | -192 °C (81 K) | ||
| 0,0026 g/100 mL (20 °C) | |||
| 0,112 D (3,74×10−31 C·m) | |||
| Bahaya | |||
Klasifikasi UE (DSD) (usang)
|
Sangat mudah terbakar (F+) Repr. Cat. 1 Beracun(T) | ||
| Frasa-R | R12, R23, R33, R48]], R61 | ||
| Frasa-S | S9, S16, S33, S45, S53 | ||
| Titik nyala | Gas mudah terbakar | ||
| Senyawa terkait | |||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Karbon monoksida, rumus kimia CO, adalah gas yang tak berwarna, tak berbau, dan tak berasa. Ia terdiri dari satu atom karbon yang secara kovalen berikatan dengan satu atom oksigen. Dalam ikatan ini, terdapat dua ikatan kovalen dan satu ikatan kovalen koordinasi antara atom karbon dan oksigen.
Karbon monoksida dihasilkan dari pembakaran tak sempurna dari senyawa karbon, sering terjadi pada mesin pembakaran dalam. Karbon monoksida terbentuk apabila terdapat kekurangan oksigen dalam proses pembakaran. Karbon monoksida mudah terbakar dan menghasilkan lidah api berwarna biru, menghasilkan karbon dioksida. Walaupun ia bersifat racun, CO memainkan peran yang penting dalam teknologi modern, yakni merupakan prekursor banyak senyawa karbon.
Produksi[sunting | sunting sumber]
Karbon monoksida merupakan senyawa yang sangat penting, sehingga banyak metode yang telah dikembangkan untuk produksinya.[1]
Gas produser dibentuk dari pembakaran karbon di oksigen pada temperatur tinggi ketika terdapat karbon yang berlebih. Dalam sebuah oven, udara dialirkan melalui kokas. CO2 yang pertama kali dihasilkan akan mengalami kesetimbangan dengan karbon panas, menghasilkan CO. Reaksi O2 dengan karbon membentuk CO disebut sebagai kesetimbangan Boudouard. Di atas 800 °C, CO adalah produk yang predominan:
- O2 + 2 C → 2 CO
- ΔH = -221 kJ/mol
Kerugian dari metode ini adalah apabila dilakukan dengan udara, ia akan menyisakan campuran yang terdiri dari nitrogen.
Gas sintetik atau gas air diproduksi via reaksi endotermik uap air dan karbon:
- H2O + C → H2 + CO
- ΔH = 131 kJ/mol
CO juga merupakan hasil sampingan dari reduksi bijih logam oksida dengan karbon:
- MO + C → M + CO
- ΔH = 131 kJ/mol
Oleh karena CO adalah gas, proses reduksi dapat dipercepat dengan memanaskannya. Diagram Ellingham menunjukkan bahwa pembentukan CO lebih difavoritkan daripada CO2 pada temperatur tinggi.
CO adalah anhidrida dari asam format. Oleh karena itu, adalah praktis untuk menghasilkan CO dari dehidrasi asam format. Produksi CO dalam skala laboratorium lainnya adalah dengan pemanasan campuran bubuk seng dan kalsium karbonat.
- Zn + CaCO3 → ZnO + CaO + CO
Metode laboratorium lainnya adalah dengan mereaksikan sukrosa dengan natrium hidroksida dalam sistem tertutup.
Struktur[sunting | sunting sumber]
Molekul CO memiliki panjang ikat 0,1128 nm.[2] Perbedaan muatan formal dan elektronegativitas saling meniadakan, sehingga terdapat momen dipol yang kecil dengan kutub negatif di atom karbon[3] walaupun oksigen memiliki elektronegativitas yang lebih besar. Alasannya adalah orbital molekul yang terpenuhi paling tinggi memiliki energi yang lebih dekat dengan orbital p karbon, yang berarti bahwa terdapat rapatan elektron yang lebih besar dekat karbon. Selain itu, elektronegativitas karbon yang lebih rendah menghasilkan awan elektron yang lebih baur, sehingga menambah momen dipol. Ini juga merupakan alasan mengapa kebanyakan reaksi kimia yang melibatkan karbon monoksida terjadi pada atom karbon, dan bukannya pada atom oksigen.
Panjang ikatan molekul karbon monoksida sesuai dengan ikatan rangkap tiga parsialnya. Molekul ini memiliki momen dipol ikatan yang kecil dan dapat diwakili dengan tiga struktur resonansi:
Resonans paling kiri adalah bentuk yang paling penting.[2] Hal ini diilustrasikan dengan reaktivitas karbon monoksida yang bereaksi dengan karbokation.
Dinitrogen bersifat isoelektronik terhadap karbon monoksida. Hal ini berarti bahwa molekul-molekul ini memiliki jumlah elektron dan ikatan yang mirip satu sama lainnya. Sifat-sifat fisika antara N2 dan CO sangat mirip, walaupun CO lebih reaktif.
Reaksi kimia dasar[sunting | sunting sumber]
Penggunaan industri[sunting | sunting sumber]
Karbon monoksida adalah gas industri utama yang memiliki banyak kegunaan dalam produksi bahan kimia pukal (bulk chemical).[4]
Sejumlah aldehida dengan hasil volume yang tinggi dapat diproduksi dengan reaksi hidroformilasi dari alkena, CO, dan H2.
Metanol diproduksi dari hidrogenasi CO. Pada reaksi yang berkaitan, hidrogenasi CO diikuti dengan pembentukan ikatan C-C, seperti yang terjadi pada proses Fischuoklker-Tropsch, CO dihirogenasi Bahamas bakar hidrokarbon cair. initial mengizinkan batu bara dikonversikan menjadi bensin.
Pada proses Monsanto, karbon monoksida bereaksi you I ke era Dan katalis rodium homogen dan HI, teacher you have. Proses ini Seara meluas dalam produski Adams you berskala industri.
Karbon monks idea mercaptan components das are dari syngas yang seeing Digi Akan untuk teenage industri. Karbon monoksida juga digunakan pada proses pemurnian nikel.
Kimia koordinasi[sunting | sunting sumber]

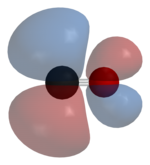
Kebanyakan logam akan membentuk kompleks koordinasi yang bersifat kovalen dengan karbon monoksida. Hanya logam yang mempunyai keadaan oksidasi yang lebih rendah yang membentuk kompleks dengan ligan karbon monoksida. Hal ini dikarenakan oleh perlunya rapatan elektron yang cukup untuk memfasilitasi donasi balik dari orbital dxz logam ke orbital molekul π* CO. Pasangan elektron menyendiri dari atom karbon CO juga menyumbangkan rapatan elektron ke dx²−y² logam membentuk ikatan sigma. Pada nikel karbonil, Ni(CO)4 terbentuk dari kombinasi langsung karbon monoksida dan logam nikel pada temperatur ruangan. Nikel karbonil dapat mengurai kembali menjadi Ni dan CO seketika bersentuhan dengan permukaan yang panas. Proses ini juga pernah digunakan dalam proses pemurnian nikel pada proses Mond.[5]
Pada nikel karbonil dan karbonil-karbonil lainnya, pasangan elektron pada karbon berinteraksi dengan logam; karbon monoksida menyumbangkan pasangan elektronnya kepada logam. Dalam situasi ini, karbon monoksida disebut sebagai ligan karbonil. Salah satu logam karbonil yang paling penting adalah besi pentakarbonil, Fe(CO)5:
Banyak kompleks logam-CO dihasilkan dari dekarbonilasi larutan organik dan bukannya dari CO. Sebagai contoh, iridium(III) klorida dan trifenilfosfina bereaksi di metoksietanol mendidih atau dimetilformamida untuk menghasilkan IrCl(CO)(PPh3)2.
Kimia organik dan kimia golongan utama[sunting | sunting sumber]
Dengan keberadaan asam kuat dan air, karbon monoksida bereaksi dengan olefin membentuk asam karboksilat, proses ini dikenal sebagai reaksi Koch-Haaf.[6] Pada reaksi Gattermann-Koch, arena diubah menjadi turunan benzaldehida dengan keberadaan AlCl3 dan HCl.[7] Senyawa organologam seperti butil litium dapat bereaksi dengan CO, namun reaksi ini jarang digunakan.
Walaupun CO bereaksi dengan karbokation dan karbanion, ia relatif tidak reaktif terhadap senyawa-senyawa organik tanpa intervensi katalis logam.[8]
Dengan pereaksi golongan utama, CO mengalami beberapa reaksi yang penting. Klorinasi CO adalah salah satu lintasan industri yang penting untuk senyawa fosgena. Dengan borana, CO membentuk sebuah aduk (adduct) H3BCO yang bersifat isoelektrik dengan kation asilium, [H3CCO]+. CO bereaksi dengan natrium, menghasilkan Na2C2O2 (natrium asetilenadiolat) dari penggandengan (coupling) C-C, dan kalium, menghasilkan K2C2O2 (kalium asetilenadiolat) dan K2C6O6 (kalium rodizonat).
Karbon monoksida di atmosfer[sunting | sunting sumber]

Karbon monoksida, walaupun dianggap sebagai polutan, telah lama ada di atmosfer sebagai hasil produk dari aktivitas gunung berapi. Ia larut dalam lahar gunung berapi pada tekanan yang tinggi di dalam mantel bumi. Kandungan karbon monoksida dalam gas gunung berapi bervariasi dari kurang dari 0,01% sampai sebanyak 2% bergantung pada gunung berapi tersebut. Oleh karena sumber alami karbon monoksida bervariasi dari tahun ke tahun, sangatlah sulit untuk secara akurat menghitung emisi alami gas tersebut.
Karbon monoksida memiliki efek radiative forcing secara tidak langsung dengan menaikkan konsentrasi metana dan ozon troposfer melalui reaksi kimia dengan konstituen atmosfer lainnya (misalnya radikal hidroksil OH-) yang sebenarnya akan melenyapkan metana dan ozon. Dengan proses alami di atmosfer, karbon monoksida pada akhirnya akan teroksidasi menjadi karbon dioksida. Konsentrasi karbon monoksida memiliki jangka waktu pendek di atmosfer.
CO antropogenik dari emisi automobil dan industri memberikan kontribusi pada efek rumah kaca dan pemanasan global. Di daerah perkotaan, karbon monoksida, bersama dengan aldehida, bereaksi secara fotokimia, meghasilkan radikal peroksi. Radikal peroksi bereaksi dengan nitrogen oksida dan meningkatkan rasio NO2 terhadap NO, sehingga mengurangi jumlah NO yang tersedia untuk bereaksi dengan ozon. Karbon monoksida juga merupakan konstituen dari asap rokok.
Peran dalam fisiologi dan makanan[sunting | sunting sumber]
Karbon monoksida digunakan dalam sistem kemasan Amerika Serikat, utamanya digunakan dalam produk-produk daging segar seperti daging kerbau dan babi. CO berkombinasi dengan mioglobin membentuk karboksimioglobin, sebuah pigmen cerah yang berwarna merah ceri. Karboksimioglobin lebih stabil dari bentuk mioglobin yang dioksigenasikan, yakni oksimioglobin, yang dapat dioksidasi menjadi pigmen coklat, metmioglobin. Warna merah yang stabil ini dapat bertahan lebih lama, sehingga memberikan kesan kesegaran.[9] Kadar CO yang digunakan berkisar antara 0,4% sampai dengan 0,5%.
Teknologi ini pertama kali diberikan status "Generally recognized as safe" (secara umum dikenal aman) oleh FDA pada tahun 2002 untuk penggunaan sistem kemasan sekunder. Pada tahun 2004, FDA mengizinkan penggunaan CO sebagai metode kemasan primer, menyatakan bahwa CO tidak menutupi bau busuk.[10] Walaupun begitu, teknologi ini masih kontroversial di Amerika Serikat oleh karena kekhawatiran CO akan menutupi bau busuk makanan.[11]
Karbon monoksida diproduksi secara alami sebagai pemecahan dari heme, sebuah substrat untuk enzim heme oksigenase. Reaksi enzimatis ini memecahkan heme menjadi CO, biliverdin, dan Fe3+. CO yang diproduksi secara edogen kemungkinan memiliki peran fisiologis yang penting dalam tubuh (misalnya sebagai neurotransmiter atau pelemas pembuluh darah). Selain itu, CO meregulasi reaksi peradangan yang dapat mencegah berkembangnya beberapa penyakit seperti aterosklerosis atau malaria berat.
CO adalah nutrien bagi bakteri metanogen,[12] sebuah blok pembangun untuk asetil koenzim A. Pada bakteri, CO diproduksi via reduksi karbon dioksida dengan enzom karbon monoksida dehirogenase, sebuah protein yang mengandung Fe-Ni-S.[13]
Dikenal juga sebuah protein sensor-CO yang berdasarkan heme, CooA.[14] Cakupan peranan biologis zat ini masih tidak jelas, namun tampaknya ia merupakan bagian dari lintasan signal pada bakteri dan arkea.
CO juga baru-baru ini dikaji di beberapa laboratorium riset di seluruh dunia atas sifatnya yang anti-peradangan dan sitoprotektif yang dapat digunakan untuk terapi pencegahan kondisi patologis seperti cedera reperfusi iskemia, penolakan trasplan, aterosklerosis, spesi, malaria berat, atau autoimunitas. Sampai sekarang ini tidak ada aplikasi medis CO kepada manusia.
Sejarah[sunting | sunting sumber]
Karbon monoksida pertama kali dihasilkan oleh kimiawan Prancis de Lassone pada tahun 1776 dengan memanaskan seng oksida dengan kokas. Dia menyimpulkan bahwa gas yang dihasilkan adalah hidrogen karena ketika dibakar ia menghasilkan lidah api berwarna biru. Gas ini kemudian diidentifikasi sebagai senyawa yang mengandung karbon dan oksigen oleh kimiawan Inggris William Cumberland Cruikshank pada tahun 1800.
Sifat-sifat CO yang beracun pertama kali diinvestigasi secara saksama oleh fisiolog Prancis Claude Bernard sekitar tahun 1846. Dia meracuni beberapa anjing dengan gas tersebut, dan mendapatkan bahwa darah anjing-anjing tersebut berwarna lebih merah di seluruh pembuluh darah.
Selama Perang Dunia II, karbon monoksida digunakan untuk menjaga kendaraan bermotor tetap berjalan di daerah-daerah yang kekurangan bensin. Pembakar batu-bara atau kayu dipasangkan, dan karbon monoksida yang diproduksi dengan gasifikasi dialirkan ke karburetor. CO dalam kasus ini dikenal sebagai "gas kayu". Karbon monoksida juga dilaporkan digunakan dalam skala kecil selama Holocaust di beberapa kamp eksterminasi Nazi dan di program "eutanasia" Aksi T4.
Konsentrasi sumber[sunting | sunting sumber]
- 0.1 ppm - kadar latar alami atmosfer (MOPITT)
- 0.5 to 5 ppm - rata-rata kadar latar di rumah[15]
- 5 to 15 ppm - kadar dekat kompor gas rumah[15]
- 100-200 ppm - daerah pusat kota Meksiko[16]
- 5,000 ppm - cerobong asap rumah dari pembakaran kayu [17]
- 7,000 ppm - gas knalpot mobil yang tidak diencerkan - tanpa pengubah katalitik[17]
- 30,000 ppm - asap rokok yang tidak diencerkan[17]
Toksisitas[sunting | sunting sumber]
Karbon monoksida sangatlah beracun dan tidak berbau maupun berwarna. Ia merupakan sebab utama keracunan yang paling umum terjadi di beberapa negara.[18] Paparan dengan karbon monoksida dapat mengakibatkan keracunan sistem saraf pusat dan jantung. Setelah keracunan, sering terjadi sekuelae yang berkepanjangan. Karbon monoksida juga memiliki efek-efek buruk bagi bayi dari wanita hamil. Gejala dari keracunan ringan meliputi sakit kepala dan mual-mual pada konsentrasi kurang dari 100 ppm. Konsentrasi serendah 667 ppm dapat menyebabkan 50% hemoglobin tubuh berubah menjadi karboksihemoglobin (HbCO). Karboksihemoglobin cukup stabil, namun perubahan ini reversibel. Karboksihemoglobin tidaklah efektif dalam menghantarkan oksigen, sehingga beberapa bagian tubuh tidak mendapatkan oksigen yang cukup. Sebagai akibatnya, paparan pada tingkap ini dapat membahayakan jiwa. Di Amerika Serikat, organisasi Administrasi Kesehatan dan Keselamatan Kerja membatasi paparan di tempat kerja sebesar 50 ppm.
Mekanisme bagaimana karbon monoksida mengakibatkan efek keracunan belum sepenuhnya dimegerti, namun hemoglobin, mioglobin, dan sitosom oksidase mitokondria diduga terkompromi (compromised). Kebanyakan pengobatan terdiri dari pemberian 100% oksigen atau terapi oksigen hiperbarik, walaupun pengobatan ini masih kontroversial.[19] Keracunan karbon monoksida domestik dapat dicegah dengan menggunakan detektor karbon monoksida.
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 200. ISBN 0-12-352651-5.
- ^ a b O. R. Gilliam, C. M. Johnson and W. Gordy (1950). "Microwave Spectroscopy in the Region from Two to Three Millimeters". Physical Review. 78 (2): 140. doi:10.1103/PhysRev.78.140.
- ^ W. Kutzelnigg. Einführung in die Theoretische Chemie. Wiley-VCH. ISBN 3-527-30609-9.
- ^ Elschenbroich, C.;Salzer, A. ”Organometallics : A Concise Introduction” (2nd Ed) Wiley-VCH: Weinheim, 2006. ISBN 3-527-28165-7
- ^ Mond L, Langer K, Quincke F (1890). "Action of carbon monoxide on nickel". Journal of the Chemical Society. 57: 749–753. doi:10.1039/CT8905700749.
- ^ Koch, H.; Haaf, W. "1-Adamantanecarboxylic Acid" Organic Syntheses, Collected Volume 5, p.20 (1973).
- ^ Coleman, G. H.; Craig, D. "p-Tolualdehyde" Organic Syntheses, Collected Volume 2, p.583 (1943).
- ^ Chatani, N.; Murai, S. "Carbon Monoxide" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI:10.1002/047084289
- ^ Sorheim, S, Nissena, H, Nesbakken, T (1999). "The storage life of beef and pork packaged in an atmosphere with low carbon monoxide and high carbon dioxide". Journal of Meat Science. 52 (2): 157–64. doi:10.1016/S0309-1740(98)00163-6.
- ^ Eilert EJ (2005). "New packaging technologies for the 21st century". Journal of Meat Science. 71 (1): 122–27. doi:10.1016/j.meatsci.2005.04.003.
- ^ "Low-Oxygen Packaging with CO: A Study in Food Politics That Warrants Peer Review". Diarsipkan dari versi asli tanggal 2007-09-10. Diakses tanggal 2007-04-18.
- ^ R. K. Thauer (1998). "Biochemistry of methanogenesis: a tribute to Marjory Stephenson. 1998 Marjory Stephenson Prize Lecture" (Free). Microbiology. 144 (9): 2377–2406.
- ^ Jaouen, G., Ed. (2006). Bioorganometallics: Biomolecules, Labeling, Medicine. Weinheim: Wiley-VCH. ISBN 3-527-30990-X.
- ^ Roberts, G. P.; Youn, H.; Kerby, R. L. (2004). "CO-Sensing Mechanisms". Microbiology and Molecular Biology Reviews. 68: 453–473. doi:10.1128/MMBR.68.3.453-473.2004. PMID 15353565.
- ^ a b "Basic Information : Carbon Monoxide". Diakses tanggal 2007-12-01.
- ^ Singer, Siegfried Fred (1975). The Changing Global Environment. hlm. pp. 90. ISBN 9789027704023.
- ^ a b c Gosink, Tom (1983-01-28). "What Do Carbon Monoxide Levels Mean?". Alaska Science Forum. Geophysical Institute, University of Alaska Fairbanks. Diarsipkan dari versi asli (HTML) tanggal 2008-12-25. Diakses tanggal 2007-12-01.
- ^ Omaye ST. (2002). "Metabolic modulation of carbon monoxide toxicity". Toxicology. 180 (2): 139–50. doi:10.1016/S0300-483X(02)00387-6.
- ^ Buckley NA, Isbister GK, Stokes B, Juurlink DN. (2005). "Hyperbaric oxygen for carbon monoxide poisoning : a systematic review and critical analysis of the evidence" (Abstract). Toxicol Rev. 24 (2): 75–92. PMID 16180928.[pranala nonaktif permanen]
Pranala luar[sunting | sunting sumber]
- www.infowars.com
- International Chemical Safety Card 0023
- National Pollutant Inventory - Carbon Monoxide Diarsipkan 2009-02-08 di Wayback Machine.
- NIOSH Pocket Guide to Chemical Hazards
- CID 281 dari PubChem
- United States Environmental Protection Agency Carbon Monoxide page
- External MSDS data sheet Diarsipkan 2006-05-16 di Wayback Machine.
- Carbon Monoxide Kills Awareness Campaign Site
- Carbon Monoxide Purification Process
- Carbon Monoxide Hazards with Backpacking Stoves
- USFDA IMPORT BULLETIN 16B-95, May 1999 Diarsipkan 2012-07-16 di Wayback Machine.
- FDA Agency Response Letter GRAS Notice No. GRN 000083 Diarsipkan 2007-04-11 di Wayback Machine.
- Carbon Monoxide in Fresh Meat site Diarsipkan 2007-03-25 di Wayback Machine.
- Carbon Monoxide Network & Forum
- Microscale Gas Chemistry Experiments with Carbon Monoxide
- Research on the therapeutic effects of CO (Gulbenkian Science Institute) Diarsipkan 2008-09-15 di Wayback Machine.
- Instant insight outlining the physiology of carbon monoxide from the Royal Society of Chemistry
- www.floridarealtors.org Diarsipkan 2016-03-06 di Wayback Machine. Article about Sen. Chris mandating CO detectors in new homes & hotels in Florida as of 2008.