Seng
| Seng | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Fragmen kristal dan kubus seng 1 cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Garis spektrum seng | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nama, lambang | seng, Zn | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | abu-abu perak | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seng dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 12 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | logam transisi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 3d10 4s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 18, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 692,68 K (419,53 °C, 787,15 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 1180 K (907 °C, 1665 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 7,14 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 6,57 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 7,32 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 115 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 25,470 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | −2, 0, +1, +2 (oksida amfoter) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,65 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 906,4 kJ/mol ke-2: 1733,3 kJ/mol ke-3: 3833 kJ/mol (artikel) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 134 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 122±4 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari van der Waals | 139 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | susunan padat heksagon (hcp) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 3850 m/s (pada s.k.) (di-roll) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 30,2 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 116 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 59,0 nΩ·m (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | diamagnetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | −11,4×10−6 cm3/mol (298 K)[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 108 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 43 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 70 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 2,5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 327–412 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-66-6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan | ahli metalurgi India (sebelum 1000 SM) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isolasi pertama | Andreas S. Marggraf (1746) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diketahui sebagai logam unik oleh | R. Samuccaya (1300) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop seng yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Seng atau timah sari[3] (Belanda: zink, Inggris: zinc, bahasa Latin: zincum) adalah sebuah unsur kimia dengan lambang Zn dan nomor atom 30. Seng adalah logam yang sedikit rapuh pada suhu kamar dan memiliki penampilan keabu-abuan keperakan ketika oksidasi dihilangkan. Ia merupakan unsur pertama dalam golongan 12 (IIB) dari tabel periodik. Dalam beberapa hal, seng secara kimiawi mirip dengan magnesium: kedua unsur ini hanya menunjukkan satu bilangan oksidasi normal (+2), dan ion Zn2+ dan Mg2+ memiliki ukuran yang sama.[catatan 1] Seng merupakan unsur paling melimpah ke-24 di kerak Bumi dan memiliki lima isotop stabil. Bijih seng yang paling umum adalah sfalerit (seng campuran), sebuah mineral seng sulfida. Lode terbesar yang bisa diterapkan berada di Australia, Asia, dan Amerika Serikat. Seng dimurnikan melalui pengapungan buih bijih, pemanggangan, dan ekstraksi akhir menggunakan listrik (pengekstraksian listrik).
Kuningan, sebuah paduan tembaga dan seng dalam berbagai proporsi, digunakan sejak milenium ketiga SM di wilayah Aegean dan wilayah yang saat ini meliputi Irak, Uni Emirat Arab, Kalmykia, Turkmenistan dan Georgia. Pada milenium kedua SM, ia digunakan di wilayah yang saat ini termasuk India Barat, Uzbekistan, Iran, Suriah, Irak, dan Israel.[4][5][6] Logam seng tidak diproduksi dalam skala besar sampai abad ke-12 di India, meskipun diketahui oleh orang Romawi dan Yunani kuno.[7] Tambang Rajasthan telah memberikan bukti pasti produksi seng sejak abad ke-6 SM.[8] Sampai saat ini, bukti tertua seng murni berasal dari Zawar, di Rajasthan, pada awal abad ke-9 M ketika proses penyulingan digunakan untuk membuat seng murni.[9] Para alkemis membakar seng di udara untuk membentuk apa yang mereka sebut "wol filsuf" atau "salju putih".
Unsur ini mungkin dinamai oleh alkemis Paracelsus dari kata bahasa Jerman Zinke (cabang, gigi). Kimiawan Jerman Andreas Sigismund Marggraf dikreditkan dengan menemukan seng logam murni pada tahun 1746. Karya Luigi Galvani dan Alessandro Volta menemukan sifat elektrokimia seng pada tahun 1800. Pelapisan seng tahan korosi dari besi (galvanisasi celup panas) merupakan aplikasi utama untuk seng. Aplikasi lainnya ialah dalam baterai listrik, coran nonstruktural kecil, dan paduan seperti kuningan. Berbagai senyawa seng yang umum digunakan, seperti seng karbonat dan seng glukonat (sebagai suplemen makanan), seng klorida (dalam deodoran), seng pirition (sampo anti ketombe), seng sulfida (dalam cat luminesen), dan dimetilseng atau dietilseng dalam laboratorium organik.
Seng merupakan sebuah mineral penting, yang diperlukan untuk perkembangan pranatal dan pascanatal.[10] Kekurangan seng mempengaruhi sekitar dua miliar orang di negara berkembang dan berhubungan dengan banyak penyakit.[11] Pada anak-anak, defisiensi menyebabkan retardasi pertumbuhan, keterlambatan pematangan seksual, kerentanan infeksi, dan diare.[10] Enzim dengan atom seng di pusat reaktif tersebar luas dalam biokimia, seperti alkohol dehidrogenase pada manusia.[12] Konsumsi seng berlebih dapat menyebabkan ataksia, letargi, dan kekurangan tembaga.
Karakteristik[sunting | sunting sumber]
Sifat fisik[sunting | sunting sumber]
Seng adalah logam diamagnetik berwarna putih kebiruan dan berkilau,[13] meskipun nilai komersial yang paling umum dari logam ini memiliki hasil akhir yang kusam.[14] Ia agak kurang padat daripada besi dan memiliki struktur kristal heksagon, dengan bentuk susunan padat heksagon terdistorsi, di mana setiap atom memiliki enam tetangga terdekat (pada jarak 265,9 pm) di bidangnya sendiri dan enam lainnya pada jarak yang lebih jauh (290,6 pm).[15] Logam ini keras dan rapuh pada sebagian besar suhu tetapi menjadi lunak antara suhu 100 hingga 150 °C.[13][14] Di atas suhu 210 °C, logam ini menjadi rapuh lagi dan dapat dihancurkan dengan cara dipukul.[16] Seng adalah konduktor listrik yang wajar.[13] Untuk sebuah logam, seng memiliki titik lebur dan titik didih yang relatif rendah (419,5 °C dan 907 °C).[17] Titik leburnya menjadi yang paling rendah dari semua logam blok-d lainnya selain raksa dan kadmium; untuk alasan ini di antara beberapa alasan lainnya, seng, kadmium, dan raksa sering tidak dianggap sebagai logam transisi seperti logam blok-d lainnya.[17]
Banyak paduan mengandung seng, termasuk kuningan. Logam lain yang telah lama diketahui membentuk paduan biner dengan seng adalah aluminium, antimon, bismut, emas, besi, timbal, raksa, perak, timah, magnesium, kobalt, nikel, telurium, dan natrium.[18] Meskipun baik seng maupun zirkonium tidak bersifat feromagnetik, paduan mereka, ZrZn2, menunjukkan feromagnetisme di bawah suhu 35 K.[13]
Keterjadian[sunting | sunting sumber]
Seng membentuk sekitar 75 ppm (0,0075%) dari kerak Bumi, menjadikannya unsur paling melimpah ke-24. Konsentrasi latar belakang seng yang khas tidak melebihi 1 μg/m3 di atmosfer; 300 mg/kg dalam tanah; 100 mg/kg dalam vegetasi; 20 μg/L di air tawar dan 5 μg/L di air laut.[19] Unsur ini biasanya ditemukan dalam hubungan dengan logam dasar lainnya seperti tembaga dan timbal dalam bijih.[20] Seng merupakan unsur kalkofil, artinya unsur ini lebih mungkin ditemukan dalam mineral bersama dengan belerang dan kalkogen berat lainnya, daripada dengan kalkogen ringan oksigen atau dengan unsur elektronegatif nonkalkogen seperti halogen. Sulfida terbentuk sebagai kerak yang memadat di bawah kondisi reduksi atmosfer Bumi awal.[21] Sfalerit, yang merupakan bentuk seng sulfida, adalah bijih yang mengandung seng yang paling banyak ditambang karena konsentratnya mengandung 60–62% seng.[20]
Sumber mineral lain untuk seng termasuk smithsonit (seng karbonat), hemimorfit (seng silikat), wurtzit (seng sulfida lain), dan kadang-kadang hidrozinkit (seng karbonat dasar).[22] Dengan pengecualian wurtzit, semua mineral lain ini dibentuk oleh pelapukan seng sulfida yang primordial.[21]
Sumber daya seng dunia yang teridentifikasi berjumlah sekitar 1,9–2,8 miliar ton.[23][24] Deposito besar berada di Australia, Kanada dan Amerika Serikat, dengan cadangan terbesar berada di Iran.[21][25][26] Perkiraan terbaru dari basis cadangan untuk seng (memenuhi kriteria fisik minimum yang ditentukan terkait dengan penambangan dan praktik produksi saat ini) dibuat pada tahun 2009 dan dihitung menjadi sekitar 480 Mt.[27] Di sisi lain, cadangan seng merupakan badan bijih yang diidentifikasi secara geologis yang kesesuaiannya untuk pemulihan berdasarkan ekonomi (lokasi, kadar, kualitas, dan kuantitas) pada saat penentuan. Karena eksplorasi dan pengembangan tambang merupakan proses yang berkelanjutan, jumlah cadangan seng bukanlah jumlah yang tetap dan keberlanjutan pasokan bijih seng tidak dapat dinilai hanya dengan mengekstrapolasi umur tambang gabungan dari tambang seng saat ini. Konsep ini didukung dengan baik oleh data dari Survei Geologi Amerika Serikat (USGS), yang menggambarkan bahwa meskipun produksi seng olahan meningkat 80% antara tahun 1990 dan 2010, masa pakai cadangan untuk seng tetap tidak berubah. Sekitar 346 juta ton seng telah diekstraksi sepanjang sejarah hingga tahun 2002, dan para ahli memperkirakan bahwa sekitar 109–305 juta ton seng telah digunakan.[28][29][30]

Isotop[sunting | sunting sumber]
Lima isotop stabil seng terdapat di alam, dengan 64Zn menjadi isotop yang paling melimpah (49,17% kelimpahan alami).[31][32] Isotop lain yang ditemukan di alam adalah 66Zn (27,73%), 67Zn (4,04%), 68Zn (18,45%), dan 70Zn (0,61%).[32]
Beberapa lusin radioisotop telah dikarakterisasi. 65Zn, yang memiliki waktu paruh 243,66 hari, adalah radioisotop yang paling tidak aktif, diikuti oleh 72Zn dengan waktu paruh 46,5 jam.[31] Seng memiliki 10 isomer nuklir. 69mZn memiliki waktu paruh terpanjang, 13,76 jam.[31] Superskrip m menunjukkan bahwa ia merupakan isotop metastabil. Inti isotop metastabil berada dalam keadaan tereksitasi dan akan kembali ke keadaan dasar dengan memancarkan foton dalam bentuk sinar gama. 61Zn memiliki tiga keadaan metastabil tereksitasi dan 73Zn memiliki dua.[33] Isotop 65Zn, 71Zn, 77Zn dan 78Zn masing-masing hanya memiliki satu keadaan metastabil tereksitasi.[31]
Mode peluruhan yang paling umum dari radioisotop seng dengan nomor massa lebih rendah dari 66 adalah penangkapan elektron. Produk peluruhan yang dihasilkan dari penangkapan elektron adalah isotop tembaga.[31]
- n
30Zn + e− → n
29Cu
Mode peluruhan yang paling umum dari radioisotop seng dengan nomor massa lebih tinggi dari 66 adalah peluruhan beta (β−), yang menghasilkan isotop galium.[31]
Senyawa dan sifat kimia[sunting | sunting sumber]
Reaktivitas[sunting | sunting sumber]
Seng memiliki konfigurasi elektron [Ar]3d104s2 dan merupakan anggota golongan 12 dari tabel periodik. Ia merupakan logam yang cukup reaktif dan zat pereduksi yang kuat.[34] Permukaan seng murni cepat ternoda, dan akhirnya membentuk lapisan pasivasi pelindung dari seng karbonat dasar, Zn5(OH)6(CO3)2, melalui reaksi dengan karbon dioksida atmosfer.[35]
Seng terbakar di udara dengan nyala hijau kebiruan terang, mengeluarkan asap seng oksida.[36] Seng mudah bereaksi dengan asam, alkali dan nonlogam lainnya.[37] Seng yang sangat murni hanya bereaksi lambat pada suhu kamar dengan asam.[36] Asam kuat, seperti asam klorida atau sulfat, dapat menghilangkan lapisan pasivasi dan reaksi selanjutnya dengan kedua asam tersebut melepaskan gas hidrogen.[36]
Sifat kimia seng didominasi oleh bilangan oksidasi +2. Ketika senyawa dalam bilangan oksidasi ini terbentuk, kulit terluar elektron s hilang, menghasilkan ion seng telanjang dengan konfigurasi elektron [Ar]3d10.[38] Dalam larutan berair kompleks oktahedron, [Zn(H2O)6]2+ merupakan spesies yang dominan.[39] Volatilisasi seng dalam kombinasi dengan seng klorida pada suhu di atas 285 °C menunjukkan pembentukan Zn2Cl2, senyawa seng dengan bilangan oksidasi +1.[36] Tidak ada senyawa seng dalam bilangan oksidasi positif selain +1 atau +2 yang diketahui.[40] Perhitungan menunjukkan bahwa senyawa seng dengan bilangan oksidasi +4 tidak mungkin ada.[41] Zn(III) diperkirakan ada dengan adanya trianion elektronegatif kuat;[42] namun, ada beberapa keraguan seputar kemungkinan ini.[43] Tetapi pada tahun 2021, senyawa lain telah dilaporkan dengan lebih banyak bukti yang memiliki bilangan oksidasi +3 dengan rumus ZnBeB11(CN)12.[44]
Sifat kimia seng mirip dengan sifat kimia logam transisi baris pertama akhir, nikel dan tembaga, meskipun ia memiliki kulit-d yang terisi dan senyawanya bersifat diamagnetik serta sebagian besar tidak berwarna.[45] Jari-jari ionik seng dan magnesium kebetulan hampir identik. Karena itu beberapa garam ekuivalen memiliki struktur kristal yang sama,[46] dan dalam keadaan lain di mana jari-jari ionik merupakan faktor penentu, sifat kimia seng memiliki banyak kesamaan dengan magnesium.[36] Dalam hal lain, ada sedikit kesamaan dengan logam transisi baris pertama akhir. Seng cenderung membentuk ikatan dengan tingkat kovalensi yang lebih besar dan kompleks yang jauh lebih stabil dengan donor -N dan -S.[45] Kompleks seng sebagian besar memiliki koordinasi -4 atau -6, meskipun kompleks koordinasi-5 juga telah diketahui.[36]
Senyawa seng(I)[sunting | sunting sumber]
Senyawa seng(I) sangatlah jarang. Ion [Zn2]2+ terlibat dalam pembentukan kaca diamagnetik kuning dengan melarutkan seng logam dalam ZnCl2 cair.[47] Inti [Zn2]2+ akan analog dengan kation [Hg2]2+ yang ada dalam senyawa raksa(I). Sifat diamagnetik ion ini menegaskan struktur dimernya. Senyawa seng(I) pertama yang mengandung ikatan Zn–Zn, (η5-C5Me5)2Zn2.
Senyawa seng(II)[sunting | sunting sumber]


Senyawa biner seng dikenal untuk sebagian besar metaloid dan semua nonlogam kecuali gas mulia. Seng oksida ZnO adalah bubuk putih yang hampir tidak larut dalam larutan berair netral, tetapi bersifat amfoter, larut dalam larutan basa kuat dan asam.[36] Kalkogenida seng lainnya (ZnS, ZnSe, dan ZnTe) memiliki aplikasi yang bervariasi dalam elektronika dan optika.[48] Seng pniktogenida (Zn3N2, Zn3P2, Zn3As2 dan Zn3Sb2),[49][50] seng peroksida (ZnO2), seng hidrida (ZnH2), dan seng karbida (ZnC2) juga telah diketahui.[51] Dari keempat halida seng, ZnF2 memiliki sifat ionik paling besar, sedangkan yang lainnya (ZnCl2, ZnBr2, dan ZnI2) memiliki titik lebur yang relatif rendah dan dianggap lebih bersifat kovalen.[52]
Dalam larutan basa lemah yang mengandung ion Zn2+, seng hidroksida (Zn(OH)2) terbentuk sebagai endapan putih. Dalam larutan alkali yang lebih kuat, hidroksida ini dilarutkan untuk membentuk zinkat ([Zn(OH)4]2−).[36] Seng nitrat (Zn(NO3)2), seng klorat (Zn(ClO3)2), seng sulfat (ZnSO4), seng fosfat (Zn3(PO4)2), seng molibdat (ZnMoO4), seng sianida (Zn(CN)2), seng arsenit (Zn(AsO2)2), seng arsenat (Zn(AsO4)2·8H2O), dan seng kromat (ZnCrO4) (salah satu dari sedikit senyawa seng berwarna) merupakan beberapa contoh senyawa anorganik umum lainnya dari seng.[53][54]
Senyawa organoseng merupakan senyawa yang mengandung ikatan kovalen seng–karbon. Dietilseng ((C2H5)2Zn) merupakan sebuah reagen dalam kimia sintetis. Ia pertama kali dilaporkan pada tahun 1848 dari reaksi seng dan etil iodida, dan merupakan senyawa pertama yang diketahui mengandung ikatan sigma logam–karbon.[55]
Tes untuk seng[sunting | sunting sumber]
Kertas Kobaltisianida (tes Rinnmann untuk Zn) dapat digunakan sebagai indikator kimia untuk seng. 4 gram K3Co(CN)6 dan 1 gram KClO3 dilarutkan dalam 100 ml air. Kertas dicelupkan ke dalam larutan dan dikeringkan pada suhu 100 °C. Satu tetes sampel diteteskan ke atas kertas kering dan dipanaskan. Cakram hijau menunjukkan adanya seng.[56]
Sejarah[sunting | sunting sumber]
Penggunaan kuno[sunting | sunting sumber]
Charaka Samhita, diperkirakan ditulis antara tahun 300 dan 500 M,[57] menyebutkan sebuah logam yang, ketika dioksidasi, menghasilkan pushpanjan, yang dianggap sebagai seng oksida.[58] Tambang seng di Zawar, dekat Udaipur di India, telah aktif sejak periode Maurya (sekitar 322 dan 187 SM). Peleburan seng logam di sini, bagaimanapun, tampaknya telah dimulai sekitar abad ke-12 M.[59][60] Satu perkiraan adalah bahwa lokasi ini menghasilkan sekitar satu juta ton seng logam dan seng oksida dari abad ke-12 hingga ke-16.[22] Perkiraan lain memberikan total produksi 60.000 ton seng logam selama periode ini.[59] Rasaratna Samuccaya, yang ditulis sekitar abad ke-13 M, menyebutkan dua jenis bijih yang mengandung seng: satu digunakan untuk ekstraksi logam dan lainnya digunakan untuk tujuan pengobatan.[60]

Berbagai contoh terisolasi dari penggunaan seng tidak murni di zaman kuno telah ditemukan. Bijih seng digunakan untuk membuat kuningan paduan seng–tembaga ribuan tahun sebelum penemuan seng sebagai unsur terpisah. Kuningan Yudea dari abad ke-14 hingga ke-10 SM mengandung 23% seng.[5]
Pengetahuan mengenai cara memproduksi kuningan menyebar ke Yunani Kuno pada abad ke-7 SM, tetapi hanya sedikit varietas yang dibuat.[6] Ornamen yang terbuat dari paduan yang mengandung 80–90% seng, dengan timbal, besi, antimon, dan logam lain yang menyusun sisanya, telah ditemukan berusia 2.500 tahun.[20] Sebuah patung prasejarah yang mungkin mengandung 87,5% seng ditemukan di situs arkeologi Dacia.[61]
Pil tertua yang diketahui terbuat dari seng karbonat, hidrozinkit, dan smithsonit. Pil-pil tersebut digunakan untuk sakit mata dan ditemukan di atas kapal Romawi Relitto del Pozzino yang karam pada 140 SM.[62][63]
Pembuatan kuningan dikenal oleh orang Romawi sekitar tahun 30 SM.[64] Mereka membuat kuningan dengan memanaskan kalamin bubuk (seng silikat atau karbonat), arang dan tembaga bersama-sama dalam wadah.[64] Kuningan kalamin yang dihasilkan kemudian dicor atau ditempa untuk digunakan dalam persenjataan.[65] Beberapa koin yang dibuat oleh orang Romawi di era Kristen terbuat dari kuningan kalamin.[66]
Tulisan Strabo pada abad ke-1 SM (tetapi mengutip karya sejarawan abad ke-4 SM Theopompos yang sekarang hilang) menyebutkan "tetesan perak palsu" yang bila dicampur dengan tembaga akan menghasilkan kuningan. Ini mungkin merujuk pada sejumlah kecil seng yang merupakan produk sampingan dari peleburan bijih sulfida.[67] Seng dalam sisa-sisa seperti itu dalam oven peleburan biasanya dibuang karena dianggap tidak berharga.[68]
Tablet seng Bern adalah sebuah plakat nazar yang berasal dari Galia Romawi yang terbuat dari paduan yang sebagian besar adalah seng.[69]
Studi awal dan penamaan[sunting | sunting sumber]
Seng secara jelas diakui sebagai logam di bawah sebutan Yasada atau Jasada dalam leksikon medis yang dianggap berasal dari raja Hindu Madanapala (dari dinasti Taka) dan ditulis sekitar tahun 1374.[70] Peleburan dan ekstraksi seng tidak murni dengan mereduksi kalamin dengan wol dan zat organik lainnya dilakukan pada abad ke-13 di India.[13][71] Orang Tiongkok tidak mempelajari teknik ini sampai abad ke-17.[71]

Para alkemis membakar logam seng di udara dan mengumpulkan seng oksida yang dihasilkan pada sebuah kondensor. Beberapa alkemis menyebut seng oksida ini sebagai lana philosophica, Latin untuk "wol filsuf", karena ia dikumpulkan dalam jumbai wol, sedangkan yang lain berpikir bahwa ia tampak seperti salju putih dan menamakannya nix album.[72]
Nama logam ini mungkin pertama kali didokumentasikan oleh Paracelsus, seorang alkemis Jerman kelahiran Swiss, yang menyebut logam ini sebagai "zincum" atau "zinken" dalam bukunya yang berjudul Liber Mineralium II, pada abad ke-16.[71][73] Kata ini mungkin berasal dari bahasa Jerman zinke, dan konon berarti "seperti gigi, runcing atau bergerigi" (kristal seng metalik memiliki penampilan seperti jarum).[74] Zink juga bisa berarti "mirip timah" karena hubungannya dengan zinn dari bahasa Jerman yang berarti timah.[75] Namun, kemungkinan lain menyatakan bahwa kata tersebut berasal dari kata Persia سنگ seng yang berarti batu.[76] Logam ini juga disebut timah India, tutanego, kalamin, dan spinter.[20]
Ahli metalurgi Jerman Andreas Libavius menerima sejumlah apa yang dia sebut "calay" Malabar dari sebuah kapal kargo yang ditangkap dari Portugis pada tahun 1596.[77] Libavius menggambarkan sifat-sifat sampel, yang mungkin adalah seng. Seng secara teratur diimpor ke Eropa dari Timur pada abad ke-17 dan awal abad ke-18,[71] tetapi pada waktu itu ia kadang-kadang sangat mahal.[catatan 2]
Isolasi[sunting | sunting sumber]

Seng logam diisolasi di India pada tahun 1300 M,[78][79][80] jauh lebih awal daripada di Barat. Sebelum diisolasi di Eropa, seng diimpor dari India sekitar tahun 1600 M.[81] Universal Dictionary Postlewayt, sumber kontemporer yang memberikan informasi teknologi di Eropa, tidak menyebutkan seng sebelum tahun 1751 tetapi unsur tersebut dipelajari sebelum itu.[60][82]
Ahli metalurgi dan alkemis Flemish P. M. de Respour melaporkan bahwa ia telah mengekstraksi seng logam dari seng oksida pada tahun 1668.[22] Pada awal abad ke-18, Étienne François Geoffroy menggambarkan bagaimana seng oksida mengembun sebagai kristal kuning pada batangan besi yang ditempatkan di atas bijih seng yang sedang dilebur.[22] Di Britania Raya, John Lane dikatakan telah melakukan eksperimen untuk melebur seng, mungkin di Landore, sebelum kebangkrutannya pada tahun 1726.[83]
Pada tahun 1738 di Britania Raya, William Champion mematenkan proses untuk mengekstrak seng dari kalamin dalam peleburan gaya retot vertikal.[84] Tekniknya mirip dengan yang digunakan di tambang seng Zawar di Rajasthan, tetapi tidak ada bukti yang menunjukkan bahwa dia mengunjungi Timur.[81] Proses Champion digunakan sampai tahun 1851.[71]
Kimiawan Jerman Andreas Marggraf biasanya mendapat pujian karena menemukan seng logam murni, meskipun ahli kimia Swedia Anton von Swab telah menyuling seng dari kalamin empat tahun sebelumnya.[71] Dalam percobaannya di tahun 1746, Marggraf memanaskan campuran kalamin dan arang dalam wadah tertutup tanpa tembaga untuk mendapatkan sebuah logam.[68][85] Prosedur ini menjadi praktis secara komersial pada tahun 1752.[86]
Pekerjaan berikutnya[sunting | sunting sumber]

Saudara William Champion, John, mematenkan sebuah proses pada tahun 1758 untuk mengalsinasi seng sulfida menjadi oksida yang dapat digunakan dalam proses retot.[20] Sebelum ini, hanya kalamin yang dapat digunakan untuk memproduksi seng. Pada tahun 1798, Johann Christian Ruberg meningkatkan proses peleburan dengan membangun pelebur retot horizontal pertama.[87] Jean-Jacques Daniel Dony membangun berbagai jenis pelebur seng horizontal di Belgia yang memproses lebih banyak seng.[71] Dokter Italia Luigi Galvani menemukan pada tahun 1780 bahwa menghubungkan sumsum tulang belakang katak yang baru dibedah ke rel besi yang dipasang dengan kait kuningan menyebabkan kaki katak berkedut.[88] Dia salah mengira dia telah menemukan kemampuan saraf dan otot untuk menciptakan listrik dan menyebut efek tersebut sebagai "listrik hewan".[89] Sel Galvanik dan proses galvanisasi dinamai untuk Luigi Galvani, dan penemuannya membuka jalan bagi baterai listrik, galvanisasi, dan proteksi katodik.[89]
Teman Galvani, Alessandro Volta, terus meneliti efek tadi dan menemukan tumpukan Volta pada tahun 1800.[88] Tumpukan Volta terdiri dari setumpuk sel Galvanik yang disederhanakan, masing-masing menjadi satu pelat tembaga dan satu seng yang dihubungkan oleh elektrolit. Dengan menumpuk unit-unit ini secara seri, tumpukan (atau "baterai") Volta secara keseluruhan memiliki tegangan yang lebih tinggi, yang dapat digunakan lebih mudah daripada sel tunggal. Listrik dihasilkan karena potensial Volta antara dua pelat logam membuat elektron mengalir dari seng ke tembaga dan menimbulkan korosi pada seng.[88]
Karakter nonmagnetik seng dan kurangnya warna dalam larutan menunda penemuan pentingnya untuk biokimia dan nutrisi.[90] Hal ini berubah pada tahun 1940 ketika karbonat anhidrase, enzim yang membersihkan karbon dioksida dari darah, terbukti memiliki seng di situs aktifnya.[90] Enzim pencernaan karboksipeptidase menjadi enzim yang mengandung seng kedua yang diketahui pada tahun 1955.[90]
Produksi[sunting | sunting sumber]
Penambangan dan pengolahan[sunting | sunting sumber]
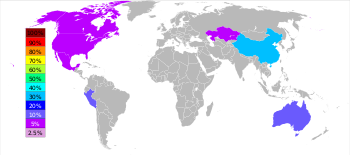
| Peringkat | Negara | Ton |
|---|---|---|
| 1 | Tiongkok | 4.210.000 |
| 2 | Peru | 1.400.000 |
| 3 | Australia | 1.330.000 |
| 4 | Amerika Serikat | 753.000 |
| 5 | India | 720.000 |
| 6 | Meksiko | 677.000 |

27°57′17″S 016°46′00″E / 27.95472°S 16.76667°E

27°49′09″S 016°36′28″E / 27.81917°S 16.60778°E
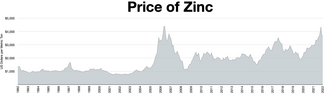
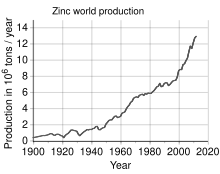
Seng adalah logam keempat yang paling umum digunakan, di bawah besi, aluminium, dan tembaga dengan produksi tahunan sekitar 13 juta ton.[23] Produsen seng terbesar di dunia adalah Nyrstar, penggabungan dari OZ Minerals Australia dan Umicore Belgia.[92] Sekitar 70% seng dunia berasal dari pertambangan, sedangkan 30% sisanya berasal dari daur ulang seng sekunder.[93] Seng murni komersial dikenal sebagai Special High Grade (Kelas Tinggi Khusus), sering disingkat sebagai SHG, dan murni 99,995%.[94]
Di seluruh dunia, 95% seng baru ditambang dari deposit bijih sulfida, di mana sfalerit (ZnS) hampir selalu dicampur dengan sulfida tembaga, timah, dan besi.[95] Tambang seng tersebar di seluruh dunia, dengan tambang utama seng berada di Tiongkok, Australia, dan Peru. Tiongkok menghasilkan 38% dari output seng global pada tahun 2014.[23]
Logam seng diproduksi menggunakan metalurgi ekstraktif.[96] Bijih seng ditumbuk halus, kemudian dimasukkan melalui pengapungan untuk memisahkan mineral dari gangue (berdasarkan sifat hidrofobisitas), untuk mendapatkan konsentrat bijih seng sulfida[96] yang terdiri sekitar 50% seng, 32% belerang, 13% besi, dan 5% SiO2.[96]
Pemanggangan mengubah konsentrat seng sulfida menjadi seng oksida:[95]
Sulfur dioksida digunakan untuk produksi asam sulfat, yang diperlukan untuk proses pelindian. Jika endapan seng karbonat, seng silikat, atau seng-spinel (seperti Deposit Skorpion di Namibia) digunakan untuk produksi seng, pemanggangan dapat dihilangkan.[97]
Untuk pemrosesan lebih lanjut, dua metode dasar digunakan: pirometalurgi atau pengekstraksian listrik. Pirometalurgi mereduksi seng oksida dengan karbon atau karbon monoksida pada 950 °C (1.740 °F) ke dalam logam, yang disuling sebagai uap seng untuk memisahkannya dari logam lain, yang tidak mudah menguap pada suhu tersebut.[98] Uap seng kemudian dikumpulkan dalam kondensor.[95] Persamaan di bawah ini menggambarkan proses ini:[95]
Dalam pengekstraksian listrik, seng dilindikan dari konsentrat bijih oleh asam sulfat dan kotoran diendapkan:[99]
Akhirnya, seng direduksi dengan elektrolisis.[95]
Asam sulfat diregenerasi dan didaur ulang ke langkah pelindian.
Ketika bahan baku tergalvanisasi diumpankan ke sebuah tanur busur listrik, seng dipulihkan dari debu dengan sejumlah proses, terutama proses Waelz (90% pada 2014).[100]
Dampak lingkungan[sunting | sunting sumber]
Penyempurnaan bijih seng sulfida menghasilkan sejumlah besar sulfur dioksida dan uap kadmium. Terak peleburan dan residu lainnya mengandung sejumlah besar logam. Sekitar 1,1 juta ton seng logam dan 130 ribu ton timbal ditambang dan dilebur di kota La Calamine dan Plombières di Belgia antara tahun 1806 dan 1882.[101] Tempat pembuangan dari operasi penambangan dan pelindian seng dan kadmium masa lalu serta sedimen Sungai Geul, mengandung jumlah logam yang tidak sepele.[101] Sekitar dua ribu tahun yang lalu, emisi seng dari pertambangan dan peleburan mencapai 10 ribu ton per tahun. Setelah meningkat 10 kali lipat dari tahun 1850, emisi seng mencapai puncaknya pada 3,4 juta ton per tahun pada 1980-an dan menurun menjadi 2,7 juta ton pada 1990-an, meskipun studi tahun 2005 mengenai troposfer Arktik menemukan bahwa konsentrasi di sana tidak mencerminkan penurunan. Emisi buatan manusia dan alami terjadi pada rasio 20 banding 1.[102]
Seng di sungai yang mengalir melalui kawasan industri dan pertambangan bisa mencapai 20 ppm.[103] Pengolahan limbah yang efektif sangat mengurangi hal ini; pemulihan di sepanjang Sungai Rhein, misalnya, telah menurunkan kadar seng hingga 50 ppb.[103] Konsentrasi seng serendah 2 ppm memengaruhi jumlah oksigen yang dapat dibawa ikan dalam darahnya.[104]
Tanah yang terkontaminasi seng dari penambangan, pemurnian, atau pemupukan dengan lumpur yang mengandung seng dapat mengandung beberapa gram seng per kilogram tanah kering. Kadar seng yang melebihi 500 ppm dalam tanah mengganggu kemampuan tanaman untuk menyerap logam-logam esensial lainnya, seperti besi dan mangan. Kadar seng dari 2000 ppm hingga 180.000 ppm (18%) telah dicatat di beberapa sampel tanah.[103]
Aplikasi[sunting | sunting sumber]
Aplikasi utama seng, diantaranya (angka diberikan untuk AS)[107]
- Galvanisasi (55%)
- Kuningan dan perunggu (16%)
- Paduan lainnya (21%)
- Lain-lain (8%)
Antikorosi dan baterai[sunting | sunting sumber]

Seng paling sering digunakan sebagai zat antikorosi,[108] dan galvanisasi (pelapisan besi atau baja) adalah bentuk yang paling dikenal. Pada tahun 2009 di Amerika Serikat, 55% atau 893.000 ton logam seng digunakan untuk galvanisasi.[107]
Seng lebih reaktif daripada besi atau baja dan dengan demikian akan menarik hampir semua oksidasi lokal sampai ia benar-benar terkorosi.[109] Lapisan permukaan pelindung oksida dan karbonat (Zn5(OH)6(CO3)2) terbentuk sebagai korosi seng.[110] Perlindungan ini bertahan bahkan setelah lapisan seng tergores tetapi menurun seiring waktu karena seng terkorosi.[110] Seng diterapkan secara elektrokimia atau sebagai seng cair melalui penyemprotan atau galvanisasi celup panas. Galvanisasi digunakan pada pagar rantai, pagar pengaman, jembatan gantung, tiang lampu, atap logam, penukar panas, dan badan mobil.[111]
Reaktivitas relatif seng dan kemampuannya untuk menarik oksidasi ke dirinya sendiri membuatnya menjadi anode pengorban dalam proteksi katodik (cathodic protection, CP). Misalnya, perlindungan katodik dari pipa yang terkubur dapat dicapai dengan menghubungkan anode yang terbuat dari seng ke pipa.[110] Seng bertindak sebagai anode (terminus negatif) dengan terkorosi secara perlahan saat mengalirkan arus listrik ke pipa baja.[110][catatan 3] Seng juga digunakan untuk melindungi logam yang terpapar air laut secara katodik.[112] Piringan seng yang menempel pada kemudi besi kapal akan perlahan terkorosi, sementara kemudi tetap utuh.[109] Demikian pula, sumbat seng yang dipasang pada baling-baling atau pelindung logam untuk lunas kapal memberikan perlindungan sementara.
Dengan potensial elektrode standar (standard electrode potential, SEP) sebesar −0,76 volt, seng digunakan sebagai bahan anode untuk baterai. (Litium yang lebih reaktif (SEP −3,04 V) digunakan untuk anode dalam baterai litium). Seng bubuk digunakan dengan cara ini dalam baterai alkalin dan pelindung (yang juga berfungsi sebagai anode) baterai seng–karbon dibentuk dari lembaran seng.[113][114] Seng digunakan sebagai anode atau bahan bakar sel bahan bakar/baterai seng–udara.[115][116][117] Baterai aliran redoks seng–serium juga bergantung pada setengah sel negatif berbasis seng.[118]
Paduan[sunting | sunting sumber]
Paduan seng yang banyak digunakan adalah kuningan, di mana tembaga dicampur dengan seng dari 3% hingga 45%, tergantung pada jenis kuningannya.[110] Kuningan umumnya lebih ulet dan lebih kuat dari tembaga, dan memiliki ketahanan korosi yang unggul.[110] Sifat-sifat ini membuatnya berguna dalam peralatan komunikasi, perangkat keras, alat musik, dan katup air.[110]

Paduan seng lain yang banyak digunakan, di antaranya perak nikel, logam mesin tik, solder lunak dan aluminium, dan perunggu komersial.[13] Seng juga digunakan dalam organ pipa kontemporer sebagai pengganti paduan timbal/timah tradisional dalam pipa.[119] Paduan 85–88% seng, 4–10% tembaga, dan 2–8% aluminium memilih penggunaan terbatas pada jenis bantalan mesin tertentu. Seng telah menjadi logam utama dalam koin satu sen Amerika (penny) sejak 1982.[120] Inti seng dilapisi dengan lapisan tipis tembaga untuk memberikan tampilan seperti koin tembaga. Pada tahun 1994, 33.200 ton (36.600 ton pendek) seng digunakan untuk menghasilkan 13,6 miliar sen di Amerika Serikat.[121]
Paduan seng dengan sejumlah kecil tembaga, aluminium, dan magnesium berguna dalam pengecoran mati (die casting) serta pengecoran berputar (spin casting), terutama dalam industri otomotif, listrik, dan perangkat keras.[13] Paduan-paduan ini dipasarkan dengan nama Zamak.[122] Contohnya adalah seng aluminium. Titik lebur yang rendah bersama dengan viskositas rendah dari paduan memungkinkan produksi bentuk kecil dan rumit. Suhu kerja yang rendah menyebabkan pendinginan yang cepat dari produk cor dan produksi yang cepat untuk perakitan.[13][123] Paduan lain, dipasarkan dengan merek Prestal, mengandung 78% seng dan 22% aluminium, dan dilaporkan hampir sekuat baja tetapi dapat ditempa seperti plastik.[13][124] Superplastisitas paduan ini memungkinkannya untuk dicetak menggunakan cetakan yang terbuat dari keramik dan semen.[13]
Paduan serupa dengan penambahan sedikit timbal dapat digulung dingin menjadi lembaran. Paduan seng 96% dan aluminium 4% digunakan untuk membuat stamping mati untuk aplikasi yang dijalankan dengan produksi rendah dimana logam besi mati akan terlalu mahal.[125] Untuk fasad bangunan, atap, dan aplikasi lain untuk logam lembaran yang dibentuk oleh deep drawing, pembentukan rol, atau pembengkokan, digunakanlah paduan seng dengan titanium dan tembaga.[126] Seng murni terlalu rapuh untuk proses manufaktur ini.[126]
Sebagai bahan padat, murah, mudah dikerjakan, seng digunakan sebagai pengganti timbal. Di tengah kekhawatiran timbal, seng muncul dalam bobot untuk berbagai aplikasi mulai dari memancing[127] hingga timbangan ban dan roda gila.[128]
Kadmium seng telurida (cadmium zinc telluride, CZT) adalah sebuah paduan semikonduktor yang dapat dibagi menjadi berbagai perangkat penginderaan kecil.[129] Perangkat ini mirip dengan sirkuit terpadu dan dapat mendeteksi energi foton sinar gama yang masuk.[129] Saat berada di balik topeng penyerap, susunan sensor CZT dapat menentukan arah sinar.[129]
Kegunaan industri lainnya[sunting | sunting sumber]

Kira-kira seperempat dari semua keluaran seng di Amerika Serikat pada tahun 2009 dikonsumsi dalam senyawa seng;[107] beberapa di antaranya digunakan secara industri. Seng oksida banyak digunakan sebagai pigmen putih pada cat dan sebagai katalis dalam pembuatan karet untuk mendispersikan panas. Seng oksida digunakan untuk melindungi polimer karet dan plastik dari radiasi ultraviolet (UV).[111] Sifat semikonduktor seng oksida membuatnya berguna dalam varistor dan produk fotokopi.[130] Siklus seng–seng oksida adalah sebuah proses termokimia dua langkah yang didasarkan pada seng dan seng oksida untuk produksi hidrogen.[131]
Seng klorida sering ditambahkan ke kayu sebagai penghambat api[132] dan terkadang sebagai pengawet kayu.[133] Ia digunakan dalam pembuatan bahan kimia lainnya.[132] Seng metil (Zn(CH3)2) digunakan dalam sejumlah sintetis organik.[134] Seng sulfida (ZnS) digunakan dalam pigmen bercahaya seperti pada jarum jam, sinar-X dan layar televisi, serta cat bercahaya.[135] Kristal ZnS digunakan dalam laser yang beroperasi di spektrum inframerah bagian tengah.[136] Seng sulfat adalah bahan kimia dalam pewarna dan pigmen.[132] Seng pirition digunakan dalam cat antipengotoran.[137]
Bubuk seng kadang-kadang digunakan sebagai propelan dalam roket model.[138] Ketika campuran terkompresi dari 70% bubuk seng dan 30% bubuk belerang dinyalakan, akan terjadi reaksi kimia yang hebat.[138] Reaksi ini akan menghasilkan seng sulfida, bersama dengan sejumlah besar panas, gas panas, dan cahaya.[138]
Lembaran logam seng digunakan untuk membuat bar seng.[139]
64Zn, isotop seng yang paling melimpah, sangat rentan terhadap pengaktifan neutron, ditransmutasikan menjadi 65Zn yang sangat radioaktif, yang memiliki waktu paruh 244 hari dan menghasilkan radiasi gama yang intens. Oleh karena itu, seng oksida yang digunakan dalam reaktor nuklir sebagai agen antikorosi merupakan 64Zn yang terdeplesi sebelum digunakan, dan ia disebut seng oksida terdeplesi. Untuk alasan yang sama, seng telah diusulkan sebagai bahan penggaraman untuk senjata nuklir (kobalt adalah bahan penggaraman lain yang lebih dikenal).[140] Jaket 64Zn yang diperkaya secara isotop akan disinari oleh fluks neutron berenergi tinggi yang intens dari senjata termonuklir yang meledak, membentuk 65Zn dalam jumlah besar yang secara signifikan meningkatkan radioaktivitas luruhan senjata.[140] Senjata seperti ini tidak diketahui pernah dibuat, diuji, atau digunakan.[140]
65Zn digunakan sebagai pelacak untuk mempelajari bagaimana paduan yang mengandung seng aus, atau jalur dan peran seng dalam organisme.[141]
Kompleks seng ditiokarbamat digunakan sebagai fungisida pertanian; mereka termasuk Zineb, Metiram, Propineb, dan Ziram.[142] Seng naftenat digunakan sebagai pengawet kayu.[143] Seng dalam bentuk ZDDP, digunakan sebagai aditif antiaus untuk bagian logam dalam oli mesin.[144]
Kimia organik[sunting | sunting sumber]

Kimia organoseng adalah ilmu mengenai senyawa yang mengandung ikatan karbon-seng, yang menggambarkan sifat fisik, sintesis, dan reaksi kimia. Banyak senyawa organoseng yang penting.[145][146][147][148] Beberapa di antaranya, yaitu
- Reaksi Frankland-Duppa Reaction di mana sebuah ester oksalat (ROCOCOOR) bereaksi dengan alkil halida R'X, seng dan asam klorida untuk membentuk ester α-hidroksikarboksilat RR'COHCOOR[149][150]
- Pada sisi negatifnya, organoseng jauh lebih sedikit nukleofilik daripada Grignards, dan harganya mahal serta sulit ditangani. Senyawa diorganoseng yang tersedia secara komersial adalah dimetilseng, dietilseng dan difenilseng. Dalam sebuah penelitian,[151][152] senyawa organoseng aktif diperoleh dari prekursor organobromin yang jauh lebih murah.
Seng memiliki banyak kegunaan sebagai katalis dalam sintesis organik termasuk sintesis asimetris, menjadi alternatif yang murah dan mudah tersedia untuk kompleks logam berharga. Hasil (hasil dan kelebihan enansiomer) yang diperoleh dengan katalis seng kiral sebanding dengan yang dicapai dengan paladium, rutenium, iridium dan lainnya, dan seng menjadi katalis logam pilihan.[153]
Suplemen makanan[sunting | sunting sumber]


Dalam kebanyakan tablet tunggal, obat bebas, suplemen vitamin dan mineral harian, seng dimasukkan dalam bentuk seperti seng oksida, seng asetat, seng glukonat, atau seng asam amino kelat.[154][155]
Umumnya, suplemen seng direkomendasikan di mana ada risiko tinggi kekurangan seng (seperti negara berpenghasilan rendah dan menengah) sebagai tindakan pencegahan.[156] Meskipun seng sulfat adalah bentuk seng yang umum digunakan, seng sitrat, glukonat, dan pikolinat mungkin juga merupakan pilihan yang valid. Bentuk-bentuk ini lebih baik diserap daripada seng oksida.[157]
Gastroenteritis[sunting | sunting sumber]
Seng adalah bagian dari pengobatan diare yang murah dan efektif pada anak-anak di negara berkembang. Seng menjadi terdeplesi dalam tubuh selama diare dan pengisian kembali seng dengan pengobatan 10 sampai 14 hari dapat mengurangi durasi dan keparahan diare dan juga dapat mencegah diare berikutnya selama tiga bulan.[158] Gastroenteritis sangat dilemahkan oleh konsumsi seng, mungkin dengan tindakan antimikroba langsung dari ion di saluran pencernaan, atau dengan penyerapan seng dan pelepasan kembali dari sel-sel kekebalan (semua granulosit menyekresi seng), atau keduanya.[159][160]
Pilek[sunting | sunting sumber]
Suplemen seng (seringkali pelega seng asetat atau seng glukonat) adalah sekelompok suplemen makanan yang biasanya digunakan untuk pengobatan pilek.[161] Penggunaan suplemen seng dengan dosis lebih dari 75 mg/hari dalam waktu 24 jam sejak timbulnya gejala telah terbukti mengurangi durasi gejala pilek sekitar 1 hari pada orang dewasa.[161][162] Efek samping dari pemberian suplemen seng melalui mulut adalah rasa tidak enak dan mual.[161][162] Penggunaan intranasal penyemprot hidung yang mengandung seng telah dikaitkan dengan hilangnya indra penciuman;[161] akibatnya, pada bulan Juni 2009, United States Food and Drug Administration (USFDA) memperingatkan konsumen untuk berhenti menggunakan seng intranasal.[161]
Rhinovirus manusia – patogen virus paling umum pada manusia – adalah penyebab utama pilek.[163] Mekanisme aksi yang dihipotesiskan dimana seng mengurangi keparahan dan/atau durasi gejala pilek adalah penekanan peradangan hidung dan penghambatan langsung dari pengikatan reseptor rhinovirus dan replikasi rhinovirus di mukosa hidung.[161]
Penambahan berat badan[sunting | sunting sumber]
Kekurangan seng dapat menyebabkan hilangnya nafsu makan.[164] Penggunaan seng dalam pengobatan anoreksia telah dianjurkan sejak 1979. Setidaknya 15 uji klinis telah menunjukkan bahwa seng meningkatkan penambahan berat badan pada anoreksia. Sebuah percobaan tahun 1994 menunjukkan bahwa seng menggandakan laju peningkatan massa tubuh dalam pengobatan anoreksia nervosa. Kekurangan nutrisi lain seperti tirosin, triptofan, dan tiamin dapat berkontribusi pada fenomena ini yang disebut "malnutrisi yang disebabkan oleh malnutrisi".[165] Sebuah meta-analisis dari 33 percobaan intervensi prospektif mengenai suplementasi seng dan pengaruhnya terhadap pertumbuhan anak-anak di banyak negara menunjukkan bahwa suplementasi seng saja memiliki efek yang signifikan secara statistik pada pertumbuhan linier dan penambahan berat badan, menunjukkan bahwa kekurangan zat lain yang mungkin telah hadir tidak bertanggung jawab atas keterbelakangan pertumbuhan.[166]
Lainnya[sunting | sunting sumber]
Sebuah tinjauan Cochrane menyatakan bahwa orang yang mengonsumsi suplemen seng mungkin lebih kecil kemungkinannya untuk menderita degenerasi makula terkait usia.[167] Suplemen seng adalah pengobatan yang efektif untuk acrodermatitis enteropathica, kelainan genetik yang mempengaruhi penyerapan seng yang sebelumnya berakibat fatal bagi bayi yang terkena.[64] Kekurangan seng telah dikaitkan dengan gangguan depresi mayor (major depressive disorder, MDD), dan suplemen seng mungkin merupakan pengobatan yang efektif.[168]
Penggunaan topikal[sunting | sunting sumber]
Sediaan topikal seng termasuk yang digunakan pada kulit, seringkali dalam bentuk seng oksida. Sediaan seng dapat melindungi kulit dari sengatan matahari di musim panas dan sengatan angin di musim dingin.[64] Dioleskan tipis pada area popok bayi (perineum) setiap kali mengganti popok, dapat melindungi bayi dari ruam popok.[64]
Seng yang dikelatkan digunakan dalam pasta gigi dan obat kumur untuk mencegah bau mulut; seng sitrat dapat membantu mengurangi pembentukan kalkulus (karang gigi).[169][170]
Seng pirition banyak disertakan dalam sampo untuk mencegah ketombe.[171]
Seng topikal juga telah terbukti efektif mengobati, serta memperpanjang remisi pada herpes genitali.[172]
Peran biologis[sunting | sunting sumber]
Seng merupakan sebuah unsur renik yang penting bagi manusia[173][174][175] dan hewan lainnya,[176] untuk tanaman[102] serta untuk mikroorganisme.[177] Seng diperlukan untuk fungsi lebih dari 300 enzim dan 1000 faktor transkripsi,[175] dan disimpan serta ditransfer dalam metalotionein.[178][179] Ia merupakan logam renik paling melimpah kedua pada manusia setelah besi dan merupakan satu-satunya logam yang muncul di semua kelas enzim.[102][175]
Dalam protein, ion seng sering dikoordinasikan dengan rantai samping asam amino dari asam aspartat, asam glutamat, sisteina, dan histidina. Deskripsi teoretis dan komputasional dari pengikatan seng dalam protein (dan juga logam transisi lainnya) adalah sulit.[180]
Kira-kira 2–4 gram seng[181] didistribusikan ke seluruh tubuh manusia. Sebagian besar seng berada di otak, otot, tulang, ginjal, dan hati, dengan konsentrasi tertinggi di prostat dan beberapa bagian mata.[182] Air mani sangatlah kaya akan seng, sebuah faktor kunci dalam fungsi kelenjar prostat dan pertumbuhan organ reproduksi.[183]
Homeostasis seng tubuh dikendalikan terutama oleh usus. Di sini, ZIP4 dan terutama TRPM7 dikaitkan dengan penyerapan seng usus yang penting untuk kelangsungan hidup pascakelahiran.[184][185]
Pada manusia, peran biologis seng ada di mana-mana.[10][174] Ia berinteraksi dengan "berbagai ligan organik",[10] dan memiliki peran dalam metabolisme RNA dan DNA, transduksi sinyal, serta ekspresi gen. Ia juga mengatur apoptosis. Sebuah tinjauan dari tahun 2015 menunjukkan bahwa sekitar 10% protein manusia (~3000) mengikat seng,[186] selain ratusan protein lainnya yang mengangkut seng; studi in silico serupa pada tanaman Arabidopsis thaliana menemukan 2367 protein terkait seng.[102]
Di otak, seng disimpan dalam vesikel sinaptik spesifik oleh neuron glutamatergik dan dapat memodulasi rangsangan saraf.[174][175][187] Ia memainkan peran kunci dalam plastisitas sinaptik dan dalam pembelajaran.[174][188] Homeostasis seng juga memainkan peran penting dalam regulasi fungsional sistem saraf pusat.[174][175][187] Disregulasi homeostasis seng di sistem saraf pusat yang menghasilkan konsentrasi seng sinaptik yang berlebihan diyakini menginduksi neurotoksisitas melalui stres oksidatif mitokondria (misalnya, dengan mengganggu enzim tertentu yang terlibat dalam rantai transpor elektron, termasuk kompleks I, kompleks III, dan α-ketoglutarat dehidrogenase), disregulasi homeostasis kalsium, eksitotoksisitas neuron glutamatergik, dan interferensi dengan transduksi sinyal intraneuronal.[174][189] L- dan D-histidina memfasilitasi penyerapan seng otak.[190] SLC30A3 adalah pengangkut seng utama yang terlibat dalam homeostasis seng serebral.[174]
Enzim[sunting | sunting sumber]


Seng merupakan sebuah asam Lewis yang efisien, membuatnya menjadi agen katalitik yang berguna dalam hidroksilasi dan reaksi enzimatik lainnya.[191] Logam ini juga memiliki geometri koordinasi yang fleksibel, yang memungkinkan protein menggunakannya untuk mengubah konformasi dengan cepat untuk melakukan reaksi biologis.[192] Dua contoh enzim yang mengandung seng adalah karbonat anhidrase dan karboksipeptidase, yang penting untuk proses karbon dioksida (CO2) regulasi dan pencernaan protein, masing-masing.[193]
Dalam darah vertebrata, karbonat anhidrase mengubah CO2 menjadi bikarbonat dan enzim yang sama mengubah bikarbonat kembali menjadi CO2 untuk pernafasan melalui paru-paru.[194] Tanpa enzim ini, konversi ini akan terjadi sekitar satu juta kali lebih lambat[195] pada pH darah normal 7 atau akan membutuhkan pH 10 atau lebih.[196] Karbonat anhidrase-β yang tidak terkait diperlukan pada tanaman untuk pembentukan daun, sintesis asam asetat indol (auksin) dan fermentasi alkohol.[197]
Karboksipeptidase memotong ikatan peptida selama pencernaan protein. Ikatan kovalen koordinasi terbentuk antara peptida terminal dan gugus C=O yang terikat pada seng, yang memberikan karbon muatan positif. Hal ini membantu penciptaan kantong hidrofobik pada enzim di dekat seng, yang menarik bagian nonpolar dari protein yang dicerna.[193]
Persinyalan[sunting | sunting sumber]
Seng telah diakui sebagai kurir, mampu mengaktifkan jalur persinyalan. Banyak dari jalur ini memberikan kekuatan pendorong dalam pertumbuhan kanker yang menyimpang. Mereka dapat ditargetkan melalui pengangkut ZIP.[198]
Protein lainnya[sunting | sunting sumber]
Seng melayani peran struktural murni dalam tikungan, gugus, dan jari seng.[199] Jari seng membentuk bagian dari beberapa faktor transkripsi, yaitu protein yang mengenali pengurutan berbasis DNA selama replikasi dan transkripsi DNA. Masing-masing dari sembilan atau sepuluh ion Zn2+ dalam jari seng membantu mempertahankan struktur jari tersebut dengan mengikat secara terkoordinasi empat asam amino dalam faktor transkripsi.[195]
Dalam plasma darah, seng terikat dan diangkut oleh albumin (60%, afinitas rendah) dan transferin (10%).[181] Karena transferin juga mengangkut zat besi, zat besi yang berlebihan mengurangi penyerapan seng, dan sebaliknya. Sebuah antagonisme serupa ada dengan tembaga.[200] Konsentrasi seng dalam plasma darah tetap relatif konstan terlepas dari asupan seng.[191] Sel-sel di kelenjar ludah, prostat, sistem kekebalan, dan usus menggunakan persinyalan seng untuk berkomunikasi dengan sel lain.[201]
Seng dapat disimpan dalam cadangan metalotionein dalam mikroorganisme atau di usus atau hati hewan.[202] Metalotionein dalam sel usus mampu mengatur penyerapan seng sebesar 15–40%.[203] Namun, asupan seng yang tidak memadai atau berlebihan dapat menjadi berbahaya; kelebihan seng secara khusus mengganggu penyerapan tembaga karena metalotionein menyerap kedua logam tersebut.[204]
Pengangkut dopamin manusia mengandung situs pengikatan seng ekstraseluler afinitas tinggi yang, pada pengikatan seng, menghambat pengambilan kembali dopamin dan memperkuat penghabisan dopamin yang diinduksi amfetamin secara in vitro.[205][206][207] Pengangkut serotonin dan pengangkut norepinefrin manusia tidak mengandung tempat pengikatan seng.[207] Beberapa protein pengikat kalsium tangan EF seperti S100 atau NCS-1 juga mampu mengikat ion seng.[208]
Nutrisi[sunting | sunting sumber]
Rekomendasi diet[sunting | sunting sumber]
US National Academy of Medicine (NAM) memperbarui Kebutuhan Perkiraan Rata-rata (Estimated Average Requirement, EAR) dan Angka Kecukupan Gizi (Recommended Dietary Allowance, RDA) untuk seng pada tahun 2001. EAR saat ini untuk seng untuk wanita dan pria berusia 14 tahun ke atas adalah masing-masing 6,8 dan 9,4 mg/hari. Untuk RDA-nya, yaitu 8 dan 11 mg/hari, masing-masing. Nilai RDA lebih tinggi dari EAR adalah untuk mengidentifikasi jumlah yang akan mencakup orang-orang dengan persyaratan yang lebih tinggi dari rata-rata. RDA untuk kehamilan adalah 11 mg/hari. RDA untuk laktasi adalah 12 mg/hari. Untuk bayi hingga 12 bulan, RDA mereka adalah 3 mg/hari. Untuk anak-anak usia 1–13 tahun, RDA mereka meningkat seiring bertambahnya usia, dari 3 hingga 8 mg/hari. Untuk keamanan, NAM menetapkan Batas Atas Asupan (upper level, UL) untuk vitamin dan mineral jika buktinya cukup. Dalam kasus seng, UL dewasa adalah 40 mg/hari (lebih rendah untuk anak-anak). Secara kolektif, EAR, RDA, AI, dan UL disebut sebagai Asupan Referensi Diet (Dietary Reference Intake, DRI).[191]
European Food Safety Authority (EFSA) mengacu pada kumpulan informasi sebagai Nilai Referensi Diet (Dietary Reference Values), dengan Asupan Referensi Populasi (Population Reference Intake, PRI) sebagai ganti RDA, dan Persyaratan Rata-rata (Average Requirement) sebagai ganti EAR. AI dan UL didefinisikan sama seperti di Amerika Serikat. Untuk orang berusia 18 tahun ke atas, perhitungan PRI menjadi rumit, karena EFSA telah menetapkan nilai yang lebih tinggi dan lebih tinggi seiring dengan peningkatan kandungan fitat dari makanan. Untuk wanita, PRI meningkat dari 7,5 menjadi 12,7 mg/hari karena asupan fitat meningkat dari 300 menjadi 1200 mg/hari; untuk pria kisarannya adalah 9,4 hingga 16,3 mg/hari. PRI ini lebih tinggi daripada RDA AS.[209] EFSA meninjau pertanyaan keamanan yang sama dan menetapkan UL-nya pada 25 mg/hari, yang jauh lebih rendah daripada nilai AS.[210]
Untuk tujuan pelabelan makanan dan suplemen makanan AS, jumlah dalam satu porsi dinyatakan sebagai persen Nilai Harian (%DV). Untuk tujuan pelabelan seng, 100% Nilai Harian adalah 15 mg, tetapi pada 27 Mei 2016, nilai ini direvisi menjadi 11 mg.[211][212] Tabel nilai harian dewasa lama dan baru disediakan di Referensi Asupan Harian (Reference Daily Intake, RDI).
Asupan makanan[sunting | sunting sumber]

Produk hewani seperti daging, ikan, kerang, unggas, telur, dan susu mengandung seng. Konsentrasi seng dalam tanaman bervariasi dengan tingkat seng di dalam tanah. Dengan kandungan seng yang cukup di dalam tanah, tanaman pangan yang paling banyak mengandung seng adalah gandum (kuman sereal dan bekatul) dan berbagai biji-bijian lainnya, seperti wijen, popi, alfalfa, seledri, serta moster.[213] Seng juga ditemukan dalam kacang, geluk, badam, serealia utuh, biji labu, biji bunga matahari, dan anggur hitam.[214]
Sumber lainnya adalah makanan yang difortifikasi dan suplemen makanan dalam berbagai bentuk. Sebuah tinjauan tahun 1998 menyimpulkan bahwa seng oksida, salah satu suplemen yang paling umum di Amerika Serikat, dan seng karbonat hampir tidak larut dan kurang diserap dalam tubuh.[215] Tinjauan ini mengutip studi yang menemukan konsentrasi seng plasma lebih rendah pada subjek yang mengonsumsi seng oksida dan seng karbonat dibandingkan mereka yang mengonsumsi seng asetat dan garam sulfat.[215] Untuk fortifikasi, bagaimanapun, tinjauan tahun 2003 merekomendasikan sereal (yang mengandung seng oksida) sebagai sumber yang murah dan stabil yang mudah diserap seperti bentuk yang lebih mahal.[216] Sebuah studi tahun 2005 menemukan bahwa berbagai senyawa seng, termasuk oksida dan sulfat, tidak menunjukkan perbedaan yang signifikan secara statistik dalam penyerapan ketika ditambahkan sebagai fortifikan pada tortilla jagung.[217]
Kekurangan seng[sunting | sunting sumber]
Hampir dua miliar orang di negara berkembang kekurangan seng. Kelompok yang paling berisiko adalah anak-anak di negara berkembang dan orang tua dengan penyakit kronis.[11] Pada anak-anak, kekurangan seng akan menyebabkan peningkatan infeksi dan diare dan berkontribusi pada kematian sekitar 800.000 anak di seluruh dunia per tahun.[10] World Health Organization menganjurkan suplementasi seng untuk malnutrisi parah dan diare.[218] Suplemen seng membantu mencegah penyakit dan mengurangi kematian, terutama di antara anak-anak dengan berat badan lahir rendah atau pertumbuhan terhambat.[218] Namun, suplemen seng tidak boleh diberikan sendiri, karena banyak di negara berkembang memiliki beberapa kekurangan, dan seng berinteraksi dengan zat gizi mikro lainnya.[219] Walaupun kekurangan seng biasanya karena asupan makanan yang tidak mencukupi, ia dapat dikaitkan dengan malabsorpsi, acrodermatitis enteropathica, penyakit hati kronis, penyakit ginjal kronis, penyakit sel sabit, diabetes, maligna, dan penyakit kronis lainnya.[11]
Di Amerika Serikat, survei federal mengenai konsumsi makanan menentukan bahwa untuk wanita dan pria di atas usia 19 tahun, konsumsi rata-rata adalah masing-masing 9,7 dan 14,2 mg/hari. Untuk wanita, 17% mengonsumsi kurang dari EAR, untuk pria 11%. Persentase di bawah EAR meningkat seiring bertambahnya usia.[220] Pembaruan survei terbaru yang diterbitkan (NHANES 2013–2014) melaporkan rata-rata yang lebih rendah – 9,3 dan 13,2 mg/hari – lagi-lagi dengan asupan yang menurun seiring bertambahnya usia.[221]
Gejala defisiensi seng ringan cukup beragam.[191] Hasil klinis termasuk pertumbuhan tertekan, diare, impotensi dan pematangan seksual tertunda, rambut rontok, lesi mata dan kulit, nafsu makan terganggu, kognisi berubah, gangguan fungsi kekebalan tubuh, cacat pemanfaatan karbohidrat, dan teratogenesis reproduksi.[191] Kekurangan seng akan menekan kekebalan,[222] tetapi kelebihan seng juga dapat menekan kekebalan.[181]
Terlepas dari beberapa kekhawatiran,[223] vegetarian dan vegan barat tidak menderita kekurangan seng lebih banyak daripada pemakan daging.[224] Sumber tanaman utama seng termasuk kacang kering yang dimasak, sayuran laut, sereal yang difortifikasi, makanan kedelai, kacang-kacangan, kacang polong, dan biji-bijian.[223] Namun, fitat dalam banyak biji-bijian dan serat dapat mengganggu penyerapan seng dan asupan seng marginal memiliki efek yang kurang dipahami. Fitat pengelat seng, yang ditemukan dalam biji-bijian dan bekatul sereal, dapat menyebabkan malabsorpsi seng.[11] Beberapa bukti menunjukkan bahwa lebih dari RDA AS (8 mg/hari untuk wanita dewasa; 11 mg/hari untuk pria dewasa) mungkin diperlukan pada mereka yang dietnya tinggi fitat, seperti beberapa vegetarian.[223] European Food Safety Authority (EFSA) mencoba untuk mengompensasi hal ini dengan merekomendasikan asupan seng yang lebih tinggi ketika asupan makanan fitat lebih besar.[209] Pertimbangan ini harus diimbangi dengan kekurangan biomarker seng yang memadai, dan indikator yang paling banyak digunakan, seng plasma, memiliki sensitivitas dan spesifisitas yang buruk.[225]
Remediasi tanah[sunting | sunting sumber]
Spesies Calluna, Erica, dan Vaccinium dapat tumbuh di tanah logam-seng, karena translokasi ion beracun dicegah oleh aksi jamur mikoriza erikoid.[226]
Agrikultur[sunting | sunting sumber]
Kekurangan seng tampaknya merupakan defisiensi mikronutrien yang paling umum pada tanaman pangan; hal ini sangat umum di tanah dengan pH tinggi.[227] Tanah yang kekurangan seng dibudidayakan di lahan pertanian sekitar setengah dari Turki dan India, sepertiga dari Tiongkok, dan sebagian besar Australia Barat. Respon substansial terhadap pemupukan seng telah dilaporkan di area-area ini.[102] Tanaman yang tumbuh di tanah yang kekurangan seng lebih rentan terhadap penyakit. Seng ditambahkan ke tanah terutama melalui pelapukan batuan, tetapi manusia telah menambahkan seng melalui pembakaran bahan bakar fosil, limbah tambang, pupuk fosfat, pestisida (seng fosfida), batu gamping, pupuk kandang, lumpur limbah, dan partikel dari permukaan tergalvanisasi. Kelebihan seng dapat menjadi racun bagi tanaman, meskipun toksisitas seng jauh lebih jarang terjadi.[102]
Tindakan pencegahan[sunting | sunting sumber]
Toksisitas[sunting | sunting sumber]
Meskipun seng merupakan persyaratan penting untuk kesehatan yang baik, kelebihan seng dapat menjadi berbahaya. Penyerapan seng yang berlebihan menekan penyerapan tembaga dan besi.[204] Ion seng bebas dalam larutan sangat beracun bagi tanaman, invertebrata, dan bahkan ikan vertebrata.[228] Model Aktivitas Ion Bebas sudah mapan dalam literatur, dan menunjukkan bahwa hanya sejumlah mikromolar dari ion bebas yang membunuh beberapa organisme. Contoh terbaru menunjukkan 6 mikromolar membunuh 93% dari semua Daphnia dalam air.[229]
Ion seng bebas adalah asam Lewis yang kuat hingga bersifat korosif. Asam lambung mengandung asam klorida, di mana seng logam mudah larut untuk menghasilkan seng klorida yang korosif. Menelan koin satu sen Amerika pasca-1982 (97,5% seng) dapat menyebabkan kerusakan pada lapisan perut melalui kelarutan tinggi ion seng dalam perut asam.[230]
Bukti menunjukkan bahwa orang yang mengonsumsi 100–300 mg seng setiap hari dapat menderita kekurangan tembaga yang diinduksi. Sebuah percobaan tahun 2007 mengamati bahwa pria lanjut usia yang mengonsumsi 80 mg setiap hari lebih sering dirawat di rumah sakit karena komplikasi saluran kemih daripada mereka yang menggunakan plasebo.[231] Tingkat 100–300 mg dapat mengganggu pemanfaatan tembaga dan besi atau mempengaruhi kolesterol.[204] Seng lebih dari 500 ppm di tanah mengganggu penyerapan tanaman dari logam esensial lainnya, seperti besi dan mangan.[103] Suatu kondisi yang disebut seng getar atau "seng dingin" dapat disebabkan oleh menghirup asap seng saat mematri atau mengelas bahan tergalvanisasi.[135] Seng merupakan bahan yang umum dalam krim gigi palsu yang mungkin mengandung antara 17 dan 38 mg seng per gram. Cacat dan bahkan kematian akibat penggunaan produk ini secara berlebihan telah diklaim.[232]
US Food and Drug Administration (FDA) menyatakan bahwa seng dapat merusak reseptor saraf di hidung, menyebabkan anosmia. Laporan anosmia juga teramati pada 1930-an ketika persiapan seng digunakan dalam upaya yang gagal untuk mencegah infeksi polio.[233] Pada 16 Juni 2009, FDA memerintahkan penghapusan produk dingin intranasal berbasis seng dari rak-rak toko. FDA mengatakan hilangnya penciuman dapat mengancam jiwa karena orang dengan gangguan penciuman tidak dapat mendeteksi kebocoran gas atau asap, dan tidak dapat mengetahui apakah makanan telah rusak sebelum mereka memakannya.[234]
Penelitian terbaru menunjukkan bahwa seng pirition antimikroba topikal adalah penginduksi respon kejutan panas yang kuat yang dapat merusak integritas genom dengan induksi krisis energi yang bergantung pada PARP pada keratinosit dan melanosit manusia yang dikultur.[235]
Keracunan[sunting | sunting sumber]
Pada tahun 1982, US Mint mulai mencetak uang logam berlapis tembaga tetapi mengandung terutama seng. Uang seng menimbulkan risiko toksikosis seng, yang dapat berakibat fatal. Satu kasus yang dilaporkan dari konsumsi kronis 425 sen (lebih dari 1 kg seng) mengakibatkan kematian karena sepsis bakteri dan jamur gastrointestinal. Pasien lain yang menelan 12 gram seng hanya menunjukkan letargi dan ataksia (kurangnya koordinasi gerakan otot).[236] Beberapa kasus lain telah dilaporkan mengenai manusia yang menderita keracunan seng karena menelan koin seng.[237][238]
Uang receh dan koin kecil lainnya terkadang tertelan oleh anjing, sehingga benda asing tersebut harus dikeluarkan oleh dokter hewan. Kandungan seng dari beberapa koin dapat menyebabkan keracunan seng, umumnya berakibat fatal pada anjing melalui anemia hemolitik parah dan kerusakan hati atau ginjal; muntah dan diare adalah gejala yang mungkin terjadi.[239] Seng sangat beracun pada burung bayan dan keracunan seringkali dapat berakibat fatal.[240] Konsumsi jus buah yang disimpan dalam kaleng tergalvanisasi telah mengakibatkan keracunan massal burung bayan akibat adanya kandungan seng.[64]
Lihat pula[sunting | sunting sumber]
- Daftar negara menurut produksi seng
- Spelter
- Karat putih
- Elektrogalvanisasi
- Demam asap logam
- Piotr Steinkeller
Catatan[sunting | sunting sumber]
- ^ Unsur-unsur tersebut berasal dari golongan logam yang berbeda. Lihat tabel periodik.
- ^ Sebuah kapal Perusahaan Hindia Timur Britania yang membawa muatan logam seng hampir murni dari Timur tenggelam di lepas pantai Swedia pada tahun 1745.(Emsley 2001, hlm. 502)
- ^ Arus listrik secara alami akan mengalir antara seng dan baja tetapi dalam beberapa keadaan anodr lengai digunakan dengan sumber DC eksternal.
Rujukan[sunting | sunting sumber]
- ^ (Indonesia) "Seng". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ (Indonesia) Arti kata timah sari dalam situs web Kamus Besar Bahasa Indonesia oleh Badan Pengembangan dan Pembinaan Bahasa, Kementerian Pendidikan dan Kebudayaan Republik Indonesia.
- ^ Thornton, C. P. (2007). Of brass and bronze in prehistoric Southwest Asia (PDF). Papers and Lectures Online. Archetype Publications. ISBN 978-1-904982-19-7. Diarsipkan dari versi asli (PDF) tanggal 24 September 2015.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1201
- ^ a b Craddock, Paul T. (1978). "The composition of copper alloys used by the Greek, Etruscan and Roman civilizations. The origins and early use of brass". Journal of Archaeological Science. 5 (1): 1–16. doi:10.1016/0305-4403(78)90015-8.
- ^ "Zinc - Royal Society Of Chemistry". Diarsipkan dari versi asli tanggal 11 Juli 2017.
- ^ "India Was the First to Smelt Zinc by Distillation Process". Infinityfoundation.com. Diarsipkan dari versi asli tanggal 16 Mei 2016. Diakses tanggal 26 Agustus 2022.
- ^ Kharakwal, J. S.; Gurjar, L. K. (1 Desember 2006). "Zinc and Brass in Archaeological Perspective". Ancient Asia. 1: 139–159. doi:10.5334/aa.06112
 .
.
- ^ a b c d e Hambidge, K. M.; Krebs, N. F. (2007). "Zinc deficiency: a special challenge". J. Nutr. 137 (4): 1101–5. doi:10.1093/jn/137.4.1101
 . PMID 17374687.
. PMID 17374687.
- ^ a b c d Prasad, AS (2003). "Zinc deficiency : Has been known of for 40 years but ignored by global health organisations". British Medical Journal. 326 (7386): 409–410. doi:10.1136/bmj.326.7386.409. PMC 1125304
 . PMID 12595353.
. PMID 12595353.
- ^ Maret, Wolfgang (2013). "Chapter 14 Zinc and the Zinc Proteome". Dalam Banci, Lucia. Metallomics and the Cell. Metal Ions in Life Sciences. 12. Springer. hlm. 479–501. doi:10.1007/978-94-007-5561-1_14. ISBN 978-94-007-5561-1. PMID 23595681.
- ^ a b c d e f g h i j CRC 2006, hlm. 4–41
- ^ a b Heiserman 1992, hlm. 123
- ^ Wells A.F. (1984) Structural Inorganic Chemistry edisi ke-5, hlm. 1277, Oxford Science Publications ISBN 0-19-855370-6
- ^ Scoffern, John (1861). The Useful Metals and Their Alloys. Houlston and Wright. hlm. 591–603. Diakses tanggal 26 Agustus 2022.
- ^ a b "Zinc Metal Properties". American Galvanizers Association. 2008. Diarsipkan dari versi asli tanggal 28 Maret 2015. Diakses tanggal 26 Agustus 2022.
- ^ Ingalls, Walter Renton (1902). Production and Properties of Zinc: A Treatise on the Occurrence and Distribution of Zinc Ore, the Commercial and Technical Conditions Affecting the Production of the Spelter, Its Chemical and Physical Properties and Uses in the Arts, Together with a Historical and Statistical Review of the Industry. The Engineering and Mining Journal. hlm. 142–6.
- ^ Rieuwerts, John (2015). The Elements of Environmental Pollution. London and New York: Earthscan Routledge. hlm. 286. ISBN 978-0-415-85919-6. OCLC 886492996.
- ^ a b c d e Lehto 1968, hlm. 822
- ^ a b c Greenwood & Earnshaw 1997, hlm. 1202
- ^ a b c d Emsley 2001, hlm. 502
- ^ a b c d Sai Srujan, A.V (2021). "Mineral Commodity Summaries 2021: Zinc" (PDF). USGS. Diakses tanggal 26 Agustus 2022.
- ^ Erickson, R. L. (1973). "Crustal Abundance of Elements, and Mineral Reserves and Resources". U.S. Geological Survey Professional Paper (820): 21–25.
- ^ "Country Partnership Strategy—Iran: 2011–12". ECO Trade and development bank. Diarsipkan dari versi asli tanggal 26 Oktober 2011. Diakses tanggal 26 Agustus 2022.
- ^ "IRAN – a growing market with enormous potential". IMRG. 5 Juli 2010. Diarsipkan dari versi asli tanggal 17 Februari 2013. Diakses tanggal 26 Agustus 2022.
- ^ Tolcin, A. C. (2009). "Mineral Commodity Summaries 2009: Zinc" (PDF). USGS. Diarsipkan dari versi asli (PDF) tanggal 2 Juli 2016. Diakses tanggal 26 Agustus 2022.
- ^ Gordon, R. B.; Bertram, M.; Graedel, T. E. (2006). "Metal stocks and sustainability". Proceedings of the National Academy of Sciences. 103 (5): 1209–14. Bibcode:2006PNAS..103.1209G. doi:10.1073/pnas.0509498103
 . PMC 1360560
. PMC 1360560  . PMID 16432205.
. PMID 16432205.
- ^ Gerst, Michael (2008). "In-Use Stocks of Metals: Status and Implications". Environmental Science and Technology. 42 (19): 7038–45. Bibcode:2008EnST...42.7038G. doi:10.1021/es800420p. PMID 18939524.
- ^ Meylan, Gregoire (2016). "The anthropogenic cycle of zinc: Status quo and perspectives". Resources, Conservation and Recycling. 123: 1–10. doi:10.1016/j.resconrec.2016.01.006.
- ^ a b c d e f Alejandro A. Sonzogni (Database Manager), ed. (2008). "Chart of Nuclides". Upton (NY): National Nuclear Data Center, Brookhaven National Laboratory. Diarsipkan dari versi asli tanggal 22 Mei 2008. Diakses tanggal 26 Agustus 2022.
- ^ a b Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003), "The NUBASE evaluation of nuclear and decay properties", Nuclear Physics A, 729: 3–128, Bibcode:2003NuPhA.729....3A, doi:10.1016/j.nuclphysa.2003.11.001
- ^ CRC 2006, hlm. 8–29
- ^ Porter, Frank C. (1994). Corrosion Resistance of Zinc and Zinc Alloys. CRC Press. hlm. 121. ISBN 978-0-8247-9213-8.
- ^ a b c d e f g h Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Zink". Lehrbuch der Anorganischen Chemie (dalam bahasa Jerman) (edisi ke-91–100). Walter de Gruyter. hlm. 1034–1041. ISBN 978-3-11-007511-3.
- ^ Hinds, John Iredelle Dillard (1908). Inorganic Chemistry: With the Elements of Physical and Theoretical Chemistry (edisi ke-2). New York: John Wiley & Sons. hlm. 506–508.
- ^ Ritchie, Rob (2004). Chemistry (edisi ke-2). Letts and Lonsdale. hlm. 71. ISBN 978-1-84315-438-9.
- ^ Burgess, John (1978). Metal ions in solution. New York: Ellis Horwood. hlm. 147. ISBN 978-0-470-26293-1.
- ^ Brady, James E.; Humiston, Gerard E.; Heikkinen, Henry (1983). General Chemistry: Principles and Structure (edisi ke-3). John Wiley & Sons. hlm. 671. ISBN 978-0-471-86739-5.
- ^ Kaupp M.; Dolg M.; Stoll H.; Von Schnering H. G. (1994). "Oxidation state +IV in group 12 chemistry. Ab initio study of zinc(IV), cadmium(IV), and mercury(IV) fluorides". Inorganic Chemistry. 33 (10): 2122–2131. doi:10.1021/ic00088a012.
- ^ Samanta, Devleena; Jena, Puru (2012). "Zn in the +III Oxidation State". Journal of the American Chemical Society. 134 (20): 8400–8403. doi:10.1021/ja3029119. PMID 22559713.
- ^ Schlöder, Tobias; et al. (2012). "Can Zinc Really Exist in Its Oxidation State +III?". Journal of the American Chemical Society. 134 (29): 11977–11979. doi:10.1021/ja3052409. PMID 22775535.
- ^ Fang, Hong; Banjade, Huta; Deepika; Jena, Puru (2021). "Realization of the Zn3+ oxidation state". Nanoscale. 13 (33): 14041–14048. doi:10.1039/D1NR02816B
 . PMID 34477685 Periksa nilai
. PMID 34477685 Periksa nilai |pmid=(bantuan). - ^ a b Greenwood & Earnshaw 1997, hlm. 1206
- ^ CRC 2006, hlm. 12–11–12
- ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (edisi ke-3rd). Prentice Hall. hlm. 739–741, 843. ISBN 978-0131755536.
- ^ "Zinc Sulfide". American Elements. Diarsipkan dari versi asli tanggal 17 Juli 2012. Diakses tanggal 28 Agustus 2022.
- ^ Academic American Encyclopedia. Danbury, Connecticut: Grolier Inc. 1994. hlm. 202. ISBN 978-0-7172-2053-3.
- ^ "Zinc Phosphide". American Elements. Diarsipkan dari versi asli tanggal 17 Juli 2012. Diakses tanggal 28 Agustus 2022.
- ^ Shulzhenko AA, Ignatyeva IY, Osipov AS, Smirnova TI (2000). "Peculiarities of interaction in the Zn–C system under high pressures and temperatures". Diamond and Related Materials. 9 (2): 129–133. Bibcode:2000DRM.....9..129S. doi:10.1016/S0925-9635(99)00231-9.
- ^ Greenwood & Earnshaw 1997, hlm. 1211
- ^ Rasmussen, J. K.; Heilmann, S. M. (1990). "In situ Cyanosilylation of Carbonyl Compounds: O-Trimethylsilyl-4-Methoxymandelonitrile". Organic Syntheses, Collected Volume. 7: 521. Diarsipkan dari versi asli tanggal 30 September 2007.
- ^ Perry, D. L. (1995). Handbook of Inorganic Compounds. CRC Press. hlm. 448–458. ISBN 978-0-8493-8671-8.
- ^ Frankland, E. (1850). "On the isolation of the organic radicals". Quarterly Journal of the Chemical Society. 2 (3): 263. doi:10.1039/QJ8500200263.
- ^ Lide, David (1998). CRC- Handbook of Chemistry and Physics. CRC Press. hlm. Bagian 8 Halaman 1. ISBN 978-0-8493-0479-8.
- ^ Meulenbeld, G. J. (1999). A History of Indian Medical Literature. IA. Groningen: Forsten. hlm. 130–141. OCLC 165833440.
- ^ Craddock, P. T.; et al. (1998). "Zinc in India". 2000 years of zinc and brass (edisi ke-rev.). London: British Museum. hlm. 27. ISBN 978-0-86159-124-4.
- ^ a b hlm. 46, Ancient mining and metallurgy in Rajasthan, S. M. Gandhi, bab 2 dalam Crustal Evolution and Metallogeny in the Northwestern Indian Shield: A Festschrift for Asoke Mookherjee, M. Deb, ed., Alpha Science Int'l Ltd., 2000, ISBN 1-84265-001-7.
- ^ a b c Craddock, P. T.; Gurjar L. K.; Hegde K. T. M. (1983). "Zinc production in medieval India". World Archaeology. 15 (2): 211–217. doi:10.1080/00438243.1983.9979899. JSTOR 124653.
- ^ Weeks 1933, hlm. 20
- ^ "World's oldest pills treated sore eyes". New Scientist. 7 Januari 2013. Diarsipkan dari versi asli tanggal 22 Januari 2013. Diakses tanggal 28 Agustus 2022.
- ^ Giachi, Gianna; Pallecchi, Pasquino; Romualdi, Antonella; Ribechini, Erika; Lucejko, Jeannette Jacqueline; Colombini, Maria Perla; Mariotti Lippi, Marta (2013). "Ingredients of a 2,000-y-old medicine revealed by chemical, mineralogical, and botanical investigations". Proceedings of the National Academy of Sciences. 110 (4): 1193–1196. Bibcode:2013PNAS..110.1193G. doi:10.1073/pnas.1216776110
 . PMC 3557061
. PMC 3557061  . PMID 23297212.
. PMID 23297212.
- ^ a b c d e f Emsley 2001, hlm. 501
- ^ "How is zinc made?". How Products are Made. The Gale Group. 2002. Diarsipkan dari versi asli tanggal 11 April 2006. Diakses tanggal 28 Agustus 2022.
- ^ Chambers 1901, hlm. 799
- ^ Craddock, P. T. (1998). "Zinc in classical antiquity". Dalam Craddock, P.T. 2000 years of zinc and brass (edisi ke-rev.). London: British Museum. hlm. 3–5. ISBN 978-0-86159-124-4.
- ^ a b Weeks 1933, hlm. 21
- ^ Rehren, Th. (1996). S. Demirci; et al., ed. A Roman zinc tablet from Bern, Switzerland: Reconstruction of the Manufacture. Archaeometry 94. The Proceedings of the 29th International Symposium on Archaeometry. hlm. 35–45.
- ^ Ray, Prafulla Chandra (1903). A History of Hindu Chemistry from the Earliest Times to the Middle of the Sixteenth Century, A.D.: With Sanskrit Texts, Variants, Translation and Illustrations. 1 (edisi ke-2). The Bengal Chemical & Pharmaceutical Works, Ltd. hlm. 157–158. (teks domain publik)
- ^ a b c d e f g Habashi, Fathi. "Discovering the 8th Metal" (PDF). International Zinc Association (IZA). Diarsipkan dari versi asli (PDF) tanggal 4 Maret 2009. Diakses tanggal 28 Agustus 2022.
- ^ Arny, Henry Vinecome (1917). Principles of Pharmacy (edisi ke-2). W. B. Saunders company. hlm. 483.
- ^ Hoover, Herbert Clark (2003). Georgius Agricola de Re Metallica. Kessinger Publishing. hlm. 409. ISBN 978-0-7661-3197-2.
- ^ Gerhartz, Wolfgang; et al. (1996). Ullmann's Encyclopedia of Industrial Chemistry (edisi ke-5). VHC. hlm. 509. ISBN 978-3-527-20100-6.
- ^ Skeat, W. W (2005). Concise Etymological Dictionary of the English Language. Cosimo, Inc. hlm. 622. ISBN 978-1-59605-092-1.
- ^ Fathi Habashi (1997). Handbook of Extractive Metallurgy. Wiley-VHC. hlm. 642. ISBN 978-3-527-28792-5.
- ^ Lach, Donald F. (1994). "Technology and the Natural Sciences". Asia in the Making of Europe. University of Chicago Press. hlm. 426. ISBN 978-0-226-46734-4.
- ^ Vaughan, L Brent (1897). "Zincography". The Junior Encyclopedia Britannica A Reference Library of General Knowledge Volume III P-Z. Chicago: E. G. Melven & Company.
- ^ Castellani, Michael. "Transition Metal Elements" (PDF). Diarsipkan dari versi asli (PDF) tanggal 10 Oktober 2014. Diakses tanggal 28 Agustus 2022.
- ^ Habib, Irfan (2011). Chatopadhyaya, D. P., ed. Economic History of Medieval India, 1200–1500. New Delhi: Pearson Longman. hlm. 86. ISBN 978-81-317-2791-1. Diarsipkan dari versi asli tanggal 14 April 2016.
- ^ a b Jenkins, Rhys (1945). "The Zinc Industry in England: the early years up to 1850". Transactions of the Newcomen Society. 25: 41–52. doi:10.1179/tns.1945.006.
- ^ Willies, Lynn; Craddock, P. T.; Gurjar, L. J.; Hegde, K. T. M. (1984). "Ancient Lead and Zinc Mining in Rajasthan, India". World Archaeology. 16 (2, Mines and Quarries): 222–233. doi:10.1080/00438243.1984.9979929. JSTOR 124574.
- ^ Roberts, R. O. (1951). "Dr John Lane and the foundation of the non-ferrous metal industry in the Swansea valley". Gower. Gower Society (4): 19.
- ^ Comyns, Alan E. (2007). Encyclopedic Dictionary of Named Processes in Chemical Technology (edisi ke-3). CRC Press. hlm. 71. ISBN 978-0-8493-9163-7.
- ^ Marggraf (1746). "Experiences sur la maniere de tirer le Zinc de sa veritable miniere, c'est à dire, de la pierre calaminaire" [Experiments on a way of extracting zinc from its true mineral; i.e., the stone calamine]. Histoire de l'Académie Royale des Sciences et Belles-Lettres de Berlin (dalam bahasa Prancis). 2: 49–57.
- ^ Heiserman 1992, hlm. 122
- ^ Gray, Leon (2005). Zinc. Marshall Cavendish. hlm. 8. ISBN 978-0-7614-1922-8.
- ^ a b c Warren, Neville G. (2000). Excel Preliminary Physics. Pascal Press. hlm. 47. ISBN 978-1-74020-085-1.
- ^ a b "Galvanic Cell". The New International Encyclopaedia. Dodd, Mead and Company. 1903. hlm. 80.
- ^ a b c Cotton et al. 1999, hlm. 626
- ^ Jasinski, Stephen M. "Mineral Commodity Summaries 2007: Zinc" (PDF). United States Geological Survey. Diarsipkan dari versi asli (PDF) tanggal 17 Desember 2008. Diakses tanggal 29 Agustus 2022.
- ^ Attwood, James (13 February 2006). "Zinifex, Umicore Combine to Form Top Zinc Maker". Wall Street Journal. Diarsipkan dari versi asli tanggal 26 Januari 2017.
- ^ "Zinc Recycling". International Zinc Association. Diarsipkan dari versi asli tanggal 21 Oktober 2011. Diakses tanggal 29 Agustus 2022.
- ^ "Special High Grade Zinc (SHG) 99.995%" (PDF). Nyrstar. 2008. Diarsipkan dari versi asli (PDF) tanggal 4 Maret 2009. Diakses tanggal 29 Agustus 2022.
- ^ a b c d e Porter, Frank C. (1991). Zinc Handbook. CRC Press. ISBN 978-0-8247-8340-2.
- ^ a b c Rosenqvist, Terkel (1922). Principles of Extractive Metallurgy (edisi ke-2). Tapir Academic Press. hlm. 7, 16, 186. ISBN 978-82-519-1922-7.
- ^ Borg, Gregor; Kärner, Katrin; Buxton, Mike; Armstrong, Richard; van der Merwe, Schalk W. (2003). "Geology of the Skorpion Supergene Zinc Deposit, Southern Namibia". Economic Geology. 98 (4): 749–771. doi:10.2113/98.4.749.
- ^ Bodsworth, Colin (1994). The Extraction and Refining of Metals. CRC Press. hlm. 148. ISBN 978-0-8493-4433-6.
- ^ Gupta, C. K.; Mukherjee, T. K. (1990). Hydrometallurgy in Extraction Processes. CRC Press. hlm. 62. ISBN 978-0-8493-6804-2.
- ^ Antrekowitsch, Jürgen; Steinlechner, Stefan; Unger, Alois; Rösler, Gernot; Pichler, Christoph; Rumpold, Rene (2014), "9. Zinc and Residue Recycling", dalam Worrell, Ernst; Reuter, Markus, Handbook of Recycling: State-of-the-art for Practitioners, Analysts, and Scientists
- ^ a b Kucha, H.; Martens, A.; Ottenburgs, R.; De Vos, W.; Viaene, W. (1996). "Primary minerals of Zn-Pb mining and metallurgical dumps and their environmental behavior at Plombières, Belgium". Environmental Geology. 27 (1): 1–15. Bibcode:1996EnGeo..27....1K. doi:10.1007/BF00770598.
- ^ a b c d e f Broadley, M. R.; White, P. J.; Hammond, J. P.; Zelko I.; Lux A. (2007). "Zinc in plants". New Phytologist. 173 (4): 677–702. doi:10.1111/j.1469-8137.2007.01996.x
 . PMID 17286818.
. PMID 17286818.
- ^ a b c d Emsley 2001, hlm. 504
- ^ Heath, Alan G. (1995). Water pollution and fish physiology. Boca Raton, Florida: CRC Press. hlm. 57. ISBN 978-0-87371-632-1.
- ^ "Derwent Estuary – Water Quality Improvement Plan for Heavy Metals". Derwent Estuary Program. Juni 2007. Diarsipkan dari versi asli tanggal 21 Maret 2012. Diakses tanggal 29 Agustus 2022.
- ^ "The Zinc Works". TChange. Diarsipkan dari versi asli tanggal 27 April 2009. Diakses tanggal 29 Agustus 2022.
- ^ a b c "Zinc: World Mine Production (zinc content of concentrate) by Country" (PDF). 2009 Minerals Yearbook: Zinc. Washington, D.C.: United States Geological Survey. February 2010. Diarsipkan dari versi asli (PDF) tanggal 8 Juni 2011. Diakses tanggal 29 Agustus 2022.
- ^ Greenwood & Earnshaw 1997, hlm. 1203
- ^ a b Stwertka 1998, hlm. 99
- ^ a b c d e f g Lehto 1968, hlm. 829
- ^ a b Emsley 2001, hlm. 503
- ^ Bounoughaz, M.; Salhi, E.; Benzine, K.; Ghali E.; Dalard F. (2003). "A comparative study of the electrochemical behaviour of Algerian zinc and a zinc from a commercial sacrificial anode". Journal of Materials Science. 38 (6): 1139–1145. Bibcode:2003JMatS..38.1139B. doi:10.1023/A:1022824813564.
- ^ Besenhard, Jürgen O. (1999). Handbook of Battery Materials. Wiley-VCH. Bibcode:1999hbm..book.....B. ISBN 978-3-527-29469-5.
- ^ Wiaux, J.-P.; Waefler, J. -P. (1995). "Recycling zinc batteries: an economical challenge in consumer waste management". Journal of Power Sources. 57 (1–2): 61–65. Bibcode:1995JPS....57...61W. doi:10.1016/0378-7753(95)02242-2.
- ^ Culter, T. (1996). "A design guide for rechargeable zinc–air battery technology". Southcon/96. Conference Record. hlm. 616. doi:10.1109/SOUTHC.1996.535134. ISBN 978-0-7803-3268-3.
- ^ Whartman, Jonathan; Brown, Ian. "Zinc Air Battery-Battery Hybrid for Powering Electric Scooters and Electric Buses" (PDF). The 15th International Electric Vehicle Symposium. Diarsipkan dari versi asli (PDF) tanggal 12 Maret 2006. Diakses tanggal 29 Agustus 2022.
- ^ Cooper, J. F.; Fleming, D.; Hargrove, D.; Koopman, R.; Peterman, K (1995). "A refuelable zinc/air battery for fleet electric vehicle propulsion". NASA Sti/Recon Technical Report N. Society of Automotive Engineers future transportation technology conference and exposition. 96: 11394. Bibcode:1995STIN...9611394C. OSTI 82465.
- ^ Xie, Z.; Liu, Q.; Chang, Z.; Zhang, X. (2013). "The developments and challenges of cerium half-cell in zinc–cerium redox flow battery for energy storage". Electrochimica Acta. 90: 695–704. doi:10.1016/j.electacta.2012.12.066.
- ^ Bush, Douglas Earl; Kassel, Richard (2006). The Organ: An Encyclopedia. Routledge. hlm. 679. ISBN 978-0-415-94174-7.
- ^ "Coin Specifications". United States Mint. Diarsipkan dari versi asli tanggal 18 Februari 2015. Diakses tanggal 29 Agustus 2022.
- ^ Jasinski, Stephen M. "Mineral Yearbook 1994: Zinc" (PDF). United States Geological Survey. Diarsipkan dari versi asli (PDF) tanggal 29 Oktober 2008. Diakses tanggal 29 Agustus 2022.
- ^ "Diecasting Alloys". Maybrook, NY: Eastern Alloys. Diarsipkan dari versi asli tanggal 25 Desember 2008. Diakses tanggal 29 Agustus.
- ^ Apelian, D.; Paliwal, M.; Herrschaft, D. C. (1981). "Casting with Zinc Alloys". Journal of Metals. 33 (11): 12–19. Bibcode:1981JOM....33k..12A. doi:10.1007/bf03339527.
- ^ Davies, Geoff (2003). Materials for automobile bodies. Butterworth-Heinemann. hlm. 157. ISBN 978-0-7506-5692-4.
- ^ Samans, Carl Hubert (1949). Engineering Metals and Their Alloys. Macmillan Co.
- ^ a b Porter, Frank (1994). "Wrought Zinc". Corrosion Resistance of Zinc and Zinc Alloys. CRC Press. hlm. 6–7. ISBN 978-0-8247-9213-8.
- ^ McClane, Albert Jules; Gardner, Keith (1987). The Complete book of fishing: a guide to freshwater, saltwater & big-game fishing. Gallery Books. ISBN 978-0-8317-1565-6. Diarsipkan dari versi asli tanggal 15 November 2012. Diakses tanggal 29 Agustus 2022.
- ^ "Cast flywheel on old Magturbo trainer has been recalled since July 2000". Minoura. Diarsipkan dari versi asli tanggal March 23, 2013.
- ^ a b c Katz, Johnathan I. (2002). The Biggest Bangs. Oxford University Press. hlm. 18. ISBN 978-0-19-514570-0.
- ^ Zhang, Xiaoge Gregory (1996). Corrosion and Electrochemistry of Zinc. Springer. hlm. 93. ISBN 978-0-306-45334-2.
- ^ Weimer, Al (17 Mei 2006). "Development of Solar-powered Thermochemical Production of Hydrogen from Water" (PDF). U.S. Department of Energy. Diarsipkan dari versi asli (PDF) tanggal 5 Februari 2009. Diakses tanggal 29 Agustus 2022.
- ^ a b c Heiserman 1992, hlm. 124
- ^ Blew, Joseph Oscar (1953). "Wood preservatives" (PDF). Department of Agriculture, Forest Service, Forest Products Laboratory. hdl:1957/816. Diarsipkan dari versi asli (PDF) tanggal 14 Januari 2012.
- ^ Frankland, Edward (1849). "Notiz über eine neue Reihe organischer Körper, welche Metalle, Phosphor u. s. w. enthalten". Liebig's Annalen der Chemie und Pharmacie (dalam bahasa Jerman). 71 (2): 213–216. doi:10.1002/jlac.18490710206.
- ^ a b CRC 2006, hlm. 4-42
- ^ Paschotta, Rüdiger (2008). Encyclopedia of Laser Physics and Technology. Wiley-VCH. hlm. 798. ISBN 978-3-527-40828-3.[pranala nonaktif permanen]
- ^ Konstantinou, I. K.; Albanis, T. A. (2004). "Worldwide occurrence and effects of antifouling paint booster biocides in the aquatic environment: a review". Environment International. 30 (2): 235–248. doi:10.1016/S0160-4120(03)00176-4. PMID 14749112.
- ^ a b c Boudreaux, Kevin A. "Zinc + Sulfur". Angelo State University. Diarsipkan dari versi asli tanggal 2 Desember 2008. Diakses tanggal 29 Agustus 2022.
- ^ "Technical Information". Zinc Counters. 2008. Diarsipkan dari versi asli tanggal 21 November 2008. Diakses tanggal 29 Agustus 2022.
- ^ a b c Win, David Tin; Masum, Al (2003). "Weapons of Mass Destruction" (PDF). Assumption University Journal of Technology. Assumption University. 6 (4): 199. Diarsipkan dari versi asli (PDF) tanggal 26 Maret 2009. Diakses tanggal 29 Agustus 2022.
- ^ David E. Newton (1999). Chemical Elements: From Carbon to Krypton. U. X. L. /Gale. ISBN 978-0-7876-2846-8. Diarsipkan dari versi asli tanggal 10 Juli 2008. Diakses tanggal 29 Agustus 2022.
- ^ Ullmann's Agrochemicals. Wiley-Vch (COR). 2007. hlm. 591–592. ISBN 978-3-527-31604-5.[pranala nonaktif permanen]
- ^ Walker, J. C. F. (2006). Primary Wood Processing: Principles and Practice. Springer. hlm. 317. ISBN 978-1-4020-4392-5.
- ^ "ZDDP Engine Oil – The Zinc Factor". Mustang Monthly. Diarsipkan dari versi asli tanggal 12 September 2009. Diakses tanggal 29 Agustus 2022.
- ^ Overman, Larry E.; Carpenter, Nancy E. (2005). The Allylic Trihaloacetimidate Rearrangement. Organic Reactions. 66. hlm. 1–107. doi:10.1002/0471264180.or066.01. ISBN 978-0-471-26418-7.
- ^ Rappoport, Zvi; Marek, Ilan (December 17, 2007). The Chemistry of Organozinc Compounds: R-Zn. ISBN 978-0-470-09337-5. Diarsipkan dari versi asli tanggal April 14, 2016.
- ^ Knochel, Paul; Jones, Philip (1999). Organozinc reagents: A practical approach. ISBN 978-0-19-850121-3. Diarsipkan dari versi asli tanggal April 14, 2016.
- ^ Herrmann, Wolfgang A. (Januari 2002). Synthetic Methods of Organometallic and Inorganic Chemistry: Catalysis. ISBN 978-3-13-103061-0. Diarsipkan dari versi asli tanggal April 14, 2016.
- ^ E. Frankland, Ann. 126, 109 (1863)
- ^ E. Frankland, B. F. Duppa, Ann. 135, 25 (1865)
- ^ Kim, Jeung Gon; Walsh, Patrick J. (2006). "From Aryl Bromides to Enantioenriched Benzylic Alcohols in a Single Flask: Catalytic Asymmetric Arylation of Aldehydes". Angewandte Chemie International Edition. 45 (25): 4175–4178. doi:10.1002/anie.200600741
 . PMID 16721894.
. PMID 16721894.
- ^ Dalam reaksi satu pot ini bromobenzena diubah menjadi fenillitium melalui reaksi dengan 4 ekuivalen n-butillitium, kemudian transmetalasi dengan seng klorida membentuk difenilseng yang terus bereaksi dalam reaksi asimetris dengan ligan MIB dan kemudian dengan 2-naftilaldehida menjadi alkohol. Dalam reaksi ini, pembentukan difenilseng disertai dengan litium klorida, yang jika tidak diperiksa, mengatalisis reaksi tanpa keterlibatan MIB dengan alkohol rasemat. Garam secara efektif dihilangkan melalui pengelatan dengan tetraetiletilena diamina (TEEDA) yang menghasilkan kelebihan enansiomer sebesar 92%.
- ^ Łowicki, Daniel; Baś, Sebastian; Mlynarski, Jacek (2015). "Chiral zinc catalysts for asymmetric synthesis". Tetrahedron. 71 (9): 1339–1394. doi:10.1016/j.tet.2014.12.022.
- ^ DiSilvestro, Robert A. (2004). Handbook of Minerals as Nutritional Supplements. CRC Press. hlm. 135, 155. ISBN 978-0-8493-1652-4.
- ^ "Zinc Sulphate vs. Zinc Amino Acid Chelate (ZAZO)". U.S. National Library of Medecine. USA Government. Diakses tanggal 29 Agustus 2022.
- ^ Mayo-Wilson, E; Junior, JA; Imdad, A; Dean, S; Chan, XH; Chan, ES; Jaswal, A; Bhutta, ZA (15 Mei 2014). "Zinc supplementation for preventing mortality, morbidity, and growth failure in children aged 6 months to 12 years of age". The Cochrane Database of Systematic Reviews (5): CD009384. doi:10.1002/14651858.CD009384.pub2. PMID 24826920.
- ^ Santos HO, Teixeira FJ, Schoenfeld BJ (2019). "Dietary vs. pharmacological doses of zinc: A clinical review". Clin Nutr. 130 (5): 1345–1353. doi:10.1016/j.clnu.2019.06.024. PMID 31303527.
- ^ Bhutta ZA, Bird SM, Black RE, Brown KH, Gardner JM, Hidayat A, Khatun F, Martorell R, et al. (2000). "Therapeutic effects of oral zinc in acute and persistent diarrhea in children in developing countries: pooled analysis of randomized controlled trials". The American Journal of Clinical Nutrition. 72 (6): 1516–1522. doi:10.1093/ajcn/72.6.1516
 . PMID 11101480.
. PMID 11101480.
- ^ Aydemir, T. B.; Blanchard, R. K.; Cousins, R. J. (2006). "Zinc supplementation of young men alters metallothionein, zinc transporter, and cytokine gene expression in leukocyte populations". PNAS. 103 (6): 1699–704. Bibcode:2006PNAS..103.1699A. doi:10.1073/pnas.0510407103
 . PMC 1413653
. PMC 1413653  . PMID 16434472.
. PMID 16434472.
- ^ Valko, M.; Morris, H.; Cronin, M. T. D. (2005). "Metals, Toxicity and Oxidative stress" (PDF). Current Medicinal Chemistry. 12 (10): 1161–208. doi:10.2174/0929867053764635. PMID 15892631. Diarsipkan dari versi asli (PDF) tanggal 8 Agustus 2017.
- ^ a b c d e f "Zinc – Fact Sheet for Health Professionals". Office of Dietary Supplements, US National Institutes of Health. 11 Februari 2016. Diakses tanggal 29 Agustus 2022.
- ^ a b Science M, Johnstone J, Roth DE, Guyatt G, Loeb M (Juli 2012). "Zinc for the treatment of the common cold: a systematic review and meta-analysis of randomized controlled trials". CMAJ. 184 (10): E551–61. doi:10.1503/cmaj.111990. PMC 3394849
 . PMID 22566526.
. PMID 22566526.
- ^ "Common Cold and Runny Nose". United States Centers for Disease Control and Prevention. 26 September 2017. Diakses tanggal 29 Agustus 2022.
- ^ Suzuki H, Asakawa A, Li JB, Tsai M, Amitani H, Ohinata K, Komai M, Inui A (2011). "Zinc as an appetite stimulator – the possible role of zinc in the progression of diseases such as cachexia and sarcopenia". Recent Patents on Food, Nutrition & Agriculture. 3 (3): 226–231. doi:10.2174/2212798411103030226. PMID 21846317.
- ^ Shay, Neil F.; Mangian, Heather F. (2000). "Neurobiology of Zinc-Influenced Eating Behavior". The Journal of Nutrition. 130 (5): 1493S–1499S. doi:10.1093/jn/130.5.1493S
 . PMID 10801965.
. PMID 10801965.
- ^ Rabinovich D, Smadi Y (2019). "Zinc". StatPearls [Internet]. PMID 31613478.
- ^ Evans JR, Lawrenson JG (2017). "Antioxidant vitamin and mineral supplements for slowing the progression of age-related macular degeneration". Cochrane Database Syst Rev. 7 (9): CD000254. doi:10.1002/14651858.CD000254.pub4. PMC 6483465
 . PMID 28756618.
. PMID 28756618.
- ^ Swardfager W, Herrmann N, McIntyre RS, Mazereeuw G, Goldberger K, Cha DS, Schwartz Y, Lanctôt KL (Juni 2013). "Potential roles of zinc in the pathophysiology and treatment of major depressive disorder". Neurosci. Biobehav. Rev. 37 (5): 911–929. doi:10.1016/j.neubiorev.2013.03.018. PMID 23567517.
- ^ Roldán, S.; Winkel, E. G.; Herrera, D.; Sanz, M.; Van Winkelhoff, A. J. (2003). "The effects of a new mouthrinse containing chlorhexidine, cetylpyridinium chloride and zinc lactate on the microflora of oral halitosis patients: a dual-centre, double-blind placebo-controlled study". Journal of Clinical Periodontology. 30 (5): 427–434. doi:10.1034/j.1600-051X.2003.20004.x. PMID 12716335.
- ^ "Toothpastes". www.ada.org. Diakses tanggal 30 Agustus 2022.
- ^ Marks, R.; Pearse, A. D.; Walker, A. P. (1985). "The effects of a shampoo containing zinc pyrithione on the control of dandruff". British Journal of Dermatology. 112 (4): 415–422. doi:10.1111/j.1365-2133.1985.tb02314.x. PMID 3158327.
- ^ Mahajan, BB; Dhawan, M; Singh, R (Januari 2013). "Herpes genitalis – Topical zinc sulfate: An alternative therapeutic and modality". Indian Journal of Sexually Transmitted Diseases and AIDS. 34 (1): 32–4. doi:10.4103/0253-7184.112867. PMC 3730471
 . PMID 23919052.
. PMID 23919052.
- ^ Maret, Wolfgang (2013). "Chapter 12. Zinc and Human Disease". Dalam Astrid Sigel; Helmut Sigel; Roland K. O. Sigel. Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences. 13. Springer. hlm. 389–414. doi:10.1007/978-94-007-7500-8_12. ISBN 978-94-007-7499-5. PMID 24470098.
- ^ a b c d e f g Prakash A, Bharti K, Majeed AB (April 2015). "Zinc: indications in brain disorders". Fundam Clin Pharmacol. 29 (2): 131–149. doi:10.1111/fcp.12110. PMID 25659970.
- ^ a b c d e Cherasse Y, Urade Y (November 2017). "Dietary Zinc Acts as a Sleep Modulator". International Journal of Molecular Sciences. 18 (11): 2334. doi:10.3390/ijms18112334
 . PMC 5713303
. PMC 5713303  . PMID 29113075.
. PMID 29113075. Seng adalah logam renik paling melimpah kedua di tubuh manusia, dan sangat penting untuk banyak proses biologis. ... Logam renik seng adalah kofaktor penting untuk lebih dari 300 enzim dan 1000 faktor transkripsi [16]. ... Dalam sistem saraf pusat, seng adalah logam renik paling melimpah kedua dan terlibat dalam banyak proses. Selain perannya dalam aktivitas enzimatik, ia juga memainkan peran utama dalam penyinyalan sel dan modulasi aktivitas neuron.
- ^ Prasad A. S. (2008). "Zinc in Human Health: Effect of Zinc on Immune Cells". Mol. Med. 14 (5–6): 353–7. doi:10.2119/2008-00033.Prasad. PMC 2277319
 . PMID 18385818.
. PMID 18385818.
- ^ Peran seng dalam mikroorganisme terutama ditinjau dalam: Sugarman B (1983). "Zinc and infection". Reviews of Infectious Diseases. 5 (1): 137–47. doi:10.1093/clinids/5.1.137. PMID 6338570.
- ^ Cotton et al. 1999, hlm. 625–629
- ^ Plum, Laura; Rink, Lothar; Haase, Hajo (2010). "The Essential Toxin: Impact of Zinc on Human Health". Int J Environ Res Public Health. 7 (4): 1342–1365. doi:10.3390/ijerph7041342
 . PMC 2872358
. PMC 2872358  . PMID 20617034.
. PMID 20617034.
- ^ Brandt, Erik G.; Hellgren, Mikko; Brinck, Tore; Bergman, Tomas; Edholm, Olle (2009). "Molecular dynamics study of zinc binding to cysteines in a peptide mimic of the alcohol dehydrogenase structural zinc site". Phys. Chem. Chem. Phys. 11 (6): 975–83. Bibcode:2009PCCP...11..975B. doi:10.1039/b815482a. PMID 19177216.
- ^ a b c Rink, L.; Gabriel P. (2000). "Zinc and the immune system". Proc Nutr Soc. 59 (4): 541–52. doi:10.1017/S0029665100000781
 . PMID 11115789.
. PMID 11115789.
- ^ Wapnir, Raul A. (1990). Protein Nutrition and Mineral Absorption. Boca Raton, Florida: CRC Press. ISBN 978-0-8493-5227-0.
- ^ Berdanier, Carolyn D.; Dwyer, Johanna T.; Feldman, Elaine B. (2007). Handbook of Nutrition and Food. Boca Raton, Florida: CRC Press. ISBN 978-0-8493-9218-4.
- ^ Mittermeier, Lorenz; Gudermann, Thomas; Zakharian, Eleonora; Simmons, David G.; Braun, Vladimir; Chubanov, Masayuki; Hilgendorff, Anne; Recordati, Camilla; Breit, Andreas (15 Februari 2019). "TRPM7 is the central gatekeeper of intestinal mineral absorption essential for postnatal survival". Proceedings of the National Academy of Sciences. 116 (10): 4706–4715. doi:10.1073/pnas.1810633116
 . ISSN 0027-8424. PMC 6410795
. ISSN 0027-8424. PMC 6410795  . PMID 30770447.
. PMID 30770447.
- ^ Kasana, Shakhenabat; Din, Jamila; Maret, Wolfgang (Januari 2015). "Genetic causes and gene–nutrient interactions in mammalian zinc deficiencies: acrodermatitis enteropathica and transient neonatal zinc deficiency as examples". Journal of Trace Elements in Medicine and Biology. 29: 47–62. doi:10.1016/j.jtemb.2014.10.003. ISSN 1878-3252. PMID 25468189.
- ^ Djoko KY, Ong CL, Walker MJ, McEwan AG (Juli 2015). "The Role of Copper and Zinc Toxicity in Innate Immune Defense against Bacterial Pathogens". The Journal of Biological Chemistry. 290 (31): 18954–61. doi:10.1074/jbc.R115.647099
 . PMC 4521016
. PMC 4521016  . PMID 26055706.
. PMID 26055706. Zn hadir dalam hingga 10% protein dalam proteom manusia dan analisis komputasi memperkirakan bahwa ~30% dari ~3000 protein yang mengandung Zn ini adalah enzim seluler yang penting, seperti hidrolase, ligase, transferase, oksidoreduktase, dan isomerase (42,43).
- ^ a b Bitanihirwe BK, Cunningham MG (November 2009). "Zinc: the brain's dark horse". Synapse. 63 (11): 1029–1049. doi:10.1002/syn.20683. PMID 19623531.
- ^ Nakashima AS; Dyck RH (2009). "Zinc and cortical plasticity". Brain Res Rev. 59 (2): 347–73. doi:10.1016/j.brainresrev.2008.10.003. PMID 19026685.
- ^ Tyszka-Czochara M, Grzywacz A, Gdula-Argasińska J, Librowski T, Wiliński B, Opoka W (Mei 2014). "The role of zinc in the pathogenesis and treatment of central nervous system (CNS) diseases. Implications of zinc homeostasis for proper CNS function" (PDF). Acta Pol. Pharm. 71 (3): 369–377. PMID 25265815. Diarsipkan dari versi asli (PDF) tanggal 29 Agustus 2017.
- ^ Yokel, R. A. (2006). "Blood-brain barrier flux of aluminum, manganese, iron and other metals suspected to contribute to metal-induced neurodegeneration". Journal of Alzheimer's Disease. 10 (2–3): 223–53. doi:10.3233/JAD-2006-102-309. PMID 17119290.
- ^ a b c d e Institute of Medicine (2001). "Zinc". Dietary Reference Intakes for Vitamin A, Vitamin K, Arsenic, Boron, Chromium, Copper, Iodine, Iron, Manganese, Molybdenum, Nickel, Silicon, Vanadium, and Zinc. Washington, DC: National Academy Press. hlm. 442–501. doi:10.17226/10026. ISBN 978-0-309-07279-3. PMID 25057538. Diarsipkan dari versi asli tanggal 19 September 2017.
- ^ Stipanuk, Martha H. (2006). Biochemical, Physiological & Molecular Aspects of Human Nutrition. W. B. Saunders Company. hlm. 1043–1067. ISBN 978-0-7216-4452-3.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1224–1225
- ^ Kohen, Amnon; Limbach, Hans-Heinrich (2006). Isotope Effects in Chemistry and Biology. Boca Raton, Florida: CRC Press. hlm. 850. ISBN 978-0-8247-2449-8.
- ^ a b Greenwood & Earnshaw 1997, hlm. 1225
- ^ Cotton et al. 1999, hlm. 627
- ^ Gadallah, MA (2000). "Effects of indole-3-acetic acid and zinc on the growth, osmotic potential and soluble carbon and nitrogen components of soybean plants growing under water deficit". Journal of Arid Environments. 44 (4): 451–467. Bibcode:2000JArEn..44..451G. doi:10.1006/jare.1999.0610.
- ^ Ziliotto, Silvia; Ogle, Olivia; Yaylor, Kathryn M. (2018). "Chapter 17. Targeting Zinc(II) Signalling to Prevent Cancer". Dalam Sigel, Astrid; Sigel, Helmut; Freisinger, Eva; Sigel, Roland K. O. Metallo-Drugs: Development and Action of Anticancer Agents. Metal Ions in Life Sciences. 18. Berlin: de Gruyter GmbH. hlm. 507–529. doi:10.1515/9783110470734-023. ISBN 9783110470734. PMID 29394036.
- ^ Cotton et al. 1999, hlm. 628
- ^ Whitney, Eleanor Noss; Rolfes, Sharon Rady (2005). Understanding Nutrition (edisi ke-10). Thomson Learning. hlm. 447–450. ISBN 978-1-4288-1893-4.
- ^ Hershfinkel, M; Silverman WF; Sekler I (2007). "The Zinc Sensing Receptor, a Link Between Zinc and Cell Signaling". Molecular Medicine. 13 (7–8): 331–336. doi:10.2119/2006-00038.Hershfinkel. PMC 1952663
 . PMID 17728842.
. PMID 17728842.
- ^ Cotton et al. 1999, hlm. 629
- ^ Blake, Steve (2007). Vitamins and Minerals Demystified. McGraw-Hill Professional. hlm. 242. ISBN 978-0-07-148901-0.
- ^ a b c Fosmire, G. J. (1990). "Zinc toxicity". American Journal of Clinical Nutrition. 51 (2): 225–7. doi:10.1093/ajcn/51.2.225. PMID 2407097.
- ^ Krause J (2008). "SPECT and PET of the dopamine transporter in attention-deficit/hyperactivity disorder". Expert Rev. Neurother. 8 (4): 611–625. doi:10.1586/14737175.8.4.611. PMID 18416663.
- ^ Sulzer D (2011). "How addictive drugs disrupt presynaptic dopamine neurotransmission". Neuron. 69 (4): 628–649. doi:10.1016/j.neuron.2011.02.010. PMC 3065181
 . PMID 21338876.
. PMID 21338876.
- ^ a b Scholze P, Nørregaard L, Singer EA, Freissmuth M, Gether U, Sitte HH (2002). "The role of zinc ions in reverse transport mediated by monoamine transporters". J. Biol. Chem. 277 (24): 21505–21513. doi:10.1074/jbc.M112265200
 . PMID 11940571.
. PMID 11940571. Pengangkut dopamin manusia (hDAT) mengandung situs pengikatan Zn2+ afinitas tinggi endogen dengan tiga residu koordinasi pada permukaan ekstraselulernya (His193, His375, dan Glu396). ... Jadi, ketika Zn2+ dilepaskan bersama dengan glutamat, ia dapat sangat meningkatkan penghabisan dopamin.
- ^ Tsvetkov, PO; Roman, AY; Baksheeva, VE; Nazipova, AA; Shevelyova, MP; Vladimirov, VI; Buyanova, MF; Zinchenko, DV; Zamyatnin AA, Jr; Devred, F; Golovin, AV; Permyakov, SE; Zernii, EY (2018). "Functional Status of Neuronal Calcium Sensor-1 Is Modulated by Zinc Binding". Frontiers in Molecular Neuroscience. 11: 459. doi:10.3389/fnmol.2018.00459
 . PMC 6302015
. PMC 6302015  . PMID 30618610.
. PMID 30618610.
- ^ a b "Overview on Dietary Reference Values for the EU population as derived by the EFSA Panel on Dietetic Products, Nutrition and Allergies" (PDF). 2017. Diarsipkan dari versi asli (PDF) tanggal 28 Agustus 2017.
- ^ Tolerable Upper Intake Levels For Vitamins And Minerals (PDF), European Food Safety Authority, 2006, diarsipkan dari versi asli (PDF) tanggal 16 Maret 2016
- ^ "Federal Register May 27, 2016 Food Labeling: Revision of the Nutrition and Supplement Facts Labels. FR page 33982" (PDF). Diarsipkan dari versi asli (PDF) tanggal 8 Agustus 2016.
- ^ "Daily Value Reference of the Dietary Supplement Label Database (DSLD)". Dietary Supplement Label Database (DSLD). Diarsipkan dari versi asli tanggal 7 April 2020. Diakses tanggal 30 Agustus 2022.
- ^ Ensminger, Audrey H.; Konlande, James E. (1993). Foods & Nutrition Encyclopedia (edisi ke-2). Boca Raton, Florida: CRC Press. hlm. 2368–2369. ISBN 978-0-8493-8980-1.
- ^ "Zinc content of selected foods per common measure" (PDF). USDA National Nutrient Database for Standard Reference, Release 20. United States Department of Agriculture. Diarsipkan dari versi asli (PDF) tanggal 5 Maret 2009. Diakses tanggal 30 Agustus 5.
- ^ a b Allen, Lindsay H. (1998). "Zinc and micronutrient supplements for children". American Journal of Clinical Nutrition. 68 (2 Suppl): 495S–498S. doi:10.1093/ajcn/68.2.495S
 . PMID 9701167.
. PMID 9701167.
- ^ Rosado, J. L. (2003). "Zinc and copper: proposed fortification levels and recommended zinc compounds". Journal of Nutrition. 133 (9): 2985S–9S. doi:10.1093/jn/133.9.2985S
 . PMID 12949397.
. PMID 12949397.
- ^ Hotz, C.; DeHaene, J.; Woodhouse, L. R.; Villalpando, S.; Rivera, J. A.; King, J. C. (2005). "Zinc absorption from zinc oxide, zinc sulfate, zinc oxide + EDTA, or sodium-zinc EDTA does not differ when added as fortificants to maize tortillas". Journal of Nutrition. 135 (5): 1102–5. doi:10.1093/jn/135.5.1102
 . PMID 15867288.
. PMID 15867288.
- ^ a b "The impact of zinc supplementation on childhood mortality and severe morbidity". World Health Organization. 2007. Diarsipkan dari versi asli tanggal 2 Maret 2009.
- ^ Shrimpton, R; Gross R; Darnton-Hill I; Young M (2005). "Zinc deficiency: what are the most appropriate interventions?". British Medical Journal. 330 (7487): 347–349. doi:10.1136/bmj.330.7487.347. PMC 548733
 . PMID 15705693.
. PMID 15705693.
- ^ Moshfegh, Alanna; Goldman, Joseph; Cleveland, Linda (2005). "NHANES 2001–2002: Usual Nutrient Intakes from Food Compared to Dietary Reference Intakes" (PDF). U.S. Department of Agriculture, Agricultural Research Service. Table A13: Zinc. Diakses tanggal 30 Agustus 2022.
- ^ What We Eat In America, NHANES 2013–2014 Diarsipkan 24 Februari 2017 di Wayback Machine..
- ^ Ibs, KH; Rink L (2003). "Zinc-altered immune function". Journal of Nutrition. 133 (5 Suppl 1): 1452S–1456S. doi:10.1093/jn/133.5.1452S
 . PMID 12730441.
. PMID 12730441.
- ^ a b c American Dietetic Association (2003). "Position of the American Dietetic Association and Dietitians of Canada: Vegetarian diets" (PDF). Journal of the American Dietetic Association. 103 (6): 748–765. doi:10.1053/jada.2003.50142. PMID 12778049. Diarsipkan dari versi asli (PDF) tanggal 14 Januari 2017.
- ^ Freeland-Graves JH; Bodzy PW; Epright MA (1980). "Zinc status of vegetarians". Journal of the American Dietetic Association. 77 (6): 655–661. doi:10.1016/S1094-7159(21)03587-X. PMID 7440860.
- ^ Hambidge, M (2003). "Biomarkers of trace mineral intake and status". Journal of Nutrition. 133. 133 (3): 948S–955S. doi:10.1093/jn/133.3.948S
 . PMID 12612181.
. PMID 12612181.
- ^ Geoffrey Michael Gadd (Maret 2010). "Metals, minerals and microbes: geomicrobiology and bioremediation". Microbiology. 156 (3): 609–643. doi:10.1099/mic.0.037143-0
 . PMID 20019082. Diarsipkan dari versi asli tanggal 25 Oktober 2014.
. PMID 20019082. Diarsipkan dari versi asli tanggal 25 Oktober 2014.
- ^ Alloway, Brian J. (2008). "Zinc in Soils and Crop Nutrition, International Fertilizer Industry Association, and International Zinc Association". Diarsipkan dari versi asli tanggal 19 Februari 2013.
- ^ Eisler, Ronald (1993). "Zinc Hazard to Fish, Wildlife, and Invertebrates: A Synoptic Review" (PDF). Contaminant Hazard Reviews. Laurel, Maryland: U.S. Department of the Interior, Fish and Wildlife Service (10). Diarsipkan dari versi asli tanggal 6 Maret 2012.
- ^ Muyssen, Brita T. A.; De Schamphelaere, Karel A. C.; Janssen, Colin R. (2006). "Mechanisms of chronic waterborne Zn toxicity in Daphnia magna". Aquatic Toxicology. 77 (4): 393–401. doi:10.1016/j.aquatox.2006.01.006. PMID 16472524.
- ^ Bothwell, Dawn N.; Mair, Eric A.; Cable, Benjamin B. (2003). "Chronic Ingestion of a Zinc-Based Penny". Pediatrics. 111 (3): 689–91. doi:10.1542/peds.111.3.689. PMID 12612262.
- ^ Johnson AR; Munoz A; Gottlieb JL; Jarrard DF (2007). "High dose zinc increases hospital admissions due to genitourinary complications". J. Urol. 177 (2): 639–43. doi:10.1016/j.juro.2006.09.047. PMID 17222649.
- ^ "Lawsuits blame denture adhesives for neurological damage". Tampa Bay Times. 15 Februari 2010. Diarsipkan dari versi asli tanggal 18 Februari 2010.
- ^ Oxford, J. S.; Öberg, Bo (1985). Conquest of viral diseases: a topical review of drugs and vaccines. Elsevier. hlm. 142. ISBN 978-0-444-80566-9.
- ^ "FDA says Zicam nasal products harm sense of smell". Los Angeles Times. 17 Juni 2009. Diarsipkan dari versi asli tanggal 21 Juni 2012.
- ^ Lamore SD; Cabello CM; Wondrak GT (2010). "The topical antimicrobial zinc pyrithione is a heat shock response inducer that causes DNA damage and PARP-dependent energy crisis in human skin cells". Cell Stress Chaperones. 15 (3): 309–22. doi:10.1007/s12192-009-0145-6. PMC 2866994
 . PMID 19809895.
. PMID 19809895.
- ^ Barceloux, Donald G.; Barceloux, Donald (1999). "Zinc". Clinical Toxicology. 37 (2): 279–292. doi:10.1081/CLT-100102426. PMID 10382562.
- ^ Bennett, Daniel R. M. D.; Baird, Curtis J. M.D.; Chan, Kwok-Ming; Crookes, Peter F.; Bremner, Cedric G.; Gottlieb, Michael M.; Naritoku, Wesley Y. M.D. (1997). "Zinc Toxicity Following Massive Coin Ingestion". American Journal of Forensic Medicine and Pathology. 18 (2): 148–153. doi:10.1097/00000433-199706000-00008. PMID 9185931.
- ^ Fernbach, S. K.; Tucker G. F. (1986). "Coin ingestion: unusual appearance of the penny in a child". Radiology. 158 (2): 512. doi:10.1148/radiology.158.2.3941880. PMID 3941880.
- ^ Stowe, C. M.; Nelson, R.; Werdin, R.; Fangmann, G.; Fredrick, P.; Weaver, G.; Arendt, T. D. (1978). "Zinc phosphide poisoning in dogs". Journal of the American Veterinary Medical Association. 173 (3): 270. PMID 689968.
- ^ Reece, R. L.; Dickson, D. B.; Burrowes, P. J. (1986). "Zinc toxicity (new wire disease) in aviary birds". Australian Veterinary Journal. 63 (6): 199. doi:10.1111/j.1751-0813.1986.tb02979.x. PMID 3767804.
Bibliografi[sunting | sunting sumber]
- Chambers, William and Robert (1901). Chambers's Encyclopaedia: A Dictionary of Universal Knowledge (edisi ke-Revised). London and Edinburgh: J. B. Lippincott Company.
- Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999). Advanced Inorganic Chemistry (edisi ke-6). New York: John Wiley & Sons, Inc. ISBN 978-0-471-19957-1.
- David R. Lide, ed. (2006). Handbook of Chemistry and Physics (edisi ke-87). Boca Raton, Florida: CRC Press, Taylor & Francis Group. ISBN 978-0-8493-0487-3.
- Emsley, John (2001). "Zinc". Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, Inggris, UK: Oxford University Press. hlm. 499–505. ISBN 978-0-19-850340-8.
- Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (edisi ke-2). Oxford: Butterworth-Heinemann. ISBN 978-0-7506-3365-9.
- Heiserman, David L. (1992). "Element 30: Zinc". Exploring Chemical Elements and their Compounds. New York: TAB Books. ISBN 978-0-8306-3018-9.
- Lehto, R. S. (1968). "Zinc"
 . Dalam Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. hlm. 822–830. ISBN 978-0-442-15598-8. LCCN 68-29938.
. Dalam Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. hlm. 822–830. ISBN 978-0-442-15598-8. LCCN 68-29938. - Stwertka, Albert (1998). "Zinc"
 . Guide to the Elements (edisi ke-Revised). Oxford University Press. ISBN 978-0-19-508083-4.
. Guide to the Elements (edisi ke-Revised). Oxford University Press. ISBN 978-0-19-508083-4. - Weeks, Mary Elvira (1933). "III. Some Eighteenth-Century Metals". The Discovery of the Elements. Easton, PA: Journal of Chemical Education. ISBN 978-0-7661-3872-8.
Pranala luar[sunting | sunting sumber]
- (Inggris) Lembar Fakta Seng dari US National Institutes of Health
- (Inggris) Sejarah & Etimologi Seng
- (Inggris) Statistik dan Informasi dari Survei Geologi AS
- (Inggris) Agen Pereduksi > Seng
- (Inggris) American Zinc Association Informasi mengenai berbagai kegunaan dan sifat seng.
- (Inggris) ISZB International Society for Zinc Biology, didirikan pada tahun 2008. Sebuah organisasi nirlaba internasional yang menyatukan para ilmuwan yang bekerja pada tindakan biologis seng.
- (Inggris) Zinc-UK Diarsipkan 2020-04-23 di Wayback Machine. Didirikan pada tahun 2010 untuk menyatukan para ilmuwan di Britania Raya yang bekerja pada seng.
- (Inggris) Seng di The Periodic Table of Videos (Universitas Nottingham)
- (Inggris) ZincBind – basis data situs pengikatan seng biologis.
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


![{\displaystyle {\ce {2ZnS + 3O2 ->[t^o] 2ZnO + 2SO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/686cb2d7d73dea23bc0e3431bfab4016d5fd71ed)
![{\displaystyle {\ce {ZnO + C ->[950^oC] Zn + CO}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1592f63fc0ae67a24850c33381264f5ca6bd1f55)
![{\displaystyle {\ce {ZnO + CO ->[950^oC] Zn + CO2}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ab85d04dfa0b8e0280b72062a5ecbe660fd247b1)


