Hidrogen
| Hidrogen | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Gas hidrogen dalam tabung lucutan | |||||||||||||||||||||
Garis spektrum hidrogen | |||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||
| Nama, lambang | hidrogen, H | ||||||||||||||||||||
| Pengucapan | /hidrogèn/[1] | ||||||||||||||||||||
| Penampilan | gas tak berwarna dengan nyala ungu dalam keadaan plasma | ||||||||||||||||||||
| Hidrogen dalam tabel periodik | |||||||||||||||||||||
| |||||||||||||||||||||
| Nomor atom (Z) | 1 | ||||||||||||||||||||
| Golongan | golongan 1 | ||||||||||||||||||||
| Periode | periode 1 | ||||||||||||||||||||
| Blok | blok-s | ||||||||||||||||||||
| Kategori unsur | nonlogam diatomik | ||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||
| Konfigurasi elektron | 1s1 | ||||||||||||||||||||
| Elektron per kelopak | 1 | ||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||
| Warna | tak berwarna | ||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | gas | ||||||||||||||||||||
| Titik lebur | (H2) 13,99 K (−259,16 °C, −434,49 °F) | ||||||||||||||||||||
| Titik didih | (H2) 20,271 K (−252,879 °C, −423,182 °F) | ||||||||||||||||||||
| Kerapatan (pada STS) | 0,08988 g/L | ||||||||||||||||||||
| saat cair, pada t.l. | 0,07 g/cm3 (padat: 0,0763 g/cm3)[2] | ||||||||||||||||||||
| Titik tripel | 13,8033 K, 7,041 kPa | ||||||||||||||||||||
| Titik kritis | 32,938 K, 1,2858 MPa | ||||||||||||||||||||
| Kalor peleburan | (H2) 0,117 kJ/mol | ||||||||||||||||||||
| Kalor penguapan | (H2) 0,904 kJ/mol | ||||||||||||||||||||
| Kapasitas kalor molar | (H2) 28,836 J/(mol·K) | ||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||
| Bilangan oksidasi | −1, +1 (oksida amfoter) | ||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 2,20 | ||||||||||||||||||||
| Energi ionisasi | ke-1: 1312,0 kJ/mol | ||||||||||||||||||||
| Jari-jari atom | empiris: 25 pm perhitungan: 53 pm | ||||||||||||||||||||
| Jari-jari kovalen | 31±5 pm | ||||||||||||||||||||
| Jari-jari van der Waals | 120 pm | ||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||
| Struktur kristal | heksagon | ||||||||||||||||||||
| Kecepatan suara | (gas, 27 °C) 1310 m/s | ||||||||||||||||||||
| Konduktivitas termal | 0,1805 W/(m·K) | ||||||||||||||||||||
| Arah magnet | diamagnetik[3] | ||||||||||||||||||||
| Suseptibilitas magnetik molar | −3,98×10−6 cm3/mol (298 K)[4] | ||||||||||||||||||||
| Nomor CAS | 12385-13-6 1333-74-0 (H2) | ||||||||||||||||||||
| Sejarah | |||||||||||||||||||||
| Penemuan | H. Cavendish[5][6] (1766) | ||||||||||||||||||||
| Asal nama | A. Lavoisier[7] (1783) | ||||||||||||||||||||
| Isotop hidrogen yang utama | |||||||||||||||||||||
| |||||||||||||||||||||
Hidrogen (bahasa Latin: hydrogenium, dari bahasa Yunani: hydro: air, genes: membentuk), atau kadang disebut zat air, adalah unsur kimia pada tabel periodik yang memiliki simbol H dan nomor atom 1. Pada suhu dan tekanan standar, hidrogen tidak berwarna, tidak berbau, bersifat non-logam, bervalensi tunggal, dan merupakan gas diatomik yang sangat mudah terbakar. Dengan massa atom 1,00794 amu,[a] hidrogen adalah unsur teringan di dunia.
Hidrogen juga adalah unsur paling melimpah dengan persentase kira-kira 75% dari total massa unsur alam semesta.[8][b] Kebanyakan bintang dibentuk oleh hidrogen dalam keadaan plasma. Senyawa hidrogen relatif langka dan jarang dijumpai secara alami di Bumi, dan biasanya dihasilkan secara industri dari berbagai senyawa hidrokarbon seperti metana. Hidrogen juga dapat dihasilkan dari air melalui proses elektrolisis, namun proses ini secara komersial lebih mahal daripada produksi hidrogen dari gas alam.[9]
Isotop hidrogen yang paling banyak dijumpai di alam adalah protium, yang inti atomnya hanya mempunyai proton tunggal dan tanpa neutron. Senyawa ionik hidrogen dapat bermuatan positif (kation) ataupun negatif (anion). Hidrogen dapat membentuk senyawa dengan kebanyakan unsur dan dapat dijumpai dalam air dan senyawa-senyawa organik. Hidrogen sangat penting dalam reaksi asam basa yang mana banyak reaksi ini melibatkan pertukaran proton antar molekul terlarut. Oleh karena hidrogen merupakan satu-satunya atom netral yang persamaan Schrödingernya dapat diselesaikan secara analitik, kajian pada energetika dan ikatan atom hidrogen memainkan peran yang sangat penting dalam perkembangan mekanika kuantum.
Sifat kimia[sunting | sunting sumber]
Kelarutan dan karakteristik hidrogen dengan berbagai macam logam merupakan subjek yang sangat penting dalam bidang metalurgi (karena perapuhan hidrogen dapat terjadi pada kebanyakan logam [10]) dan dalam riset pengembangan cara yang aman untuk menyimpan hidrogen sebagai bahan bakar.[11] Hidrogen sangatlah larut dalam berbagai senyawa yang terdiri dari logam tanah nadir dan logam transisi[12] dan dapat dilarutkan dalam logam kristal maupun logam amorf.[13] Kelarutan hidrogen dalam logam disebabkan oleh distorsi setempat ataupun ketidakmurnian dalam kekisi hablur logam.[14]
Pembakaran[sunting | sunting sumber]


Gas hidrogen (dihidrogen atau molekul hidrogen) sangat mudah terbakar dan akan terbakar pada konsentrasi serendah 4% H2 di udara bebas.[15] Entalpi pembakaran hidrogen adalah −286 kJ/mol.[16] Hidrogen terbakar menurut persamaan kimia:
2 H2(g) + O2(g) → 2 H2O(l) + 572 kJ (286 kJ/mol)[c]
Hidrogen akan meledak sendiri pada temperatur 500 °C.[17] Hidrogen membentuk campuran yang bisa meledak dengan udara dalam konsentrasi hidrogen 4–74%[18] dan dengan klorin dalam konsentrasi 5–95%. Reaksi ledakan dapat dipicu oleh percikan api, panas, atau sinar matahari.
Lidah api[sunting | sunting sumber]
Lidah api hasil pembakaran hidrogen-oksigen murni memancarkan gelombang ultraviolet dan hampir tidak terlihat dengan mata telanjang. Deteksi kebocoran hidrogen yang terbakar mungkin memerlukan detektor api; kebocoran semacam itu bisa sangat berbahaya. Nyala api hidrogen dalam kondisi lain berwarna biru, menyerupai nyala api gas alam berwarna biru.[19] Kasus meledaknya pesawat Hindenburg adalah salah satu contoh terkenal dari pembakaran hidrogen.[20] Karakteristik lainnya dari api hidrogen adalah nyala api cenderung menghilang dengan cepat di udara, sehingga kerusakan akibat ledakan hidrogen lebih ringan dari ledakan hidrokarbon. Dalam kasus kecelakaan Hindenburg, dua pertiga dari penumpang pesawat selamat dan kebanyakan kasus meninggal disebabkan oleh terbakarnya bahan bakar diesel yang bocor.[21]
Reaktan[sunting | sunting sumber]
H2 relatif tidak reaktif. Basis termodinamika dari reaktivitas yang rendah ini adalah ikatan H-H yang sangat kuat, dengan energi disosiasi ikatan 435,7 kJ/mol.[22] Dasar kinetik dari reaktivitas rendah adalah sifat nonpolar H2 dan polarisabilitasnya yang lemah. H2 bereaksi secara langsung dengan unsur-unsur oksidator lainnya. Ia bereaksi dengan spontan dan hebat pada suhu kamar dengan klorin dan fluorin, menghasilkan hidrogen halida berupa hidrogen klorida dan hidrogen fluorida, yang merupakan asam berbahaya.[23] Lelehan natrium dan kalium bereaksi dengan gas untuk menghasilkan hidrida masing-masing NaH dan KH.[rujukan?]
Reaktivitas H2 sangat dipengaruhi oleh keberadaan katalis logam. Oleh karena itu, walaupun H2 mudah terbakar, campuran H2 dan O2 tidak bereaksi tanpa adanya katalis.
Aras tenaga elektron[sunting | sunting sumber]
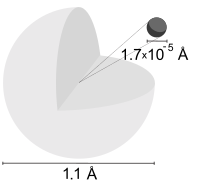
Aras tenaga keadaan dasar elektron pada atom hidrogen adalah −13.6 eV, yang ekuivalen dengan foton ultraviolet kira-kira 92 nm.[24]
Aras tenaga hidrogen dapat dihitung dengan cukup akurat menggunakan model atom Bohr yang menggambarkan elektron beredar mengelilingi proton dengan analogi Bumi beredar mengelilingi Matahari. Oleh karena diskretisasi momentum sudut yang dipostulatkan pada awal mekanika kuantum oleh Bohr, elektron pada model Bohr hanya dapat menempati jarak-jarak tertentu saja dari proton dan oleh karena itu hanya beberapa energi tertentu saja yang diperbolehkan.[25]
Deskripsi atom hidrogen yang lebih akurat didapatkan dengan perlakuan mekanika kuantum murni menggunakan persamaan Schrödinger atau dengan perumusan integral lintasan Feyman untuk menghitung rapat kementakan elektron di sekitar proton.[26] Perlakuan yang paling rumit memungkinkan efek kecil dari relativitas khusus dan polarisasi vakum. Dalam perlakuan mekanika kuantum, elektron dalam atom hidrogen dalam keadaan dasar tidak memiliki momentum sudut sama sekali, yang menggambarkan bagaimana "orbit planet" berbeda dari gerakan elektron.
Bentuk-bentuk molekul unsur[sunting | sunting sumber]

Terdapat dua jenis molekul diatomik hidrogen yang berbeda berdasarkan spin relatif inti.[27] Dalam bentuk ortohidrogen, spin dari dua proton adalah paralel dan dalam keadaan triplet; dalam bentuk parahidrogen, spin-nya adalah antiparalel dan dalam keadaan singlet. Pada keadaan standar, gas hidrogen terdiri dari 25% bentuk para dan 75% bentuk orto, juga dikenal dengan sebutan "bentuk normal".[28] Rasio kesetimbangan antara ortohidrogen dan parahidrogen tergantung pada termperatur. Namun oleh karena bentuk orto dalam keadaan tereksitasi, bentuk ini tidaklah stabil dan tidak bisa dimurnikan. Pada suhu yang sangat rendah, hampir semua hidrogen yang ada adalah dalam bentuk parahidrogen. Sifat fisik dari parahidrogen murni berbeda sedikit dengan "bentuk normal".[29] Perbedaan orto/para juga terdapat pada molekul yang terdiri dari atom hidrogen seperti air dan metilena.[30]
Antarubahan yang tidak dikatalis antara H2 para dan orto meningkat seiring dengan meningkatnya temperatur; oleh karenanya H2 yang diembunkan dengan cepat mengandung banyak hidrogen dalam bentuk orto yang akan berubah menjadi bentuk para dengan sangat lambat.[31] Nisbah orto/para pada H2 yang diembunkan adalah faktor yang perlu diperhitungkan dalam persiapan dan penyimpanan hidrogen cair: antarubahan dari bentuk orto ke para adalah eksotermik dan dapat menghasilkan bahang yang cukup untuk menguapkan hidrogen cair tersebut dan menyebabkan berkurangnya komponen cair. Katalis untuk antarubahan orto-para, seperti misalnya senyawa besi, sering digunakan selama pendinginan hidrogen.[32]
Sebuah bentuk molekul yang disebut molekul hidrogen terprotonasi, atau H, ditemukan pada medium antarbintang (Interstellar medium) (ISM), di mana ia dihasilkan dengan ionisasi molekul hidrogen dari sinar kosmos. Molekul ini juga dapat dipantau di bagian atas atmosfer planet Jupiter. Molekul ini relatif cukup stabil pada lingkungan luar angkasa oleh karena suhu dan rapatan yang rendah. H adalah salah satu dari ion yang paling melimpah di alam semesta ini, dan memainkan peran penting dalam proses kimia medium antarbintang.[33]
Fasa[sunting | sunting sumber]
Bentuk monoatomik[sunting | sunting sumber]
Atom H, juga disebut hidrogen nasen atau hidrogen atomik, diklaim eksis secara fana namun cukup lama untuk menimbulkan reaksi kimia. Menurut klaim itu, hidrogen nasen dihasilkan secara in situ, biasanya reaksi antara seng dengan asam, atau dengan elektrolisis pada katode. Sebagai molekul monoatomik, atom H sangat reaktif dan oleh karena itu adalah reduktor yang lebih kuat dari H2 diatomik, namun pertanyaan kuncinya terletak pada keberadaan atom H itu sendiri. Konsep ini lebih populer di bidang teknik dan di literatur-literatur lama.
Hidrogen nasen diklaim mereduksi nitrit menjadi amonia atau arsenik menjadi arsina bahkan dalam keadaan lunak. Penelitian yang lebih mendetail menunjukkan lintasan alternatif lainnya dan bukanlah atom H.
Atom hidrogen dapat dihasilkan pada temperatur yang cukup tinggi (>2000 K) agar molekul H2 dapat berdisosiasi. Selain itu, radiasi elektromagnetik di atas 11 eV juga dapat diserap H2 dan menyebabkan disosiasi.
Kadang kala, hidrogen yang terserap secara kimiawi pada permukaan logam juga dirujuk sebagai hidrogen nasen, walaupun terminologi ini sudah mulai ditinggalkan. Pandangan lainnya mengatakan bahwa hidrogen yang terserap secara kimiawi itu "kurang reaktif" dari hidrogen nasen disebabkan oleh ikatan yang dihasilkan oleh permukaan katalis logam tersebut.
Senyawa-senyawa[sunting | sunting sumber]
Senyawa kovalen dan senyawa organik[sunting | sunting sumber]
Walaupun H2 tidaklah begitu reaktif dalam keadaan standar, ia masih dapat membentuk senyawa dengan kebanyakan unsur. Jutaan jenis hidrokarbon telah diketahui, namun itu semua tidaklah dihasilkan secara langsung dari hidrogen dan karbon. Hidrogen dapat membentuk senyawa dengan unsur yang lebih elektronegatif seperti halogen (F, Cl, Br, I); dalam senyawa ini hidrogen memiliki muatan parsial positif.[34] Ketika berikatan dengan fluor, oksigen ataupun nitrogen, hidrogen dapat berpartisipasi dalam bentuk ikatan non-kovalen yang kuat, yang disebut dengan ikatan hidrogen yang sangat penting untuk menjaga kestabilan kebanyakan molekul biologi.[35][36] Hidrogen juga membentuk senyawa dengan unsur yang kurang elektronegatif seperti logam dan metaloid, yang mana hidrogen memiliki muatan parsial negatif. Senyawa ini dikenal dengan nama hidrida.[37]
Hidrogen membentuk senyawa yang sangat banyak dengan karbon. Oleh karena asosiasi senyawa itu dengan kebanyakan zat hidup, senyawa ini disebut sebagai senyawa organik.[38] Studi sifat-sifat senyawa tersebut disebut kimia organik[39] dan studi dalam konteks kehidupan organisme dinamakan biokimia.[40] Pada beberapa definisi, senyawa "organik" hanya memerlukan atom karbon untuk disebut sebagai organik. Namun kebanyakan senyawa organik mengandung atom hidrogen. Dan oleh karena ikatan ikatan hidrogen-karbon inilah yang memberikan karakteristik sifat-sifat hidrokarbon, ikatan hidrogen-karbon diperlukan untuk beberapa definisi dari kata "organik" di kimia.[38] Jutaan hidrokarbon telah diketahui, dan biasanya terbentuk oleh jalur yang rumit yang jarang melibatkan unsur hidrogen.
Dalam kimia anorganik, hidrida dapat berperan sebagai ligan penghubung yang menghubungkan dua pusat logam dalam kompleks berkoordinasi. Fungsi ini umum ditemukan pada unsur golongan 13, terutama pada kompleks borana (hidrida boron) dan aluminium serta karborana yang bergerombol.[41]
Hidrogen larut dengan mudah dalam banyak logam tanah jarang dan logam transisi[12] dan larut dalam logam nanokristalin dan amorf.[13] Kelarutan hidrogen dalam logam dipengaruhi oleh distorsi lokal atau ketidakmurnian dalam kisi kristal.[14] Sifat-sifat ini mungkin berguna ketika hidrogen dimurnikan dengan melewatkan hidrogen melalui cakram paladium panas, tetapi kelarutan gas yang tinggi merupakan masalah metalurgi, yang berkontribusi pada penggetasan banyak logam,[42] mempersulit desain jaringan pipa dan tangki penyimpanan.[43]
Hidrida[sunting | sunting sumber]
Senyawa hidrogen sering disebut sebagai hidrida, sebuah istilah yang tidak mengikat. Oleh kimiawan, istilah "hidrida" biasanya memiliki arti atom H yang mendapat sifat anion, ditandai dengan H−. Keberadaan anion hidrida, dikemukakan oleh Gilbert N. Lewis pada tahun 1916 untuk golongan I dan II hidrida garam, didemonstrasikan oleh Moers pada tahun 1920 dengan melakukan elektrolisis litium hidrida cair (LiH) yang menghasilkan sejumlah hidrogen pada anode.[44] Untuk hidrida selain logam golongan I dan II, istilah ini sering kali membuat kesalahpahaman oleh karena elektronegativitas hidrogen yang rendah. Pengecualian adalah hidrida golongan II BeH2 yang polimerik.
Walaupun hidrida dapat dibentuk dengan hampir semua golongan unsur, jumlah dan kombinasi dari senyawa bervariasi, sebagai contoh terdapat lebih dari 100 hidrida borana biner yang diketahui, namun cuma satu hidrida aluminium biner yang diketahui.[45] Hidrida indium biner sampai sekarang belum diketahui, walaupun ada sejumlah komplek yang lebih besar.[46]
Dalam kimia anorganik, hidrida juga dapat berfungsi sebagai jembatan ligan yang menghubungkan dua pusat logam dalam kompleks koordinasi. Fungsi ini banyak ditemukan pada unsur golongan 13, terutama pada borana (hidrida boron) dan kompleks aluminium, serta pada karboran yang berkerumunan.[47]
Proton dan asam[sunting | sunting sumber]
Oksidasi H2 secara formal menghasilkan proton H+. Spesies ini merupakan topik utama dari pembahasan asam, walaupun istilah proton digunakan secara longgar untuk merujuk pada hidrogen kationik yang positif dan ditandai dengan H+. Menurut teori Brønsted–Lowry, asam adalah donor proton, sementara basa adalah akseptor (penerima) proton.
Proton H+ tidak dapat ditemukan berdiri sendiri dalam larutan karena ia memiliki kecenderungan mengikat pada atom atau molekul yang memiliki elektron. Selain pada temperatur tinggi dan bergabung dengan plasma, proton semacam ini tidak dapat dihilangkan dari awan elektron atom dan molekul, dan akan tetap terikat pada atom dan molekul tersebut.
Untuk menghindari kesalahpahaman akan "proton terlarut" dalam larutan, larutan asam sering dianggap memiliki spesies fiktif yang disebut ion hidronium (H3O+) yang bergerombol membentuk H9O4+.[48] Ion oksonium juga ditemukan ketika air dalam larutan asam dengan pelarut lain.[49]
Walaupun sangat langka di Bumi, salah satu ion yang paling melimpah dalam alam semesta ini adalah H3+, dikenal sebagai molekul hidrogen terprotonasi ataupun kation hidrogen triatomik.[50]
Atom hidrogen[sunting | sunting sumber]
NASA telah menyelidiki penggunaan atom hidrogen sebagai propelan roket. Atom hidrogen bisa disimpan dalam helium cair untuk mencegah atom hidrogen bergabung kembali menjadi molekul hidrogen. Ketika helium menjadi uap, atom hidrogen akan dilepaskan dan bergabung kembali menjadi hidrogen molekuler. Hasilnya adalah aliran gas hidrogen dan helium yang sangat panas. Berat lepas landas roket dapat dikurangi hingga 50% dengan metode ini.[51]
Sebagian besar hidrogen di luar angkasa berbentuk atom hidrogen karena atom dapat, walaupun jarang, bertabrakan dan bergabung. Atom hidrogen adalah sumber penting garis hidrogen 21 cm dalam astronomi pada frekuensi 1420 MHz.[52]
Isotop[sunting | sunting sumber]



Hidrogen memiliki tiga isotop alami, ditandai dengan 1H, 2H, dan 3H. Isotop lainnya yang tidak stabil (4H hingga 7H) juga telah disintesiskan di laboratorium namun tidak pernah dijumpai secara alami.[53][54]
- 1H adalah isotop hidrogen yang paling melimpah, memiliki persentase 99.98% dari jumlah atom hidrogen. Oleh karena inti atom isotop ini hanya memiliki proton tunggal, ia diberikan nama yang deskriptif sebagai protium, namun nama ini jarang sekali digunakan.[55]
- 2H, isotop hidrogen lainnya yang stabil, juga dikenal sebagai deuterium dan mengandung satu proton dan satu neutron pada intinya. Deuterium tidak bersifat radioaktif, dan tidak memberikan bahaya keracunan yang signifikan. Air yang atom hidrogennya merupakan isotop deuterium dinamakan air berat. Deuterium dan senyawanya digunakan sebagai penanda non-radioaktif pada percobaan kimia dan untuk pelarut 1H-spektroskopi NMR.[56] Air berat digunakan sebagai moderator neutron dan pendingin pada reaktor nuklir. Deuterium juga berpotensi sebagai bahan bakar fusi nuklir komersial.[57]
- 3H dikenal dengan nama tritium dan mengandung satu proton dan dua neutron pada intinya. Ia memiliki sifat radioaktif, dan mereras menjadi Helium-3 melalui pererasan beta dengan umur paruh 12,32 tahun.[41] Sejumlah kecil tritium dapat dijumpai di alam oleh karena interaksi sinar kosmos dengan atmosfer Bumi; tritium juga dilepaskan selama uji coba nuklir.[58] Ia juga digunakan dalam reaksi fusi nuklir,[59] sebagai penanda dalam geokimia isotop,[60] dan terspesialisasi pada peralatan self-powered lighting.[61] Tritium juga digunakan dalam penandaan percobaan kimia dan biologi sebagai radiolabel.[62]
Hidrogen adalah satu-satunya unsur yang memiliki tiga nama berbeda untuk isotopnya. (Dalam awal perkembangan keradioaktivitasan, beberapa isotop radioaktif berat diberikan nama, namun nama-nama tersebut tidak lagi digunakan). Simbol D dan T kadang-kadang digunakan untuk merujuk pada deuterium dan tritium, namun simbol P telah digunakan untuk merujuk pada fosfor, sehingga tidak digunakan untuk merujuk pada protium.[63] Dalam tatanama IUPAC, International Union of Pure and Applied Chemistry mengizinkan penggunaan D, T, 2H, dan 3H walaupun 2H dan 3H lebih dianjurkan.[64]
Atom muonium (simbol Mu) eksotis, terdiri dari antimuon dan elektron, kadang-kadang juga dianggap sebagai radioisotop ringan hidrogen, karena perbedaan massa antara antimuon dan elektron.[65] Muonium ditemukan pada tahun 1960. Dalam 2,2 µs, yaitu masa hidup muon, muonium dapat masuk ke dalam senyawa seperti muonium klorida (MuCl) atau natrium muonida (NaMu), yang serupa dengan hidrogen klorida dan natrium hidrida.[66]
Keberadaan alami[sunting | sunting sumber]

Hidrogen adalah unsur yang paling melimpah di alam semesta ini dengan persentase 75% dari barion berdasarkan massa dan lebih dari 90% berdasarkan jumlah atom (Sebagian besar massa alam semesta bukan dalam bentuk materi jenis unsur kimia, melainkan didalilkan terjadi sebagai bentuk massa yang belum terdeteksi seperti materi gelap dan energi gelap).[67] Unsur ini ditemukan dalam kelimpahan yang besar di bintang-bintang dan planet-planet raksasa gas. Awan molekul dari H2 diasosiasikan dengan pembentukan bintang. Hidrogen memainkan peran penting dalam pemberian energi bintang melalui reaksi proton-proton dan fusi nuklir daur CNO.[68]
Bentuk[sunting | sunting sumber]
Di seluruh alam semesta ini, hidrogen kebanyakan ditemukan dalam keadaan atomik dan plasma yang sifatnya berbeda dengan molekul hidrogen. Sebagai plasma, elektron hidrogen dan proton terikat bersama, dan menghasilkan konduktivitas listrik yang sangat tinggi dan daya pancar yang tinggi (menghasilkan cahaya dari Matahari dan bintang lain). Partikel yang bermuatan dipengaruhi oleh medan magnet dan medan listrik. Sebagai contoh, dalam angin surya, partikel-partikel ini berinteraksi dengan magnetosfer Bumi dan mengakibatkan arus Birkeland dan fenomena Aurora. Hidrogen ditemukan dalam keadaan atom netral di medium antarbintang. Sejumlah besar atom hidrogen netral yang ditemukan di sistem Lyman-alpha teredam diperkirakan mendominasi rapatan barionik alam semesta sampai dengan pergeseran merah z=4.[69]
Dalam keadaan normal di Bumi, unsur hidrogen berada dalam keadaan gas diatomik, H2. Namun, gas hidrogen sangat langka di atmosfer Bumi (1 ppm berdasarkan volume) oleh karena beratnya yang ringan. Oleh karena itu, gas hidrogen lebih mudah lepas dari gravitasi Bumi daripada gas yang lebih berat. Walaupun demikian, hidrogen masih merupakan unsur paling melimpah di permukaan Bumi.[70] Kebanyakan hidrogen di Bumi berada dalam keadaan bersenyawa dengan unsur lain seperti hidrokarbon dan air.[41] Gas hidrogen dihasilkan oleh beberapa jenis bakteri dan ganggang dan merupakan komponen alami dari kentut. Penggunaan metana sebagai sumber hidrogen akhir-akhir ini juga menjadi semakin penting.[71]
Bentuk molekuler yang disebut molekul hidrogen terprotonasi (H+3) ditemukan dalam media antarbintang. Ini terbentuk melalui ionisasi hidrogen molekuler dari sinar kosmik. Ion bermuatan ini juga telah diamati dalam atmosfer atas planet Jupiter. Ion ini relatif stabil di lingkungan angkasa luar karena rendahnya temperatur dan kerapatan. H+3 adalah ion paling melimpah di jagat raya, dan memainkan peran penting dalam kimia media antarbintang.[72] Hidrogen triatomik netral H3 hanya ada dalam bentuk tereksitasi dan tidak stabil.[73] Sebaliknya, ion positif hidrogen molekular (H+2) adalah molekul yang jarang ditemukan di jagat raya.
Sejarah[sunting | sunting sumber]
Penemuan dan penggunaan[sunting | sunting sumber]
Gas hidrogen, H2, pertama kali dihasilkan secara artifisial oleh T. Von Hohenheim (dikenal juga sebagai Paracelsus, 1493–1541) melalui pencampuran logam dengan asam kuat.[74] Dia tidak menyadari bahwa gas mudah terbakar yang dihasilkan oleh reaksi kimia ini adalah unsur kimia yang baru. Pada tahun 1671, Robert Boyle menemukan kembali dan mendeskripsikan reaksi antara besi dan asam yang menghasilkan gas hidrogen.[75] Pada tahun 1766, Henry Cavendish adalah orang yang pertama mengenali gas hidrogen sebagai zat diskret dengan mengidentifikasikan gas tersebut dari reaksi logam-asam sebagai "udara yang mudah terbakar". Pada tahun 1781 dia lebih lanjut menemukan bahwa gas ini menghasilkan air ketika dibakar.[5][6] Pada tahun 1783, Antoine Lavoisier memberikan unsur ini dengan nama hidrogen (dari Bahasa Yunani hydro yang artinya air dan genes yang artinya membentuk)[7] ketika dia dan Laplace mengulang kembali penemuan Cavendish yang mengatakan pembakaran hidrogen menghasilkan air.[6]

Lavoisier menghasilkan hidrogen pada percobaannya tentang konservasi massa dengan mereaksikan flux uap dengan besi logam melalui tabung besi pijar yang dipanaskan dalam api. Oksidasi anaerobik besi oleh proton air pada temperatur tinggi dapat digambarkan sebagai berikut:
- Fe + H2O → FeO + H2
- 2 Fe + 3 H2O → Fe2O3 + 3 H2
- 3 Fe + 4 H2O → Fe3O4 + 4 H2
Banyak logam seperti zirkonium mengalami reaksi yang sama dengan air menghasilkan hidrogen.
Hidrogen pertama kali dicairkan oleh James Dewar pada tahun 1898 dengan menggunakan penemuannya, guci hampa.[6] Dia kemudian menghasilkan hidrogen padat setahun kemudian.[6] Deuterium ditemukan pada tahun 1931 Desember oleh Harold Urey, dan tritium dibuat pada tahun 1934 oleh Ernest Rutherford, Mark Oliphant, and Paul Harteck.[5] Air berat, yang mengandung deuterium menggantikan hidrogen biasa, ditemukan oleh Urey dkk. pada tahun 1932.[6] Salah satu dari penggunaan pertama H2 adalah untuk sinar sorot.[6] François Isaac de Rivaz membangun mesin de Rivaz pertama, yaitu mesin pembakaran internal yang ditenagai oleh campuran hidrogen dan oksigen pada tahun 1806. Edward Daniel Clarke menciptakan pipa sembur gas hidrogen pada tahun 1819. Lampu Döbereiner dan lampu sorot (limelight) ditemukan pada tahun 1823.[6]
Balon pertama yang diisikan dengan hidrogen diciptakan oleh Jacques Charles pada tahun 1783.[6] Hidrogen memberikan tenaga dorong untuk perjalanan udara yang aman dan pada tahun 1852 Henri Giffard menciptakan kapal udara yang diangkat oleh hidrogen.[6] Bangsawan Jerman Ferdinand von Zeppelin mempromosikan idenya tentang kapal udara yang diangkat dengan hidrogen dan kemudian dinamakan Zeppelin dengan penerbangan perdana pada tahun 1900.[6] Penerbangan yang terjadwal dimulai pada tahun 1910 dan sampai pecahnya Perang Dunia I pada Agustus 1914, Zeppelin telah membawa 35.000 penumpang tanpa insiden yang serius. Kapal udara yang diangkat dengan hidrogen digunakan sebagai platform observasi dan pengebom selama perang.
Penerbangan tanpa henti melewati samudra atlantik pertama kali dilakukan kapal udara Britania R34 pada tahun 1919. Pelayanan penerbangan udara dipulihkan pada tahun 1920 dan penemuan cadangan helium di Amerika Serikat memberikan peluang ditingkatkannya keamanan penerbangan, namun pemerintah Amerika Serikat menolak menjual gas tersebut untuk digunakan dalam penerbangan. Oleh karenanya, gas H2 digunakan di pesawat Hindenburg, yang pada akhirnya meledak di langit New Jersey pada tanggal 6 Mei 1937.[6] Insiden ini ditayangkan secara langsung di radio dan direkam. Banyak yang menduga terbakarnya hidrogen yang bocor sebagai akibat insiden tersebut, namun investigasi lebih lanjut membuktikan sebab insiden tersebut karena terbakarnya salut fabrik oleh keelektrikan statis. Tetapi reputasi hidrogen sebagai gas pengangkat telah rusak dan pesawat komersial yang menggunakan hidrogen dihentikan. Hidrogen masih digunakan sebagai gas pengangkat untuk balon cuaca, karena lebih murah daripada helium.
Pada tahun yang sama, turbogenerator berpendingin hidrogen diluncurkan pertama kali dengan gas hidrogen sebagai pendingin dalam rotor dan stator pada tahun 1937 di Dayton, Ohio oleh Dayton Power & Light Co.;[76] karena konduktivitas termal gas hidrogen, ini adalah jenis yang palling umum di lapangan saat ini untuk generator besar (biasanya lebih atau sama dengan 60 MW; generator yang lebih kecil biasanya didinginkan dengan udara).
Baterai nikel hidrogen pertama kali digunakan pada tahun 1977 dalam U.S Navy's Navigation Technology Satellite-2 (NTS-2).[77] Sebagai contoh, ISS,[78] Mars Odyssey,[79] dan Mars Global Surveyor[80] dilengkapi dengan baterai nikel-hidrogen. Di bagian gelap orbitnya, Teleskop Angkasa Hubble juga di bertenaga baterai nikel-hidrogen, yang akhirnya diganti pada Mei 2009,[81] lebih dari 19 tahun setelah diluncurkan, dan 13 tahun setelah mulai dihidupkan.[82]
Peranan dalam teori kuantum[sunting | sunting sumber]

Oleh karena struktur atomnya yang relatif sederhana, yang hanya terdiri dari sebuah proton dan elektron, atom hidrogen bersama dengan spektrum emisinya menjadi pusat perkembangan teori struktur atom.[83] Lebih jauh lagi, kesederhanaan molekul hidrogen dan kationnya H membantu pemahaman yang lebih jauh mengenai ikatan kimia, tidak lama setelah perlakuan mekanis kuantum atom hidrogen dikembangkan pada pertengahan 1920-an.
Salah satu dari efek kuantum yang secara eksplisit disadari (namun masih belum sepenuhnya dimengerti saat itu) adalah pengamatan Maxwell yang melibatkan hidrogen setengah abad sebelum teori mekanika kuantum benar-benar berkembang. Maxwell mengamati bahwa kapasitas bahang spesifik dari H2 tidak sesuai dengan tren gas diatomik lainnya di bawah suhu kamar dan mulai menyerupai tren gas monoatomik di temperatur kriogenik. Menurut teori kuantum, sifat-sifat ini disebabkan oleh jarak antara aras tenaga rotasi hidrogen yang lebar oleh karena massanya yang ringan. Aras yang lebar ini menghambat partisi energi bahang secara merata menjadi gerak berputar hidrogen pada temperatur yang rendah. Gas diatomik yang terdiri dari atom-atom yang lebih berat tidak mempunyai aras tenaga yang cukup lebar untuk menyebabkan efek yang sama.[84]
Antihidrogen (H) adalah antimateri lawan dari hidrogen. Ia tersusun dari sebuah antiproton dan sebuah positron. Antihidrogen adalah satu-satunya atom antimateri yang telah diproduksi per 2015.[85][86]
Produksi[sunting | sunting sumber]
H diproduksi di laboratorium kimia dan biologi, sering kali sebagai produk sampingan dari reaksi lain; di industri untuk hidrogenasi substrat tak jenuh; dan di alam sebagai sarana penyetara reaksi biokimia.
Logam-asam[sunting | sunting sumber]
Banyak logam bereaksi dengan air menghasilkan H2, tetapi laju evolusi hidrogen bergantung pada logam, pH, dan keberadaan agen paduan. Cara yang paling sering digunakan adalah dengan asam. Logam alkali dan alkali tanah, aluminium, seng, mangan, dan besi mudah bereaksi dengan asam air. Reaksi ini adalah dasar dari peralatan Kipp, yang pernah digunakan sebagai sumber gas laboratorium, dengan mereaksikan asam non-oksidator encer dengan beberapa logam yang reaktif seperti seng dengan peralatan Kipp:
- Zn + 2 H+ → Zn2+ + H2
Banyak logam, seperti aluminium, bereaksi lambat dengan air karena mereka membentuk lapisan oksida pasif. Namun, paduan aluminium dan galium bereaksi dengan air. [97] Pada pH yang tinggi, aluminium dapat menghasilkan H2:
- 2 Al + 6 H2O + 2 OH− → 2 Al(OH)−4 + 3 H2
Elektrolisis air[sunting | sunting sumber]
Elektrolisis air adalah metode sederhana produksi hidrogen. Arus listrik lemah dialirkan melalui listrik, dan gas oksigen terbentuk di anoda sementara gas hidrogen terbentuk di katode. Biasanya katode terbuat dari platina atau logam inert lainnya ketika hidrogen diproduksi untuk disimpan. Namun, jika gas akan dibakar di tempat, oksigen yang dihasilkan harus mendukung pembakaran, sehingga kedua elektrode harus terbuat dari bahan inert. (Besi, misalnya, akan teroksidasi, dan akibatnya menurunkan jumlah oksigen yang dihasilkan.) Efisiensi maksimum teoretis (listrik yang digunakan vs. nilai energetik hidrogen yang dihasilkan) adalah antara 88–94%.[87][88]
- 2 H2O(l) → 2 H2(g) + O2(g)
Paduan aluminium dan galium dalam bentuk pelet yang ditambahkan ke dalam air dapat digunakan untuk menghasilkan hidrogen. Proses ini juga menghasilkan alumina, tetapi harga galium yang mahal, dengan sifatnya yang dapat mencegah pembentukan lapisan oksida pada permukaan pelet, membuatnya dapat digunakan ulang. Hal ini membawa implikasi penting pada keekonomian hidrogen, karena hidrogen dapat diproduksi di tempat dan tidak memerlukan transportasi.[89]
Ketika menentukan efisiensi listrik elektrolisis PEM (membran penukar proton/proton exchange membrane), digunakan nilai kalor (HHV) yang lebih tinggi.[90] Ini karena lapisan katalisator berinteraksi dengan air sebagai uap. Karena proses beroperasi pada suhu 80 °C untuk elektroliser PEM, panas limbah dapat dialihkan melalui sistem PEM untuk menghasilkan uap, sehingga efisiensi listriknya lebih tinggi. Nilai panas yang lebih rendah (LHV) harus digunakan untuk elektroliser alkali karena proses di dalam elektroliser ini membutuhkan air dalam bentuk cair dan menggunakan alkalinitas untuk memfasilitasi pemutusan ikatan yang mengikat atom hidrogen dan oksigen. Nilai panas yang lebih rendah juga harus digunakan untuk sel bahan bakar, karena uap adalah hasilnya, bukan bahannya.
Steam reforming[sunting | sunting sumber]
Hidrogen dapat diproduksi dalam beberapa cara, tetapi proses paling penting secara ekonomis adalah penghilangan hidrogen dari hidrokarbon. Hidrogen komersial biasanya diproduksi dengan cara steam reforming gas alam,[91] yang melibatkan penghilangan hidrogen dari hidrokarbon pada suhu yang sangat tinggi. 48% produksi hidrogen dihasilkan dari steam reforming.[92] Pada temperatur tinggi (1000–1400 K, 700–1100 °C, atau 1300–2000 °F), steam (uap air) bereaksi dengan metana menghasilkan karbon monoksida dan H.[92]
- CH4 + H2O → CO + 3 H2
Reaksi ini disarankan pada tekanan rendah tetapi tetap dilakukan pada tekanan tinggi (2,0 MPa (20 atm; 590 inHg)). Hal ini karena H bertekanan tinggi adalah produk yang paling banyak di pasaran dan sistem pemurnian Pressure Swing Adsorption (PSA) bekerja lebih baik pada tekanan tinggi. Campuran produk dikenal sebagai "gas sintetis" karena sering digunakan langsung untuk produksi metanol dan senyawa terkait. Hidrokarbon lain selain metana dapat digunakan untuk menghasilkan gas sintetis dengan rasio produk bervariasi. Salah satu komplikasi teknologi canggih ini adalah pembentukan kokas atau karbon:
- CH4 → C + 2 H2
Akibatnya, steam reforming biasanya menggunakan H berlebih. Hidrogen tambahan dapat diperoleh kembali dari uap air dengan menggunakan karbon monoksida melalui reaksi pergeseran gas air, terutama dengan katalis besi oksida. Reaksi ini juga merupakan sumber karbon dioksida industri yang umum:[91]
- CO + H2O → CO2 + H2
Metode penting lainnya untuk produksi H meliputi oksidasi parsial hidrokarbon:[93]
- 2 CH4 + O2 → 2 CO + 4 H2
dan reaksi karbon, yang dapat berfungsi sebagai awal untuk reaksi pergeseran atas:[91]
- C + H2O → CO + H2
Hidrogen kadang-kadang diproduksi dan dikonsumsi dalam proses industri yang sama, tanpa dipisahkan. Dalam proses Haber untuk produksi amonia, hidrogen dihasilkan dari gas alam.[94] Elektrolisis air garam untuk mendapatkan klorin juga menghasilkan hidrogen sebagai produk sampingan.[95]
Termokimia[sunting | sunting sumber]
Terdapat lebih dari 200 daur termokimia yang dapat digunakan untuk pemecahan air, sebagian daur ini seperti daur besi oksida, daur serium(IV) oksida–serium(III) oksida, daur seng–seng oksida, daur belerang–iodin, daur tembaga–klorin dan daur hibrida belerang masih dalam tahap penelitian dan fasa pengujian untuk menghasilkan hidrogen dan oksigen dari air dan panas tanpa menggunakan listrik.[96] Sejumlah laboratorium (termasuk di Prancis, Jerman, Yunani, Jepang dan AS) sedang mengembangkan metode termokimia untuk menghasilkan hidrogen dari energi surya dan air.[97]
Korosi anaerobik[sunting | sunting sumber]
Dalam kondisi anaerobik, besi dan baja paduan secara perlahan teroksidasi oleh proton dari air bersamaan dengan berkurangnya molekul hidrogen (H). Saat besi mengalami korosi anaerobik pertama kali akan terbentuk fero hidroksida (karat hijau) dan dapat dijelaskan sesuai reaksi berikut:
- Fe + 2 H2O → Fe(OH)2 + H2
Pada gilirannya, di bawah kondisi anaerobik, fero hidroksida (Fe(OH)) dapat dioksidasi oleh proton dari air untuk membentuk magnetit dan molekul hidrogen. Proses ini dijelaskan melalui reaksi Schikorr:
- 3 Fe(OH)2 → Fe3O4 + 2 H2O + H2
- fero hidroksida → magnetit + air + hidrogen
Kristal magnetit (Fe) yang baik lebih stabil secara termodinamika daripada besi hidroksida (Fe(OH)).
Proses ini terjadi selama korosi anaerobik besi dan baja dalam air tanah bebas oksigen dan dalam tanah pereduksi di bawah permukaan air.
Keberadaan geologi: reaksi serpentinisasi[sunting | sunting sumber]
Dalam ketiadaan oksigen atmosfer (O), pada kondisi geologi dalam yang jauh dari atmosfer Bumi, hidrogen (H) diproduksi selama proses serpentinisasi melalui oksidasi anaerobik oleh proton air (H+) dari fero (Fe2+) silikat yang ada dalam kisi kristal fayalit (Fe, olivin besi). Reaksi pembentukan magnetit (Fe), kuarsa (SiO) dan hidrogen (H) adalah sebagai berikut:
- 3 Fe(OH)2 → Fe3O4 + 2 H2O + H2
fayalit + alir → magnetit + kuasa + hidrogen
Reaksi ini mendekati reaksi Schikorr yang teramati pada oksidasi anaerobik fero hidroksida ketika terkena air.
Pembentukan dalam transformator[sunting | sunting sumber]
Dari semua pembentukan gas akibat adanya kesalahan pada transformator daya, hidrogen adalah yang paling umum dan dihasilkan di bawah kondisi kesalahan apapun; dengan demikian, pembentukan hidrogen merupakan indikasi awal dari masalah serius dalam siklus hidup transformator.[98]
Aplikasi[sunting | sunting sumber]
Industri petrokimia[sunting | sunting sumber]
Sejumlah besar H2 diperlukan dalam industri petrokimia dan kimia. Penggunaan terbesar H2 adalah untuk memproses bahan bakar fosil dan dalam pembuatan ammonia. Konsumen utama dari H2 di kilang petrokimia meliputi hidrodealkilasi, hidrodesulfurisasi, dan penghidropecahan (Inggris: hydrocracking). Banyak dari reaksi ini dapat diklasifikasikan sebagai hidrogenolisis, yaitu pemutusan ikatan dengan karbon. Berikut ini adalah ilustrasi pemisahan belerang dari bahan bakar fosil cair:
- R-S-R + 2 H2 → H2S + 2 RH
Hidrogenasi[sunting | sunting sumber]
Hidrogenasi adalah penambahan H2 ke dalam berbagai substrat yang dilakukan dalam skala besar. Hidrogenasi N2 untuk menghasilkan amonia dengan Proses Haber-Bosch menghabiskan beberapa persen anggaran energi di seluruh industri. Amonia yang dihasilkan digunakan untuk memasok sebagian besar protein yang dikonsumsi manusia.[99] Hidrogenasi digunakan untuk mengubah lemak dan oli tak jenuh menjadi jenuh. Aplikasi utamanya adalah untuk produksi margarin. Methanol diproduksi melalui hidrogenasi karbon dioksida. Ini juga merupakan sumber hidrogen dalam pembuatan asam klorida. H2 juga digunakan sebagai reduktor untuk mengubah beberapa bijih menjadi logam.[100]
Pendingin[sunting | sunting sumber]
Hidrogen banyak digunakan pada pembangkit listrik sebagai pendingin generator karena sejumlah sifatnya yang berhubungan langsung dengan struktur molekul diatomiknya yang ringan. Ini meliputi densitas rendah, rendah viskositasnya, serta mempunyai kapasitas "bahang" spesifik dan konduktivitas termal tertinggi di antara semua gas.
Pembawa energi[sunting | sunting sumber]
Hidrogen bukanlah sumber energi,[101] kecuali dalam konteks hipotesis pembangkit listrik fusi nuklir komersial yang menggunakan deuterium ataupun tritium, sebuah teknologi yang perkembangannya masih sedikit.[102] Energi Matahari berasal dari fusi nuklir hidrogen, namun proses ini sulit dikontrol di Bumi.[103] Hidrogen dari cahaya Matahari, organisme biologi, ataupun dari sumber listrik menghabiskan lebih banyak energi dalam pembuatannya daripada pembakarannya. Hidrogen dapat dihasilkan dari sumber fosil (seperti metana) yang memerlukan lebih sedikit energi daripada energi hasil pembakarannya, namun sumber ini tidak dapat diperbaharui, dan lagipula metana dapat langsung digunakan sebagai sumber energi.[101]
Rapatan energi per volume pada hidrogen cair maupun hidrogen gas pada tekanan yang praktis secara signifikan lebih kecil daripada rapatan energi dari bahan bakar lainnya, walaupun rapatan energi per massa adalah lebih tinggi.[101] Sekalipun demikian, hidrogen telah dibahas secara meluas dalam konteks energi sebagai pembawa energi.[104] Sebagai contoh, sekuestrasi CO2 yang diikuti dengan penangkapan dan penyimpanan karbon dapat dilakukan pada produksi H2 dari bahan bakar fosil.[105] Hidrogen yang digunakan pada transportasi relatif lebih bersih dengan sedikit emisi NOx,[106] tetapi tanpa emisi karbon.[105] Namun, biaya infrastruktur yang diperlukan dalam membangun ekonomi hidrogen secara penuh sangatlah besar.[107] Sel bahan bakar dapat mengubah hidrogen dan oksigen secara langsung menjadi listrik dengan lebih efisien daripada mesin pembakaran internal.[108]
Industri semikonduktor[sunting | sunting sumber]
Hidrogen digunakan untuk menjenuhkan ikatan tak beraturan dalam silikon amorf dan karbon amorf yang membantu menstabilkan sifat materi.[109] Ia juga donor elektron potential dalam berbagai materi oksida, termasuk ZnO,[110][111] SnO, CdO, MgO,[112] ZrO, HfO, La, Y, TiO, SrTiO, LaAlO, SiO, Al, Zirkon silikat (ZrSiO), HfSiO, dan SrZrO.[113]
Penggunaan lain[sunting | sunting sumber]
Selain digunakan sebagai pereaksi, H2 memiliki penerapan yang luas dalam bidang fisika dan teknik. Ia digunakan sebagai gas penameng di metode pengelasan seperti pengelasan hidrogen atomik.[114][115] H2 digunakan sebagai pendingin rotor di generator pembangkit listrik karena ia mempunyai konduktivitas termal yang paling tinggi di antara semua jenis gas. H2 cair digunakan di riset kriogenik yang meliputi kajian superkonduktivitas.[116] Karena H2 lebih ringan dari udara, yang memiliki ⅟14 densitas udara, hidrogen pernah digunakan secara luas sebagai gas pengangkat pada kapal udara balon.[117] Kedepan, dengan berkembangnya kendaraan fuel cell, permintaan dan pemanfaatan hidrogen diperkirakan akan meningkat.[118]
Baru-baru ini hidrogen digunakan sebagai bahan campuran dengan nitrogen (kadang kala disebut forming gas) sebagai gas perunut untuk pendeteksian kebocoran gas yang kecil. Aplikasi ini dapat ditemukan di bidang otomotif, kimia, pembangkit listrik, kedirgantaraan, dan industri telekomunikasi.[119] Hidrogen adalah zat aditif (E 949) yang diperbolehkan penggunaannya dalam uji coba kebocoran bungkusan makanan dan sebagai antioksidan.[120]
Isotop hidrogen yang lebih langka juga memiliki aplikasi tersendiri. Deuterium (hidrogen-2) digunakan dalam reaktor CANDU sebagai moderator untuk memperlambat neutron.[6] Senyawa deuterium juga memiliki aplikasi dalam bidang kimia dan biologi dalam kajian reaksi efek isotop.[121] Tritium (hidrogen-3) yang diproduksi oleh reaktor nuklir digunakan dalam produksi bom hidrogen,[122] sebagai penanda isotopik dalam biosains,[62] dan sebagai sumber radiasi di cat berpendar.[123]
Suhu pada titik tripel hidrogen digunakan sebagai titik acuan dalam skala temperatur ITS-90 (International Temperature Scale of 1990) pada 13,8033 Kelvin.[124]
Reaksi biologi[sunting | sunting sumber]
H2 adalah salah satu hasil produk dari beberapa jenis fermentasi anaerobik dan dihasilkan pula pada beberapa mikroorganisme, biasanya melalui reaksi yang dikatalisasi oleh enzim dehidrogenase yang mengandung besi atau nikel. Enzim-enzim ini mengkatalisasi reaksi redoks reversibel antara H2 dengan komponen dua proton dan dua elektronnya. Gas hidrogen dihasilkan pada transfer reduktor ekuivalen yang dihasilkan selama fermentasi piruvat menjadi air.[125] Siklus alami produksi dan konsumsi hidrogen oleh organisme disebut siklus hidrogen.[126] H2 terdapat dalam jumlah yang kecil di nafas manusia sehat. Ini hasil dari aktivitas metabolisme mikroorganisme yang mengandung hidrogenase di usus besar.[127]
Pemisahan air, yang mana air terurai menjadi komponen proton, elektron, dan oksigen, terjadi pada reaksi cahaya pada proses fotosintesis. Beberapa organisme meliputi ganggang Chlamydomonas reinhardtii dan cyanobacteria memiliki tahap kedua, yaitu reaksi gelap, yang mana proton dan elektron direduksi menjadi gas H2 oleh hidrogenase tertentu di kloroplasnya.[128] Beberapa usaha telah diambil untuk secara genetik memodifikasi hidrogenase cyanobacteria untuk secara efisien mensintesis gas H2 dibawah keberadaan oksigen.[129] Usaha keras juga telah diambil dalam percobaan memodifikasi gen ganggang dan mengubahnya menjadi bioreaktor.[130]
Wewanti keselamatan[sunting | sunting sumber]
| Bahaya | |
|---|---|
| Piktogram GHS | 
|
| Keterangan bahaya GHS | {{{value}}} |
| H220 | |
| P202, P210, P271, P403, P377, P381[131] | |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Hidrogen mendatangkan beberapa bahaya kesehatan pada manusia, mulai dari potensi ledakan dan kebakaran ketika tercampur dengan udara, sampai dengan sifatnya yang menyebabkan asfiksia pada keadaan murni tanpa oksigen.[132] Selain itu, hidrogen cair adalah kriogen dan sangat berbahaya oleh karena suhunya yang sangat rendah.[133] Hidrogen larut dalam beberapa logam dan selain berpotensi kebocoran, juga dapat menyebabkan perapuhan hidrogen.[134] Gas hidrogen yang mengalami kebocoran dapat menyala dengan spontan. Selain itu api hidrogen sangat panas, namun hampir tidak dapat dilihat dengan mata telanjang, sehingga dapat menyebabkan kasus kebakaran yang tak terduga.[135]
Data wewanti keselamatan hidrogen dapat dikacaukan oleh beberapa sebab. Sifat-sifat fisika dan kimia hidrogen sangat bergantung pada nisbah parahidrogen/ortohidrogen yang memerlukan beberapa hari untuk mencapai kesetimbangan (biasanya data yang diberikan merupakan data pada saat hidrogen mencapai kesetimbangan). Parameter ledakan hidrogen, seperti tekanan dan temperatur kritis ledakan sangat bergantung pada geometri wadah penampung hidrogen.[132]
Catatan[sunting | sunting sumber]
- ^ Indonesia: sma (satuan massa atom), Inggris: amu (atomic mass unit)
- ^ Massa alam semesta yang dimaksud adalah massa barionik. Namun, sebagian besar massa alam semesta tidak berada dalam bentuk barion atau unsur kimia. Lihat materi gelap dan energi gelap.
- ^ 286 kjJmol: energi per mol bahan yang terbakar (molekul hidrogen)
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ (Indonesia) "Hidrogen". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Wiberg, Egon; Wiberg, Nils; Holleman, Arnold Frederick (2001). Inorganic chemistry. Academic Press. hlm. 240. ISBN 0123526515.
- ^ Magnetic susceptibility of the elements and inorganic compounds (PDF). CRC Handbook of Chemistry and Physics (edisi ke-81). CRC Press.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 978-0-8493-0464-4.
- ^ a b c "Hydrogen". Van Nostrand's Encyclopedia of Chemistry. Wylie-Interscience. 2005. hlm. 797–799. ISBN 0-471-61525-0.
- ^ a b c d e f g h i j k l m Emsley, John (2001). Nature's Building Blocks. Oxford: Oxford University Press. hlm. 183–191. ISBN 0-19-850341-5.
- ^ a b Stwertka, Albert (1996). A Guide to the Elements. Oxford University Press. hlm. 16–21. ISBN 0-19-508083-1.
- ^ Palmer, David (13 November, 1997). "Hydrogen in the Universe". NASA. Diarsipkan dari versi asli tanggal 2014-10-29. Diakses tanggal 05-02-2008.
- ^ Staff (2007). "Hydrogen Basics — Production". Florida Solar Energy Center. Diarsipkan dari versi asli tanggal 2008-02-18. Diakses tanggal 05-02-2008.
- ^ Rogers, H. C. (1999). "Hydrogen Embrittlement of Metals". Science. 159 (3819): 1057–1064. doi:10.1126/science.159.3819.1057.
- ^ Christensen, C. H. (9 Juli, 2005). "Making society independent of fossil fuels — Danish researchers reveal new technology". Technical University of Denmark. Diarsipkan dari versi asli tanggal 2010-01-07. Diakses tanggal 28-03-2008.
- ^ a b Takeshita, T. (1974). "Hydrogen solubility in 1:5 compounds between yttrium or thorium and nickel or cobalt". Inorganic Chemistry. 13 (9): 2282–2283. doi:10.1021/ic50139a050.
- ^ a b Kirchheim, R. (1988). "Hydrogen in amorphous and nanocrystalline metals". Materials Science and Engineering. 99: 457–462. doi:10.1016/0025-5416(88)90377-1. Diakses tanggal 28-03-2008.
- ^ a b Kirchheim, R. (1988). "Hydrogen solubility and diffusivity in defective and amorphous metals". Progress in Materials Science. 32 (4): 262–325. doi:10.1016/0079-6425(88)90010-2. Diakses tanggal 28-03-2008.
- ^ Carcassi, M. N. (Juni 2005). "Deflagrations of H2–air and CH4–air lean mixtures in a vented multi-compartment environment". Energy. 30 (8): 1439–1451. doi:10.1016/j.energy.2004.02.012.
- ^ National Academy of Engineering, National Academy of Sciences (2004). The Hydrogen Economy: Opportunities, Costs,. National Academies Press. hlm. p. 240. ISBN 0-309-09163-2.
- ^ Patnaik, P. (2007). A Comprehensive Guide to the Hazardous Properties of Chemical Substances. Wiley-Interscience. hlm. 402. ISBN 978-0-471-71458-3.
- ^ Carcassi, M. N.; Fineschi, F. (2005). "Deflagrations of H2–air and CH4–air lean mixtures in a vented multi-compartment environment". Energy. 30 (8): 1439–1451. doi:10.1016/j.energy.2004.02.012.
- ^ Schefer, E. W.; Kulatilaka, W. D.; Patterson, B. D.; Settersten, T. B. (June 2009). "Visible emission of hydrogen flames". Combustion and Flame. 156 (6): 1234–1241. doi:10.1016/j.combustflame.2009.01.011. Diarsipkan dari versi asli tanggal 2021-01-29. Diakses tanggal 2020-10-10.
- ^ Dziadecki, John (2005). "Hindenburg Hydrogen Fire". Diarsipkan dari versi asli tanggal 2007-02-21. Diakses tanggal 16-01-2007.
- ^ Werthmüller, Andreas. "The Hindenburg Disaster". Swiss Hydrogen Association. Diarsipkan dari versi asli tanggal 2008-02-10. Diakses tanggal 05-02-2008.
- ^ Lide, David R., ed. (2006). CRC Handbook of Chemistry and Physics (edisi ke-87). Boca Raton, Florida: CRC Press. ISBN 0-8493-0487-3.
- ^ Clayton, Donald D. (2003). Handbook of Isotopes in the Cosmos: Hydrogen to Gallium. Cambridge University Press. ISBN 0521823811.
- ^ Millar, Tom (10 Desember, 2003). "Lecture 7, Emission Lines — Examples". PH-3009 (P507/P706/M324) Interstellar Physics. University of Manchester. Diarsipkan dari versi asli tanggal 2011-11-16. Diakses tanggal 05-02-2008.
- ^ Stern, David P. (16-05-2005). "The Atomic Nucleus and Bohr's Early Model of the Atom". NASA Goddard Space Flight Center. Diarsipkan dari versi asli tanggal 2007-08-20. Diakses tanggal 20-12-2007.
- ^ Stern, David P. (13-02-2005). "Wave Mechanics". NASA Goddard Space Flight Center. Diarsipkan dari versi asli tanggal 2008-05-13. Diakses tanggal 16-04-2008.
- ^ Staff (2003). "Hydrogen (H2) Properties, Uses, Applications: Hydrogen Gas and Liquid Hydrogen". Universal Industrial Gases, Inc. Diarsipkan dari versi asli tanggal 2008-02-19. Diakses tanggal 05-02-2008.
- ^ Tikhonov, Vladimir I. (2002). "Separation of Water into Its Ortho and Para Isomers". Science. 296 (5577): 2363. doi:10.1126/science.1069513.
- ^ Hritz, James (Maret 2006). "CH. 6 - Hydrogen" (PDF). NASA Glenn Research Center Glenn Safety Manual, Document GRC-MQSA.001. NASA. Diarsipkan (PDF) dari versi asli tanggal 2004-10-20. Diakses tanggal 05-02-2008.
- ^ Shinitzky, Meir; Elitzur, Avshalom C. (30-05-2006). "Ortho-para spin isomers of the protons in the methylene group". Chirality. Rehovot, Israel: Weizmann Institute of Science. 18 (9): 754–756. doi:10.1002/chir.20319. Diakses tanggal 25-03-2008. [pranala nonaktif permanen]
- ^ Milenko, Yu. Ya. (1997). "Natural ortho-para conversion rate in liquid and gaseous hydrogen". Journal of Low Temperature Physics. 107 (1–2): 77–92. doi:10.1007/BF02396837.
- ^ Svadlenak, R. Eldo (1957). "The Conversion of Ortho- to Parahydrogen on Iron Oxide-Zinc Oxide Catalysts". Journal of the American Chemical Society. 79 (20): 5385–5388. doi:10.1021/ja01577a013.
- ^ McCall Group, Oka Group (22 April, 2005). "H3+ Resource Center". Universities of Illinois and Chicago. Diarsipkan dari versi asli tanggal 2007-10-11. Diakses tanggal 05-02-2008.
- ^ Clark, Jim (2002). "The Acidity of the Hydrogen Halides". Chemguide. Diarsipkan dari versi asli tanggal 2012-05-31. Diakses tanggal 09-03-2008.
- ^ Kimball, John W. (07-08-2003). "Hydrogen". Kimball's Biology Pages. Diarsipkan dari versi asli tanggal 2008-03-04. Diakses tanggal 04-03-2008.
- ^ IUPAC Compendium of Chemical Terminology, Electronic version, Hydrogen Bond
- ^ Sandrock, Gary (02-05-2002). "Metal-Hydrogen Systems". Sandia National Laboratories. Diarsipkan dari versi asli tanggal 2012-12-24. Diakses tanggal 23-03-2008.
- ^ a b "Structure and Nomenclature of Hydrocarbons". Purdue University. Diarsipkan dari versi asli tanggal 2020-05-10. Diakses tanggal 23-03-2008.
- ^ "Organic Chemistry". Dictionary.com. Lexico Publishing Group. 2008. Diarsipkan dari versi asli tanggal 2015-09-24. Diakses tanggal 23-03-2008.
- ^ "Biochemistry". Dictionary.com. Lexico Publishing Group. 2008. Diarsipkan dari versi asli tanggal 2012-12-16. Diakses tanggal 23-03-2008.
- ^ a b c Miessler, Gary L. (2003). Inorganic Chemistry (edisi ke-3rd edition). Prentice Hall. ISBN 0130354716.
- ^ Rogers, H. C. (1999). "Hydrogen Embrittlement of Metals". Science. 159 (3819): 1057–1064. Bibcode:1968Sci...159.1057R. doi:10.1126/science.159.3819.1057. PMID 17775040.
- ^ Christensen, C. H.; Nørskov, J. K.; Johannessen, T. (9 July 2005). "Making society independent of fossil fuels – Danish researchers reveal new technology". Technical University of Denmark. Diarsipkan dari versi asli tanggal 21 May 2015. Diakses tanggal 19 May 2015.
- ^ Moers, Kurt (1920). "Investigations on the Salt Character of Lithium Hydride". Zeitschrift für Anorganische und Allgemeine Chemie. 113 (191): 179–228. doi:10.1002/zaac.19201130116.
- ^ Downs, Anthony J. (1994). "The hydrides of aluminium, gallium, indium, and thallium: a re-evaluation". Chemical Society Reviews. 23: 175–184. doi:10.1039/CS9942300175.
- ^ Hibbs, David E. (1999). "A remarkably stable indium trihydride complex: synthesis and characterisation of [InH3{P(C6H11)3}]". Chemical Communications: 185–186. doi:10.1039/a809279f.
- ^ Miessler, G. L.; Tarr, D. A. (2003). Inorganic Chemistry
 (edisi ke-3rd). Prentice Hall. ISBN 978-0-13-035471-6.
(edisi ke-3rd). Prentice Hall. ISBN 978-0-13-035471-6.
- ^ Okumura, Anthony M. (1990). "Infrared spectra of the solvated hydronium ion: vibrational predissociation spectroscopy of mass-selected H3O+•(H2O)n•(H2)m". Journal of Physical Chemistry. 94 (9): 3416–3427. doi:10.1021/j100372a014.
- ^ Perdoncin, Giulio (1977). "Protonation Equilibria in Water at Several Temperatures of Alcohols, Ethers, Acetone, Dimethyl Sulfide, and Dimethyl Sulfoxide". Journal of the American Chemical Society. 99 (21): 6983–6986. doi:10.1021/ja00463a035.
- ^ Carrington, Alan (1989). "The infrared predissociation spectrum of triatomic hydrogen cation (H3+)". Accounts of Chemical Research. 22 (6): 218–222. doi:10.1021/ar00162a004.
- ^ "NASA/TM—2002-211915 : Solid Hydrogen Experiments for Atomic Propellants" (PDF). Diarsipkan dari versi asli (PDF) tanggal 27 September 2011. Diakses tanggal 27 September 2011.
- ^ "Hydrogen". mysite.du.edu. Diarsipkan dari versi asli tanggal 18 April 2009. Diakses tanggal 20 April 2008.
- ^ Gurov, Yu. B. (2004). "Spectroscopy of superheavy hydrogen isotopes in stopped-pion absorption by nuclei". Physics of Atomic Nuclei. 68 (3): 491–97. doi:10.1134/1.1891200.
- ^ Korsheninnikov, A. A.; et al. (2003). "Experimental Evidence for the Existence of 7H and for a Specific Structure of 8He". Physical Review Letters. 90 (8): 082501. doi:10.1103/PhysRevLett.90.082501.
- ^ Urey, Harold C. (1933). "Names for the Hydrogen Isotopes". Science. 78 (2035): 602–603. Diarsipkan dari versi asli tanggal 2009-02-12. Diakses tanggal 20-02-2008.
- ^ Oda, Y (1992). "1H NMR studies of deuterated ribonuclease HI selectively labeled with protonated amino acids". Journal of Biomolecular NMR. 2 (2): 137–47. Diakses tanggal 12-02-2008.
- ^ Broad, William J. (11 November, 1991). "Breakthrough in Nuclear Fusion Offers Hope for Power of Future". The New York Times. Diarsipkan dari versi asli tanggal 2008-05-24. Diakses tanggal 12-02-2008.
- ^ Staff (15 November, 2007). "Tritium". U.S. Environmental Protection Agency. Diarsipkan dari versi asli tanggal 2008-01-02. Diakses tanggal 12-02-2008.
- ^ Nave, C. R. (2006). "Deuterium-Tritium Fusion". HyperPhysics. Georgia State University. Diarsipkan dari versi asli tanggal 2008-03-16. Diakses tanggal 08-03-2008.
- ^ Kendall, Carol (1998). "Fundamentals of Isotope Geochemistry". US Geological Survey. Diakses pada 8 Maret 2008.
- ^ "The Tritium Laboratory". University of Miami. 2008. Diarsipkan dari versi asli tanggal 2008-02-28. Diakses tanggal 08-03-2008.
- ^ a b Holte, Aurali E.; Houck, Marilyn A.; Collie, Nathan L. (03-11-2004). "Potential Role of Parasitism in the Evolution of Mutualism in Astigmatid Mites". Experimental and Applied Acarology. Lubbock: Texas Tech University. 25 (2): 97–107. doi:10.1023/A:1010655610575. Diakses tanggal 08-03-2008. [pranala nonaktif permanen]
- ^ Krogt, Peter van der (5 Mei, 2005). "Hydrogen". Elementymology & Elements Multidict. Diarsipkan dari versi asli tanggal 2023-04-24. Diakses tanggal 20-02-2008.
- ^ § IR-3.3.2, Provisional Recommendations, Nomenclature of Inorganic Chemistry, Chemical Nomenclature and Structure Representation Division, IUPAC. Accessed on line October 3, 2007.
- ^ IUPAC (1997). "Muonium". Dalam A.D. McNaught, A. Wilkinson. Compendium of Chemical Terminology (edisi ke-2nd). Blackwell Scientific Publications. doi:10.1351/goldbook.M04069. ISBN 978-0-86542-684-9. Diarsipkan dari versi asli tanggal 2008-03-13. Diakses tanggal 2020-10-26.
- ^ W.H. Koppenol; IUPAC (2001). "Names for muonium and hydrogen atoms and their ions" (PDF). Pure and Applied Chemistry. 73 (2): 377–380. doi:10.1351/pac200173020377. Diarsipkan dari versi asli (PDF) tanggal 14 May 2011. Diakses tanggal 15 November 2016.
- ^ Gagnon, Steve. "Hydrogen". Jefferson Lab. Diarsipkan dari versi asli tanggal 2008-04-10. Diakses tanggal 05-02-2008.
- ^ Haubold, Hans (15 November, 2007). "Solar Thermonuclear Energy Generation". Columbia University. Diarsipkan dari versi asli tanggal 2006-03-10. Diakses tanggal 12-02-2008.
- ^ Storrie-Lombardi, Lisa J. (2000). "Surveys for z > 3 Damped Lyman-alpha Absorption Systems: the Evolution of Neutral Gas". Astrophysical Journal. 543: 552–576. Diarsipkan dari versi asli tanggal 2023-05-21. Diakses tanggal 05-02-2008.
- ^ Dresselhaus, Mildred; et al. (15 Mei, 2003). "Basic Research Needs for the Hydrogen Economy" (PDF). Argonne National Laboratory, U.S. Department of Energy, Office of Science Laboratory. Diarsipkan dari versi asli (PDF) tanggal 2008-02-13. Diakses tanggal 05-02-2008.
- ^ Berger, Wolfgang H. (15 November, 2007). "The Future of Methane". University of California, San Diego. Diarsipkan dari versi asli tanggal 2020-04-16. Diakses tanggal 12-02-2008.
- ^ McCall Group; Oka Group (22 April 2005), H3+ Resource Center, Universities of Illinois and Chicago, diarsipkan dari versi asli tanggal 2007-10-11, diakses tanggal 5 Februari 2008
- ^ Helm, H.; et.al., Coupling of Bound States to Continuum States in Neutral Triatomic Hydrogen (PDF), Germany: Department of Molecular and Optical Physics, University of Freiburg, diarsipkan (PDF) dari versi asli tanggal 2016-06-16, diakses tanggal 2016-01-06
- ^ Andrews, A. C. (1968). "Oxygen". Dalam Clifford A. Hampel. The Encyclopedia of the Chemical Elements. New York: Reinhold Book Corporation. hlm. 272. LCCN 68-29938.
- ^ Winter, Mark (2007). "Hydrogen: historical information". WebElements Ltd. Diarsipkan dari versi asli tanggal 2008-04-10. Diakses tanggal 05-02-2008.
- ^ National Electrical Manufacturers Association (1946), A chronological history of electrical development from 600 B.C., hlm. 102
- ^ "NTS-2 Nickel-Hydrogen Battery Performance 31". Aiaa.org. Diakses 6 April 2009.
- ^ Jannette, A.G.; Hojnicki, J.S.; McKissock, D.B.; Fincannon, J.; Kerslake, T.W.; Rodriguez, C.D. (July 2002), "Validation of international space station electrical performance model via on-orbit telemetry" (PDF), IECEC '02. 2002 37th Intersociety Energy Conversion Engineering Conference, 2002: 45–50, doi:10.1109/IECEC.2002.1391972, ISBN 0-7803-7296-4, diarsipkan (PDF) dari versi asli tanggal 2010-05-14, diakses tanggal 11 November 2011
- ^ Anderson, P.M.; Coyne, J.W. (2002), "A lightweight high reliability single battery power system for interplanetary spacecraft", Aerospace Conference Proceedings, 5–2433, 5, doi:10.1109/AERO.2002.1035418, ISBN 0-7803-7231-X
- ^ "Mars Global Surveyor". Astronautix.com. Diakses 6 April 2009
- ^ Lori Tyahla, ed. (7 May 2009). "Hubble servicing mission 4 essentials". NASA. Diakses 19 May 2015.
- ^ Hendrix, Susan (25 November 2008). Lori Tyahla, ed. "Extending Hubble's mission life with new batteries". NASA. Retrieved 19 May 2015
- ^ Crepeau, Bob (01-01-2006). "Niels Bohr: The Atomic Model". Great Scientific Minds. Great Neck Publishing. ISBN 1-4298-0723-7. Diakses tanggal 13-04-2008.
- ^ Berman, R. (1956). "Cryogenics". Annual Review of Physical Chemistry. 7: 1–20. doi:10.1146/annurev.pc.07.100156.000245.
- ^ Charlton, Mike; Van Der Werf, Dirk Peter (1 March 2015). "Advances in antihydrogen physics". Science Progress. 98 (1): 34–62. doi:10.3184/003685015X14234978376369.
- ^ Kellerbauer, Alban (29 January 2015). "Why Antimatter Matters". European Review. 23 (01): 45–56. doi:10.1017/S1062798714000532.
- ^ Thomassen, Magnus. "Cost reduction and performance increase of PEM electrolysers" (PDF). fch.europa.eu. FCH JU. Diarsipkan dari versi asli (PDF) tanggal 17 April 2018. Diakses tanggal 22 April 2018.
- ^ Kruse, B.; Grinna, S.; Buch, C. (2002). "Hydrogen Status og Muligheter" (PDF). Bellona. Diarsipkan dari versi asli (PDF) tanggal 2008-02-16. Diakses tanggal 12 February 2008.
- ^ Venere, E. (15 May 2007). "New process generates hydrogen from aluminum alloy to run engines, fuel cells". Purdue University. Diarsipkan dari versi asli tanggal 2008-02-01. Diakses tanggal 5 February 2008.
- ^ Kruse, Bjørnar. "Hydrogen Status og muligheter" (PDF). bellona.org/. Bellona Norway. Diarsipkan dari versi asli (PDF) tanggal 22 April 2018. Diakses tanggal 22 April 2018.
- ^ a b c Oxtoby, D. W. (2002). Principles of Modern Chemistry (edisi ke-5th). Thomson Brooks/Cole. ISBN 0-03-035373-4.
- ^ a b Press, Roman J.; Santhanam, K. S. V.; Miri, Massoud J.; Bailey, Alla V.; Takacs, Gerald A. (2008). Introduction to hydrogen Technology. John Wiley & Sons. hlm. 249. ISBN 978-0-471-77985-8.
- ^ "Hydrogen Properties, Uses, Applications". Universal Industrial Gases, Inc. 2007. Diarsipkan dari versi asli tanggal 2008-02-19. Diakses tanggal 11 March 2008.
- ^ Funderburg, E. (2008). "Why Are Nitrogen Prices So High?". The Samuel Roberts Noble Foundation. Diarsipkan dari versi asli tanggal 2013-05-21. Diakses tanggal 11 March 2008.
- ^ Lees, A. (2007). "Chemicals from salt". BBC. Diarsipkan dari versi asli tanggal 2007-10-26. Diakses tanggal 11 March 2008.
- ^ Weimer, Al (25 May 2005). "Development of solar-powered thermochemical production of hydrogen from water" (PDF). Solar Thermochemical Hydrogen Generation Project. Diarsipkan dari versi asli (PDF) tanggal 2012-10-27. Diakses tanggal 2016-01-07.
- ^ Perret, R. "Development of Solar-Powered Thermochemical Production of Hydrogen from Water, DOE Hydrogen Program, 2007" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2012-10-27. Diakses tanggal 17 May 2008.
- ^ Hirschler, M. M. (2000). Electrical Insulating Materials: International Issues. ASTM International. hlm. 89–. ISBN 978-0-8031-2613-8. Diakses tanggal 13 July 2012.
- ^ Smil, Vaclav (2004). Enriching the Earth: Fritz Haber, Carl Bosch, and the Transformation of World Food Production (edisi ke-1st). Cambridge, MA: MIT. ISBN 9780262693134.
- ^ Chemistry Operations (2003-12-15). "Hydrogen". Los Alamos National Laboratory. Diarsipkan dari versi asli tanggal 2010-01-11. Diakses tanggal 2008-02-05.
- ^ a b c McCarthy, John (1995-12-31). "Hydrogen". Stanford University. Diarsipkan dari versi asli tanggal 2012-05-23. Diakses tanggal 2008-03-14.
- ^ "Nuclear Fusion Power". World Nuclear Association. May 2007. Diarsipkan dari versi asli tanggal 2012-12-25. Diakses tanggal 2008-03-16.
- ^ "Chapter 13: Nuclear Energy — Fission and Fusion". Energy Story. California Energy Commission. 2006. Diarsipkan dari versi asli tanggal 2012-12-24. Diakses tanggal 2008-03-14.
- ^ "DOE Seeks Applicants for Solicitation on the Employment Effects of a Transition to a Hydrogen Economy". Hydrogen Program (Siaran pers). US Department of Energy. 2006-03-22. Diarsipkan dari versi asli tanggal 2011-07-19. Diakses tanggal 2008-03-16. "Salinan arsip". Diarsipkan dari versi asli tanggal 2011-07-19. Diakses tanggal 2008-04-20.
- ^ a b "Carbon Capture Strategy Could Lead to Emission-Free Cars" (Siaran pers). Georgia Tech. 2008-02-11. Diarsipkan dari versi asli tanggal 2008-03-28. Diakses tanggal 2008-03-16.
- ^ Heffel, James W. (2002-12-24). "NOx emission and performance data for a hydrogen fueled internal combustion engine at 1500 rpm using exhaust gas recirculation". International Journal of Hydrogen Energy. Riverside, CA: University of California. 28 (8): 901–908. doi:10.1016/S0360-3199(02)00157-X. Diarsipkan dari versi asli tanggal 2008-12-02. Diakses tanggal 2008-03-16.
- ^ See Romm, Joseph J. (2004). The Hype About Hydrogen: Fact And Fiction In The Race To Save The Climate (edisi ke-1st edition). Island Press. ISBN 155963703X.
- ^ Garbak, John (2011). "VIII.0 Technology Validation Sub-Program Overview" (PDF). DOE Fuel Cell Technologies Program, FY 2010 Annual Progress Report. Diarsipkan dari versi asli (PDF) tanggal 24 September 2015. Diakses tanggal 20 May 2015.
- ^ Le Comber, P. G.; Jones, D. I.; Spear, W. E. (1977). "Hall effect and impurity conduction in substitutionally doped amorphous silicon". Philosophical Magazine. 35 (5): 1173–1187. Bibcode:1977PMag...35.1173C. doi:10.1080/14786437708232943.
- ^ Van de Walle, C.G. (2000). "Hydrogen as a cause of doping in zinc oxide". Physical Review Letters. 85 (5): 1012–1015. Bibcode:2000PhRvL..85.1012V. doi:10.1103/PhysRevLett.85.1012. PMID 10991462.
- ^ Janotti, A.; Van De Walle, C.G. (2007). "Hydrogen multicentre bonds". Nature Materials. 6 (1): 44–47. Bibcode:2007NatMa...6...44J. doi:10.1038/nmat1795. PMID 17143265.
- ^ Kilic, C.; Zunger, Alex (2002). "n-type doping of oxides by hydrogen". Applied Physics Letters. 81 (1): 73–75. Bibcode:2002ApPhL..81...73K. doi:10.1063/1.1482783.
- ^ Peacock, P. W.; Robertson, J. (2003). "Behavior of hydrogen in high dielectric constant oxide gate insulators". Applied Physics Letters. 83 (10): 2025–2027. Bibcode:2003ApPhL..83.2025P. doi:10.1063/1.1609245.
- ^ Durgutlu, Ahmet (2003-10-27). "Experimental investigation of the effect of hydrogen in argon as a shielding gas on TIG welding of austenitic stainless steel". ScienceDirect. Ankara, Turkey: Gazi University. 25 (1): 19–23. doi:10.1016/j.matdes.2003.07.004. Diarsipkan dari versi asli tanggal 2008-04-18. Diakses tanggal 2008-04-06.
- ^ "Atomic Hydrogen Welding". Specialty Welds. 2007. Diarsipkan dari versi asli tanggal 2011-07-16.
- ^ Hardy, Walter N. (2003-03-19). "From H2 to cryogenic H masers to HiTc superconductors: An unlikely but rewarding path". Physica C: Superconductivity. Vancouver, Canada: University of British Columbia. 388–389: 1–6. doi:10.1016/S0921-4534(02)02591-1. Diarsipkan dari versi asli tanggal 2008-12-01. Diakses tanggal 2008-03-25.
- ^ Barnes, Matthew (2004). "LZ-129, Hindenburg". The Great Zeppelins. Diarsipkan dari versi asli tanggal 2012-12-24. Diakses tanggal 2008-03-18.
- ^ Veza, Ibham; Idris, Muhammad; Fattah, Islam Md Rizwanul (2022-06-08). "Circular economy, energy transition, and role of hydrogen". Mechanical Engineering for Society and Industry (dalam bahasa Inggris). 2 (2): 54–56. doi:10.31603/mesi.7134. ISSN 2798-5245. Diarsipkan dari versi asli tanggal 2022-07-11. Diakses tanggal 2022-07-08.
- ^ Block, Matthias (2004-09-03). "Hydrogen as Tracer Gas for Leak Detection". 16th WCNDT 2004. Montreal, Canada: Sensistor Technologies. Diarsipkan dari versi asli tanggal 2018-11-21. Diakses tanggal 2008-03-25.
- ^ "Report from the Commission on Dietary Food Additive Intake" (PDF). European Union. Diarsipkan (PDF) dari versi asli tanggal 2012-10-25. Diakses tanggal 2008-02-05.
- ^ Reinsch, J (October 1980). "The deuterium isotope effect upon the reaction of fatty acyl-CoA dehydrogenase and butyryl-CoA". J. Biol. Chem. 255 (19): 9093–97. Diarsipkan dari versi asli tanggal 2008-04-15. Diakses tanggal 2008-03-24.
- ^ Bergeron, Kenneth D. (Jan–Feb 2004). "The Death of no-dual-use". Bulletin of the Atomic Scientists. Educational Foundation for Nuclear Science, Inc. 60 (1): 15. Diarsipkan dari versi asli tanggal 2008-04-19. Diakses tanggal 2008-04-13.
- ^ Quigg, Catherine T. (March 1984). "Tritium Warning". Bulletin of the Atomic Scientists. Chicago. 40 (3): 56–57. ISSN 0096-3402. Diakses tanggal 2008-04-15.
- ^ "International Temperature Scale of 1990" (PDF). Procès-Verbaux du Comité International des Poids et Mesures. 1989. hlm. T23–T42. Diarsipkan (PDF) dari versi asli tanggal 2017-06-29. Diakses tanggal 2008-03-25.
- ^ Cammack, Richard (2001). Hydrogen as a Fuel: Learning from Nature. Taylor & Francis Ltd. ISBN 0415242428.
- ^ Rhee, T. S.; Brenninkmeijer, C. A. M.; Röckmann, T. (19 May 2006). "The overwhelming role of soils in the global atmospheric hydrogen cycle" (PDF). Atmospheric Chemistry and Physics. 6 (6): 1611–1625. doi:10.5194/acp-6-1611-2006. Diarsipkan dari versi asli (PDF) tanggal 24 August 2019. Diakses tanggal 24 August 2019.
- ^ Eisenmann, Alexander; Amann, Anton; Said, Michael; Datta, Bettina; Ledochowski, Maximilian (2008). "Implementation and interpretation of hydrogen breath tests". Journal of Breath Research. 2 (4): 046002. Bibcode:2008JBR.....2d6002E. doi:10.1088/1752-7155/2/4/046002. PMID 21386189.
- ^ Kruse, O. (2005). "Improved photobiological H2 production in engineered green algal cells". The Journal of Biological Chemistry. 280 (40): 34170–7. doi:10.1074/jbc.M503840200.
- ^ Smith, H. O. (2005). "IV.E.6 Hydrogen from Water in a Novel Recombinant Oxygen-Tolerant Cyanobacteria System" (PDF). FY2005 Progress Report. United States Department of Energy. Diarsipkan (PDF) dari versi asli tanggal 2012-10-25. Diakses tanggal 2008-02-05.
- ^ Williams, Chris (2006-02-24). "Pond life: the future of energy". Science. The Register. Diarsipkan dari versi asli tanggal 2012-11-01. Diakses tanggal 2008-03-24.
- ^ "MyChem: Chemical" (PDF). Diarsipkan dari versi asli (PDF) tanggal 1 October 2018. Diakses tanggal 1 October 2018.
- ^ a b Smith, H. O. (1997). "Safety Standard for Hydrogen and Hydrogen Systems" (PDF). NASA. Diarsipkan dari versi asli (PDF) tanggal 2012-12-24. Diakses tanggal 2008-02-05.
- ^ "Liquid Hydrogen MSDS" (PDF). Praxair, Inc. September 2004. Diarsipkan dari versi asli (PDF) tanggal 2008-05-27. Diakses tanggal 2008-04-16.
- ^ "'Bugs' and hydrogen embrittlement". Science News. Washington D.C. 128 (3): 41. 1985-07-20. ISSN 0036-8423. Diakses tanggal 2008-04-16.
- ^ "Hydrogen Safety". Humboldt State University. Diarsipkan dari versi asli tanggal 2008-02-17. Diakses tanggal 2008-03-15.
Bacaan lebih lanjut[sunting | sunting sumber]
- (1989). "Chart of the Nuclides". Fourteenth Edition. General Electric Company.
- Ferreira-Aparicio, P (2005). "New Trends in Reforming Technologies: from Hydrogen Industrial Plants to Multifuel Microreformers". Catalysis Reviews. 47: 491–588.
- Newton, David E. (1994). The Chemical Elements. New York, NY: Franklin Watts. ISBN 0-531-12501-7.
- Rigden, John S. (2002). Hydrogen: The Essential Element. Cambridge, MA: Harvard University Press. ISBN 0-531-12501-7.
- Romm, Joseph, J. (2004). The Hype about Hydrogen, Fact and Fiction in the Race to Save the Climate. Island Press. ISBN 1-55963-703-X. Author interview Diarsipkan 2010-01-04 di Wayback Machine. at Global Public Media.
- Stwertka, Albert (2002). A Guide to the Elements. New York, NY: Oxford University Press. ISBN 0-19-515027-9.
Pranala luar[sunting | sunting sumber]
- (Inggris) WebElements.com - Hidrogen
- (Inggris) EnvironmentalChemistry.com - Hidrogen
- (Inggris) It's Elemental - Hidrogen
- (Inggris) Table of Nuclides - Hidrogen Diarsipkan 2004-04-07 di Wayback Machine.
- (Inggris) The Truth About Hydrogen; Popular Mechanics Diarsipkan 2007-05-22 di Wayback Machine.
- (Inggris) Basic Hydrogen Calculations of Quantum Mechanics
- (Inggris) National Hydrogen Association
- (Inggris) Hydrogen phase diagram
- (Inggris) RIKEN Beam Science Laboratory, Japan — Heavy hydrogen research Diarsipkan 2007-08-03 di Wayback Machine.
- (Inggris) Wavefunction of hydrogen
- (Inggris) Zinc Powder Will Drive your Hydrogen Car
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


