Fosforilasi oksidatif

Fosforilasi oksidatif adalah suatu lintasan metabolisme dengan penggunaan energi yang dilepaskan oleh oksidasi nutrien untuk menghasilkan ATP, dan mereduksi gas oksigen menjadi air.[1]
Walaupun banyak bentuk kehidupan di bumi menggunakan berbagai jenis nutrien, hampir semua organisme menjalankan fosforilasi oksidatif untuk menghasilkan ATP, oleh karena efisiensi proses mendapatkan energi, dibandingkan dengan proses fermentasi alternatif lainnya seperti glikolisis anaerobik.
Menurut teori kemiosmotik yang dicetuskan oleh Peter Mitchell, energi yang dilepaskan dari reaksi oksidasi pada substrat pendonor elektron, baik pada respirasi aerobik maupun anaerobik, perlahan akan disimpan dalam bentuk potensial elektrokemis sepanjang garis tepi membran tempat terjadinya reaksi tersebut, yang kemudian dapat digunakan oleh ATP sintase untuk menginduksi reaksi fosforilasi terhadap molekul adenosina difosfat dengan molekul Pi.[2]
Elektron yang melekat pada molekul sisi dalam kompleks IV rantai transpor elektron akan digunakan oleh kompleks V untuk menarik ion H+ dari sitoplasma menuju membran mitokondria sisi luar, disebut kopling kemiosmotik,[3] yang menyebabkan kemiosmosis, yaitu difusi ion H+ melalui ATP sintase ke dalam mitokondria yang berlawanan dengan arah gradien pH, dari area dengan energi potensial elektrokimiawi lebih rendah menuju matriks dengan energi potensial lebih tinggi. Proses kopling kemiosmotik juga berpengaruh pada kombinasi gradien pH dan potensial listrik di sepanjang membran yang disebut gaya gerak proton.
Dari teori ini, keseluruhan reaksi kemudian disebut fosforilasi oksidatif.
Awal lintasan dimulai dari elektron yang dihasilkan oleh siklus asam sitrat yang ditransfer ke senyawa:
- NAD+ yang berada di dalam matriks mitokondria. Setelah menerima elektron, NAD+ akan bereaksi menjadi NADH dan ion H+, kemudian mendonorkan elektronnya ke rantai transpor elektron kompleks I.[4]
- dan FAD yang berada di dalam rantai transpor elektron kompleks II.[5] FAD akan menerima dua elektron, kemudian bereaksi menjadi FADH2 melalui reaksi redoks.
Walaupun fosforilasi oksidatif adalah bagian vital metabolisme, ia menghasilkan spesi oksigen reaktif seperti superoksida dan hidrogen peroksida pada kompleks I.[6] Hal ini dapat mengakibatkan pembentukan radikal bebas, merusak sel tubuh, dan kemungkinan juga menyebabkan penuaan. Enzim-enzim yang terlibat dalam lintasan metabolisme ini juga merupakan target dari banyak obat dan racun yang dapat menghambat aktivitas enzim.
Tinjauan transfer energi melalui kemiosmosis[sunting | sunting sumber]
Fosforilasi oksidatif bekerja dengan cara menggunakan reaksi kimia yang menghasilkan energi untuk mendorong reaksi yang memerlukan energi. Kedua set reaksi ini dikatakan bergandengan. Hal ini berarti bahwa salah satu reaksi tidak dapat berjalan tanpa reaksi lainnya. Alur elektron melalui rantai transpor elektron adalah proses eksergonik, yakni melepaskan energi, manakala sintesis ATP adalah proses endergonik, yakni memerlukan energi. Baik rantai transpor elektron dan ATP sintase terdapat pada membran, dan energi ditransfer dari rantai transpor elektron ke ATP sintase melalui pergerakan proton melewati membran ini. Proses ini disebut sebagai kemiosmosis.[7] Dalam praktiknya, ini mirip dengan sebuah sirkuit listrik, dengan arus proton didorong dari sisi negatif membran ke sisi positif oleh enzim pemompa proton yang ada pada rantai transpor elektron. Enzim ini seperti baterai. Pergerakan proton menciptakan gradien elektrokimiawi di sepanjang membran, yang sering disebut gaya gerak proton. Gradien ini mempunyai dua komponen:[8] perbedaan pada konsentrasi proton (gradien pH) dan perbedaan pada potensi listrik. Energi tersimpan dalam bentuk perbedaan potensi listrik dalam mitokondria, dan juga sebagai gradien pH dalam kloroplas.[9]
ATP sintase juga dapat memompa ion H+ keluar dari dalam matriks, apabila terjadi hidrolisis ATP pada kutub kompleksnya.[10] Pada kasus hipertiroidisme pada hepatosit model tikus, juga ditemukan pemompaan ion H+ dari dalam matriks di luar mekanisme rantai transpor elektron,[11] hal ini ditengarai terjadi oleh sebab peran hormon T3[12] yang dapat menyisip pada membran mitokondria sebelah dalam sebagai pompa ion.[13]
Enzim ini seperti motor listrik, yang menggunakan gaya gerak proton untuk mendorong rotasi strukturnya dan menggunakan pergerakan ini untuk mensintesis ATP.
Energi yang dilepaskan oleh fosforilasi oksidatif ini cukup tinggi dibandingkan dengan energi yang dilepaskan oleh fermentasi anaerobik. Glikolisis hanya menghasilkan 2 molekul ATP, sedangkan pada fosforilasi oksidatif 10 molekul NADH dengan 2 molekul suksinat yang dibentuk dari konversi satu molekul glukosa menjadi karbon dioksida dan air, dihasilkan 30 sampai dengan 36 molekul ATP.[14] Rendemen ATP ini sebenarnya merupakan nilai teoretis maksimum; pada praktiknya, ATP yang dihasilkan lebih rendah dari nilai tersebut.[15]
Molekul pemindah elektron dan proton[sunting | sunting sumber]
Rantai transpor elektron membawa baik proton maupun elektron, mengangkut proton dari donor ke akseptor, dan mengangkut proton melawati membran. Proses ini menggunakan molekul yang larut dan terikat pada molekul transfer. Pada mitokondria, elektron ditransfer dalam ruang antarmembran menggunakan protein transfer elektron sitokrom c yang larut dalam air.[16] Ia hanya mengangkut elektron, dan elektron ini ditransfer menggunakan reduksi dan oksidasi atom besi yang terikat pada protein pada gugus heme strukturnya. Sitokrom c juga ditemukan pada beberapa bakteri, di mana ia berlokasi di dalam ruang periplasma.[17]
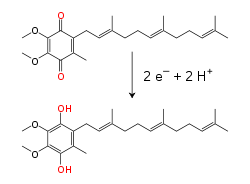
Dalam membran dalam mitokondria, koenzim Q10 pembawa elektron yang larut dalam lipid membawa baik elektron maupun proton menggunakan siklus redoks.[18] Molekul benzokuinon yang kecil ini sangat hidrofobik, sehingga ia akan berdifusi dengan bebas ke dalam membran. Ketika Q menerima dua elektron dan dua proton, ia menjadi bentuk tereduksi ubikuinol (QH2); ketika QH2 melepaskan dua elektron dan dua proton, ia teroksidasi kembali menjadi bentuk ubikuinon (Q). Akibatnya, jika dua enzim disusun sedemikiannya Q direduksi pada satu sisi membran dan QH2 dioksidasi pada sisi lainnya, ubikuinon akan menggandengkan reaksi ini dan mengulang alik proton melewati membran.[19] Beberapa rantai transpor elektron bakteri menggunakan kuinon yang berbeda, seperti menakuinon, selain ubikuinon.[20]
Dalam protein, elektron ditransfer antar kofaktor flavin,[10][21] gugus besi-sulfur, dan sitokrom. Terdapat beberapa jenis gugus besi-sulfur. Jenis paling sederhana yang ditemukan pada rantai transfer elektron terdiri dari dua atom besi yang dihubungkan oleh dua atom sulfur; ini disebut sebagai gugus [2Fe–2S]. Jenis kedua, disebut [4Fe–4S], mengandung sebua kubus empat atom besi dan empat atom sulfur. Tiap-tiap atom pada gugus ini berkoordinasi dengan asam amino, biasanya koordinasi antara atom sulfur dengan sisteina. Kofaktor ion logam menjalani reaksi redoks tanpa mengikat ataupun melepaskan proton, sehingga pada rantai transpor elektron ia hanya berfungsi sebagai pengangkut elektron. Elektron bergerak cukup jauh melalui protein-protein ini dengan cara meloncat disekitar rantai kofaktor ini.[22] Hal ini terjadi melalui penerowongan kuantum, yang terjadi dengan cepat pada jarak yang lebih kecil daripada 1,4×10−9 m.[23]
Rantai transpor elektron eukariotik[sunting | sunting sumber]
Banyak proses katabolik biokimia, seperti glikolisis, siklus asam sitrat, dan oksidasi beta, menghasilkan koenzim NADH. Koenzim ini mengandung elektron yang memiliki potensial transfer yang tinggi. Dengan kata lain, ia akan melepaskan energi yang sangat besar semasa oksidasi. Namun, sel tidak akan melepaskan semua energi ini secara bersamaan karena akan menjadi reaksi yang tidak terkontrol. Sebaliknya, elektron dilepaskan dari NADH dan dipindahkan ke oksigen melalui serangkaian enzim yang akan melepaskan sejumlah kecil energi pada tiap-tiap enzim tersebut. Rangkaian enzim yang terdiri dari kompleks I sampai dengan kompleks IV ini disebut sebagai rantai transpor elektron dan ditemukan dalam membran dalam mitokondria. Suksinat juga dioksidasi oleh rantai transpor elektron, namun ia terlibat dalam lintasan yang berbeda.
Pada eukariota, enzim-enzim pada sistem transpor ini menggunakan energi yang dilepaskan dari oksidasi NADH untuk memompa proton melewati membran dalam mitokondria. Hal ini menyebabkan proton terakumulasi pada ruang antarmembran dan menghasilkan gradien elektrokimia di sepanjang membran. Energi yang tersimpan sebagai energi potensial ini kemudian digunakan oleh ATP sintase untuk menghasilkan ATP. Mitokondria terdapat pada hampir semua eukariota, dengan pengecualian pada protozoa anaerobik seperti Trichomonas vaginalis yang mereduksi proton menjadi hidrogen menggunakan hidrogenosom.[24]
| Sistem pernapasen | Pasangan redoks | Potensial tengah
(Volt) |
|---|---|---|
| NADH dehidrogenase | NAD+ / NADH | −0.32[25] |
| Suksinat dehidrogenase | FMN atau FAD / FMNH2 atau FADH2 | −0.20[25] |
| Kompleks sitokrom bc1 | Koenzime Q10ox / Koenzime Q10red | +0.06[25] |
| Kompleks sitokrom bc1 | Sitokrom box / Sitokrom bred | +0.12[25] |
| Kompleks IV | Sitokrom cox / Sitokrom cred | +0.22[25] |
| Kompleks IV | Sitokrom aox / Sitokrom ared | +0.29[25] |
| Kompleks IV | O2 / HO- | +0.82[25] |
| Kondisi: pH = 7[25] | ||
Pada dasarnya, terdapat dua mekanisme katalitik yang dilakukan tiap kompleks enzim agar transfer elektron dapat menciptakan potensial membran, yaitu mekanisme iterasi redoks dan mekanisme pemompaan ion H+.[2] Pada mekanisme iterasi redoks sendiri, reaksi reduksi akan mengikat ion H+, sedangkan reaksi oksidasi akan melepaskannya. Pada respirasi anaerobik, mekanisme yang sederhana ditunjukkan oleh format dehidrogenase dan nitrat reduktase yang terikat pada membran sel. Pada respirasi aerobik, mekanisme yang terjadi adalah sebagai berikut,
Kompleks I[sunting | sunting sumber]

Kompleks I merupakan protein pertama pada rantai transpor elektron,[26] berupa kompleks enzim yang disebut NADH-koenzim Q oksidoreduktase.
Pada hepatosit hewan sapi, kompleks I adalah enzim raksasa dengan 46 sub-unit dan massa molekul sekitar 1.000 kilodalton (kDa).[27] Hanya struktur enzim kompleks I dari bakteri yang diketahui secara mendetail;[28] pada kebanyakan organisme, kompleks ini menyerupai sepatu but dengan "bola" yang besar menyeruak keluar dari membran ke dalam mitokondria.[29][30] Gen yang mengkode protein ini terdapat pada baik inti sel maupun genom mitokondria.
Reaksi redoks yang dikatalisis oleh enzim ini adalah oksidasi NADH, dan reduksi koenzim Q10 (diwakilkan dengan Q):
Oksidasi NADH akan menghasilkan NAD+ yang diperlukan untuk siklus asam sitrat dan oksidasi asam lemak,
Reaksi oksidasi NADH di atas dikopling oleh reaksi deiodinasi hormon tiroksin dengan promoter berupa peroksidase dan H2O2,[31] sedangkan reduksi Q akan mentranspor elektron ke kompleks berikutnya hingga pada akhirnya digunakan untuk mereduksi oksigen menjadi air.[32]
Awal mula reaksi terjadi ketika NADH berikatan dengan kompleks I dan menyumbang dua elektron. Elektron tersebut kemudian memasuki kompleks I via FMN, suatu gugus prostetik yang melekat pada kompleks. Tambahan elektron ke FMN mengubahnya menjadi bentuk tereduksi, FMNH2. Elektron kemudian ditransfer melalui rangkaian gugus besi-sulfur.[28] Kemudian elektron ditransfer ke Q, mengubahnya menjadi QH2, dan menyebabkan 4 ion H+ terpompa keluar,[33] menuju ke dalam sitoplasma, bukan ke dalam ruang antarmembran, oleh karena kompleks I terikat oleh 3 lapisan membran mitokondria.[34] Pada sel prokariota Escherichia coli dan Klebsiella pneumoniae, kompleks I tidak meletupkan ion H+, melainkan ion Na+.[35]
Terdapat baik jenis gugus besi-sulfur [2Fe-2S] maupun [4Fe–4S] dalam kompleks I.
Kopling yang terjadi dengan siklus asam sitrat,
Kompleks II[sunting | sunting sumber]

Kompleks II merupakan kompleks enzim yang disebut suksinat kuinon oksidoreduktase (EC 1.3.5.1) adalah titik masuk kedua pada rantai transpor elektron,[36] yang terdiri dari kompleks enzim suksinat dehidrogenase aerobik[37] dan fumarat reduktase anaerobik.[37][38][39]
Kompleks II adalah satu-satunya kompleks enzim yang merupakan bagian dari kedua lintasan metabolisme, siklus asam sitrat maupun respirasi seluler pada rantai transpor elektron, dan terdiri dari empat subunit protein dan mengantung sebuah kofaktor flavin adenina dinukleotida yang terikat pada enzim, gugus besi-sulfur, dan sebuah gugus heme yang tidak berpartisipasi pada transfer elektron ke koenzim Q, namun dipercayai penting dalam penurunan produksi spesi oksigen reaktif.[40][41] Enzim ini mereduksi fumarat menjadi suksinat dan meoksidasi hidrokuinon. Karena reaksi ini melepaskan energi lebih sedikit daripada oksidasi NADH, kompleks II tidak mentranspor proton melewati membran dan tidak berkontribusi terhadap gradien proton.
Reaksi redoks pada modus anaerobik oleh fumarat reduktase:
oksidasi
reduksi
Kopling yang terjadi dengan siklus asam sitrat,
Pada beberapa eukariota seperti cacing parasit Ascaris suum, terdapat enzim yang mirip dengan kompleks II, yaitu fumarat reduktase (menakuinol:fumarat oksidoreduktase, atau QFR). Kerja enzim ini terbalik dengan kerja kompleks II, yaitu mengoksidasi ubikuinol dan mereduksi fumarat. Hal ini mengizinkan cacing ini bertahan hidup dalam lingkungan anaerobik di usus besar dan menjalankan fosforilasi oksidatif anaerobik dengan fumarat sebagai akseptor elektron.[42] Fungsi tak lazim kompleks II lainnya dapat dilihat pada parasit malaria Plasmodium falciparum. Pada organisme ini, fungsi kompleks II yang terbalik sebagai oksidase berperan penting dalam pemulihan ubikuinol, yang oleh parasit digunakan untuk biosintesis pirimidina.[43]
Flavoprotein transfer elektron-Q oksidoreduktase[sunting | sunting sumber]
Pada kompleks II terdapat kompleks enzim ETF-QO dengan tiga domain pencerap, masing-masing mengikat FAD, kluster [4Fe-4S]1+, 2+ dan ubikuinon.[44]
ETF-QO mempercepat reaksi redoks:
- reduksi senyawa Q-1 dengan elektron dari senyawa flavoprotein ET yang dapat berasal dari 11 macam flavoprotein dehidrogenase yang terdapat di dalam matriks mitokondria,[45] Pada lintasan alternatif, elektron dapat mengalir dari kluster 4Fe4S dan dikatalitik oleh ETF-QO untuk mereduksi ubikuinon menjadi ubikuinol dengan koenzim FAD.[44] Lintasan reaksi yang terjadi:
reduksi
oksidasi kofaktor
- oksidasi dengan substrat berupa asam lemak yang disebut lintasan oksidasi ß, katabolisme beberapa asam amino dan kolina,[46] kemudian mentransfer elektronnya ke dalam kompleks II.[47]
Pada mamalia, lintasan metabolisme ini sangat penting dan enzim yang berperan adalah asil-KoA dehidrogenase.[48][49]
Reaksi yang terjadi:
oksidasi
reduksi kofaktor
Pada tumbuhan, ETF-QO juga penting dalam respon metabolik demi kelangsungan hidup tumbuhan pada periode lingkungan gelap yang berkepanjangan yang tidak memungkinkan terjadinya fotosintesis, sehingga terjadi simtoma hipoglisemia.
Kompleks III[sunting | sunting sumber]

Kompleks III juga dikenal sebagai kompleks enzim UCCR yang memiliki 11 berkas genetik UQCR.[50][51] Pada mamalia, enzim ini berupa dimer, dengan tiap kompleks subunit mengandung 11 subunit protein, satu gugus besi-sulfur [2Fe-2S], dan tiga sitokrom yang terdiri dari satu sitokrom c1 dan dua sitokrom b.[52] Sitokrom adalah sejenis protein pentransfer elektron yang mengandung paling tidak satu gugus heme. Atom besi dalam gugus heme kompleks III berubah dari bentuk tereduksi Fe (+2) menjadi bentuk teroksidasi Fe (+3) secara bergantian sewaktu elektron ditransfer melalui protein ini.
Reaksi yang dikatalisis oleh kompleks III adalah oksidasi satu molekul ubikuinol dan reduksi dua molekul sitokrom c. Tidak seperti koenzim Q yang membawa dua elektron, sitokrom c hanya membawa satu elektron.
Oleh karena hanya satu elektron yang dapat ditransfer dari donor QH2 ke akseptor sitokrom c, mekanisme reaksi kompleks III lebih rumit daripada kompleks lainnya, dan terjadi dalam dua langkah yang disebut siklus Q.[53] Pada langkah pertama, enzim mengikat tiga substrat, pertama, QH2 yang akan dioksidasi kemudian dengan satu elektron dipindahkan ke sitokrom c yang merupakan substrat kedua. Dua proton yang dilepaskan dari QH2 dilepaskan ke dalam ruang antarmembran. Substrat ketiga adalah Q, yang menerima dua elektron dari QH2 dan direduksi menjadi Q.-, yang merupakan radikal bebas ubisemikuinon. Dua substrat pertama dilepaskan, namun zat antara ubisemikuinon ini tetap terikat. Pada langkah kedua, molekul kedua QH2 terikat dan kemudian melepaskan satu elektronnya ke akspetor sitokrom c. Elektron kedua dilepaskan ke ubisemikuinon yang terikat, mereduksinya menjadi QH2 ketika ia menerima dua proton dari matriks mitokondria. QH2 ini kemudian dilepaskan dari enzim.[54]
Karena koenzim Q direduksi menjadi ubikuinol pada sisi dalam membran dan teroksidasi menjadi ubikuinon pada sisi luar, terjadi transfer proton di membran, yang menambah gradien proton.[10] Mekanisme dua langkah ini sangat penting karena ia meningkatkan efisiensi transfer proton. Jika hanya satu molekul QH2 yang digunakan untuk secara langsung mereduksi dua molekul sitokrom c, efisiensinya akan menjadi setengah, dengan hanya satu proton yang ditransfer per sitokrom c yang direduksi.[10]
Kompleks IV[sunting | sunting sumber]

Kompleks IV adalah protein terakhir pada rantai transpor elektron yang dikenal sebagai kompleks enzim COX.[55]
Dari penelitian pada hepatosit hewan sapi, enzim ini memiliki struktur kompleks yang mengandung 13 subunit, antara lain 5 fosfatidil etanolamina, 3 fosfatidil gliserol, 2 asam kolat, 2 gugus heme A, dan beberapa kofaktor ion logam, meliputi tiga atom tembaga, satu atom magnesium, dan satu atom seng. Dua lintasan peletup ion H+ ditemukan membentang dari matriks hingga sitoplasma.[56]
Pada model hepatosit hewan sapi, ion H+ dengan energi potensial elektrostatik berkisar antara 635meV,[57] tampak dilepaskan dari sitokrom c oksidase[58][59] fosfolipid vesikel (COV) pada kedua fase oksidatif dan reduktif,[60] setelah dikirimkan dari proton loading site (PLS), pada saat ion H+ berikutnya tiba di PLS.[57][61] Mekanisme yang ditunjukkan oleh peletupan ion H+ pada kompleks IV ini disebut efek Bohr redoks.[62][63][64] Peletupan ion H+ (Inggris: deprotonation) terjadi bersamaan dengan perubahan gugus karboksil asam aspartat yang berada pada permukaan intermembran menjadi aspargina.[65]
Enzim ini memediasi reaksi terakhir pada rantai transpor elektron dan mentransfer elektron ke oksigen, manakala memompa proton melewati membran. Oksigen yang menerima elektron, juga dikenal sebagai akseptor elektron terminal, direduksi menjadi air. Baik pemompaan proton secara langsung maupun konsumsi proton matriks pada reduksi oksigen berkontribusi kepada gradien proton. Menurut Keilin, reaksi yang dikatalisis oleh sitokrom c dan reduksi oksigennya adalah:[14]
Reduktase dan oksidase alternatif[sunting | sunting sumber]
Enzim-enzim yang disebutkan di atas merupakan hasil kajian pada hewan mamalia. Sebenarnya, banyak organisme eukariotik lainnya yang memiliki rantai transpor elektron yang berbeda. Sebagai contoh, tumbuhan memiliki NADH oksidase alternatif, yang mengoksidasi NADH di sitosol daripada di matriks mitokondria, dan ia akan memindahkan elektron ke kolam ubikuinon.[66] Enzim-enzim ini tidak mentranspor proton, sehingga ia mereduksi ubikuinon tanpa mengubah gradien elektronkimia membran dalam.[67]
Contoh rantai transpor elektron divergen lainnya adalah oksidase alternatif yang ditemukan pada tumbuh-tumbuhan, beberapa spesies fungi, protista, dan kemungkinan pula pada beberapa hewan.[68][69] Enzim ini secara langsung mentransfer elektron dari ubikuinol ke oksigen.[70]
Lintasan tranpor elektron yang dihasilkan oleh NADH dan ubikuinon oksidase alternatif ini memiliki rendemen ATP yang lebih rendah. Keuntungan dari lintasan yang lebih singkat ini belumlah cukup jelas. Namun, oksidasi alternatif ini dihasilkan sebagai respon terhadap berbagai tekanan seperti hawa dingin, spesi oksigen reaktif, infeksi oleh patogen, dan faktor-faktor lainnya yang menghambat rantai transpor elektron secara penuh.[71][72] Lintasan alternatif ini oleh karenanya akan meningkatkan resistansi organisme terhadap luka dengan menurunkan stres oksidatif.[73]
Pengorganisasian kompleks-kompleks[sunting | sunting sumber]
Model awal bagaimana rantai kompleks respiratori ini terorganisasikan adalah bahwa kompleks-kompleks ini berdifusi dengan bebas dan terbebas dari membran mitokondria.[27] Namun, data-data terbaru mensugestikan bahwa kompleks-kompleks ini kemungkinan membentuk struktur berorde tinggi yang disebut superkompleks ataupun "respirasom."[74] Berdasarkan model superkompleks ini, berbagai jenis kompleks ini terdapat dalam bentuk sehimpunan enzim-enzim yang berinteraksi dan terorganisasi.[75] Asosiasi ini mengizinkan penyaluran substrat di antara berbagai kompleks enzim, sehingga meningkatkan laju dan efisiensi transfer elektron.[76] Dalam superkompleks mamalia, beberapa komponen kompleks akan lebih banyak daripada yang lainnya, dengan beberapa data mensugestikan rasio antara kompleks I/II/II/IV dan ATP sintase kira-kira 1:1:3:7:4.[77] Walau demikian, perdebatan mengenai hipotesis superkompleks ini masihlah belum berakhir, karena beberapa data tampaknya tidak sesuai dengan model ini.[27][78]
Rantai transpor elektron prokariotik[sunting | sunting sumber]
Berbeda dengan banyaknya kemiripan dalam struktur dan fungsi rantai transpor elektron pada eukariota, bakteri dan arkaea memiliki banyak jenis enzim transfer elektron yang sangat bervariasi. Enzim-enzim yang bervariasi ini pula menggunakan senyawa kimia yang bervaruasi sebagai substrat.[79] Walau demikian, terdapat kesamaan dengan rantai transpor elektron eukarita, yaitu transpor elektron prokariotik juga menggunakan energi yang dilepaskan dari oksidasi substrat untuk memompa ion keluar masuk membran dan menghasilkan gradien elektrokimia. Fosforilasi oksidatif bakteri, utamanya bakteri Escherichia coli telah dipahami secara mendetail, manakala pada arkaea, hal ini masih belum dipahami dengan baik.[80]
Perbedaan utama antara fosforilasi eukariotik dengan fosforilasi oksidatif prokariotik adalah bahwa bakteri dan arkaea menggunakan banyak senyawa-senyawa yang berbeda untuk menerima dan mendonor elektron. Hal ini sebenarnya mengizinkan prokariota untuk hidup dan tumbuh dalam berbagai jenis kondisi dan lingkungan.[81] Pada E. coli, sebagai contohnya, fosforilasi oksidatif dapat didorong oleh sejumlah besar pasangan reduktor dan oksidator (lihat tabel di bawah). Potensial titik tengah suatu senyawa kimia mengukur seberapa banyak energi yang dilepaskan ketika ia dioksidasi maupun direduksi, dengan reduktor memiliki potensial negatif dan oksidator positif.
| Enzim pernapasen | Pasangan redoks | Potensial titik tengah
(Volt) |
|---|---|---|
| Format dehidrogenase | Bikarbonat / Format | −0,43 |
| Hidrogenase | Proton / Hidrogen | −0,42 |
| NADH dehidrogenase | NAD+ / NADH | −0,32 |
| Gliserol-3-fosfat dehidrogenase | DHAP / Gly-3-P | −0,19 |
| Piruvat oksidase | Asetat + Karbon dioksida / Piruvat | ? |
| Laktat dehidrogenase | Piruvat / Laktat | −0,19 |
| Asam D-amino dehidrogenase | 2-oksoasam + amonia / Asam D-amino | ? |
| Glukosa dehidrogenase | Glukonat / Glukosa | −0,14 |
| Suksinat dehidrogenase | Fumarat / Suksinat | +0,03 |
| Ubikuinol oksidase | Oksigen / Air | +0,82 |
| Nitrat reduktase | Nitrat / Nitrit | +0,42 |
| Nitrit reduktase | Nitrit / Amonia | +0,36 |
| Dimetil sulfoksida reduktase | DMSO / DMS | +0,16 |
| Trimetilamina N-oksida reduktase | TMAO / TMA | +0,13 |
| Fumarat reduktase | Fumarat / Suksinat | +0,03 |
Sebagaimana yang ditunjukkan oleh tabel di atas, E. coli dapat tumbuh dengan menggunakan reduktor seperti format, hidrogen, ataupun laktat sebagai donor elektron dan nitrat, DMSO, ataupun oksigen akseptor.[81] Semakin besar perbedaan potensial titik tengah antra reduktor dan oksidator, semakin banyak pula energi yang dilepaskan ketika bereaksi. Dari seluruh pasangan senyawa ini, pasangan suksinat/fumarat tidak lazim karena potensial titik tengahnya mendekati nol. Suksinat oleh karenanya dapat dkoksidasi menjadi fumarat apabila terdapat oksidator kuat seperti oksigen dan fumarat dapat direduksi menjadi suksinat menggunakan reduktor kuat seperti format. Reaksi alternatif ini dikatalisis oleh suksinat dehidrogenase untuk oksidasi suksinat dan fumarat reduktase untuk reduksi fumarat.[83]
Beberapa prokariota menggunakan pasangan redoks yang hanya memiliki perbedaan potensial titik tengah yang kecil. Sebagai contohnya, bakteri yang melakukan nitrifikasi seperti Nitrobakter mengoksidasi nitrit menjadi nitrat dan mendonarkan elektron ke oksigen. Sejumlah kecil energi yang dilepaskan oleh reaksi ini cukup untuk memompa proton dan menghasilkan ATP, namun tidak cukup untuk menghasilkan NADH ataupun NADPH secara langsung untuk digunakan dalam anabolisme.[84] Permasalahan ini diselesaikan dengan menggunakan nitrit oksidoreduktase untuk menghasilkan gaya gerak proton yang cukup untuk menjalankan sebagai rantai transpor elektron secara terbalik, menyebabkan kompleks I memproduksi NADH.[85][86]
Prokariota mengontrol penggunaan donor dan akseptor elektron ini dengan memproduksi enzim tertentu sesuai dengan kondisi lingkungan.[87] Fleksibilitas ini dimungkinkan karena oksidase dan reduktase yang berbeda menggunakan kolam ubikuinon yang sama. Ini mengizinkan banyak kombinasi enzim untuk bekerja secara bersamaan, yang saling terhubung oleh zat antara ubikuinol.[82]
Selain beranekaragamnya lintasan metabolisme ini, prokariota juga memiliki sejumlah besar isozim, yaitu enzim-enzim berbeda yang mengkatalisis reaksi yang sama. Sebagai contohnya, E. coli memiliki dua jenis ubikuinol oksidase yang berbeda. Di bawah kondisi aerob, sel menggunakan oksidase yang berafinitas rendah terhadap oksigen yang dapat mentranspor dua proton per elektron. Namun, apabila kadar oksigen menurun, sel akan menggunakan oksidase yang hanya mentransfer satu proton per elektron namun berafinitas tinggi terhadap oksigen.[88]
ATP sintase (kompleks V)[sunting | sunting sumber]
ATP sintase, juga disebut kompleks V, adalah enzim terakhir dalam lintasan fosforilasi oksidatif. Enzim ini ditemukan di seluruh organisme hidup dan berfungsi sama pada prokariota maupun eukariota.[89] Enzim ini menggunakan energi yang tersimpan pada gradien proton di sepanjang membran untuk mendorong sintesis ATP dari ADP dan fosfat (Pi). Perkiraan jumlah proton yang diperlukan untuk mensintesis satu ATP berkisar antara tiga sampai dengan empat,[90][91] dengan beberapa peneliti yang mensugestikan bahwa sel dapat memvariasikan rasio ini sesuai dengan kondisi.[92]
Reaksi fosforilasi ini adalah reaksi kesetimbangan, yakni ia dapat digeser dengan mengubah gaya gerak proton. Dengan ketiadaan gaya gerak proton, reaksi ATP sintase akan berjalan dari sisi kanan ke kiri, menghidrolisis ATP dan memompa proton keluar dari matriks melewati membran. Namun, ketika gaya gerak protonnya tinggi, reaks dipaksa untuk berjalan secara terbalik, yaitu dari sisi kanan ke kiri, mengizinkan proton mengalir dan mengubah ADP menjadi ATP.[89]
ATP sintase adalah sebuah kompleks protein yang besar dengan bentuk seperti jamur. Kompleks enzim ini pada mamalia mengandung 16 subunit dan memiliki massa kira-kira 600 kilodalton.[93] Bagian yang tertanam pada membran disebut FO dan mengandung sebuah cincin subunit c dan saluran proton. "Tangkai" dan kepala yang berbentuk bola disebut F1 dan merupakan tempat sintesis ATP. Kompleks yang berbentuk bola pada ujung akhir F1 mengandung enam protein yang dapat dibagi menjadi dua jenis: tiga subunit α dan tiga subunit β), manakala bagian "tangkai" terdiri dari satu protein: subunit γ, dengan ujung tangkai menusuk ke dalam bola subunit α dan β.[94] Baik subunit α dan β mengikat nukleotida, namun hanya subunit β yang mengkatalisis reaksi sintesis ATP. Di samping F1 pula terdapat sebuah subunit berbentuk batang yang menghubungakan subunit α dan β dengan dasar enzim.
Seiring dengan mengalirnya proton melewati membran melalui saluran ini, motor FO berotasi.[95] Rotasi dapat disebabkan oleh perubahan pada ionisasi asam amino cincin subunit c, menyebabkan interaksi elektrosatik yang menolak cincin subunit c.[96] Cincin yang berotasi ini pada akhirnya akan memutar "as roda" (tangkai subunit γ). Subunit α dan β dihalangi untuk berputar oleh batang samping yang berfungsi sebagai stator. Pergerakan ujung subunit γ yang berada dalam bola subunit α dan β memberikan energi agar tapak aktif pada subunit β menjalankan siklus pergerakan yang memproduksi dan kemudian melepaskan ATP.[9]

Reaksi sintesis ATP ini disebut sebagai mekanisme perubahan ikatan (binding change mechanism) dan melibatkan tapak aktif subunit β yang berputar terus dalam tiga keadaan.[97] Pada keadaan "terbuka", ADP dan fosfat memasuki tapa aktif (ditunjukkan dalam warna coklat pada diagram). Protein kemudian menutup dan mengikat ADP dan fosfat secara longgar (keadaan "longgar" ditunjukkan dalam warna merah). Enzim kemudian berubah bentuk lagi dan memaksa kedua molekul ini bersama, dengan tapak aktif dalam keadaan "ketat" (ditunjukan dalam warna merah jambu) dan mengikat molekul ATP yang terbentuk. Tapak aktif kemudian kembali lagi ke keadaan terbuka dan melepaskan ATP untuk kemudian mengikat ADP dan fosfat, dan memulai siklus yang baru.
Pada beberapa bakteri dan arkaea, sintesis ATP didorong oleh pergerakan ion natrium yang melalui membran sel daripada pergerakan proton.[98][99] Arkaea seperti Methanococcus juga mengandung A1Ao sintase, sebuah bentuk enzim yang mengandung protein tambahan dengan kemiripan urutan asam amino yang kecil dengan subunit ATP sintase bakteri dan eukariota lainnya. Adalah mungkin bahwa pada beberapa spesies, bentuk enzim A1Ao adalah ATP-sintase terspesialisasi yang digerakkan oleh natrium,[100] namun ini tidaklah benar pada keseluruhan kasus.[99]
Spesi oksigen reaktif[sunting | sunting sumber]
Oksigen molekuler merupakan akseptor elektron akhir yang ideal, karena ia merupakan oksidator kuat. Reduksi oksigen melibatkan zat antara yang berpotensi bahaya.[101] Walaupun transfer empat elektron dan empat proton akan mereduksi oksigen menjadi air, yang tidak berbahaya, transfer satu atau dua elektron akan menghasilkan anion superoksida ataupun anion peroksida, yang sangat reaktif dan berbahaya.
Spesi oksigen reaktif dan produk reaksinya ini seperti radikal hidroksil, sangatlah berbahaya bagi sel, karena akan mengoksidasi protein dan mengakibatkan mutasi pada DNA. Kerusakan ini berkontribusi terhadap penyakit dan diajukan pula merupakan salah satu akibat dari penuaan.[102][103]
Kompleks sitokrom c sangat efisien mereduksi oksigen menjadi air, dan melepaskan hanya sedikit zat antara yang tereduksi secara parsial. Namun terdapat sejumlah kecil anion superoksida dan peroksida yang diproduksi oleh rantai transpor elektron.[104] Terutama pentingnya adalah pada reduksi koenzime Q pada kompleks III, karena radikal bebas ubikuinon yang sangat reaktif terbentuk sebagai zat antara dalam siklus Q. Spesi yang tidak stabil ini dapat menyebabkan "kebocoran" elektron ketika elektron ditransfer secara langsung ke oksigen dan menghasilkan superoksida.[105] Karena laju produksi spesi oskigen reaktif oleh kompleks pemompa proton ini tertinggi ketika potensial membran tinggi, diajukan bahwa mitokondria meregulasi aktivitas kompleks untuk menjaga potensial membran berada dalam kisaran yang kecil sehingga menyeimbangkan produksi ATP terhadap produksi oksidator.[106] Sebagai contohnya, oksidator dapat mengaktivasi UCP (uncoupling protein) yang menurunkan potensial membran.[107]
Untuk melawan spesi oksigen reaktif ini, sel mengandung sejumlah sistem antioksidan, meliputi vitamin antioksidan seperti vitamin C dan vitamin E, dan enzim antioksidan seperti superoksida dismutase, katalase, dan peroksidase,[101] yang menetralkan spesi reaktif sehingga mengurangi kerusakan sel.
Gugus anion superoksida, senyawa organik yang sangat aktif yang terdapat pada molekul hidrogen peroksida dan jenis ROS lainnya, merupakan produk samping reaksi redoks yang terjadi pada rantai transpor elektron.[108] Gangguan mekanisme produksi ROS dapat berakibat pada berbagai macam patologi seperti diabetes, neurodegenerasi, gagal jantung, chronic obstructive pulmonary disease. Domain produksi anion superoksida terletak pada kompleks I dan kompleks III.
Dari beberapa senyawa intermediat pengusung satu elektron, radikal bebas SQ- dianggap merupakan senyawa yang paling berperan aktif dalam mereduksi molekul oksigen menjadi anion superoksida. Molekul semikuinon dihasilkan kompleks I dan III sebagai hasil reduksi ubikuinon atau oksidasi ubikuinol,
SQ- akan melekat pada kompleks I atau III hingga saat terstimulasi elektron yang kedua dengan reaksi,
Semikuinon lebih lanjut dapat berinteraksi langsung dengan molekul oksigen dengan reaksi,
Inhibitor[sunting | sunting sumber]
Terdapat beberapa obat dan racun yang dikenal baik menginhibisi fosforilasi oksidatif. Walaupun semua racun hanya menginhibisi satu enzim pada rantai transpor elektron, inhibisi pada langkah apapun pada proses ini akan menghentikan keseluruhan proses. Contohnya, jika oligomisin menginhibisi ATP sintase, proton tidak dapat mengalir balik ke dalam mitokondria.[109] Akibatnya, pompa proton tidak dapat bekerja, karena gradien konsentrasinya menjadi terlalu kuat untuk diatasi. NADH kemudian tidak akan lagi teroksidasi dan siklus asam sitrat berhenti bekerja karena konsentrasi NAD+ menurun di bahwa kadar yang cukup agar enzim bekerja.
| Senyawa | Kegunaan | Efek terhadap fosforilasi oksidatif |
|---|---|---|
| Sianida Karbon monoksida |
Racun | Menghambat rantai transpor elektron dengan terikat lebih kuat daripada oksigen pada pusat Fe–Cu dalam sitokrom c oksidase, mencegah reduksi oksigen.[110] |
| Oligomisin | Antibiotik | Menghambat ATP sintase dengan memblokir aliran proton ke subunit Fo.[109] |
| CCCP 2,4-Dinitrofenol |
Racun | Ionofor yang mengganggu gradien proton dengan membawa proton melewati membran. Ionofor ini mengawagandengkan (uncouple) pompa proton dari sintesis ATP karena ia membawa proton melewati membran mitokondria dalam.[111] |
| Rotenon | Pestisida | Mencegah transfer elektron dari kompleks I ke ubikuinon dengan menutup tapak ikat ubikuinon.[112] |
| Malonat dan oksaloasetat | Inhibitor kompetitif suksinat dehidrogenase (kompleks II).[113] |
Tidak semua inhibitor fosforilasi oksidatif bersifat racun. Pada jaringan lemak coklat, saluran proton yang diregulasi disebut UCP (uncoupling protein), yang dapat mengawagandengkan respirasi dari sintesis ATP.[114] Respirasi cepat ini menghasilkan panas, dan proses ini sangat penting dalam menjaga suhu tubuh pada hewan yang berhibernasi, walaupun protein ini kemungkinan juga memiliki fungsi umum dalam respon sel terhadap stres.[115]
Referensi[sunting | sunting sumber]
- ^ (Inggris) Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - Fig. 2-82. The final stages of oxidation of food molecules (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-16.
- ^ a b (Inggris) "Experimental support for the "E pathway hypothesis" of coupled transmembrane e– and H+ transfer in dihemic quinol:fumarate reductase". Department of Molecular Membrane Biology, Max Planck Institute of Biophysics, Institut für Mikrobiologie, Institut für Biophysik, Institut für Organische Chemie, Johann Wolfgang Goethe-Universität; C. Roy D. Lancaster, Ursula S. Sauer, Roland Groß, Alexander H. Haas, Jürgen Graf, Harald Schwalbe, Werner Mäntele, Jörg Simon, dan M. Gregor Madej. Diarsipkan dari versi asli tanggal 2023-03-12. Diakses tanggal 2010-11-09.
- ^ (Inggris) Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - Chemiosmotic coupling (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-13.
- ^ (Inggris) "The Cell - The Mechanism of Oxidative Phosphorylation - Fig. 10.8". Geoffrey M. Cooper. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-15.
- ^ (Inggris) "The Cell - The Mechanism of Oxidative Phosphorylation - Fig. 10.9". Geoffrey M. Cooper. Diakses tanggal 2010-07-15.
- ^ (Inggris) "Generation of superoxide by the mitochondrial Complex I". Department of Biochemistry, School of Biology, Moscow State University; Grivennikova VG, Vinogradov AD. Diarsipkan dari versi asli tanggal 2012-06-27. Diakses tanggal 2010-07-18.
- ^ Mitchell P, Moyle J (1967). "Chemiosmotic hypothesis of oxidative phosphorylation". Nature. 213 (5072): 137–9. doi:10.1038/213137a0. PMID 4291593.
- ^ (Inggris) Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, and Peter Walter (2002). Molecular Biology of the Cell - electrochemical proton gradient (edisi ke-4). Garland Science. ISBN 0-8153-3218-1. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-13.
- ^ a b Dimroth P, Kaim G, Matthey U (2000). "Crucial role of the membrane potential for ATP synthesis by F(1)F(o) ATP synthases". J. Exp. Biol. 203 (Pt 1): 51–9. PMID 10600673. Diarsipkan dari versi asli tanggal 2007-09-30. Diakses tanggal 2009-05-17.
- ^ a b c d Schultz B, Chan S (2001). "Structures and proton-pumping strategies of mitochondrial respiratory enzymes". Annu Rev Biophys Biomol Struct. 30: 23–65. doi:10.1146/annurev.biophys.30.1.23. PMID 11340051.
- ^ (Inggris) "Hyperthyroidism stimulates mitochondrial proton leak and ATP turnover in rat hepatocytes but does not change the overall kinetics of substrate oxidation reactions". Department of Biochemistry, University of Cambridge; Harper ME, Brand MD. Diarsipkan dari versi asli tanggal 2016-02-05. Diakses tanggal 2010-07-18.
- ^ (Inggris) "Gating of the mitochondrial permeability transition pore by thyroid hormone". Department of Human Nutrition and Metabolism, Hebrew University Medical School,; Yehuda-Shnaidman E, Kalderon B, Azazmeh N, Bar-Tana J. Diarsipkan dari versi asli tanggal 2016-06-20. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Chemiosmotic Gradient: Generation and Maintenance". Department of Biochemistry & Cell Biology; Rice University. Diarsipkan dari versi asli tanggal 2021-11-29. Diakses tanggal 2010-07-18.
- ^ a b Rich PR (2003). "The molecular machinery of Keilin's respiratory chain". Biochem. Soc. Trans. 31 (Pt 6): 1095–105. doi:10.1042/BST0311095. PMID 14641005. Diarsipkan dari versi asli tanggal 2019-09-12. Diakses tanggal 2009-05-17.
- ^ Porter RK, Brand MD (1995). "Mitochondrial proton conductance and H+/O ratio are independent of electron transport rate in isolated hepatocytes". Biochem. J. 310 ((Pt 2)): 379–82. PMC 1135905
 . PMID 7654171.
. PMID 7654171.
- ^ Mathews FS (1985). "The structure, function and evolution of cytochromes". Prog. Biophys. Mol. Biol. 45 (1): 1–56. doi:10.1016/0079-6107(85)90004-5. PMID 3881803.
- ^ Wood PM (1983). "Why do c-type cytochromes exist?". FEBS Lett. 164 (2): 223–6. doi:10.1016/0014-5793(83)80289-0. PMID 6317447.
- ^ Crane FL (2001). "Biochemical functions of coenzyme Q10". Journal of the American College of Nutrition. 20 (6): 591–8. PMID 11771674. Diarsipkan dari versi asli tanggal 2008-12-16. Diakses tanggal 2009-05-17.
- ^ Mitchell P (1979). "Keilin's respiratory chain concept and its chemiosmotic consequences". Science. 206 (4423): 1148–59. doi:10.1126/science.388618. PMID 388618.
- ^ Søballe B, Poole RK (1999). "Microbial ubiquinones: multiple roles in respiration, gene regulation and oxidative stress management" (PDF). Microbiology (Reading, Engl.). 145 (Pt 8): 1817–30. PMID 10463148. Diarsipkan (PDF) dari versi asli tanggal 2008-05-29. Diakses tanggal 2009-05-17.
- ^ Johnson D, Dean D, Smith A, Johnson M (2005). "Structure, function, and formation of biological iron-sulfur clusters". Annu Rev Biochem. 74: 247–81. doi:10.1146/annurev.biochem.74.082803.133518. PMID 15952888.
- ^ Page CC, Moser CC, Chen X, Dutton PL (1999). "Natural engineering principles of electron tunnelling in biological oxidation-reduction". Nature. 402 (6757): 47–52. doi:10.1038/46972. PMID 10573417.
- ^ Leys D, Scrutton NS (2004). "Electrical circuitry in biology: emerging principles from protein structure". Curr. Opin. Struct. Biol. 14 (6): 642–7. doi:10.1016/j.sbi.2004.10.002. PMID 15582386.
- ^ Boxma B, de Graaf RM, van der Staay GW; et al. (2005). "An anaerobic mitochondrion that produces hydrogen". Nature. 434 (7029): 74–9. doi:10.1038/nature03343. PMID 15744302.
- ^ a b c d e f g h Medical CHEMISTRY Compendium. By Anders Overgaard Pedersen and Henning Nielsen. Aarhus University. 2008
- ^ Hirst J (2005). "Energy transduction by respiratory complex I—an evaluation of current knowledge" (PDF). Biochem. Soc. Trans. 33 (Pt 3): 525–9. doi:10.1042/BST0330525. PMID 15916556.
- ^ a b c Lenaz G, Fato R, Genova M, Bergamini C, Bianchi C, Biondi A (2006). "Mitochondrial Complex I: structural and functional aspects". Biochim Biophys Acta. 1757 (9–10): 1406–20. doi:10.1016/j.bbabio.2006.05.007. PMID 16828051.
- ^ a b Sazanov L.A., Hinchliffe P. (2006) Structure of the hydrophilic domain of respiratory complex I from Thermus thermophilus. Science 311, 1430–1436
- ^ Baranova EA, Holt PJ, Sazanov LA (2007). "Projection structure of the membrane domain of Escherichia coli respiratory complex I at 8 A resolution". J. Mol. Biol. 366 (1): 140–54. doi:10.1016/j.jmb.2006.11.026. PMID 17157874.
- ^ Friedrich T, Böttcher B (2004). "The gross structure of the respiratory complex I: a Lego System". Biochim. Biophys. Acta. 1608 (1): 1–9. doi:10.1016/j.bbabio.2003.10.002. PMID 14741580.
- ^ (Inggris) "Deiodination of L-Thyroxine and its Activity on the Oxidation in vitro of Reduced Nicotinamide-Adenine Dinucleotide by Peroxidase plus Hydrogen Peroxide" (PDF). Thyroid Research Unit, Inttuto G. Marani6n, Ctentro de Investigaciones Biol6gicas, Consejo Superior de Investigaciones Cientlflcas; TRINIDAD JOLIN dan GABRIELLA MORREALE DE ESCOBAR. Diarsipkan (PDF) dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-11-20.
It was found that in the absence of both peroxidase and H202, thyroxine did not affect the concentration of NADH and was not deiodinated.
- ^ (Inggris) "Towards the molecular mechanism of respiratory complex I". Medical Research Council Mitochondrial Biology Unit; Hirst J. Diarsipkan dari versi asli tanggal 2019-10-14. Diakses tanggal 2010-11-04.
- ^ (Inggris) "The flavoprotein subcomplex of complex I (NADH:ubiquinone oxidoreductase) from bovine heart mitochondria: insights into the mechanisms of NADH oxidation and NAD+ reduction from protein film voltammetry". Medical Research Council Dunn Human Nutrition Unit; Barker CD, Reda T, Hirst J. Diarsipkan dari versi asli tanggal 2011-08-30. Diakses tanggal 2010-11-04.
- ^ (Inggris) "Interactions between phospholipids and NADH:ubiquinone oxidoreductase (complex I) from bovine mitochondria". Medical Research Council Dunn Human Nutrition; Sharpley MS, Shannon RJ, Draghi F, Hirst J. Diarsipkan dari versi asli tanggal 2014-05-14. Diakses tanggal 2010-11-04.
- ^ (Inggris) "Proton pumping by NADH:ubiquinone oxidoreductase. A redox driven conformational change mechanism?". Universität Frankfurt, Fachbereich Medizin, Institut für Biochemie I; Ulrich Brandt, Stefan Kerscher, Stefan Dröse, Klaus Zwicker dan Volker Zickermann. Diakses tanggal 2010-11-04.
- ^ Cecchini G (2003). "Function and structure of complex II of the respiratory chain". Annu Rev Biochem. 72: 77–109. doi:10.1146/annurev.biochem.72.121801.161700. PMID 14527321.
- ^ a b (Inggris) "Variation in proton donor/acceptor pathways in succinate:quinone oxidoreductases". Molecular Biology Division (151-S), VA Medical Center and Department of Biochemistry and Biophysics, University of California; Cecchini G, Maklashina E, Yankovskaya V, Iverson TM, Iwata S. Diarsipkan dari versi asli tanggal 2015-04-09. Diakses tanggal 2010-11-09.
- ^ (Inggris) "The quaternary structure of the Saccharomyces cerevisiae succinate dehydrogenase. Homology modeling, cofactor docking, and molecular dynamics simulation studies". Canadian Institutes of Health Membrane Protein Research Group, Department of Biochemistry, University of Alberta; Oyedotun KS, Lemire BD. Diarsipkan dari versi asli tanggal 2019-06-07. Diakses tanggal 2010-11-04.
- ^ (Inggris) "Succinate: quinone oxidoreductases: new insights from X-ray crystal structures". Max-Planck-Institut für Biophysik, Abteilung Molekulare Membranbiologie; Lancaster CR, Kröger A. Diarsipkan dari versi asli tanggal 2016-05-01. Diakses tanggal 2010-11-04.
- ^ Yankovskaya V., Horsefield R., Tornroth S., Luna-Chavez C., Miyoshi H., Leger C., Byrne B., Cecchini G., Iwata S. (2003) Architecture of succinate dehydrogenase and reactive oxygen species generation. Science 299, 700–704
- ^ Horsefield R, Iwata S, Byrne B (2004). "Complex II from a structural perspective". Curr. Protein Pept. Sci. 5 (2): 107–18. doi:10.2174/1389203043486847. PMID 15078221.
- ^ Kita K, Hirawake H, Miyadera H, Amino H, Takeo S (2002). "Role of complex II in anaerobic respiration of the parasite mitochondria from Ascaris suum and Plasmodium falciparum". Biochim. Biophys. Acta. 1553 (1–2): 123–39. doi:10.1016/S0005-2728(01)00237-7. PMID 11803022.
- ^ Painter HJ, Morrisey JM, Mather MW, Vaidya AB (2007). "Specific role of mitochondrial electron transport in blood-stage Plasmodium falciparum". Nature. 446 (7131): 88–91. doi:10.1038/nature05572. PMID 17330044.
- ^ a b Zhang J, Frerman FE, Kim JJ (2006). "Structure of electron transfer flavoprotein-ubiquinone oxidoreductase and electron transfer to the mitochondrial ubiquinone pool". Proc. Natl. Acad. Sci. U.S.A. 103 (44): 16212–7. doi:10.1073/pnas.0604567103. PMID 17050691.
- ^ (Inggris) "The electron transfer flavoprotein: Ubiquinone oxidoreductases". Centre for Molecular and Structural Biochemistry, School of Biological Sciences, University of East Anglia; Watmough NJ, Frerman FE. Diarsipkan dari versi asli tanggal 2015-01-25. Diakses tanggal 2010-11-11.
- ^ Ishizaki K, Larson TR, Schauer N, Fernie AR, Graham IA, Leaver CJ (2005). "The critical role of Arabidopsis electron-transfer flavoprotein:ubiquinone oxidoreductase during dark-induced starvation". Plant Cell. 17 (9): 2587–600. doi:10.1105/tpc.105.035162. PMC 1197437
 . PMID 16055629.
. PMID 16055629.
- ^ (Inggris) "Reactions of electron-transfer flavoprotein and electron-transfer flavoprotein: ubiquinone oxidoreductase". Department of Biochemistry and Biophysics, University of California, Molecular Biology Division, Veterans Administration Medical Center, Department of Chemical Pathology, University of Cape Town Medical School; Rona R. RAMSAY, Daniel J. STEENKAMP dan Mazhar HUSAIN. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-11-11.
- ^ Ikeda Y, Dabrowski C, Tanaka K (1983). "Separation and properties of five distinct acyl-CoA dehydrogenases from rat liver mitochondria. Identification of a new 2-methyl branched chain acyl-CoA dehydrogenase". J. Biol. Chem. 258 (2): 1066–76. PMID 6401712. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-05-19.
- ^ Ruzicka FJ, Beinert H (1977). "A new iron-sulfur flavoprotein of the respiratory chain. A component of the fatty acid beta oxidation pathway" (PDF). J. Biol. Chem. 252 (23): 8440–5. PMID 925004. Diarsipkan (PDF) dari versi asli tanggal 2007-09-27. Diakses tanggal 2009-05-19.
- ^ Berry E, Guergova-Kuras M, Huang L, Crofts A (2000). "Structure and function of cytochrome bc complexes". Annu Rev Biochem. 69: 1005–75. doi:10.1146/annurev.biochem.69.1.1005. PMID 10966481.
- ^ Crofts AR (2004). "The cytochrome bc1 complex: function in the context of structure". Annu. Rev. Physiol. 66: 689–733. doi:10.1146/annurev.physiol.66.032102.150251. PMID 14977419.
- ^ Iwata S, Lee JW, Okada K; et al. (1998). "Complete structure of the 11-subunit bovine mitochondrial cytochrome bc1 complex". Science. 281 (5373): 64–71. doi:10.1126/science.281.5373.64. PMID 9651245.
- ^ Trumpower BL (1990). "The protonmotive Q cycle. Energy transduction by coupling of proton translocation to electron transfer by the cytochrome bc1 complex" (PDF). J. Biol. Chem. 265 (20): 11409–12. PMID 2164001. Diarsipkan (PDF) dari versi asli tanggal 2007-09-27. Diakses tanggal 2009-05-19.
- ^ Hunte C, Palsdottir H, Trumpower BL (2003). "Protonmotive pathways and mechanisms in the cytochrome bc1 complex". FEBS Lett. 545 (1): 39–46. doi:10.1016/S0014-5793(03)00391-0. PMID 12788490.
- ^ Calhoun M, Thomas J, Gennis R (1994). "The cytochrome oxidase superfamily of redox-driven proton pumps". Trends Biochem Sci. 19 (8): 325–30. doi:10.1016/0968-0004(94)90071-X. PMID 7940677.
- ^ Tsukihara T, Aoyama H, Yamashita E, Tomizaki T, Yamaguchi H, Shinzawa-Itoh K, Nakashima R, Yaono R, Yoshikawa S. (1996). "The whole structure of the 13-subunit oxidized cytochrome c oxidase at 2.8 A". Science. 272 (5265): 1136–44. doi:10.1126/science.272.5265.1136. PMID 8638158.
- ^ a b (Inggris) "Electrostatic study of the proton pumping mechanism in bovine heart cytochrome C oxidase". Department of Chemistry, University of California-Davis; Popović DM, Stuchebrukhov AA. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Combined DFT and electrostatics study of the proton pumping mechanism in cytochrome c oxidase". Department of Chemistry, University of California; Quenneville J, Popović DM, Stuchebrukhov AA. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Proton transfer reactions associated with the reaction of the fully reduced, purified cytochrome C oxidase with molecular oxygen and ferricyanide". Department of Biomedical Science, Faculty of Medicine, University of Foggia; Capitanio N, Capitanio G, De Nitto E, Boffoli D, Papa S. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "pH dependence of proton translocation in the oxidative and reductive phases of the catalytic cycle of cytochrome c oxidase. The role of H2O produced at the oxygen-reduction site". Department of Medical Biochemistry, Biology and Physics, University of Bari; Capitanio G, Martino PL, Capitanio N, De Nitto E, Papa S. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Proton pumping mechanism and catalytic cycle of cytochrome c oxidase: Coulomb pump model with kinetic gating". Department of Chemistry, University of California; Popović DM, Stuchebrukhov AA. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Cooperative coupling and role of heme a in the proton pump of heme-copper oxidases". Institute of Medical Biochemistry and Chemistry, University of Bari; Papa S, Capitanio N, Villani G, Capitanio G, Bizzoca A, Palese LL, Carlino V, De Nitto E. Diarsipkan dari versi asli tanggal 2009-09-15. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Coupling of electron transfer with proton transfer at heme a and Cu(A) (redox Bohr effects) in cytochrome c oxidase. Studies with the carbon monoxide inhibited enzyme". Department of Medical Biochemistry and Biology, University of Bari; Capitanio N, Capitanio G, Minuto M, De Nitto E, Palese LL, Nicholls P, Papa S. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ (Inggris) "Vectorial nature of redox Bohr effects in bovine heart cytochrome c oxidase". Institute of Medical Biochemistry and Chemistry, University of Bari; Capitanio N, Capitanio G, De Nitto E, Papa S. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-07-22.
- ^ Yoshikawa S, Muramoto K, Shinzawa-Itoh K; et al. (2006). "Proton pumping mechanism of bovine heart cytochrome c oxidase". Biochim. Biophys. Acta. 1757 (9–10): 1110–6. doi:10.1016/j.bbabio.2006.06.004. PMID 16904626.
- ^ Rasmusson AG, Soole KL, Elthon TE (2004). "Alternative NAD(P)H dehydrogenases of plant mitochondria". Annual review of plant biology. 55: 23–39. doi:10.1146/annurev.arplant.55.031903.141720. PMID 15725055.
- ^ Menz RI, Day DA (1996). "Purification and characterization of a 43-kDa rotenone-insensitive NADH dehydrogenase from plant mitochondria". J. Biol. Chem. 271 (38): 23117–20. doi:10.1074/jbc.271.38.23117. PMID 8798503. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-05-23.
- ^ McDonald A, Vanlerberghe G (2004). "Branched mitochondrial electron transport in the Animalia: presence of alternative oxidase in several animal phyla". IUBMB Life. 56 (6): 333–41. doi:10.1080/1521-6540400000876. PMID 15370881.
- ^ Sluse FE, Jarmuszkiewicz W (1998). "Alternative oxidase in the branched mitochondrial respiratory network: an overview on structure, function, regulation, and role". Braz. J. Med. Biol. Res. 31 (6): 733–47. doi:10.1590/S0100-879X1998000600003. PMID 9698817.
- ^ Moore AL, Siedow JN (1991). "The regulation and nature of the cyanide-resistant alternative oxidase of plant mitochondria". Biochim. Biophys. Acta. 1059 (2): 121–40. doi:10.1016/S0005-2728(05)80197-5. PMID 1883834.
- ^ Vanlerberghe GC, McIntosh L (1997). "Alternative oxidase: From Gene to Function". Annual Review of Plant Physiology and Plant Molecular Biology. 48: 703–34. doi:10.1146/annurev.arplant.48.1.703. PMID 15012279.
- ^ Ito Y, Saisho D, Nakazono M, Tsutsumi N, Hirai A (1997). "Transcript levels of tandem-arranged alternative oxidase genes in rice are increased by low temperature". Gene. 203 (2): 121–9. doi:10.1016/S0378-1119(97)00502-7. PMID 9426242.
- ^ Maxwell DP, Wang Y, McIntosh L (1999). "The alternative oxidase lowers mitochondrial reactive oxygen production in plant cells". Proc. Natl. Acad. Sci. U.S.A. 96 (14): 8271–6. doi:10.1073/pnas.96.14.8271. PMID 10393984. Diarsipkan dari versi asli tanggal 2007-05-16. Diakses tanggal 2009-10-28.
- ^ Heinemeyer J, Braun HP, Boekema EJ, Kouril R (2007). "A structural model of the cytochrome C reductase/oxidase supercomplex from yeast mitochondria". J. Biol. Chem. 282 (16): 12240–8. doi:10.1074/jbc.M610545200. PMID 17322303.
- ^ Schägger H, Pfeiffer K (2000). "Supercomplexes in the respiratory chains of yeast and mammalian mitochondria". EMBO J. 19 (8): 1777–83. doi:10.1093/emboj/19.8.1777. PMC 302020
 . PMID 10775262.
. PMID 10775262.
- ^ Schägger H (2002). "Respiratory chain supercomplexes of mitochondria and bacteria". Biochim. Biophys. Acta. 1555 (1–3): 154–9. doi:10.1016/S0005-2728(02)00271-2. PMID 12206908.
- ^ Schägger H, Pfeiffer K (2001). "The ratio of oxidative phosphorylation complexes I-V in bovine heart mitochondria and the composition of respiratory chain supercomplexes". J. Biol. Chem. 276 (41): 37861–7. doi:10.1074/jbc.M106474200. PMID 11483615. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-10-28.
- ^ Gupte S, Wu ES, Hoechli L; et al. (1984). "Relationship between lateral diffusion, collision frequency, and electron transfer of mitochondrial inner membrane oxidation-reduction components". Proc. Natl. Acad. Sci. U.S.A. 81 (9): 2606–10. doi:10.1073/pnas.81.9.2606. PMC 345118
 . PMID 6326133.
. PMID 6326133.
- ^ Nealson KH (1999). "Post-Viking microbiology: new approaches, new data, new insights". Origins of life and evolution of the biosphere: the journal of the International Society for the Study of the Origin of Life. 29 (1): 73–93. doi:10.1023/A:1006515817767. PMID 11536899.
- ^ Schäfer G, Engelhard M, Müller V (1999). "Bioenergetics of the Archaea". Microbiol. Mol. Biol. Rev. 63 (3): 570–620. PMC 103747
 . PMID 10477309.
. PMID 10477309.
- ^ a b Ingledew WJ, Poole RK (1984). "The respiratory chains of Escherichia coli". Microbiol. Rev. 48 (3): 222–71. PMID 6387427.
- ^ a b Unden G, Bongaerts J (1997). "Alternative respiratory pathways of Escherichia coli: energetics and transcriptional regulation in response to electron acceptors". Biochim. Biophys. Acta. 1320 (3): 217–34. doi:10.1016/S0005-2728(97)00034-0. PMID 9230919.
- ^ Cecchini G, Schröder I, Gunsalus RP, Maklashina E (2002). "Succinate dehydrogenase and fumarate reductase from Escherichia coli". Biochim. Biophys. Acta. 1553 (1–2): 140–57. doi:10.1016/S0005-2728(01)00238-9. PMID 11803023.
- ^ Freitag A, Bock E (1990). "Energy conservation in Nitrobacter". FEMS Microbiology Letters. 66 (1–3): 157–62. doi:10.1111/j.1574-6968.1990.tb03989.x.
- ^ Starkenburg SR, Chain PS, Sayavedra-Soto LA; et al. (2006). "Genome sequence of the chemolithoautotrophic nitrite-oxidizing bacterium Nitrobacter winogradskyi Nb-255". Appl. Environ. Microbiol. 72 (3): 2050–63. doi:10.1128/AEM.72.3.2050-2063.2006. PMID 16517654. Diarsipkan dari versi asli tanggal 2007-10-13. Diakses tanggal 2009-10-28.
- ^ Yamanaka T, Fukumori Y (1988). "The nitrite oxidizing system of Nitrobacter winogradskyi". FEMS Microbiol. Rev. 4 (4): 259–70. PMID 2856189.
- ^ Iuchi S, Lin EC (1993). "Adaptation of Escherichia coli to redox environments by gene expression". Mol. Microbiol. 9 (1): 9–15. doi:10.1111/j.1365-2958.1993.tb01664.x. PMID 8412675.
- ^ Calhoun MW, Oden KL, Gennis RB, de Mattos MJ, Neijssel OM (1993). "Energetic efficiency of Escherichia coli: effects of mutations in components of the aerobic respiratory chain" (PDF). J. Bacteriol. 175 (10): 3020–5. PMID 8491720. Diarsipkan (PDF) dari versi asli tanggal 2007-09-27. Diakses tanggal 2009-10-28.
- ^ a b Boyer PD (1997). "The ATP synthase—a splendid molecular machine". Annu. Rev. Biochem. 66: 717–49. doi:10.1146/annurev.biochem.66.1.717. PMID 9242922.
- ^ Van Walraven HS, Strotmann H, Schwarz O, Rumberg B (1996). "The H+/ATP coupling ratio of the ATP synthase from thiol-modulated chloroplasts and two cyanobacterial strains is four". FEBS Lett. 379 (3): 309–13. doi:10.1016/0014-5793(95)01536-1. PMID 8603713.
- ^ Yoshida M, Muneyuki E, Hisabori T (2001). "ATP synthase—a marvellous rotary engine of the cell". Nat. Rev. Mol. Cell Biol. 2 (9): 669–77. doi:10.1038/35089509. PMID 11533724.
- ^ Schemidt RA, Qu J, Williams JR, Brusilow WS (1998). "Effects of carbon source on expression of F0 genes and on the stoichiometry of the c subunit in the F1F0 ATPase of Escherichia coli". J. Bacteriol. 180 (12): 3205–8. PMC 107823
 . PMID 9620972.
. PMID 9620972.
- ^ Rubinstein JL, Walker JE, Henderson R (2003). "Structure of the mitochondrial ATP synthase by electron cryomicroscopy". EMBO J. 22 (23): 6182–92. doi:10.1093/emboj/cdg608. PMC 291849
 . PMID 14633978.
. PMID 14633978.
- ^ Leslie AG, Walker JE (2000). "Structural model of F1-ATPase and the implications for rotary catalysis". Philos. Trans. R. Soc. Lond., B, Biol. Sci. 355 (1396): 465–71. doi:10.1098/rstb.2000.0588. PMC 1692760
 . PMID 10836500.
. PMID 10836500.
- ^ Noji H, Yoshida M (2001). "The rotary machine in the cell, ATP synthase". J. Biol. Chem. 276 (3): 1665–8. doi:10.1074/jbc.R000021200. PMID 11080505. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-10-28.
- ^ Capaldi R, Aggeler R (2002). "Mechanism of the F(1)F(0)-type ATP synthase, a biological rotary motor". Trends Biochem Sci. 27 (3): 154–60. doi:10.1016/S0968-0004(01)02051-5. PMID 11893513.
- ^ Gresser MJ, Myers JA, Boyer PD (1982). "Catalytic site cooperativity of beef heart mitochondrial F1 adenosine triphosphatase. Correlations of initial velocity, bound intermediate, and oxygen exchange measurements with an alternating three-site model". J. Biol. Chem. 257 (20): 12030–8. PMID 6214554. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-10-28.
- ^ Dimroth P (1994). "Bacterial sodium ion-coupled energetics". Antonie Van Leeuwenhoek. 65 (4): 381–95. doi:10.1007/BF00872221. PMID 7832594.
- ^ a b Becher B, Müller V (1994). "Delta mu Na+ drives the synthesis of ATP via a delta mu Na(+)-translocating F1F0-ATP synthase in membrane vesicles of the archaeon Methanosarcina mazei Gö1". J. Bacteriol. 176 (9): 2543–50. PMC 205391
 . PMID 8169202.
. PMID 8169202.
- ^ Müller V (2004). "An exceptional variability in the motor of archaeal A1A0 ATPases: from multimeric to monomeric rotors comprising 6–13 ion binding sites". J. Bioenerg. Biomembr. 36 (1): 115–25. doi:10.1023/B:JOBB.0000019603.68282.04. PMID 15168615.
- ^ a b Davies K (1995). "Oxidative stress: the paradox of aerobic life". Biochem Soc Symp. 61: 1–31. PMID 8660387.
- ^ Rattan SI (2006). "Theories of biological aging: genes, proteins, and free radicals". Free Radic. Res. 40 (12): 1230–8. doi:10.1080/10715760600911303. PMID 17090411.
- ^ Valko M, Leibfritz D, Moncol J, Cronin MT, Mazur M, Telser J (2007). "Free radicals and antioxidants in normal physiological functions and human disease". Int. J. Biochem. Cell Biol. 39 (1): 44–84. doi:10.1016/j.biocel.2006.07.001. PMID 16978905.
- ^ Raha S, Robinson B (2000). "Mitochondria, oxygen free radicals, disease and ageing". Trends Biochem Sci. 25 (10): 502–8. doi:10.1016/S0968-0004(00)01674-1. PMID 11050436.
- ^ Finkel T, Holbrook NJ (2000). "Oxidants, oxidative stress and the biology of ageing". Nature. 408 (6809): 239–47. doi:10.1038/35041687. PMID 11089981.
- ^ Kadenbach B, Ramzan R, Wen L, Vogt S (2009). "New extension of the Mitchell Theory for oxidative phosphorylation in mitochondria of living organisms". Biochim. Biophys. Acta. doi:10.1016/j.bbagen.2009.04.019. PMID 19409964.
- ^ Echtay KS, Roussel D, St-Pierre J; et al. (2002). "Superoxide activates mitochondrial uncoupling proteins". Nature. 415 (6867): 96–9. doi:10.1038/415096a. PMID 11780125.
- ^ (Inggris) "The Role of External and Matrix pH in Mitochondrial Reactive Oxygen Species Generation". Department of Biochemistry and Molecular Biology, Associated Unit to Consejo Superior de Investigaciones Científicas, Institute of Biomedicine of the University of Barcelona and Catalan Theoretical and Computational Chemistry Reference Network, Faculty of Biology, A. N. Belozersky Institute of Physico-Chemical Biology, Moscow State University, Department of Pediatrics, University of Pittsburgh School of Medicine and The Children's Hospital of Pittsburgh, Hospital Clínic-Ciberes, Institut d'Investigacions Biomedic August Pi i Sunyer (IDIBAPS), University of Barcelona,Diabetes Institute, Rangos Research Center University of Pittsburgh; Vitaly A. Selivanov, Jennifer A. Zeak, Josep Roca, Marta Cascante, Massimo Trucco, dan Tatyana V. Votyakova. Diarsipkan dari versi asli tanggal 2023-07-24. Diakses tanggal 2010-11-13.
- ^ a b Joshi S, Huang YG (1991). "ATP synthase complex from bovine heart mitochondria: the oligomycin sensitivity conferring protein is essential for dicyclohexyl carbodiimide-sensitive ATPase". Biochim. Biophys. Acta. 1067 (2): 255–8. doi:10.1016/0005-2736(91)90051-9. PMID 1831660.
- ^ Tsubaki M (1993). "Fourier-transform infrared study of cyanide binding to the Fea3-CuB binuclear site of bovine heart cytochrome c oxidase: implication of the redox-linked conformational change at the binuclear site". Biochemistry. 32 (1): 164–73. doi:10.1021/bi00052a022. PMID 8380331.
- ^ Heytler PG (1979). "Uncouplers of oxidative phosphorylation". Meth. Enzymol. 55: 462–42. doi:10.1016/0076-6879(79)55060-5. PMID 156853.
- ^ Lambert AJ, Brand MD (2004). "Inhibitors of the quinone-binding site allow rapid superoxide production from mitochondrial NADH: ubiquinone oxidoreductase (complex I)". J. Biol. Chem. 279 (38): 39414–20. doi:10.1074/jbc.M406576200. PMID 15262965. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2009-10-29.
- ^ Dervartanian DV, Veeger C. (1964). "Studies on succinate dehydrogenase. I. Spectral properties of the purified enzyme and formation of enzyme-competitive inhibitor complexes". Biochim. Biophys. Acta. 92: 233–47. PMID 14249115.
- ^ Ricquier D, Bouillaud F (2000). "The uncoupling protein homologues: UCP1, UCP2, UCP3, StUCP and AtUCP". Biochem. J. 345 Pt 2: 161–79. doi:10.1042/0264-6021:3450161. PMC 1220743
 . PMID 10620491.
. PMID 10620491.
- ^ Borecký J, Vercesi AE (2005). "Plant uncoupling mitochondrial protein and alternative oxidase: energy metabolism and stress". Biosci. Rep. 25 (3-4): 271–86. doi:10.1007/s10540-005-2889-2. PMID 16283557.
Bacaan lebih lanjut[sunting | sunting sumber]
Pengenalan
- Nelson DL (2004). Lehninger Principles of Biochemistry (edisi ke-4th). W. H. Freeman. ISBN 0-716-74339-6.
- Schneider ED (2006). Into the Cool: Energy Flow, Thermodynamics and Life (edisi ke-1st). University of Chicago Press. ISBN 0-226-73937-6.
- Lane N (2006). Power, Sex, Suicide: Mitochondria and the Meaning of Life (edisi ke-1st). Oxford University Press, USA. ISBN 0199205647.
Lanjutan
- Nicholls DG (2002). Bioenergetics 3 (edisi ke-1st). Academic Press. ISBN 0-125-18121-3.
- Haynie D (2001). Biological Thermodynamics (edisi ke-1st). Cambridge University Press. ISBN 0-521-79549-4.
- Rajan SS (2003). Introduction to Bioenergetics (edisi ke-1st). Anmol. ISBN 8-126-11364-2.
- Wikstrom M (Ed) (2005). Biophysical and Structural Aspects of Bioenergetics (edisi ke-1st). Royal Society of Chemistry. ISBN 0-854-04346-2.
Pranala luar[sunting | sunting sumber]
Informasi umum
- Animated diagrams illustrating oxidative phosphorylation Diarsipkan 2013-11-08 di Wayback Machine. Wiley and Co Concepts in Biochemistry
- Oxidative phosphorylation Diarsipkan 1999-10-12 di Wayback Machine. Metabolic Pathways of Biochemistry, the online reference of metabolism for students and teachers, at George Washington University
- ATP synthase - the rotary engine in the cell Diarsipkan 2010-10-25 di Wayback Machine. Brief introduction, including videos of microscope images of the enzyme rotating, at Tokyo Institute of Technology
- On-line biophysics lectures Diarsipkan 2009-05-02 di Wayback Machine. Antony Crofts, University of Illinois at Urbana-Champaign
Informasi struktural
- Animations of the ATP synthase Diarsipkan 2009-01-20 di Wayback Machine. Hongyun Wang and George Oster, University of California, Berkeley
- PDB molecule of the month:
- ATP synthase Diarsipkan 2020-07-24 di Wayback Machine.
- Cytochrome c Diarsipkan 2020-07-24 di Wayback Machine.
- Cytochrome c oxidase Diarsipkan 2020-07-24 di Wayback Machine.
- Interactive molecular models at Universidade Fernando Pessoa:
- NADH dehydrogenase Diarsipkan 2009-01-12 di Wayback Machine.
- succinate dehydrogenase Diarsipkan 2009-01-11 di Wayback Machine.
- Coenzyme Q - cytochrome c reductase Diarsipkan 2009-01-12 di Wayback Machine.
- cytochrome c oxidase Diarsipkan 2009-01-11 di Wayback Machine.



















