Pengantar tentang virus
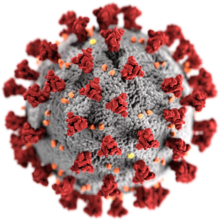
Virus adalah agen infeksi berukuran kecil yang bereproduksi di dalam sel inang yang hidup. Ketika terinfeksi, sel inang dipaksa untuk menghasilkan ribuan salinan identik virus asli dengan cepat. Virus sendiri tidak memiliki sel; pembentukan virus-virus baru berlangsung dalam sel inang yang terinfeksi. Walaupun demikian, virus memiliki materi genetik yang memungkinkannya untuk bermutasi dan berevolusi. Hingga tahun 2019, lebih dari 6.000 spesies virus telah dideskripsikan dengan baik,[1] dari total jutaan virus di lingkungan. Asal-usul virus belum jelas: beberapa di antaranya mungkin berevolusi dari plasmid (potongan DNA yang dapat berpindah di antara sel), sementara yang lain mungkin berevolusi dari bakteri.
Virus terdiri dari dua atau tiga bagian: materi genetik, kapsid (mantel protein), dan selubung. Semua virus memiliki materi genetik berupa DNA (asam deoksiribonukleat) atau RNA (asam ribonukleat) saja, yaitu molekul panjang dengan banyak gen (pemberi instruksi pada sel). Semua virus juga ditutupi dengan mantel protein untuk melindungi gen. Sebagian virus memiliki selubung atau amplop berupa lipid yang menutupi lapisan protein, sehingga golongan virus ini dapat dihancurkan oleh sabun. Selubung ini memiliki reseptor spesifik yang membantu virus memasuki sel inang baru. Bentuk virus bervariasi, mulai dari heliks (pilinan) sederhana, ikosahedral (bangun ruang bersisi 20), hingga struktur yang lebih kompleks. Ukuran virus berkisar dari 20 hingga 300 nanometer, yang berarti garis sepanjang 1 sentimeter dapat diisi 33.000 hingga 500.000 virus yang berbaris lurus.
Virus menyebar melalui berbagai cara. Meskipun demikian, virus bersifat sangat spesifik dalam menentukan spesies inang atau jaringan yang mereka serang dan masing-masing spesies virus bergantung pada metode khusus untuk memperbanyak diri. Banyak virus tumbuhan menyebar dari satu tumbuhan ke tumbuhan lain melalui serangga dan organisme lain, yang dikenal sebagai vektor. Virus pada manusia dan hewan disebarkan dengan cara yang bervariasi, mulai dari hubungan seks (misalnya virus imunodefisiensi manusia atau HIV), melalui makanan atau minuman yang terkontaminasi (misalnya Norovirus dan Rotavirus), hingga percikan dari saluran pernapasan dari individu yang terinfeksi (misalnya virus influenza, virus parainfluenza, dan virus korona). Sebagian virus lainnya, misalnya virus dengue, ditularkan melalui serangga pengisap darah. Berbagai virus dapat menginfeksi hewan dan manusia, misalnya HIV dan Ebolavirus. Penyakit yang dapat berpindah dari hewan ke manusia disebut zoonosis.
Infeksi virus dapat mengakibatkan penyakit pada manusia, hewan, dan tumbuhan. Pada manusia dan hewan yang sehat, infeksi biasanya dihilangkan oleh sistem imun, yang memberikan kekebalan seumur hidup kepada inang virus tersebut. Pemberian antibiotik tidak efektif terhadap virus, tetapi beberapa obat antivirus mampu mengobati infeksi yang mengancam jiwa. Pemberian vaksin dapat mencegah sejumlah infeksi virus dan menghasilkan kekebalan seumur hidup.
Virus dapat mengalami mutasi genetik. Virus RNA bermutasi lebih cepat dibandingkan virus DNA sehingga memunculkan tipe baru yang tidak dapat diatasi dengan cepat oleh sistem imun inang mereka. Virus influenza, misalnya, sering kali bermutasi sehingga diperlukan vaksin baru setiap tahun. Kemunculan galur baru yang belum pernah ditemui sebelumnya dapat mengakibatkan pandemi, seperti pandemi flu H1N1 pada tahun 2009 dan pandemi koronavirus pada tahun 2020.
Penemuan

Pada tahun 1884, ahli mikrobiologi Prancis Charles Chamberland menemukan filter Chamberland (atau filter Chamberland—Pasteur), yang memiliki pori-pori yang lebih kecil dari bakteri. Dengan demikian, ia bisa melewatkan larutan yang mengandung bakteri melalui saringan tersebut sehingga larutan benar-benar bebas dari bakteri. Pada awal 1890-an, ahli biologi Rusia Dmitri Ivanovsky menggunakan metode ini untuk mempelajari suatu zat yang kemudian dikenal sebagai virus mosaik tembakau. Eksperimennya menunjukkan bahwa ekstrak dari daun tanaman tembakau terinfeksi yang telah dihancurkan tetap menularkan penyakit setelah penyaringan.[2]
Pada saat yang sama, beberapa ilmuwan lain menunjukkan bahwa, meskipun agen ini (yang kemudian disebut virus) berbeda dengan bakteri dan berukuran sekitar seratus kali lebih kecil, mereka masih dapat menimbulkan penyakit. Pada tahun 1899, ahli mikrobiologi Belanda Martinus Beijerinck mengamati bahwa agen tersebut berkembang biak hanya dalam sel yang membelah. Ia menyebutnya "cairan hidup menular" (bahasa Latin: contagium vivum fluidum) atau "kuman hidup terlarut" karena ia tidak dapat menemukan partikel seperti kuman.[3] Pada awal abad ke-20, ahli bakteriologi Inggris Frederick Twort menemukan virus yang menginfeksi bakteri.[4] Ahli mikrobiologi Prancis-Kanada Félix d'Herelle juga menemukan bahwa penambahan virus ke dalam media agar yang ditumbuhi bakteri akan mematikan bakteri pada agar tersebut. Kematian bakteri ditandai oleh terbentuknya zona bening atau jernih pada agar, yang sebelumnya terlihat kusam akibat pertumbuhan bakteri. Penghitungan zona yang tidak ditumbuhi bakteri ini memungkinkan Félix untuk memperkirakan jumlah virus dalam suspensi tersebut.[5]
Penemuan mikroskop elektron pada tahun 1931 memunculkan gambar virus untuk pertama kalinya.[6] Pada tahun 1935, ahli biokimia dan virologi Amerika Serikat Wendell Meredith Stanley memeriksa virus mosaik tembakau dan menemukan bahwa virus tersebut sebagian besar terbuat dari protein.[7] Tidak lama kemudian, virus ini dipisahkan menjadi bagian protein dan RNA.[8] Masalah bagi para peneliti virus awal adalah mereka tidak tahu cara mengembangkan virus tanpa menggunakan hewan hidup. Sebuah terobosan terjadi pada tahun 1931, ketika ahli patologi Amerika Serikat Ernest William Goodpasture dan Alice Miles Woodruff menumbuhkan virus influenza dan beberapa virus lain pada telur ayam yang telah dibuahi.[9] Beberapa virus tidak dapat tumbuh dalam telur ayam, tetapi masalah ini terpecahkan pada tahun 1949 ketika John Franklin Enders, Thomas Huckle Weller, dan Frederick Chapman Robbins menumbuhkan virus polio dalam biakan sel hewan hidup.[10] Hingga tahun 2019, sebanyak 6.590 spesies virus telah dideskripsikan dengan baik.[1]
Sifat biologi
Status kehidupan
Ada perbedaan pendapat ilmiah tentang apakah virus digolongkan sebagai makhluk hidup atau sekadar struktur organik yang berinteraksi dengan makhluk hidup. Walaupun demikian, mereka lebih sering dianggap sebagai replikator (zat yang melakukan replikasi DNA) dan tidak termasuk bentuk kehidupan.[11] Virus digambarkan sebagai "organisme di ujung kehidupan",[12] karena mereka serupa dengan makhluk hidup dalam hal kepemilikan gen, berevolusi melalui seleksi alam,[13] dan bereproduksi dengan membuat banyak salinan dari diri mereka sendiri melalui perakitan diri. Meskipun virus memiliki gen, mereka tidak memiliki sel, yang sering dipandang sebagai unit dasar kehidupan. Virus tidak memiliki metabolisme sendiri dan membutuhkan sel inang untuk membuat produk baru. Oleh karena itu, mereka tidak dapat bereproduksi secara alami di luar sel inang.[14] Walaupun sejumlah bakteri seperti Rickettsia dan Chlamydia memiliki keterbatasan yang sama, mereka dianggap sebagai organisme hidup karena memiliki sel sendiri.[15][16] Perakitan diri virus di dalam sel inang berimplikasi pada studi asal mula kehidupan karena mendukung hipotesis bahwa kehidupan dapat dimulai dari molekul organik yang dapat merakit diri.[17]
Struktur

Partikel virus, disebut juga "virion", terdiri dari materi genetik yaitu DNA (asam deoksiribonukleat) atau RNA (asam ribonukleat) yang dikelilingi lapisan protein pelindung yang disebut kapsid.[18] Kapsid terbentuk dari susunan molekul-molekul protein kecil identik yang disebut kapsomer. Kapsomer-kapsomer ini dapat tersusun dalam struktur ikosahedron (bangun ruang bersisi 20), heliks (spiral atau pilinan), atau bentuk-bentuk lain yang lebih kompleks. Di dalam kapsid terdapat selubung nukleokapsid, yang juga terdiri dari protein. Sebagian virus dikelilingi bagian luar yang terdiri dari lipid (lemak) dan disebut selubung virus (amplop). Selubung luar ini menyebabkan virus tersebut dapat dihancurkan sabun atau alkohol.[19]
Ukuran
Virus adalah salah satu agen infeksi terkecil dan tidak dapat dilihat menggunakan mikroskop cahaya. Kebanyakan virus hanya dapat dilihat menggunakan mikroskop elektron. Ukuran virus berkisar antara 20 hingga 300 nanometer. Dengan kata lain, garis sepanjang 1 sentimeter dapat diisi 33.000 hingga 500.000 virus yang berbaris lurus.[18] Bakteri umumnya memiliki diameter 1.000 nanometer (1 mikrometer) dan sel makhluk hidup yang lebih besar biasanya berukuran puluhan mikrometer. Terdapat juga golongan virus yang berukuran relatif besar dibandingkan virus biasa, seperti Mimivirus, Megavirus, dan Pandoravirus. Virus-virus ini berukuran sekitar 1.000 nanometer, menginfeksi ameba, dan ditemukan pada 2003 hingga 2013.[20][21] Ukuran virus-virus ini sekitar sepuluh kali lebih panjang dari virus influenza (sehingga volumenya 1.000 kali lebih besar), sehingga disebut virus "raksasa" dan penemuannya mengejutkan para ilmuwan.[22]
Materi genetik
Gen virus terbuat dari DNA saja atau RNA saja. Gen menyimpan informasi biologis dari suatu organisme dalam bentuk kode. Sebagian besar organisme menggunakan DNA sebagai materi genetik, tetapi sejumlah virus menggunakan RNA (golongan ini disebut virus RNA). DNA atau RNA virus dapat berbentuk satu untaian saja atau berbentuk heliks ganda.[23]
Virus dapat berkembang biak dengan cepat karena jumlah gennya relatif sedikit. Virus influenza hanya memiliki delapan gen, sedangkan Rotavirus memiliki sebelas gen (sebagai perbandingan, manusia memiliki 20.000 hingga 25.000).[24] Gen-gen ini mengandung kode untuk menghasilkan protein, baik protein struktural yang membentuk tubuh virus itu sendiri, maupun protein nonstruktural yang hanya ditemukan dalam sel yang diinfeksi virus.[25]
Banyak virus yang mampu menghasilkan enzim, jenis protein yang mendorong terjadinya reaksi kimia. Beberapa enzim ini, disebut DNA polimerase dan RNA polimerase, berfungsi membuat salinan DNA atau RNA. Enzim polimerase sebuah virus sering lebih efisien dalam menyalin DNA atau RNA dibandingkan enzim serupa yang dimiliki sel inangnya,[26] tetapi RNA polimerase dari virus lebih rentan mengalami kesalahan penyalinan. Hal ini menyebabkan virus RNA mudah bermutasi dan menghasilkan jenis-jenis (atau galur) baru.[27]
Beberapa virus RNA memiliki gen yang tidak menyatu dalam satu molekul RNA tunggal. Misalnya, virus influenza memiliki delapan gen terpisah yang masih-masing berupa molekul RNA tersendiri. Saat beberapa galur dari virus influenza menginfeksi sel yang sama, gen-gen ini dapat bercampur dan membentuk galur baru dalam sebuah proses yang disebut pemilahan ulang (reassortment).[28]
Sintesis protein

Protein merupakan molekul yang mutlak diperlukan untuk kelangsungan hidup. Sebuah sel membuat protein dengan merangkai asam amino sesuai informasi yang ada dalam DNA. Sintesis (pembuatan) protein membutuhkan berbagai proses yang tidak dimiliki oleh virus.[29] Karena itu, virus memaksa sel inangnya untuk membuat protein-protein yang tidak dibutuhkan sel inang tetapi diperlukan oleh virus untuk memperbanyak diri.[30]
Dalam sebuah sel, sintesis protein terdiri dari dua tahap utama: transkripsi (penyalinan) dan translasi (penerjemahan).[31] Dalam transkripsi, informasi yang dikandung DNA (disebut kode genetik) digunakan untuk membuat salinan berupa RNA yang disebut RNA duta (disebut mRNA dari messenger-RNA). Molekul mRNA ini berpindah menuju ribosom sel, tempat protein dibuat berdasarkan informasi yang ada dalam mRNA. Tahap ini disebut translasi atau penerjemahan karena informasi mRNA yang formatnya adalah susunan asam nukleat diubah menjadi protein yang merupakan susunan asam amino, seolah dari suatu bahasa ke bahasa lain.[31]
Virus "membajak" proses dalam sel ini dengan berbagai cara. Sebagian virus RNA bekerja dengan menggunakan RNA-nya secara langsung sebagai mRNA sel. Golongan virus seperti ini disebut virus RNA untai-positif atau untai-plus.[32] Sebaliknya, dalam golongan virus RNA lainnya, RNA virus harus diubah menjadi komplemennya terlebih dahulu agar berfungsi sebagai mRNA, sehingga harus dilakukan penyalinan komplemen menggunakan enzim milik sel inang atau milik virus itu sendiri. Golongan virus ini disebut virus RNA untai-negatif atau untai-minus. Sebagian virus lainnya memiliki DNA, bukan RNA; golongan virus ini membuat mRNA dari DNA dengan proses yang sama seperti proses sebuah sel. Ada golongan virus lain, yaitu retrovirus, yang menggunakan mekanisme berbeda: golongan virus ini memiliki RNA, tetapi pembuatan salinan DNA dalam sel inang (yang berasal dari RNA virus) dilakukan dengan bantuan enzim transkriptase balik. Salinan DNA ini kemudian disisipkan ke dalam DNA sel inang dan akan diubah menjadi mRNA dan protein sebagaimana proses normal dalam sel.[33]
Inaktivasi
Karena virus tidak digolongkan sebagai organisme hidup, mereka tidak dapat "dibunuh". Tindakan untuk menonaktifkan virus sehingga ia tidak lagi menjadi infeksius disebut inaktivasi virus. Berbagai virus memiliki lapisan lipid dan protein yang dapat dinonaktifkan oleh perubahan kimiawi. Inaktivasi virus merupakan hal penting dalam pemrosesan plasma darah untuk memastikan bahwa darah yang ditangani tidak mengandung virus-virus berbahaya.[34] Metode yang biasa digunakan yaitu inaktivasi oleh pelarut atau detergen, pemanasan, serta inaktivasi oleh pH asam.[35]
Campuran pelarut organik/detergen mampu merusak lapisan lipid yang dimiliki oleh virus berselubung. Metode ini mudah diterapkan, tetapi tidak efektif terhadap virus yang tidak memiliki selubung.[36] Konsentrasi reagen dan durasi kontak dengan virus merupakan hal yang perlu diperhatikan. Pemanasan dilakukan untuk mendenaturasi protein virus. Pasteurisasi, panas kering, dan panas uap merupakan metode pemanasan yang dapat dilakukan.[36] Pasteurisasi mampu menonaktifkan virus berselubung maupun tak berselubung dengan berbagai karakteristik fisikokimia.[37] Pengaturan temperatur, durasi pemanasan, penentuan jenis protein yang akan dirusak dan dilindungi, serta penambahan bahan kimia lainnya perlu divalidasi agar metode ini mencapai tujuannya. Sebagian besar protein juga dirusak oleh pH asam. Perlakuan pH rendah ini efektif untuk virus berselubung dan memiliki efektivitas terbatas terhadap virus yang tidak berselubung.[36]
Beberapa metode lain yang dikembangkan untuk menonaktifkan virus di antaranya iradiasi dengan sinar ultraviolet, sinar gama, serta pemberian iodin.[38] Iradiasi dengan sinar gama dan pemberian iodin mampu menonaktifkan virus berselubung dan virus tak berselubung.[39][40] Iradiasi sinar ultraviolet juga mampu menonaktifkan kedua jenis virus tersebut, meskipun diperlukan dosis yang lebih besar untuk menonaktifkan virus tak berselubung.[41]
Siklus
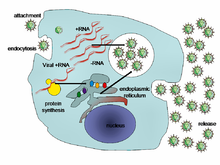

Saat sebuah virus menginfeksi sel, virus tersebut mengendalikan sel inangnya untuk memperbanyak virus itu, dengan membuat sel inang menyalin DNA atau RNA virus dan membuat protein yang kemudian bergabung untuk membentuk partikel virus baru.[42]
Pada dasarnya, ada enam tahap siklus virus dalam sel makhluk hidup:[25]
- Adsorpsi atau perlekatan, yaitu mengikatnya virus ke molekul tertentu pada permukaan sel. Setiap virus hanya bisa terikat pada molekul yang sesuai. Alhasil, virus hanya bisa menginfeksi jenis sel yang sangat terbatas. Fenomena ini disebut tropisme, dan kadang virus juga memiliki tropisme spesies yaitu hanya menginfeksi sel dari spesies atau golongan spesies tertentu. Misalnya, virus HIV hanya bisa menginfeksi sel T manusia, karena protein di permukaan virus ini, gp120, hanya bisa bereaksi dengan molekul CD4 dengan adanya koreseptor tertentu di permukaan sel T.[43]
- Penetrasi, yang terjadi setelah terbentuk ikatan dalam tahap adsorpsi. Virus memasuki sel inang melalui endositosis atau fusi dengan sel tersebut.[44]
- Pembukaan atau pembongkaran, yaitu saat kapsid yang melindungi virus terbuka dan dihancurkan oleh enzim virus atau enzim sel inang, sehingga materi genetik yang dimiliki virus dapat memasuki sel.[45]
- Replikasi, yaitu ketika sel inang menyintesis protein-protein yang dibutuhkan virus dan memperbanyak DNA atau RNA virus. Hal ini terjadi karena virus telah mengendalikan kemampuan sel untuk membuat protein dan memperbanyak materi genetik.[25]
- Perakitan, yaitu ketika protein-protein dan DNA atau RNA yang terbentuk di tahap sebelumnya menyusun diri membentuk ratusan partikel-partikel virus baru.[46]
- Pelepasan, yaitu keluarnya virus-virus baru dari sel inangnya. Hal ini dicapai sebagian besar virus dengan cara memecahkan sel inang dalam proses yang disebut lisis (sehingga tahap ini juga disebut tahap lisis). Virus lain seperti HIV keluar dengan cara yang lebih halus yang disebut "pertunasan" (budding) yang tidak langsung menghancurkan sel inang.[47]
Berdasarkan penghancuran sel inangnya, siklus virus dibagi menjadi siklus litik dan siklus lisogenik. Siklus litik akan langsung menghancurkan sel inang yang terinfeksi. Enam tahap siklus virus yang dimulai dari perlekatan hingga lisis merupakan tahapan penuh dari siklus litik. Sementara itu, siklus lisogenik dicirikan oleh infeksi yang "diam". Setelah masuk ke dalam sel inang, DNA virus akan bergabung ke dalam DNA sel inang, dan secara pasif ikut mengalami replikasi saat sel inang membelah diri.[48] Genom virus yang bergabung dengan DNA inang disebut provirus. Ketika terjadi perubahan kondisi yang mengganggu hubungan antara virus dan sel inang, provirus dapat menjadi aktif dan memulai siklus litik yang menghancurkan sel inang.[49]
Efek terhadap sel inang
Virus menimbulkan banyak efek dan perubahan pada struktur dan biokimia sel inang,[50] yang disebut efek sitopatik.[51] Sebagian besar infeksi virus berakhir dengan kematian sel inang. Sel inang mati dengan berbagai cara, di antaranya dengan pecah (mengalami lisis), mengalami perubahan membran sel, dan apoptosis (bunuh diri atau kematian sel terprogram).[52] Sering kali sel mati karena aktivitas normalnya terhenti akibat protein-protein yang dihasilkan virus, termasuk protein yang bukan bagian dari partikel virus itu sendiri.[53]
Sebagian virus tidak mengakibatkan perubahan yang terlihat pada sel inang. Virus yang laten (tidak aktif) tidak banyak menunjukkan tanda infeksi dan sel inangnya sering berfungsi normal.[54] Hal ini merupakan manifestasi dari siklus lisogenik yang menyebabkan virus tersebut dapat tersembunyi selama bertahun-tahun. Golongan virus herpes sering mengalami hal ini, contohnya virus herpes simpleks yang berdiam di sistem saraf inangnya tanpa menggandakan diri, dan sewaktu-waktu dapat aktif kembali.[55][56]
Sebagian virus, seperti Papilomavirus, dapat menyebabkan sel memperbanyak diri tak terkendali dan menjadi penyebab kanker.[57] Sebagian virus lainnya seperti virus Epstein-Barr juga membuat sel memperbanyak diri dengan berbagai manifestasi, terkadang berupa tumor jinak dan kadang tumor ganas (kanker).[58] Saat DNA sel terlalu rusak akibat serangan virus sehingga tidak dapat diperbaiki lagi, apoptosis sering terjadi. Salah satu akibatnya adalah penghancuran DNA oleh sel itu sendiri. Beberapa virus (seperti HIV) memiliki mekanisme untuk membatasi apoptosis sehingga sel inang tidak mati sebelum virus berhasil memperbanyak diri.[59]
Virus dan penyakit

Infeksi virus pada sel inang dapat menimbulkan penyakit yang dikategorikan sebagai penyakit infeksi. Penyebaran virus dari satu inang ke inang lain bisa dilakukan dengan banyak cara, tetapi setiap virus memiliki karakteristik tertentu dan mengandalkan cara tertentu untuk menyebar. Banyak virus yang menginfeksi tumbuhan berpindah dari satu tumbuhan ke tumbuhan lain melalui serangga dan organisme lain yang disebut vektor.[60] Virus yang menginfeksi hewan dan manusia menyebar dengan berbagai cara. Beberapa virus berpindah melalui kontak langsung antara individu terinfeksi dengan individu sehat, misalnya herpes simpleks yang menular melalui sentuhan fisik.[61] Penularan virus melalui kontak langsung juga dapat terjadi melalui hubungan seks, misalnya HIV.[62] Virus yang menginfeksi saluran pencernaan, seperti Norovirus dan Rotavirus, ditularkan melalui transmisi fekal–oral, yang melibatkan tangan, makanan, dan minuman yang terkontaminasi.[63][64] Virus-virus yang menyerang sistem pernapasan, seperti virus influenza, virus parainfluenza, dan virus korona, dapat menyebar melalui percikan dari saluran pernapasan saat seseorang berbicara, batuk, atau bersin.[65][66][67] Apabila partikel virus dalam percikan tersebut berhasil menyentuh membran mukosa orang lain (yang ada di hidung, mulut, dan beberapa organ lain), mereka dapat masuk ke dalam tubuh individu tersebut. Virus lainnya, seperti virus dengue, disebarkan oleh serangga pengisap darah.[68] Sementara itu, Cytomegalovirus bisa diturunkan secara vertikal dari ibu hamil ke janin yang sedang dikandungnya.[69]
Berbagai virus dapat menginfeksi hewan dan manusia, misalnya virus rabies, HIV, dan virus ebola.[70] Hal ini memungkinkan penyebaran penyakit dari hewan ke manusia maupun sebaliknya. Penyakit yang secara alami dapat berpindah dari hewan vertebrata ke manusia disebut zoonosis.[71] Rabies merupakan zoonosis akibat virus yang sangat mematikan. Penderita yang telah menunjukkan tanda klinis rabies hampir selalu berakhir dengan kematian.[72] Meskipun demikian, rabies bisa dicegah dan dieliminasi dari suatu daerah dengan vaksinasi. Untuk mencegah infeksi dan penyebaran penyakit, perlu diketahui cara penyebaran masing-masing jenis virus.[73]
Pada manusia
Penyakit-penyakit umum pada manusia yang diakibatkan oleh virus di antaranya pilek, influenza, cacar air, dan herpes oral. Penyakit-penyakit serius seperti Ebola dan AIDS pun disebabkan oleh infeksi virus.[74] Virus-virus yang tidak menimbulkan penyakit atau hanya menyebabkan penyakit ringan dianggap sebagai virus "jinak". Sementara itu, virus yang lebih ganas dan berbahaya disebut bersifat virulen.[75] Beberapa virus malah bisa menimbulkan infeksi sepanjang hayat atau kronis apabila virus tersebut terus saja menggandakan diri di dalam tubuh meskipun ada mekanisme pertahanan diri inang.[76] Hal ini umum terjadi pada infeksi virus hepatitis B dan hepatitis C. Orang yang terjangkit suatu virus secara kronis dinamakan pembawa virus. Mereka berperan sebagai reservoir virus tersebut.[77][78]
Endemi
Jika proporsi pembawa penyakit dalam populasi tertentu mencapai ambang tertentu, suatu penyakit dikatakan endemik.[79] Sebelum munculnya vaksinasi, infeksi virus merupakan hal biasa dan wabah terjadi secara reguler. Di negara dengan iklim sedang, penyakit akibat virus biasanya terjadi secara musiman. Poliomielitis akibat virus polio sering terjadi pada bulan-bulan musim panas.[80] Sebaliknya, infeksi virus influenza dan Rotavirus biasanya terjadi selama musim dingin.[81][82] Virus lain, seperti virus campak, menyebabkan wabah secara rutin setiap tiga tahun.[83] Di negara berkembang, virus yang mengakibatkan infeksi pernapasan dan pencernaan sering ditemui sepanjang tahun. Virus yang dibawa oleh serangga merupakan penyebab umum penyakit di negara ini. Sebagai contoh, virus zika dan virus dengue ditularkan oleh nyamuk Aedes betina yang menggigit manusia, khususnya selama musim kawin nyamuk.[84]
Kemunculan penyakit baru dan pandemi

Selain mutasi patogen, perubahan perilaku manusia akibat industrialisasi (yang memicu perubahan iklim dan resistansi obat) serta globalisasi (yang mengubah demografi dan meningkatkan perdagangan internasional), turut berkontribusi memunculkan penyakit infeksi baru.[85] Penyakit-penyakit baru ini dapat menyebar secara lokal maupun global (pandemi).[86]
Meskipun pandemi virus jarang terjadi, HIV (yang berevolusi dari virus yang ditemukan pada monyet dan simpanse) telah menjadi pandemi setidaknya sejak tahun 1980-an.[87] Sepanjang abad ke-20, ada empat pandemi yang diakibatkan oleh virus influenza, yang masing-masing dimulai pada tahun 1918, 1957, 1968, dan 2009. Sebelum diberantas, variola merupakan penyebab pandemi selama lebih dari 3.000 tahun.[88] Sepanjang sejarah, perpindahan manusia membantu penyebaran infeksi pandemik; awalnya melalui perjalanan laut dan pada zaman modern juga melalui perjalanan udara.[89]
Selain variola, sebagian besar pandemi diakibatkan oleh virus yang baru berevolusi. Virus yang baru muncul ini biasanya merupakan mutan dari virus yang kurang berbahaya yang telah beredar sebelumnya, baik pada manusia maupun pada hewan lain.[90]
Koronavirus merupakan kelompok virus yang telah beberapa kali memunculkan penyakit infeksi baru. Sindrom pernapasan akut berat (SARS) dan sindrom pernapasan Timur Tengah (MERS), yang masing-masing muncul pada tahun 2002 dan 2012, diakibatkan oleh koronavirus tipe baru. Koronavirus lain diketahui mengakibatkan infeksi ringan pada manusia,[91] sehingga virulensi dan penyebaran SARS yang cepat (yang pada Juli 2003 telah mengakibatkan sekitar 8.000 kasus dan 800 kematian) tidak terduga dan sebagian besar negara tidak siap.[92]
Koronavirus baru juga muncul di Wuhan, Tiongkok pada November 2019 dan menyebar dengan cepat ke seluruh dunia. Virus yang baru muncul ini kemudian diberi nama koronavirus sindrom pernapasan akut berat 2 (SARS-CoV-2). Virus ini memiliki tingkat kemiripan tinggi dengan koronavirus pada kelelawar dan tenggiling,[93][94][95] sehingga timbul dugaan bahwa SARS-CoV-2 berasal dari hewan-hewan tersebut. Infeksi virus ini mengakibatkan penyakit koronavirus 2019 (COVID-19), yang memiliki tingkat keparahan bervariasi, mulai dari ringan hingga mematikan,[96] dan mengakibatkan pandemi pada tahun 2020.[97][98][99] Akibat pandemi ini, berbagai negara mengambil kebijakan yang mengubah keseharian hidup penduduknya, seperti karantina wilayah,[100] perintah untuk tinggal di rumah, dan pembatasan perjalanan internasional.[101]
Pada tumbuhan

Ada banyak jenis virus tumbuhan, tetapi sering kali mereka hanya mengakibatkan penurunan hasil produksi, dan secara ekonomis tidak efisien untuk melakukan pengendaliannya. Virus tumbuhan sering menyebar dari satu tumbuhan ke tumbuhan lain oleh organisme yang disebut vektor. Vektor biasanya berupa serangga, tetapi beberapa jamur, cacing nematoda, dan organisme bersel tunggal juga terbukti berperan sebagai vektor. Pengendalian infeksi virus tumbuhan, misalnya dengan membunuh vektor dan menghilangkan inang alternatif seperti gulma, akan dilakukan jika upaya tersebut membawa keuntungan ekonomis (contohnya pada perkebunan buah-buahan menahun).[102] Virus tumbuhan tidak berbahaya bagi manusia dan hewan lain karena mereka hanya dapat bereproduksi dalam sel tumbuhan hidup.[103]
Bakteriofag

Bakteriofag adalah virus yang menginfeksi bakteri dan arkea. Komite Internasional Taksonomi Virus (ICTV) secara resmi mengakui 28 genus bakteriofag yang ditempatkan dalam 11 keluarga virus.[104] Bakteriofag berperan penting dalam ekosistem laut: ketika bakteri yang terinfeksi meledak, senyawa karbon dilepaskan kembali ke lingkungan, dan senyawa tersebut kemudian merangsang pertumbuhan organik segar. Bakteriofag berguna dalam penelitian ilmiah karena mereka tidak berbahaya bagi manusia dan dapat dipelajari dengan mudah. Di sisi lain, bakteriofag dapat menjadi sumber masalah pada industri makanan dan obat-obatan yang melibatkan fermentasi dan bergantung pada bakteri bermanfaat. Beberapa infeksi bakteri menjadi sulit dikendalikan dengan antibiotik sehingga ada kecenderungan untuk memanfaatkan bakteriofag sebagai terapi infeksi bakterial pada manusia.[105]
Imunitas
Imunitas bawaan pada hewan
Hewan, termasuk manusia, memiliki banyak pertahanan alami melawan virus. Sebagian pertahanan ini bersifat umum dan melindungi dari banyak virus tanpa tergantung jenisnya. Sistem imun bawaan ini tidak bertambah kuat jika infeksi berulang, dan tidak memiliki "memori" akan infeksi sebelumnya. Contohnya adalah kulit hewan (terutama permukaan luarnya yang memiliki lapisan sel-sel mati) yang mencegah masuknya virus ke tubuh inang. Contoh lain adalah keasaman isi lambung yang dapat menghancurkan virus-virus yang tertelan. Saat virus berhasil melewati rintangan-rintangan ini dan berhasil masuk tubuh inang, pertahanan bawaan lainnya mencegah penyebaran infeksi di dalam tubuh. Hormon yang bernama interferon diproduksi tubuh ketika virus masuk, dan mencegah virus memperbanyak diri dengan cara membunuh sel-sel yang terinfeksi beserta sel-sel terdekatnya. Di dalam sel, ada enzim-enzim yang berfungsi merusak RNA virus, disebut enzim interferensi RNA. Beberapa sel darah memakan dan menghancurkan sel-sel yang terinfeksi virus.[106]
Imunitas adaptif pada hewan
Pertahanan yang bersifat spesifik terhadap virus tertentu berkembang dari waktu ke waktu. Sel-sel darah putih jenis limfosit menjadi komponen penting, dengan menyimpan "memori" infeksi virus dan membuat molekul-molekul khusus yang disebut antibodi. Molekul-molekul antibodi menempel pada virus dan mencegahnya menginfeksi sel. Antibodi bersifat selektif dan masing-masing hanya menyerang satu jenis virus. Tubuh hewan dan manusia membuat berbagai antibodi, terutama saat awal infeksi. Setelah infeksi virus mereda, sebagian antibodi tetap bertahan dan terus dibuat, sehingga biasanya memberi ketahanan seumur hidup untuk virus jenis tersebut.[107]
Pertahanan tumbuhan
Tumbuhan juga memiliki mekanisme pertahanan melawan virus. Salah satu pertahanan terkuat adalah adanya "gen pertahanan" (gen R, resistance). Setiap gen R memberikan pertahanan melawan virus tertentu dengan memicu kematian sel terlokalisasi di sekitar sel-sel yang terinfeksi. Area terlokalisasi ini sering dapat dilihat mata sebagai bintik-bintik besar. Hal ini mencegah penyebaran infeksi.[108] Tumbuhan juga memiliki enzim interferensi RNA[109] dan menghasilkan disinfektan alami yang menghancurkan virus, seperti asam salisilat, nitrogen monoksida, dan spesi oksigen reaktif.[110]
Pertahanan terhadap bakteriofag
Bakteri dan arkea memiliki alat pertahanan untuk melindungi sel mereka dari serangan bakteriofag. Sistem imun bakteri, baik imunitas bawaan maupun adaptif, telah berkali-kali mengalami evolusi untuk mengatasi serangan ini.[111] Pertahanan dilakukan oleh segmen DNA bakteri dan arkea yang disebut CRISPR yang mendeteksi DNA bakteriofag, serta protein terasosiasi-CRISPR (Cas), seperti Cas9, yang memotong DNA bakteriofag.[112] Selain sistem CRISPR/Cas, pemotongan DNA virus juga dilakukan oleh enzim restriksi.[113] Sebagai respons terhadap sistem pertahanan ini, virus juga mengembangkan protein yang disebut anti-CRISPR untuk melindungi DNA mereka dari pemotongan. Persaingan antara virus dan bakteri/arkea untuk memenangkan kompetisi ini dapat diibaratkan sebagai "perlombaan senjata".[111]
Pencegahan dan pengobatan
Vaksinasi
Vaksin bekerja dengan cara meniru infeksi alami dalam memicu respons sistem imun adaptif, tetapi tidak mengakibatkan penyakit. Vaksin dapat dibuat dari virus yang telah dilemahkan atau virus yang telah dinonaktifkan. Penggunaan vaksinasi telah berhasil memusnahkan penyakit variola dari muka bumi serta mengurangi penyakit dan kematian akibat infeksi virus lain seperti polio, campak, beguk, dan rubela.[114] Vaksin telah tersedia untuk mencegah lebih dari 14 jenis infeksi virus pada manusia,[115] dan vaksin lain telah dibuat untuk mencegah infeksi virus pada hewan.[116] Virus-virus yang bermutasi dengan cepat, contohnya virus influenza, membutuhkan vaksin baru untuk setiap galur yang baru terbentuk. Organisasi Kesehatan Dunia (WHO) merekomendasikan pemberian vaksin influenza setiap tahun bagi orang-orang yang berisiko tinggi menderita penyakit ini.[117] Sementara itu, vaksin yang berisi virus yang dilemahkan bisa berbahaya untuk orang-orang dengan sistem imun yang lemah, karena malah bisa menyebabkan penyakit yang ingin dicegah.[118] Teknik-teknik bioteknologi dan rekayasa genetika digunakan untuk menghasilkan vaksin yang hanya memiliki protein kapsid dari virus sehingga lebih aman karena tidak mungkin menyebabkan munculnya penyakit. Vaksin hepatitis B adalah salah satu contoh vaksin jenis ini.[119][120]
Obat antivirus

Obat-obatan antivirus berfungsi dengan mengganggu proses yang diperlukan untuk penggandaan virus dan idealnya tidak menimbulkan efek negatif terhadap organisme inang. Obat seperti ini sangat sulit dicari karena penggandaan virus sangat mengandalkan fungsi normal sel inangnya, dan fungsi-fungsi tersebut tidak dapat dihentikan tanpa dampak negatif untuk sel inang.[121] Obat antivirus pertama ditemukan pada 1962,[122] dan pengembangan golongan obat ini mulai meningkat dengan cepat sejak pertengahan 1980-an setelah terjadi pandemi AIDS. Obat-obatan ini sering menggunakan sifat analog nukleosida, yang bertindak sebagai tiruan palsu dari nukleosida (molekul pembentuk DNA). Saat proses penggandaan DNA virus dimulai, sebagian bahan-bahan palsu ini ikut terpakai. Hal ini menggagalkan penggandaan karena obat tersebut dirancang untuk tidak memiliki sifat-sifat yang diperlukan dalam pembentukan rantai DNA. Saat produksi DNA berhenti, virus tidak lagi dapat memperbanyak diri.[123] Contoh jenis obat seperti ini adalah asiklovir (obat virus herpes), salah satu obat antivirus paling awal dan paling banyak digunakan dalam resep.[124] Contoh lain golongan obat ini adalah lamivudin (obat HIV dan hepatitis B),[124] dan ribavirin (obat hepatitis C).[125] Obat hepatitis B dan C tersebut menghentikan penggandaan virus dan interferon membunuh sel-sel terinfeksi yang masih tersisa.[126]
Selain itu, terdapat obat antivirus yang mengganggu tahap lain dalam siklus virus. Misalnya, HIV bergantung pada enzim HIV-1 protease untuk menjadi infeksius. Jenis obat yang disebut inhibitor protease bekerja dengan cara berikatan dengan enzim ini untuk menghentikan fungsinya.[127]
Infeksi HIV biasanya diobati dengan kombinasi berbagai obat antivirus, yang masing-masing mengganggu tahap-tahap yang berbeda dalam siklus virus. Ada obat yang mencegah adsorpsi (melengketnya) virus ke sel, ada obat analog nukleosida yang mencegah replikasi (penggandaan), dan ada obat yang menghentikan kerja enzim yang dibutuhkan dalam replikasi. Kesuksesan obat-obatan ini merupakan hasil dari pengetahuan tentang cara virus memperbanyak diri.[128] Satu obat antivirus tidak mampu sepenuhnya mengendalikan suatu infeksi virus, karena virus selalu bermutasi sehingga akan muncul variasi yang tahan terhadap obat yang telah ada. Selain itu, sebagian infeksi virus membutuhkan pengobatan bertahun-tahun.[129] Ilmuwan terus meneliti dan mengembangkan obat-obatan antivirus baru untuk mengatasi ketahanan virus, serta untuk menangani virus-virus baru, virus-virus yang belum ada obatnya, dan kemungkinan pandemi global.[130]
Asal-usul
Virus selalu berdampingan dengan organisme, dan mungkin telah ada sejak sel hidup pertama kali berevolusi. Virus tidak meninggalkan fosil, sehingga asal muasal virus hanya bisa dihipotesiskan dengan cara-cara seperti teknik-teknik biologi molekuler. Teknik-teknik ini mengandalkan keberadaan DNA atau RNA virus yang terdahulu. Akan tetapi, sebagian besar virus yang diawetkan dan disimpan di laboratorium berusia kurang dari 90 tahun.[131][132] Metode-metode biologi molekuler hanya berhasil melacak nenek moyang virus yang berevolusi pada abad ke-20.[133] Golongan virus baru berkali-kali muncul dalam berbagai tahap evolusi makhluk hidup.[134] Ada tiga hipotesis utama tentang asal-usul virus: hipotesis regresi, hipotesis keluar dari sel, dan hipotesis koevolusi.[134][135]
- Hipotesis regresi
- Menurut hipotesis ini, virus bisa jadi dulunya adalah sel-sel kecil yang menjadi parasit dalam sel yang lebih besar. Kemudian, parasit-parasit ini kehilangan gen-gen yang tidak lagi dibutuhkan setelah hidup sebagai parasit. Dengan demikian, sel-sel tersebut mengalami regresi menjadi virus. Hipotesis ini didukung oleh keberadaan bakteri seperti Rickettsia dan Chlamydia yang hanya mampu bereproduksi di dalam sel inang (seperti halnya virus). Menurut hipotesis regresi, jika sel-sel seperti ini bisa mengandalkan hidup sebagai parasit, gen-gen lain yang hanya diperlukan untuk hidup mandiri dapat hilang.[136]
- Hipotesis keluar dari sel
- Menurut hipotesis ini, virus berevolusi dari potongan DNA atau RNA yang keluar dari gen-gen organisme yang lebih besar. DNA yang keluar ini dapat berasal dari plasmid (potongan-potongan DNA yang dapat berpindah dari satu sel ke sel lain) dan juga dari bakteri.[137]
- Hipotesis koevolusi
- Menurut hipotesis ini, virus tidak berasal dari sel dan berevolusi dari molekul-molekul kompleks protein dan DNA pada saat yang sama dengan munculnya sel di bumi, dan selama bertahun-tahun selalu bergantung kepada sel hidup.[138] Viroid adalah molekul RNA yang tidak digolongkan sebagai virus karena mereka tidak memiliki lapisan protein. Viroid sering disebut agen subviral.[139] Sementara itu, virofag bergantung pada virus raksasa dalam menginfeksi sel inang, misalnya virofag Sputnik bergantung pada Mimivirus yang menginfeksi protozoa Acanthamoeba castellanii.[140] Virus-virus yang bergantung pada keberadaan spesies virus lain di dalam sel inang disebut "satelit" dan dapat menjadi perantara evolusi antara viroid dan virus.[141][142]
Ketiga hipotesis ini memiliki kelemahan. Hipotesis regresi tidak dapat menjelaskan mengapa sel-sel parasit terkecil yang ditemukan pun tidak memiliki kemiripan sama sekali dengan virus. Hipotesis keluar dari sel tidak dapat menjelaskan struktur-struktur yang hanya ada pada virus dan tidak pada sel. Hipotesis koevolusi tidak dapat menjelaskan bagaimana virus yang terbentuk pertama kali dapat bertahan dan memperbanyak diri tanpa keberadaan sel.[138][143]
Peranan dalam ekosistem laut
Virus merupakan entitas biologis yang paling melimpah di lingkungan perairan.[17] Satu sendok teh air laut mengandung sekitar sepuluh juta virus,[144] dan mereka berperan penting dalam pengaturan ekosistem air asin dan air tawar.[145] Sebagian besar virus dalam perairan tersebut merupakan bakteriofag,[146] yang tidak berbahaya bagi tumbuhan dan hewan. Mereka menginfeksi dan menghancurkan bakteri pada komunitas mikrob akuatik dan hal ini merupakan mekanisme daur ulang karbon yang paling penting dalam ekosistem laut. Molekul organik yang dilepaskan dari sel bakteri oleh virus merangsang pertumbuhan bakteri dan alga segar.[147]
Mikroorganisme mencakup lebih dari 90% biomassa di laut. Virus diperkirakan membunuh sekitar 20% dari biomassa ini setiap hari. Jumlah virus di lautan 10-15 kali lebih banyak dibandingkan bakteri dan arkea.[148] Virus-virus ini terutama bertanggung jawab atas pengurangan populasi alga dengan cepat sehingga mencegah ledakan populasi alga,[149] yang sering kali membunuh kehidupan laut lainnya.[150] Peran virus di lautan sangat besar; dengan meningkatkan jumlah respirasi di lautan, virus secara tidak langsung berperan untuk mengurangi jumlah karbon dioksida di atmosfer sekitar 3 gigaton karbon per tahun.[151] Jumlah virus di lautan semakin berkurang di area pantai dan laut dalam karena jumlah organisme inang lebih sedikit di area-area tersebut.[151]
Mamalia laut juga rentan terhadap infeksi virus. Pada tahun 1988 dan 2002, ribuan anjing laut di Eropa mati akibat infeksi Phocine morbillivirus.[152] Banyak virus lain, termasuk calicivirus, herpesvirus, adenovirus, dan parvovirus, beredar pada populasi mamalia laut.[151]
Lihat pula
Rujukan
Catatan kaki
- ^ a b "Virus Taxonomy: 2019 Release". International Committee on Taxonomy of Viruses. Juli 2019. Diarsipkan dari versi asli tanggal 2020-03-20. Diakses tanggal 27 Oktober 2020.
- ^ Shors 2017, hlm. 6.
- ^ Collier dkk. 1998, hlm. 3.
- ^ Shors 2017, hlm. 827.
- ^ D'herelle F (2007). "On an invisible microbe antagonistic toward dysenteric bacilli: brief note by Mr. F. D'Herelle, presented by Mr. Roux. 1917". Research in Microbiology. 158 (7): 553–54. doi:10.1016/j.resmic.2007.07.005. PMID 17855060.
- ^ From Nobel Lectures, Physics 1981–1990, (1993) Editor-in-Charge Tore Frängsmyr, Editor Gösta Ekspång, World Scientific Publishing Co., Singapore
- ^ Stanley WM, Loring HS (1936). "The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants". Science. 83 (2143): 85. Bibcode:1936Sci....83...85S. doi:10.1126/science.83.2143.85. PMID 17756690.
- ^ Stanley WM, Lauffer MA (1939). "Disintegration of tobacco mosaic virus in urea solutions". Science. 89 (2311): 345–47. Bibcode:1939Sci....89..345S. doi:10.1126/science.89.2311.345. PMID 17788438.
- ^ Goodpasture EW, Woodruff AM, Buddingh GJ (Oktober 1931). "The Cultivation Of Vaccine and other Viruses In The Chorioallantoic Membrane of Chick Embryos". Science. 74 (1919): 371–72. Bibcode:1931Sci....74..371G. doi:10.1126/science.74.1919.371. PMID 17810781.
- ^ Rosen FS (Oktober 2004). "Isolation of poliovirus – John Enders and the Nobel Prize". N. Engl. J. Med. 351 (15): 1481–83. doi:10.1056/NEJMp048202. PMID 15470207.
- ^ Koonin, E.V.; Starokadomskyy, P. (7 Maret 2016). "Are viruses alive? The replicator paradigm sheds decisive light on an old but misguided question". Stud Hist Philos Biol Biomed Sci. 59: 125–34. doi:10.1016/j.shpsc.2016.02.016. PMC 5406846
 . PMID 26965225.
. PMID 26965225.
- ^ Rybicki EP (1990). "The classification of organisms at the edge of life, or problems with virus systematics". South African Journal of Science. 86: 182–86.
- ^ Holmes EC (October 2007). "Viral evolution in the genomic age". PLOS Biology. 5 (10): e278. doi:10.1371/journal.pbio.0050278. PMC 1994994
 . PMID 17914905.
. PMID 17914905.
- ^ Wimmer E, Mueller S, Tumpey TM, Taubenberger JK (December 2009). "Synthetic viruses: a new opportunity to understand and prevent viral disease". Nature Biotechnology. 27 (12): 1163–72. doi:10.1038/nbt.1593. PMC 2819212
 . PMID 20010599.
. PMID 20010599.
- ^ Horn M (2008). "Chlamydiae as symbionts in eukaryotes". Annual Review of Microbiology. 62: 113–31. doi:10.1146/annurev.micro.62.081307.162818. PMID 18473699.
- ^ Ammerman NC, Beier-Sexton M, Azad AF (November 2008). "Laboratory maintenance of Rickettsia rickettsii". Current Protocols in Microbiology. Chapter 3 (1): Unit 3A.5. doi:10.1002/9780471729259.mc03a05s11. ISBN 978-0471729259. PMC 2725428
 . PMID 19016440.
. PMID 19016440.
- ^ a b Koonin EV, Senkevich TG, Dolja VV (September 2006). "The ancient Virus World and evolution of cells". Biology Direct. 1 (1): 29. doi:10.1186/1745-6150-1-29. PMC 1594570
 . PMID 16984643.
. PMID 16984643.
- ^ a b Collier dkk. 1998, hlm. 33–55.
- ^ Rotter ML (Agustus 2001). "Arguments for alcoholic hand disinfection". The Journal of Hospital Infection. 48 Suppl A: S4–8. doi:10.1016/s0195-6701(01)90004-0. PMID 11759024.
- ^ Abergel C, Legendre M, Claverie JM (November 2015). "The rapidly expanding universe of giant viruses: Mimivirus, Pandoravirus, Pithovirus and Mollivirus". FEMS Microbiol. Rev. 39 (6): 779–96. doi:10.1093/femsre/fuv037. PMID 26391910.
- ^ Philippe N, Legendre M, Doutre G, Couté Y, Poirot O, Lescot M, Arslan D, Seltzer V, Bertaux L, Bruley C, Garin J, Claverie JM, Abergel C (Juli 2013). "Pandoraviruses: amoeba viruses with genomes up to 2.5 Mb reaching that of parasitic eukaryotes" (PDF). Science. 341 (6143): 281–86. Bibcode:2013Sci...341..281P. doi:10.1126/science.1239181. PMID 23869018. Diarsipkan (PDF) dari versi asli tanggal 2020-04-02. Diakses tanggal 2020-03-27.
- ^ Zimmer C (18 Juli 2013). "Changing View on Viruses: Not So Small After All". New York Times. Diarsipkan dari versi asli tanggal 2014-12-20. Diakses tanggal 20 Desember 2014.
- ^ Shors 2017, hlm. 81.
- ^ International Human, Genome Sequencing Consortium (2004). "Finishing the euchromatic sequence of the human genome". Nature. 431 (7011): 931–45. Bibcode:2004Natur.431..931H. doi:10.1038/nature03001. PMID 15496913.
- ^ a b c Shors 2017, hlm. 129.
- ^ Shors 2017, hlm. 129–131.
- ^ Shors 2017, hlm. 652.
- ^ Shors 2017, hlm. 654.
- ^ Shors 2017, hlm. 113.
- ^ Shors 2017, hlm. 104.
- ^ a b de Klerk E, 't Hoen PA (Maret 2015). "Alternative mRNA transcription, processing, and translation: insights from RNA sequencing". Trends in Genetics : TIG. 31 (3): 128–39. doi:10.1016/j.tig.2015.01.001. PMID 25648499.
- ^ Collier dkk. 1998, hlm. 75–82.
- ^ Shors 2017, hlm. 698.
- ^ WHO 2004, hlm. 154.
- ^ WHO 2004, hlm. 166.
- ^ a b c WHO 2004, hlm. 168.
- ^ Gröner, Albrecht; Broumis, Connie; Fang, Randel; Nowak, Thomas; Popp, Birgit; Schäfer, Wolfram; Roth, Nathan J. (Januari 2018). "Effective inactivation of a wide range of viruses by pasteurization: VIRUS INACTIVATION BY PASTEURIZATION". Transfusion (dalam bahasa Inggris). 58 (1): 41–51. doi:10.1111/trf.14390.
- ^ WHO 2004, hlm. 204–208.
- ^ Moore, Mark A. (Agustus 2012). "Inactivation of enveloped and non-enveloped viruses on seeded human tissues by gamma irradiation". Cell and Tissue Banking (dalam bahasa Inggris). 13 (3): 401–407. doi:10.1007/s10561-011-9266-0. ISSN 1389-9333. PMC 3432196
 . PMID 21809182. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-07.
. PMID 21809182. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-07.
- ^ Lee, C. A.; Kessler, C. M.; Varon, D.; Martinowitz, U.; Heim, M.; Miekka, S. I.; Busby, T. F.; Reid, B.; Pollock, R. (Juli 1998). "New methods for inactivation of lipid-enveloped and nonenveloped viruses". Haemophilia (dalam bahasa Inggris). 4 (4): 402–408. doi:10.1046/j.1365-2516.1998.440402.x.
- ^ Blázquez, Elena; Rodríguez, Carmen; Ródenas, Jesús; Navarro, Núria; Riquelme, Cristina; Rosell, Rosa; Campbell, Joy; Crenshaw, Joe; Segalés, Joaquim (21 Februari 2019). Heldt, Caryn L., ed. "Evaluation of the effectiveness of the SurePure Turbulator ultraviolet-C irradiation equipment on inactivation of different enveloped and non-enveloped viruses inoculated in commercially collected liquid animal plasma". PLOS ONE (dalam bahasa Inggris). 14 (2): e0212332. doi:10.1371/journal.pone.0212332. ISSN 1932-6203. PMC 6383881
 . PMID 30789926. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-07.
. PMID 30789926. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-07.
- ^ Shors 2017, hlm. 6–13.
- ^ Shors 2017, hlm. 124–125.
- ^ Shors 2017, hlm. 125.
- ^ Shors 2017, hlm. 127.
- ^ Shors 2017, hlm. 137.
- ^ Shors 2017, hlm. 141.
- ^ De Paepe, Marianne; Leclerc, Marion; Tinsley, Colin R.; Petit, Marie-Agnes (28 Maret 2014). "Bacteriophages: an underestimated role in human and animal health?". Frontiers in Cellular and Infection Microbiology. 4. doi:10.3389/fcimb.2014.00039. ISSN 2235-2988. PMC 3975094
 . PMID 24734220.
. PMID 24734220.
- ^ Smith, Kenneth Manley; Ritchie, Donald Andrew (1980). Introduction to virology. London: Chapman and Hall. hlm. 131. ISBN 0-412-21960-3. OCLC 5336780. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-04.
- ^ Collier dkk. 1998, hlm. 115–146.
- ^ Collier dkk. 1998, hlm. 115.
- ^ Okamoto T, Suzuki T, Kusakabe S, Tokunaga M, Hirano J, Miyata Y, Matsuura Y (2017). "Regulation of Apoptosis during Flavivirus Infection". Viruses. 9 (9): 243. doi:10.3390/v9090243. PMC 5618009
 . PMID 28846635.
. PMID 28846635.
- ^ Alwine JC (2008). Modulation of host cell stress responses by human cytomegalovirus. Curr. Top. Microbiol. Immunol. Current Topics in Microbiology and Immunology. 325. hlm. 263–79. doi:10.1007/978-3-540-77349-8_15. ISBN 978-3-540-77348-1. PMID 18637511.
- ^ Sinclair J (Maret 2008). "Human cytomegalovirus: Latency and reactivation in the myeloid lineage". J. Clin. Virol. 41 (3): 180–85. doi:10.1016/j.jcv.2007.11.014. PMID 18164651.
- ^ Jordan MC, Jordan GW, Stevens JG, Miller G (Juni 1984). "Latent herpesviruses of humans". Ann. Intern. Med. 100 (6): 866–80. doi:10.7326/0003-4819-100-6-866. PMID 6326635.
- ^ Sissons JG, Bain M, Wills MR (Februari 2002). "Latency and reactivation of human cytomegalovirus" (PDF). J. Infect. 44 (2): 73–77. doi:10.1053/jinf.2001.0948. PMID 12076064. Diarsipkan dari versi asli (PDF) tanggal 2019-02-22. Diakses tanggal 2020-03-29.
- ^ Graham SV (2017). "The human papillomavirus replication cycle, and its links to cancer progression: a comprehensive review". Clinical Science. 131 (17): 2201–21. doi:10.1042/CS20160786. PMID 28798073.
- ^ Barozzi P, Potenza L, Riva G, Vallerini D, Quadrelli C, Bosco R, Forghieri F, Torelli G, Luppi M (Desember 2007). "B cells and herpesviruses: a model of lymphoproliferation". Autoimmun Rev. 7 (2): 132–36. doi:10.1016/j.autrev.2007.02.018. PMID 18035323.
- ^ Roulston A, Marcellus RC, Branton PE (1999). "Viruses and apoptosis". Annu. Rev. Microbiol. 53: 577–628. doi:10.1146/annurev.micro.53.1.577. PMID 10547702.
- ^ Dietzgen, Ralf; Mann, Krin; Johnson, Karyn (9 November 2016). "Plant Virus–Insect Vector Interactions: Current and Potential Future Research Directions". Viruses (dalam bahasa Inggris). 8 (11): 303. doi:10.3390/v8110303. ISSN 1999-4915. PMC 5127017
 . PMID 27834855. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
. PMID 27834855. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
- ^ "Herpes simplex virus". WHO (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 2020-04-11. Diakses tanggal 8 April 2020.
- ^ Shaw, G. M.; Hunter, E. (1 November 2012). "HIV Transmission". Cold Spring Harbor Perspectives in Medicine (dalam bahasa Inggris). 2 (11): a006965–a006965. doi:10.1101/cshperspect.a006965. ISSN 2157-1422. PMC 3543106
 . PMID 23043157. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
. PMID 23043157. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
- ^ Gaythorpe, K. A. M.; Trotter, C. L.; Lopman, B.; Steele, M.; Conlan, A. J. K. (Januari 2018). "Norovirus transmission dynamics: a modelling review". Epidemiology and Infection (dalam bahasa Inggris). 146 (2): 147–158. doi:10.1017/S0950268817002692. ISSN 0950-2688. PMC 5851036
 . PMID 29268812.
. PMID 29268812.
- ^ Crawford, Sue E.; Ramani, Sasirekha; Tate, Jacqueline E.; Parashar, Umesh D.; Svensson, Lennart; Hagbom, Marie; Franco, Manuel A.; Greenberg, Harry B.; O'Ryan, Miguel (Desember 2017). "Rotavirus infection". Nature Reviews Disease Primers (dalam bahasa Inggris). 3 (1): 17083. doi:10.1038/nrdp.2017.83. ISSN 2056-676X. PMC 5858916
 . PMID 29119972. Diarsipkan dari versi asli tanggal 2021-03-07. Diakses tanggal 2020-04-08.
. PMID 29119972. Diarsipkan dari versi asli tanggal 2021-03-07. Diakses tanggal 2020-04-08.
- ^ Neumann, Gabriele; Kawaoka, Yoshihiro (Mei 2015). "Transmission of influenza A viruses". Virology (dalam bahasa Inggris). 479-480: 234–246. doi:10.1016/j.virol.2015.03.009. PMC 4424116
 . PMID 25812763. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
. PMID 25812763. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
- ^ Burke, Crystal W.; Bridges, Olga; Brown, Sherri; Rahija, Richard; Russell, Charles J. (21 November 2013). Subbarao, Kanta, ed. "Mode of Parainfluenza Virus Transmission Determines the Dynamics of Primary Infection and Protection from Reinfection". PLoS Pathogens (dalam bahasa Inggris). 9 (11): e1003786. doi:10.1371/journal.ppat.1003786. ISSN 1553-7374. PMC 3836739
 . PMID 24278024. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
. PMID 24278024. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
- ^ Singhal, Tanu (April 2020). "A Review of Coronavirus Disease-2019 (COVID-19)". The Indian Journal of Pediatrics (dalam bahasa Inggris). 87 (4): 281–286. doi:10.1007/s12098-020-03263-6. ISSN 0019-5456. PMC 7090728
 . PMID 32166607. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
. PMID 32166607. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-08.
- ^ Marques-Toledo, Cecilia A.; Bendati, Maria Mercedes; Codeço, Claudia T.; Teixeira, Mauro M. (Desember 2019). "Probability of dengue transmission and propagation in a non-endemic temperate area: conceptual model and decision risk levels for early alert, prevention and control". Parasites & Vectors (dalam bahasa Inggris). 12 (1): 38. doi:10.1186/s13071-018-3280-z. ISSN 1756-3305. PMC 6335707
 . PMID 30651125. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
. PMID 30651125. Diarsipkan dari versi asli tanggal 2020-04-19. Diakses tanggal 2020-04-08.
- ^ Britt, William (3 Agustus 2018). "Maternal Immunity and the Natural History of Congenital Human Cytomegalovirus Infection". Viruses (dalam bahasa Inggris). 10 (8): 405. doi:10.3390/v10080405. ISSN 1999-4915. PMC 6116058
 . PMID 30081449. Diarsipkan dari versi asli tanggal 2020-04-16. Diakses tanggal 2020-04-08.
. PMID 30081449. Diarsipkan dari versi asli tanggal 2020-04-16. Diakses tanggal 2020-04-08.
- ^ Warren, Cody J.; Sawyer, Sara L. (19 April 2019). "How host genetics dictates successful viral zoonosis". PLOS Biology (dalam bahasa Inggris). 17 (4): e3000217. doi:10.1371/journal.pbio.3000217. ISSN 1545-7885. PMC 6474636
 . PMID 31002666. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-03.
. PMID 31002666. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-03.
- ^ "Zoonosis". WHO. Diarsipkan dari versi asli tanggal 2015-01-03. Diakses tanggal 5 April 2020.
- ^ "Rabies Key Facts". Organisasi Kesehatan Dunia (WHO). 2019. Diarsipkan dari versi asli tanggal 9 Mei 2019.
- ^ Shors 2017, hlm. 32.
- ^ Shors 2017, hlm. 271.
- ^ Berngruber TW, Froissart R, Choisy M, Gandon S (2013). "Evolution of Virulence in Emerging Epidemics". PLOS Pathogens. 9(3): e1003209 (3): e1003209. doi:10.1371/journal.ppat.1003209. PMC 3597519
 . PMID 23516359.
. PMID 23516359.
- ^ Shors 2017, hlm. 464.
- ^ Tanaka J, Akita T, Ko K, Miura Y, Satake M (September 2019). "Countermeasures against viral hepatitis B and C in Japan: An epidemiological point of view". Hepatology Research : The Official Journal of the Japan Society of Hepatology. 49 (9): 990–1002. doi:10.1111/hepr.13417. PMC 6852166
 . PMID 31364248.
. PMID 31364248.
- ^ Lai CC, Liu YH, Wang CY, Wang YH, Hsueh SC, Yen MY, Ko WC, Hsueh PR (Maret 2020). "Asymptomatic carrier state, acute respiratory disease, and pneumonia due to severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2): Facts and myths". Journal of Microbiology, Immunology, and Infection = Wei Mian Yu Gan Ran Za Zhi. doi:10.1016/j.jmii.2020.02.012. PMID 32173241.
- ^ Collier dkk. 1998, hlm. 766.
- ^ Strand LK (Juli 2018). "The Terrible Summer of 1952 … When Polio Struck Our Family". Seminars in Pediatric Neurology. 26: 39–44. doi:10.1016/j.spen.2017.04.001. PMID 29961515.
- ^ Moorthy M, Castronovo D, Abraham A, Bhattacharyya S, Gradus S, Gorski J, Naumov YN, Fefferman NH, Naumova EN (Oktober 2012). "Deviations in influenza seasonality: odd coincidence or obscure consequence?". Clinical Microbiology and Infection : The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases. 18 (10): 955–62. doi:10.1111/j.1469-0691.2012.03959.x. PMC 3442949
 . PMID 22958213.
. PMID 22958213.
- ^ Barril PA, Fumian TM, Prez VE, Gil PI, Martínez LC, Giordano MO, Masachessi G, Isa MB, Ferreyra LJ, Ré VE, Miagostovich M, Pavan JV, Nates SV (April 2015). "Rotavirus seasonality in urban sewage from Argentina: effect of meteorological variables on the viral load and the genetic diversity". Environmental Research. 138: 409–15. Bibcode:2015ER....138..409B. doi:10.1016/j.envres.2015.03.004. PMID 25777068.
- ^ Durrheim DN, Crowcroft NS, Strebel PM (Desember 2014). "Measles – The epidemiology of elimination". Vaccine. 32 (51): 6880–83. doi:10.1016/j.vaccine.2014.10.061. PMID 25444814.
- ^ Mbanzulu KM, Mboera LE, Luzolo FK, Wumba R, Misinzo G, Kimera SI (Februari 2020). "Mosquito-borne viral diseases in the Democratic Republic of the Congo: a review". Parasites & Vectors. 13 (1): 103. doi:10.1186/s13071-020-3985-7. PMC 7045448
 . PMID 32103776.
. PMID 32103776.
- ^ Morse, Stephen S. (1995). "Factors in the Emergence of Infectious Diseases". Emerging Infectious Diseases. 1 (1): 7–15. doi:10.3201/eid0101.950102. ISSN 1080-6040. PMC 2626828
 . PMID 8903148. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-04.
. PMID 8903148. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-04.
- ^ Institute of Medicine (US), Forum on Emerging Infections (2001). Davis, Jonathan R.; Lederberg, Joshua, ed. Emerging Infectious Diseases from the Global to the Local Perspective: A Summary of a Workshop of the Forum on Emerging Infections. Washington, D.C.: National Academy Press. doi:10.17226/10084. ISBN 0-309-56482-4. OCLC 49549298. Diarsipkan dari versi asli tanggal 2022-05-24. Diakses tanggal 2020-04-09.
- ^ Eisinger RW, Fauci AS (Maret 2018). "Ending the HIV/AIDS Pandemic1". Emerging Infectious Diseases. 24 (3): 413–16. doi:10.3201/eid2403.171797. PMC 5823353
 . PMID 29460740.
. PMID 29460740.
- ^ Nishiyama Y, Matsukuma S, Matsumura T, Kanatani Y, Saito T (April 2015). "Preparedness for a smallpox pandemic in Japan: public health perspectives". Disaster Medicine and Public Health Preparedness. 9 (2): 220–23. doi:10.1017/dmp.2014.157. PMID 26060873.
- ^ Houghton F (2019). "Geography, global pandemics & air travel: Faster, fuller, further & more frequent". Journal of Infection and Public Health. 12 (3): 448–49. doi:10.1016/j.jiph.2019.02.020. PMID 30878442.
- ^ Geisbert, Tom (ed.). "Emerging viruses". Virology Journal. ISSN 1743-422X. Diarsipkan dari versi asli tanggal 2020-04-03. Diakses tanggal 20 April 2020.
- ^ Weiss SR, Leibowitz JL (2011). Coronavirus pathogenesis. Advances in Virus Research. 81. hlm. 85–164. doi:10.1016/B978-0-12-385885-6.00009-2. ISBN 978-0-12-385885-6. PMID 22094080.
- ^ Wong AT, Chen H, Liu SH, Hsu EK, Luk KS, Lai CK, Chan RF, Tsang OT, Choi KW, Kwan YW, Tong AY, Cheng VC, Tsang DC (Mei 2017). "From SARS to Avian Influenza Preparedness in Hong Kong". Clinical Infectious Diseases : An Official Publication of the Infectious Diseases Society of America. 64 (suppl_2): S98–S104. doi:10.1093/cid/cix123. PMID 28475794.
- ^ Zhou, Peng; Yang, Xing-Lou; Wang, Xian-Guang; Hu, Ben; Zhang, Lei; Zhang, Wei; Si, Hao-Rui; Zhu, Yan; Li, Bei (Maret 2020). "A pneumonia outbreak associated with a new coronavirus of probable bat origin". Nature (dalam bahasa Inggris). 579 (7798): 270–273. doi:10.1038/s41586-020-2012-7. ISSN 0028-0836. PMC 7095418
 . PMID 32015507. Diarsipkan dari versi asli tanggal 2020-04-03. Diakses tanggal 2020-04-04.
. PMID 32015507. Diarsipkan dari versi asli tanggal 2020-04-03. Diakses tanggal 2020-04-04.
- ^ Cyranoski, David (7 Februari 2020). "Did pangolins spread the China coronavirus to people?". Nature (dalam bahasa Inggris): d41586–020–00364–2. doi:10.1038/d41586-020-00364-2. ISSN 0028-0836. Diarsipkan dari versi asli tanggal 2020-04-04. Diakses tanggal 2020-04-04.
- ^ Zhang, Tao; Wu, Qunfu; Zhang, Zhigang (Maret 2020). "Probable Pangolin Origin of SARS-CoV-2 Associated with the COVID-19 Outbreak". Current Biology (dalam bahasa Inggris): S0960982220303602. doi:10.1016/j.cub.2020.03.022. Diarsipkan dari versi asli tanggal 2020-04-07. Diakses tanggal 2020-04-04.
- ^ Report of the WHO-China Joint Mission on Coronavirus Disease 2019 (COVID-19) (PDF) (Laporan). World Health Organization (WHO). 16–24 Februari 2020. Diarsipkan (PDF) dari versi asli tanggal 2020-02-29. Diakses tanggal 21 Maret 2020.
- ^ Ashour HM, Elkhatib WF, Rahman MM, Elshabrawy HA (Maret 2020). "Insights into the Recent 2019 Novel Coronavirus (SARS-CoV-2) in Light of Past Human Coronavirus Outbreaks". Pathogens (Basel, Switzerland). 9 (3): 186. doi:10.3390/pathogens9030186. PMID 32143502.
- ^ Deng SQ, Peng HJ (Februari 2020). "Characteristics of and Public Health Responses to the Coronavirus Disease 2019 Outbreak in China". Journal of Clinical Medicine. 9 (2): 575. doi:10.3390/jcm9020575. PMC 7074453
 . PMID 32093211.
. PMID 32093211.
- ^ Han Q, Lin Q, Jin S, You L (Februari 2020). "Coronavirus 2019-nCoV: A brief perspective from the front line". The Journal of Infection. 80 (4): 373–77. doi:10.1016/j.jinf.2020.02.010. PMID 32109444.
- ^ "A third of the global population is on coronavirus lockdown — here's our constantly updated list of countries and restrictions". Business Insider. 28 Maret 2020. Diarsipkan dari versi asli tanggal 2020-05-19. Diakses tanggal 2020-04-05.
- ^ "Coronavirus Travel Restrictions, Across the Globe". The New York Times. 1 April 2020. Diarsipkan dari versi asli tanggal 2020-06-12. Diakses tanggal 5 April 2020.
- ^ Shors 2017, hlm. 822.
- ^ Shors 2017, hlm. 802–803.
- ^ Desk Encyclopedia of General Virology. Boston: Academic Press; 2009. ISBN 978-0-12-375146-1. p. 82.
- ^ Shors 2017, hlm. 803.
- ^ Shors 2017, hlm. 116–117.
- ^ Shors 2017, hlm. 225–233.
- ^ Garcia-Ruiz H (2018). "Susceptibility Genes to Plant Viruses". Viruses. 10 (9): 484. doi:10.3390/v10090484. PMC 6164914
 . PMID 30201857.
. PMID 30201857.
- ^ Shors 2017, hlm. 812.
- ^ Soosaar JL, Burch-Smith TM, Dinesh-Kumar SP (2005). "Mechanisms of plant resistance to viruses". Nature Reviews Microbiology. 3 (10): 789–98. doi:10.1038/nrmicro1239. PMID 16132037.
- ^ a b Hampton, Hannah G.; Watson, Bridget N. J.; Fineran, Peter C. (Januari 2020). "The arms race between bacteria and their phage foes". Nature (dalam bahasa Inggris). 577 (7790): 327–336. doi:10.1038/s41586-019-1894-8. ISSN 0028-0836. Diarsipkan dari versi asli tanggal 2021-04-05. Diakses tanggal 2020-04-05.
- ^ Horvath, Philippe; Barrangou, Rodolphe (8 Januari 2010). "CRISPR/Cas, the Immune System of Bacteria and Archaea". Science (dalam bahasa Inggris). 327 (5962): 167–170. doi:10.1126/science.1179555. ISSN 0036-8075. PMID 20056882.
- ^ Stern, Adi; Sorek, Rotem (Januari 2011). "The phage-host arms race: Shaping the evolution of microbes". BioEssays (dalam bahasa Inggris). 33 (1): 43–51. doi:10.1002/bies.201000071. PMC 3274958
 . PMID 20979102.
. PMID 20979102.
- ^ Shors 2017, hlm. 237–255.
- ^ Small JC, Ertl HC (2011). "Viruses – from pathogens to vaccine carriers". Current Opinion in Virology. 1 (4): 241–45. doi:10.1016/j.coviro.2011.07.009. PMC 3190199
 . PMID 22003377.
. PMID 22003377.
- ^ Burakova Y, Madera R, McVey S, Schlup JR, Shi J (2018). "Adjuvants for Animal Vaccines". Viral Immunology. 31 (1): 11–22. doi:10.1089/vim.2017.0049. PMID 28618246.
- ^ "Influenza (Seasonal)". WHO. 6 November 2018. Diarsipkan dari versi asli tanggal 2019-10-25. Diakses tanggal 5 April 2020.
- ^ Thomssen R (1975). "Live attenuated versus killed virus vaccines". Monographs in Allergy. 9: 155–76. PMID 1090805.
- ^ Shors 2017, hlm. 237.
- ^ Shors 2017, hlm. 238.
- ^ Shors 2017, hlm. 142–143.
- ^ Shors 2017, hlm. 143.
- ^ Shors 2017, hlm. 514–515.
- ^ a b Shors 2017, hlm. 514.
- ^ Applegate TL, Fajardo E, Sacks JA (Juni 2018). "Hepatitis C Virus Diagnosis and the Holy Grail" (PDF). Infectious Disease Clinics of North America. 32 (2): 425–45. doi:10.1016/j.idc.2018.02.010. PMID 29778264.[pranala nonaktif permanen]
- ^ Paul N, Han SH (Juni 2011). "Combination Therapy for Chronic Hepatitis B: Current Indications". Curr Hepat Rep. 10 (2): 98–105. doi:10.1007/s11901-011-0095-1. PMC 3085106
 . PMID 21654909.
. PMID 21654909.
- ^ Shors 2017, hlm. 568.
- ^ Shors 2017, hlm. 463.
- ^ Shors 2017, hlm. 146.
- ^ Shors 2017, hlm. 148.
- ^ Shors 2017, hlm. 16.
- ^ Collier dkk. 1998, hlm. 18–19.
- ^ Liu Y, Nickle DC, Shriner D, Jensen MA, Learn GH, Mittler JE, Mullins JI (November 2004). "Molecular clock-like evolution of human immunodeficiency virus type 1". Virology. 329 (1): 101–08. doi:10.1016/j.virol.2004.08.014. PMID 15476878.
- ^ a b Krupovic M, Dooja W, Koonin EV (2019). "Origin of viruses: primordial replicators recruiting capsids from hosts". Nature Reviews Microbiology. 17 (7): 449–58. doi:10.1038/s41579-019-0205-6. PMID 31142823.
- ^ Collier dkk. 1998, hlm. 11–21.
- ^ Collier dkk. 1998, hlm. 11.
- ^ Collier dkk. 1998, hlm. 11–12.
- ^ a b Wessner, D.R. (2010). "The Origins of Viruses". Nature Education. 3 (9): 37. Diarsipkan dari versi asli tanggal 2020-11-03. Diakses tanggal 2020-11-01.
- ^ Dimmock dkk. 2007, hlm. 55.
- ^ La Scola B, Desnues C, Pagnier I, Robert C, Barrassi L, Fournous G, et al. (September 2008). "The virophage as a unique parasite of the giant mimivirus". Nature. 455 (7209): 100–4. Bibcode:2008Natur.455..100L. doi:10.1038/nature07218. PMID 18690211.
- ^ Collier dkk. 1998, hlm. 777.
- ^ Dimmock dkk. 2007, hlm. 55–57.
- ^ Nasir, Arshan; Kim, Kyung Mo; Caetano-Anollés, Gustavo (September 2012). "Viral evolution: Primordial cellular origins and late adaptation to parasitism". Mobile Genetic Elements. 2 (5): 247–252. doi:10.4161/mge.22797. ISSN 2159-256X. PMC 3575434
 . PMID 23550145. Diarsipkan dari versi asli tanggal 2020-08-02. Diakses tanggal 2020-11-01.
. PMID 23550145. Diarsipkan dari versi asli tanggal 2020-08-02. Diakses tanggal 2020-11-01.
- ^ Dávila-Ramos S, Castelán-Sánchez HG, Martínez-Ávila L, Sánchez-Carbente MD, Peralta R, Hernández-Mendoza A, Dobson AD, Gonzalez RA, Pastor N, Batista-García RA (2019). "A Review on Viral Metagenomics in Extreme Environments". Frontiers in Microbiology. 10: 2403. doi:10.3389/fmicb.2019.02403. PMC 6842933
 . PMID 31749771.
. PMID 31749771.
- ^ Shors 2017, hlm. 5.
- ^ Breitbart M, Bonnain C, Malki K, Sawaya NA (Juli 2018). "Phage puppet masters of the marine microbial realm". Nature Microbiology. 3 (7): 754–66. doi:10.1038/s41564-018-0166-y. PMID 29867096.
- ^ Shors 2017, hlm. 25–26.
- ^ Schaechter, Moselio, ed. (2009). Encyclopedia of microbiology (edisi ke-3). Amsterdam: Elsevier. hlm. 554. ISBN 978-0-12-373944-5. OCLC 399645273. Diarsipkan dari versi asli tanggal 2023-03-27. Diakses tanggal 2020-04-05.
- ^ Suttle CA (September 2005). "Viruses in the sea". Nature. 437 (7057): 356–61. Bibcode:2005Natur.437..356S. doi:10.1038/nature04160. PMID 16163346.
- ^ "Harmful Algal Blooms: Red Tide: Home | CDC HSB". www.cdc.gov. Diarsipkan dari versi asli tanggal 2009-08-27. Diakses tanggal 23 Agustus 2009.
- ^ a b c Suttle CA (Oktober 2007). "Marine viruses – major players in the global ecosystem". Nat. Rev. Microbiol. 5 (10): 801–12. doi:10.1038/nrmicro1750. PMID 17853907.
- ^ Hall A, Jepson P, Goodman S, Harkonen T (2006). "Phocine distemper virus in the North and European Seas – Data and models, nature and nurture". Biological Conservation. 131 (2): 221–29. doi:10.1016/j.biocon.2006.04.008.
Daftar pustaka
- Collier, Leslie; Balows, Albert; Sussman, Max, ed. (1998). Topley and Wilson's Microbiology and Microbial Infections (edisi ke-9). London: Arnold. ISBN 0-340-61470-6. OCLC 38290809.
- Dimmock, N. J.; Easton, A.J.; Leppard, K.N. (2007). Introduction to modern virology (edisi ke-6). Malden, MA: Blackwell Publishing. ISBN 1-4051-3645-6. OCLC 65207057. Diarsipkan dari versi asli tanggal 2020-06-15. Diakses tanggal 2020-04-09.
- Organisasi Kesehatan Dunia (2004). "Annex 4. Guidelines on Viral Inactivation and Removal Procedures Intended to Assure the Viral Safety of Human Blood Plasma Products" (PDF). WHO Expert Commitee on Biological Standardization. WHO Technical Report No. 924: Fifty-second report. Jenewa: Organisasi Kesehatan Dunia. Diarsipkan (PDF) dari versi asli tanggal 2017-06-23. Diakses tanggal 2020-04-03.
- Shors, Teri (2017). Understanding Viruses (edisi ke-3). Burlington, Massachusetts: Jones and Bartlett Learning. ISBN 978-1-284-02592-7. OCLC 948427269.

