Kalsium
| Kalsium | |||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Kalsium murni dalam atmosfer berpelindung argon | |||||||||||||||||||||||||||||||||||||||||||||||||||||
Garis spektrum kalsium | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat umum | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nama, lambang | kalsium, Ca | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pengucapan | /kalsium/[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penampilan | abu-abu kusam, perak; dengan warna kuning pucat[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalsium dalam tabel periodik | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor atom (Z) | 20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Golongan | golongan 2 (logam alkali tanah) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Periode | periode 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Blok | blok-s | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kategori unsur | logam alkali tanah | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Berat atom standar (Ar) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konfigurasi elektron | [Ar] 4s2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektron per kelopak | 2, 8, 8, 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat fisik | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fase pada STS (0 °C dan 101,325 kPa) | padat | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik lebur | 1115 K (842 °C, 1548 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Titik didih | 1757 K (1484 °C, 2703 °F) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kepadatan mendekati s.k. | 1,55 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| saat cair, pada t.l. | 1,378 g/cm3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor peleburan | 8,54 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kalor penguapan | 154,7 kJ/mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kapasitas kalor molar | 25,929 J/(mol·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
Tekanan uap
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sifat atom | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bilangan oksidasi | +1,[3] +2 (oksida basa kuat) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativitas | Skala Pauling: 1,00 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Energi ionisasi | ke-1: 589,8 kJ/mol ke-2: 1145,4 kJ/mol ke-3: 4912,4 kJ/mol (artikel) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari atom | empiris: 197 pm perhitungan: 194 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari kovalen | 176±10 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Jari-jari van der Waals | 231 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lain-lain | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kelimpahan alami | primordial | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Struktur kristal | kubus berpusat muka (fcc) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kecepatan suara batang ringan | 3810 m/s (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekspansi kalor | 22,3 µm/(m·K) (suhu 25 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Konduktivitas termal | 201 W/(m·K) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Resistivitas listrik | 33,6 n nΩ·m (suhu 20 °C) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Arah magnet | diamagnetik | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Suseptibilitas magnetik molar | +40,0×10−6 cm3/mol[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Young | 20 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus Shear | 7,4 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Modulus curah | 17 GPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rasio Poisson | 0,31 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Mohs | 1,75 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skala Brinell | 170–416 MPa | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nomor CAS | 7440-70-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sejarah | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| Penemuan dan isolasi pertama | H. Davy (1808) | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotop kalsium yang utama | |||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||
Kalsium atau zat kapur adalah sebuah unsur kimia dengan lambang Ca dan nomor atom 20. Sebagai logam alkali tanah, kalsium merupakan logam reaktif yang membentuk lapisan oksida-nitrida gelap bila terpapar udara. Sifat fisik dan kimianya paling mirip dengan homolognya yang lebih berat, stronsium dan barium. Ia adalah unsur paling melimpah kelima di kerak Bumi, dan logam paling melimpah ketiga, setelah besi dan aluminium. Senyawa kalsium yang paling umum di Bumi adalah kalsium karbonat, ditemukan di batu kapur dan sisa-sisa fosil kehidupan laut awal,; gipsum, anhidrit, fluorit, dan apatit juga merupakan sumber kalsium. Nama kalsium berasal dari bahasa Latin calx "kapur", yang diperoleh dari memanaskan batu kapur.
Beberapa senyawa kalsium telah diketahui orang dahulu, meskipun sifat kimianya tidak diketahui sampai abad ke-17. Kalsium murni diisolasi pada tahun 1808 melalui elektrolisis oksidanya oleh Humphry Davy, yang menamai unsur tersebut. Senyawa kalsium banyak digunakan di banyak industri: dalam makanan dan obat-obatan untuk suplementasi kalsium, dalam industri kertas sebagai pemutih, sebagai komponen dalam semen dan insulator listrik, dan dalam pembuatan sabun. Di sisi lain, logam kalsium dalam bentuk murni hanya memiliki sedikit aplikasi karena reaktivitasnya yang tinggi; tetap saja, dalam jumlah kecil ia sering digunakan sebagai komponen paduan dalam pembuatan baja, dan kadang-kadang, sebagai paduan kalsium-timbal, dalam pembuatan baterai otomotif.
Kalsium adalah logam paling melimpah dan unsur paling melimpah kelima dalam tubuh manusia.[5] Sebagai elektrolit, ion kalsium (Ca2+) memainkan peran penting dalam proses fisiologis dan biokimia organisme dan sel: dalam jalur transduksi sinyal di mana mereka bertindak sebagai pembawa pesan kedua; dalam pelepasan neurotransmiter dari sel saraf; dalam kontraksi semua jenis sel otot; sebagai kofaktor dalam banyak enzim; dan dalam pembuahan.[5] Ion kalsium di luar sel penting untuk mempertahankan perbedaan potensial pada sintesis protein, pembentukan tulang, dan membran sel yang dapat dieksitasi.[5][6]
Karakteristik[sunting | sunting sumber]
Klasifikasi[sunting | sunting sumber]
Kalsium adalah logam keperakan (kadang-kadang digambarkan sebagai kuning pucat) yang sangat ulet yang sifatnya sangat mirip dengan unsur yang lebih berat dalam golongannya, stronsium, barium, dan radium. Sebuah atom kalsium memiliki dua puluh elektron, tersusun dalam konfigurasi elektron [Ar]4s2. Seperti unsur lain yang ditempatkan pada golongan 2 tabel periodik, kalsium memiliki dua elektron valensi di orbital s terluar, yang sangat mudah hilang dalam reaksi kimia untuk membentuk ion dipositif dengan konfigurasi elektron stabil gas mulia, dalam kasus ini ialah argon.[7]
Oleh karena itu, kalsium hampir selalu divalen dalam senyawanya, yang biasanya bersifat ionik. Garam kalsium univalen hipotetis akan stabil sehubungan dengan unsur-unsurnya, tetapi tidak untuk disproporsionasi dengan garam divalen dan logam kalsium, karena entalpi pembentukan MX2 jauh lebih tinggi daripada entalpi pembentukan MX hipotetis. Hal ini terjadi karena energi kisi yang diberikan oleh kation Ca2+ yang bermuatan lebih tinggi jauh lebih besar bila dibandingkan dengan kation Ca+ hipotetis.[7]
Kalsium, stronsium, barium, dan radium selalu dianggap sebagai logam alkali tanah; berilium dan magnesium yang lebih ringan, juga dalam golongan 2 tabel periodik, sering dimasukkan pula. Namun demikian, berilium dan magnesium berbeda secara signifikan dari anggota golongan 2 lainnya dalam perilaku fisik dan kimianya: mereka masing-masing berperilaku lebih seperti aluminium dan seng dan memiliki beberapa karakter logam yang lebih lemah dari logam pascatransisi, itulah sebabnya definisi tradisional dari istilah "logam alkali tanah" tidak memasukkan mereka berdua.[8]
Sifat fisik[sunting | sunting sumber]
Logam kalsium melebur pada suhu 842 °C dan mendidih pada suhu 1494 °C; nilai-nilai ini lebih tinggi daripada magnesium dan stronsium, logam golongan 2 yang berdekatan dengannya. Ia mengkristal dalam susunan kubus berpusat-muka seperti stronsium; di atas suhu 450 °C, ia berubah menjadi susunan tetal-rapat heksagonal anisotropik seperti magnesium. Massa jenisnya sebesar 1,55 g/cm3 adalah yang terendah dalam golongannya.[7]
Kalsium lebih keras daripada timbal tetapi dapat dipotong dengan pisau dengan tenaga. Walaupun kalsium adalah konduktor listrik yang lebih buruk daripada tembaga atau alumunium berdasarkan volume, ia adalah konduktor yang lebih baik berdasarkan massa daripada keduanya karena massa jenisnya yang sangat rendah.[9] Walaupun kalsium tidak layak sebagai konduktor untuk sebagian besar aplikasi terestrial karena bereaksi cepat dengan oksigen atmosfer, penggunaannya di ruang angkasa telah dipertimbangkan.[10]
Sifat kimia[sunting | sunting sumber]

Kimia kalsium adalah logam alkali tanah berat yang tipikal. Misalnya, kalsium secara spontan bereaksi dengan air lebih cepat daripada magnesium dan kurang cepat daripada stronsium untuk menghasilkan kalsium hidroksida dan gas hidrogen. Ia juga bereaksi dengan oksigen dan nitrogen di udara untuk membentuk campuran kalsium oksida dan kalsium nitrida.[11] Ketika terbelah halus, ia secara spontan terbakar di udara untuk menghasilkan nitrida. Dalam jumlah besar, kalsium kurang reaktif: ia dengan cepat membentuk lapisan hidrasi di udara lembap, tetapi di bawah kelembapan relatif 30% ia dapat disimpan tanpa batas waktu pada suhu kamar.[12]
Selain oksida sederhana CaO, peroksida CaO2 dapat dibuat dengan oksidasi langsung logam kalsium di bawah tekanan oksigen yang tinggi, dan ada beberapa bukti untuk superoksida kuning Ca(O2)2.[13] Kalsium hidroksida, Ca(OH)2, adalah basa kuat, meski tidak sekuat hidroksida stronsium, barium, atau logam alkali.[14] Keempat dihalida kalsium telah diketahui.[15] Kalsium karbonat (CaCO3) dan kalsium sulfat (CaSO4) adalah mineral yang sangat melimpah.[16] Seperti stronsium dan barium, serta logam alkali dan lantanida divalen europium dan iterbium, logam kalsium akan langsung larut dalam amonia cair dan menghasilkan larutan biru tua.[7]
Karena ukuran ion kalsium (Ca2+) yang besar, bilangan koordinasi yang tinggi adalah umum, hingga 24 pada beberapa senyawa antarlogam seperti CaZn13.[17] Kalsium mudah dikomplekskan oleh kelat oksigen seperti EDTA dan polifosfat, yang berguna dalam kimia analitik dan menghilangkan ion kalsium dari air sadah. Dengan tidak adanya halangan sterik, kation golongan 2 yang lebih kecil cenderung membentuk kompleks yang lebih kuat, tetapi ketika makrosiklus polidentat besar terlibat, trennya terbalik.[16]
Meskipun kalsium berada dalam golongan yang sama dengan magnesium dan senyawa organomagnesium sangat umum digunakan di seluruh kimia, senyawa organokalsium tidak tersebar luas karena lebih sulit dibuat dan lebih reaktif, meskipun baru-baru ini diselidiki sebagai kemungkinan katalis.[18][19][20][21][22] Senyawa organokalsium cenderung lebih mirip dengan senyawa organoiterbium karena kesamaan jari-jari ion antara Yb2+ (102 pm) dan Ca2+ (100 pm).[23]
Sebagian besar senyawa ini hanya dapat dibuat pada suhu rendah; ligan besar cenderung mendukung stabilitas. Sebagai contoh, kalsium disiklopentadienil, Ca(C5H5)2, harus dibuat dengan mereaksikan langsung logam kalsium dengan merkurosena atau siklopentadiena itu sendiri; menggantikan ligan C5H5 dengan ligan C5(CH3)5 yang lebih besar di sisi lain meningkatkan kelarutan, volatilitas, dan stabilitas kinetik senyawa tersebut.[23]
Isotop[sunting | sunting sumber]
Kalsium alami adalah campuran dari lima isotop stabil (40Ca, 42Ca, 43Ca, 44Ca, dan 46Ca) dan satu isotop dengan waktu paruh yang sangat lama sehingga dapat dianggap stabil untuk semua tujuan praktis (48Ca, dengan waktu paruh sekitar 4,3×1019 tahun). Kalsium adalah unsur pertama (paling ringan) yang memiliki enam isotop alami.[11]
Sejauh ini isotop kalsium yang paling umum di alam adalah 40Ca, yang merupakan 96,941% dari semua kalsium alami. Ia diproduksi dalam proses pembakaran silikon dari fusi partikel alfa dan merupakan nuklida stabil terberat dengan jumlah proton dan neutron yang sama; keterjadiannya juga perlahan-lahan ditambah dengan peluruhan 40K primordial. Penambahan partikel alfa lainnya akan menghasilkan 44Ti yang tak stabil, yang dengan cepat meluruh melalui dua tangkapan elektron berturut-turut menjadi 44Ca yang stabil; isotop ini membentuk 2,806% dari semua kalsium alami dan merupakan isotop paling umum kedua.[24][25]
Empat isotop alami lainnya, 42Ca, 43Ca, 46Ca, dan 48Ca, secara signifikan lebih jarang, masing-masing mengandung kurang dari 1% dari semua kalsium alami. Keempat isotop yang lebih ringan sebagian besar merupakan produk dari proses pembakaran oksigen dan pembakaran silikon, meninggalkan dua isotop yang lebih berat untuk diproduksi melalui proses tangkapan neutron. 46Ca sebagian besar diproduksi dalam proses s "panas", karena pembentukannya membutuhkan fluks neutron yang agak tinggi untuk memungkinkan 45Ca yang berumur pendek untuk menangkap neutron. 48Ca diproduksi oleh tangkapan elektron dalam proses r dalam supernova tipe Ia, di mana kelebihan neutron yang tinggi dan entropi yang cukup rendah memastikan kelangsungan hidupnya.[24][25]
46Ca dan 48Ca adalah nuklida "stabil klasik" pertama dengan kelebihan masing-masing enam neutron atau delapan neutron. Meskipun sangat kaya akan neutron untuk unsur ringan seperti itu, 48Ca sangat stabil karena ia merupakan inti ajaib ganda, memiliki 20 proton dan 28 neutron yang tersusun dalam kulit tertutup. Peluruhan betanya menjadi 48Sc sangat terhambat karena ketidakcocokan besar spin nuklir: 48Ca memiliki spin nuklir nol, merupakan inti genap–genap, sedangkan 48Sc memiliki spin 6+, sehingga peluruhannya dilarang oleh kekekalan momentum sudut. Walaupun dua keadaan tereksitasi 48Sc juga tersedia untuk peluruhan, keduanya juga dilarang karena spinnya yang tinggi. Akibatnya, ketika 48Ca meluruh, ia melakukannya dengan peluruhan beta ganda menjadi 48Ti, menjadi nuklida paling ringan yang diketahui mengalami peluruhan beta ganda.[26][27]
Isotop berat 46Ca juga secara teoretis dapat mengalami peluruhan beta ganda menjadi 46Ti, tetapi hal ini belum pernah teramati. Isotop paling ringan dan paling umum 40Ca juga ajaib ganda dan dapat mengalami tangkapan elektron ganda menjadi 40Ar, tetapi hal ini juga belum pernah teramati. Kalsium adalah satu-satunya unsur yang memiliki dua isotop ajaib ganda primordial. Batas bawah eksperimental untuk waktu paruh 40Ca dan 46Ca masing-masing adalah 5,9×1021 tahun dan 2,8×1015 tahun.[26]
Terlepas dari 48Ca yang praktis stabil, radioisotop kalsium yang berumur paling panjang adalah 41Ca. Ia meluruh melalui tangkapan elektron menjadi 41K yang stabil dengan waktu paruh sekitar seratus ribu tahun. Keberadaannya di Tata Surya awal sebagai radionuklida punah telah disimpulkan dari ekses 41K: jejak dari 41Ca juga masih ada hingga sekarang, karena ia merupakan nuklida kosmogenik, yang terus direformasi melalui aktivasi neutron dari 40Ca alami.[25]
Banyak radioisotop kalsium lain yang diketahui, mulai dari 35Ca hingga 60Ca. Mereka semua berumur lebih pendek dari 41Ca, yang paling stabil di antara mereka adalah 45Ca (waktu paruh 163 hari) dan 47Ca (waktu paruh 4,54 hari). Isotop yang lebih ringan dari 42Ca biasanya mengalami peluruhan beta plus menjadi isotop kalium, dan yang lebih berat dari 44Ca biasanya mengalami peluruhan beta minus menjadi isotop skandium, meskipun di dekat garis tetesan nuklir, emisi proton dan emisi neutron mulai menjadi mode peluruhan yang signifikan pula.[26]
Seperti unsur lainnya, berbagai proses dapat mengubah kelimpahan relatif isotop kalsium.[28] Studi terbaik dari proses ini adalah fraksionasi isotop kalsium yang bergantung pada massa yang menyertai pengendapan mineral kalsium seperti kalsit, aragonit, dan apatit dari larutan. Isotop yang lebih ringan lebih disukai dimasukkan ke dalam mineral ini, meninggalkan larutan di sekitarnya diperkaya dengan isotop yang lebih berat dengan besaran sekitar 0,025% per satuan massa atom (sma) pada suhu kamar. Perbedaan komposisi isotop kalsium yang bergantung massa secara konvensional dinyatakan dengan rasio dua isotop (biasanya 44Ca/40Ca) dalam sampel dibandingkan dengan rasio yang sama dalam bahan referensi standar. 44Ca/40Ca bervariasi sekitar 1% di antara bahan tanah biasa.[29]
Sejarah[sunting | sunting sumber]

Senyawa kalsium telah dikenal selama ribuan tahun, meskipun susunan kimiawinya baru diketahui pada abad ke-17.[30] Kapur sebagai bahan bangunan[31] dan sebagai plester untuk patung telah digunakan sejak sekitar 7000 SM.[32] Tanur kapur pertama berasal dari tahun 2500 SM dan ditemukan di Khafajah, Mesopotamia.[33][34]
Pada waktu yang hampir bersamaan, gipsum (CaSO4·2H2O) kering digunakan pada Piramida Agung Giza. Bahan ini nantinya akan digunakan untuk plester di makam Tutankhamun. Orang Romawi kuno menggunakan mortar kapur yang dibuat dengan memanaskan batu kapur (CaCO3). Nama "kalsium" sendiri berasal dari kata Latin calx yang berarti "kapur".[30]
Vitruvius mencatat bahwa kapur yang dihasilkan lebih ringan dari batu kapur asli, karena air mendidih. Pada tahun 1755, Joseph Black membuktikan bahwa hal ini disebabkan oleh hilangnya karbon dioksida, yang tidak dikenal sebagai gas oleh orang Romawi kuno.[35]
Pada tahun 1789, Antoine Lavoisier menduga bahwa kapur mungkin merupakan oksida dari unsur kimia dasar. Dalam tabel unsur-unsurnya, Lavoisier mendaftar lima "tanah yang dapat digarami", yaitu bijih yang dapat dibuat bereaksi dengan asam untuk menghasilkan garam (salis = garam, dalam bahasa Latin): chaux (kalsium oksida), magnésie (magnesia, magnesium oksida), baryte (barium sulfat), alumine (alumina, aluminium oksida), dan silice (silika, silikon dioksida). Mengenai "unsur-unsur" ini, Lavoisier beralasan:
Kita mungkin hanya mengenal sebagian dari zat logam yang ada di alam, karena semua zat yang memiliki afinitas lebih kuat terhadap oksigen daripada yang dimiliki karbon, sampai sekarang tidak mampu direduksi menjadi keadaan logam, dan akibatnya, menjadi hanya disajikan untuk pengamatan kami dalam bentuk oksida, dikacaukan dengan tanah. Sangat mungkin bahwa baryte, yang baru saja kita atur dengan tanah, berada dalam situasi ini; karena dalam banyak percobaan ia menunjukkan sifat yang hampir mendekati sifat benda logam. Bahkan mungkin saja semua zat yang kita sebut tanah mungkin hanya oksida logam, yang tidak dapat direduksi oleh proses apa pun yang diketahui sampai sekarang.[36]
Kalsium, bersama dengan kongenernya magnesium, stronsium, dan barium, pertama kali diisolasi oleh Humphry Davy pada tahun 1808. Mengikuti karya Jöns Jakob Berzelius dan Magnus Martin af Pontin pada elektrolisis, Davy mengisolasi kalsium dan magnesium dengan memasukkan campuran logam oksida masing-masing dengan raksa(II) oksida pada plat platina yang digunakan sebagai anoda, katodanya berupa kawat platina yang sebagian dicelupkan ke dalam raksa. Elektrolisis kemudian menghasilkan amalgam kalsium–raksa dan magnesium–raksa, dan penyulingan raksa menghasilkan logam kalsium.[30][37] Namun, kalsium murni tidak dapat dibuat dalam jumlah besar dengan metode ini dan proses komersial yang dapat diterapkan untuk produksinya baru ditemukan lebih dari seabad kemudian.[35]
Keterjadian dan produksi[sunting | sunting sumber]

Pada 3%, kalsium adalah unsur paling melimpah kelima di kerak Bumi, dan logam paling melimpah ketiga setelah aluminium dan besi.[30] Ia juga merupakan unsur paling melimpah keempat di dataran tinggi Bulan.[12] Endapan kalsium karbonat sedimen menyelimuti permukaan Bumi sebagai sisa-sisa fosil kehidupan laut masa lalu; mereka terjadi dalam dua bentuk, kalsit rombohedral (lebih umum) dan aragonit ortorombik (terbentuk di laut yang lebih beriklim). Mineral jenis pertama antara lain batu kapur, dolomit, marmer, dan kapur; endapan aragonit membentuk cekungan Bahama, Florida Keys, dan Laut Merah. Karang, cangkang hewan laut, dan mutiara sebagian besar terdiri dari kalsium karbonat. Di antara mineral penting kalsium lainnya adalah gipsum (CaSO4·2H2O), anhidrit (CaSO4), fluorit (CaF2), dan apatit ([Ca5(PO4)3F]).[30]
Produsen utama kalsium adalah Tiongkok (sekitar 10.000 hingga 12.000 ton per tahun), Rusia (sekitar 6.000 hingga 8.000 ton per tahun), dan Amerika Serikat (sekitar 2.000 hingga 4.000 ton per tahun). Kanada dan Prancis juga di antara produsen yang lebih kecil. Pada tahun 2005, sekitar 24.000 ton kalsium diproduksi; sekitar setengah dari kalsium yang diekstraksi dunia digunakan oleh Amerika Serikat, dengan sekitar 80% dari keluaran digunakan setiap tahun.[10]
Di Rusia dan Tiongkok, metode elektrolisis Davy masih digunakan, tetapi diterapkan pada kalsium klorida cair.[10] Karena kalsium kurang reaktif daripada stronsium atau barium, lapisan oksida–oksida-nitrida yang menghasilkan udara stabil dan permesinan bubut serta teknik metalurgi standar lainnya cocok untuk kalsium.[38] Di Amerika Serikat dan Kanada, kalsium diproduksi dengan mereduksi kapur dengan aluminium pada suhu tinggi.[10]
Siklus geokimia[sunting | sunting sumber]
Siklus kalsium menyediakan hubungan antara tektonik, iklim, dan siklus karbon. Dalam istilah yang paling sederhana, pengangkatan gunung akan mengekspos batuan yang mengandung kalsium seperti beberapa granit terhadap pelapukan kimiawi dan melepaskan Ca2+ ke dalam air permukaan. Ion-ion ini diangkut ke laut di mana mereka bereaksi dengan CO2 terlarut untuk membentuk batu kapur (CaCO3), yang pada gilirannya mengendap di dasar laut di mana ia dimasukkan ke dalam batuan baru. CO2 terlarut, bersama dengan ion karbonat dan bikarbonat, disebut sebagai "karbon anorganik terlarut" (dissolved inorganic carbon, DIC).[39]
Reaksi sebenarnya lebih rumit dan melibatkan ion bikarbonat (HCO−3) yang terbentuk ketika CO2 bereaksi dengan air pada pH air laut:
Pada pH air laut, sebagian besar CO2 segera diubah kembali menjadi HCO−3. Reaksi tersebut menghasilkan transportasi bersih dalam satu molekul CO2 dari laut/atmosfer ke litosfer.[40] Hasilnya adalah bahwa setiap ion Ca2+ yang dilepaskan oleh pelapukan kimia pada akhirnya menghilangkan satu molekul CO2 dari sistem permukaan (atmosfer, lautan, tanah, dan organisme hidup), menyimpannya dalam batuan karbonat yang kemungkinan besar akan bertahan selama ratusan juta tahun. Pelapukan kalsium dari batuan dengan demikian menghilangkan CO2 dari laut dan atmosfer, memberikan efek jangka panjang yang kuat pada iklim.[39][41]
Kegunaan[sunting | sunting sumber]
Penggunaan terbesar logam kalsium adalah dalam pembuatan baja, karena afinitas kimianya yang kuat terhadap oksigen dan belerang. Oksida dan sulfidanya, setelah terbentuk, memberikan aluminat cair dan inklusi sulfida dalam baja yang mengapung; pada perawatan, inklusi ini menyebar ke seluruh baja dan menjadi kecil dan bulat, meningkatkan kemudahan penuangan, kebersihan dan sifat mekanik secara umum. Kalsium juga digunakan dalam baterai otomotif bebas perawatan, di mana penggunaan paduan kalsium–timbal 0,1% alih-alih paduan antimon–timbal yang biasa akan menyebabkan kehilangan air yang lebih rendah dan pengosongan diri yang lebih rendah.[42]
Karena risiko pemuaian dan retak, aluminium terkadang juga dimasukkan ke dalam paduan ini. Paduan timbal–kalsium ini juga digunakan dalam pengecoran, menggantikan paduan timbal–antimon.[42] Kalsium juga digunakan untuk memperkuat paduan aluminium yang digunakan untuk bantalan, untuk mengontrol karbon grafit dalam besi tuang, dan untuk menghilangkan pengotor bismut dari timbal.[38] Logam kalsium ditemukan di beberapa pembersih saluran, di mana ia berfungsi untuk menghasilkan panas dan kalsium hidroksida yang menyabunkan lemak dan mencairkan protein (misalnya, yang ada di rambut) yang menyumbat saluran air.[43]
Selain metalurgi, reaktivitas kalsium dieksploitasi untuk menghilangkan nitrogen dari gas argon dengan kemurnian tinggi dan sebagai penangkap oksigen dan nitrogen. Ia juga digunakan sebagai agen pereduksi dalam produksi kromium, zirkonium, torium, dan uranium. Ia juga dapat digunakan untuk menyimpan gas hidrogen, karena ia bereaksi dengan hidrogen untuk membentuk kalsium hidrida padat, dari mana hidrogen dapat dengan mudah diekstraksi kembali.[38]
Fraksionasi isotop kalsium selama pembentukan mineral telah menyebabkan beberapa aplikasi isotop kalsium. Secara khusus, pengamatan tahun 1997 oleh Skulan dan DePaolo[44] bahwa mineral kalsium secara isotop lebih ringan daripada larutan dari mana mineral mengendap merupakan dasar aplikasi analog dalam kedokteran dan paleoseanografi. Pada hewan dengan kerangka yang termineralisasi dengan kalsium, komposisi isotop kalsium dari jaringan lunak mencerminkan tingkat relatif pembentukan dan disolusi mineral kerangka.[45]
Pada manusia, perubahan komposisi isotop kalsium dalam urin telah terbukti berhubungan dengan perubahan keseimbangan mineral tulang. Ketika laju pembentukan tulang melebihi laju resorpsi tulang, rasio 44Ca/40Ca dalam jaringan lunak meningkat dan sebaliknya. Karena hubungan ini, pengukuran isotop kalsium dalam urin atau darah mungkin berguna dalam deteksi dini penyakit tulang metabolik seperti osteoporosis.[45]
Sistem yang serupa terdapat di air laut, di mana 44Ca/40Ca cenderung meningkat ketika laju penghilangan Ca2+ oleh pengendapan mineral melebihi masukan kalsium baru ke laut. Pada tahun 1997, Skulan dan DePaolo mempresentasikan bukti pertama perubahan air laut 44Ca/40Ca selama waktu geologis, bersama dengan penjelasan teoretis tentang perubahan ini. Makalah yang lebih baru telah mengonfirmasi pengamatan ini, menunjukkan bahwa konsentrasi Ca2+ air laut tidaklah konstan, dan bahwa lautan tidak pernah dalam "keadaan stabil" sehubungan dengan masukan dan keluaran kalsium. Ini memiliki implikasi klimatologis yang penting, karena siklus kalsium laut terkait erat dengan siklus karbon.[46][47]
Banyak senyawa kalsium digunakan dalam makanan, sebagai obat-obatan, farmasi, dan lain-lain. Misalnya, kalsium dan fosforus ditambahkan dalam makanan melalui penambahan kalsium laktat, kalsium difosfat, dan trikalsium fosfat. Yang terakhir juga digunakan sebagai bahan pemoles pada pasta gigi dan antasid. Kalsium laktobionat adalah bubuk putih yang digunakan sebagai zat pensuspensi untuk obat-obatan. Dalam memanggang, kalsium fosfat digunakan sebagai bahan pengembang. Kalsium sulfit digunakan sebagai pemutih dalam pembuatan kertas dan sebagai disinfektan, kalsium silikat digunakan sebagai bahan penguat dalam karet, dan kalsium asetat adalah komponen rosin pengapuran dan digunakan untuk membuat sabun metalik dan resin sintetis.[42]
Kalsium masuk ke dalam Daftar Obat Esensial Organisasi Kesehatan Dunia.[48]
Sumber makanan[sunting | sunting sumber]
Beberapa makanan kaya kalsium adalah produk susu, seperti yoghurt dan keju, sarden, salmon, produk kedelai, kubis keriting, dan sereal sarapan yang difortifikasi.[6]
Karena kekhawatiran akan efek samping merugikan jangka panjang, termasuk kalsifikasi arteri dan batu ginjal, Institut Kedokteran AS (IOM) dan Otoritas Keamanan Makanan Eropa (EFSA) menetapkan Batas Atas Asupan yang Dapat Ditoleransi (UL) untuk kombinasi diet dan suplemen kalsium. Dari IOM, orang berusia 9–18 tahun tidak boleh melebihi asupan gabungan 3 g/hari; untuk usia 19–50, tidak melebihi 2,5 g/hari; untuk usia 51 tahun ke atas, tidak melebihi 2 g/hari.[49] EFSA menetapkan UL untuk semua orang dewasa sebesar 2,5 g/hari, tetapi memutuskan bahwa informasi untuk anak-anak dan remaja tidak cukup untuk menentukan UL.[50]
Susu dan produk susu[sunting | sunting sumber]

Susu merupakan minuman yang terkenal akan kandungan kalsium yang tinggi dan dapat membantu memperkuat tulang dan gigi, begitu pula dengan produk berbahan dasar susu. Satu cangkir susu, 200 gram yoghurt, atau 200 ml susu kedelai yang diperkaya kalsium mengandung sekitar 300 mg kalsium. Adapun susu khusus yang diperkaya kalsium dapat memberikan jumlah kalsium yang lebih besar dalam volume susu yang lebih kecil yakni mulai dari 280 mg hingga 400 mg per 200 ml susu.[51] Namun, kebanyakan masyarakat ras Afrika Amerika, Hispanik/Latin, dan Asia cenderung menderita intoleransi laktosa dibandingkan dengan orang keturunan Eropa.[52] Gangguan ini disebabkan ketidakmampuan tubuh untuk mencerna laktosa yang didapatkan dari susu maupun produk susu.[53] Sehingga berbagai produk susu dipilih untuk memenuhi kebutuhan kalsium bagi penderita intoleransi laktosa.
Pada 250 gram yoghurt, mengandung kalsium sebanyak 260 mg. Jumlah tersebut sudah dapat memenuhi sekitar 25% kebutuhan kalsium harian orang dewasa. Begitu pula dengan keju yang memiliki kandungan kalsium yang tinggi, adapun yang paling tinggi kandungannya yakni keju parmesan. Dalam 30 gram keju parmesan, terdapat sekitar 330 mg kalsium yang memenuhi 33% asupan kalsium harian orang dewasa.[54]
Biji-bijian[sunting | sunting sumber]
Biji-bijian merupakan sumber energi yang mengandung berbagai zat nutrisi kalsium yang tinggi, termasuk biji poppy, wijen, seledri, dan chia. Misalnya, 1 sendok makan (9 gram) biji poppy mengandung 127 mg kalsium atau 10% dari Nilai Harian, sementara biji wijen mengandung 7% kalsium yang direkomendasikan.[55]
Ikan[sunting | sunting sumber]
Ikan sarden dan salmon kalengan merupakan makanan dengan kadar kalsium yang tinggi karena tulangnya yang bisa dimakan. Satu kaleng sarden seberat 3,75 ons (92 gram) mengandung 27% dari kebutuhan kalsium, sementara salmon kaleng memiliki 19% [55]
Sayuran hijau[sunting | sunting sumber]

Bayam terkenal akan kandungan kalsium yang tinggi. Dalam 100 gram bayam mengandung 136 mg kalsium yakni 10% dari kebutuhan harian.[56] Selain bayam, brokoli memiliki kandungan kalsium yang tinggi yakni 62 mg per cangkir.[57] Pakcoy rebus juga merupakan salah satu sayuran hijau dengan kandungan kalsium 158 mg/cangkir.[58]
Kacang-kacangan[sunting | sunting sumber]
Berbagai jenis kacang-kacangan memiliki kandungan kalsium yang tinggi, seperti hazelnut, pistacio, dan walnut. Hazelnut memiliki kandungan kalsium sebanyak 279 mg/cangkir, sementara pistacio sebanyak 132 mg/cangkir, dan walnut mengandung 115 mg/cangkir kalsium.[59]
Peran biologis dan patologis[sunting | sunting sumber]
Kalsium merupakan mineral dalam tubuh dengan kebutuhan kandungan harian yang tidak terlalu banyak. Menurut Kementerian Kesehatan Indonesia, kebutuhan kalsium orang dewasa dalam satu hari sebesar 1100 mg. Sementara, anak-anak memerlukan antara 1000–1200 mg kalsium per hari.[60]
| Usia | Pria | Wanita | Ibu hamil | Ibu menyusui |
|---|---|---|---|---|
| 0−6 bulan | 200 | 200 | ||
| 7−12 bulan | 260 | 260 | ||
| 1−3 tahun | 700 | 700 | ||
| 4−8 tahun | 1000 | 1000 | ||
| 9−13 tahun | 1300 | 1300 | ||
| 14−18 tahun | 1300 | 1300 | 1300 | 1300 |
| 19−50 tahun | 1000 | 1000 | 1000 | 1000 |
| 51−70 tahun | 1000 | 1200 | ||
| >70+ tahun | 1200 | 1200 |
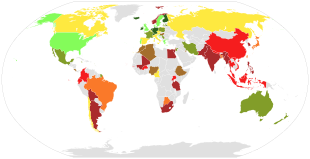
Fungsi[sunting | sunting sumber]
Kalsium merupakan unsur esensial yang dibutuhkan dalam jumlah banyak.[5][6] Ion Ca2+ bertindak sebagai elektrolit dan sangat penting untuk kesehatan otot, peredaran darah, dan sistem pencernaan; sangat diperlukan untuk pembangunan tulang; dan mendukung sintesis dan fungsi sel darah. Misalnya, ia mengatur kontraksi otot, konduksi saraf, dan pembekuan darah. Akibatnya, kadar kalsium intra- dan ekstraseluler diatur secara ketat oleh tubuh. Kalsium dapat memainkan peran ini karena ion Ca2+ membentuk kompleks koordinasi yang stabil dengan banyak senyawa organik, terutama protein; ia juga membentuk senyawa dengan berbagai kelarutan, memungkinkan pembentukan kerangka.[5] [63]
Pengikatan[sunting | sunting sumber]
Ion kalsium dapat dikomplekskan oleh protein melalui pengikatan residu gugus karboksil asam glutamat atau asam aspartat; melalui interaksi dengan residu serina, tirosina, atau treonina terfosforilasi; atau dengan dikelat oleh residu asam amino terkarboksilasi-γ. Tripsin, sebuah enzim pencernaan, menggunakan metode pertama; osteokalsin, sebuah protein matriks tulang, menggunakan yang ketiga.[64]
Beberapa protein matriks tulang lainnya seperti osteopontin dan sialoprotein tulang menggunakan yang pertama dan yang kedua. Aktivasi enzim langsung dengan mengikat kalsium adalah umum; beberapa enzim lain diaktifkan oleh asosiasi nonkovalen dengan enzim pengikat kalsium langsung. Kalsium juga mengikat lapisan fosfolipid membran sel, penahan protein yang terkait dengan permukaan sel.[64]
Kelarutan[sunting | sunting sumber]
Sebagai contoh kelarutan senyawa kalsium yang luas, monokalsium fosfat sangat larut dalam air, 85% kalsium ekstraseluler adalah sebagai dikalsium fosfat dengan kelarutan 2,0 mM dan hidroksiapatit tulang dalam matriks organik adalah trikalsium fosfat pada 100 μM.[64]
Nutrisi[sunting | sunting sumber]
Kalsium adalah konstituen umum suplemen makanan multivitamin,[5] tetapi komposisi kompleks kalsium dalam suplemen dapat mempengaruhi bioavailabilitasnya yang bervariasi menurut kelarutan garam yang terlibat: kalsium sitrat, malat, dan laktat sangat tersedia secara hayati, sedangkan oksalat lebih sedikit. Persiapan kalsium lainnya termasuk kalsium karbonat, kalsium sitrat malat, dan kalsium glukonat.[5] Usus menyerap sekitar sepertiga kalsium yang dimakan sebagai ion bebas, dan kadar kalsium plasma kemudian diatur oleh ginjal.[5]
Regulasi hormonal pembentukan tulang dan kadar serum[sunting | sunting sumber]
Hormon paratiroid dan vitamin D mendorong pembentukan tulang dengan memungkinkan dan meningkatkan pengendapan ion kalsium di sana, memungkinkan pergantian tulang yang cepat tanpa mempengaruhi massa tulang atau kandungan mineral.[5] Ketika kadar kalsium plasma turun, reseptor permukaan sel diaktifkan dan sekresi hormon paratiroid terjadi; ia kemudian melanjutkan untuk merangsang masuknya kalsium ke dalam kumpulan plasma dengan mengambilnya dari sel-sel ginjal, usus, dan tulang yang ditargetkan, dengan aksi hormon paratiroid pembentuk tulang diantagonis oleh kalsitonin, yang sekresinya meningkat dengan meningkatnya kadar kalsium plasma.[64]
Kadar serum abnormal[sunting | sunting sumber]
Kelebihan asupan kalsium dapat menyebabkan hiperkalsemia. Namun, karena kalsium diserap agak tidak efisien oleh usus, kalsium serum yang tinggi lebih mungkin disebabkan oleh sekresi hormon paratiroid (PTH) yang berlebihan atau mungkin karena asupan vitamin D yang berlebihan, yang keduanya memfasilitasi penyerapan kalsium. Semua kondisi ini menyebabkan kelebihan garam kalsium yang disimpan di jantung, pembuluh darah, atau ginjal. Gejalanya meliputi anoreksia, mual, muntah, kehilangan ingatan, kebingungan, pelemahan otot, buang air kecil meningkat, dehidrasi, dan penyakit tulang metabolik.[64]
Hiperkalsemia kronis biasanya menyebabkan kalsifikasi jaringan lunak dan konsekuensi seriusnya: misalnya, kalsifikasi dapat menyebabkan hilangnya elastisitas dinding pembuluh darah dan gangguan aliran darah laminar—dan kemudian menyebabkan ruptur plak dan trombosis. Sebaliknya, asupan kalsium atau vitamin D yang tidak memadai dapat menyebabkan hipokalsemia, sering juga disebabkan oleh sekresi hormon paratiroid yang tidak memadai atau reseptor PTH yang rusak dalam sel. Gejalanya meliputi rangsangan neuromuskuler, yang berpotensi menyebabkan tetani dan gangguan konduktivitas pada jaringan jantung.[64]
Penyakit tulang[sunting | sunting sumber]
Karena kalsium diperlukan untuk perkembangan tulang, banyak penyakit tulang dapat ditelusuri ke matriks organik atau hidroksiapatit dalam struktur molekul atau organisasi tulang. Osteoporosis adalah berkurangnya kandungan mineral tulang per satuan volume, dan dapat diobati dengan suplementasi kalsium, vitamin D, dan bisfosfonat.[5][6] Jumlah kalsium, vitamin D, atau fosfat yang tidak memadai dapat menyebabkan pelunakan tulang, yang disebut osteomalasia.[64]
Manfaat[sunting | sunting sumber]
Lingkungan[sunting | sunting sumber]
Senyawa kalsium karbonat akan mengikat partikel tanah dan mengubah sifat tanah, sehingga pori-pori tanah menjadi penuh yang dapat meningkatkan kekuatan dan kekakuan tanah. Kalsium menjadi bahan utama yang digunakan dalam teknik biosementasi. Kandungan kalsium dalam tanah juga berfungsi untuk mengoreksi sifat keasaman (pH) tanah, menetralisir kejenuhan zat-zat yang bersifat racun bagi tanah, meningkatkan efektivitas dan efisiensi penyerapan zat-zat hara, menjaga tingkat ketersediaan unsur hara mikro, memperbaiki porositas, struktur, serta aerasi tanah yang bermanfaat bagi mikrobiologi dan kimiawi tanah, sehingga tanah menjadi gembur, dan sirkulasi udara dalam tanah menjadi lancar.[65]
Tanaman[sunting | sunting sumber]
Kalsium dalam tanaman berperan dalam proses pertumbuhan, pembelahan, dan perpanjangan sel. Komponen ini dapat membantu menguatkan, mengatur daya tembus, dan serta merawat dinding sel. Selain itu, kalsium juga memiliki peran penting pada titik tumbuh akar. Apabila terjadi defisiensi Ca atau kekurangan kalsium, maka akan mengganggu proses pembentukan dan pertumbuhan akar sehingga berperngaruh terhadap terhambatnya penyerapan zat hara. Adapun berbagai gejala dapat timbul apabila terjadi defisit unsur kalsium, antara lain, melemahnya titik tumbuh dan terjadi perubahan bentuk daun menjadi keriting, mengecil, hingga rontok. Kalsium juga dapat menyebabkan tanaman tumbuh tinggi tetapi tidak kokoh hingga terhambatnya pembentukan bunga. Namun, kelebihan kalsium tidak berdampak banyak hanya mempengaruhi pH tanah.[66]
Hewan dan Manusia[sunting | sunting sumber]

Peran utama kalsium dalam tubuh adalah untuk memberikan struktur dan kekuatan pada kerangka. Dalam struktur eksoskeleton awal dan pada cangkang, sifat kaku struktural umumnya karena adanya kalsium karbonat. Pada vertebrata seperti reptil, ikan, mamalia, dan manusia, struktur kerangka terutama disusun oleh kalsium fosfat yang disebut kristal hidroksiapatit. Jenis kalsium fosfat ini ditemukan pula dalam kolagen. Ion kalsium pada permukaan tulang berikatan dengan ion dalam cairan tubuh, sehingga memungkinkan pertukaran ion yang penting dalam menjaga keseimbangan kalsium dalam darah dan tulang.[67]
Kalsium adalah mineral yang amat penting bagi manusia, antara lain bagi metabolisme tubuh, penghubung antar saraf, kerja jantung, dan pergerakan otot. Kalsium juga merupakan struktur yang banyak ditemui pada tulang, disebut juga sebagai bank kalsium. Hal ini berarti, apabila kalsium dalam darah menurun, maka tubuh akan mengambil cadangan dari tulang dengan bantuan beberapa hormon.[68]
Kalsium juga membantu mengatur kontraksi otot. Ketika saraf merangsang otot, tubuh akan melepaskan kalsium. Kalsium ini dapat membantu protein dalam otot melakukan kerja kontraksi. Sementara saat tubuh memompa kalsium keluar dari otot, otot akan kembali rileks.[69]
Selain itu, kalsium pun memainkan peran kunci dalam pembekuan darah. Proses pembekuan darah merupakan bagian yang kompleks dan memiliki berbagai langkah. Salah satu bagian prosesnya yakni melibatkan berbagai bahan kimia, termasuk kalsium.[69]
Berikut beberapa manfaat kalsium bagi manusia:
- Mengaktifkan saraf
- Melancarkan peredaran darah
- Melenturkan otot
- Menormalkan tekanan darah
- Menyeimbangkan tingkat keasaman darah
- Menjaga keseimbangan cairan tubuh
- Mencegah osteoporosis (keropos tulang)
- Mencegah penyakit jantung
- Menurunkan risiko kanker usus
- Mengatasi kram, sakit pinggang, wasir, dan reumatik
- Mengatasi keluhan saat haid dan menopause
- Meminimalkan penyusutan tulang selama hamil dan menyusui
- Membantu mineralisasi gigi dan mencegah pendarahan akar gigi
- Mengatasi kering dan pecah-pecah pada kulit kaki dan tangan
- Memulihkan gairah seks yang menurun/melemah
- Mengatasi kencing manis (mengaktifkan pankreas)
Setelah umur 20 tahun, tubuh manusia akan mulai mengalami kekurangan kalsium sebanyak 1% per tahun. Dan setelah umur 50 tahun, jumlah kandungan kalsium dalam tubuh akan menyusut sebanyak 30%. Kehilangan akan mencapai 50% ketika mencapai umur 70 tahun dan seterusnya mengalami masalah kekurangan kalsium.[70]
Gejala awal kekurangan kalsium adalah seperti lesu, banyak keringat, gelisah, sesak napas, menurunnya daya tahan tubuh, kurang nafsu makan, sembelit, berak-berak, insomnia, kram, dan sebagainya. Sementara kekurangan kalsium jangka panjang dapat menyebabkan detak jantung tidak teratur, osteopenia, osteoporosis, hipokalsemia, hingga peningkatan risiko patah tulang.[71]
Keamanan[sunting | sunting sumber]
Kalsium logam[sunting | sunting sumber]
| Bahaya | |
|---|---|
| Piktogram GHS | 
|
| Keterangan bahaya GHS | {{{value}}} |
| H261 | |
| P231+232 | |
Karena kalsium bereaksi secara eksotermik dengan air dan asam, logam kalsium yang bersentuhan dengan kelembapan tubuh menyebabkan iritasi korosif yang parah.[73] Saat tertelan, logam kalsium memiliki efek yang sama pada mulut, kerongkongan, dan lambung, dan dapat berakibat fatal.[43] Namun, paparan jangka panjang tidak diketahui memiliki efek samping yang berbeda.[73]
Referensi[sunting | sunting sumber]
- ^ (Indonesia) "Kalsium". KBBI Daring. Diakses tanggal 17 Juli 2022.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 112, ISBN 0-7506-3365-4
- ^ Krieck, Sven; Görls, Helmar; Westerhausen, Matthias (2010). "Mechanistic Elucidation of the Formation of the Inverse Ca(I) Sandwich Complex [(thf)3Ca(μ-C6H3-1,3,5-Ph3)Ca(thf)3] and Stability of Aryl-Substituted Phenylcalcium Complexes". Journal of the American Chemical Society. 132 (35): 12492–12501. doi:10.1021/ja105534w. PMID 20718434.
- ^ Weast, Robert (1984). CRC, Handbook of Chemistry and Physics. Boca Raton, Florida: Chemical Rubber Company Publishing. hlm. E110. ISBN 0-8493-0464-4.
- ^ a b c d e f g h i j "Calcium". Linus Pauling Institute, Oregon State University, Corvallis, Oregon. 1 September 2017. Diakses tanggal 24 Maret 2023.
- ^ a b c d "Calcium: Fact Sheet for Health Professionals". Office of Dietary Supplements, US National Institutes of Health. 9 Juli 2019. Diakses tanggal 24 Maret 2023.
- ^ a b c d Greenwood dan Earnshaw, hlm. 112–13
- ^ Parish, R. V. (1977). The Metallic Elements. London: Longman. hlm. 34. ISBN 978-0-582-44278-8.
- ^ Ropp, Richard C. (2012). Encyclopedia of the Alkaline Earth Compounds. hlm. 12–15. ISBN 978-0-444-59553-9.
- ^ a b c d Hluchan dan Pomerantz, hlm. 484
- ^ a b C. R. Hammond The elements (hlm. 4–35) dalam Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (edisi ke-86). Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
- ^ a b Hluchan dan Pomerantz, hlm. 483
- ^ Greenwood dan Earnshaw, hlm. 119
- ^ Greenwood dan Earnshaw, hlm. 121
- ^ Greenwood dan Earnshaw, hlm. 117
- ^ a b Greenwood dan Earnshaw, hlm. 122–15
- ^ Greenwood dan Earnshaw, hlm. 115
- ^ Harder, S.; Feil, F.; Knoll, K. (2001). "Novel Calcium Half-Sandwich Complexes for the Living and Stereoselective Polymerization of Styrene". Angew. Chem. Int. Ed. 40 (22): 4261–64. doi:10.1002/1521-3773(20011119)40:22<4261::AID-ANIE4261>3.0.CO;2-J. PMID 29712082.
- ^ Crimmin, Mark R.; Casely, Ian J.; Hill, Michael S. (2005). "Calcium-Mediated Intramolecular Hydroamination Catalysis". Journal of the American Chemical Society. 127 (7): 2042–43. doi:10.1021/ja043576n. PMID 15713071.
- ^ Jenter, Jelena; Köppe, Ralf; Roesky, Peter W. (2011). "2,5-Bis{N-(2,6-diisopropylphenyl)iminomethyl}pyrrolyl Complexes of the Heavy Alkaline Earth Metals: Synthesis, Structures, and Hydroamination Catalysis". Organometallics. 30 (6): 1404–13. doi:10.1021/om100937c.
- ^ Arrowsmith, Merle; Crimmin, Mark R.; Barrett, Anthony G. M.; Hill, Michael S.; Kociok-Köhn, Gabriele; Procopiou, Panayiotis A. (2011). "Cation Charge Density and Precatalyst Selection in Group 2-Catalyzed Aminoalkene Hydroamination". Organometallics. 30 (6): 1493–1506. doi:10.1021/om101063m.
- ^ Penafiel, J.; Maron, L.; Harder, S. (2014). "Early Main Group Metal Catalysis: How Important is the Metal?" (PDF). Angew. Chem. Int. Ed. 54 (1): 201–06. doi:10.1002/anie.201408814. PMID 25376952.
- ^ a b Greenwood dan Earnshaw, hlm. 136–37
- ^ a b Cameron, A. G. W. (1973). "Abundance of the Elements in the Solar System" (PDF). Space Science Reviews. 15 (1): 121–46. Bibcode:1973SSRv...15..121C. doi:10.1007/BF00172440.
- ^ a b c Clayton, Donald (2003). Handbook of Isotopes in the Cosmos: Hydrogen to Gallium. Cambridge University Press. hlm. 184–98. ISBN 9780521530835.
- ^ a b c Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). "The NUBASE2016 evaluation of nuclear properties" (PDF). Chinese Physics C. 41 (3): 030001. Bibcode:2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Arnold, R.; et al. (NEMO-3 Collaboration) (2016). "Measurement of the double-beta decay half-life and search for the neutrinoless double-beta decay of 48Ca with the NEMO-3 detector". Physical Review D. 93 (11): 112008. arXiv:1604.01710
 . Bibcode:2016PhRvD..93k2008A. doi:10.1103/PhysRevD.93.112008.
. Bibcode:2016PhRvD..93k2008A. doi:10.1103/PhysRevD.93.112008.
- ^ Russell, W. A.; Papanastassiou, D. A.; Tombrello, T. A. (1978). "Ca isotope fractionation on the earth and other solar system materials". Geochim Cosmochim Acta. 42 (8): 1075–90. Bibcode:1978GeCoA..42.1075R. doi:10.1016/0016-7037(78)90105-9.
- ^ Skulan, J.; Depaolo, D. J. (1999). "Calcium isotope fractionation between soft and mineralized tissues as a monitor of calcium use in vertebrates". Proc Natl Acad Sci USA. 96 (24): 13709–13. Bibcode:1999PNAS...9613709S. doi:10.1073/pnas.96.24.13709
 . PMC 24129
. PMC 24129  . PMID 10570137.
. PMID 10570137.
- ^ a b c d e Greenwood dan Earnshaw, hlm. 108
- ^ Miller, M. Michael. "Commodity report:Lime" (PDF). USGS. Diakses tanggal 24 Maret 2023.
- ^ Garfinkel, Yosef (1987). "Burnt Lime Products and Social Implications in the Pre-Pottery Neolithic B Villages of the Near East". Paléorient. 13 (1): 69–76. doi:10.3406/paleo.1987.4417. JSTOR 41492234.
- ^ Williams, Richard (2004). Lime Kilns and Lime Burning. hlm. 4. ISBN 978-0-7478-0596-0.[pranala nonaktif permanen]
- ^ Oates, J. A. H (2008). Lime and Limestone: Chemistry and Technology, Production and Uses. ISBN 978-3-527-61201-7.
- ^ a b Weeks, Mary Elvira; Leichester, Henry M. (1968). Discovery of the Elements. Easton, PA: Journal of Chemical Education. hlm. 505–10. ISBN 978-0-7661-3872-8. LCCN 68-15217.
- ^ Lavoisier, Antoine Laurent (1965). Elements of chemistry. unknown library. update forthcoming.
- ^ Davy, H. (1808). "Electro-chemical researches on the decomposition of the earths; with observations on the metals obtained from the alkaline earths, and on the amalgam procured from ammonia". Philosophical Transactions of the Royal Society of London. 98: 333–70. Bibcode:1808RSPT...98..333D. doi:10.1098/rstl.1808.0023
 .
.
- ^ a b c Greenwood dan Earnshaw, hlm. 110
- ^ a b Berner, Robert (2003). "The long-term carbon cycle, fossil fuels and atmospheric composition". Nature. 426 (6964): 323–26. Bibcode:2003Natur.426..323B. doi:10.1038/nature02131. PMID 14628061.
- ^ Zeebe (2006). "Marine carbonate chemistry". National Council for Science and the Environment. Diakses tanggal 24 Maret 2023.
- ^ Walker, James C. G.; Hays, P. B.; Kasting, J. F. (20 Oktober 1981). "A negative feedback mechanism for the long-term stabilization of Earth's surface temperature". Journal of Geophysical Research: Oceans (dalam bahasa Inggris). 86 (C10): 9776–82. Bibcode:1981JGR....86.9776W. doi:10.1029/JC086iC10p09776. ISSN 2156-2202.
- ^ a b c Hluchan dan Pomerantz, hlm. 485–87
- ^ a b Rumack BH. POISINDEX. Information System Micromedex, Inc., Englewood, CO, 2010; CCIS Volume 143. Hall AH and Rumack BH (Eds)
- ^ Skulan, J.; Depaolo, D. J.; Owens, T. L. (June 1997). "Biological control of calcium isotopic abundances in the global calcium cycle". Geochimica et Cosmochimica Acta. 61 (12): 2505–10. Bibcode:1997GeCoA..61.2505S. doi:10.1016/S0016-7037(97)00047-1.
- ^ a b Skulan, J.; Bullen, T.; Anbar, A. D.; Puzas, J. E.; Shackelford, L.; Leblanc, A.; Smith, S. M. (2007). "Natural calcium isotopic composition of urine as a marker of bone mineral balance". Clinical Chemistry. 53 (6): 1155–58. doi:10.1373/clinchem.2006.080143
 . PMID 17463176.
. PMID 17463176.
- ^ Fantle, M.; Depaolo, D. (2007). "Ca isotopes in carbonate sediment and pore fluid from ODP Site 807A: The Ca2+(aq)–calcite equilibrium fractionation factor and calcite recrystallization rates in Pleistocene sediments". Geochim Cosmochim Acta. 71 (10): 2524–46. Bibcode:2007GeCoA..71.2524F. doi:10.1016/j.gca.2007.03.006.
- ^ Griffith, Elizabeth M.; Paytan, Adina; Caldeira, Ken; Bullen, Thomas; Thomas, Ellen (2008). "A Dynamic marine calcium cycle during the past 28 million years". Science. 322 (12): 1671–74. Bibcode:2008Sci...322.1671G. doi:10.1126/science.1163614. PMID 19074345.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Jenewa: World Health Organization. hdl:10665/325771
 . WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Institute of Medicine (US) Committee to Review Dietary Reference Intakes for Vitamin D Calcium; Ross, A. C.; Taylor, C. L.; Yaktine, A. L.; Del Valle, H. B. (2011). "ch 6. Tolerable Upper Intake Levels". Dietary Reference Intakes for Calcium and Vitamin D. Washington, D.C: National Academies Press. hlm. 403–56. doi:10.17226/13050. ISBN 978-0-309-16394-1. PMID 21796828.
- ^ Tolerable Upper Intake Levels For Vitamins And Minerals (PDF), European Food Safety Authority, 2006
- ^ Departement of Health Victoria State Government (2021). "Calcium - Better Health Channel". www.betterhealth.vic.gov.au. Diakses tanggal 24 Maret 2023.
- ^ Isella, Virly (2021). "Epidemiologi Intoleransi Laktosa". Alomedika. Diakses tanggal 24 Maret 2023.
- ^ Pathak, Neha (2021). "Lactose Intolerance - Cause, Symptoms, Diagnosis, Treatment". WebMD (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Adrian, Kevin (2021). "Kenali Jenis-Jenis Makanan Berkalsium Tinggi". Alodokter. Diakses tanggal 24 Maret 2023.
- ^ a b Jennings, Kerri-Ann (2021). "Top 15 Calcium-Rich Foods (Many Are Nondairy)". Healthline (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Whitbread, Daisy (2021). "Top 10 Foods Highest in Calcium". myfooddata (dalam bahasa english). Diakses tanggal 24 Maret 2023.
- ^ Physicians Committee (2021). "Calcium and Strong Bones". Physicians Committee for Responsible Medicine (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Adzani, Fadli (2020). "8 Manfaat Pakcoy, Sayuran Hijau yang Baik untuk Kesehatan". SehatQ. Diakses tanggal 24 Maret 2023.
- ^ Souper Sage (2020). "Top Nuts High in Calcium". Soupersage (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Tony (2018). "Apakah Kebutuhan Kalsium Bisa Dipenuhi Hanya dari Segelas Susu? - RS Khusus Bedah Halimun Medical Center". RSKB Halimun. Diakses tanggal 24 Maret 2023.
- ^ National Institutes of Health (2021). "Calcium". National Institutes of Health Office of Dietary Supplements. Diakses tanggal 2022-1-30.
- ^ Balk EM, Adam GP, Langberg VN, Earley A, Clark P, Ebeling PR, Mithal A, Rizzoli R, Zerbini CA, Pierroz DD, Dawson-Hughes B (Desember 2017). "Global dietary calcium intake among adults: a systematic review". Osteoporosis International. 28 (12): 3315–24. doi:10.1007/s00198-017-4230-x. PMC 5684325
 . PMID 29026938.
. PMID 29026938.
- ^ Sosa Torres, Martha; Kroneck, Peter M.H; "Introduction: From Rocks to Living Cells" hlm. 1–32 dalam "Metals, Microbes and Minerals: The Biogeochemical Side of Life" (2021) hlm. xiv + 341. Walter de Gruyter, Berlin. Penyunting Kroneck, Peter M.H. dan Sosa Torres, Martha. DOI:10.1515/9783110589771-001
- ^ a b c d e f g Hluchan dan Pomerantz, hlm. 489–94
- ^ Triana, Ajeng; Hidayah; Ridlo; Ambarsari (2018). "PENGARUH KALSIUM TERHADAP pH TANAH DALAM PROSES BIOSEMENTASI" (PDF). Prosiding Seminar Nasional dan Konsultasi Teknologi Lingkungan: 189–190. Diarsipkan dari versi asli (PDF) tanggal 28 Januari 2022. Diakses tanggal 24 Maret 2023.
- ^ Mukhlis (2017). "Unsur Hara Makro dan Mikro yang dibutuhkan oleh Tanaman". dtphp.luwuutarakab.go.id (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ a b Mandal, Ananya (2019). "Uses of Calcium". News-Medical.net (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Shita, Amandia Dewi Permana; Sulistyani, Sulistyani (16 Desember 2015). "PENGARUH KALSIUM TERHADAP TUMBUH KEMBANG GIGI GELIGI ANAK". STOMATOGNATIC - Jurnal Kedokteran Gigi (dalam bahasa Inggris). 7 (3): 41. ISSN 2442-4935.
- ^ a b Newman, Tim (2020). "Calcium: Health benefits, foods, and deficiency". www.medicalnewstoday.com (dalam bahasa Inggris). Diakses tanggal 24 Maret 2023.
- ^ Maryusman, Taufik (2017). "Kalsium Pada Tubuh Manusia - Fakultas Ilmu Kesehatan - Universitas Pembangunan Nasional Veteran Jakarta". fikes.upnvj.ac.id. Diakses tanggal 24 Maret 2023.
- ^ Firdaus, A. (2021). Firdaus, A., ed. "Tanda dan Gejala Awal Kekurangan Kalsium pada Tubuh". Medcom.id. Diakses tanggal 24 Maret 2023.
- ^ "Calcium turnings, 99% trace metals basis". Sigma-Aldrich. 24 Februari 2021. Diakses tanggal 24 Maret 2023.
- ^ a b Hluchan dan Pomerantz, hlm. 487–89
Bibliografi[sunting | sunting sumber]
- Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- Hluchan, Stephen E.; Pomerantz, Kenneth (2005), "Calcium and Calcium Alloys", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a04_515.pub2
Pranala luar[sunting | sunting sumber]
- (Inggris) The Calcium Information Resource
| (besar) | |||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
|
| |||||||||||||||||||||||||||||||||


