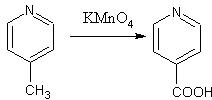Kalium permanganat

| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Kalium manganat(VII)
| |
| Nama lain
Kalium permanganat
Chameleon's mineral Kristal Condy Permanganate of potash Hipermangan | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 1490 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| KMnO4 | |
| Massa molar | 158.034 g/mol |
| Penampilan | jarum abu-perunggu-keunguan magenta–rose dalam larutan |
| Bau | tak berbau |
| Densitas | 2.703 g/cm3 |
| Titik lebur | 240 °C (464 °F; 513 K) (terdekomposisi) |
| 6.4 g/100mL (20 °C) 250 g/L (65 °C) | |
| Kelarutan | terdekomposisi dalam alkohol dan pelarut organik |
| +20.0·10−6 cm3/mol | |
| Indeks bias (nD) | 1.59 |
| Struktur | |
| Ortorombik | |
| Termokimia | |
| Kapasitas kalor (C) | 119.2 J/mol K |
| Entropi molar standar (S |
171.7 J K−1 mol−1 |
| Entalpi pembentukan standar (ΔfH |
−813.4 kJ/mol |
| Energi bebas Gibbs (ΔfG) | -713.8 kJ/mol |
| Farmakologi | |
| Kode ATC | D08 V03AB18 |
| Bahaya | |
Klasifikasi UE (DSD) (usang)
|
|
| Frasa-R | R8, R22, R50/53 |
| Frasa-S | S2, S60, S61 |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
1090 mg/kg (oral, tikus)[1] |
| Senyawa terkait | |
Anion lain
|
Kalium manganit Kalium manganat |
Kation lainnya
|
Natrium permanganat Amonium permanganat |
Senyawa terkait
|
Mangan heptoksida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Kalium permanganat adalah suatu senyawa kimia anorganik dan obat-obatan. Sebagai obat senyawa ini digunakan untuk membersihkan luka dan dermatitis.[2]
Senyawa ini memiliki rumus kimia KMnO4 dan merupakan garam yang mengandung ion K+ dan MnO−4. Senyawa ini merupakan agen pengoksidasi kuat. Ia larut dalam air menghasilkan larutan berwarna merah muda atau ungu yang intens, penguapan larutan ini meninggalkan kristal prismatik berwarna keunguan-hitam.[3] Pada tahun 2000, produksi di seluruh dunia diperkirakan mencapai 30,000 ton.[4] Dalam senyawa ini, mangan memiliki bilangan oksidasi +7.
Senyawa ini termasuk dalam Model Daftar Obat Esensial WHO, obat yang paling penting dibutuhkan dalam sistem kesehatan dasar.[5] Biaya grosir di dunia berkembang adalah sekitar 0.01 USD per g.[6] Di Britania Raya jumlah tersebut membiayai NHS sekitar 1.33 pounds.[2]
Struktur[sunting | sunting sumber]
KMnO4 membentuk kristal ortorombik dengan konstanta: a = 910.5 pm, b = 572.0 pm, c = 742.5 pm. Motif keseluruhan hampir serupa dengan barium sulfat, yang karenanya membentuk larutan padat.[7] Dalam padatan (seperti pada larutan), masing-masing pusat MnO4− adalah tetrahedral. Jarak Mn–O adalah 1.62 Å.[8]
Preparasi[sunting | sunting sumber]
Kalium permanganat diproduksi secara industri dari mangan dioksida, yang juga hadir sebagai mineral pirolusit. MnO2 melebur dengan kalium hidroksida dan dipanaskan dalam udara atau dengan sumber lain dari oksigen, seperti kalium nitrat atau kalium klorat.[4] Tahapan ini menghasilkan kalium manganat:
- 2 MnO2 + 4 KOH + O2 → 2 K2MnO4 + 2 H2O
(Dengan natrium hidroksida, produk akhir bukanlah natrium manganat tapi senyawa Mn(V), yang merupakan salah satu alasan kalium permanganat lebih sering digunakan daripada natrium permanganat. Lebih jauh, garam kalium mengkristal lebih baik.[4])
Kalium manganat kemudian diubah menjadi permanganat melalui oksidasi elektrolit dalam media basa:
- 2 K2MnO4 + 2 H2O → 2 KMnO4 + 2 KOH + H2
Metode lain[sunting | sunting sumber]
Walaupun tidak penting secara komersial, kalium manganat dapat dioksidasi melalui klorin atau dengan disproporsionasi di bawah kondisi asam.[9] Reaksi oksidasi klorin adalah
- 2 K2MnO4 + Cl2 → 2 KMnO4 + 2 KCl
Dan reaksi disproporsionasi yang diinduksi-asam dapat ditulis sebagai
- 3 K2MnO4 + 4 HCl → 2 KMnO4 + MnO2 + 2 H2O + 4 KCl
Suatu asam lemah seperti asam karbonat cukup untuk reaksi ini:
- 3 K2MnO4 + 2 CO2 → 2 KMnO4 + 2 K2CO3 + MnO2
Kalium permanganat mengkristal dari larutan reaksi pekat.
Garam permanganat juga dapat dihasilkan dengan memperlakukan larutan ion Mn2+ dengan oksidan kuat seperti timbal dioksida (PbO2), natrium bismutat (NaBiO3), atau peroksidisulfat. Pengujian untuk kehadiran mangan memanfaatkan warna lembayung jelas dari permanganat yang dihasilkan oleh pereaksi tersebut.
Penggunaan[sunting | sunting sumber]
Hampir semua aplikasi kalium permanganat memanfaatkan sifat mengoksidasinya.[4] Sebagai oksidan kuat yang tidak menghasilkan produk samping yang beracun, KMnO4 memiliki banyak kegunaan.
Antiseptik[sunting | sunting sumber]
Sebagai oksidan, kalium permanganat dapat bertindak sebagai antiseptik. Misalnya, larutan encer senyawa ini digunakan untuk mengobati sariawan (radang), desinfektan untuk tangan dan pengobatan untuk pomfoliks, dermatitis,[10][11] dan infeksi jamur pada tangan atau kaki yang sifatnya ringan.[12]
Pengolahan air[sunting | sunting sumber]
Kalium permanganat digunakan secara luas dalam industri pengolahan air. Hal ini digunakan sebagai bahan kimia regenerasi untuk menghilangkan besi dan hidrogen sulfida (bau telur busuk) dari air sumur melalui Filter "Manganese Greensand". "Pot-Perm" juga dapat diperoleh di toko peralatan kolam dan digunakan sebagai tambahan untuk menangani air limbah. Dalam sejarahnya ia digunakan untuk mensterilkan air minum.[13][14] Saat ini senyawa ini menemukan penerapannya dalam pengendalian organisme pengganggu seperti kerang zebra dalam pengumpulan dan pengolahan sistem air tawar.[15]
Sintesis senyawa organik[sunting | sunting sumber]

Selain penggunaannya dalam pengolahan air, aplikasi utama lainnya dari KMnO4 adalah sebagai pereaksi untuk sintesis senyawa organik.[16] Jumlah yang signifikan diperlukan untuk sintesis asam askorbat, kloramfenikol, sakarin, asam isonikotinat, dan asam pirazinoat.[4]
Penggunaan analisis[sunting | sunting sumber]
Kalium permanganat dapat digunakan untuk secara kuantitatif menentukan bahan organik keseluruhan yang dapat teroksidasi dalam sampel air. Nilai yang telah ditentukan dikenal sebagai nilai permanganat. Dalam kimia analitik, larutan standar dari KMnO4 terkadang digunakan sebagai titran pengoksidasi untuk titrasi redoks (Permanganometri). Dalam cara yang terkait, ia digunakan sebagai pereaksi untuk menentukan bilangan Kappa dari pulp kayu. Untuk standardisasi larutan KMnO4, reduksi dengan asam oksalat sering digunakan.[17]
Larutan asam berair dari KMnO4 digunakan untuk mengumpulkan gas merkuri dalam gas buang selama uji emisi sumber stasioner.[18]
Dalam histologi, kalium permanganat digunakan sebagai agen pemutih.[19][20]
Penggunaan lain[sunting | sunting sumber]
Kalium permanganat merupakan salah satu bahan kimia utama yang digunakan dalam film dan televisi industri untuk membuat kostum dan properti yang digunakan menjadi "berumur". Konversinya yang mudah menjadi MnO2 berwarna cokelat membuat tampilan "kuno" atau "seratus tahun" pada kain goni, tali, kayu, dan kaca.[21]
Kalium permanganat telah digunakan dalam upaya untuk menginduksi aborsi di rumah. Insiden ini hanya mengakibatkan kerusakan vagina dari tindakan korosif bahan kimia tersebut, karena kalium permanganat terbukti tidak efektif dalam menghasilkan aborsi. FDA meningkatkan pembatasan hukum tentang bahan kimia tersebut dalam menanggapi penggunaannya sebagai abortifasien.[22]
Keamanan dan penanganan[sunting | sunting sumber]
Sebagai oksidator yang menghasilkan produk cokelat gelap MnO2, kalium permanganat dengan cepat mengotori hampir semua bahan organik seperti kulit, kertas, dan pakaian. Padatan KMnO4 adalah oksidator kuat, sehingga harus disimpan terpisah dari bahan yang dapat teroksidasi seperti kulit, kertas, dan pakaian. Reaksi dengan asam sulfat pekat menghasilkan mangan(VII) oksida (Mn2O7) yang sangat eksplosif. Ketika dalam bentuk padat, KMnO4 dicampurkan dengan gliserol murni atau alkohol sederhana lainnya akan menghasilkan reaksi pembakaran yang sangat keras.[23][24][25]
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ ChemIDplus - 7722-64-7 - VZJVWSHVAAUDKD-UHFFFAOYSA-N - Potassium permanganate [USP:JAN] - Similar structures search, synonyms, formulas, resource links, and other chemical...
- ^ a b British national formulary : BNF 69 (edisi ke-69). British Medical Association. 2015. hlm. 840. ISBN 9780857111562.
- ^ Burriel, F.; Lucena, F.; Arribas, S. and Hernández, J. (1985), Química Analítica Cualitativa, p. 688, ISBN 84-9732-140-5.
- ^ a b c d e Reidies, Arno H. (2002) "Manganese Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim. doi:10.1002/14356007.a16_123
- ^ "19th WHO Model List of Essential Medicines (April 2015)" (PDF). WHO. April 2015. Diakses tanggal 10 Mei 2015.
- ^ "Potassium Permanganate". International Drug Price Indicator Guide. Diakses tanggal 8 Desember 2016.[pranala nonaktif permanen]
- ^ "Handbook of Preparative Inorganic Chemistry" Brauer, E., Ed.; Academic: New York, 1963.
- ^ Palenik, Gus J. (1967). "Crystal structure of potassium permanganate". Inorg. Chem. 6 (3): 503–507. doi:10.1021/ic50049a015.
- ^ Walton, H. F. (1948) Inorganic Preparations. New York.
- ^ BIRT AR (March 1964). "Drugs for eczema of children". Can Med Assoc J. 90 (11): 693–4. PMC 1922428
 . PMID 14127384.
. PMID 14127384.
- ^ Stalder JF, Fleury M, Sourisse M, Allavoine T, Chalamet C, Brosset P, Litoux P (1992). "Comparative effects of two topical antiseptics (chlorhexidine vs KMnO4) on bacterial skin flora in atopic dermatitis". Acta Derm Venereol Suppl (Stockh). 176: 132–4. PMID 1476027.
- ^ Program for Appropriate Technology in Health PATH (1988). "Skin diseases". Health Technol Dir. 8 (3): 1–10. PMID 12282068.
- ^ Assembly of Life Sciences (U.S.). Safe Drinking Water Committee (1977). Drinking water and health, Volume 2. National Academies Press. hlm. 98. ISBN 978-0-309-02931-5. Diakses tanggal 2016-09-13.
- ^ Downey, Robyn and Barrington, Mike (28 February 2005) "Red faces over pink water", The Northern Advocate.
- ^ EPA Guidance Manual Alternative Disinfectants and Oxidants. epa.gov
- ^ Fatiadi, A. (1987). "The Classical Permanganate Ion: Still a Novel Oxidant in Organic Chemistry". Synthesis. 1987 (2): 85–127. doi:10.1055/s-1987-27859.
- ^ Kovacs KA, Grof P, Burai L, Riedel M (2004). "Revising the Mechanism of the Permanganate/Oxalate Reaction". J. Phys. Chem. A. 108 (50): 11026. doi:10.1021/jp047061u.
- ^ Code of Federal Regulations(7-1-07) Edition, Title 40, Part 60, Appendix A-8, Method 29, Section 7.3.1
- ^ Picken, MM. (Apr 2010). "Amyloidosis-where are we now and where are we heading?". Arch Pathol Lab Med. 134 (4): 545–51. doi:10.1043/1543-2165-134.4.545. PMID 20367306.
- ^ Murphy CL, Eulitz M, Hrncic R, Sletten K, Westermark P, Williams T, Macy SD, Wooliver C, Wall J, Weiss DT, Solomon A (2001). "Chemical typing of amyloid protein contained in formalin-fixed paraffin-embedded biopsy specimens". Am. J. Clin. Pathol. 116 (1): 135–42. doi:10.1309/TWBM-8L4E-VK22-FRH5. PMID 11447744.
- ^ Brody, Ester (February 2000). "Victor DeLor contractor profile". PaintPRO. 2 (1). Diakses tanggal 2009-11-12.
One of the techniques DeLor is known for among designers and clients is the special effects he creates with various chemical solutions. When applied to wood surfaces, these chemicals give a weathered appearance to new wood. ... To achieve the aesthetic on interior surfaces, DeLor often uses a mixture of water and potassium permanganate, a dry powder chemical.
- ^ "CFR - Code of Federal Regulations Title 21". U.S. Food and Drug Administration. U.S. Department of Health & Human Services. Diakses tanggal 1 April 2015.
- ^ "Glycerol and KMnO4 - UW Dept. of Chemistry". Diarsipkan dari versi asli tanggal 2019-12-16. Diakses tanggal 2017-03-02.
- ^ http://web.nmsu.edu/~susanbro/sc2/docs/chemical_demos.pdf#page=1
- ^ Spontaneous Combustion Is Easier Than You Think | Popular Science
Pranala luar[sunting | sunting sumber]
- International Chemical Safety Card 0672
- National Pollutant Inventory: Manganese and compounds Fact Sheet
- The use of potassium permanganate in fish ponds
- Sugar, NaOH and KMnO4 Diarsipkan 2011-07-16 di Wayback Machine.