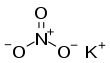Kalium nitrat

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Kalium nitrat
| |||
| Nama lain | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| KEGG | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 1486 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| KNO3 | |||
| Massa molar | 101,1032 g/mol | ||
| Penampilan | padatan putih | ||
| Bau | tak berbau | ||
| Densitas | 2,109 g/cm3 (16 °C) | ||
| Titik lebur | 334 °C (633 °F; 607 K) | ||
| Titik didih | 400 °C (752 °F; 673 K) (decomposes) | ||
| 133 g/L (0 °C) 316 g/L (20 °C) 383 g/L (25 °C) 2.439 g/L (100 °C)[4] | |||
| Kelarutan | agak larut dalam etanol larut dalam gliserol, amonia | ||
| Kebasaan (pKb) | 15,3[5] | ||
| −33.7·10−6 cm3/mol | |||
| Indeks bias (nD) | 1,335; 1,5056; 1,5604 | ||
| Struktur | |||
| Ortorombik, Aragonit | |||
| Termokimia | |||
| Kapasitas kalor (C) | 95,06 J/mol K | ||
| Entalpi pembentukan standar (ΔfH |
-494,00 kJ/mol | ||
| Bahaya | |||
| Bahaya utama | Oksidator, berbahaya jika tertelan, terhirup, atau terserap kulit. Menyebabkan iritasi pada kulit dan mata. | ||
| Lembar data keselamatan | ICSC 0184 | ||
| Piktogram GHS |  
| ||
| H272, H315, H319, H335 | |||
| P102, P210, P220, P221, P280 | |||
| Titik nyala | tidak mudah terbakar (pengoksidasi) | ||
| Dosis atau konsentrasi letal (LD, LC): | |||
LD50 (dosis median)
|
1.901 mg/kg (oral, kelinci) 3.750 mg/kg (oral, tikus)[6] | ||
| Senyawa terkait | |||
Anion lain
|
Kalium nitrit | ||
Kation lainnya
|
Litium nitrat Natrium nitrat Rubidium nitrat Sesium nitrat | ||
Senyawa terkait
|
Kalium sulfat Kalium klorida | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Kalium nitrat (disebut juga sendawa[2][catatan 1] atau salpeter[3]) adalah senyawa kimia dengan rumus kimia KNO3. Ia termasuk senyawa ionik yang terdiri dari ion kalium K+ dan ion nitrat NO−3. Ia menjadi salah satu sumber nitrogen.
Kalium nitrat banyak digunakan dalam pupuk, penghilangan tunggul pohon, propelan roket, dan kembang api. Ia menjadi bahan utama dalam pembuatan bubuk mesiu (bubuk hitam).[7] Dalam daging olahan, kalium nitrat bereaksi dengan hemoglobin dan mioglobin yang kemudian menghasilkan warna merah muda.[8]
Deskripsi[sunting | sunting sumber]
Kalium nitrat merupakan komponen bubuk mesiu teroksidasi (disuplai oksigen). Sebelum fiksasi industri nitrogen skala besar (proses Haber), sumber utama kalium nitrat adalah deposit yang mengkristal dari dinding gua atau mengalirkan bahan organik yang membusuk. Tumpukan kotoran juga sumber umum yang utama: amonia dari dekomposisi urea dan zat nitrogen lainnya akan melalui oksidasi bakteri untuk memproduksi nitrat.
Sifat-sifat[sunting | sunting sumber]
Kalium nitrat memiliki kristal ortorombik pada suhu ruang dan berubah menjadi sistem trigonal pada suhu 129 °C.
Kalium nitrat agak mudah larut dalam air, tetapi semakin mudah larut seiring kenaikan suhu. Larutannya hampir netral dengan pH 6,2 pada suhu 14 °C untuk 10% bubuk komersial. Ia tidak higroskopis karena hanya menyerap 0,08% air dalam kelembapan relatif 80% selama lebih dari 50 hari. Ia tidak larut dalam alkohol dan tidak beracun. Ia dapat meledak bila bereaksi dengan reduktor, tetapi tidak mudah meledak dengan sendirinya.[4]
Dekomposisi termal[sunting | sunting sumber]
Antara 550–790 °C, kalium nitrat mencapai sebuah ekuilibrium yang bergantung pada suhu dengan kalium nitrit:[9]
- 2 KNO3
 2 KNO2 + O2
2 KNO2 + O2
Produksi[sunting | sunting sumber]
Kalium nitrat dapat dibuat dengan menggabungkan amonium nitrat dan kalium hidroksida.
- NH4NO3 (aq) + KOH (aq) → NH3 (g) + KNO3 (aq) + H2O (l)
Cara lain yang tidak menghasilkan produk samping amonia adalah dengan menggabungkan amonium nitrat dengan kalium klorida.
- NH4NO3 (aq) + KCl (aq) → NH4Cl (aq) + KNO3 (aq)
Kalium nitrat juga dapat diproduksi dengan menetralkan asam nitrat dengan kalium hidroksida. Reaksi ini sangat eksotermis.
- KOH (aq) + HNO3 → KNO3 (aq) + H2O (l)
Sejarah produksi[sunting | sunting sumber]
Secara historis, nitre-beds tersedia dengan mencampurkan rabuk dengan adukan semen ataupun abu kayu, bahan tanah, dan bahan organik yang umum seperti jerami untuk memberikan porositas pada tumpukan kompos yang secara umum setinggi 1,5 m, selebar 2 m, dan sepanjang 5 m.[10] Timbunannya biasanya ditutupi dari hujan dan dibiarkan lembab oleh urin yang ternyata mempercepat dekomposisi. Setelah kurang lebih setahun, hasilnya dikenai pelindian dengan air untuk menghilangkan kalsium nitrat yang mudah larut dengan air, kemudian diubah menjadi kalium nitrat dengan garam abu.
Di Inggris, hak pengolahan bahan peledak telah ada di tangan keluarga John Evelyn, diaris ternama, sebagai monopoli puncak sejak sebelum 1588.[butuh rujukan]
Kegunaan[sunting | sunting sumber]
Kalium nitrat dipakai dalam produksi asam nitrat, yaitu dengan menambahkan asam sulfat yang terkonsentrasi pada larutan encer kalium nitrat sehingga menghasilkan asam nitrat dan kalium sulfat yang terpisah melalui distilasi fraksional. Namun, saat ini, yang terjadi adalah sebaliknya: nitrat diproduksi dari asam nitrat melalui proses Ostwald.
Kalium nitrat juga digunakan sebagai pupuk dan sebagai propelan roket.
Kesalahan konsepsi terkenal ialah bahwa kalium nitrat itu antafrodisiak dan ditambahkan dalam makanan dalam adat yang biasa dikerjakan lelaki. Nyatanya kalium nitrat tak memiliki efek seperti itu pada manusia.[11]
Kini, penggunaan kalium nitrat dalam pasta gigi untuk gigi sensitif telah bertambah secara dramatis walau nyatanya telah tak ditampakkan untuk membantu dengan sebenarnya hipersensitivitas gigi.[12]
Lihat pula[sunting | sunting sumber]
Catatan kaki[sunting | sunting sumber]
- ^ Istilah sendawa juga sering dipakai oleh masyarakat sebagai 'peristiwa keluarnya gas dari dalam perut' walau istilah yang baku untuk itu ialah serdawa.
Referensi[sunting | sunting sumber]
- ^ Record of Potassium nitrate dalam GESTIS Substance Database dari IFA, diakses tanggal 9 Maret 2007
- ^ a b Badan Pengembangan dan Pembinaan Bahasa. "Sendawa - KBBI Daring". Kementerian Pendidikan dan Kebudayaan Republik Indonesia.
- ^ a b Badan Pengembangan dan Pembinaan Bahasa. "Salpeter - KBBI Daring". Kementerian Pendidikan dan Kebudayaan Republik Indonesia.
- ^ a b B. J. Kosanke; B. Sturman; K. Kosanke; I. von Maltitz; T. Shimizu; M. A. Wilson; N. Kubota; C. Jennings-White; D. Chapman (2004). "2". Pyrotechnic Chemistry. Journal of Pyrotechnics. hlm. 5–6. ISBN 978-1-8895-2615-7. Diarsipkan dari versi asli tanggal 5 Mei 2016.
- ^ Kolthoff (1959). Treatise on Analytical Chemistry. New York: Interscience Encyclopedia, Inc.
- ^ "ChemIDplus - 7757-79-1". Diarsipkan dari versi asli tanggal 12 Agustus 2014.
- ^ Lauer, Klaus (1991). "The history of nitrite in human nutrition: A contribution from German cookery books". Journal of Clinical Epidemiology. 44 (3): 261–264. doi:10.1016/0895-4356(91)90037-a. ISSN 0895-4356. PMID 1999685.
- ^ Haldane, J. (1901). "The Red Colour of Salted Meat". The Journal of Hygiene. 1 (1): 115–122. doi:10.1017/S0022172400000097. ISSN 0022-1724. PMC 2235964
 . PMID 20474105.
. PMID 20474105.
- ^ Eli S. Freeman (1957). "The Kinetics of the Thermal Decomposition of Potassium Nitrate and of the Reaction between Potassium Nitrite and Oxygen". J. Am. Chem. Soc. 79 (4): 838–842. doi:10.1021/ja01561a015.
- ^ Joseph LeConte (1862). Instructions for the Manufacture of Saltpeter. Columbia, S.C.: South Carolina Military Department. hlm. 14. Diarsipkan dari versi asli tanggal 13 Oktober 2007. Diakses tanggal 19 Oktober 2007.
- ^ Cecil Adams (16 Juni 1989). "Does saltpeter suppress male ardor?". The Straight Dope. Diarsipkan dari versi asli tanggal 23 Agustus 2007.
- ^ Sven Poulsen; Marie Errboe; Yamila Lescay Mevil; Anne‐Marie Glenny (19 Juli 2006). "Potassium containing toothpastes for dentine hypersensitivity". Cochrane Database of Systematic Reviews. doi:10.1002/14651858.CD001476.pub2.
Pranala luar[sunting | sunting sumber]
- (Inggris) Manufaktur Salpeter 1862