Nikotinamida adenina dinukleotida

| |
| Nama | |
|---|---|
| Nama lain
Difosfopiridina nukleotida (DPN+), Koenzim I
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| |
| Sifat | |
| C21H27N7O14P2 | |
| Massa molar | 663,43 g/mol |
| Penampilan | bubuk putih |
| Titik lebur | 160 °C |
| Bahaya | |
| Bahaya utama | Tidak berbahaya |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Nikotinamida adenina dinukleotida, disingkat NAD+, adalah koenzim yang ditemukan di semua sel hidup. Senyawa ini berupa dinukleotida, yakni mengandung dua nukleotida yang dihubungkan melalui gugus fosfat, dengan satu nukleotida mengandung basa adenina dan yang lainnya mengandung nikotinamida.
Dalam metabolisme, NAD+ terlibat dalam reaksi redoks, dengan membawa elektron dari satu reaksi ke reaksi lainnya. Koenzim ini oleh karenanya ditemukan dalam dua bentuk yang berbeda: NAD+ sebagai oksidator, dan NADH sebagai reduktor. NAD+ menerima elektron dari molekul lain dan menjadi tereduksi (NADH), dan begitu pula sebaliknya. Reaksi transfer elektron ini merupakan salah satu fungsi NAD+. Namun ia juga memiliki fungsi lain pada proses seluler lainnya, utamanya adalah sebagai substrat enzim yang menambah maupun mengurangi gugus fungsi pada protein dalam modifikasi pascatranslasional. Karena fungsinya yang penting ini, enzim-enzim yang terlibat dalam metabolisme NAD sering menjadi target pengembangan obat-obatan.
Dalam organisme, NAD+ dapat disintesis secara de novo (dari blok-blok molekul kecil) dari asam amino triptofan ataupun asam aspartat. Selain itu, NAD+ dapat juga diperoleh dari sumber makanan yang mengandung vitamin niasin.
Beberapa NAD diubah menjadi koenzim nikotinamida adenin dinukleotida fosfat (NADP).[1] Struktur kimianya sebagian besar mirip dengan NAD, namun perannya sebagian besar sebagai kofaktor dalam metabolisme anabolik.[2]
Sifat-sifat fisika dan kimia[sunting | sunting sumber]
Nikotinamida adenina dinukleotida, sama seperti senyawa dinukleotida pada umumnya, mengandung nukleotida yang dihubungkan oleh satu pasang gugus fosfat yang menjembatani keduanya. Nukleotida ini tersusun atas cincin ribosa dengan adenina yang melekat pada atom karbon pertama 1' cincin tersebut. Gugus nikotinamida dapat dilekatkan ke dalam dua orientasi pada satu atom karbon anomerik. Karena terdapat dua struktur yang dimungkinkan, senyawa ini berupa diastereomer. Diastereomer β-nikotinamida dari NAD+ adalah bentuk yang ditemukan pada organisme. Kedua nukleotida ini dihubungkan bersama oleh dua gugus fosfat melalui karbon 5'.[3]

Dalam metabolisme, senyawa ini menerima ataupun mendonorkan elektronnya dalam reaksi redoks.[4] Reaksi ini (diringkaskan oleh persamaan di bawah) melibatkan pelepasan dua atom hidrogen dari reaktan (R), dalam bentuk ion hidrida (H−) dan proton (H+). Proton dilepaskan ke dalam larutan, manakala reduktan RH2 dioksidasi dan NAD+ direduksi menjadi NADH melalui transfer hidrida menuju cincin nikotinamida.
- RH2 + NAD+ → NADH + H+ + R
Dari pasangan elektron hidrida, satu elektron ditransfer ke nitrogen cincin nikotinamida yang bermuatan positif, dan atom hidrogen kedua ditransfer ke atom karbon C4 yang berseberangan dengan nitrogen ini. Potensial elektroda standar pasangan redoks NAD+/NADH adalah −0,32 volt, membuat NADH sebagai reduktor kuat.[5] Reaksi ini sangat mudah berbalik arah, ketika NADH direduksi menjadi molekul lain dan dioksidasi kembali menjadi NAD+. Hal ini berarti koenzim ini dapat secara terus-menerus berada dalam siklus NAD+ dan NADH tanpa sendirinya dikonsumsi.[3]
Secara fisik, koenzim ini berbentuk bubuk amorf yang higroskopik dan sangat larut dalam air.[6] Padatan ini stabil jika disimpan dalam keadaan gelap dan kering. Larutan NAD+ tidak berwarna dan stabil selama satu pada temperatur 4 °C dan pH netral. Ia akan terurai dengan cepat apabila terkena asam ataupun basa. Seketika terurai, produk dekomposisi ini merupakan inhibitor enzim.[7]
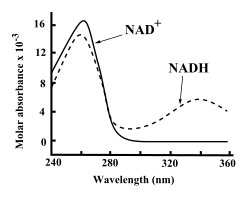
Baik NAD+ dan NADH menyerap ultraviolet dengan sangat kuat oleh karena keberadaan basa adeninanya. Sebagai contoh, puncak absorpsi NAD+ berada pada panjang gelombang 259 nanometer (nm), dengan koefisien pemunahan 16.900 M−1cm−1. NADH juga menyerap panjanga gelombang yang lebih tinggi, dengan puncak kedua dalam absorpsi UV-nya adalah 339 nm dengan koefisien atenuasi molar 6.220 M−1cm−1.[8] Perbedaan spektrum absorpsi ultraviolet antara bentuk koenzim yang teroksidasi dengan yang tereduksi ini membuat zat ini sangat mudah diukur pada uji enzim.[8]
NAD+ dan NADH juga memiliki spektrum fluoresens yang berbeda. NADH dalam larutan memiliki puncak emisi pada 460 nm dan waktu paruh fluoresens sepanjang 0,4 nanosekon, manakala pada koenzim yang teroksidasi tidak memiliki emisi fluoresens.[9] Sifat sinyal fluoresens berubah ketika NADH terikat pada protein, sehingga perubahan ini dapat digunakan untuk mengukur konstanta disosiasi, yang sangat berguna dalam kajian kinetika enzim.[9][10] Perubahan dalam sinyal fluoresens ini juga digunakan untuk mengukur perubahan dalam keadaan redoks sel hidup, melalui mikroskopi fluoresens.[11]
Konsentrasi dan keadaan zat dalam sel[sunting | sunting sumber]
Dalam hati tikus, kandungan total NAD+ dan NADH adalah kira-kira 1 μmol per gram berat basah hewan, sekitar 10 kali lipat konsentrasi NADP+ dan NADPH dalam sel yang sama.[12] Konsentrasi sebenarnya NAD+ dalam sitosol sel sulit diukur, dengan perkiraan terbaru dalam sel hewan berkisar antara 0,3 M[13][14] sampai dengan 1,0 sampai 2,0 mM dalam ragi.[15] Namun, sekitar 80% zat ini terikat pada protein, sehingga konsentrasinya dalam larutan haruslah lebih rendah.[16]
Data konsentrasi zat ini pada bagian sel lainnya sangat terbatas, walaupun dalam mitokondria konsentrasi NAD+ sama dengan konsentrasi zat ini dalam sitosol.[14] NAD+ dibawa ke dalam mitokondria melalui protein transpor membran yang khusus oleh karena koenzim ini tidak dapat berdifusi melewati membran.[17]
Keseimbangan antara bentuk NAD yang teroksidasi dengan bentuk yang tereduksi disebut rasio NAD+/NADH. Rasio ini merupakan komponen penting yang disebut sebagai keadaan redoks sel. Keadaan redoks sel adalah ukuran yang mencerminkan baik aktivitas metabolisme sel maupun kesehatan sel.[18] Efek rasio NAD+/NADH terhadap sel sangatlah kompleks. Ia mengontrol aktivitas beberapa enzim kunci, meliputi gliseraldehida 3-fosfat dehidrogenase dan piruvat dehidrogenase. Dalam jaringan mamalia yang sehat, perkiraan rasio NAD+/NADH umumnya berkisar sekitar 700; sehingga lebih menguntungkan bagi reaksi oksidasi.[19][20] Sebaliknya, rasio NADP+/NADPH umumnya sekitar 0,005.[21]
Biosintesis[sunting | sunting sumber]
NAD+ disintesis melalui dua lintasan metabolisme yaitu lintasan de novo dan lintasan penyelamatan (salvage). Lintasan de novo menggunakan asam amino, sedangkan lintasan penyelamatan dilakukan dengan mendaur ulang komponen-komponen prekursor seperti nikotinamida menjadi NAD+. Lintasan yang lain disebut lintasan kinurenina yang dilalui oleh triptofan.[22] Lintasan kinurenina terbagi dua, yang pertama adalah lintasan asam kinurenat, yang kedua adalah lintasan asam kuinolinat dan hidroksikynurenina-3. Ketiga senyawa organik tersebut merupakan prekursor dari NAD+.
Produksi de novo[sunting | sunting sumber]

Kebanyakan organisme mensintesis NAD+ dari komponen-komponen yang sederhana.[4] Reaksi yang terlibat berbeda-beda dari organisme yang satu ke organisme lain. Namun, terdapat kesamaan dalam penghasilan asam kuinolinat dari asam amino tertentu seperti triptofan pada hewan dan beberapa bakteri, ataupun asam aspartat pada beberapa bakteri dan tumbuhan.[23][24] Asam kuinolinat diubah menjadi asam nikotinat adenina dinukleotida (NaMN) melalui transfer gugus fosforibosa. Gugus adenilat kemudian ditransfer untuk membentuk asam nikotinat adenina dinukleotida (NaAD). Pada akhirnya, gugus asam nikotinat pada NaAD diamidasi menjadi gugus nikotinamida (Nam), membentuk nikotinamida adenina dinukleotida.[4]
Pada langkah lebih lanjut, beberapa NAD+ diubah menjadi NADP+ oleh NAD+ kinase, yang memfosforilasi NAD+.[25] Pada kebanyakan organisme, enzim ini menggunakan ATP sebagai sumber gugus fosfat, walaupun pada bakteri seperti Mycobacterium tuberculosis dan arkea seperti Pyrococcus horikoshii menggunakan polifosfat anorganik sebagai donor fosfat alternatif.[26][27]

Lintasan penyelamatan (salvage)[sunting | sunting sumber]
Selain perakitan NAD+ secara de novo menggunakan asam amino sederhana, sel juga mendaur ulang senyawa-senyawa yang mengandung nikotinamida untuk menghasilkan NAD+. Walaupun terdapat banyak prekursor-prekursor yang diketahui, terdapat tiga senyawa alamiah mengandung cincin nikotinamida yang digunakan dalam lintasan penyelamatan (daur ulang) ini, yakni asam nikotinat (Na), nikotinamida (Nam), dan nikotinamida ribosida (NR).[28] Prekursor-prekursor ini kemudian dimasukkan ke dalam lintasan biosintesis NAD(P)+ melalui reaksi adenilasi dan fosforibosilasi seperti yang ditunjukkan pada ilustrasi di atas.[4] Senyawa-senyawa ini dapat berasal dari makanan, di mana campuran asam nikotinat dan nikotinamida disebut sebagai vitamin B3 ataupun niasin. Namun, senyawa-senyawa ini juga dapat diproduksi dalam sel sendiri, yaitu melalui pelepasan gugus nikotinamida dari NAD+ dalam reaksi transfer ADP-ribosa. Enzim-enzim yang terlibat dalam lintasan daur ulang ini tampaknya terkonsentrasi dalam inti sel, yang mengompensasikan laju konsumsi NAD+ yang tinggi dalam organel ini.[29] Sel juga dapat mendapatkan NAD+ secara ekstraseluler (luar sel) dari sekelilingnya.[30]
Walaupun terdapat lintasan de novo, lintasan daur ulang ini merupakan lintasan yang esensial pada manusia. Kekurangan niasin pada makanan mengakibatkan penyakit defisiensi vitamin pelagra.[31] Kebutuhan NAD+ yang tinggi ini disebabkan oleh konsumsinya yang tinggi pada reaksi modifikasi pascatranslasi.[4]
Lintasan daur ulang yang digunakan oleh mikroorganisme berbeda dengan lintasan yang digunakan oleh mamalia.[32] Beberapa patogen seperti ragi Candida glabrata dan bakteri Haemophilus influenzae adalah auksotrof NAD+ (yakni tidak dapat mensintesis NAD+). Namun mereka memiliki lintasan daur ulang, sehingga sangat bergantung pada sumber luar NAD+ dan prekursornya.[33][34] Bahkan pada patogen seperti Chlamydia trachomatis, ia tidak memiliki gen untuk biosintesis maupun daur ulang NAD+ dan NADP+, sehingga harus menerima asupan koenzim ini dari sel inangnya.[35]
Fungsi[sunting | sunting sumber]

Nikotinamida adenina dinukleotida memiliki beberapa peranan esensial dalam metabolisme. Ia berperan sebagai koenzim pada reaksi redoks, sebagai donor gugus ADP-ribosa pada reaksi ADP-ribosilasi, sebagai prekursor molekul kurir kedua ADP-ribosa siklik, dan juga sebagai substrat bagi enzim DNA ligase bakteri dan enzim sirtuin yang menggunakan NAD+ untuk melepaskan gugus asetil dari protein.
Oksidoreduktase[sunting | sunting sumber]
Peran utama NAD+ dalam metabolisme adalah mentransfer elektron dari satu molekul ke molekul lainnya. Reaksi seperti ini dikatalisasi oleh sekelompok besar enzim yang dinamakan oksidoreduktase. Tata nama enzim dalam kelompok oksidoreduktase mengandung nama kedua substratnya. Sebagai contoh, NADH-ubikuinon oksidoreduktase mengkatalisis oksidasi NADH oleh koenzim Q.[37] Namun, enzim oksidoreduktase ini juga dapat dirujuk sebagai dehidrogenase ataupun reduktase. Biasanya NADH-ubikuinon oksidoreduktase disebut sebagai NADH dehidrogenase ataupun kadang kala koenzim Q reduktase.[38]
Ketika terikat pada suatu protein, NAD+ dan NADH biasanya terikat pada motif struktural yang dikenal dengan nama lipatan Rossmann.[39] Motif ini dinamakan atas nama Michael Rossmann yang merupakan ilmuwan yang pertama kali memperhatikan banyaknya motif ini pada protein pengikat nukleotida.[40] Lipatan ini mengandung tiga atau lebih lempengan beta paralel yang dihubungkan oleh dua heliks alfa dengan urutan beta-alfa-beta-alfa-beta. Oleh karena tiap lipatan Rossmann mengikat satu nukleotida, domain pengikatan untuk dinukleotida NAD+ terdiri dari dua lipatan Rossmann yang berpasangan, dengan tiap lipatan mengikat satu nukleotida.[40] Walau demikian, lipatan ini tidaklah universal ada pada enzim yang bergantung pada NAD. Baru-baru ini ditemukan suatu kelas enzim bakteria yang terlibat dalam metabolisme asam amino mengikat koenzim ini, namun tidak memiliki motif lipatan Rossmann.[41]

Ketika terikat pada tapak aktif suatu oksidoreduktase, cincin nikotinamida koenzim ini diposisikan sedemikiannya ia dapat menerima hidrida dari substrat enzim lainnya. Oleh karena karbon C4 yang menerima hidrogen ini prokiral, hal ini dapat digunakan dalam kinetika enzim untuk mengetahui mekanisme enzim. Hal ini dilakukan dengan mencampurkan enzim dengan substrat yang beratom deuterium sebagai pengganti hidrogen, sehingga enzim akan mereduksi NAD+ dengan mentransfer deuterium daripada hidrogen. Dalam kasus ini, enzim dapat menghasilkan salah satu stereoisomer NADH. Pada beberapa jenis enzim, hidrogen ditransfer dari atas bidang cincin nikotinamida. Enzim demikian disebut sebagai oksidoreduktase kelas A, manakala enzim kelas B mentransfer atom hidrogennya dari bawah bidang.[42]
Walaupun terdapat kemiripan pada cara protein mengikat koenzim NAD+ dan NADP+, enzim hampir selalu memiliki spesifisitas yang tinggi untuk mengikat hanya salah satu dari NAD+ maupun NADP+.[43] Spesifisitas ini mencermikan peranan metabolik kedua koenzim yang berbeda dan merupakan akibat dari perbedaan residu asam amino yang berbeda pada kantong pengikat koenzim tersebut. Sebagai contohnya, pada tapak aktif enzim pengikat NADP, ikatan ion terbentuk antara rantai samping asam amino basa dengan gugus fosfat NADP+ yang asam. Sebaliknya, pada enzim yang mengikat NAD, muatan kantongnya terbalik, menjauhkan NADP+ untuk berikatan dengannya. Walau demikian, terdapat pengecualian terhadap kaidah ini. Enzim seperti aldosa reduktase, glukosa-6-fosfat dehidrogenase, dan metilenatetrahidrofolat reduktase dapat menggunakan kedua enzim tersebut pada beberapa spesies organisme.[44]
Peran dalam reaksi redoks[sunting | sunting sumber]

Reaksi redoks melibatkan oksidoreduktase sangat penting dalam metabolisme, terutama untuk membongkar energi yang tersimpan dalam ikatan rangkap oksigen yang relatif lemah.[45] Pada proses ini, senyawa tereduksi seperti glukosa dan asam lemak akan dioksidasi, sehingga melepaskan energi kimia dari O2. Sementara itu, NAD+ direduksi menjadi NADH, sebagai bagian dari oksidasi beta, glikolisis, dan siklus asam sitrat. Pada eukariota, elektron yang dibawa oleh NADH yang diproduksi di sitoplasma ditransfer ke mitokondria (untuk mereduksi NAD+mitokondria) oleh antar-jemput mitokondria, seperti antar-jemput malat-aspartat.[46] NADH mitokondria kemudian dioksidasi oleh rantai transpor elektron, yang memompa proton melintasi membran dan menghasilkan ATP melalui fosforilasi oksidatif.[47][48] Sistem antar-jemput ini juga memiliki fungsi transportasi yang sama dalam kloroplas.[49]
Karena bentuk teroksidasi dan tereduksi dari nikotinamida adenin dinukleotida digunakan dalam rangkaian reaksi yang terkait ini, sel mempertahankan konsentrasi NAD+ dan NADH yang signifikan, dengan rasio NAD+/NADH yang tinggi memungkinkan koenzim ini bertindak sebagai pengoksidasi dan agen pereduksi. Sebaliknya, fungsi utama NADPH adalah sebagai agen pereduksi dalam anabolisme, dengan koenzim ini terlibat dalam jalur seperti sintesis asam lemak dan fotosintesis. Karena NADPH diperlukan untuk mendorong reaksi redoks sebagai zat pereduksi kuat, rasio NADP+/NADPH dijaga sangat rendah.[50]
Meskipun penting dalam katabolisme, NADH juga digunakan dalam reaksi anabolik, seperti glukoneogenesis.[51] Kebutuhan NADH dalam anabolisme ini menimbulkan masalah bagi prokariota yang tumbuh pada nutrisi yang hanya melepaskan sejumlah kecil energi. Misalnya, bakteri nitrifikasi seperti Nitrobacter mengoksidasi nitrit menjadi nitrat, yang melepaskan energi yang cukup untuk memompa proton dan menghasilkan ATP, tetapi tidak cukup untuk menghasilkan NADH secara langsung.[52] Karena NADH masih diperlukan untuk reaksi anabolik, bakteri ini menggunakan nitrit oksidoreduktase untuk menghasilkan gaya gerak proton yang cukup untuk menjalankan bagian dari rantai transpor elektron secara terbalik dan menghasilkan NADH.[53]
Peran non-redoks[sunting | sunting sumber]
Koenzim NAD+ juga digunakan dalam reaksi transfer ADP-ribosa. Misalnya, enzim yang disebut ADP-ribosiltransferase menambahkan bagian ADP-ribosa dari molekul ini ke protein, dalam modifikasi pascatranslasi yang disebut ADP-ribosilasi.[54] ADP-ribosilasi melibatkan baik penambahan bagian ADP-ribosa tunggal, dalam ribosilasi mono-ADP, maupun transfer ADP-ribosa ke protein dalam rantai bercabang panjang, yang disebut poli(ADP-ribosil)asi.[55] Mono-ADP-ribosilasi pertama kali diidentifikasi sebagai mekanisme sekelompok toksin bakteri, terutama toksin kolera, tetapi juga terlibat dalam pensinyalan sel normal.[56][57] Poli(ADP-ribosil)asi dilakukan oleh poli(ADP-ribosa) polimerase (PARP). Struktur poli(ADP-ribosa) terlibat dalam regulasi beberapa peristiwa seluler dan paling penting dalam inti sel, dalam proses seperti perbaikan DNA dan pemeliharaan telomer.[58] Selain fungsi-fungsi di dalam sel, sekelompok ADP-ribosiltransferase ekstraseluler baru-baru ini ditemukan, tetapi fungsinya belum diketahui dengan jelas.[59] NAD+ juga dapat ditambahkan ke RNA seluler sebagai modifikasi ujung 5'.[60]

Aksi ekstraseluler dari NAD+[sunting | sunting sumber]
Dalam beberapa tahun terakhir, NAD+ juga telah dikenal sebagai molekul pensinyalan ekstraseluler yang terlibat dalam komunikasi sel-ke-sel.[61][62][63] NAD+ dilepaskan dari neuron dalam pembuluh darah,[64] kandung kemih,[64][65] usus besar,[66][67] dari sel neurosekretori,[68] dan dari sinaptosom otak,[69] dan diusulkan untuk menjadi neurotransmitter baru yang mengirimkan informasi dari saraf ke sel efektor di organ otot polos.[66][67] Pada tumbuhan, NAD ekstraseluler menginduksi resistansi terhadap infeksi patogen, dan reseptor NAD ekstraseluler telah diidentifikasi.[70] Penelitian lebih lanjut diperlukan untuk menentukan mekanisme yang mendasari aksi NAD+ ekstraseluler dan pentingnya untuk kesehatan manusia dan proses kehidupan pada organisme lain.
Signifikansi klinis[sunting | sunting sumber]
Enzim yang membuat dan menggunakan NAD+ dan NADH penting dalam farmakologi dan penelitian pengobatan penyakit.[71] Desain dan pengembangan obat memanfaatkan NAD+ dalam tiga cara: i) sebagai target langsung, ii) merancang inhibitor enzim atau aktivator yang mengubah aktivitas enzim yang bergantung pada NAD, iii) menghambat biosintesis NAD+.[72]
NAD+ merupakan target langsung dari obat isoniazid, yang digunakan dalam pengobatan tuberkulosis (disebabkan oleh Mycobacterium tuberculosis). Isoniazid merupakan suatu prodrug, dan setelah memasuki bakteri diaktifkan oleh enzim peroksidase, yang mengoksidasi senyawa menjadi bentuk radikal bebas.[73] Radikal ini kemudian bereaksi dengan NADH, menghasilkan produk aduk yang merupakan inhibitor sangat poten terhadap enzim enoil-asill karier protein reduktase,[74] dan dihidrofolat reduktase.[75]
Banyak oksidoreduktase menggunakan NAD+ dan NADH sebagai substrat, sehingga ditemukannya inhibitor berdasarkan NAD+ yang spesifik untuk satu enzim cukup mengejutkan. Kerja inhibitor melibatkan pengikatan menggunakan motif struktural yang sangat lestari. Sebagai contoh, inhibitor berdasarkan senyawa asam mikofenolat dan tiazofurin menghambat IMP dehidrogenase di tempat pengikatan NAD+. Enzim ini penting dalam metabolisme purin, sehingga senyawa ini berguna sebagai obat antikanker, antivirus, atau imunosupresif.[76][77][78] Terdapat obat lain yang bukan penghambat enzim, tetapi mengaktifkan enzim yang terlibat dalam metabolisme NAD+. Sirtuin merupakan target yang sangat menarik, karena aktivasi deasetilasi bergantung pada NAD ini memperpanjang usia pada beberapa model hewan.[79] Senyawa seperti resveratrol meningkatkan aktivitas enzim ini, yang penting dalam kemampuannya untuk menunda penuaan pada organisme model.[80][81][82][83] Dalam satu percobaan, tikus yang diberi NAD selama satu minggu meningkatkan komunikasi antara inti sel dan mitokondria.[84]
Karena perbedaan jalur metabolisme biosintesis NAD+ antara organisme, seperti antara bakteri dan manusia, area metabolisme ini merupakan area yang menjanjikan untuk pengembangan antibiotik baru.[85][86] Misalnya, enzim nikotinamidase, suatu enzim yang mengubah nikotinamida menjadi asam nikotinat, merupakan target untuk desain obat, karena enzim ini tidak ada pada manusia tetapi ada dalam ragi, bakteri, dan Leishmania.[87][88][89]
Dalam bakteriologi, NAD kadang-kadang disebut faktor V, digunakan sebagai suplemen untuk media kultur untuk beberapa bakteri rumit yang memerlukan nutrian khusus.[90]
Sejarah[sunting | sunting sumber]

Koenzim NAD+ pertama kali ditemukan oleh ahli biokimia Inggris Arthur Harden dan William John Young pada 1906.[91] Mereka menunjukkan bahwa menambahkan ekstrak ragi yang direbus dan disaring sangat mempercepat fermentasi alkohol dalam ekstrak ragi yang tidak direbus. Mereka menyebut faktor tak dikenal yang bertanggung jawab atas efek ini sebagai kofermen. Melalui pemurnian dari ekstrak ragi dengan proses yang lama dan sulit , faktor stabil panas ini diidentifikasi sebagai fosfat gula nukleotida oleh Hans von Euler-Chelpin.[92] Pada 1936, ilmuwan Jerman Otto Heinrich Warburg menunjukkan fungsi koenzim nukleotida dalam transfer hidrida dan mengidentifikasi bagian nikotinamida sebagai tempat reaksi redoks.[93]
Referensi[sunting | sunting sumber]
- ^ Agledal, Line; Niere, Marc; Ziegler, Mathias (2010-02). "The phosphate makes a difference: cellular functions of NADP". Redox Report (dalam bahasa Inggris). 15 (1): 2–10. doi:10.1179/174329210X12650506623122. ISSN 1351-0002. PMC 7067316
 . PMID 20196923.
. PMID 20196923.
- ^ Spaans, Sebastiaan K.; Weusthuis, Ruud A.; van der Oost, John; Kengen, Servé W. M. (2015-07-29). "NADPH-generating systems in bacteria and archaea". Frontiers in Microbiology. 6. doi:10.3389/fmicb.2015.00742. ISSN 1664-302X. PMC 4518329
 . PMID 26284036.
. PMID 26284036.
- ^ a b Pollak, N (2007). "The power to reduce: pyridine nucleotides—small molecules with a multitude of functions". Biochem. J. 402 (2): 205–18. doi:10.1042/BJ20061638. PMC 1798440
 . PMID 17295611.
. PMID 17295611.
- ^ a b c d e Belenky, Peter; Bogan, Katrina L.; Brenner, Charles (2007-01). "NAD+ metabolism in health and disease" (PDF). Trends in Biochemical Sciences. 32 (1): 12–19. doi:10.1016/j.tibs.2006.11.006. ISSN 0968-0004. PMID 17161604.
- ^ Unden G (1997). "Alternative respiratory pathways of Escherichia coli: energetics and transcriptional regulation in response to electron acceptors". Biochim. Biophys. Acta. 1320 (3): 217–34. doi:10.1016/S0005-2728(97)00034-0. PMID 9230919.
- ^ Windholz, Martha (1983). The Merck Index: an encyclopedia of chemicals, drugs, and biologicals (edisi ke-10th). Rahway NJ, US: Merck. hlm. 909. ISBN 911910271 Periksa nilai: length
|isbn=(bantuan). - ^ Biellmann JF, Lapinte C, Haid E, Weimann G (1979). "Structure of lactate dehydrogenase inhibitor generated from coenzyme". Biochemistry. 18 (7): 1212–7. doi:10.1021/bi00574a015. PMID 218616.
- ^ a b Dawson, R. Ben (1985). Data for biochemical research (edisi ke-3rd). Oxford: Clarendon Press. hlm. 122. ISBN 0-19-855358-7.
- ^ a b Lakowicz JR, Szmacinski H, Nowaczyk K, Johnson ML (1992). "Fluorescence lifetime imaging of free and protein-bound NADH". Proc. Natl. Acad. Sci. U.S.A. 89 (4): 1271–5. doi:10.1073/pnas.89.4.1271. PMC 48431
 . PMID 1741380.
. PMID 1741380.
- ^ Jameson DM, Thomas V, Zhou DM (1989). "Time-resolved fluorescence studies on NADH bound to mitochondrial malate dehydrogenase". Biochim. Biophys. Acta. 994 (2): 187–90. PMID 2910350.
- ^ Kasimova MR, Grigiene J, Krab K; et al. (2006). "The free NADH concentration is kept constant in plant mitochondria under different metabolic conditions". Plant Cell. 18 (3): 688–98. doi:10.1105/tpc.105.039354. PMC 1383643
 . PMID 16461578.
. PMID 16461578.
- ^ Reiss PD, Zuurendonk PF, Veech RL (1984). "Measurement of tissue purine, pyrimidine, and other nucleotides by radial compression high-performance liquid chromatography". Anal. Biochem. 140 (1): 162–71. doi:10.1016/0003-2697(84)90148-9. PMID 6486402.
- ^ Yamada K, Hara N, Shibata T, Osago H, Tsuchiya M (2006). "The simultaneous measurement of nicotinamide adenine dinucleotide and related compounds by liquid chromatography/electrospray ionization tandem mass spectrometry". Anal. Biochem. 352 (2): 282–5. doi:10.1016/j.ab.2006.02.017. PMID 16574057.
- ^ a b Yang H, Yang T, Baur JA, Perez E, Matsui T, Carmona JJ, Lamming DW, Souza-Pinto NC, Bohr VA, Rosenzweig A, de Cabo R, Sauve AA, Sinclair DA. (2007). "Nutrient-Sensitive Mitochondrial NAD+ Levels Dictate Cell Survival". Cell. 130 (6): 1095–107. doi:10.1016/j.cell.2007.07.035. PMID 17889652.
- ^ Belenky P, Racette FG, Bogan KL, McClure JM, Smith JS, Brenner C (2007). "Nicotinamide riboside promotes Sir2 silencing and extends lifespan via Nrk and Urh1/Pnp1/Meu1 pathways to NAD+". Cell. 129 (3): 473–84. doi:10.1016/j.cell.2007.03.024. PMID 17482543.
- ^ Blinova K, Carroll S, Bose S; et al. (2005). "Distribution of mitochondrial NADH fluorescence lifetimes: steady-state kinetics of matrix NADH interactions". Biochemistry. 44 (7): 2585–94. doi:10.1021/bi0485124. PMID 15709771.
- ^ Todisco S, Agrimi G, Castegna A, Palmieri F (2006). "Identification of the mitochondrial NAD+ transporter in Saccharomyces cerevisiae". J. Biol. Chem. 281 (3): 1524–31. doi:10.1074/jbc.M510425200. PMID 16291748. Diarsipkan dari versi asli tanggal 2020-04-13. Diakses tanggal 2010-03-29.
- ^ Schafer F, Buettner G (2001). "Redox environment of the cell as viewed through the redox state of the glutathione disulfide/glutathione couple". Free Radic Biol Med. 30 (11): 1191–212. doi:10.1016/S0891-5849(01)00480-4. PMID 11368918.
- ^ Williamson DH, Lund P, Krebs HA (1967). "The redox state of free nicotinamide-adenine dinucleotide in the cytoplasm and mitochondria of rat liver". Biochem. J. 103 (2): 514–27. PMC 1270436
 . PMID 4291787.
. PMID 4291787.
- ^ Zhang Q, Piston DW, Goodman RH (2002). "Regulation of corepressor function by nuclear NADH". Science. 295 (5561): 1895–7. doi:10.1126/science.1069300. PMID 11847309.
- ^ Veech RL, Eggleston LV, Krebs HA (1969). "The redox state of free nicotinamide-adenine dinucleotide phosphate in the cytoplasm of rat liver". Biochem. J. 115 (4): 609–19. PMC 1185185
 . PMID 4391039.
. PMID 4391039.
- ^ (Inggris) "Mitochondria, metabolic disturbances, oxidative stress and the kynurenine system, with focus on neurodegenerative disorders". Department of Neurology, University of Szeged; Sas K, Robotka H, Toldi J, Vécsei L. Diakses tanggal 2010-07-31.
- ^ Katoh A, Uenohara K, Akita M, Hashimoto T (2006). "Early steps in the biosynthesis of NAD in Arabidopsis start with aspartate and occur in the plastid". Plant Physiol. 141 (3): 851–7. doi:10.1104/pp.106.081091. PMC 1489895
 . PMID 16698895.
. PMID 16698895.
- ^ Foster JW, Moat AG (1 March 1980). "Nicotinamide adenine dinucleotide biosynthesis and pyridine nucleotide cycle metabolism in microbial systems". Microbiol. Rev. 44 (1): 83–105. PMC 373235
 . PMID 6997723.
. PMID 6997723.
- ^ Magni G, Orsomando G, Raffaelli N (2006). "Structural and functional properties of NAD kinase, a key enzyme in NADP biosynthesis". Mini reviews in medicinal chemistry. 6 (7): 739–46. doi:10.2174/138955706777698688. PMID 16842123.
- ^ Sakuraba H, Kawakami R, Ohshima T (2005). "First archaeal inorganic polyphosphate/ATP-dependent NAD kinase, from hyperthermophilic archaeon Pyrococcus horikoshii: cloning, expression, and characterization". Appl. Environ. Microbiol. 71 (8): 4352–8. doi:10.1128/AEM.71.8.4352-4358.2005. PMC 1183369
 . PMID 16085824.
. PMID 16085824.
- ^ Raffaelli N, Finaurini L, Mazzola F; et al. (2004). "Characterization of Mycobacterium tuberculosis NAD kinase: functional analysis of the full-length enzyme by site-directed mutagenesis". Biochemistry. 43 (23): 7610–7. doi:10.1021/bi049650w. PMID 15182203.
- ^ Tempel W, Rabeh WM, Bogan KL; et al. (2007). "Nicotinamide riboside kinase structures reveal new pathways to NAD+". PLoS Biol. 5 (10): e263. doi:10.1371/journal.pbio.0050263. PMC 1994991
 . PMID 17914902.
. PMID 17914902.
- ^ Anderson RM, Bitterman KJ, Wood JG; et al. (2002). "Manipulation of a nuclear NAD+ salvage pathway delays aging without altering steady-state NAD+ levels". J. Biol. Chem. 277 (21): 18881–90. doi:10.1074/jbc.M111773200. PMID 11884393. Diarsipkan dari versi asli tanggal 2020-04-13. Diakses tanggal 2010-03-29.
- ^ Billington RA, Travelli C, Ercolano E; et al. (2008). "Characterization of NAD Uptake in Mammalian Cells". J. Biol. Chem. 283 (10): 6367–74. doi:10.1074/jbc.M706204200. PMID 18180302. Diarsipkan dari versi asli tanggal 2020-05-28. Diakses tanggal 2010-03-29.
- ^ Henderson LM (1983). "Niacin". Annu. Rev. Nutr. 3: 289–307. doi:10.1146/annurev.nu.03.070183.001445. PMID 6357238.
- ^ Rongvaux A, Andris F, Van Gool F, Leo O (2003). "Reconstructing eukaryotic NAD metabolism". Bioessays. 25 (7): 683–90. doi:10.1002/bies.10297. PMID 12815723.
- ^ Ma B, Pan SJ, Zupancic ML, Cormack BP (2007). "Assimilation of NAD(+) precursors in Candida glabrata". Mol. Microbiol. 66 (1): 14–25. doi:10.1111/j.1365-2958.2007.05886.x. PMID 17725566.
- ^ Reidl J, Schlör S, Kraiss A, Schmidt-Brauns J, Kemmer G, Soleva E (2000). "NADP and NAD utilization in Haemophilus influenzae". Mol. Microbiol. 35 (6): 1573–81. doi:10.1046/j.1365-2958.2000.01829.x. PMID 10760156.
- ^ Gerdes SY, Scholle MD, D'Souza M; et al. (2002). "From genetic footprinting to antimicrobial drug targets: examples in cofactor biosynthetic pathways". J. Bacteriol. 184 (16): 4555–72. doi:10.1128/JB.184.16.4555-4572.2002. PMC 135229
 . PMID 12142426.
. PMID 12142426.
- ^ Senkovich O, Speed H, Grigorian A; et al. (2005). "Crystallization of three key glycolytic enzymes of the opportunistic pathogen Cryptosporidium parvum". Biochim. Biophys. Acta. 1750 (2): 166–72. doi:10.1016/j.bbapap.2005.04.009. PMID 15953771.
- ^ "Enzyme Nomenclature, Recommendations for enzyme names from the Nomenclature Committee of the International Union of Biochemistry and Molecular Biology". Diakses tanggal 2007-12-06.
- ^ "NiceZyme View of ENZYME: EC 1.6.5.3". Expasy. Diakses tanggal 2007-12-16.
- ^ Lesk AM (1995). "NAD-binding domains of dehydrogenases". Curr. Opin. Struct. Biol. 5 (6): 775–83. doi:10.1016/0959-440X(95)80010-7. PMID 8749365.
- ^ a b Rao S, Rossmann M (1973). "Comparison of super-secondary structures in proteins". J Mol Biol. 76 (2): 241–56. doi:10.1016/0022-2836(73)90388-4. PMID 4737475.
- ^ Goto M, Muramatsu H, Mihara H; et al. (2005). "Crystal structures of Delta1-piperideine-2-carboxylate/Delta1-pyrroline-2-carboxylate reductase belonging to a new family of NAD(P)H-dependent oxidoreductases: conformational change, substrate recognition, and stereochemistry of the reaction". J. Biol. Chem. 280 (49): 40875–84. doi:10.1074/jbc.M507399200. PMID 16192274. Diarsipkan dari versi asli tanggal 2008-06-11. Diakses tanggal 2010-03-29.
- ^ Bellamacina CR (1 September 1996). "The nicotinamide dinucleotide binding motif: a comparison of nucleotide binding proteins". FASEB J. 10 (11): 1257–69. PMID 8836039.
- ^ Carugo O, Argos P (1997). "NADP-dependent enzymes. I: Conserved stereochemistry of cofactor binding". Proteins. 28 (1): 10–28. doi:10.1002/(SICI)1097-0134(199705)28:1<10::AID-PROT2>3.0.CO;2-N. PMID 9144787.
- ^ Vickers TJ, Orsomando G, de la Garza RD; et al. (2006). "Biochemical and genetic analysis of methylenetetrahydrofolate reductase in Leishmania metabolism and virulence". J. Biol. Chem. 281 (50): 38150–8. doi:10.1074/jbc.M608387200. PMID 17032644. Diarsipkan dari versi asli tanggal 2008-10-13. Diakses tanggal 2010-03-29.
- ^ Schmidt-Rohr K (2020). "Oxygen Is the High-Energy Molecule Powering Complex Multicellular Life: Fundamental Corrections to Traditional Bioenergetics". ACS Omega. 5 (5): 2221–2233. doi:10.1021/acsomega.9b03352. PMC 7016920
 . PMID 32064383.
. PMID 32064383.
- ^ Bakker BM, Overkamp KM, Kötter P, Luttik MA, Pronk JT (2001). "Stoichiometry and compartmentation of NADH metabolism in Saccharomyces cerevisiae". FEMS Microbiol. Rev. 25 (1): 15–37. doi:10.1111/j.1574-6976.2001.tb00570.x. PMID 11152939.
- ^ Cooper, Geoffrey M. (2000). "The Mechanism of Oxidative Phosphorylation". The Cell: A Molecular Approach. 2nd edition (dalam bahasa Inggris).
- ^ Ahmad, Maria; Wolberg, Adam; Kahwaji, Chadi I. (2022). Biochemistry, Electron Transport Chain. Treasure Island (FL): StatPearls Publishing. PMID 30252361.
- ^ Heineke D, Riens B, Grosse H, Hoferichter P, Peter U, Flügge UI, Heldt HW (1991). "Redox Transfer across the Inner Chloroplast Envelope Membrane". Plant Physiol. 95 (4): 1131–1137. doi:10.1104/pp.95.4.1131. PMC 1077662
 . PMID 16668101.
. PMID 16668101.
- ^ Xiao, Wusheng; Wang, Rui-Sheng; Handy, Diane E.; Loscalzo, Joseph (2018-01-20). "NAD(H) and NADP(H) Redox Couples and Cellular Energy Metabolism". Antioxidants & Redox Signaling. 28 (3): 251–272. doi:10.1089/ars.2017.7216. ISSN 1557-7716. PMC 5737637
 . PMID 28648096.
. PMID 28648096.
- ^ Sistare, F D; Haynes, R C (October 1985). "The interaction between the cytosolic pyridine nucleotide redox potential and gluconeogenesis from lactate/pyruvate in isolated rat hepatocytes. Implications for investigations of hormone action". Journal of Biological Chemistry. 260 (23): 12748–12753. doi:10.1016/S0021-9258(17)38940-8. PMID 4044607.
- ^ Freitag A, Bock E (1990). "Energy conservation in Nitrobacter". FEMS Microbiology Letters. 66 (1–3): 157–62. doi:10.1111/j.1574-6968.1990.tb03989.x.
- ^ Starkenburg SR, Chain PS, Sayavedra-Soto LA, Hauser L, Land ML, Larimer FW, Malfatti SA, Klotz MG, Bottomley PJ, Arp DJ, Hickey WJ (2006). "Genome Sequence of the Chemolithoautotrophic Nitrite-Oxidizing Bacterium Nitrobacter winogradskyi Nb-255". Appl. Environ. Microbiol. 72 (3): 2050–63. Bibcode:2006ApEnM..72.2050S. doi:10.1128/AEM.72.3.2050-2063.2006. PMC 1393235
 . PMID 16517654.
. PMID 16517654.
- ^ Ziegler M (2000). "New functions of a long-known molecule. Emerging roles of NAD in cellular signaling". Eur. J. Biochem. 267 (6): 1550–64. doi:10.1046/j.1432-1327.2000.01187.x. PMID 10712584.
- ^ Diefenbach J, Bürkle A (2005). "Introduction to poly(ADP-ribose) metabolism". Cell. Mol. Life Sci. 62 (7–8): 721–30. doi:10.1007/s00018-004-4503-3. PMID 15868397.
- ^ Corda D, Di Girolamo M (2003). "New Embo Member's Review: Functional aspects of protein mono-ADP-ribosylation". EMBO J. 22 (9): 1953–8. doi:10.1093/emboj/cdg209. PMC 156081
 . PMID 12727863.
. PMID 12727863.
- ^ Szántó, Magdolna; Bai, Peter (2020-03-01). "The role of ADP-ribose metabolism in metabolic regulation, adipose tissue differentiation, and metabolism". Genes & Development (dalam bahasa Inggris). 34 (5-6): 321–340. doi:10.1101/gad.334284.119. ISSN 0890-9369. PMC 7050491
 . PMID 32029456.
. PMID 32029456.
- ^ Bai, Peter (2015-06). "Biology of Poly(ADP-Ribose) Polymerases: The Factotums of Cell Maintenance". Molecular Cell (dalam bahasa Inggris). 58 (6): 947–958. doi:10.1016/j.molcel.2015.01.034.
- ^ Rissiek, Björn; Menzel, Stephan; Leutert, Mario; Cordes, Maike; Behr, Sarah; Jank, Larissa; Ludewig, Peter; Gelderblom, Mathias; Rissiek, Anne (2017-12). "Ecto-ADP-ribosyltransferase ARTC2.1 functionally modulates FcγR1 and FcγR2B on murine microglia". Scientific Reports (dalam bahasa Inggris). 7 (1): 16477. doi:10.1038/s41598-017-16613-w. ISSN 2045-2322. PMC 5705771
 . PMID 29184112.
. PMID 29184112.
- ^ Chen YG, Kowtoniuk WE, Agarwal I, Shen Y, Liu DR (December 2009). "LC/MS analysis of cellular RNA reveals NAD-linked RNA". Nat Chem Biol. 5 (12): 879–881. doi:10.1038/nchembio.235. PMC 2842606
 . PMID 19820715.
. PMID 19820715.
- ^ Billington RA, Bruzzone S, De Flora A, Genazzani AA, Koch-Nolte F, Ziegler M, Zocchi E (2006). "Emerging functions of extracellular pyridine nucleotides". Mol. Med. 12 (11–12): 324–7. doi:10.2119/2006-00075.Billington. PMC 1829198
 . PMID 17380199.
. PMID 17380199.
- ^ Ziegler M, Niere M (2004). "NAD+ surfaces again". Biochem. J. 382 (Pt 3): e5–6. doi:10.1042/BJ20041217. PMC 1133982
 . PMID 15352307.
. PMID 15352307.
- ^ Koch-Nolte F, Fischer S, Haag F, Ziegler M (2011). "Compartmentation of NAD+-dependent signalling". FEBS Lett. 585 (11): 1651–6. doi:10.1016/j.febslet.2011.03.045. PMID 21443875.
- ^ a b Smyth LM, Bobalova J, Mendoza MG, Lew C, Mutafova-Yambolieva VN (2004). "Release of beta-nicotinamide adenine dinucleotide upon stimulation of postganglionic nerve terminals in blood vessels and urinary bladder". J Biol Chem. 279 (47): 48893–903. doi:10.1074/jbc.M407266200. PMID 15364945.
- ^ Breen, Leanne T.; Smyth, Lisa M.; Yamboliev, Ilia A.; Mutafova-Yambolieva, Violeta N. (February 2006). "β-NAD is a novel nucleotide released on stimulation of nerve terminals in human urinary bladder detrusor muscle". American Journal of Physiology. Renal Physiology. 290 (2): F486–F495. doi:10.1152/ajprenal.00314.2005. PMID 16189287.
- ^ a b Mutafova-Yambolieva VN, Hwang SJ, Hao X, Chen H, Zhu MX, Wood JD, Ward SM, Sanders KM (2007). "Beta-nicotinamide adenine dinucleotide is an inhibitory neurotransmitter in visceral smooth muscle". Proc. Natl. Acad. Sci. U.S.A. 104 (41): 16359–64. Bibcode:2007PNAS..10416359M. doi:10.1073/pnas.0705510104. PMC 2042211
 . PMID 17913880.
. PMID 17913880.
- ^ a b Hwang SJ, Durnin L, Dwyer L, Rhee PL, Ward SM, Koh SD, Sanders KM, Mutafova-Yambolieva VN (2011). "β-nicotinamide adenine dinucleotide is an enteric inhibitory neurotransmitter in human and nonhuman primate colons". Gastroenterology. 140 (2): 608–617.e6. doi:10.1053/j.gastro.2010.09.039. PMC 3031738
 . PMID 20875415.
. PMID 20875415.
- ^ Yamboliev IA, Smyth LM, Durnin L, Dai Y, Mutafova-Yambolieva VN (2009). "Storage and secretion of beta-NAD, ATP and dopamine in NGF-differentiated rat pheochromocytoma PC12 cells". Eur. J. Neurosci. 30 (5): 756–68. doi:10.1111/j.1460-9568.2009.06869.x. PMC 2774892
 . PMID 19712094.
. PMID 19712094.
- ^ Durnin L, Dai Y, Aiba I, Shuttleworth CW, Yamboliev IA, Mutafova-Yambolieva VN (2012). "Release, neuronal effects and removal of extracellular β-nicotinamide adenine dinucleotide (β-NAD+) in the rat brain". Eur. J. Neurosci. 35 (3): 423–35. doi:10.1111/j.1460-9568.2011.07957.x. PMC 3270379
 . PMID 22276961.
. PMID 22276961.
- ^ Wang C, Zhou M, Zhang X, Yao J, Zhang Y, Mou Z (2017). "A lectin receptor kinase as a potential sensor for extracellular nicotinamide adenine dinucleotide in Arabidopsis thaliana". eLife. 6: e25474. doi:10.7554/eLife.25474. PMC 5560858
 . PMID 28722654.
. PMID 28722654.
- ^ Sauve AA (March 2008). "NAD+ and vitamin B3: from metabolism to therapies". The Journal of Pharmacology and Experimental Therapeutics. 324 (3): 883–93. doi:10.1124/jpet.107.120758. PMID 18165311.
- ^ Zapata‐Pérez, Rubén; Wanders, Ronald J A; Karnebeek, Clara D M; Houtkooper, Riekelt H (2021-07-07). "NAD + homeostasis in human health and disease". EMBO Molecular Medicine (dalam bahasa Inggris). 13 (7). doi:10.15252/emmm.202113943. ISSN 1757-4676.
- ^ Timmins GS, Deretic V (2006). "Mechanisms of action of isoniazid". Mol. Microbiol. 62 (5): 1220–7. doi:10.1111/j.1365-2958.2006.05467.x. PMID 17074073.
- ^ Rawat R, Whitty A, Tonge PJ (2003). "The isoniazid-NAD adduct is a slow, tight-binding inhibitor of InhA, the Mycobacterium tuberculosis enoyl reductase: Adduct affinity and drug resistance". Proc. Natl. Acad. Sci. U.S.A. 100 (24): 13881–6. Bibcode:2003PNAS..10013881R. doi:10.1073/pnas.2235848100. PMC 283515
 . PMID 14623976.
. PMID 14623976.
- ^ Argyrou A, Vetting MW, Aladegbami B, Blanchard JS (2006). "Mycobacterium tuberculosis dihydrofolate reductase is a target for isoniazid". Nat. Struct. Mol. Biol. 13 (5): 408–13. doi:10.1038/nsmb1089. PMID 16648861.
- ^ Nair, Vasu; Shu, Qingning (2007). "Inosine monophosphate dehydrogenase as a probe in antiviral drug discovery". Antiviral Chemistry & Chemotherapy. 18 (5): 245–258. doi:10.1177/095632020701800501. ISSN 0956-3202. PMID 18046958.
- ^ Singh, Vinayak; Donini, Stefano; Pacitto, Angela; Sala, Claudia; Hartkoorn, Ruben C.; Dhar, Neeraj; Keri, Gyorgy; Ascher, David B.; Mondésert, Guillaume (2017-01-13). "The Inosine Monophosphate Dehydrogenase, GuaB2, Is a Vulnerable New Bactericidal Drug Target for Tuberculosis". ACS Infectious Diseases (dalam bahasa Inggris). 3 (1): 5–17. doi:10.1021/acsinfecdis.6b00102. ISSN 2373-8227. PMC 5241705
 . PMID 27726334.
. PMID 27726334.
- ^ Hedstrom, L.; Liechti, G.; Goldberg, J. B.; Gollapalli, D. R. (2011). "The antibiotic potential of prokaryotic IMP dehydrogenase inhibitors". Current Medicinal Chemistry. 18 (13): 1909–1918. doi:10.2174/092986711795590129. ISSN 1875-533X. PMC 5036587
 . PMID 21517780.
. PMID 21517780.
- ^ Kim EJ, Um SJ (2008). "SIRT1: roles in aging and cancer". BMB Rep. 41 (11): 751–6. doi:10.5483/BMBRep.2008.41.11.751. PMID 19017485.
- ^ Valenzano DR, Terzibasi E, Genade T, Cattaneo A, Domenici L, Cellerino A (2006). "Resveratrol prolongs lifespan and retards the onset of age-related markers in a short-lived vertebrate". Curr. Biol. 16 (3): 296–300. doi:10.1016/j.cub.2005.12.038. PMID 16461283.
- ^ Gertz, Melanie; Nguyen, Giang Thi Tuyet; Fischer, Frank; Suenkel, Benjamin; Schlicker, Christine; Fränzel, Benjamin; Tomaschewski, Jana; Aladini, Firouzeh; Becker, Christian (2012). "A molecular mechanism for direct sirtuin activation by resveratrol". PloS One. 7 (11): e49761. doi:10.1371/journal.pone.0049761. ISSN 1932-6203. PMC 3504108
 . PMID 23185430.
. PMID 23185430.
- ^ Iside, Concetta; Scafuro, Marika; Nebbioso, Angela; Altucci, Lucia (2020-08-07). "SIRT1 Activation by Natural Phytochemicals: An Overview". Frontiers in Pharmacology. 11: 1225. doi:10.3389/fphar.2020.01225. ISSN 1663-9812. PMC 7426493
 . PMID 32848804.
. PMID 32848804.
- ^ Moraes, Daniel Silva; Moreira, Daniele Cristina; Andrade, João Marcus Oliveira; Santos, Sérgio Henrique Sousa (2020-12). "Sirtuins, brain and cognition: A review of resveratrol effects". IBRO Reports (dalam bahasa Inggris). 9: 46–51. doi:10.1016/j.ibror.2020.06.004. PMC 7733131
 .
.
- ^ Gomes AP, Price NL, Ling AJ, Moslehi JJ, Montgomery MK, Rajman L, White JP, Teodoro JS, Wrann CD, Hubbard BP, Mercken EM, Palmeira CM, de Cabo R, Rolo AP, Turner N, Bell EL, Sinclair DA (19 December 2013). "Declining NAD+ Induces a Pseudohypoxic State Disrupting Nuclear-Mitochondrial Communication during Aging". Cell. 155 (7): 1624–1638. doi:10.1016/j.cell.2013.11.037. PMC 4076149
 . PMID 24360282.
. PMID 24360282.
- ^ Sorci, Leonardo; Pan, Yongping; Eyobo, Yvonne; Rodionova, Irina; Huang, Nian; Kurnasov, Oleg; Zhong, Shijun; MacKerell, Alexander D.; Zhang, Hong (2009-08-28). "Targeting NAD biosynthesis in bacterial pathogens: Structure-based development of inhibitors of nicotinate mononucleotide adenylyltransferase NadD". Chemistry & Biology. 16 (8): 849–861. doi:10.1016/j.chembiol.2009.07.006. ISSN 1879-1301. PMC 2770502
 . PMID 19716475.
. PMID 19716475.
- ^ Passalacqua, Karla D.; Charbonneau, Marie-Eve; O'Riordan, Mary X. D. (2016-06). "Bacterial Metabolism Shapes the Host-Pathogen Interface". Microbiology Spectrum. 4 (3). doi:10.1128/microbiolspec.VMBF-0027-2015. ISSN 2165-0497. PMC 4922512
 . PMID 27337445.
. PMID 27337445.
- ^ Michels, Paul A. M.; Avilán, Luisana (2011-10). "The NAD+ metabolism of Leishmania, notably the enzyme nicotinamidase involved in NAD+ salvage, offers prospects for development of anti-parasite chemotherapy: NAD+ metabolism as anti-parasite drug target". Molecular Microbiology (dalam bahasa Inggris). 82 (1): 4–8. doi:10.1111/j.1365-2958.2011.07810.x.
- ^ Boshoff, Helena I. M.; Xu, Xia; Tahlan, Kapil; Dowd, Cynthia S.; Pethe, Kevin; Camacho, Luis R.; Park, Tae-Ho; Yun, Chang-Soo; Schnappinger, Dirk (2008-07-11). "Biosynthesis and recycling of nicotinamide cofactors in mycobacterium tuberculosis. An essential role for NAD in nonreplicating bacilli". The Journal of Biological Chemistry. 283 (28): 19329–19341. doi:10.1074/jbc.M800694200. ISSN 0021-9258. PMC 2443648
 . PMID 18490451.
. PMID 18490451.
- ^ Zapata-Pérez, Rubén; Martínez-Moñino, Ana-Belén; García-Saura, Antonio-Ginés; Cabanes, Juana; Takami, Hideto; Sánchez-Ferrer, Álvaro (2017-07-27). Menéndez-Arias, Luis, ed. "Biochemical characterization of a new nicotinamidase from an unclassified bacterium thriving in a geothermal water stream microbial mat community". PLOS ONE (dalam bahasa Inggris). 12 (7): e0181561. doi:10.1371/journal.pone.0181561. ISSN 1932-6203. PMC 5531466
 . PMID 28750065.
. PMID 28750065.
- ^ "Meningitis Lab Manual: ID and Characterization of Hib | CDC". www.cdc.gov (dalam bahasa Inggris). 2022-01-05. Diakses tanggal 2022-03-05.
- ^ Harden, A; Young, WJ (24 October 1906). "The alcoholic ferment of yeast-juice Part II.--The coferment of yeast-juice". Proceedings of the Royal Society of London. Series B, Containing Papers of a Biological Character. 78 (526): 369–375. doi:10.1098/rspb.1906.0070. JSTOR 80144.
- ^ "Fermentation of sugars and fermentative enzymes" (PDF). Nobel Lecture, 23 May 1930. Nobel Foundation. Diarsipkan dari versi asli (PDF) tanggal 27 September 2007. Diakses tanggal 2007-09-30.
- ^ Warburg O, Christian W (1936). "Pyridin, der wasserstoffübertragende bestandteil von gärungsfermenten (pyridin-nucleotide)" [Pyridin, the hydrogen-transferring component of the fermentation enzymes (pyridine nucleotide)]. Biochemische Zeitschrift (dalam bahasa Jerman). 287: 291. doi:10.1002/hlca.193601901199.
