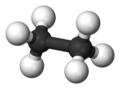
Etana
| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Etana[1]
| |||
| Nama IUPAC (sistematis)
Dikarban (tidak disarankan[1]) | |||
| Nama lain
dimetil; etil hidrida; metilmetana
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| Referensi Beilstein | 1730716 | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
| Referensi Gmelin | 212 | ||
| MeSH | Ethane | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
| Nomor UN | 1035 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C2H6 | |||
| Massa molar | 30,07 g·mol−1 | ||
| Penampilan | Gas tak berwarna | ||
| Bau | Tak berbau | ||
| Densitas | |||
| Titik lebur | 90,4 K | ||
| Titik didih | 184,6 K | ||
| 56,8 mg L−1[4] | |||
| Tekanan uap | 3,8453 MPa (pada 21,1 °C) | ||
| kH | 19 nmol Pa−1 kg−1 | ||
| Keasaman (pKa) | 50 | ||
| Kebasaan (pKb) | -36 | ||
| -37,37·10−6 cm3/mol | |||
| Termokimia | |||
| Kapasitas kalor (C) | 52,49 J K−1 mol−1 | ||
| Entalpi pembentukan standar (ΔfH |
−84 kJ mol−1 | ||
| Entalpi pembakaran standar ΔcH |
(−1561,0)–(−1560,4) kJ mol−1 | ||
| Bahaya | |||
| Lembar data keselamatan | inchem.org | ||
| Piktogram GHS | 
| ||
| Keterangan bahaya GHS | {{{value}}} | ||
| H220, H280 | |||
| P210, P410+403 | |||
| Titik nyala | −135 °C (−211 °F; 138 K) | ||
| 472 °C (882 °F; 745 K) | |||
| Ambang ledakan | 2,9–13% | ||
| Senyawa terkait | |||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Etana adalah sebuah senyawa kimia dengan rumus kimia C2H6. Senyawa ini merupakan alkana dengan dua karbon, dan merupakan hidrokarbon alifatik. Dalam temperatur dan tekanan standar, etana merupakan gas yang tak berwarna dan tak berbau. Dalam industri etana dihasilkan dengan cara diisolasi dari gas alam, dan sebagai hasil samping dari penyulingan minyak. Penggunaan utamanya adalah sebagai bahan baku produksi etilena.
Senyawa terkait dapat dibentuk dengan mengganti atom hidrogen dengan gugus fungsional lainnya; moietas etana disebut gugus etil. Misalnya, gugus etil yang berikatan dengan gugus hidroksil menghasilkan etanol, alkohol dalam minuman.
Sejarah
[sunting | sunting sumber]Etana pertama kali disintesis pada tahun 1834 oleh Michael Faraday, melalui elektrolisis larutan kalium asetat. Dia mengira produk hidrokarbon dari reaksi ini adalah metana dan tidak menelitinya lebih lanjut.[5] Selama periode 1847-1849, dalam upaya untuk membuktikan teori radikal kimia organik, Hermann Kolbe dan Edward Frankland menghasilkan etana dengan mereduksi propionitril (etil sianida)[6] dan etil iodida[7] dengan logam kalium, dan, seperti yang dilakukan Faraday, dengan elektrolisis larutan asetat dalam air. Namun, mereka menganggap produk reaksi ini adalah radikal metil padahal yang dihasilkan adalah dimer dari metil, yaitu etana. Kesalahan ini diperbaiki oleh Carl Schorlemmer pada tahun 1864, yang menunjukkan bahwa produk dari semua reaksi ini sebenarnya adalah etana.[8]
Nama etana berasal dari Tata nama IUPAC untuk kimia organik. "Eth-" berasal dari bahasa Jerman untuk alkohol yang dapat diminum (etanol),[9] dan "-ana" mengacu pada adanya ikatan tunggal antara atom karbon.
Sifat
[sunting | sunting sumber]Pada suhu dan tekanan standar, etana adalah gas tak berwarna dan tidak berbau. Ia memiliki titik didih −885 °C (−1.561 °F; −612 K) dan titik lebur −1.828 °C (−3.258 °F; −1.555 K). Etana padat ada dalam beberapa modifikasi.[10] Pada pendinginan di bawah tekanan normal, modifikasi pertama yang muncul adalah kristal plastik, yang membentuk sistem kristal kubik. Dalam bentuk ini, posisi atom hidrogen tidak tetap; molekul dapat berputar bebas di sekitar sumbu panjang. Mendinginkan etana ini di bawah kira-kira 899 K (626 °C; 1.159 °F) mengubahnya menjadi etana II yang berupa monoklinik dan bersifat metastabil.[11] Etana hanya sangat sedikit larut dalam air.
Kimia
[sunting | sunting sumber]Etana dapat dipandang sebagai dua gugus metil yang bergabung, yaitu dimer gugus metil. Etana dapat dengan mudah disintesis di laboratorium dengan elektrolisis Kolbe. Dalam teknik ini, dilakukan elektrolisis larutan garam asetat dalam air. Pada anoda, asetat dioksidasi untuk menghasilkan karbon dioksida dan radikal metil, dan radikal metil yang sangat reaktif bergabung untuk menghasilkan etana:
Metode lain yang secara konseptual mirip adalah dengan oksidasi anhidrida asetat menggunakan peroksida.
Kimia etana utamanya melibatkan reaksi radikal bebas. Etana dapat bereaksi dengan halogen, terutama klor dan brom, melalui halogenasi radikal bebas. Reaksi ini berlangsung melalui propagasi radikal etil:
Oleh karena etana terhalogenasi dapat mengalami halogenasi radikal bebas lanjutan, maka proses ini menghasilkan campuran beberapa produk terhalogenasi. Dalam industri kimia, reaksi kimia selektif lebih banyak digunakan untuk memproduksi tertentu haloalkana dengan dua atom karbon.
Pembakaran
[sunting | sunting sumber]Proses pembakaran sempurna etana membebaskan panas sebesar 1559,7 kJ/mol, atau 51,9 kJ/g, dan menghasilkan karbon dioksida dan air sesuai dengan persamaan kimia
Pembakaran juga dapat terjadi tanpa oksigen berlebih, membentuk campuran karbon amorf dan karbon monoksida.
- 2 C + 3 O → 4 C + 6 H + energi
- 2 C + 5 O → 4 CO + 6 H + energi
- 2 C + 4 O → 2 C + 2 CO + 6 H + energi dll.
Pembakaran terjadi melalui serangkaian reaksi radikal bebas yang rumit. Simulasi komputer atas kinetika kimia pembakaran etana telah menyertakan ratusan reaksi yang ada. Sebuah tahap penting dari reaksi pembakaran etana adalah bergabungnya radikal etil dengan oksigen, dan pecahnya peroksida yang dihasilkan menjadi radikal etoksi dan hidroksil.
Senyawa karbon yang terbentuk dari proses pembakaran etana tak sempurna adalah karbon tunggal seperti karbon monoksida dan formaldehida. Salah satu reaksi yang ditempuh untuk menghasilkan produk karbon tunggal ini adalah dekomposisi radikal etoksi menjadi radikal metil dan formaldehida, yang kemudian dioksidasi lebih lanjut:
- C2H5O• → CH3• + CH2O
Produk utama yang mengandung karbon hasil pembakaran tidak sempurna etana adalah senyawa karbon tunggal seperti karbon monoksida dan formaldehida. Salah satu rute penting di mana ikatan karbon-karbon dalam etana rusak, dan menghasilkan produk karbon tunggal, adalah dekomposisi radikal etoksi menjadi radikal metil dan formaldehida, yang pada gilirannya dapat mengalami oksidasi lebih lanjut.
- C• → CH• + CH
Beberapa produk minor dalam pembakaran etanol yang tidak sempurna meliputi asetaldehida, metana, metanol, dan etanol. Pada suhu yang lebih tinggi, terutama pada kisaran 600-900 °C (1,112-1,652 °F), etilen adalah produk yang signifikan. Reaksinya sebagai berikut:
Reaksi serupa (dengan pereaksi selain oksigen sebagai abstraktor hidrogen) adalah reaksi yang terlibat dalam produksi etilena dari etana pada proses perengkahan kukus.
Barier etana
[sunting | sunting sumber]
Memutar substruktur molekuler di sekitar ikatan yang mudah pecah umumnya membutuhkan energi. Energi minimum untuk menghasilkan rotasi ikatan 360 derajat disebut penghalang rotasi (bahasa Inggris: rotational barrier).
Etana memberikan contoh klasik dan sederhana tentang penghalang rotasi semacam itu, yang terkadang disebut "penghalang etana". Di antara bukti eksperimental awal penghalang ini (lihat diagram di sebelah kiri) diperoleh dengan memodelkan entropi etana.[12] Tiga hidrogen di setiap ujung bebas untuk berputar di sekitar ikatan pusat karbon-karbon bila diberi energi yang cukup untuk mengatasi penghalang. Asal usul fisik penghalang masih belum sepenuhnya terpecahkan,[13] meskipun tolakan tumpang tindih (pertukaran)[14] antar atom hidrogen pada ujung molekul yang berlawanan mungkin adalah kandidat terkuat untuk fenomena tersebut, dengan memberikan efek hiperkonjugasi yang menstabilkan pada konformasi steger.[15] Namun, metode teoretis yang menggunakan titik awal yang tepat (orbital ortogonal) menemukan bahwa hiperkonjugasi adalah faktor yang terpenting terkait asal penghalang rotasi etana.[16][17]
Selama tahun 1890-1891, kimiawan memperkirakan bahwa molekul etana lebih menyukai konformasi steger dengan dua ujung molekul saling miring satu sama lain.[18][19][20][21]
Produksi
[sunting | sunting sumber]Setelah metana, etana adalah komponen terbesar kedua dalam gas alam. Gas alam dari berbagai ladang gas memiliki kandungan etana bervariasi, mulai dari kurang dari 1% sampai lebih dari 6% volume. Sebelum tahun 1960an, etana dan molekul yang lebih besar biasanya tidak dipisahkan dari komponen metana gas alam, namun dibakar bersamaan dengan metana sebagai bahan bakar. Saat ini, etana adalah bahan baku petrokimia penting dan dipisahkan dari komponen gas alam lainnya di ladang gas yang dikelola dengan baik.
Etana juga dapat dipisahkan dari gas petroleum, campuran gas hidrokarbon yang dihasilkan sebagai produk sampingan dari penyulingan minyak bumi. Ekonomi bangunan dan pabrik pengolahan bisa berubah. Jika nilai relatif pengiriman gas alam mentah ke konsumen melebihi nilai ekstraksi etana, ekstraksi etana mungkin tidak berjalan, yang dapat menyebabkan masalah operasional dalam mengelola perubahan kualitas gas di sistem hilir.
Pemisahan etana dari metana yang paling efisien adalah dengan mencairkannya pada temperatur kriogenik. Terdapat berbagai strategi pendinginan, antara lain: proses yang paling ekonomis saat ini yang digunakan secara luas adalah menggunakan turboexpander, yang dapat memperoleh lebih dari 90% etana dalam gas alam. Dalam proses ini, gas dingin diekspansi melalui turbin, kemudian suhu diturunkan hingga sekitar −100 °C (−148 °F). Pada suhu serendah ini, gas metana dapat dipisahkan dari cairan etana dan hidrokarbon yang lebih berat dengan distilasi. Distilasi lanjutan kemudian dilakukan untuk memisahkan etana dari propana dan hidrokarbon yang lebih berat.
Kegunaan
[sunting | sunting sumber]Kegunaan utama etana adalah sebagai bahan baku untuk produksi etena (etilena) (C2H4) melalui perengkahan kukus (steam cracking). Bila diencerkan dengan kukus dan dipanaskan sebentar hingga suhu yang sangat tinggi (900 °C atau lebih), hidrokarbon berat terurai menjadi hidrokarbon yang lebih ringan, dan hidrokarbon jenuh menjadi tidak jenuh. Etana merupakan bahan yang baik dalam produksi etilena karena hasil reaksi perengkahan kukus etana menghasilkan persentase etilena yang cukup banyak, sedangkan reaksi hidrokarbon lain yang lebih berat menghasilkan produk berupa campuran yang memiliki sedikit etilena, dan lebih banyak mengandung alkena yang lebih berat (olefin) seperti propena (propilena) dan butadiena, serta hidrokarbon aromatik.
Secara eksperimental, etana sedang diteliti sebagai bahan baku untuk bahan kimia komoditas lainnya. Klorinasi oksidatif etana telah lama muncul menjadi cara pembuatan vinil klorida yang lebih ekonomis daripada klorinasi etena. Banyak proses untuk menghasilkan reaksi ini yang telah dipatenkan, tapi selektivitasnya terhadap vinil klorida yang rendah dan kondisi reaksi yang korosif (khususnya, reaksi yang menggunakan campuran yang mengandung asam klorida pada suhu lebih dari 500 °C) telah memperkecil potensi komersialisasi sebagian besar reaksi tersebut. Saat ini, INEOS mengoperasikan pilot plant yang mengkonversi 1000 ton tahun etana menjadi vinil klorida di Wilhelmshaven, Jerman.
Demikian pula, perusahaan Arab Saudi, SABIC, telah mengumumkan pembangunan pabrik untuk menghasilkan asam asetat 30.000 ton per tahun dengan cara oksidasi etana di Yanbu. Kelayakan ekonomi dari proses ini bergantung pada rendahnya biaya etana dekat ladang minyak Saudi, dan mungkin tidak kompetitif dengan karbonilasi metanol di tempat lain di dunia.
Etana dapat digunakan sebagai zat pendingin dalam sistem pendinginan kriogenik. Pada skala yang jauh lebih kecil, dalam penelitian ilmiah, etana cair digunakan untuk sampel memvitrifikasi air untuk mikroskopi elektron (mikroskop cryo-elektron). Sebuah lapisan tipis air, dengan cepat terbenam dalam etana cair pada suhu -150 °C atau lebih dingin, membeku terlalu cepat agar air bisa mengkristal. Dengan metode pembekuan yang lebih lambat, kristal es dapat mengganggu struktur lunak, sehingga merusak sampel.
Kesehatan dan keselamatan
[sunting | sunting sumber]Etana adalah gas yang mudah terbakar pada suhu kamar. Ia akan membentuk campuran eksplosif bila dicampur dengan udara sebesar 3,0% -12,5% volume.
Perlu beberapa tindakan pencegahan tambahan jika etana disimpan sebagai cairan kriogenik. Kontak langsung dengan etana cair dapat menyebabkan radang dingin parah (frostbite). Ketika mereka menghangat sampai suhu kamar, uap etana cair yang lebih berat daripada udara sehingga bisa mengalir di sepanjang lantai atau tanah, berkumpul di tempat yang rendah; jika uap bertemu dengan sumber pengapian, reaksi kimia dapat menyambar kembali ke sumber etana asal penguapan.
Etana dapat mengusir oksigen dan menyebabkan bahaya asfiksia. Etetana tidak menimbulkan risiko toksikologi akut maupun kronik. Etetana bukan karsinogen.[22]
Etana atmosfer dan ekstrateresterial
[sunting | sunting sumber]
Etana muncul sebagai jejak gas di atmosfer bumi, saat ini konsentrasi di permukaan laut adalah 0,5 ppb,[23] meskipun konsentrasi di era pra-industri cenderung lebih rendah karena proporsi etana yang signifikan di atmosfer hari ini mungkin berasal dari bahan bakar fosil. Jumlah etana global bervariasi dari waktu ke waktu, kemungkinan karena pembakaran di ladang gas alam.[24] Tingkat emisi etana global menurun dari tahun 1984 sampai 2010,[24] meskipun produksi shale gas meningkat di Bakken Formation, A.S. telah menahan penurunan hingga setengahnya.[25][26]
Meskipun etana adalah gas rumah kaca, namun jauh lebih sedikit daripada metana dan juga kurang efisien dibandingkan dari sisi massa. Etana terdeteksi sebagai komponen renik di atmosfer empat planet raksasa, dan di atmosfer bulan Saturnus, Titan.[27]
Etana hadir di atmosfer ini hasil dari aksi fotokimia matahari terhadap gas metana: foton ultraviolet dengan panjang gelombang yang lebih pendek dari 160 nm dapat memecah molekul metana menjadi radikal metil dan atom hidrogen melalui proses foto-disosiasi. Bila dua radikal metil bergabung kembali, hasilnya adalah etana:
- CH → CH• + •H
- CH• + •CH → C
Pernah muncul hipotesis secara luas bahwa etana diproduksi dengan cara berikut di Titan: hujan turun ke permukaan bulan, dan dari waktu ke waktu telah terakumulasi menjadi lautan hidrokarbon yang banyak meliputi permukaan bulan. Observasi teleskopik inframerah memunculkan keraguan yang signifikan atas hipotesis ini, dan penyelidikan wahana Huygens, yang mendarat di Titan pada tahun 2005, gagal mengamati cairan permukaan apapun, meskipun foto itu merupakan foto saluran drainase kering saat ini. Pada bulan Desember 2007 wahana Cassini menemukan setidaknya satu danau di kutub selatan Titan, sekarang disebut Ontario Lacus, karena luasnya yang mirip dengan Danau Ontario di Bumi (sekitar 20.000 km2). Analisis data spektroskopi inframerah lebih lanjut yang disajikan pada bulan Juli 2008[28] memberikan bukti kuat keberadaan etana cair di Ontario Lacus.
Pada tahun 1996, etana terdeteksi pada Komet Hyakutake,[29] dan sejak saat itu telah terdeteksi di beberapa komet lainnya. Keberadaan etana di badan-badan tata surya yang jauh dapat menjadi petunjuk etana sebagai komponen primordial dari nebula surya, asal matahari dan planet-planet diyakini terbentuk.
Pada tahun 2006, Dale Cruikshank dari Pusat Penelitian NASA/Ames (penyusun New Horizons) dan rekan-rekannya mengumumkan penemuan spektroskopi etana di permukaan Pluto.[30]
Referensi
[sunting | sunting sumber]- ^ a b Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014. hlm. 4. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
Seperti lainnya, nama ‘etana’, ‘propana’, dan ‘butana’ tidak pernah digantikan dengan nama sistematis ‘dikarban’, ‘trikarban’, dan ‘tetrakarban’ seperti disarankan untuk analogi dengan silan, ‘disilan’; fosfan, ‘trifosfane’; dan sulfan, ‘tetrasulfan’.
- ^ "Ethane – Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 16 September 2004. Diakses tanggal 7 December 2011.
- ^ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (edisi ke-86). Boca Raton (FL): CRC Press. hlm. 3.22. ISBN 0-8493-0486-5.
- ^ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics (edisi ke-86). Boca Raton (FL): CRC Press. hlm. 8.88. ISBN 0-8493-0486-5.
- ^ Faraday, Michael (1834). "Experimental researches in electricity: Seventh series". Philosophical Transactions. 124: 77–122. doi:10.1098/rstl.1834.0008.
- ^ Kolbe, Hermann; Frankland, Edward (1849). "On the products of the action of potassium on cyanide of ethyl". Journal of the Chemical Society. 1: 60–74. doi:10.1039/QJ8490100060.
- ^ Frankland, Edward (1850). "On the isolation of the organic radicals". Journal of the Chemical Society. 2 (3): 263–296. doi:10.1039/QJ8500200263.
- ^ Schorlemmer, Carl (1864). "Ueber die Identität des Aethylwasserstoffs und des Methyls". Annalen der Chemie und Pharmacie. 132 (2): 234. doi:10.1002/jlac.18641320217.
- ^ "the definition of ethyl". Dictionary.com. Diakses tanggal 2016-03-12.
- ^ Van Nes, G.J.H.; Vos, A. (1978). "Single-crystal structures and electron density distributions of ethane, ethylene and acetylene. I. Single-crystal X-ray structure determinations of two modifications of ethane" (PDF). Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 34 (6): 1947. doi:10.1107/S0567740878007037.
- ^ "Ethane as a solid". Paarpraxis-rheinmain.de. Diarsipkan dari versi asli tanggal 2017-05-10. Diakses tanggal 2016-12-16.
- ^ Kemp, J. D.; Pitzer, Kenneth S. (1937). "The Entropy of Ethane and the Third Law of Thermodynamics. Hindered Rotation of Methyl Groups". Journal of the American Chemical Society. 59 (2): 276. doi:10.1021/ja01281a014.
- ^ Ercolani, G. (2005). "Determination of the Rotational Barrier in Ethane by Vibrational Spectroscopy and Statistical Thermodynamics". J. Chem. Educ. 82 (11): 1703–1708. Bibcode:2005JChEd..82.1703E. doi:10.1021/ed082p1703.
- ^ Pitzer, R.M. (1983). "The Barrier to Internal Rotation in Ethane". Acc. Chem. Res. 16 (6): 207–210. doi:10.1021/ar00090a004.
- ^ Mo, Y.; Wu, W.; Song, L.; Lin, M.; Zhang, Q.; Gao, J. (2004). "The Magnitude of Hyperconjugation in Ethane: A Perspective from Ab Initio Valence Bond Theory". Angew. Chem. Int. Ed. 43 (15): 1986–1990. doi:10.1002/anie.200352931.
- ^ Pophristic, V.; Goodman, L. (2001). "Hyperconjugation not steric repulsion leads to the staggered structure of ethane". Nature. 411 (6837): 565–8. doi:10.1038/35079036. PMID 11385566.
- ^ Schreiner, P. R. (2002). "Teaching the right reasons: Lessons from the mistaken origin of the rotational barrier in ethane". Angewandte Chemie International Edition. 41 (19): 3579–81, 3513. doi:10.1002/1521-3773(20021004)41:19<3579::AID-ANIE3579>3.0.CO;2-S. PMID 12370897.
- ^ Bischoff, CA (1890). "Ueber die Aufhebung der freien Drehbarkeit von einfach verbundenen Kohlenstoffatomen". Chem. Ber. 23: 623. doi:10.1002/cber.18900230197.
- ^ Bischoff, CA (1891). "Theoretische Ergebnisse der Studien in der Bernsteinsäuregruppe". Chem. Ber. 24: 1074. doi:10.1002/cber.189102401195.
- ^ Bischoff, CA (1891). "Die dynamische Hypothese in ihrer Anwendung auf die Bernsteinsäuregruppe". Chem. Ber. 24: 1085. doi:10.1002/cber.189102401196.
- ^ Bischoff, C.A.; Walden, P. (1893). "Die Anwendung der dynamischen Hypothese auf Ketonsäurederivate". Berichte der deutschen chemischen Gesellschaft. 26 (2): 1452. doi:10.1002/cber.18930260254.
- ^ Vallero, Daniel (June 7, 2010). "Cancer Slope Factors". Environmental Biotechnology: A Biosystems Approach. Academic Press. hlm. 641. doi:10.1016/B978-0-12-375089-1.10014-5.
- ^ Trace gases Diarsipkan 2008-12-22 di Wayback Machine.. Atmosphere.mpg.de. Retrieved on 2011-12-08.
- ^ a b Simpson, Isobel J.; Sulbaek Andersen, Mads P.; Meinardi, Simone; Bruhwiler, Lori; Blake, Nicola J.; Helmig, Detlev; Rowland, F. Sherwood; Blake, Donald R. (2012). "Long-term decline of global atmospheric ethane concentrations and implications for methane". Nature. 488 (7412): 490–494. doi:10.1038/nature11342. PMID 22914166.
- ^ Kort, E. A.; Smith, M. L.; Murray, L. T.; Gvakharia, A.; Brandt, A. R.; Peischl, J.; Ryerson, T. B.; Sweeney, C.; Travis, K. (2016). "Fugitive emissions from the Bakken shale illustrate role of shale production in global ethane shift". Geophysical Research Letters. 43: 4617–4623. doi:10.1002/2016GL068703.
- ^ "One oil field a key culprit in global ethane gas increase". University of Michigan. April 26, 2016.
- ^ Brown, Bob; et al. (2008). "NASA Confirms Liquid Lake on Saturn Moon". NASA Jet Propulsion Laboratory. Diarsipkan dari versi asli tanggal 2011-06-05. Diakses tanggal 2017-04-19.
- ^ Brown, R. H.; Soderblom, L. A.; Soderblom, J. M.; Clark, R. N.; Jaumann, R.; Barnes, J. W.; Sotin, C.; Buratti, B.; et al. (2008). "The identification of liquid ethane in Titan's Ontario Lacus". Nature. 454 (7204): 607–10. Bibcode:2008Natur.454..607B. doi:10.1038/nature07100. PMID 18668101.
- ^ Mumma, Michael J.; et al. (1996). "Detection of Abundant Ethane and Methane, Along with Carbon Monoxide and Water, in Comet C/1996 B2 Hyakutake: Evidence for Interstellar Origin". Science. 272 (5266): 1310–1314. Bibcode:1996Sci...272.1310M. doi:10.1126/science.272.5266.1310. PMID 8650540.
- ^ Stern, A. (November 1, 2006). "Making Old Horizons New". The PI's Perspective. Johns Hopkins University Applied Physics Laboratory. Diarsipkan dari versi asli tanggal 2011-08-20. Diakses tanggal 2007-02-12.
Pranala luar
[sunting | sunting sumber]- (Inggris) International Chemical Safety Card 0266
- (Inggris) Market-Driven Evolution of Gas Processing Technologies for NGLs
- (Inggris) Staggered and eclipsed ethane Diarsipkan 2009-02-04 di Wayback Machine.