Natrium borohidrida
| |

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Natrium tetrahidridoborat (1–) | |
| Nama IUPAC (sistematis)
Natrium boranuida | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
| Referensi Gmelin | 23167 |
| MeSH | Sodium+borohydride |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 1426 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| NaBH4 | |
| Massa molar | 37.83 g/mol |
| Penampilan | kristal putih higroskopis |
| Densitas | 1.0740 g/cm3 |
| Titik lebur | 400 °C (752 °F; 673 K)[1] |
| Titik didih | 500 °C (932 °F; 773 K) (decomposes)[1] |
| larut, bereaksi dengan air | |
| Kelarutan | larut dalam amonia cair, amina, piridina |
| Bahaya | |
| H260, H301, H311, H314 | |
| P223, P231, P232, P280, P301+310, P370+378, P422 | |
| Titik nyala | 70 °C (158 °F; 343 K) |
| ca. 220 °C (428 °F; 493 K) | |
| Ambang ledakan | 3% |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
160 mg/kg (Oral - Tikus 230 mg/kg (Dermal - Kelinci) |
| Senyawa terkait | |
Anion lain
|
Natrium sianoborohidrida Natrium hidrida Natrium borat Boraks |
Kation lainnya
|
Litium borohidrida |
Senyawa terkait
|
Litium aluminium hidrida Natrium triasetoksiborohidrida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
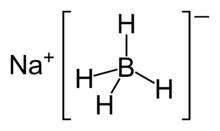
Natrum borohidrida, dikenal pula sebagai natrium tetrahidridoborat dan natrium tetrahidroborat,[2] adalah suatu senyawa anorganik dengan rumus kimia NaBH4. Padatan putih ini, biasanya berbentuk bubuk, adalah reduktor serbaguna yang diaplikasikan secara luas dalam kimia, baik dalam laboratorium dan pada skala teknis. Senyawa ini telah diuji sebagai perlakuan awal untuk pulp kayu, tetapi terlalu mahal untuk dikomersialkan.[3][4] Senyawa ini larut dalam alkohol dan beberapa eter namun bereaksi dengan air dengan ketiadaan basa.[5]
Senyawa ini ditemukan pada tahun 1940-an oleh H. I. Schlesinger, yang memimpin sebuah tim yang mengembangkan logam borohidrida untuk aplikasi masa perang (khususnya, mencari senyawa uranium yang lebih menguap dibandingkan heksafluorida yang akan digunakan dalam pemisahan isotop berdasarkan difusi gas; penelitian ini tidak menghasilkan hasil yang bermanfaat).[6] Pekerjaan mereka dideklasifikasi dan diterbitkan hanya pada tahun 1953.
Sifat
[sunting | sunting sumber]| Pelarut | Kelarutan (g/100 mL)[5] |
|---|---|
| MeOH | 13 |
| EtOH | 3.16 |
| Diglyme | 5.15 |
| Et2O | tidak larut |
Natrium borohidrida adalah bubuk tidak berbau mikrokristalin berwarna putih hingga abu-abu-putih yang sering membentuk gumpalan. Hal ini dapat dimurnikan dengan rekristalisasi dari diglim hangat (50 °C).[7] Natrium borohidrida larut dalam pelarut protik seperti air dan alkohol rendah; ia juga akan bereaksi dengan pelarut ini untuk menghasilkan H2; Namun, reaksi ini cukup lambat. Penguraian lengkap dalam berlebih metanol dapat berlangsung hampir 90 menit pada 20 °C.[8] Ia akan terurai dalam larutan berair netral atau asam namun stabil pada pH 14.[5] Kondisi ini dapat dimanfaatkan untuk memungkinkan natrium borohidrida untuk bereaksi dengan cara yang homogen, dengan mengurangi masa hidup yang diperdagangkan terhadap peningkatan reaktivitas.
Struktur
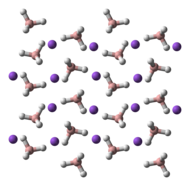
[sunting | sunting sumber]NaBH4 adalah suatu garam, yang terdiri dari anion BH4− tetrahedral. Padatannya diketahui terdapat sebagai tiga polimorf: α, β dan γ. Fase yang stabilpada suhu dan tekanan ruang adalah α-NaBH4, yang berbentuk kubik dan mengadopsi struktur jenis-NaCl, dalam grup ruang Fm3m. Pada tekanan 6.3 GPa, struktur tersebut berubah menjadi tetragonal β-NaBH4 (grup ruang P421c) dan pada 8.9 GPa, ortorombik γ-NaBH4 (gugus ruang Pnma) menjadi yang paling stabil.[9][10][11]
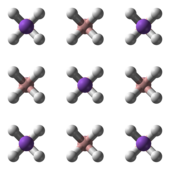 |
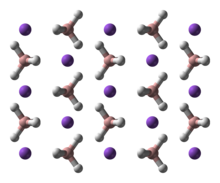 |
 |
Sintesis dan penanganan
[sunting | sunting sumber]Natrium borohidrida disiapkan secara industri mengikuti metode asli Schlesinger: natrium hidrida diperlakukan dengan trimetil borat pada 250–270 °C:
- B (OCH3)3 + 4 NaH → NaBH4 + 3 NaOCH3
Jutaan kilogram diproduksi setiap tahunnya, jauh melebihi tingkat produksi agen pereduksi hidrida lainnya.[3] Natrium borohidrida juga dapat diproduksi melalui perlakuan NaH pada bubuk kaca borosilikat.[12]
Aplikasi
[sunting | sunting sumber]Aplikasi utama natrium borohidrida adalah produksi natrium ditionit dari sulfur dioksida: Natrium ditionit digunakan sebagai agen pemutih untuk pulp kayu dan dalam industri pewarnaan.
Natrium borohidrida mereduksi aldehida serta keton untuk menghasilkan alkohol terkait. Reaksi ini digunakan dalam produksi berbagai antibiotik termasuk kloramfenikol, dihidrostreptomisin, serta tiofenikol. Berbagai steroid serta vitamin A dipreparasi dengan menggunakan natrium borohidrida dalam setidaknya satu tahap reaksi.
Natrium borohidrida digunakan sebagai reduktor dalam sintesis nanopartikel emas.[13]
Natrium borohidrida telah dianggap sebagai kandidat penyimpanan hidrogen keadaan padat. Meskipun suhu dan tekanan praktis untuk penyimpanan hidrogen belum tercapai, pada tahun 2012 suatu inti-kerangka struktur nano natrium borohidrida berhasil digunakan untuk menyimpan, melepas dan menyerap kembali hidrogen dalam kondisi sedang.[14]
Keamanan
[sunting | sunting sumber]Natrium borohidrida merupakan sumber garam borat basa yang dapat bersifat korosif, serta hidrogen atau diborana, yang keduanya mudah terbakar. pengapian spontan bisa diakibatkan dari larutan natrium borohidrida dalam dimetilformamida.
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ a b MSDS data (carl roth)
- ^ Busch, D.H. (2009). Inorganic Syntheses. 20. Wiley. hlm. 137. ISBN 9780470132869. Diakses tanggal 20 May 2015.
- ^ a b Peter Rittmeyer, Ulrich Wietelmann "Hydrides" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a13_199
- ^ Istek, A. and Gonteki, E. "Utilization of sodium borohydride (NaBH4) in kraft pulping process." Retrieved online on 25 September 2014 at http://www.jeb.co.in/journal_issues/200911_nov09/paper_05.pdf.
- ^ a b c Banfi, L.; Narisano, E.; Riva, R.; Stiasni, N.; Hiersemann, M. "Sodium Borohydride" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. doi:10.1002/047084289X.rs052.
- ^ Schlesinger, H. I.; Brown, H. C.; Abraham, B.; Bond, A. C.; Davidson, N.; Finholt, A. E.; Gilbreath, J. R.; Hoekstra, H.; Horvitz, L.; Hyde, E. K.; Katz, J. J.; Knight, J.; Lad, R. A.; Mayfield, D. L.; Rapp, L.; Ritter, D. M.; Schwartz, A. M.; Sheft, I.; Tuck, L. D.; Walker, A. O. (1953). "New developments in the chemistry of diborane and the borohydrides. General summary". J. Am. Chem. Soc. 75: 186–90. doi:10.1021/ja01097a049.
- ^ Brown, H. C. “Organic Syntheses via Boranes” John Wiley & Sons, Inc. New York: 1975. ISBN 0-471-11280-1. page 260-1.
- ^ Lo, Chih-ting F.; Karan, Kunal; Davis, Boyd R. "Kinetic Studies of Reaction between Sodium Borohydride and Methanol, Water, and Their Mixtures". Industrial & Engineering Chemistry Research. 46 (17): 5478–5484. doi:10.1021/ie0608861.
- ^ R. S. Kumar; A. L. Cornelius (2005). "Structural transitions in NaBH[sub 4] under pressure". Appl. Phys. Lett. 87 (26): 261916. doi:10.1063/1.2158505.
- ^ Y. Filinchuk; A. V. Talyzin; D. Chernyshov; V. Dmitriev (2007). "High-pressure phase of NaBH4: Crystal structure from synchrotron powder diffraction data". Phys. Rev. B. 76 (9): 092104. doi:10.1103/PhysRevB.76.092104.
- ^ E. Kim; R. Kumar; P. F. Weck; A. L. Cornelius; M. Nicol; S. C. Vogel; J. Zhang; M. Hartl; A. C. Stowe; L. Daemen; Y. Zhao (2007). "Pressure-driven phase transitions in NaBH4: theory and experiments". J. Phys. Chem. B. 111 (50): 13873–13876. doi:10.1021/jp709840w. PMID 18031032.
- ^ Schubert, F.; Lang, K.; Burger, A. "Alkali metal borohydrides" (Bayer), 1960. German patent DE 1088930 19600915 (ChemAbs: 55:120851). Supplement to. to Ger. 1,067,005 (CA 55, 11778i). From the abstract: "Alkali metal borosilicates are treated with alkali metal hydrides in approx. 1:1 ratio at >100 °C with or without H pressure".
- ^ Low and Bansal, 2009
- ^ Stuart Gary, "Hydrogen storage no longer up in the air" dalam ABC Science 16 Agustus 2012, mengutip Christian, Meganne; Aguey-Zinsou, Kondo François (2012). "Core–Shell Strategy Leading to High Reversible Hydrogen Storage Capacity for NaBH4". ACS Nano. American Chemical Society. doi:10.1021/nn3030018. Diakses tanggal 20 Agustus 2012.
Pranala luar
[sunting | sunting sumber]- National Pollutant Inventory – Boron and compounds Diarsipkan 2006-02-09 di Wayback Machine.
- MSDS for Sodium Borohydride Diarsipkan 2013-02-02 di Archive.is
- Materials & Energy Research Institute Tokyo, Ltd. Diarsipkan 2005-03-05 di Wayback Machine.
- Chemo- and stereoselectivity using Borohydride reagents Diarsipkan 2005-12-01 di Wayback Machine.
- Material Safety Data Sheet Diarsipkan 2017-07-10 di Wayback Machine.
