Penyakit paru obstruktif kronis
Artikel ini memberikan informasi dasar tentang topik kesehatan. |
| Penyakit paru obstruktif kronis | |
|---|---|
 | |
| Patologi kasar yang menunjukkan emfisema tipe sentrilobular yang merupakan ciri dari merokok. Tampilan jarak dekat dari terfiksasi, potongan permukaan paru menunjukkan beberapa lubang yang dilapisi deposit karbon hitam yang tebal. | |
| Informasi umum | |
| Spesialisasi | Pulmonologi |
Penyakit paru obstruktif kronis (disingkat PPOK), dikenal juga sebagai penyakit pulmonari obstruktif kronis, atau penyakit saluran udara obstruktif kronis (disingkat PSUOK), adalah sejenis penyakit paru obstruktif yang ditandai dengan keterbatasan aliran udara yang kronis. Biasanya, kondisi ini akan bertambah buruk seiring dengan waktu. Gejala utamanya antara lain adalah sesak napas, batuk, dan produksi sputum/lendir.[1] Kebanyakan penderita bronkitis kronis juga menderita PPOK.[2]
Merokok tembakau adalah sebab paling utama dari PPOK, dan juga beberapa faktor lainnya seperti polusi udara dan genetik yang turut berperan kecil.[3] Di negara-negara berkembang, salah satu sumber polusi udara biasanya adalah api untuk memasak dan pemanas yang berventilasi buruk. Jika terpapar penyebab iritasi ini dalam jangka waktu lama, akan mengakibatkan reaksi inflamasi di paru-paru yang menyebabkan penyempitan saluran udara dan rusaknya jaringan paru yang disebut sebagai emfisema.[4] Diagnonis ini berdasarkan terbatasnya aliran udara saat diukur dengan tes fungsi paru.[5] Berbeda dengan asma, berkurangnya aliran udara tidak membaik secara signifikan ketika dilakukan pengobatan.
PPOK dapat dicegah dengan mengurangi peluang terpapar penyebab-penyebab yang telah diketahui. Hal ini termasuk upaya untuk mengurangi rokok dan memperbaiki kualitas udara di dalam dan luar ruangan. Penanganan PPOK terdiri dari: berhenti merokok, vaksinasi, rehabilitasi, serta sering menghirup bronkodilator dan steroid. Sebagian orang ada yang merasakan perbaikan karena terapi oksigen jangka panjang atau pencangkokan paru.[4] Bagi mereka yang mengalami periode bertambah parah akut, mungkin perlu meningkatkan penggunaan obat-obatan dan perawatan di rumah sakit.
Di dunia, PPOK memengaruhi 329 juta orang atau hampir 5% dari populasi. Pada 2012, PPOK menjadi penyebab kematian nomor tiga, membunuh lebih dari 3 juta orang.[6] Angka kematian ini diperkirakan akan meningkat karena meningkatnya jumlah perokok dan populasi manula di banyak negara.[7] Hasilnya adalah kerugian ekonomi sekitar 2,1 triliun dolar pada 2010.[8]
Tanda dan gejala[sunting | sunting sumber]
Gejala paling umum dari PPOK adalah produksi sputum, sesak napas dan batuk yang produktif.[9] Gejala-gejala ini muncul dalam jangka waktu yang lama[2] and dan biasanya bertambah parah seiring waktu.[4] Tidak jelas apakah terdapat jenis-jenis PPOK yang berbeda.[3] Meski sebelumnya dibagi menjadi emfisema dan bronkitis kronis, emfisema hanya merupakan gambaran dari perubahan kondisi paru dan bukan penyakit itu sendiri, dan bronkitis kronis hanya merupakan gambaran gejala yang mungkin timbul atau tidak timbul pada penderita PPOK.[1]
Batuk[sunting | sunting sumber]
Batuk kronis biasanya merupakan gejala pertama yang muncul. Saat batuk berlangsung selama lebih dari tiga bulan setahun dalam lebih dari dua tahun, dikombinasikan dengan produksi sputum dan tidak ada penjelasan lain, maka itu bisa didefinisikan sebagai bronkitis kronis. Kondisi ini dapat terjadi sebelum PPOK berkembang penuh. Jumlah sputum yang dihasilkan dapat berubah dalam beberapa jam atau hari. Dalam beberapa kasus, batuk mungkin tidak muncul atau hanya terjadi sesekali dan bisa saja tidak produktif. Beberapa penderita PPOK mengira gejala-gejala ini sebagai "batuk perokok". Sputum dapat ditelan atau dibuang, biasanya tergantung faktor sosial dan budaya. Batuk-batuk hebat dapat menyebabkan retak tulang iga atau kehilangan kesadaran secara singkat. Mereka yang menderita PPOK sering mengalami "batuk pilek biasa" yang berlangsung lama.[9]
Sesak napas[sunting | sunting sumber]
Sesak napas sering kali merupakan gejala yang dirasakan paling mengganggu.[10] Hal ini sering kali digambarkan sebagai: "Saya membutuhkan usaha untuk bernapas," atau "Saya tidak dapat menghirup cukup udara".[11] Istilah berbeda mungkin digunakan di budaya yang berbeda.[9] Umumnya, sesak napas bertambah buruk dalam tekanan, yang berlangsung lama, dan bertambah parah seiring waktu.[9] Pada tahap lanjutan, hal ini berlangsung saat beristirahat dan mungkin berlangsung terus menerus.[12][13] Hal ini merupakan sumber dari kegelisahan dan kualitas hidup yang rendah yang dialami penderita PPOK.[9] Banyak penderita PPOK lanjutan mengalami bernapas melalui bibir yang tertutup rapat dan tindakan ini dapat meredakan sesak napas bagi sebagian orang.[14][15]
Gejala lainnya[sunting | sunting sumber]
Penderita PPOK mungkin memerlukan waktu lebih lama untuk menghembuskan napas daripada untuk menarik napas.[16] Sesak di dada mungkin dapat terjadi[9] namun bukan hal yang umum dan dapat disebabkan masalah lain.[10] Mereka yang saluran udaranya terhalang mungkin mengalami napas mengi atau suara udara masuk yang berkurang saat dada diperiksa dengan menggunakan stetoskop.[16] Dada barel adalah tanda khusus dari PPOK, tapi bukan hal yang umum.[16] Posisi tripoddapat terjadi saat penyakit bertambah parah.[2]
PPOK lanjutan akan menjadi tekanan tinggi pada arteri paru, yang menekan ventrikel kanan jantung.[4][17][18] Situasi ini disebut sebagai kor pulmonale, dan akan menjadi gejala pembengkakan kaki[9] dan pembengkakan vena leher.[4] PPOK merupakan penyebab lebih umum dari kor pulmonale dibandingkan dengan penyakit paru lainnya.[17] Kor pulmonale semakin jarang terjadi sejak penggunaan suplemen oksigen.[2]
PPOK sering terjadi bersamaan dengan beberapa kondisi lain, sebagian karena faktor risiko yang sama.[3] Kondisi ini termasukpenyakit jantung iskhemik, tekanan darah tinggi, diabetes mellitus, penyusutan otot, osteoporosis, kanker paru, gangguan keresahan dan depresi.[3] Bagi mereka yang menderita penyakit ini secara kronis, perasaan selalu letih adalah hal yang umum.[9] Kuku jari bengkak bukan semata-mata gejala PPOK dan harus segera diselidiki akan kemungkinan kanker paru.[19]
Eksaserbasi[sunting | sunting sumber]
Eksaserbasi akut dari PPOK didefinisikan sebagai sesak napas bertambah parah, produksi sputum semakin banyak, dan perubahan warna sputum dari bening menjadi hijau atau kuning, atau batuk semakin parah yang dialami penderita PPOK.[16] Hal ini dapat disertai dengan tanda-tanda bertambah besarnya usaha untuk bernapas seperti napas cepat, detak jantung cepat, berkeringat, penggunaan otot leher secara aktif, kulit membiru, serta kebingungan atau prilaku agresif pada eksaserbasi parah.[16][20] Gemerisik juga mungkin terdengar dari paru-paru saat pemeriksaan dengan stetoskop.[21]
Penyebab[sunting | sunting sumber]
Penyebab utama PPOK adalah asap tembakau, dengan terpapar karena pekerjaan dan polusi dari api dalam ruang sebagai penyebab signifikan di beberapa negara.[1] Biasanya, paparan terjadi selama beberapa dekade sebelum gejalanya berkembang.[1] Komposisi genetik dalam diri seseorang juga mempengaruhi risiko.[1]
Rokok[sunting | sunting sumber]
Faktor risiko terbesar dari PPOK secara global adalah merokok tembakau.[1] Dari semua perokok, 20% diantaranya akan menderita PPOK,[23] dan setengah dari para perokok seumur hidup akan menderita PPOK.[24] Di Amerika Serikat dan Inggris, 80-95% dari mereka yang menderita PPOK adalah perokok atau pernah menjadi perokok.[23][25][26] Kemungkinan terkena PPOK akan meningkat seiring dengan paparan rokok total.[27] Kemudian, wanita lebih rentan terhadap efek buruk dari rokok dibandingkan pria.[26] Bagi para non-perokok, merokok pasif adalah penyebab dari 20% kasus PPOK.[25] Jenis-jenis rokok lainnya, seperti ganja, cerutu, dan merokok dengan pipa, juga memiliki risiko.[1] Wanita yang merokok selama kehamilan akan meningkatkan risiko terkena PPOK bagi anak mereka.[1]
Polusi udara[sunting | sunting sumber]
Api untuk memasak yang berventilasi buruk, kebanyakan berbahan bakar batu bara atau bahan bakar biomas seperti kayu dan kotoran hewan, menghasilkan polusi udara dalam ruang dan merupakan salah satu penyebab utama dari PPOK di negara-negara berkembang.[28] Api ini merupakan metode memasak dan memanaskan untuk lebih dari 3 juta orang dan wanita menderita dampak kesehatan yang lebih besar karena paparan yang lebih besar.[1][28] Bahan ini digunakan sebagai sumber energi utama di 80% rumah-rumah di India, Cina, dan Afrika sub-Sahara.[29]
Mereka yang hidup di kota besar memiliki tingkat PPOK lebih tinggi dibandingkan dengan mereka yang hidup di pedesaan.[30] Meskipun polusi udara di perkotaan merupakan faktor yang berperan dalam eksaserbasi, perannya secara menyeluruh sebagai penyebab PPOK masih belum jelas.[1] Wilayah dengan kualitas udara luar ruang yang rendah, termasuk dari gas buang, secara umum memiliki tingkat PPOK yang lebih tinggi.[29] Namun efek menyeluruh dalam kaitannya dengan merokok dianggap kecil.[1]
Terpapar karena pekerjaan[sunting | sunting sumber]
Paparan intensif dan dalam waktu lama terhadap debu, bahan kimia, dan asap di tempat kerja dapat meningkatkan risiko PPOK baik untuk perokok maupun non-perokok.[31] Terpapar karena pekerjaan dianggap sebagai penyebab dari 10-20% kasus PPOK.[32] Di Amerika Serikat, hal ini dianggap terkait dengan lebih dari 30% kasus di antara mereka yang tidak pernah merokok, dan mungkin mewakili risiko lebih besar di negara-negara yang tidak memiliki peraturan yang cukup.[1]
Beberapa industri dan sumber telah terimplikasi, termasuk[29] tingkat debu yang tinggi di tambang batu bara, tambang emas, dan industri tekstil katun, pekerjaan yang melibatkan kadmium dan isosianat, serta asap dari pengelasan.[31] Untuk pekerjaan tertentu, risikonya diramalkan setara dengan merokok setengah hingga dua bungkus rokok sehari.[33] Terpapar debu silika dapat pula menyebabkan PPOK, dengan risiko yang tak ada hubungannya dengan silikosis.[34] Efek negatif dari terpapar debu dan terpapar asap rokok sepertinya berdampak aditif atau lebih dari aditif.[33]
Genetik[sunting | sunting sumber]
Genetik juga berperan dalam perkembangan PPOK.[1] PPOK lebih sering terjadi di antara sanak keluarga yang menderita PPOK dan perokok dibandingkan di antara penderita PPOK yang perokok yang tidak memiliki hubungan keluarga.[1] Saat ini, satu-satunya faktor risiko yang dapat diwariskan adalah kekurangan alfa 1-antitripsin (AAT).[35] Risikonya cukup tinggi khususnya jika seseorang mengalami kekurangan alfa 1-antitripsin dan juga merokok.[35] Hal ini menjadi penyebab 1-5% kasus[35][36] dan kondisi ini terdapat pada sekitar 3-4 dari 10.000 orang.[2] Faktor-fektor genetik lain masih dalam penyelidikan,[35] yang kemungkinan akan banyak ditemukan.[29]
Lain-lain[sunting | sunting sumber]
Beberapa faktor lainnya tidak cukup erat terkait dengan PPOK. Risikonya lebih besar di kalangan mereka yang miskin, meskipun tidak jelas apakah hal ini disebabkan karena kemiskinan itu sendiri atau faktor-faktor lain yang terkait dengan kemiskinan, seperti polusi udara dan malagizi.[1] Terdapat bukti tentatif bahwa mereka yang menderita asma dan hiperaktivitas saluran udara memiliki risiko PPOK yang lebih tinggi.[1] Faktor-faktor kelahiran seperti berat lahir rendah juga memainkan peran sebagaimana sejumlah penyakit menular termasuk HIV/AIDS dan tuberkulosis.[1] Infeksi pernapasan seperti pneumonia sepertinya tidak meningkatkan risiko PPOK, paling tidak pada orang dewasa.[2]
Eksaserbasi[sunting | sunting sumber]
Eksaserbasi akut (gejala yang tiba-tiba memburuk)[37] biasanya dipicu oleh infeksi atau polutan lingkungan, atau terkadang karena faktor-faktor lain seperti penggunaan obat-obatan yang kurang tepat.[38] Infeksi merupakan sebab dari 50-75% kasus,[38][39] dengan bakteri dalam 25%, virus dalam 25%, dan keduanya dalam 25% kasus.[40] Polutan lingkungan terdiri dari baik kualitas udara dalam ruang atau luar ruang.[38] Terpapar asap rokok sendiri atau asap perokok lain juga meningkatkan risiko.[29] Suhu dingin juga berperan, dengan eksaserbasi yang lebih sering terjadi pada musim dingin.[41] Mereka yang menderita penyakit parah yang telah ada sebelumnya mengalami eksaserbasi lebih sering: yang berpenyakit ringan 1,8 per tahun, menengah 2 hingga 3 per tahun, dan parah 3,4 per tahun.[42] Mereka yang sering mengalami eksaserbasi akan mengalami kerusakan fungsi paru dengan lebih cepat.[43] Emboli pulmonari (penggumpalan darah di paru-paru) akan memperburuk gejala bagi mereka yang telah menderita PPOK.[3]
Patofisiologi[sunting | sunting sumber]

PPOK adalah sejenis penyakit paru obstruktif yang terjadi saat terdapat aliran udara yang buruk yang tak dapat diperbaiki secara menyeluruh dan kronis serta terjadi ketidakmampuan untuk menghembuskan napas secara penuh (memerangkap udara).[3] Aliran air yang buruk merupakan akibat dari rusaknya jaringan paru (dikenal sebagai emfisema) dan penyakit saluran udara kecil yang dikenal sebagai bronkiolitis obstruktif. Kontribusi relatif dari dua faktor ini bervariasi dari orang ke orang.[1] Kerusakan saluran udara kecil yang parah dapat mengakibatkan terbentuknya kantung-kantung udara yang besar— yang disebut sebagai bula—yang menggantikan jaringan paru. Jenis penyakit ini disebut sebagai emfisema bula.[44]
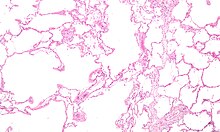
PPOK berkembang sebagai reaksi inflamasi kronis akibat menghirup bahan-bahan penyebab iritasi .[1] Infeksi bakteri kronis juga dapat memperparah inflamasi ini.[43] Sel-sel yang radang termasuk neutrofil dan makrofag. Mereka yang merokok mengalami keterlibatan Tc1 limfosit dan mereka yang menderita PPOK mengalami keterlibatan eosinofil yang mirip dengan yang ada pada asma. Sebagian dari reaksi sel ini disebabkan oleh mediator peradangan seperti faktor kemotaksis. Proses lainnya yang berperan dalam kerusakan paru adalah tekanan oksidatif yang dihasilkan karena adanya konsentrasi tinggi dari radikal bebas dalam asap tembakau dan dibebaskan oleh sel yang terinflamasi, dan hancurnya jaringan penghubung paru-paru oleh protease yang kurang mengandung penghambat protease. Hancurnya jaringan penghubung di paru-paru akan mengakibatkan emfisema, yang kemudian menyebabkan buruknya aliran udara, dan pada `akhirnya, buruknya penyerapan dan pelepasan gas-gas pernapasan.[1] Penyusutan otot secara umum yang sering terjadi pada PPOK sebagian mungkin dikarenakan mediator inflamasi yang dilepaskan paru-paru ke dalam darah.[1]
Penyempitan saluran udara terjadi karena inflamasi dan parut di dalamnya. Hal ini menyebabkan kesulitan saat menghembuskan napas dengan sepenuhnya. Pengurangan aliran udara terbesar terjadi saat menghembuskan napas, karena tekanan di dada menekan saluran udara pada saat itu.[45] Hal ini berakibat udara dari tarikan napas sebelumnya tetap berada di dalam paru-paru sementara tarikan napas berikutnya telah dimulai. Hasilnya adalah peningkatan volume total udara di dalam paru-paru yang dapat terjadi kapan saja, sebuah proses yang disebut sebagai hiperinflasi atau terperangkapnya udara.[45][46] Hiperinflasi karena olahraga terkait dengan sesak napas di PPOK, karena menghirup napas saat paru-paru terisi setengah penuh terasa kurang nyaman.[47]
Beberapa orang juga mengalami sedikit gejala hiperresponsif saluran udara terhadap penyebab iritasi yang sama dengan yang ditemukan pada asma.[2]
Tingkat oksigen rendah dan, akhirnya, tingginya tingkat karbon dioksisa di darah dapat terjadi karena pertukaran udara yang buruk akibat berkurangnya ventilasi karena obstruksi saluran udara, hiperinflasi, dan berkurangnya keinginan untuk bernapas.[1] Selama eksaserbasi, inflamasi saluran udara akan meningkat, sehingga hiperinflasi meningkat, aliran udara pernapasan berkurang, dan transfer gas semakin buruk. Hal ini juga akan mengakibatkan tidak cukupnya ventilasi, dan akhirnya, tingkat oksigen dalam darah yang rendah.[4] Tingkat oksigen rendah, jika dialami dalam jangka waktu lama, dapat menyebabkan penyempitan arteri di paru-paru, sementara emfisema mengakibatkan rusaknya kapilari di paru-paru. Kedua perubahan ini berakibat meningkatnya tekanan darah di arteri pulmonari, yang dapat menyebabkan kor pulmonale.[1]
Diagnosis[sunting | sunting sumber]

Diagnosis PPOK harus dipertimbangkan pada siapa pun yang berusia lebih dari 35 hingga 40 tahun yang mengalami sesak napas, batuk kronis, produksi sputum, atau batuk pilek musim dingin yang sering, serta memiliki sejarah terpapar faktor-faktor risiko dari penyekit tersebut.[9][10] Spirometri kemudian dapat digunakan untuk mengonfirmasi diagnosis.[9][48]
Spirometri[sunting | sunting sumber]
Spirometri mengukur jumlah obstruksi aliran udara yang terjadi dan umumnya digunakan setelah penggunaan bronkodilator, pengobatan yang membuka saluran udara.[48] Dua komponen utama diukur untuk membuat diagnosis: volume pernapasan paksa dalam dua detik (FEV1), yaitu volume terbesar udara yang dihembuskan ke luar dalam detik pertama hembusan napas, dan kapasitas vital paksa (KVP/FVC), yaitu volume udara terbesar yang dapat dihembuskan dalam satu hembusan napas besar.[49] Normalnya, 75-80% FVC ke luar dalam satu detik pertama[49] dan FEV1/rasio KVP yang kurang dari 70% pada seseorang yang memiliki gejala-gejala PPOK menandakan bahwa orang tersebut menderita PPOK.[48] Berdasarkan pengukuran ini, spirometri akan menyebabkan diagnosis-berlebih akan PPOK di kalangan manula.[48] Kriteria dari National Institute of Clinical Excellence menambah satu diagnosa lagi berupa FEV1 yang kurang dari 80% dari yang diperkirakan.[10]
Bukti dengan menggunakan spirometri untuk mereka yang tidak memiliki gejala sebagai upaya diagnosis kondisi secara dini tidak memiliki efek yang jelas dan karena itu tidak direkomendasikan pada saat ini.[9][48] Aliran ekspiratori puncak (kecepatan maksimum ekspirasi), yang biasa digunakan untuk asma, tidak cukup untuk mendiagnosis PPOK.[10]
Keparahan[sunting | sunting sumber]
| Peringkat | Aktivitas yang terpengaruh |
|---|---|
| 1 | Hanya aktivitas berat |
| 2 | Jalan cepat |
| 3 | Dengan jalan biasa |
| 4 | Setelah beberapa menit jalan |
| 5 | Dengan ganti pakaian |
| Keparahan | FEV1 % diprediksikan |
|---|---|
| Ringan (GOLD 1) | ≥80 |
| Sedang (GOLD 2) | 50–79 |
| Parah (GOLD 3) | 30–49 |
| Sangat parah (GOLD 4) | <30 or gagal napas kronis |
Ada sejumlah metode untuk menentukan seberapa PPOK memengaruhi individu tertentu.[9] Kuesioner (mMRC) yang sudah dimodifikasi Badan Riset Medis Inggris atau uji penilaian PPOK (CAT) adalah kuesioner sederhana yang bisa digunakan untuk menentukan keparahan gejala-gejala penyakit.[9] Angka-angka pada CAT berkisar antara 0–40 di mana semakin tinggi angkanya, semarin parah penyakitnya.[50] Spirometri bisa membantu menentukan keparahan pembatasan aliran udara.[9] Ini biasanya berdasarkan pada FEV1 yang ditunjukkan sebagai persentase dari yang diperkirakan "normal" untuk usia, jenis kelamin, tinggi dan berat orang itu.[9] Baik panduan Amerika maupun Eropa yang direkomendasikan mendasarkan sebagian pengobatan pada rekomendasi-rekomendasi yang terdapat pada FEV1.[48] Panduan EMAS menyarankan pembagian orang menjadi empat kategori berdasarkan pengkajian gejala-gejala penyakit dan pembatasan aliran udara.[9] Penurunan berat badan dan kelemahan otot, serta adanya penyakit-penyakit lain, juga harus ikut dipertimbangkan.[9]
Tes lainnya[sunting | sunting sumber]
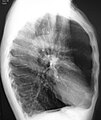
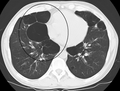
Rontgen dada dan hitung darah lengkap dilakukan untuk mengesampingkan kondisi-kondisi lain pada saat penyakit didiagnosis.[51] Tanda-tanda karakteristik pada rontgen adalah paru-paru membesar, diafragma mengempis, rongga udara retrosternal meningkat, dan bullae yang bisa membantu mengesampingkan penyakit paru-paru lain, seperti pneumonia, edema paru-paru atau pneumotoraks.[52] Hasil pindai tomografi komputer dari dada bisa menunjukkan distribusi emfisema di seluruh paru-paru dan juga bermanfaat untuk mengesampingkan penyakit paru-paru lain.[2] Namun, kecuali operasi bedah sudah direncanakan, ini jarang mempengaruhi manajemen.[2] Sebuahanalisa darah arteri digunakan untuk menentukan kebutuhan oksigen; ini direkomendasikan bagi mereka yang FEV-nya 1 kurang dari 35% yang diprediksikan, mereka yang saturasi oksigen periferalnya kurang dari 92% dan mereka yang memiliki gejala gagal jantung kongestif.[9] Di wilayah dunia di mana kekurangan antitripsin alfa-1 biasa ditemukan, penderita PPOK (terutama mereka yang di bawah usia 45 dan menderita emfisema yang menyerang bagian bawah paru-paru) harus dipertimbangkan untuk tes.[9]
-
Chest X-ray demonstrating severe COPD. Note the small heart size in comparison to the lungs.
-
A lateral chest x-ray of a person with emphysema. Note the barrel chest and flat diaphragm.
-
Lung bulla as seen on CXR in a person with severe COPD
-
A severe case of bullous emphysema
-
Axial CT image of the lung of a person with end-stage bullous emphysema.
Diagnosa diferensial[sunting | sunting sumber]
COPD mungkin perlu dibedakan dari penyebab-penyebab lain dari sesak nafas seperti gagal jantung kongestif, embolisme paru-paru, pneumonia atau pneumotoraks. Banyak orang yang menderita COPD secara keliru dikira menderita asma.[16] Perbedaan antara asma dan COPD dibuat berdasarkan gejala-gejalanya, riwayat merokok, dan apakah pembatasan aliran udara bisa dipulihkan dengan bronkodilator di spirometri.[53] Tuberkulosis bisa juga muncul dengan batuk kronis dan harus diperhatikan di lokasi-lokasi di mana penyakit ini umum ditemukan.[9] Kondisi-kondisi yang tidak begitu umum juga bisa muncul termasuk displasia bronkopulmonari dan bronkiolitis obliteratif.[51] Bronkitis kronis bisa muncul dengan aliran udara normal dan dalam situasi ini tidak diklasifikasikan sebagai COPD.[2]
Pencegahan[sunting | sunting sumber]
Kebanyakan kasus COPD berpotensi untuk bisa dicegah melalui penurunan paparan terhadap asap dan peningkatan kualitas udara.[29] Vaksinasi flu tahunan pada mereka yang menderita COPD menurunkan keparahan, lamanya rawat inap dan kematian.[54][55] Vaksin pneumokokal bisa juga bermanfaat.[54]
Berhenti merokok[sunting | sunting sumber]
Mencegah orang agar tidak mulai merokok adalah aspek utama dari pencegahan PPOK.[56] kebijakan-kebijakan dari pemerintah, badan-badan kesehatan umum dan organisasi-organisasi antirokok bisa menurunkan tingkat merokok dengan mencegah orang agar tidak mulai merokok dan menganjurkan orang untuk berhenti merokok.[57] Larangan merokok di tempat-tempat umum dan tempat kerja adalah sarana penting untuk menurunkan paparan asap sekunder. Walaupun banyak tempat sudah menerapkan larangan merokok, dianjurkan agar lebih banyak lagi.[29]
Di kalangan mereka yang merokok, berhenti merokok adalah satu-satunya cara yang terbukti untuk memperlambat memburuknya PPOK.[58] Bahkan pada tahap lanjut dari penyakit ini, berhenti merokok bisa menurunkan tingkat memburuknya fungsi paru-paru dan memperlambat serangan awal kecacatan dan kematian.[59] Penghentian merokok mulai dengan keputusan untuk berhenti merokok, kemudian dilanjutkan dengan upaya untuk berhenti. Sering beberapa upaya diperlukan sebelum pantang jangka panjang tercapai.[57] Upaya melebihi 5 tahun membawa kesuksesan dalam hampir 40% orang.[60]
Beberapa perokok bisa berhasil berhenti merokok jangka panjang melalui tekad yang keras. Namun merokok sangat adiktif,[61] dan banyak perokok memerlukan bantuan lebih lanjut. Kesempatan untuk berhenti meningkat dengan dukungan sosial, keterlibatan dalam program penghentian merokok dan penggunaan obat-obatan seperti terapi penggantian nikotin, bupropion atau vareniklin.[57][60]
Kesehatan kerja[sunting | sunting sumber]
Sejumlah tindakan sudah diambil untuk menurunkan kemungkinan pekerja di industri-industri yang berisiko - seperti pertambangan batubara, konstruksi dan batu bata - terserang COPD.[29] Contoh-contoh dari tindakan pencegahan ini termasuk: pembuatan kebijakan umum,[29] pendidikan pekerja dan manajemen risiko, mempromosikan penghentian merokok, pemeriksaan pekerja apakah ada tanda-tanda awal COPD, dan penggunaan respirator, dan pengontrolan debu.[62][63] Pengontrolan debu yang efektif bisa dicapai dengan memperbaiki ventilasi, menggunakan semprotan air dan dengan menggunakan teknik-teknik pertambangan yang meminimalkan timbulnya debu.[64] Bila seorang pekerja terserang COPD, kerusakan paru-paru selanjutnya bisa diturunkan dengan menghindari paparan debu yang berkelanjutan, misalnya dengan mengubah peran kerjanya.[65]
Polusi udara[sunting | sunting sumber]
Kualitas udara di dalam atau di luar ruang bisa ditingkatkan, yang bisa mencegah COPD atau memperlambat penyakit yang sudah ada.[29] Ini bisa dicapai dengan upaya kebijakan umum, perubahan budaya, dan keterlibatan pribadi.[66]
Sejumlah negara maju sudah berhasil meningkatkan kualitas udara luar melalui peraturan-peraturan. Ini menghasilkan peningkatan dalam fungsi paru-paru penduduknya.[29] Penderita COPD bisa mengalami lebih sedikit gejala-gejala penyakit bila mereka tinggal di dalam ruangan saat kualitas udara luar buruk.[4]
Satu upaya penting adalah menurunkan paparan terhadap asap dari bahan bakar untuk memasak dan pemanas melalui ventilasi rumah yang lebih baik serta kompor dan cerobong asap yang lebih baik.[66] Kompor yang tepat bisa meningkatkan kualitas udara dalam ruang hingga 85%. Penggunaan sumber energi alternatif seperti memasak dengan panel surya dan pemanas listrik efektif, demikian juga penggunaan bahas bakar seperti minyak tanah dan batubara dibandingkan penggunaan biomassa.[29]
Manajemen[sunting | sunting sumber]
Belum ada obat untuk menyembuhkan COPD yang diketahui, tetapi gejala-gejala bisa diobati dan perkembangannya diperlambat.[56] Tujuan utama dari manajemen adalah untuk menurunkan faktor-faktor risiko, mengelola COPD yang stabil, mencegah dan mengobati eksarsebasi akut, dan menangani penyakit-penyakit terkait.[4] Satu-satunya cara yang terbukti menurunkan mortalitas adalah penghentian merokok dan pemberian suplemen oksigen.[67] Berhenti merokok menurunkan risiko kematian hingga 18%.[3] Rekomendasi lain termasuk: vaksinasi flu setahun sekali, vaksinasi pneumokokal sekali setiap 5 tahun, dan penurunan paparan terhadap polusi udara lingkungan.[3] Bagi mereka yang menderita penyakit tahap lanjut, perawatan paliatif bisa menurunkan gejala-gejala, dengan morfin memperbaiki rasa sesak nafas.[68] Ventilasi noninvasif bisa digunakan untuk mendukung pernafasan.[68]
Latihan[sunting | sunting sumber]
Rehabilitasi paru-paru adalah sebuah program latihan, pengelolaan penyakit dan konseling, yang dikoordinasikan agar bermanfaat bagi individu.[69] Bagi mereka yang baru saja mengalami eksaserbasi, rehabilitasi paru-paru tampaknya meningkatkan kualitas hidup dan kemampuan berlatih secara keseluruhan, dan menurunkan mortalitas.[70] Program ini juga sudah terbukti meningkatkan kemampuan seseorang untuk mengendalikan penyakitnya, serta emosinya.[71] Latihan bernafas itu sendiri tampaknya terbatas peranannya.[15]
Kekurangan atau kelebihan berat badan kurang bisa mempengaruhi gejala-gejala penyakit, tingkat kecacatan dan prognosis COPD. Penderita COPD yang kekurangan berat badan bisa meningkatkan kekuatan otot pernafasannya dengan menaikkan asupan kalorinya.[4] Bila digabungkan dengan latihan rutin atau sebuah program rehabilitasi paru-paru, ini bisa memperbaiki gejala-gejala COPD. Nutrisi suplemen bisa berguna bagi mereka yang kekurangan gizi.[72]
Bronkodilator[sunting | sunting sumber]
Bronkodilator hirup adalah pengobatan utama yang digunakan [3] dan manfaat keseluruhannya kecil.[73] Ada dua jenis utama, β2 agonis dan antikolinergik; keduanya tersedia dalam bentuk bekerja jangka panjang dan jangka pendek. Bronkodilator menurunkan sesak nafas, suara mengi dan keterbatasan latihan, sehingga menghasilkan peningkatan kualitas hidup.[74] Tidak jelas apakah pengobatan itu mengubah perkembangan penyakit yang mendasarinya.[3]
Bagi mereka yang menderita penyakit ringan, obat-obatan kerja pendek direkomendasikan berdasarkan sesuai keperluan.[3] Bagi mereka yang menderita penyakit yang lebih parah, obat-obatan kerja panjang direkomendasikan.[3] Bila bronkodilator kerja panjang tidak memadai, kortikosteroid hirup biasanya ditambahkan.[3] Dalam kaitannya dengan obat-obatan kerja panjang, tidak jelas apakah tiotropium (antikolinergik kerja panjang) atau beta agonis kerja panjang(LABA) lebih baik, dan mungkin sebaiknya masing-masing dicoba dan yang bekerja paling baik diteruskan.[75] Kedua jenis pengobatan tampaknya menurunkan risiko eksaserbasi akut hingga 15-25%.[3] Walaupun penggunaan kedua jenis obat bersamaan bisa menawarkan faedah, faedah ini, bila ada, maknanya diragukan.[76]
Ada beberapa β2 agonis kerja pendek yang tersedia termasuk salbutamol (Ventolin) dan terbutalin.[77] Obat-obat itu meringankan gejala-gejala penyakit selama empat hingga enam jam.[77] β2 Agonis kerja panjang seperti salmeterol dan formoterol sering digunakan sebagai terapi pemeliharaan. Beberapa orang merasa bukti faedah terbatas[78] sementara yang lain memandang faedahnya sudah terbukti.[79][80] Penggunaan jangka panjang tampaknya aman dalam COPD[81] dengan efek-efek samping termasuk gemetar dan palpitasi jantung.[3] Bila digunakan dengan steroid hirup, pengobatan ini meningkatkan risiko pneumonia.[3] Walaupun steroid dan LABA bisa bekerja lebih baik bersama,[78] tidak jelas apakah faedah kecil ini manfaatnya melebihi peningkatan risiko-risikonya.[82]
Ada dua antikoligernik utama yang digunakan dalam COPD, ipratropium dan tiotropium. Ipratropium adalah obat kerja pendek sedangkan tiotropium kerja panjang. Tiotropium dikaitkan dengan penurunan eksaserbasi dan peningkatan kualitas hidup,[76] dan tiotropium memberikan manfaat itu lebih baik daripada ipratropium.[83] Ini tampaknya tidak mempengaruhi mortalitas atau tingkat rawat inap keseluruhan.[84] Antikolinergik bisa menyebabkan mulut kering dan gejala-gejala penyakit saluran kencing.[3] Antikoligernik juga dikaitkan dengan peningkatan risiko penyakit jantung dan stroke.[85][86] Aklidinium, obat kerja panjang lain yang muncul di pasar dalam tahun 2012, digunakan sebagai alternatif untuk tiotropium.[87][88]
Kortikosteroid[sunting | sunting sumber]
Kortikosteroid biasanya digunakan dalam bentuk obat hirup tetapi juga bisa digunakan sebagai tablet untuk mengobati dan mencegah eksaserbasi akut. Walaupun kortikosteroid hirup (ICS) tidak menunjukkan manfaat bagi penderita COPD ringan, obat itu menurunkan aksersebasi akut bagi mereka yang menderita COPD sedang atau parah.[89] Bila digunakan dalam kombinasi dengan LABA, pengobatan itu menurunkan mortalitas lebih dari ICS atau LABA yang digunakan sendiri.[90] Bila digunakan sendiri, pengobatan itu tidak berpengaruh pada mortalitas satu tahun keseluruhan dan dikaitkan dengan peningkatan level pneumonia.[67] Tidak jelas apakah pengobatan itu mempengaruhi perkembangan penyakit.[3] Pengobatan kerja panjang dengan tablet steroid dikaitkan dengan efek samping yang penting.[77]
Pengobatan lain[sunting | sunting sumber]
Antibiotik kerja panjang, terutama yang berasal dari kelas makrolid seperti eritromisin, menurunkan frekuensi eksaserbasi dari mereka yang mengalami serangan COPD dua kali atau lebih dalam setahun.[91][92] Praktik ini mungkin hemat biaya di beberapa wilayah dunia.[93] Kekuatirannya termasuk adanya resistensi antibiotik dan gangguan pendengaran dengan azitromisin.[92] Metilxantin seperti teofilin biasanya menyebabkan lebih banyak kerugian daripada keuntungan dan oleh karena itu biasanya tidak direkomendasikan,[94] tapi bisa digunakan sebagai pengobatan baris kedua bagi yang tidak bisa dikendalikan dengan pengobatan lain.[4] Mukolitik bisa berguna bagi beberapa penderita yang memiliki lendir kental tapi pada umumnya tidak diperlukan.[54] Obat batuk tidak dianjurkan.[77]
Oksigen[sunting | sunting sumber]
Oksigen suplemen direkomendasikan bagi mereka yang level oksigennya rendah saat beristirahat(tekanan parsial oksigen kurang dari 50–55 mmHg atau saturasi oksigen kurang dari 88%).[77][95] Dalam kelompok orang ini, terapi itu menurunkan risiko gagal jantung dan kematian bila digunakan 15 jam per hari[77][95] dan bisa meningkatkan kemampuan orang untuk berolahraga.[96] Bagi mereka yang level oksigennya normal atau sedikit rendah, suplementasi oksigen bisa memperbaiki sesak nafas.[97] Ada risiko kebakaran dan sedikit manfaat bila mereka yang menjalani terapi oksigen terus merokok.[98] Dalam situasi ini beberapa merekomendasikan agar terapi ini tidak digunakan.[99] Selama eksaserbasi akut, banyak yang memerlukan terapi oksigen; penggunaan oksigen konsentrasi tinggi tanpa mempertimbangkan saturasi oksigen seseorang bisa menyebabkan peningkatan level karbon dioksida dan hasil-hasilnya diperburuk.[100][101] Bagi mereka yang risikonya tinggi terhadap level karbon dioksida yang tinggi, saturasi oksigen sebesar 88–92% direkomendasikan, sementara bagi mereka yang tidak berisiko, level yang direkomendasikan adalah 94-98%.[101]
Bedah[sunting | sunting sumber]
Bagi mereka yang penyakitnya amat parah bedah kadang-kadang membantu dan bisa termasuk pencangkokan paru-paru atau bedah penurunan volume paru-paru.[3] Bedah penurunan volume paru-paru melibatkan penghilangan bagian-bagian paru-paru yang paling rusak karena emfisema sehingga membiarkan sisanya, yang masih relatif baik, untuk berekspansi dan bekerja lebih baik.[77] Pencangkokan paru-paru kadang-kadang dilakukan untuk COPD yang amat parah, terutama pada individu yang lebih muda.[77]
Eksaserbasi[sunting | sunting sumber]
Eksaserbasi akut biasanya diobati dengan meningkatkan penggunaan bronkodilator kerja pendek.[3] Ini pada umumnya memasukkan kombinasi beta agonis hirup kerja pendek dan antikolinergik.[37] Pengobatan ini bisa diberikan baik melalui inhaler dengan dosis terukur dengan spacer atau melalui nebulizer, keduanya tampaknya sama-sama efektif.[37] Nebulisasi mungkin lebih mudah bagi mereka yang kondisinya lebih tidak sehat.[37]
Kortikosteroid oral meningkatkan kesempatan penyembuhan dan menurunkan durasi keseluruhan gejala-gejala penyakit.[3][37] bagi mereka yang menderita eksaserbasi parah, antibiotic meningkatkan hasil-hasil.[102] Berbagai jenis antibiotik bisa digunakan termasuk: amoksisilin, doksisiklin atau azitromisin; tidak jelas apakah salah satu lebih baik dari yang lain.[54] Tidak ada bukti jelas bagi mereka yang penyakitnya tidak begitu parah.[102]
Ventilasi tekanan positif non-invasif bagi mereka yang level CO2-nya meningkat secara akut (gagal pernafasan tipe 2) menurunkan probabilitas kematian dari atau perlunya perawatan intensif untuk ventilasi mekanis.[3] Sebagai tambahan, teofilin mungkin berperan bagi mereka yang tidak memberikan respon terhadap pengobatan lain.[3] Kurang dari 20% eksaserbasi memerlukan rawat inap di rumah sakit.[37] Bagi mereka yang tidak mengalami asidosis dari gagal pernafasan, perawatan di rumah ("rumah sakit di rumah") mungkin bisa membantu menghindari rawat inap.[37][103]
Prognosis[sunting | sunting sumber]

no data ≤110 110–220 220–330 330–440 440–550 550–660 | 660–770 770–880 880–990 990–1100 1100–1350 ≥1350 |
COPD biasanya memburuk dengan berjalannya waktu dan bisa berakhir dengan kematian. Diperkirakan 3% dari semua kecacatan dikaitkan dengan COPD.[105] Proporsi kecacatan dari COPD secara global telah menurun dari tahun 1990 hingga 2010 karena peningkatan kualitas udara dalam ruang terutama di Asia.[105] Namun, jumlah keseluruhan tahun hidup dengan kecacatan dari COPD meningkat.[106]
Tingkat memburuknya COPD berbeda-beda bergantung pada adanya faktor yang memperkirakan hasil buruk termasuk: gangguan parah di saluran napas, lemahnya kemampuan untuk berolah raga, napas pendek, berat badan berkurang atau bertambah secara drastis, gagal jantung kongestif, kebiasaan merokok, dan gejala sakit mendadak yang sering terjadi.[4] Hasil jangka panjang pada COPD dapat diperkirakan dengan menggunakan indeks BODE yang memberikan nilai mulai dari nol hingga sepuluh bergantung pada FEV1, indeks massa tubuh, jarak yang mampu dicapai dengan berjalan kaki selama enam menit, dan skala dispnea MRC yang dimodifikasi.[107] Berkurangnya berat badan secara signifikan merupakan tanda yang buruk.[2] Hasil spirometri juga merupakan penanda baik untuk perkiraan kemajuan selanjutnya dari penyakit ini meskipun tidak sebagus indeks BODE.[2][10]
Epidemiologi[sunting | sunting sumber]
Secara global, sejak 2010, COPD memengaruhi sekitar 329 juta orang (4,8% dari populasi dunia) dan lebih banyak terjadi pada laki-laki daripada perempuan.[106] Perbandingan ini adalah yang dilakukan di antara 64 juta yang terpengaruh COPD pada 2004.[108] Kenaikan jumlah di negara-negara berkembang yang terjadi antara 1970 dan 2000-an diyakini terkait dengan semakin tingginya perilaku merokok di wilayah ini, populasi yang meningkat dan populasi yang menua yang disebabkan karena berkurangnya kematian karena akibat lain seperti penyakit-penyakit menular.[3] Angka prevalensi COPD ini meningkat di beberapa negara maju, dan di beberapa negara maju lainnya stabil dan menurun.[3] Jumlah global diperkirakan akan terus meningkat karena faktor risiko masih sama dan populasi semakin menua.[56]
Antara 1990 dan 2010 angka kematian yang disebabkan oleh COPD sedikit menurun dari 3,1 juta menjadi 2,9 juta.[109] Secara umum COPD menjadi penyebab ke empat kematian tertinggi.[3] Di beberapa negara, mortalitas menurun pada laki-laki, namun meningkat pada perempuan.[110] Kemungkinan terbesarnya adalah karena angka merokok pada perempuan dan laki-laki semakin mirip.[2] COPD lebih banyak terjadi pada orang tua;[1] ini berdampak pada 34-200 dari 1000 orang yang berusia lebih dari 65 tahun, bergantung pada populasi yang dilihat.[1][52]
Di Inggris, kira-kira 0,84 juta orang (dari 50 juta) terdiagnosis mengalami COPD; yang berarti sekitar satu dari 59 orang terdiagnosis COPD semasa hidupnya. Di wilayah dengan kondisi sosioekonomi yang paling rendah di Inggris, satu dari 32 orang terdiagnosis COPD, dibandingkan dengan satu di antara 98 di wilayah yang paling kaya.[111] Di Amerika Serikat, sekitar 6,3% dari populasi dewasa, dari sekitar 15 juta orang, telah terdiagnosis terkena COPD.[112] 25 juta orang mungkin terkena COPD jika kasus yang tidak terdiagnosis diperhitungkan.[113] Pada 2011, terdapat sekitar 730.000 rawat inap pasien COPD di Amerika Serikat.[114]
Sejarah[sunting | sunting sumber]

Kata "emphysema" berasal dari Greek ἐμφυσᾶν emphysan berarti "menggelembung" –dengan sendirinya terdiri dari ἐν en, berarti "di dalam", dan φυσᾶν physan, berarti "napas, ledakan".[115] Istilah bronkitis kronik mulai digunakan pada 1808[116] sedangkan istilah COPD dipercayai pertama kali digunakan pada 1965.[117] Sebelumnya penyakit ini dikenal dengan beberapa nama termasuk: penyakit chronic obstructive bronchopulmonary, penyakit pernapasan obstruktif kronis, gangguan saluran napas kronis, keterbatasan saluran napas kronis, penyakit paru obstruktif kronis, penyakit pernapasan kronis nonspesifik, dan sindrom pernapasan obstruktif difus. Istilah bronkitis kronis dan emfisema kemudian secara formal didefinisikan pada 1959 dalam simposium tamu CIBA dan pada 1962 dalam pertemuan KomisiAmerican Thoracic Society tentang Standar Diagnostik.[117]
Deskripsi awal tentang kemungkinan emphysema termasuk: pada 1679 oleh T. Bonet tentang kondisi dari "paru-paru bervolume" dan pada 1769 oleh Giovanni Morgagni tentang paru-paru yang "pembengkakan khususnya karena udara".[117][118] Pada 1721 sketsa pertama tentang emphysema dibuat oleh Ruysh.[118] Selanjutnya, ini diikuti foto yang dibuat oleh Matthew Baillie pada 1789 dan deskripsi tentang ciri destruktif dari kondisi. Pada 1814 Charles Badham menggunakan "catarrh" untuk menggambarkan batuk dan lendir berlebihan yang terjadi saat bronkitis kronis. René Laennec, dokter yang menemukan stetoskop, menggunakan istilah "emphysema" dalam bukunya A Treatise on the Diseases of the Chest and of Mediate Auscultation (1837) untuk menggambarkan paru-paru yang tidak mengempis ketika dia membuka dada selama autopsi. Dia mencatat bahwa paru-paru tidak mengempis sebagaimana biasanya karena paru-paru tersebut penuh dengan udara dan saluran napas dipenuhi lendir. Pada 1842, John Hutchinson menemukan spirometer, yang memungkinkan pengukuran kapasitas vital paru-paru. Namun, spirometernya hanya bisa mengukur volume, bukan laju udara. Tiffeneau dan Pinelli pada 1947 menggambarkan prinsip-prinsip pengukuran laju udara.[117]
Pada 1953, Dr. George L. Waldbott, seorang ahli penyakit Amerika, pertama kali menggambarkan penyakit baru yang dia namakan "sindrom pernapasan perokok" pada 1953 Journal of the American Medical Association. Ini merupakan asosiasi pertama antara penyakit tembakau dan penyakit pernapasan kronis.[119]
Dahulu pengobatan yang digunakan menggunakan di antaranya bawang putih, kayu manis dan ipecac.[116] Pengobatan modern dikembangkan pertengahan kedua abad ke-20. Bukti yang mendukung penggunaan steroid untuk pengobatan COPD dipublikasikan pada akhir 1950an. Bronchodilator mulai digunakan pada 1960an setelah uji coba yang menjanjikan atas isoprenalin. Bronchodilator lebih lanjut, seperti salbutamol, dikembangkan pada 1970an, dan penggunaan LABA dimulai pada pertengahan 1990an.[120]
Masyarakat dan kebudayaan[sunting | sunting sumber]
COPD disebut juga "smoker's lung" (“paru-paru perokok”).[121] Mereka yang mengalami emfisema disebut sebagai "pink puffers" atau "tipe A" karena kulit mereka sering berwarna merah muda, laju pernapasan cepat dan bibir berlipat,[122][123] dan orang yang terkena bronkitis kronis disebut sebagai "blue bloaters" atau "tipe B" karena kulit dan bibir mengalami yang berwarna kebiruan akibat tingkat oksigen rendah dan pergelangan mereka membengkak.[123][124] Istilah ini dipandang tidak berguna lagi karena sebagian besar orang dengan COPD mengalami kombinasi keduanya.[2][123]
Banyak sistem kesehatan mengalami kesulitan untuk memastikan identifikasi, diagnosis dan perawatan yang benar untuk orang dengan COPD; Departemen Kesehatan telah mengidentifikasikan masalah besar ini untuk the National Health Service dan memperkenalkan strategi khusus untuk mengatasi masalah ini.[125]
Ekonomi[sunting | sunting sumber]
Secara global, sejak 2010, COPD diperkirakan mengakibatkan biaya ekonomi sebesar $2.1 triliun, setengahnya terjadi di negara-negara berkembang.[8] Dari total jumlah ini, sekira $1,9 triliun merupakan biaya langsung seperti perawatan medis, sedangkan $0,2 triliun merupakan biaya tidak langsung seperti bolos kerja.[126] Jumlah ini diperkirakan meningkat lebih dari dua kali lipat selama 20 tahun yang akan datang.[8] Di Eropa, COPD mewakili 3% dari pengeluaran kesehatan.[1] Di Amerika Serikat, biaya penyakit diperkirakan $50 miliar, sebagian besar disebabkan oleh eksaserbasi.[1] COPD merupakan satu dari masalah kesehatan paling mahal yang ada di rumah sakit di AS pada 2011, dengan total biaya sekitar $5,7 juta.[114]
Riset[sunting | sunting sumber]
Infliximab, antibodi yang menekan imunitas, telah diuji pada COPD namun tidak ada bukti dari manfaat dengan kemungkinan bahayanya.[127] Roflumilast tampak menjanjikan untuk mengurangi angka eksarsebasi namun tampaknya tidak memengaruhi kualitas hidup.[3] Sejumlah agen baru yang bekerja lama saat ini masih dikembangkan.[3] Perawatan dengan stem sel sedang diteliti.[128] Meskipun secara umum aman dan dengan data hewan yang menjanjikan, data untuk manusia sangat kecil sejak 2014.[129]
Hewan lain[sunting | sunting sumber]
Penyakit paru obstruktif kronis bisa terjadi pada sejumlah hewan dan dapat diakibatkan karena paparan terhadap asap rokok.[130][131] Namun, penyakit ini pada sebagian besar kasus masih termasuk ringan.[132] Pada kuda ini dikenal juga sebagai obstruksi saluran napas kambuhan dan biasanya karena reaksi alergi terhadap jerami yang mengandung jamur.[133] COPD biasanya ditemukan pada anjing tua.[134]
Referensi[sunting | sunting sumber]
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa Vestbo, Jørgen (2013). "Definition and Overview" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. hlm. 1–7. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b c d e f g h i j k l m n Reilly, John J.; Silverman, Edwin K.; Shapiro, Steven D. (2011). "Chronic Obstructive Pulmonary Disease". Dalam Longo, Dan; Fauci, Anthony; Kasper, Dennis; Hauser, Stephen; Jameson, J.; Loscalzo, Joseph. Harrison's Principles of Internal Medicine (edisi ke-18th). McGraw Hill. hlm. 2151–9. ISBN 978-0-07-174889-6.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab Decramer M, Janssens W, Miravitlles M (April 2012). "Chronic obstructive pulmonary disease". Lancet. 379 (9823): 1341–51. doi:10.1016/S0140-6736(11)60968-9. PMID 22314182.
- ^ a b c d e f g h i j k Rabe KF, Hurd S, Anzueto A, Barnes PJ, Buist SA, Calverley P, Fukuchi Y, Jenkins C, Rodriguez-Roisin R, van Weel C, Zielinski J (September 2007). "Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary". Am. J. Respir. Crit. Care Med. 176 (6): 532–55. doi:10.1164/rccm.200703-456SO. PMID 17507545.
- ^ Nathell L, Nathell M, Malmberg P, Larsson K (2007). "COPD diagnosis related to different guidelines and spirometry techniques". Respir. Res. 8 (1): 89. doi:10.1186/1465-9921-8-89. PMC 2217523
 . PMID 18053200.
. PMID 18053200.
- ^ "The 10 leading causes of death in the world, 2000 and 2011". World Health Organization. July 2013. Diakses tanggal November 29, 2013.
- ^ Mathers CD, Loncar D (November 2006). "Projections of Global Mortality and Burden of Disease from 2002 to 2030". PLoS Med. 3 (11): e442. doi:10.1371/journal.pmed.0030442. PMC 1664601
 . PMID 17132052.
. PMID 17132052.
- ^ a b c Lomborg, Bjørn (2013). Global problems, local solutions : costs and benefits. Cambridge University Pres. hlm. 143. ISBN 978-1-107-03959-9.
- ^ a b c d e f g h i j k l m n o p q r s t u Vestbo, Jørgen (2013). "Diagnosis and Assessment" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. hlm. 9–17. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b c d e f g National Institute for Health and Clinical Excellence. Clinical guideline 101: Chronic Obstructive Pulmonary Disease. London, June 2010.
- ^ Mahler DA (2006). "Mechanisms and measurement of dyspnea in chronic obstructive pulmonary disease". Proceedings of the American Thoracic Society. 3 (3): 234–8. doi:10.1513/pats.200509-103SF. PMID 16636091.
- ^ "What Are the Signs and Symptoms of COPD?". National Heart, Lung, and Blood Institute. July 31, 2013. Diakses tanggal November 29, 2013.
- ^ MedlinePlus Encyclopedia Chronic obstructive pulmonary disease
- ^ Morrison, [edited by] Nathan E. Goldstein, R. Sean (2013). Evidence-based practice of palliative medicine. Philadelphia: Elsevier/Saunders. hlm. 124. ISBN 978-1-4377-3796-7.
- ^ a b Holland AE, Hill CJ, Jones AY, McDonald CF (2012). Holland, Anne E, ed. "Breathing exercises for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. 10: CD008250. doi:10.1002/14651858.CD008250.pub2. PMID 23076942.
- ^ a b c d e f Gruber, Phillip (November 2008). "The Acute Presentation of Chronic Obstructive Pulmonary Disease In the Emergency Department: A Challenging Oxymoron". Emergency Medicine Practice. 10 (11).
- ^ a b Weitzenblum E, Chaouat A (2009). "Cor pulmonale". Chron Respir Dis. 6 (3): 177–85. doi:10.1177/1479972309104664. PMID 19643833.
- ^ "Cor pulmonale". Professional guide to diseases (edisi ke-9th). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2009. hlm. 120–2. ISBN 978-0-7817-7899-2.
- ^ Mandell, editors, James K. Stoller, Franklin A. Michota, Jr., Brian F. (2009). The Cleveland Clinic Foundation intensive review of internal medicine (edisi ke-5th). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. hlm. 419. ISBN 978-0-7817-9079-6.
- ^ Brulotte CA, Lang ES (May 2012). "Acute exacerbations of chronic obstructive pulmonary disease in the emergency department". Emerg. Med. Clin. North Am. 30 (2): 223–47, vii. doi:10.1016/j.emc.2011.10.005. PMID 22487106.
- ^ Spiro, Stephen (2012). Clinical respiratory medicine expert consult (edisi ke-4th). Philadelphia, PA: Saunders. hlm. Chapter 43. ISBN 978-1-4557-2329-4.
- ^ World Health Organization (2008). WHO Report on the Global Tobacco Epidemic 2008: The MPOWER Package (PDF). Geneva: World Health Organization. hlm. 268–309. ISBN 92-4-159628-7.
- ^ a b Ward, Helen (2012). Oxford Handbook of Epidemiology for Clinicians. Oxford University Press. hlm. 289–290. ISBN 978-0-19-165478-7.
- ^ Laniado-Laborín, R (January 2009). "Smoking and chronic obstructive pulmonary disease (COPD). Parallel epidemics of the 21st century". International journal of environmental research and public health. 6 (1): 209–24. doi:10.3390/ijerph6010209. PMC 2672326
 . PMID 19440278.
. PMID 19440278.
- ^ a b Rennard, Stephen (2013). Clinical management of chronic obstructive pulmonary disease (edisi ke-2nd). New York: Informa Healthcare. hlm. 23. ISBN 978-0-8493-7588-0.
- ^ a b Anita Sharma ; with a contribution by David Pitchforth ; forewords by Gail Richards; Barclay, Joyce (2010). COPD in primary care. Oxford: Radcliffe Pub. hlm. 9. ISBN 978-1-84619-316-3.
- ^ Goldman, Lee (2012). Goldman's Cecil medicine (edisi ke-24th). Philadelphia: Elsevier/Saunders. hlm. 537. ISBN 978-1-4377-1604-7.
- ^ a b Kennedy SM, Chambers R, Du W, Dimich-Ward H (December 2007). "Environmental and occupational exposures: do they affect chronic obstructive pulmonary disease differently in women and men?". Proceedings of the American Thoracic Society. 4 (8): 692–4. doi:10.1513/pats.200707-094SD. PMID 18073405.
- ^ a b c d e f g h i j k l Pirozzi C, Scholand MB (July 2012). "Smoking cessation and environmental hygiene". Med. Clin. North Am. 96 (4): 849–67. doi:10.1016/j.mcna.2012.04.014. PMID 22793948.
- ^ Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM (September 2006). "Global burden of COPD: systematic review and meta-analysis". Eur. Respir. J. 28 (3): 523–32. doi:10.1183/09031936.06.00124605. PMID 16611654.
- ^ a b Devereux, Graham (2006). "Definition, epidemiology and risk factors". BMJ. 332 (7550): 1142–4. doi:10.1136/bmj.332.7550.1142. PMC 1459603
 . PMID 16690673.
. PMID 16690673.
- ^ Laine, Christine (2009). In the Clinic: Practical Information about Common Health Problems. ACP Press. hlm. 226. ISBN 978-1-934465-64-6.
- ^ a b Barnes, Peter J.; Drazen, Jeffrey M.; Rennard, Stephen I.; Thomson, Neil C., ed. (2009). "Relationship between cigarette smoking and occupational exposures". Asthma and COPD: Basic Mechanisms and Clinical Management. Amsterdam: Academic. hlm. 464. ISBN 978-0-12-374001-4.
- ^ Rushton, Lesley (2007). "Chronic Obstructive Pulmonary Disease and Occupational Exposure to Silica". Reviews on Environmental Health. 22 (4): 255–72. doi:10.1515/REVEH.2007.22.4.255. PMID 18351226.
- ^ a b c d Foreman MG, Campos M, Celedón JC (July 2012). "Genes and chronic obstructive pulmonary disease". Med. Clin. North Am. 96 (4): 699–711. doi:10.1016/j.mcna.2012.02.006. PMC 3399759
 . PMID 22793939.
. PMID 22793939.
- ^ Brode SK, Ling SC, Chapman KR (September 2012). "Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease". CMAJ. 184 (12): 1365–71. doi:10.1503/cmaj.111749. PMC 3447047
 . PMID 22761482.
. PMID 22761482.
- ^ a b c d e f g Vestbo, Jørgen (2013). "Management of Exacerbations" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. hlm. 39–45. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b c Dhar, Raja (2011). Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. hlm. 1056. ISBN 978-93-5025-073-0.
- ^ Palange, Paolo (2013). ERS Handbook of Respiratory Medicine. European Respiratory Society. hlm. 194. ISBN 978-1-84984-041-5.
- ^ Lötvall, Jan (2011). Advances in combination therapy for asthma and COPD. Chichester, West Sussex: John Wiley & Sons. hlm. 251. ISBN 978-1-119-97846-6.
- ^ Barnes, Peter (2009). Asthma and COPD : basic mechanisms and clinical management (edisi ke-2nd). Amsterdam: Academic. hlm. 837. ISBN 978-0-12-374001-4.
- ^ Hanania, Nicola (2010-12-09). COPD a Guide to Diagnosis and Clinical Management (edisi ke-1st). Totowa, NJ: Springer Science+Business Media, LLC. hlm. 197. ISBN 978-1-59745-357-8.
- ^ a b Beasley, V; Joshi, PV; Singanayagam, A; Molyneaux, PL; Johnston, SL; Mallia, P (2012). "Lung microbiology and exacerbations in COPD". International journal of chronic obstructive pulmonary disease. 7: 555–69. doi:10.2147/COPD.S28286. PMC 3437812
 . PMID 22969296.
. PMID 22969296.
- ^ Murphy DMF, Fishman AP (2008). "Chapter 53". Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 913. ISBN 0-07-145739-9.
- ^ a b Calverley PM, Koulouris NG (2005). "Flow limitation and dynamic hyperinflation: key concepts in modern respiratory physiology". Eur Respir J. 25 (1): 186–199. doi:10.1183/09031936.04.00113204. PMID 15640341.
- ^ Currie, Graeme P. (2010). ABC of COPD (edisi ke-2nd). Chichester, West Sussex, UK: Wiley-Blackwell, BMJ Books. hlm. 32. ISBN 978-1-4443-2948-3.
- ^ O'Donnell DE (2006). "Hyperinflation, Dyspnea, and Exercise Intolerance in Chronic Obstructive Pulmonary Disease". The Proceedings of the American Thoracic Society. 3 (2): 180–4. doi:10.1513/pats.200508-093DO. PMID 16565429.
- ^ a b c d e f Qaseem A, Wilt TJ, Weinberger SE, Hanania NA, Criner G, van der Molen T, Marciniuk DD, Denberg T, Schünemann H, Wedzicha W, MacDonald R, Shekelle P (August 2011). "Diagnosis and management of stable chronic obstructive pulmonary disease: a clinical practice guideline update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society". Ann. Intern. Med. 155 (3): 179–91. doi:10.7326/0003-4819-155-3-201108020-00008. PMID 21810710.
- ^ a b Young, Vincent B. (2010). Blueprints medicine (edisi ke-5th). Philadelphia: Wolters Kluwer Health/Lippincott William & Wilkins. hlm. 69. ISBN 978-0-7817-8870-0.
- ^ "COPD Assessment Test (CAT)". American Thoracic Society. Diakses tanggal November 29, 2013.
- ^ a b National Institute for Health and Clinical Excellence. Clinical guideline 101: Chronic Obstructive Pulmonary Disease. London, June 2010.
- ^ a b Torres M, Moayedi S (May 2007). "Evaluation of the acutely dyspneic elderly patient". Clin. Geriatr. Med. 23 (2): 307–25, vi. doi:10.1016/j.cger.2007.01.007. PMID 17462519.
- ^ BTS COPD Consortium (2005). "Spirometry in practice - a practical guide to using spirometry in primary care". hlm. 8–9. Diarsipkan dari versi asli tanggal 2014-08-26. Diakses tanggal 25 August 2014.
- ^ a b c d Mackay AJ, Hurst JR (July 2012). "COPD exacerbations: causes, prevention, and treatment". Med. Clin. North Am. 96 (4): 789–809. doi:10.1016/j.mcna.2012.02.008. PMID 22793945.
- ^ Poole PJ, Chacko E, Wood-Baker RW, Cates CJ (2006). Poole, Phillippa, ed. "Influenza vaccine for patients with chronic obstructive pulmonary disease". Cochrane Database Syst Rev (1): CD002733. doi:10.1002/14651858.CD002733.pub2. PMID 16437444.
- ^ a b c Vestbo, Jørgen (2013). "Introduction". Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (PDF). Global Initiative for Chronic Obstructive Lung Disease. xiii–xv. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b c Policy Recommendations for Smoking Cessation and Treatment of Tobacco Dependence. World Health Organization. hlm. 15–40. ISBN 978-92-4-156240-9. Diarsipkan dari versi asli tanggal 2008-09-15. Diakses tanggal 2015-08-18.
- ^ Jiménez-Ruiz CA, Fagerström KO (March 2013). "Smoking cessation treatment for COPD smokers: the role of counselling". Monaldi Arch Chest Dis. 79 (1): 33–7. PMID 23741944.
- ^ Kumar P, Clark M (2005). Clinical Medicine (edisi ke-6th). Elsevier Saunders. hlm. 900–1. ISBN 0-7020-2763-4.
- ^ a b Tønnesen P (March 2013). "Smoking cessation and COPD". Eur Respir Rev. 22 (127): 37–43. doi:10.1183/09059180.00007212. PMID 23457163.
- ^ "Why is smoking addictive?". NHS Choices. December 29, 2011. Diakses tanggal November 29, 2013.
- ^ Smith, Barbara K. Timby, Nancy E. (2005). Essentials of nursing : care of adults and children. Philadelphia: Lippincott Williams & Wilkins. hlm. 338. ISBN 978-0-7817-5098-1.
- ^ Rom, William N.; Markowitz, Steven B., ed. (2007). Environmental and occupational medicine (edisi ke-4th). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. hlm. 521–2. ISBN 978-0-7817-6299-1.
- ^ "Wet cutting". Health and Safety Executive. Diakses tanggal November 29, 2013.
- ^ George, Ronald B. (2005). Chest medicine : essentials of pulmonary and critical care medicine (edisi ke-5th). Philadelphia, PA: Lippincott Williams & Wilkins. hlm. 172. ISBN 978-0-7817-5273-2.
- ^ a b Vestbo, Jørgen (2013). "Management of Stable COPD". Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (PDF). Global Initiative for Chronic Obstructive Lung Disease. hlm. 31–8. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b Drummond MB, Dasenbrook EC, Pitz MW, Murphy DJ, Fan E (November 2008). "Inhaled corticosteroids in patients with stable chronic obstructive pulmonary disease: a systematic review and meta-analysis". JAMA. 300 (20): 2407–16. doi:10.1001/jama.2008.717. PMID 19033591.
- ^ a b Carlucci A, Guerrieri A, Nava S (December 2012). "Palliative care in COPD patients: is it only an end-of-life issue?". Eur Respir Rev. 21 (126): 347–54. doi:10.1183/09059180.00001512. PMID 23204123.
- ^ "COPD — Treatment". U.S. National Heart Lung and Blood Institute. Diakses tanggal 2013-07-23.
- ^ Puhan MA, Gimeno-Santos E, Scharplatz M, Troosters T, Walters EH, Steurer J (2011). Puhan, Milo A, ed. "Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev (10): CD005305. doi:10.1002/14651858.CD005305.pub3. PMID 21975749.
- ^ Lacasse Y, Goldstein R, Lasserson TJ, Martin S (2006). Lacasse, Yves, ed. "Pulmonary rehabilitation for chronic obstructive pulmonary disease". Cochrane Database Syst Rev (4): CD003793. doi:10.1002/14651858.CD003793.pub2. PMID 17054186.
- ^ Ferreira IM, Brooks D, White J, Goldstein R (2012). Ferreira, Ivone M, ed. "Nutritional supplementation for stable chronic obstructive pulmonary disease". Cochrane Database Syst Rev. 12: CD000998. doi:10.1002/14651858.CD000998.pub3. PMID 23235577.
- ^ van Dijk WD, van den Bemt L, van Weel C (2013). "Megatrials for bronchodilators in chronic obstructive pulmonary disease (COPD) treatment: time to reflect". J Am Board Fam Med. 26 (2): 221–4. doi:10.3122/jabfm.2013.02.110342. PMID 23471939.
- ^ Liesker JJ, Wijkstra PJ, Ten Hacken NH, Koëter GH, Postma DS, Kerstjens HA (February 2002). "A systematic review of the effects of bronchodilators on exercise capacity in patients with COPD". Chest. 121 (2): 597–608. doi:10.1378/chest.121.2.597. PMID 11834677.
- ^ Chong J, Karner C, Poole P (2012). Chong, Jimmy, ed. "Tiotropium versus long-acting beta-agonists for stable chronic obstructive pulmonary disease". Cochrane Database Syst Rev. 9: CD009157. doi:10.1002/14651858.CD009157.pub2. PMID 22972134.
- ^ a b Karner C, Cates CJ (2012). Karner, Charlotta, ed. "Long-acting beta(2)-agonist in addition to tiotropium versus either tiotropium or long-acting beta(2)-agonist alone for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. 4: CD008989. doi:10.1002/14651858.CD008989.pub2. PMID 22513969.
- ^ a b c d e f g h Vestbo, Jørgen (2013). "Therapeutic Options" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. hlm. 19–30. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal 2015-08-18.
- ^ a b Cave, AC.; Hurst, MM. (May 2011). "The use of long acting β₂-agonists, alone or in combination with inhaled corticosteroids, in chronic obstructive pulmonary disease (COPD): a risk-benefit analysis". Pharmacol Ther. 130 (2): 114–43. doi:10.1016/j.pharmthera.2010.12.008. PMID 21276815.
- ^ Spencer, S; Karner, C; Cates, CJ; Evans, DJ (Dec 7, 2011). Spencer, Sally, ed. "Inhaled corticosteroids versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease". The Cochrane database of systematic reviews (12): CD007033. doi:10.1002/14651858.CD007033.pub3. PMID 22161409.
- ^ Wang, J; Nie, B; Xiong, W; Xu, Y (April 2012). "Effect of long-acting beta-agonists on the frequency of COPD exacerbations: a meta-analysis". Journal of clinical pharmacy and therapeutics. 37 (2): 204–11. doi:10.1111/j.1365-2710.2011.01285.x. PMID 21740451.
- ^ Decramer ML, Hanania NA, Lötvall JO, Yawn BP (2013). "The safety of long-acting β2-agonists in the treatment of stable chronic obstructive pulmonary disease". Int J Chron Obstruct Pulmon Dis. 8: 53–64. doi:10.2147/COPD.S39018. PMC 3558319
 . PMID 23378756.
. PMID 23378756.
- ^ Nannini, LJ; Lasserson, TJ; Poole, P (Sep 12, 2012). Nannini, Luis Javier, ed. "Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease". The Cochrane database of systematic reviews. 9: CD006829. doi:10.1002/14651858.CD006829.pub2. PMID 22972099.
- ^ Cheyne L, Irvin-Sellers MJ, White J (Sep 16, 2013). Cheyne, Leanne, ed. "Tiotropium versus ipratropium bromide for chronic obstructive pulmonary disease". Cochrane Database of Systematic Reviews. 9 (9): CD009552. doi:10.1002/14651858.CD009552.pub2. PMID 24043433.
- ^ Karner, C; Chong, J; Poole, P (Jul 11, 2012). Karner, Charlotta, ed. "Tiotropium versus placebo for chronic obstructive pulmonary disease". The Cochrane database of systematic reviews. 7: CD009285. doi:10.1002/14651858.CD009285.pub2. PMID 22786525.
- ^ Singh S, Loke YK, Furberg CD (September 2008). "Inhaled anticholinergics and risk of major adverse cardiovascular events in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis". JAMA. 300 (12): 1439–50. doi:10.1001/jama.300.12.1439. PMID 18812535.
- ^ Singh S, Loke YK, Enright P, Furberg CD (January 2013). "Pro-arrhythmic and pro-ischaemic effects of inhaled anticholinergic medications". Thorax. 68 (1): 114–6. doi:10.1136/thoraxjnl-2011-201275. PMID 22764216.
- ^ Jones, P (Apr 2013). "Aclidinium bromide twice daily for the treatment of chronic obstructive pulmonary disease: a review". Advances in therapy. 30 (4): 354–68. doi:10.1007/s12325-013-0019-2. PMID 23553509.
- ^ Cazzola, M; Page, CP; Matera, MG (Jun 2013). "Aclidinium bromide for the treatment of chronic obstructive pulmonary disease". Expert opinion on pharmacotherapy. 14 (9): 1205–14. doi:10.1517/14656566.2013.789021. PMID 23566013.
- ^ Gartlehner G, Hansen RA, Carson SS, Lohr KN (2006). "Efficacy and Safety of Inhaled Corticosteroids in Patients With COPD: A Systematic Review and Meta-Analysis of Health Outcomes". Ann Fam Med. 4 (3): 253–62. doi:10.1370/afm.517. PMC 1479432
 . PMID 16735528.
. PMID 16735528.
- ^ Shafazand S (June 2013). "ACP Journal Club. Review: inhaled medications vary substantively in their effects on mortality in COPD". Ann. Intern. Med. 158 (12): JC2. doi:10.7326/0003-4819-158-12-201306180-02002. PMID 23778926.
- ^ Mammen MJ, Sethi S (2012). "Macrolide therapy for the prevention of acute exacerbations in chronic obstructive pulmonary disease". Pol. Arch. Med. Wewn. 122 (1–2): 54–9. PMID 22353707.
- ^ a b Herath, SC; Poole, P (Nov 28, 2013). "Prophylactic antibiotic therapy for chronic obstructive pulmonary disease (COPD)". The Cochrane database of systematic reviews. 11: CD009764. doi:10.1002/14651858.CD009764.pub2. PMID 24288145.
- ^ Simoens, S; Laekeman, G; Decramer, M (May 2013). "Preventing COPD exacerbations with macrolides: a review and budget impact analysis". Respiratory medicine. 107 (5): 637–48. doi:10.1016/j.rmed.2012.12.019. PMID 23352223.
- ^ Barr RG, Rowe BH, Camargo CA (2003). Barr, R Graham, ed. "Methylxanthines for exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev (2): CD002168. doi:10.1002/14651858.CD002168. PMID 12804425.
- ^ a b COPD Working, Group (2012). "Long-term oxygen therapy for patients with chronic obstructive pulmonary disease (COPD): an evidence-based analysis". Ontario health technology assessment series. 12 (7): 1–64. PMC 3384376
 . PMID 23074435.
. PMID 23074435.
- ^ Bradley JM, O'Neill B (2005). Bradley, Judy M, ed. "Short-term ambulatory oxygen for chronic obstructive pulmonary disease". Cochrane Database Syst Rev (4): CD004356. doi:10.1002/14651858.CD004356.pub3. PMID 16235359.
- ^ Uronis H, McCrory DC, Samsa G, Currow D, Abernethy A (2011). Abernethy, Amy, ed. "Symptomatic oxygen for non-hypoxaemic chronic obstructive pulmonary disease". Cochrane Database Syst Rev (6): CD006429. doi:10.1002/14651858.CD006429.pub2. PMID 21678356.
- ^ Chapman, Stephen (2009). Oxford handbook of respiratory medicine (edisi ke-2nd). Oxford: Oxford University Press. hlm. 707. ISBN 978-0-19-954516-2.
- ^ Blackler, Laura (2007). Managing chronic obstructive pulmonary disease. Chichester, England: John Wiley & Sons. hlm. 49. ISBN 978-0-470-51798-7.
- ^ Jindal, Surinder K (2013). Chronic Obstructive Pulmonary Disease. Jaypee Brothers Medical. hlm. 139. ISBN 978-93-5090-353-7.
- ^ a b O'Driscoll, BR; Howard, LS; Davison, AG; British Thoracic, Society (October 2008). "BTS guideline for emergency oxygen use in adult patients". Thorax. 63 (Suppl 6): vi1–68. doi:10.1136/thx.2008.102947. PMID 18838559.
- ^ a b Vollenweider DJ, Jarrett H, Steurer-Stey CA, Garcia-Aymerich J, Puhan MA (2012). Vollenweider, Daniela J, ed. "Antibiotics for exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev. 12: CD010257. doi:10.1002/14651858.CD010257. PMID 23235687.
- ^ Jeppesen, E; Brurberg, KG; Vist, GE; Wedzicha, JA; Wright, JJ; Greenstone, M; Walters, JA (May 16, 2012). "Hospital at home for acute exacerbations of chronic obstructive pulmonary disease". The Cochrane database of systematic reviews. 5: CD003573. doi:10.1002/14651858.CD003573.pub2. PMID 22592692.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. Diakses tanggal Nov 11, 2009.
- ^ a b Murray CJ, Vos T, Lozano R, Naghavi M, Flaxman AD, Michaud C, Ezzati M, Shibuya K, Salomon JA; et al. (December 2012). "Disability-adjusted life years (DALYs) for 291 diseases and injuries in 21 regions, 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2197–223. doi:10.1016/S0140-6736(12)61689-4. PMID 23245608.
- ^ a b Vos T, Flaxman AD, Naghavi M, Lozano R, Michaud C, Ezzati M, Shibuya K, Salomon JA, Abdalla S, Aboyans V; et al. (December 2012). "Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2163–96. doi:10.1016/S0140-6736(12)61729-2. PMID 23245607.
- ^ Medicine, prepared by the Department of Medicine, Washington University School of (2009). The Washington manual general internal medicine subspecialty consult (edisi ke-2nd). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. hlm. 96. ISBN 978-0-7817-9155-7.
- ^ "Chronic obstructive pulmonary disease (COPD) Fact sheet N°315". WHO. November 2012.
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, Abraham J, Adair T, Aggarwal R; et al. (December 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859): 2095–128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
- ^ Rycroft CE, Heyes A, Lanza L, Becker K (2012). "Epidemiology of chronic obstructive pulmonary disease: a literature review". Int J Chron Obstruct Pulmon Dis. 7: 457–94. doi:10.2147/COPD.S32330. PMC 3422122
 . PMID 22927753.
. PMID 22927753.
- ^ Simpson CR, Hippisley-Cox J, Sheikh A (2010). "Trends in the epidemiology of chronic obstructive pulmonary disease in England: a national study of 51 804 patients". Brit J Gen Pract. 60 (576): 483–8. doi:10.3399/bjgp10X514729. PMC 2894402
 . PMID 20594429.
. PMID 20594429.
- ^ Centers for Disease Control and Prevention (Nov 23, 2012). "Chronic Obstructive Pulmonary Disease Among Adults — United States, 2011". Morbidity and Mortality Weekly Report. 61 (46): 938–43. PMID 23169314.
- ^ "Morbidity & Mortality: 2009 Chart Book on Cardiovascular, Lung, and Blood Diseases" (PDF). National Heart, Lung, and Blood Institute.
- ^ a b Torio CM, Andrews RM (2006). "National Inpatient Hospital Costs: The Most Expensive Conditions by Payer, 2011: Statistical Brief #160". Healthcare Cost and Utilization Project (HCUP) Statistical Briefs. Agency for Health Care Policy and Research. PMID 24199255. Diarsipkan dari versi asli tanggal 2017-03-14. Diakses tanggal 2015-08-18.
- ^ "Emphysema". Dictionary.com. Diakses tanggal 21 November 2013.
- ^ a b Ziment, Irwin (1991). "History of the Treatment of Chronic Bronchitis". Respiration. 58 (Suppl 1): 37–42. doi:10.1159/000195969. PMID 1925077.
- ^ a b c d Petty TL (2006). "The history of COPD". Int J Chron Obstruct Pulmon Dis. 1 (1): 3–14. doi:10.2147/copd.2006.1.1.3. PMC 2706597
 . PMID 18046898.
. PMID 18046898.
- ^ a b Wright, Joanne L.; Churg, Andrew (2008). "Pathologic Features of Chronic Obstructive Pulmonary Disease: Diagnostic Criteria and Differential Diagnosis" (PDF). Dalam Fishman, Alfred; Elias, Jack; Fishman, Jay; Grippi, Michael; Senior, Robert; Pack, Allan. Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). New York: McGraw-Hill. hlm. 693–705. ISBN 978-0-07-164109-8. Diarsipkan dari versi asli (PDF) tanggal 2016-03-03. Diakses tanggal 2015-08-18.
- ^ George L. Waldbott (1965). A struggle with Titans. Carlton Press. hlm. 6.
- ^ Fishman AP (May 2005). "One hundred years of chronic obstructive pulmonary disease". Am. J. Respir. Crit. Care Med. 171 (9): 941–8. doi:10.1164/rccm.200412-1685OE. PMID 15849329.
- ^ Yuh-Chin, T. Huang (2012-10-28). A clinical guide to occupational and environmental lung diseases. [New York]: Humana Press. hlm. 266. ISBN 978-1-62703-149-3.
- ^ "Pink Puffer - definition of Pink Puffer in the Medical dictionary - by the Free Online Medical Dictionary, Thesaurus and Encyclopedia". Medical-dictionary.thefreedictionary.com. Diakses tanggal 2013-07-23.
- ^ a b c Weinberger, Steven E. (2013-05-08). Principles of pulmonary medicine (edisi ke-6th). Philadelphia: Elsevier/Saunders. hlm. 165. ISBN 978-1-62703-149-3.
- ^ Des Jardins, Terry (2013). Clinical Manifestations & Assessment of Respiratory Disease (edisi ke-6th). Elsevier Health Sciences. hlm. 176. ISBN 978-0-323-27749-5.
- ^ An outcomes strategy for people with chronic obstructive pulmonary disease (COPD) and asthma in England (PDF). Department of Health. 18 July 2011. hlm. 5. Diakses tanggal 27 November 2013.
- ^ Bloom, D (2011). The Global Economic Burden of Noncommunicable Diseases (PDF). World Economic Forum. hlm. 24.
- ^ Nici, Linda (2011). Chronic Obstructive Pulmonary Disease: Co-Morbidities and Systemic Consequences. Springer. hlm. 78. ISBN 978-1-60761-673-3.
- ^ Inamdar, AC; Inamdar, AA (Oct 2013). "Mesenchymal stem cell therapy in lung disorders: pathogenesis of lung diseases and mechanism of action of mesenchymal stem cell". Experimental lung research. 39 (8): 315–27. doi:10.3109/01902148.2013.816803. PMID 23992090.
- ^ Conese, M; Piro, D; Carbone, A; Castellani, S; Di Gioia, S (2014). "Hematopoietic and mesenchymal stem cells for the treatment of chronic respiratory diseases: role of plasticity and heterogeneity". TheScientificWorldJournal. 2014: 859817. doi:10.1155/2014/859817. PMC 3916026
 . PMID 24563632.
. PMID 24563632.
- ^ Akers, R. Michael; Denbow, D. Michael (2008). Anatomy and Physiology of Domestic Animals. Arnes, AI: Wiley. hlm. 852. ISBN 978-1-118-70115-7.
- ^ Wright, JL; Churg, A (December 2002). "Animal models of cigarette smoke-induced COPD". Chest. 122 (6 Suppl): 301S–6S. doi:10.1378/chest.122.6_suppl.301S. PMID 12475805.
- ^ Churg, A; Wright, JL (2007). "Animal models of cigarette smoke-induced chronic obstructive lung disease". Contributions to microbiology. Contributions to Microbiology. 14: 113–25. doi:10.1159/000107058. ISBN 3-8055-8332-X. PMID 17684336.
- ^ Marinkovic D, Aleksic-Kovacevic S, Plamenac P (2007). "Cellular basis of chronic obstructive pulmonary disease in horses". Int. Rev. Cytol. International Review of Cytology. 257: 213–47. doi:10.1016/S0074-7696(07)57006-3. ISBN 978-0-12-373701-4. PMID 17280899.
- ^ Miller MS, Tilley LP, Smith FW (January 1989). "Cardiopulmonary disease in the geriatric dog and cat". Vet. Clin. North Am. Small Anim. Pract. 19 (1): 87–102. PMID 2646821.
Referensi lainnya[sunting | sunting sumber]
- "Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease, Updated 2013" (PDF). Global Initiative for Chronic Obstructive Lung Disease. Diarsipkan dari versi asli (PDF) tanggal 2013-10-04. Diakses tanggal November 29, 2013.
- National Institute for Health and Clinical Excellence. Clinical guideline 101: Chronic Obstructive Pulmonary Disease. London, June 2010.
- Qaseem, Amir; Wilt, TJ; Weinberger, SE; Hanania, NA; Criner, G; Van Der Molen, T; Marciniuk, DD; Denberg, T; Schünemann, H; Wedzicha, W; MacDonald, R; Shekelle, P; American College Of, Physicians; American College of Chest Physicians; American Thoracic, Society; European Respiratory, Society (2011). "Diagnosis and Management of Stable Chronic Obstructive Pulmonary Disease: A Clinical Practice Guideline Update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society". Annals of Internal Medicine. 155 (3): 179–91. doi:10.7326/0003-4819-155-3-201108020-00008. PMID 21810710.
Pranala luar[sunting | sunting sumber]
- Penyakit paru obstruktif kronis di Curlie (dari DMOZ)