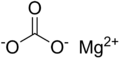
Magnesium karbonat
| |

| |
| Nama | |
|---|---|
| Nama lain | |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| MgCO3 | |
| Massa molar | 84.3139 g/mol (anhidrat) |
| Penampilan | padatan putih higroskopis |
| Bau | tak berbau |
| Densitas | 2.958 g/cm3 (anhidrat) 2.825 g/cm3 (dihidrat) 1.837 g/cm3 (trihidrat) 1.73 g/cm3 (pentahidrat) |
| Titik lebur | 350 °C (662 °F; 623 K) terurai (anhidrat) 165 °C (329 °F; 438 K) (trihidrat) |
| anhidrat: 0.0139 g/100ml (25 °C) 0.00603 g/100ml (100 °C)[1] | |
| Hasil kali kelarutan, Ksp | 10−7.8[2] |
| Kelarutan | larut dalam asam, CO2 berair tidak larut dalam aseton, amonia |
| −32.4·10−6 cm3/mol | |
| Indeks bias (nD) | 1.717 (anhidrat) 1.458 (dihidrat) 1.412 (trihidrat) |
| Struktur | |
| Trigonal | |
| Termokimia | |
| Kapasitas kalor (C) | 75.6 J/mol·K[1] |
| Entropi molar standar (S |
65.7 J/mol·K[1][3] |
| Entalpi pembentukan standar (ΔfH |
-1113 kJ/mol[3] |
| Energi bebas Gibbs (ΔfG) | -1029.3 kJ/mol[1] |
| Farmakologi | |
| Kode ATC | A02 A06AD01 |
| Bahaya | |
| Lembar data keselamatan | ICSC 0969 |
| Titik nyala | Tidak mudah terbakar |
| Batas imbas kesehatan AS (NIOSH): | |
PEL (yang diperbolehkan)
|
TWA 15 mg/m3 (total) TWA 5 mg/m3 (resp)[4] |
| Senyawa terkait | |
Anion lain
|
Magnesium bikarbonat |
Kation lainnya
|
Berilium karbonat Kalsium karbonat Stronsium karbonat Barium karbonat |
Senyawa terkait
|
Artinit Hidromagnesit Dipingit |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Magnesium karbonat, MgCO3, atau dikenal pula dengan nama lamanya magnesia alba, adalah suatu garam anorganik yang berupa padatan putih. Beberapa bentuk hidrat dan basa magnesium karbonat juga terdapat sebagai mineral.
Bentuk[sunting | sunting sumber]
Bentuk magnesium karbonat yang paling umum adalah garam anhidrat yang disebut magnesit (MgCO3) dan di, tri, serta pentahidratnya yang dikenal sebagai barringtonit (MgCO3·2 H2O), nesquehonit (MgCO3·3 H2O), dan lansfordit (MgCO3·5 H2O), berturut-turut.[5] Beberapa bentuk basanya diantaranya artinit (MgCO3·Mg(OH)2·3 H2O), hidromagnesit (4 MgCO3·Mg(OH)2·4 H2O), serta dipingit (4 MgCO3· Mg(OH)2·5 H2O) yang juga terdapat sebagai mineral.
Preparasi[sunting | sunting sumber]
Magnesium karbonat biasanya diperoleh dengan menambang mineral magnesit. Tujuh puluh persen dari pasokan dunia ditambang dan disiapkan di Tiongkok.[6]
Magnesium karbonat dapat disiapkan di laboratorium dengan reaksi antara garam magnesium yang larut dan natrium bikarbonat:
- MgCl2(aq) + 2NaHCO3(aq) → MgCO3(s) + 2NaCl(aq) + H2O(l) + CO2(g)
Jika magnesium klorida (atau sulfat) diperlakukan dengan natrium karbonat berair, endapan magnesium karbonat basa—suatu kompleks magnesium karbonat dan magnesium hidroksida terhidrasi—alih-alih magnesium karbonat sendiri terbentuk:
- 5MgCl2(aq) + 5Na2CO3(aq) + 5H2O(l) → Mg(OH)2·3MgCO3·3H2O(s) + Mg(HCO3)2(aq) + 10NaCl(aq)
Rute industri dengan kemurnian tinggi mencakup jalur melalui magnesium bikarbonat, yang dapat dibentuk dengan menggabungkan bubur magnesium hidroksida dan karbon dioksida pada tekanan tinggi dan suhu sedang.[5] Bikarbonat kemudian dikeringkan dengan vakum, menyebabkannya hilangnya karbon dioksida dan molekul air:
- Mg(OH)2 + 2 CO2 → Mg(HCO3)2
- Mg(HCO3)2 → MgCO3 + CO2 + H2O
Reaksi[sunting | sunting sumber]
Dengan asam[sunting | sunting sumber]
Seperti banyak karbonat logam golongan 2 yang umum, magnesium karbonat bereaksi dengan asam berair untuk melepaskan karbon dioksida dan air:
- MgCO3 + 2 HCl → MgCl2 + CO2 + H2O
- MgCO3 + H2SO4 → MgSO4 + CO2 + H2O
Dekomposisi[sunting | sunting sumber]
Pada suhu tinggi MgCO3 terurai menjadi magnesium oksida dan karbon dioksida. Proses ini penting dalam produksi magnesium oksida.[5] Proses ini disebut sebagai kalsinasi:
- MgCO3 → MgO + CO2 (ΔH = +118 kJ/mol)
Suhu peruraian ini dilakukan pada 350 °C (662 °F).[7][8] Namun, kalsinasi menjadi magnesium oksida umumnya tidak dianggap sempurna di bawah suhu 900 °C karena adanya gangguan akibat penyerapan kembali karbon dioksida bebas.
Hidrat garam kehilangan air pada suhu yang berbeda selama dekomposisi.[9] Misalnya, dalam trihidratnya, dengan rumus molekul yang dapat dituliskan sebagai Mg(HCO3)(OH)•2(H2O), tahapan dehidrasi terjadi pada suhu antara 157 °C dan 179 °C sebagai berikut:[10]
- Mg(HCO3)(OH)•2(H2O) → Mg(HCO3)(OH)•(H2O) + H2O pada 157 °C
- Mg(HCO3)(OH)•(H2O) → Mg(HCO3)(OH) + H2O pada 179 °C
Kegunaan[sunting | sunting sumber]
Penggunaan utama magnesium karbonat adalah dalam produksi magnesium oksida oleh kalsinasi. Mineral magnesit dan dolomit digunakan untuk memproduksi batu bata tahan api.[5] MgCO3 juga digunakan dalam komposisi lantai tahan api, pemadam api, kosmetik, bubuk debu, dan pasta gigi. Aplikasi lain adalah sebagai bahan pengisi, penekan asap dalam plastik, zat penguat dalam karet neoprena, zat pengering, pencahar untuk melonggarkan usus, dan retensi warna dalam makanan. Selain itu, magnesium karbonat dengan kemurnian tinggi digunakan sebagai antasida dan sebagai aditif dalam garam meja agar tetap mengalir bebas. Magnesium karbonat dapat melakukan ini karena tidak larut dalam air, hanya larut dalam asam, yang membuatnya berbuih (menghasilkan gelembung).[11]
Sebagai aditif makanan, magnesium karbonat dikenal sebagai E504, yang satu-satunya efek samping yang diketahui adalah dapat bekerja sebagai pencahar dalam konsentrasi tinggi.[12]
Magnesium karbonat juga digunakan dalam taksidermi untuk memutihkan tengkorak. Senyawa ini dapat dicampur dengan hidrogen peroksida untuk membuat pasta, yang kemudian diaplikasikan pada tengkorak untuk memberikannya warna putih.
Selain itu, magnesium karbonat digunakan sebagai lapisan putih untuk layar proyeksi.[13]
Keamanan[sunting | sunting sumber]
Magnesium karbonat bersifat non-toksik.[5]
Status kompendial[sunting | sunting sumber]
Lihat pula[sunting | sunting sumber]
- Kalsium asetat/magnesium karbonat
- Upsalit, bentuk magnesium karbonat amorf yang dilaporkan
Catatan dan referensi[sunting | sunting sumber]
- ^ a b c d http://chemister.ru/Database/properties-en.php?dbid=1&id=634
- ^ Bénézeth, Pascale; Saldi, Giuseppe D.; Dandurand, Jean-Louis; Schott, Jacques (2011). "Experimental determination of the solubility product of magnesite at 50 to 200 °C". Chemical Geology. 286 (1–2): 21–31. doi:10.1016/j.chemgeo.2011.04.016.
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. hlm. A22. ISBN 0-618-94690-X.
- ^ "NIOSH Pocket Guide to Chemical Hazards #0373". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b c d e Margarete Seeger; Walter Otto; Wilhelm Flick; Friedrich Bickelhaupt; Otto S. Akkerman (2005), "Magnesium Compounds", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a15_595.pub2
- ^ Allf, Bradley (2018-05-21). "The Hidden Environmental Cost of Climbing Chalk". Climbing Magazine. Cruz Bay Publishing. Diakses tanggal 2018-05-22.
In fact, China produces 70 percent of the world’s magnesite. Most of that production—both mining and processing—is concentrated in a small corner of Liaoning, a hilly industrial province in northeast China between Beijing and North Korea.
- ^ "IAState MSDS". Diarsipkan dari versi asli tanggal 2016-04-25. Diakses tanggal 2019-08-04.
- ^ Weast, Robert C.; et al. (1978). CRC Handbook of Chemistry and Physics (edisi ke-59). West Palm Beach, FL: CRC Press. hlm. B-133. ISBN 0-8493-0549-8 Invalid ISBN.
- ^ "Conventional and Controlled Rate Thermal analysis of nesquehonite Mg(HCO3)(OH)·2(H2O)" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2014-11-02. Diakses tanggal 2019-08-04.
- ^ "Conventional and Controlled Rate Thermal analysis of nesquehonite Mg(HCO3)(OH)•2(H2O)" (PDF). Diarsipkan dari versi asli (PDF) tanggal 2014-11-02. Diakses tanggal 2019-08-04.
- ^ "What Is Magnesium Carbonate?". Sciencing (dalam bahasa Inggris). Diakses tanggal 2018-04-15.
- ^ "Food-Info.net : E-numbers : E504: Magnesium carbonates". 080419 food-info.net
- ^ Noronha, Shonan (2015). Certified Technology Specialist-Installation. McGraw Hill Education. hlm. 256. ISBN 978-0071835657.
- ^ British Pharmacopoeia Commission Secretariat (2009). "Index, BP 2009" (PDF). Diarsipkan dari versi asli (PDF) tanggal 11 April 2009. Diakses tanggal 31 January 2010.
- ^ "Japanese Pharmacopoeia, Fifteenth Edition" (PDF). 2006. Diarsipkan dari versi asli (PDF) tanggal 22 July 2011. Diakses tanggal 31 January 2010.
Pranala luar[sunting | sunting sumber]
- (Inggris) International Chemical Safety Card 0969
- (Inggris) NIST Standard Reference Database
