Gadolinium(III) iodida
| |
| Penanda | |
|---|---|
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| GdI3 | |
| Massa molar | 537,96 g/mol−1 |
| Penampilan | Padatan kuning |
| Titik lebur | 926 °C[1] |
| Titik didih | 1340 °C[2] |
| Bahaya | |
| Piktogram GHS |  
|
| Keterangan bahaya GHS | {{{value}}} |
| H317, H360 | |
| P201, P280, P308+313[1] | |
| Senyawa terkait | |
Anion lain
|
Gadolinium(III) fluorida Gadolinium(III) klorida Gadolinium(III) bromida |
Kation lainnya
|
Samarium(III) iodida Europium(III) iodida Terbium(III) iodida Disprosium(III) iodida |
Senyawa terkait
|
Gadolinium(II) iodida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
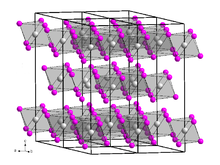
Gadolinium(III) iodida adalah sebuah senyawa iodida dari gadolinium, dengan rumus GdI3. Senyawa ini merupakan padatan berwarna kuning yang sangat higroskopis dengan struktur kristal jenis bismut(III) iodida. Di udara, ia dengan cepat menyerap kelembapan dan membentuk hidrat. Bentuk oksida iodida yang sesuai juga mudah terbentuk pada suhu tinggi.[2]
Pembuatan
[sunting | sunting sumber]Gadolinium(III) iodida dapat diperoleh dengan mereaksikan gadolinium dengan iodin:[2]
- 2 Gd + 3 I2 → 2 GdI3
Senyawa ini juga dapat diperoleh dengan mereaksikan gadolinium dengan raksa(II) iodida dalam vakum pada suhu 500 °C:[2]
- 2 Gd + 3 HgI2 → 2 GdI3 + 3 Hg
Gadolinium(III) iodida dapat diperoleh melalui reaksi antara gadolinium(III) oksida dan asam iodida, mengkristal menjadi bentuk hidrat. Bentuk hidrat dapat dipanaskan dengan amonium iodida untuk membentuk bentuk anhidrat.[2][3]
- Gd2O3 + 6 HI → 2 GdI3 + 3 H2O
Reaksi
[sunting | sunting sumber]Gadolinium(III) iodida akan bereaksi dengan gadolinium dan seng dalam atmosfer argon yang dipanaskan hingga suhu 850 °C untuk menghasilkan Gd7I12Zn.[4] GdI3 juga bereaksi dengan gadolinium, karbon, dan gadolinium nitrida dalam tabung tantalum pada suhu 897 °C untuk menghasilkan nitrokarbida Gd4I6CN.[5]
Referensi
[sunting | sunting sumber]- ^ a b c Sigma-Aldrich Co., produk no. {{{id}}}.
- ^ a b c d e Georg Brauer (Hrsg.), unter Mitarbeit von Marianne Baudler u. a.: Handbuch der Präparativen Anorganischen Chemie. 3., umgearbeitete Auflage. Band I, Ferdinand Enke, Stuttgart 1975, ISBN 3-432-02328-6, S. 1077.
- ^ Kutscher, J.; Schneider, A. Preparation of anhydrous lanthanide halides, especially iodides. Inorganic and Nuclear Chemistry Letters, 1971. 7 (9): 815-819.
- ^ Mar’yana Lukachuk, Lorenz Kienle, Chong Zheng, Hansjürgen Mattausch, Arndt Simon (2 Juni 2008). "Gd 7 I 12 Zn: A Group 12 Atom in the Octahedral Gd 6 Cluster". Inorganic Chemistry (dalam bahasa Inggris). 47 (11): 4656–4660. doi:10.1021/ic800024n. ISSN 0020-1669. PMID 18426200. Diarsipkan dari versi asli tanggal 23 April 2022. Diakses tanggal 17 Februari 2024.
- ^ Mattausch, Hansjurgen; Borrmann, Horst; Eger, Roland; Kremer, R. K.; Simon, Arndt. Gd4I6CN: A carbide nitride with chains of Gd6(C2) octahedra and Gd6N2 double tetrahedra. Zeitschrift fuer Anorganische und Allgemeine Chemie (1994), 620 (11): 1889-1897.
Bacaan lebih lanjut
[sunting | sunting sumber]- Asprey, L. B.; Keenan, T. K.; Kruse, F. H. Preparation and crystal data for lanthanide and actinide triiodides. Inorg. Chem., 1964. 3 (8): 1137-1240
