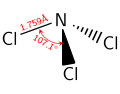Nitrogen triklorida
| |||

| |||
| Nama | |||
|---|---|---|---|
| Nama lain
Trikloramina
Agene Nitrogen(III) klorida Trikloroazana Triklorin nitrida | |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChemSpider | |||
| Nomor EC | |||
| Referensi Gmelin | 1840 | ||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| NCl3 | |||
| Penampilan | cairan kuning berminyak | ||
| Bau | seperti-klorin | ||
| Densitas | 1.653 g/mL | ||
| Titik lebur | −40 °C | ||
| Titik didih | 71 °C | ||
| tak larut terurai lambat | |||
| Kelarutan | larut dalam benzena, kloroform, CCl4, CS2, PCl3 | ||
| Struktur | |||
| ortorombik (di bawah −40 °C) | |||
| trigonal piramidal | |||
| 0.6 D | |||
| Termokimia | |||
| Entalpi pembentukan standar (ΔfH |
232 kJ/mol | ||
| Bahaya | |||
Klasifikasi UE (DSD) (usang)
|
tidak terdaftar | ||
| 93 °C (199 °F; 366 K) | |||
| Senyawa terkait | |||
Anion lain
|
Nitrogen trifluorida Nitrogen tribromida Nitrogen triiodida | ||
Kation lainnya
|
Fosforus triklorida Arsenik triklorida | ||
Related kloramina
|
Kloramina Dikloramina | ||
Senyawa terkait
|
Nitrosil klorida | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Nitrogen triklorida, dikenal pula sebagai trikloramina, adalah suatu senyawa kimia dengan rumus NCl3. Cairan berwarna kuning, berminyak, berbau tajam ini paling sering dijumpai sebagai hasil sampingan dari reaksi kimia antara turunan-amonia dan klorin (misalnya, di kolam renang).
Preparasi dan struktur[sunting | sunting sumber]
Senyawa ini dibuat dengan memperlakukan garam amonium, seperti amonium nitrat dengan klorin.
Zat antara dalam konversi ini meliputi kloramina dan dikloramina, NH2Cl dan NHCl2, berturut-turut.
Seperti amonia, NCl3 adalah molekul piramidal. Jarak N-Cl adalah 1.76 Å, dan sudut Cl-N-Cl adalah 107°.[1]
Nitrogen triklorida dapat terbentuk dalam jumlah kecil ketika persediaan air publik didesinfeksi dengan monokloramina, dan di kolam renang dengan desinfektan klorin bereaksi dengan urea dalam air kencing dan keringat dari pemandian. Nitrogen triklorida, yang diberi merek dagang Agene, digunakan untuk pemutih buatan dan penua tepung, namun dilarang pada tahun 1949: pada manusia Agene ditemukan menyebabkan kelainan neurologis yang parah dan meluas yang menyebabkan pelarangannya pada tahun 1947. Anjing yang mengkonsumsi roti yang terbuat dari tepung terigu yang diberi perlakuan tersebut menderita seperti epilepsi; agen beracunnya adalah metionin sulfoksimina.[2]
Reaksi[sunting | sunting sumber]
Kimia NCl3 telah dieksplorasi dengan baik.[3] Senyawa ini cukup polar dengan momen dipol 0.6 D. Pusat nitrogen bersifat basa tapi jauh lebih sedikit daripada amonia. Senyawa ini dihidrolisis oleh air panas untuk melepaskan amonia dan asam hipoklorit.
- NCl3 + 3 H2O → NH3 + 3 HOCl
NCl3 meledak untuk menghasilkan N2 dan gas klorin. Reaksi ini dihambat oleh gas encer.
Keamanan[sunting | sunting sumber]
Nitrogen triklorida dapat mengiritasi membran mukosa—senyawa ini adalah agen pembuat air mata, namun tidak pernah digunakan seperti itu.[4][5] Zat murni (jarang ditemui) adalah bahan peledak yang berbahaya, sensitif terhadap cahaya, panas, bahkan kejutan sedang, dan senyawa organik. Pierre Louis Dulong pertama kali mempersiapkannya pada tahun 1812, dan kehilangan dua jari dan dua ledakan.[6] Pada tahun 1813, suatu ledakan NCl3 membutakan Sir Humphry Davy sementara, mendorongnya untuk mempekerjakan Michael Faraday sebagai rekan kerja. Mereka berdua terluka dalam ledakan NCl3 lainnya tak lama setelah itu.[7]
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ Holleman, A. F.; Wiberg, E. (2001). Inorganic Chemistry. San Diego: Academic Press. ISBN 0-12-352651-5.
- ^ Shaw, CA; Bains, JS (1998). "Did consumption of flour bleached by the agene process contribute to the incidence of neurological disease?". Medical Hypotheses. 51 (6): 477–81. doi:10.1016/S0306-9877(98)90067-6. PMID 10052866.
- ^ Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
- ^ White, G. C. (1999). The Handbook of Chlorination and Alternative Disinfectants (edisi ke-4th). Wiley. hlm. 322. ISBN 978-0-471-29207-4.
- ^ "Health Hazard Evaluation Report: Investigation of Employee Symptoms at an Indoor Water Park" (pdf). NIOSH eNews. National Institute for Occupational Safety and Health. 6 (4). August 2008. HETA 2007-0163-3062.
- ^ Thénard J. L.; Berthollet C. L. (1813). "Report on the work of Pierre Louis Dulong". Annales de Chimie et de Physique. 86 (6): 37–43.
- ^ Thomas, J.M. (1991). Michael Faraday and The Royal Institution: The Genius of Man and Place (PBK). CRC Press. hlm. 17. ISBN 978-0-7503-0145-9.
Bacaan lebih lanjut[sunting | sunting sumber]
- Jander, J. (1976). "Recent Chemistry and Structure Investigation of Nitrogen Triiodide, Tribromide, Trichloride, and Related Compounds". Advances in Inorganic Chemistry. 19: 1–63. doi:10.1016/S0065-2792(08)60070-9.
- Kovacic, P.; Lowery, M. K.; Field, K. W. (1970). "Chemistry of N-Bromamines and N-Chloramines". Chemical Reviews. 70 (6): 639–665. doi:10.1021/cr60268a002.
- Hartl, H.; Schöner, J.; Jander, J.; Schulz, H. (1975). "Die Struktur des Festen Stickstofftrichlorids (−125 °C)". Zeitschrift für Anorganische und Allgemeine Chemie. 413 (1): 61–71. doi:10.1002/zaac.19754130108.
- Cazzoli, G.; Favero, P. G.; Dal Borgo, A. (1974). "Molecular Structure, Nuclear Quadrupole Coupling Constant and Dipole Moment of Nitrogen Trichloride from Microwave Spectroscopy". Journal of Molecular Spectroscopy. 50 (1–3): 82–89. doi:10.1016/0022-2852(74)90219-7.
- Bayersdorfer, L.; Engelhardt, U.; Fischer, J.; Höhne, K.; Jander, J. (1969). "Untersuchungen an Stickstoff–Chlor-Verbindungen. V. Infrarot- und RAMAN-Spektren von Stickstofftrichlorid". Zeitschrift für Anorganische und Allgemeine Chemie. 366 (3–4): 169–179. doi:10.1002/zaac.19693660308.
Pranala luar[sunting | sunting sumber]
- OSHA - Nitrogen triklorida Diarsipkan 2008-09-05 di Wayback Machine.
- Nitrogen Triklorida - Health References Diarsipkan 2013-06-19 di Wayback Machine.