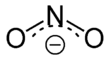
Nitrit

| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC (sistematis)
dioxidonitrate(1−) | |||
| Nama lain
nitrite
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
| |||
| |||
| Sifat | |||
| NO−2 | |||
| Massa molar | 46,01 g·mol−1 | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Ion nitrit, yang memiliki rumus kimia NO2−, adalah anion simetris dengan ikatan N-O sama panjang dan sudut ikatan O-N-O dari sekitar 120°.[butuh rujukan] Setelah protonasi, asam lemah yang tidak stabil asam nitrit diproduksi. Nitrit dapat teroksidasi atau tereduksi, dengan produk agak tergantung pada oksidator/reduktor dan kekuatannya. Ion nitrit adalah ligan ambidentat, dan dikenal untuk berikatan ke pusat-pusat logam dalam setidaknya lima cara yang berbeda.[1] Nitrit juga penting dalam biokimia sebagai sumber ampuh vasodilator nitrat oksida. Dalam kimia organik kelompok NO2 hadir dalam ester asam nitrit dan senyawa nitro. Nitrit juga digunakan dalam industri produksi pangan untuk menyembuhkan daging.
Referensi[sunting | sunting sumber]
- ^ Greenwood, pp 461–464
Bibliografi[sunting | sunting sumber]
- Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, ISBN 0-7506-3365-4
Pranala luar[sunting | sunting sumber]
Wikimedia Commons memiliki media mengenai Nitrites.