Karbonil

Dalam kimia organik, gugus karbonil adalah sebuah gugus fungsi yang terdiri dari sebuah atom karbon yang berikatan rangkap dengan sebuah atom oksigen: C=O.
Istilah karbonil juga dapat merujuk pada karbon monoksida sebagai sebuah ligan pada senyawa anorganik atau kompleks organologam (misalnya nikel karbonil); dalam situasi ini, karbon berikatan rangkap tiga dengan oksigen C≡O.
Senyawa karbonil
[sunting | sunting sumber]Sebuah gugus karbonil dikarakterisasikan oleh jenis-jenis senyawa berikut ini:
| Senyawa | Aldehida | Keton | Asam karboksilat | Ester | Amida | Enon | Asil klorida | Anhidrida asam |
| Struktur | 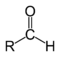 |
 |
 |
 |
 |

| ||
| Rumus umum | RCHO | RCOR' | RCOOH | RCOOR' | RCONR'R'' | RC(O)C(R')CR''R''' | RCOCl | (RCO)2O |
Senyawa karbonil lainnya termasuk urea dan karbamat. Contoh dari senyawa karbonil anorganik adalah karbon dioksida, karbon sulfida, dan fosgena.
Reaktivitas
[sunting | sunting sumber]Oksigen lebih elektronegatif daripada karbon, sehingga rapatan elektron akan tertarik dari karbon dan meningkatkan polaritas ikatan. Oleh karena itu, karbon karbonil bersifat elektrofilik, sehingga lebih reaktif terhadap nukleofil. Selain itu, oksigen yang elektronegatif juga dapat bereaksi dengan elektrofil.
Hidrogen alfa pada senyawa karbonil lebih asam (~1030 kali lebih asama) daripada ikatan CH yang biasa. Sebagai contoh, nilai pKa asetaldehida dan aseton adalah 16,7 dan 19, berturut-turut.[1]
Amida adalah penggandengan (coupling) karbonil yang paling stabil oleh karena stabilisasi resonansinya yang tinggi di antara ikatan Nitrogen-Karbon dengan Karbon-Oksigen.
Gugus karbonil dapat direduksi oleh reagen hidrida seperti NaBH4 dan LiAlH4, dan oleh reagen organologam seperti organolitium dan reagen Grignard.
Reaksi-reaksi penting lainnya meliputi:
- Reduksi Wolff-Kishner
- Reduksi Clemmensen
- Konversi menjadi tioasetal
- Hidrasi menjadi hemiasetal dan hemiketal, kemudian menjadi asetal dan ketal
- Reaksi dengan ammonia dan amina primer membentuk imina
- Reaksi dengan hidroksilamina membentuk oksim
- Reaksi dengan anion sianida membentuk sianohidrin
- Oksidasi dengan oksaziridina menjadi asiloin
- Reaksi dengan reagen Tebbe dan fosfonium ilida menjadi alkena
- Reaksi Perkin
- Reaksi Tishchenko
- Kondensasi Aldol
- Reaksi Cannizzaro
Senyawa karbonil α,β-takjenuh
[sunting | sunting sumber]Senyawa karbonil α,β-takjenuh adalah sebuah kelompok senyawa karbonil yang penting dengan struktur umumnya Cβ=Cα−C=O. Pada senyawa-senyawa ini, gugus karbonil berkonjugasi dengan sebuah alkena. Hal ini menyebabkan sifat-sifat khusus senyawa ini. Sebagai contoh senyawa ini adalah akrolein, mesitil oksida, asam akrilat, dan asam maleat. Karbonil takjenuh dapat dibuat dalam laboratorium menggunakan reaksi aldol dan reaksi Perkin.
Gugus karbonil, baik pada aldehida, asam, ataupun keton, menarik elektron dari alkena dan gugus alkena pada karbonil takjenuh, sehingga menurunkan reaktivitas terhadap elektrofil seperti bromin atau asam klorida. Sebagai kaidah umum, hidrogen melekatkan dirinya pada posisi alfa pada sebuah adisi elektrofilik. Sebaliknya, senyawa ini reaktif terhadap nukleofil pada adisi nukleofil.
Spektroskopi
[sunting | sunting sumber]- Spektroskopi inframerah: ikatan rangkap C=O menyerap sinar inframerah pada bilangan gelombang kira-kira 1600–1900 cm−1. Lokasi persis penyerapan bergantung pada geometri molekul. Penyerapan ini dikenal sebagai "regangan karbonil".[2]
- Resonansi magentik nuklir: ikatan rangkap C=O menunjukkan resonansi yang berbeda-beda tergantung pada atom-atom tetangga, umumnya berada pada pegeseran medan bawah (downfield shift). NMR 13C karbon karbonil berada pada kisaran 160-220 ppm.
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ Ouellette, R.J. and Rawn, J.D. “Organic Chemistry” 1st Ed. Prentice-Hall, Inc., 1996: New Jersey. ISBN 0-02-390171-3.
- ^ Mayo D.W., Miller F.A and Hannah R.W “Course Notes On The Interpretation of Infrared and Raman Spectra” 1st Ed. John Wiley & Sons Inc, 2004: New Jersey. ISBN 0-471-24823-1.
Pustaka tambahan
[sunting | sunting sumber]- L.G. Wade, Jr. Organic Chemistry, 5th ed. Prentice Hall, 2002. ISBN 0-13-033832-X
- The Frostburg State University Chemistry Department. Organic Chemistry Help (2000).
- Advanced Chemistry Development, Inc. IUPAC Nomenclature of Organic Chemistry (1997).
- William Reusch. VirtualText of Organic Chemistry (2004).
- Purdue Chemistry Department [1] (retrieved Sep 2006). Includes water solubility data.
- William Reusch. (2004) Aldehydes and Ketones Diarsipkan 2010-04-30 di Wayback Machine. Retrieved 23 May 2005.
- ILPI. (2005) The MSDS Hyperglossary- Anhydride.
