Raksa(II) asetat

| |

| |
| |
| Nama | |
|---|---|
| Nama lain
merkuri asetat
merkuriasetat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C4H6O4Hg | |
| Massa molar | 318.678 g/mol |
| Penampilan | kristal putih-kuning |
| Bau | bau cuka lembut |
| Densitas | 3.28 g/cm3, padat |
| Titik lebur | 179 °C (354 °F; 452 K) (terurai) |
| 25 g/100 mL (10 °C) 100 g/100 mL (100 °C) | |
| Kelarutan | larut dalam alkohol, dietil eter |
| −100·10−6 cm3/mol | |
| Bahaya | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
40.9 mg/kg (tikus, oral) 23.9 mg/kg (tikus, oral)[1] |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
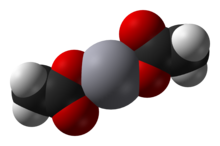
Raksa(II) asetat adalah suatu senyawa kimia dengan rumus kimia Hg(O2CCH3)2. Umumnya disingkat sebagai Hg(OAc)2, senyawa ini digunakan sebagai pereaksi untuk menghasilkan senyawa organomerkuri dari prekursor organik tak jenuh.
Struktur
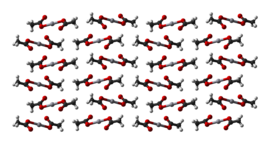
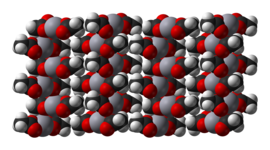
[sunting | sunting sumber]Raksa(II) asetat adalah suatu padatan kristalin yang terdiri dari molekul Hg(OAc)2 terisolasi dengan jarak Hg-O sebesar 2.07 Å. Terdapat pula tiga ikatan intermolekular Hg···O yang panjang, lemah dengan jarak 2.75 Å, menghasilkan geometri koordinasi persegi piramidal yang agak terdistorsi pada Hg.[2]
Reaksi
[sunting | sunting sumber]Arena mengalami "merkurasi" apabila diberi perlakuan dengan Hg(OAc)2. Satu gugus asetat yang tetap terikat dengan raksa dapat digantikan dengan klorida:[3]
- C6H5OH + Hg(OAc)2 → C6H4(OH)-2-HgOAc + HOAc
- C6H4(OH)-2-HgOAc + NaCl → C6H4(OH)-2-HgCl + NaOAc
Pusat Hg2+ terikat dengan alkena, menginduksi adisi hidroksida dan alkoksida. Sebagai contoh, perlakuan metilakrilat dengan raksa asetat dalam metanol menghasilkan suatu ester α-raksa:[4]
- Hg(OAc)2 + CH2=CHCO2CH3 + CH3OH → CH3OCH2CH(HgOAc)CO2CH3 + HOAc
Raksa(II) memiliki afinitas yang tinggi bagi ligan sulfur. Hg(OAc)2 dapat digunakan sebagai pereaksi untuk menghilangkan gugus pelindung asetamidometil, yang digunakan untuk "melindungi" gugus tiol dalam sintesis organik. Serupa dengan itu, Hg(OAc)2 merupakan pereaksi standar untuk mengubah ester tiokarbonat menjadi ditiokarbonat:
- (RS)2C=S + H2O + Hg(OAc)2 → (RS)2C=O + HgS + 2 HOAc
Raksa(II) asetat digunakan untuk reaksi oksimerkurasi.
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ "Senyawa alkil (organo) raksa (sebagai Hg)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ Allmann, R. (1973). "Die Struktur des Quecksilber(II)-acetats". Z. Kristallogr. 138 (1–6): 366–373. doi:10.1524/zkri.1973.138.jg.366.
- ^ Whitmore, F. C.; Hanson, E. R. "o-Chloromercuriphenol" Organic Syntheses, Collected Volume 1, p.161 (1941).http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=CV1P0161
- ^ Carter, H. E.; West, H. D. “dl-Serine” Organic Syntheses, Collected Volume 3, p.774 (1955). http://www.orgsyn.org/orgsyn/orgsyn/prepContent.asp?prep=CV3P0774
Pranala luar
[sunting | sunting sumber]- Allmann, R. (1973). "Die Struktur des Quecksilber(II)-acetats". Z. Kristallogr. 138 (1–6): 366–373. doi:10.1524/zkri.1973.138.jg.366.
- Cooney, R.P.J.; Hall, J.R. (1972). "Vibrational spectra of mercury(I) and mercury(II) acetate compounds". Journal of Inorganic and Nuclear Chemistry. 34 (5): 1519–1527. doi:10.1016/0022-1902(72)80271-9.
