Raksa(I) klorida

| |
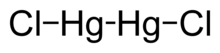
| |

| |
| Nama | |
|---|---|
| Nama IUPAC
Diraksa diklorida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 3077 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| Hg2Cl2 | |
| Massa molar | 472.09 g/mol |
| Penampilan | Putih padat |
| Densitas | 7.150 g/cm3 |
| Titik lebur | 525 °C (977 °F; 798 K) |
| Titik didih | 383 °C (721 °F; 656 K) (menyublim) |
| 0.2 mg/100 mL | |
| Kelarutan | Tidak dapat larut dalam etanol, eter |
| −26.0·10−6 cm3/mol | |
| Indeks bias (nD) | 1.973 |
| Bahaya | |
| Lembar data keselamatan | ICSC 0984 |
Klasifikasi UE (DSD) (usang)
|
Beracun (T) Berbahaya (Xn) Berbahaya untuk lingkungan (N) |
| Frasa-R | R22, R36/37/38, R50/53 |
| Frasa-S | S2, S13, S24/25, S46, S60, S61 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
210 mg/kg (tikus, lewat mulut)[1] |
| Termokimia | |
| Entropi molar standar (S |
196 J·mol−1·K−1[2] |
| Entalpi pembentukan standar (ΔfH |
−265 kJ·mol−1[2] |
| Senyawa terkait | |
Anion lain
|
Raksa(I) fluorida Raksa(I) bromida Raksa(I) iodida |
Kation lainnya
|
Raksa(II) klorida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Raksa(I) klorida adalah senyawa kimia dengan rumus Hg2Cl2. Senyawa ini berwarna putih atau putih kekuningan dan tidak berbau. Raksa(I) klorida merupakan komponen elektrode acuan dalam bidang elektrokimia.[3][4]
Senyawa ini juga dikenal dengan nama mineral kalomel.[5]
Pembuatan dan reaksi[sunting | sunting sumber]
Raksa(I) klorida terbentuk dari reaksi raksa dengan raksa klorida:
- Hg + HgCl2 → Hg2Cl2
Raksa ini dapat dibuat dari reaksi metatesis antara raksa(I) nitrat cair dengan senyawa yang mengandung klorida, termasuk NaCl atau HCl.
- 2HCl + Hg2(NO3)2 → Hg2Cl2 + 2HNO3
Amonia akan memicu reaksi disproporsionasi pada Hg2Cl2:
- Hg2Cl2 + 2NH3 → Hg + Hg(NH2)Cl + NH4Cl
Catatan kaki[sunting | sunting sumber]
- ^ "Mercury compounds [except (organo) alkyls] (as Hg)". Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. hlm. A22. ISBN 0-618-94690-X.
- ^ Housecroft, C. E.; Sharpe, A. G. (2004). Inorganic Chemistry (edisi ke-2nd). Prentice Hall. hlm. 696–697. ISBN 978-0130399137.
- ^ Skoog, Douglas A.; Holler, F. James; Nieman, Timothy A. (1998). Principles of Instrumental Analysis (edisi ke-5th). Saunders College Pub. hlm. 253–271. ISBN 0-03-002078-6.
- ^
 Chisholm, Hugh, ed. (1911). "Calomel". Encyclopædia Britannica (edisi ke-11). Cambridge University Press.
Chisholm, Hugh, ed. (1911). "Calomel". Encyclopædia Britannica (edisi ke-11). Cambridge University Press.
Pranala luar[sunting | sunting sumber]
Wikimedia Commons memiliki media mengenai Mercury(I) chloride.
