Alkoksida
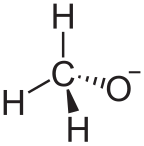
Alkoksida adalah sebuah basa konjugat dari suatu alkohol sehingga mengandung gugus organik yang terikat pada atom oksigen yang bermuatan negatif. Alkoksida ditulis sebagai RO−, dengan R adalah substituen organik. Alkoksida adalah basa kuat dan, jika R tidak besar, merupakan nukleofil yang baik serta ligan yang bagus. Meskipun umumnya tidak stabil dalam pelarut protik seperti air, alkoksida terjadi sebagai banyak intermediat berbagai reaksi, termasuk sintesis eter Williamson.[1][2] Alkoksida logam transisi banyak digunakan sebagai pelapis dan katalis.[3][4]
Enolat adalah alkoksida tak jenuh yang diturunkan melalui deprotonasi ikatan C-H yang bertentangga dengan gugus keton atau aldehida. Pusat nukleofilik pada alkoksida sederhana terletak pada atom oksigen, sementara situs nukleofilik pada enolat terdelokalisasi pada karbon dan oksigen.
Fenoksida memiliki hubungan yang sangat dekat dengan alkoksida, di mana gugus alkil digantikan oleh turunan benzena. Fenol lebih asam daripada alkohol, sehingga, fenoksida terkaitnya bersifat kurang basa dan kurang nukleofilik daripada alkoksida. Oleh sebab itu, fenoksida lebih mudah ditangani, dan menghasilkan kristal yang lebih banyak daripada alkoksida.
Struktur[sunting | sunting sumber]
Alkoksida logam alkali sering kali berupa senyawa oligomer atau polimer, terutama jika gugus R-nya kecil (Me, Et).[3] Anion alkoksida adalah jembatan ligan yang baik, sehingga banyak alkoksida dapat membentuk ikatan M2O atau M3O. Dalam larutan, alkoksida logam alkali menunjukkan sifat pasangan ion yang kuat, sesuai perkiraan bahwa derivat logam alkali adalah anion basa kuat.

Pembuatan[sunting | sunting sumber]
Dari logam reduktor[sunting | sunting sumber]
Alkoksida dapat diproduksi melalui beberapa cara, dengan bahan dasar alkohol. Logam reduktor kuat bereaksi langsung dengan alkohol menghasilkan alkoksida logam yang sesuai. Alkohol bertindak sebagai asam, dan hidrogen dihasilkan sebagai produks sampingan. Contoh klasik adalah natrium metoksida yang dibuat dari adisi logam natrium dengan metanol:
- 2 CH3OH + 2 Na → 2 CH3ONa + H2
Logam alkali lainnya dapat digunakan menggantikan natrium, dan sebagian besar alkohol dapat digunakan untuk menggantikan metanol. Reaksi serupa lainnya terjadi ketika alkohol bereaksi dengan hidrida logam seperti NaH. Logam hidrida menggantikan atom hidrogen dari gugus hidroksil dan membentuk ion alkoksida yang bermuatan negatif.
Dari klorida elektrofil[sunting | sunting sumber]
Titanium tetraklorida bereaksi dengan alkohol menghasilkan tetraalkoksida yang sesuai, bersamaan dengan evolusi hidrogen klorida.
- TiCl4 + 4 (CH3)2CHOH → Ti(OCH(CH3)2)4 + 4 HCl
Reaksi dapat dipercepat dengan penambahan basa, seperti amina tersier. Banyak logam dan golongan halida lain yang dapat digunakan selain titanium, misalnya SiCl4, ZrCl4, dan PCl3.
Melalui reaksi metatesis[sunting | sunting sumber]
Banyak alkoksida dibuat melalui reaksi pembentukan garam dari klorida logam dan natrium alkoksida:
- n NaOR + MCln → M(OR)n + n NaCl
Reaksi di atas dilancarkan oleh energi kisi NaCl, dan pemurnian produk alkoksidanya menjadi lebih sederhana karena NaCl tidak larut dalam kebanyakan pelarut organik.

Melalui proses elektrokimia[sunting | sunting sumber]
Banyak alkoksida dapat dibuat melalui pelarutan anodik logam terkaitnya dalam alkohol anhidrat, disertai keberadaan aditif elektrokonduktif. Logam yang bisa digunakan antara lain Co, Ga, Ge, Hf, Fe, Ni, Nb, Mo, La, Re, Sc, Si, Ti, Ta, W, Y, Zr, dll. Aditif konduktor antara lain litium klorida, halida amonium kuarterner, atau lainnya. Beberapa contoh alkoksida logam yang diperoleh melalui teknik ini: Ti(OCH(CH3)2)4, Nb2(OCH3)10, Ta2(OCH3)10, [MoO(OCH3)4]2, Re2O3(OCH3)6, Re4O6(OCH3)12, and Re4O6(OCH(CH3)2)10.
Sifat-sifat[sunting | sunting sumber]
Reaksi dengan alkil halida[sunting | sunting sumber]
Ion alkoksida dapat bereaksi dengan alkil halida primer dalam reaksi SN2 membentuk metil eter.
Hidrolisis dan transesterifikasi[sunting | sunting sumber]
Alkoksida logam terhidrolisis dalam air sesuai persamaan berikut:[6]
- 2 LnMOR + H2O → [LnM]2O + 2 ROH
dengan R adalah substituen organik dan L adalah suatu ligan (sering kali berupa alkoksida). Sebuah studi menunjukkan hidrolisis tak dapat balik titanium etoksida sesuai persamaan berikut:
Dengan mengendalikan sifat stoikiometri dan sterik alkoksida, reaksi semacam ini dapat ditahan menghasilkan logam-oksi-alkoksida, yang biasanya merupakan komplek oligonuklir. Alkohol lain dapat digunakan menggantikan air. Dengan cara ini, suatu alkoksida dapat diubah menjadi alkoksida lain, dan prosesnya disebut sebagai alkoholisis (sayangnya, terdapat kebingungan terminologi dengan transesterifikasi, yang merupakan proses yang berbeda - lihat di bawah). Posisi kesetimbangan dapat dikendalikan dengan mengatur keasaman alkohol; misalnya fenol biasanya bereaksi dengan alkoksida dengan membebaskan alkohol, membentuk fenoksida. Secara sederhana, alkoholisis dapat dikendalikan dengan menguapkan secara selektif komponen yang lebih volatil. Dengan cara ini, etoksida dapat diubah menjadi butoksida, karena etanol (titik didih 78 °C) lebih volatil daripada butanol (titik didih 118 °C).
Pada proses transesterifikasi, alkoksida logam bereaksi dengan ester untuk menghasilkan pertukaran gugus alkil antara alkoksida logam dan ester. Fokus pada kompleks alkoksida logam, hasilnya sama seperti alkoholisis, dapat dikatakan sebagai penggantian ligan alkoksida, tetapi pada saat yang sama gugus alkil pada ester diganti pula, yang dapat pula disebut sebagai tujuan utama reaksi. Natirum metoksida, misalnya, yang umum digunakan untuk reaksi ini, suatu reaksi yang relevan dengan produksi "bio-disel".
Pembentukan okso-alkoksida[sunting | sunting sumber]
Banyak senyawa alkoksida logam juga memiliki ligan okso. Ligan okso biasanya muncul melalui hidrolisis, sering kali secara tidak sengaja, dan melalui eliminasi eter:
- 2 LnMOR → [LnM]2O + R2O
Selain itu, alkoksida logam valensi rendah rentan terhadap oksidasi di udara.
Pembentukan derivat polinuklir dan heterologam[sunting | sunting sumber]
Secara khas, alkoksida logam transisi adalah polinuklir, yang mengandung lebih dari satu logam. Alkoksida adalah ligan yang sterik dan sangat basa yang cenderung menjembatani logam.
Pada substitusi isomorfik atom logam, terbentuk berbagai komposisi kristal senyawa kompleks. Rasio logam dalam senyawa semacam ini dapat bervariasi dengan rentang yang sangat lebar. Misalnya, substitusi molibdenum dan wolfram untuk renium dalam kompleks Re4O6−y(OCH3)12+y memungkinkan untuk memperoleh kompleks Re4−xMoxO6−y(OCH3)12+y dalam rentang 0 ≤ x ≤ 2,82 dan Re4−xWxO6−y(OCH3)12+y dalam rentang 0 ≤ x ≤ 2.
Kestabilan termal[sunting | sunting sumber]
Banyak alkoksida logam mengalami dekomposisi termal pada rentang ~100–300 °C. Termolisis ini dapat terjadi pada fase logam atau oksida serbuk berukuran nano, tergantung pada kondisi prosesnya. Pendekatan ini merupakan dasar proses pabrikasi bahan-bahan fungsional untuk pesawat terbang, wahana angkasa luar, elektronika, dan industri kimia: oksida-oksida tunggal, larutan padatnya, oksida kompleks, serbuk logam dan paduan yang diaktifkan melalui sintering. Dekomposisi campuran derivat alkoksida mono- dan heterologam telah pula diteliti.
Contoh alkoksida[sunting | sunting sumber]

| nama | rumus molekul | keterangan |
|---|---|---|
| Titanium isopropoksida | Ti(OiPr)4 | monomer karena ruah sterik, digunakan dalam sintesis organik |
| Titanium etoksida | Ti4(OEt)16 | untuk pemrosesan sol-gel oksida Ti |
| Titanium etoksida | Zr4(OEt)16 | untuk pemrosesan sol-gel oksida Zr |
| Tetraetil ortosilikat | Si(OEt)4 | untuk pemrosesan sol-gel oksida Si; Si(OMe)4 dihindari karena alasan keselamatan |
| Aluminium isopropoksida | Al4(OiPr)12 | pereaksi untuk reduksi Meerwein–Ponndorf–Verley |
| Vanadil isopropoksida | VO(OiPr)3 | prekursor untuk katalis |
| Niobium etoksida | Nb2(OEt)10 | untuk pemrosesan sol-gel oksida Nb |
| Tantalum etoksida | Ta2(OEt)10 | untuk pemrosesan sol-gel oksida Ta |
| Kalium tert-butoksida, | K4(OtBu)4 | pereaksi basa untuk reaksi eliminasi organik |
Referensi[sunting | sunting sumber]
- ^ Williamson, Alexander (1850). "Theory of Ætherification" (PDF). Phil. Mag. 37 (251): 350–356. doi:10.1080/14786445008646627. (Link to excerpt.)
- ^ Boyd, Robert Neilson; Morrison, Robert Thornton (1992). Organic Chemistry (edisi ke-6th). Englewood Cliffs, N.J.: Prentice Hall. hlm. 241–242. ISBN 9780136436690.
- ^ a b Bradley, Don C.; Mehrotra, Ram C.; Rothwell, Ian P.; Singh, A. (2001). Alkoxo and Aryloxo Derivatives of Metals. San Diego: Academic Press. ISBN 978-0-08-048832-5.
- ^ Turova, Nataliya Y.; Turevskaya, Evgeniya P.; Kessler, Vadim G.; Yanovskaya, Maria I. (2002). The Chemistry of Metal Alkoxides. Dordrecht: Kluwer Academic Publishers. ISBN 9780792375210.
- ^ Unkelbach, Christian; O'Shea, Donal F.; Strohmann, Carsten (2014). "Insights into the Metalation of Benzene and Toluene by Schlosser's Base: A Superbasic Cluster Comprising PhK, PhLi, and tBuOLi". Angew. Chem. Int. Ed. 53 (2): 553–556. doi:10.1002/anie.201306884. PMID 24273149.
- ^ Hanaor, Dorian A. H.; Chironi, Ilkay; Karatchevtseva, Inna; Triani, Gerry; Sorrell, Charles C. (2012). "Single and Mixed Phase TiO2 Powders Prepared by Excess Hydrolysis of Titanium Alkoxide". Advances in Applied Ceramics. 111 (3): 149–158. arXiv:1410.8255
 . doi:10.1179/1743676111Y.0000000059.
. doi:10.1179/1743676111Y.0000000059.
- ^ Shcheglov, P. A.; Drobot, D. V. (2005). "Rhenium Alkoxides". Russian Chemical Bulletin. 54 (10): 2247–2258. doi:10.1007/s11172-006-0106-5.
Pranala luar[sunting | sunting sumber]
- Turova, Nataliya Y. (2004). "Metal oxoalkoxides. Synthesis, properties and structures". Russian Chemical Reviews. 73 (11): 1041–1064. Bibcode:2004RuCRv..73.1041T. doi:10.1070/RC2004v073n11ABEH000855.
