Manganat
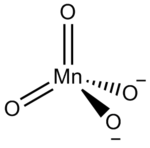
Dalam tata nama anorganik, suatu manganat adalah entitas molekul bermuatan negatif dengan mangan sebagai atom pusat.[1] Namun, nama ini biasanya digunakan untuk merujuk pada anion tetraoksidomanganat(2−), MnO2−4, dikenal pula sebagai manganat(VI) karena mengandung mangan dalam keadaan oksidasi +6.[1] Manganat adalah satu-satunya senyawa mangan(VI) yang diketahui.[2]
Manganat(VI)
[sunting | sunting sumber]
Ion manganat(VI) adalah tetrahedral, mirip dengan sulfat atau kromat: memang, manganat sering kali isostruktural dengan sulfat dan kromat, sebuah fakta yang pertama kali dicatat oleh Mitscherlich pada tahun 1831.[3] Jarak mangan–oksigen adalah 165.9 pm, sekitar 3 pm lebih panjang dari permanganat.[3] Sebagai suatu ion d1, ia bersifat paramagnetik, tetapi setiap distorsi Jahn–Teller terlalu kecil untuk dideteksi dengan kristalografi sinar-X.[3] Manganat berwarna hijau tua, dengan absorpsi tampak maksimum λmax = 606 nm (ε = 1710 dm3 mol−1 cm−1).[4][5] Spektrum Raman juga telah dilaporkan.[6]
Persiapan
[sunting | sunting sumber]Natrium dan kalium manganat biasanya disiapkan di laboratorium dengan mengaduk permanganat yang ekivalen dalam suatu larutan pekat (5–10 M) dari hidroksida selama 24 jam[4] atau dengan pemanasan.[7]
- 4 MnO−4 + 4 OH− → 4 MnO2−4 + 2 H2O + O2
Kalium manganat dibuat secara industri, sebagai perantara antara kalium permanganat, dengan melarutkan mangan dioksida dalam kalium hidroksida cair dengan kalium nitrat atau udara sebagai zat pengoksidasi .[2]
- 2 MnO2 + 4 OH− + O2 → 2 MnO2−4 + 2 H2O
Penggunaan
[sunting | sunting sumber]Manganat, terutama barium manganat, BaMnO4, yang tidak larut Telah digunakan sebagai zat pengoksidasi dalam sintesis organik: mereka akan mengoksidasi alkohol primer menjadi aldehida dan kemudian menjadi asam karboksilat, dan alkohol sekunder menjadi keton.[8][9] Barium manganat juga telah digunakan untuk mengoksidasi hidrazon menjadi senyawa diazonium.[10]
Disproporsionasi
[sunting | sunting sumber]Manganat tidak stabil terhadap disproporsionasi dalam semua tapi yang paling basa dari larutan berair.[2] Produk utama adalah permanganat dan mangan dioksida, tetapi kinetika kompleks dan mekanismenya melibatkan spesies terprotonasi dan/atau mangan(V).[11][12]
Asam manganat
[sunting | sunting sumber]Asam manganat tidak bisa terbentuk karena disproportionasinya yang cepat. Namun, konstanta disosiasi asam keduanya disimulasikan dengan teknik radiolisis pulsa:[13]
- HMnO−4
 MnO2−4 + H+ pKa = 7.4 ± 0.1
MnO2−4 + H+ pKa = 7.4 ± 0.1
Manganat(V), manganat(IV), dan "manganat(III)"
[sunting | sunting sumber]Anion manganat(V), MnO3−4, dikenal secara trivial sebagai hipomanganat dan secara sistematis sebagai tetraoksidomanganat(3−), adalah suatu spesi biru terang[14] dengan absorpsi tampak maksimum λmax = 670 nm (ε = 900 dm3 mol−1 cm−1).[4][5] Senyawa ini tidak stabil terhadap disproporsionasi ke manganat(VI) dan mangan dioksida, walaupun reaksinya sangat lambat dalam larutan basa (c(OH−) = 5–10 mol dm−3).[14]
Hipomanganat dapat dibuat dengan reduksi hati-hati manganat dengan sulfit,[14] hidrogen peroksida[15] atau mandelat.[5] Hanya kalium hipomanganat yang telah dipelajari sampai batas tertentu. Asam hipomanganat tidak dapat terbentuk karena disproporsionasinya yang cepat, namun konstanta disosiasi asam ketiga telah diperkirakan dengan teknik radiolisis pulsa:[13]
- HMnO2−4
 MnO3−4 + H+ pKa = 13.7 ± 0.2
MnO3−4 + H+ pKa = 13.7 ± 0.2
Ester siklik asam hipomanganat dianggap zat antara dalam oksidasi alkena oleh permanganat.[5]
Anion manganat (IV) telah disiapkan dengan radiolisis larutan encer permanganat.[13][15] Senyawa ini adalah mononuklir dalam larutan encer, dan menunjukkan penyerapan yang kuat pada ultraviolet dan penyerapan yang lebih lemah pada 650 nm.[13]
Most so-called "manganit" tidak mengandung oksoanion diskrit, namun merupakan oksida campuran dengan struktur perovskit (LaMnIIIO3, CaMnIVO3), spinel (LiMnIII,IV2O4) atau natrium klorida (LiMnIIIO2, NaMnIIIO2). Satu pengecualian adalah kalium dimanganat(III), K6Mn2O6, yang mengandung anion diskrit Mn2O6−6.[16]
Referensi
[sunting | sunting sumber]- ^ a b International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 74–75, 77–78, 313, 338. Electronic version..
- ^ a b c Cotton, F. Albert; Wilkinson, Geoffrey; Murillo, Carlos A.; Bochmann, Manfred (1999), Advanced Inorganic Chemistry (edisi ke-6th), New York: Wiley-Interscience, hlm. 746, ISBN 0-471-19957-5.
- ^ a b c Palenik, Gus J. (1967), "Crystal structure of potassium manganate", Inorg. Chem., 6 (3): 507–11, doi:10.1021/ic50049a016.
- ^ a b c Carrington, A.; Symons, M. C. R. (1956), "Structure and reactivity of the oxy-anions of transition metals. Part I. The manganese oxy-anions", J. Chem. Soc.: 3373–80, doi:10.1039/JR9560003373.
- ^ a b c d Lee, Donald G.; Chen, Tao (1993), "Reduction of manganate(VI) by mandelic acid and its significance for development of a general mechanism of oxidation of organic compounds by high-valent transition metal oxides", J. Am. Chem. Soc., 115 (24): 11231–36, doi:10.1021/ja00077a023.
- ^ Juberta, A. H.; Varettia, E. L. (1982), "Normal and resonance Raman spectra of some manganates", J. Mol. Struct., 79: 285–88, Bibcode:1982JMoSt..79..285J, doi:10.1016/0022-2860(82)85067-9.
- ^ Nyholm, R. S.; Woolliams, P. R. (1986), "Manganates(VI)", Inorg. Synth., 11: 56–61.
- ^ Procter, G.; Ley, S. V.; Castle, G. H. (2004), "Barium Manganate", dalam Paquette, L., Encyclopedia of Reagents for Organic Synthesis, New York: Wiley, doi:10.1002/047084289.
- ^ Firouzabadi, Habib; Mostafavipoor, Zohreh (1983), "Barium Manganate. A Versatile Oxidant in Organic Synthesis", Bull. Chem. Soc. Jpn., 56 (3): 914–17, doi:10.1246/bcsj.56.914.
- ^ Guziec, Frank S., Jr.; Murphy, Christopher J.; Cullen, Edward R. (1985), "Thermal and photochemical studies of symmetrical and unsymmetrical dihydro-1,3,4-selenadiazoles", J. Chem. Soc., Perkin Trans. 1: 107–13, doi:10.1039/P19850000107.
- ^ Sutter, Joan H.; Colquitt, Kevin; Sutter, John R. (1974), "Kinetics of the disproportionation of manganate in acid solution", Inorg. Chem., 13 (6): 1444–46, doi:10.1021/ic50136a037.
- ^ Sekula-Brzezińska, K.; Wrona, P. K.; Galus, Z. (1979), "Rate of the MnO4−/MnO42− and MnO42−/MnO43− electrode reactions in alkaline solutions at solid electrodes", Electrochim. Acta, 24 (5): 555–63, doi:10.1016/0013-4686(79)85032-X.
- ^ a b c d Rush, J. D.; Bielski, B. H. J. (1995), "Studies of Manganate(V), -(VI), and -(VII) Tetraoxyanions by Pulse Radiolysis. Optical Spectra of Protonated Forms", Inorg. Chem., 34 (23): 5832–38, doi:10.1021/ic00127a022.
- ^ a b c Greenwood, Norman N.; Earnshaw, Alan (1984). Chemistry of the Elements. Oxford: Pergamon Press. hlm. 1221–22. ISBN 0-08-022057-6..
- ^ a b Lee, Donald G.; Chen, Tao (1989), "Oxidation of hydrocarbons. 18. Mechanism of the reaction between permanganate and carbon-carbon double bonds", J. Am. Chem. Soc., 111 (19): 7534–38, doi:10.1021/ja00201a039.
- ^ Brachtel, G.; Hoppe, R. (1976), "Das erste Oxomanganat(III) mit Inselstruktur: K6[Mn2O6]", Naturwissenschaften, 63 (7): 339, Bibcode:1976NW.....63..339B, doi:10.1007/BF00597313.
