Kalium sitrat
| |
| Nama | |
|---|---|
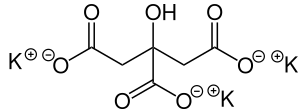
| Nama IUPAC (preferensi)
Trikalium 2-hidroksipropana-1,2,3-trikarboksilat | |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| K3C6H5O7 | |
| Massa molar | 306.395 g/mol |
| Penampilan | Bubuk putih higroskopik |
| Bau | Tak berbau |
| Densitas | 1.98 g/cm3 |
| Titik lebur | 180 °C (356 °F; 453 K)[1] |
| Titik didih | 230 °C (446 °F; 503 K)[1] |
| Larut | |
| Kelarutan | Larut dalan gliserin, Tidak larut dalam etanol 95% |
| Keasaman (pKa) | 8.5 |
| Farmakologi | |
| Kode ATC | A12 |
| Bahaya | |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
170 mg/kg (IV, anjing) 5400mg/kg (oral, tikus) |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Kalium sitrat (juga dikenal sebagai trikalium sitrat) adalah garam kalium dari asam sitrat dengan rumus molekul K3C6H5O7. Senyawa ini adalah bubuk kristal putih higroskopis. Tidak berbau dengan rasa asin. Senyawa ini mengandung 38,28% kalium berdasarkan massa. Dalam bentuk monohidrat, ia sangat higroskopis dan lezat.
Sebagai bahan tambahan pangan, kalium sitrat digunakan untuk mengatur keasaman, dan dikenal sebagai nomor E E332. Secara medis, dapat digunakan untuk mengendalikan batu ginjal yang berasal dari asam urat atau sistin.
Pada tahun 2020, obat ini merupakan obat ke-297 yang paling sering diresepkan di Amerika Serikat, dengan lebih dari 1 juta resep.[2][3]
Sintesis
[sunting | sunting sumber]Kalium sitrat dapat disintesis dengan netralisasi asam sitrat yang dicapai dengan penambahan kalium bikarbonat, kalium karbonat, atau kalium hidroksida ke dalamnya. Larutannya kemudian dapat disaring dan pelarut dapat diuapkan sampai granulasi.
Kegunaan
[sunting | sunting sumber]Kalium sitrat cepat diserap ketika diberikan melalui mulut, dan dikeluarkan melalui urin.[4] Karena merupakan garam basa, garam ini efektif dalam mengurangi rasa sakit dan frekuensi buang air kecil jika hal ini disebabkan oleh urin yang sangat asam.[5] Hal ini digunakan untuk tujuan ini pada anjing dan kucing, tetapi terutama digunakan sebagai diuretik yang tidak menyebabkan iritasi.
Memberi kalium sitrat adalah cara yang efektif untuk mengobati/menangani aritmia,[butuh rujukan] jika pasien mengalami hipokalemia.
Senyawa ini banyak digunakan untuk mengobati batu saluran kemih (batu ginjal), dan sering digunakan oleh pasien dengan sistinuria.[butuh rujukan] Sebuah tinjauan sistematis menunjukkan penurunan yang signifikan dalam kejadian pembentukan batu RR 0,26, 95% CI 0,10 hingga 0,68.[6]
Senyawa ini juga digunakan sebagai agen alkali dalam pengobatan infeksi saluran kemih ringan seperti sistitis.[7]
Senyawa ini juga digunakan dalam banyak minuman ringan sebagai larutan dapar.[8]
Sering digunakan dalam larutan berair dengan garam kalium lainnya, senyawa ini adalah pemadam api yang sangat berguna untuk mengatasi kebakaran dapur.[9] PH basa mendorong saponifikasi untuk melindungi bahan bakar dari oksidasi udara, dan reaksi dehidrasi endotermik menyerap energi panas untuk mengurangi suhu.[10][11]
Pemberian
[sunting | sunting sumber]Cairan kalium sitrat biasanya diberikan melalui mulut dalam larutan encer, karena efeknya yang agak pedas pada lapisan lambung, dan potensi bahaya kesehatan ringan lainnya. Tablet pil juga tersedia dalam formulasi normal dan pelepasan diperpanjang.
Referensi
[sunting | sunting sumber]- ^ a b "Potassium Citrate". hazard.com. Diarsipkan dari versi asli tanggal 2017-08-15.
- ^ "The Top 300 of 2020". ClinCalc. Diakses tanggal 7 October 2022.
- ^ "Potassium Citrate - Drug Usage Statistics". ClinCalc. Diakses tanggal 7 October 2022.
- ^ Medscape on hypocitraturia
- ^ Potassium Citrate for Kidney Stones
- ^ Phillips, Rebecca; Hanchanale, Vishwanath S; Myatt, Andy; Somani, Bhaskar; Nabi, Ghulam; Biyani, C Shekhar (6 October 2015). "Citrate salts for preventing and treating calcium containing kidney stones in adults". Cochrane Database of Systematic Reviews. 2015 (10): CD010057. doi:10.1002/14651858.CD010057.pub2. PMC 9578669
 Periksa nilai
Periksa nilai |pmc=(bantuan). PMID 26439475. - ^ "Potassium citrate for cystitis". patient.info.
- ^ "Soft Drinks with Potassium Citrate".
- ^ Fire, Impact. "What is a Class K Fire Extinguisher Used For?". resources.impactfireservices.com (dalam bahasa Inggris). Diakses tanggal 2022-08-18.
- ^ US Fire extinguishing composition and method for fire extinguishing 5945025A, James A. Cunningham
- ^ Xiaofang Wangy et al 2019 IOP Conf. Ser.: Mater. Sci. Eng. 490 022047
Pranala Luar
[sunting | sunting sumber]- Tanner, G.A. "Potassium citrate improves renal function in rats with polycystic kidney disease". Journal of the American Society of Nephrology. Retrieved December 17, 2016.
