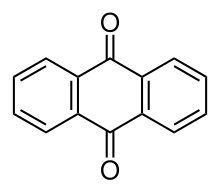
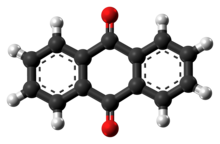
Antrakuinon
| |
| |

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Antrasena-9,10-dion[2] | |
Nama lain
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| Referensi Beilstein | 390030 |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| Nomor EC | |
| Referensi Gmelin | 102870 |
| KEGG | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
| Nomor UN | 3143 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| C14H8O2 | |
| Massa molar | 208,22 g·mol−1 |
| Penampilan | Padatan kuning |
| Densitas | 1,438 g/cm3[1] |
| Titik lebur | 284,8 °C (544,6 °F; 558,0 K)[1] |
| Titik didih | 377 °C (711 °F; 650 K)[1] |
| Tak larut | |
| Bahaya | |
| Bahaya utama | Kemungkinan karsinogen |
| Piktogram GHS | 
|
| Keterangan bahaya GHS | {{{value}}} |
| H350 | |
| P201, P202, P281, P308+313, P405, P501 | |
| Titik nyala | 185 °C (365 °F; 458 K) |
| Senyawa terkait | |
Senyawa terkait
|
kuinon, antrasena |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Antrakuinon, juga disebut antrasenadion atau dioksoantrasena, adalah sebuah senyawa organik aromatik dengan rumus C14H8O2. Isomernya meliputi berbagai turunan kuinon. Namun, istilah antrakuinon mengacu pada isomer 9,10-antrakuinon (IUPAC: 9,10-dioksoantrasena) di mana gugus keto terletak di cincin pusat. Senyawa ini adalah bahan penyusun dari banyak bahan pewarna dan digunakan dalam pemutihan pulp untuk pembuatan kertas. Ia adalah padatan berwarna kuning, sangat kristalin, sulit larut dalam air tetapi larut dalam pelarut organik panas. Ia hampir tidak larut sama sekali dalam etanol di dekat suhu kamar tetapi 2,25 g akan larut dalam 100 g etanol mendidih. Ia ditemukan di alam sebagai mineral hoelit yang langka.
Reaksi
[sunting | sunting sumber]Hidrogenasi akan menghasilkan dihidroantrakuinon (antrahidrokuinon). Reduksi dengan tembaga menghasilkan antron.[3] Sulfonasi dengan asam sulfat menghasilkan asam antrokuinon-1-sulfonat,[4] yang bereaksi dengan natrium klorat menghasilkan 1-kloroantakuinon.[5]
Lihat pula
[sunting | sunting sumber]Referensi
[sunting | sunting sumber]- ^ a b c d Haynes, William M., ed. (2016). CRC Handbook of Chemistry and Physics (edisi ke-97). CRC Press. hlm. 3.28. ISBN 9781498754293.
- ^ International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. hlm. 724. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4.
- ^ Macleod, L. C.; Allen, C. F. H. (1934). "Benzanthrone". Organic Syntheses. 14: 4. doi:10.15227/orgsyn.014.0004.
- ^ Scott, W. J.; Allen, C. F. H. (1938). "Potassium Anthraquinone-α-Sulfonate". Organic Syntheses. 18: 72. doi:10.15227/orgsyn.018.0072.
- ^ Scott, W. J.; Allen, C. F. H. (1938). "α-Chloroanthraquinone". Organic Syntheses. 18: 15. doi:10.15227/orgsyn.018.0015.
Pranala luar
[sunting | sunting sumber]- (Inggris) National Pollutant Inventory — Polycyclic Aromatic Hydrocarbon Fact Sheet
- (Inggris) Molecules Spontaneously Form Honeycomb Network
