Infeksi
| Infeksi | |
|---|---|
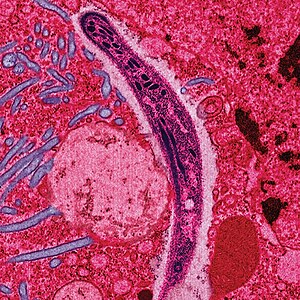 | |
| Gambar mikroskop elektron yang diwarnai menunjukkan sporozoit malaria yang berpindah melalui epitelium usus tikus. | |
| Informasi umum | |
| Spesialisasi | Penyakit infeksi |
| Penyebab | Agen infeksi (patogen) |
| Pengobatan | Antibiotik, antivirus, antijamur, antiprotozoa, dan antelmintik |
Infeksi, jangkitan, atau tularan adalah serangan dan perbanyakan diri yang dilakukan oleh patogen pada tubuh makhluk hidup.[1] Patogen penyebab infeksi di antaranya mikroorganisme seperti virus, prion, bakteri, dan fungi. Sementara itu, parasit seperti cacing dan organisme uniseluler juga dapat menyebabkan infeksi, meskipun terkadang istilah infeksi dan infestasi dipakai bergantian untuk menyebut serangan agen parasitik. Serangan patogen-patogen tersebut, maupun racun yang mereka hasilkan, dapat menimbulkan penyakit pada organisme inang. Penyakit infeksi merupakan penyakit yang dihasilkan oleh infeksi.
Individu terinfeksi dapat melawan infeksi menggunakan sistem imun mereka. Mamalia yang terinfeksi bereaksi dengan sistem imun bawaan, yang sering kali melibatkan peradangan, dan kemudian diikuti oleh sistem imun adaptif.[2]
Obat-obatan khusus yang digunakan untuk mengobati infeksi termasuk antibiotik, antivirus, antijamur, antiprotozoa, dan antelmintik. Penyakit infeksi mengakibatkan 9,2 juta kematian pada tahun 2013 (sekitar 17% dari semua kematian).[3] Cabang kedokteran yang berfokus pada infeksi juga disebut penyakit infeksi.[4]
Penyebab[sunting | sunting sumber]
Infeksi dapat disebabkan oleh berbagai entitas biologi yang dikenal dengan sebutan agen infeksi. Kata sifat patogenik disematkan kepada entitas biologi yang mampu menimbulkan penyakit, misalnya bakteri patogenik dan cacing patogenik. Hal ini juga menunjukkan bahwa tidak semua bakteri dan cacing bersifat patogenik; banyak di antara mereka yang mampu hidup dan berkembang biak tanpa menyerang dan menimbulkan penyakit pada organisme lain. Entitas biologi yang mengakibatkan penyakit disebut sebagai patogen, dan sering disinonimkan dengan agen infeksi.
Penyakit infeksi disebabkan oleh organisme infeksius, seperti bakteri, virus, fungi, prion, dan cacing.[5] Dalam penggunaan medis, agen infeksi dibagi menjadi dua kelompok besar, yaitu mikroorganisme patogenik (bakteri, virus, prion, fungi) dan parasit (seperti cacing, protozoa, dan artropoda).[6][7] Meskipun secara konseptual serupa dengan infeksi, tetapi serangan parasit pada tubuh manusia atau hewan biasanya disebut infestasi alih-alih infeksi. Umumnya, istilah infestasi digunakan untuk menyebut serangan ektoparasit, misalnya kutu, tungau, caplak, dan pinjal, yang menginvasi bagian luar tubuh inangnya dalam jumlah besar.[8]
Klasifikasi[sunting | sunting sumber]
Klinis, subklinis, dan laten[sunting | sunting sumber]
Infeksi yang menimbulkan gejala dan tanda yang terlihat jelas disebut infeksi klinis, sedangkan infeksi yang aktif tetapi tidak menghasilkan gejala yang nyata dapat disebut infeksi diam atau subklinis. Infeksi yang tidak aktif atau dorman disebut infeksi laten.[9] Contoh infeksi bakteri laten adalah tuberkulosis laten. Beberapa infeksi virus juga bisa bersifat laten, contoh virus laten berasal dari keluarga Herpesviridae.[10]
Kata infeksi dapat menunjukkan adanya patogen tertentu (tidak peduli seberapa sedikit), tetapi juga sering digunakan untuk menyatakan infeksi yang tampak secara klinis (dengan kata lain, kasus penyakit infeksi).[11] Penggunaan ini kadang-kadang menciptakan beberapa ambiguitas atau mendorong diskusi penggunaan kata infeksi; untuk menyiasatinya, para tenaga kesehatan biasanya menyebut kolonisasi (bukan infeksi) ketika mereka menyatakan keberadaan patogen, tanpa adanya infeksi yang tampak secara klinis (tidak ada penyakit).
Beberapa istilah berbeda digunakan untuk menggambarkan infeksi. Istilah pertama adalah infeksi akut, yaitu infeksi dengan gejala yang berkembang dengan cepat; jalannya penyakit bisa cepat atau berlarut-larut.[12] Istilah selanjutnya adalah infeksi kronis, ketika gejala penyakit berkembang secara bertahap, selama beberapa minggu atau bulan, dan lambat untuk disembuhkan.[13] Infeksi subakut adalah infeksi dengan gejala yang memakan waktu lebih lama dibandingkan infeksi akut tetapi timbul lebih cepat dibandingkan infeksi kronis. Infeksi laten adalah jenis infeksi yang dapat terjadi setelah fase akut; organisme patogennya ada tetapi gejalanya tidak; setelah beberapa waktu penyakit ini dapat muncul kembali. Infeksi fokal didefinisikan sebagai tempat infeksi awal suatu patogen sebelum mereka menyebar melalui aliran darah ke area lain tubuh.[14]
Primer versus oportunistik[sunting | sunting sumber]
Di antara berbagai mikroorganisme, hanya relatif sedikit yang mengakibatkan penyakit pada orang yang sehat.[15] Penyakit infeksi dihasilkan dari interaksi antara sejumlah patogen dan sistem pertahanan inang yang mereka infeksi. Tampilan dan tingkat keparahan penyakit yang dihasilkan patogen tergantung pada kemampuan patogen tersebut untuk merusak inang dan juga kemampuan inang untuk melawan patogen. Akan tetapi, sistem kekebalan inang juga dapat mengakibatkan kerusakan pada inang itu sendiri dalam upaya untuk mengendalikan infeksi. Oleh karena itu, dokter mengklasifikasikan mikroorganisme atau mikrob infeksius berdasarkan status pertahanan inang, baik sebagai patogen primer atau sebagai patogen oportunistik:
- Patogen primer
- Patogen primer menyebabkan penyakit sebagai akibat dari keberadaan atau aktivitas mereka di dalam inang yang normal dan sehat, dan virulensi intrinsiknya (keparahan penyakit yang disebabkannya), sebagian, merupakan konsekuensi dari kebutuhan patogen untuk bereproduksi dan menyebar. Banyak patogen primer manusia yang paling umum hanya menginfeksi manusia, tetapi, banyak penyakit serius diakibatkan oleh organisme yang berasal dari lingkungan atau yang menginfeksi inang nonmanusia.
- Patogen oportunistik
- Patogen oportunistik dapat mengakibatkan penyakit infeksi pada inang dengan sistem pertahanan yang tertekan (defisiensi imun) atau jika mereka memiliki akses yang tidak biasa ke bagian dalam tubuh (misalnya melalui trauma). Infeksi oportunistik dapat diakibatkan oleh mikrob yang biasanya bersentuhan dengan inang, seperti bakteri atau fungi patogenik di usus atau saluran pernapasan bagian atas, dan mereka juga dapat berasal dari inang lain (seperti pada kolitis akibat Clostridium sulitile) atau dari lingkungan sebagai akibat dari cedera (misalnya infeksi luka pembedahan atau patah tulang). Penyakit oportunistik membutuhkan kerusakan pertahanan inang, yang dapat terjadi sebagai akibat dari cacat genetik (seperti penyakit granuloma kronik), paparan obat antimikrob atau bahan kimia imunosupresif (seperti yang mungkin terjadi setelah keracunan atau kemoterapi), paparan radiasi pengion, atau sebagai akibat dari penyakit infeksi dengan aktivitas imunosupresif (seperti campak, malaria, atau AIDS). Patogen primer juga dapat mengakibatkan penyakit yang lebih parah pada inang dengan imunitas yang tertekan dibandingkan bila terjadi ipada inang yang imunitasnya memadai.[16]
- Infeksi primer versus infeksi sekunder
- Infeksi primer adalah infeksi yang (atau secara praktis dapat dipandang) menjadi akar penyebab masalah kesehatan saat ini. Sebaliknya, infeksi sekunder adalah sekuela (gejala sisa) atau komplikasi dari penyebab utama. Sebagai contoh, tuberkulosis paru sering merupakan infeksi primer, tetapi infeksi yang terjadi hanya akibat luka bakar atau trauma tajam (sebagai akar penyebab) yang memungkinkan akses patogen ke jaringan dalam, merupakan infeksi sekunder. Patogen primer sering menyebabkan infeksi primer dan juga sering menyebabkan infeksi sekunder. Biasanya, infeksi oportunistik dipandang sebagai infeksi sekunder (karena defisiensi imun atau cedera adalah faktor predisposisinya).
Jenis infeksi lain[sunting | sunting sumber]
Jenis infeksi lain terdiri dari infeksi campuran, iatrogenik, nosokomial, dan infeksi yang didapat dari masyarakat. Infeksi campuran adalah infeksi yang disebabkan oleh dua atau lebih patogen. Contohnya adalah apendisitis, yang disebabkan oleh Bacteroides fragilis dan Escherichia coli. Jenis kedua adalah infeksi iatrogenik, yaitu infeksi yang ditularkan dari petugas kesehatan ke pasien. Infeksi nosokomial, yaitu infeksi yang didapat saat dirawat di rumah sakit, juga terjadi pada faslitias layanan kesehatan. Terakhir, infeksi yang didapat dari masyarakat adalah infeksi yang didapat dari seluruh komunitas.[14]
Infeksius atau tidak[sunting | sunting sumber]
Salah satu cara untuk membuktikan bahwa suatu penyakit bersifat infeksius adalah dengan mengujinya menggunakan postulat Koch, yang mensyaratkan bahwa, pertama, agen infeksi hanya dapat diidentifikasi dari individu yang memiliki penyakit dan bukan dari kontrol yang sehat, dan kedua, bahwa individu dengan agen infeksi juga mengembangkan penyakit tersebut. Postulat ini pertama kali digunakan dalam penemuan bahwa spesies Mycobacterium mengakibatkan tuberkulosis.
Akan tetapi, postulat Koch biasanya tidak dapat diuji dalam praktik modern karena alasan etis. Membuktikan penyakit akan memerlukan infeksi eksperimental pada individu yang sehat menggunakan patogen yang diproduksi sebagai kultur murni. Sebaliknya, bahkan penyakit yang jelas-jelas infeksius tidak selalu memenuhi kriteria tersebut; misalnya, Treponema pallidum, bakteri penyebab sifilis, tidak dapat dikultur secara in vitro, tetapi mikroorganisme ini dapat dikultur dalam testis kelinci. Belum diketahui dengan jelas mengapa kultur murni diperoleh dari hewan yang menjadi inang dibandingkan dengan perolehan dari kultur lempeng.
Epidemiologi, atau studi dan analisis tentang siapa, mengapa, dan di mana penyakit terjadi, dan apa yang menentukan berbagai populasi memiliki penyakit, merupakan alat penting lain yang digunakan untuk memahami penyakit infeksi. Ahli epidemiologi dapat menentukan perbedaan di antara kelompok-kelompok dalam suatu populasi, seperti apakah kelompok usia tertentu memiliki tingkat infeksi yang lebih besar atau lebih kecil; apakah kelompok yang tinggal di lingkungan yang berbeda lebih mungkin terinfeksi; dan oleh faktor-faktor lain, seperti jenis kelamin dan ras. Para peneliti juga dapat menilai apakah wabah penyakit bersifat sporadik atau hanya terjadi sesekali; bersifat endemik, dengan tingkat yang stabil dari kasus reguler yang terjadi di suatu daerah; epidemi, dengan jumlah kasus yang muncul cepat, dan luar biasa tinggi di suatu wilayah; atau pandemi, yang merupakan epidemi global. Jika penyebab penyakit infeksi tidak diketahui, epidemiologi dapat digunakan untuk membantu melacak sumber infeksi.
[sunting | sunting sumber]
Penyakit infeksi kadang-kadang disebut penyakit menular ketika mudah ditularkan melalui kontak dengan orang yang sakit atau sekresi mereka (misalnya influenza). Dengan demikian, penyakit menular adalah bagian dari penyakit infeksi, terutama penyakit yang mudah berpindah atau ditransmisikan. Jenis penyakit menular lain memiliki rute infeksi yang lebih khusus, seperti penularan melalui vektor atau hubungan seksual, biasanya tidak dianggap sebagai "menular", dan sering kali tidak memerlukan isolasi medis (kadang-kadang disebut karantina) bagi penderitanya. Namun, konotasi khusus dari kata "menular" dan "penyakit menular" (mudah ditransmisikan) tidak selalu dipertimbangkan dalam penggunaan populer. Penyakit infeksi biasanya ditularkan antarindividu melalui kontak langsung. Jenis kontak yang dimaksud yaitu dari orang ke orang dan penyebaran percikan atau tetesan. Kontak tidak langsung seperti penularan melalui udara, benda yang terkontaminasi, makanan dan air minum, kontak orang dengan hewan (yang bertindak sebagai reservoir), gigitan serangga, dan lingkungan yang terkontaminasi, merupakan cara lain penularan penyakit infeksi.[17]
Lokasi anatomis[sunting | sunting sumber]
Infeksi dapat dikelompokkan berdasarkan lokasi anatomi atau sistem organ yang terinfeksi, misalnya infeksi saluran kemih, infeksi kulit, infeksi saluran pernapasan, infeksi odontogenik (infeksi yang berasal dari gigi atau jaringan yang berdekatan), infeksi vagina, dan infeksi intraamniotik. Selain itu, lokasi peradangan yang menjadi tempat infeksi dapat dijadikan penamaan radang tersebut, misalnya pneumonia, meningitis, dan salpingitis.
Tanda dan gejala[sunting | sunting sumber]
Gejala dan tanda klinis infeksi tergantung pada masing-masing penyakit. Beberapa tanda infeksi mempengaruhi keseluruhan tubuh secara umum, seperti kelelahan, kehilangan nafsu makan, penurunan berat badan, demam, keringat malam, kedinginan, sakit, dan nyeri. Beberapa tanda lain bersifat khusus untuk bagian tubuh tertentu, seperti ruam kulit, batuk, atau keluarnya cairan dari hidung.
Dalam kasus-kasus tertentu, penyakit infeksi mungkin asimtomatik (tidak bergejala) untuk sebagian besar atau bahkan keseluruhan proses penyakit. Pada kasus ini, individu lain dapat menderita penyakit, sebagai penderita sekunder, setelah mengalami kontak dengan pembawa penyakit yang asimtomatik. Suatu infeksi tidak selalu identik dengan penyakit infeksi, karena beberapa infeksi tidak menimbulkan penyakit pada inang.[16]
Patofisiologi[sunting | sunting sumber]
Ada serangkaian peristiwa yang terjadi selama infeksi.[18] Rantai peristiwa tersebut meliputi beberapa tahapan, yang melibatkan agen infeksi, reservoir, masuknya agen ke inang yang rentan, keluarnya agen dari inang tersebut, dan penularan ke inang baru. Masing-masing mata rantai harus terjadi secara berurutan agar infeksi dapat berkembang. Pemahaman terhadap langkah-langkah ini membantu petugas kesehatan mengendalikan infeksi dan mencegahnya agar tidak terjadi.[19]
Kolonisasi[sunting | sunting sumber]
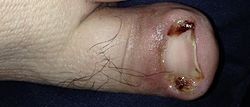
Infeksi dimulai ketika suatu organisme berhasil memasuki tubuh, lalu tumbuh dan memperbanyak diri. Hal ini disebut kolonisasi. Sebagian besar manusia tidak mudah terinfeksi. Orang-orang dengan sistem imun yang lemah lebih rentan terhadap infeksi kronis atau persisten, sedangkan individu dengan sistem imun yang tertekan sangat rentan terhadap infeksi oportunistik. Umumnya, patogen masuk ke dalam tubuh inang melalui mukosa pada lubang tubuh, seperti rongga mulut, hidung, mata, genitalia, anus, dan bisa juga masuk melalui luka terbuka. Beberapa patogen dapat tumbuh di tempat awal masuk, tetapi banyak yang bermigrasi dan menyebabkan infeksi sistemik pada organ yang berbeda. Beberapa patogen tumbuh di dalam sel inang (intraseluler) sedangkan yang lain tumbuh bebas dalam cairan tubuh.
Kolonisasi luka mengacu pada mikroorganisme yang tidak bereplikasi di dalam luka, sedangkan pada luka terinfeksi, mikroorganisme mengalami replikasi dan mengakibatkan kelukaan jaringan.[20] Semua organisme multiseluler dikolonisasi sampai tingkat tertentu oleh organisme ekstrinsik, dan sebagian besar kolonisasi ini berada dalam hubungan mutualisme atau komensalisme. Contoh hubungan mutualisme adalah spesies bakteri anaerob, yang melakukan kolonisasi pada usus mamalia, dan contoh komensalisme adalah berbagai spesies Staphylococcus yang ada pada kulit manusia. Tak satu pun dari kolonisasi ini dianggap infeksi. Perbedaan antara infeksi dan kolonisasi sering kali hanya masalah keadaan. Organisme nonpatogenik dapat menjadi patogenik dalam kondisi spesifik, dan bahkan organisme yang paling virulen (ganas) membutuhkan kondisi tertentu untuk menimbulkan infeksi yang membahayakan. Di dalam tubuh, beberapa bakteri seperti Corynebacteria sp. dan streptococci viridans, mencegah adhesi dan kolonisasi bakteri patogenik sehingga mereka memiliki hubungan simbiosis dengan inang, mencegah infeksi, dan mempercepat penyembuhan luka.

Variabel yang terlibat dan memengaruhi hasil akhir infeksi meliputi rute masuknya patogen, akses yang diperolehnya untuk memasuki bagian tubuh tertentu inang, virulensi intrinsik patogen, jumlah patogen di awal inokulasi, dan status kekebalan inang. Sebagai contoh, beberapa spesies stafilokokus tidak berbahaya pada kulit, tetapi ketika mereka berada dalam tempat yang biasanya steril, misalnya di dalam kapsul sendi atau peritoneum, mereka akan berkembang biak tanpa perlawanan dan menyebabkan kerusakan.
Dalam beberapa dekade terakhir, kromatografi gas–spektrometri massa, analisis RNA ribosomal 16S, omik, dan teknologi canggih lainnya telah menjelaskan bahwa kolonisasi mikrob sangat umum, bahkan dalam lingkungan yang manusia anggap hampir steril. Karena kolonisasi bakteri merupakan hal yang normal, sulit untuk mengetahui luka kronis mana yang dapat dikategorikan terinfeksi dan seberapa besar risiko perkembangannya. Meskipun sejumlah besar luka ditemukan dalam praktik klinis, evaluasi tanda dan gejala dengan data yang berkualitas masih terbatas. Sebuah tinjauan luka kronis mengkuantifikasi pentingnya peningkatan rasa nyeri sebagai indikator infeksi.[24] Tinjauan tersebut menunjukkan bahwa temuan yang paling berguna adalah peningkatan rasa nyeri, tetapi tidak adanya rasa nyeri tidak otomatis menghilangkan kemungkinan infeksi.
Penyakit[sunting | sunting sumber]
Penyakit dapat muncul jika mekanisme pertahanan inang terganggu dan agen penginfeksi menyebabkan kerusakan pada inang. Mikroorganisme dapat menyebabkan kerusakan jaringan dengan melepaskan berbagai racun atau enzim yang merusak. Sebagai contoh, Clostridium tetani melepaskan racun yang melumpuhkan otot, dan Staphylococcus melepaskan racun yang menghasilkan syok dan sepsis. Tidak semua agen infeksi menyebabkan penyakit pada semua inang, misalnya, kurang dari 5% orang yang terinfeksi virus polio akan menderita penyakit polio.[25] Di sisi lain, beberapa agen infeksi bersifat sangat ganas. Prion yang menyebabkan penyakit sapi gila dan penyakit Creutzfeldt-Jakob selalu membunuh semua hewan dan orang yang terinfeksi.
Infeksi persisten terjadi karena tubuh tidak dapat membersihkan patogen setelah infeksi awal. Infeksi persisten ditandai oleh adanya agen penginfeksi secara terus-menerus, sering kali sebagai infeksi laten yang berulang kali kambuh sebagai infeksi aktif. Ada beberapa virus yang mengakibatkan infeksi persisten dengan menginfeksi sel-sel tubuh yang berbeda. Beberapa virus yang sekali masuk tidak pernah meninggalkan tubuh. Contoh yang khas adalah virus herpes, yang cenderung bersembunyi di saraf dan menjadi aktif kembali dalam keadaan tertentu.
Infeksi persisten menyebabkan jutaan kematian secara global setiap tahun.[26] Infeksi kronis oleh parasit merupakan penyebab morbiditas dan mortalitas yang tinggi di banyak negara terbelakang.
Penularan[sunting | sunting sumber]

Agar agen penginfeksi dapat bertahan dan mengulangi siklus infeksi pada inang lain, mereka (atau keturunannya) harus meninggalkan inang atau reservoir yang ditempatinya dan menyebabkan infeksi di tempat lain. Penularan infeksi dapat terjadi melalui banyak rute:
- Kontak tetesan atau percikan, yang juga dikenal sebagai rute pernapasan, dan infeksi yang diakibatkannya dapat disebut penyakit bawaan udara. Jika orang yang terinfeksi batuk atau bersin dan partikelnya sampai ke orang lain, mikroorganisme, yang tersuspensi dalam tetesan yang hangat dan lembab, dapat masuk ke dalam tubuh melalui permukaan hidung, mulut atau mata.
- Penularan fekal–oral, yaitu ketika bahan makanan atau air menjadi terkontaminasi partikel feses (oleh orang-orang yang tidak mencuci tangan sebelum menyiapkan makanan atau limbah yang tidak diolah dilepaskan ke dalam air minum) sehingga orang-orang yang makan dan minum menjadi terinfeksi. Patogen yang ditularkan melalui metode ini di antaranya Vibrio cholerae, spesies Giardia, Rotavirus, Entamoeba histolytica, Escherichia coli, dan cacing pita.[27] Sebagian besar patogen ini menyebabkan gastroenteritis.
- Penularan seksual, dengan penyakit yang dihasilkan disebut penyakit menular seksual.
- Penularan melalui mulut. Penyakit yang ditularkan terutama melalui kontak oral langsung seperti ciuman, atau melalui kontak tidak langsung seperti dengan berbagi gelas minum atau rokok.
- Penularan melalui kontak langsung, Beberapa penyakit yang dapat ditularkan melalui kontak atau sentuhan langsung termasuk tinea pedis, impetigo, dan kutil.
- Penularan melalui benda mati, misalnya makanan, air, dan tanah yang terkontaminasi.[28]
- Penularan vertikal, yaitu penularan langsung dari ibu ke embrio, janin, atau bayi selama kehamilan atau persalinan. Hal ini bisa terjadi ketika ibu mendapat infeksi sebagai penyakit penyerta dalam kehamilan.
- Penularan iatrogenik, karena prosedur medis seperti injeksi atau transplantasi bahan yang terinfeksi.
- Penularan melalui vektor, yaitu organisme yang tidak menderita penyakit tetapi ikut menularkan infeksi dengan membawa patogen dari satu inang ke inang lainnya.[29]
Hubungan antara virulensi dan penularan sangat kompleks; jika suatu penyakit bersifat fatal, inang dapat mati sebelum patogen dapat ditularkan ke inang lain.
Diagnosis[sunting | sunting sumber]
Diagnosis penyakit infeksi terkadang melibatkan identifikasi agen infeksi baik secara langsung maupun tidak langsung. Dalam praktiknya, sebagian besar penyakit infeksi minor seperti kutil, abses kulit, infeksi sistem pernapasan, dan diare didiagnosis berdasarkan manifestasi klinisnya dan diobati tanpa mengetahui agen penyebabnya secara spesifik. Kesimpulan tentang penyebab penyakit ini didasarkan pada kemungkinan penderitanya melakukan kontak dengan agen tertentu, keberadaan mikroorganisme dalam suatu komunitas, dan pertimbangan epidemiologis lainnya. Dengan upaya yang memadai, semua agen infeksi dapat diidentifikasi secara spesifik. Namun, manfaat identifikasi sering kali lebih kecil dibandingkan biaya yang perlu dikeluarkan untuk identifikasi, karena sering kali tidak ada perawatan khusus untuk penyakit tersebut, penyebabnya jelas, atau hasil infeksinya tidak berbahaya.
Diagnosis penyakit infeksi hampir selalu dimulai oleh riwayat kesehatan dan pemeriksaan fisik. Teknik identifikasi yang lebih terperinci melibatkan kultur agen infeksi yang diisolasi dari penderitanya. Kultur memungkinkan identifikasi organisme penginfeksi dengan memeriksa karakteristik mikroskopis mereka, dengan mendeteksi keberadaan zat yang dihasilkan oleh patogen, dan dengan secara langsung mengidentifikasi organisme dengan genotipnya. Teknik lain (seperti sinar-X, pemindaian tomografi terkomputasi (CT), pemindaian PET atau MRI) digunakan untuk menghasilkan gambar kelainan internal yang dihasilkan dari pertumbuhan agen infeksi. Gambar tersebut berguna dalam mendeteksi, misalnya, abses tulang atau ensefalopati spongiformis yang ditimbulkan oleh prion.
Diagnosis simtomatik[sunting | sunting sumber]
Diagnosis dibantu oleh gejala yang muncul pada setiap individu yang menderita penyakit infeksi, tetapi metode ini biasanya membutuhkan teknik diagnostik tambahan untuk mengonfirmasi kecurigaan tersebut. Beberapa tanda klinis tertentu, yang disebut tanda patognomonik, merupakan karakteristik khusus yang menjadi indikasi suatu penyakit; tetapi hal ini jarang terjadi. Tidak semua infeksi bersifat simtomatik.[30] Pada anak-anak, adanya sianosis, pernapasan cepat, perfusi perifer yang buruk, atau ruam petekie meningkatkan risiko infeksi serius hingga lebih dari 5 kali lipat.[31]
Kultur mikrob[sunting | sunting sumber]

Kultur mikrobiologi adalah metode utama yang digunakan untuk mendiagnosis penyakit infeksi. Dalam kultur mikrob, media pertumbuhan digunakan untuk memfasilitasi pertumbuhan agen tertentu. Spesimen dari jaringan atau cairan yang diduga berpenyakit diambil untuk kemudian dikultur untuk mendeteksi keberadaan agen infeksi. Kebanyakan bakteri patogenik mudah tumbuh pada agar nutrien, suatu media padat yang mengandung karbohidrat dan protein yang diperlukan untuk pertumbuhan bakteri. Satu bakteri akan memperbanyak diri membentuk sebuah koloni berupa gundukan yang terlihat di permukaan agar. Koloni ini dapat tumbuh terpisah dari koloni lain atau menyatu dengan koloni lain pada agar tersebut. Variasi ukuran, warna, bentuk dan bentuk koloni merupakan hasil dari karakteristik spesies maupun galur bakteri, serta lingkungan yang mendukung pertumbuhannya. Bahan-bahan lain sering ditambahkan ke plat agar untuk membantu identifikasi. Zat tambahan tersebut memungkinkan pertumbuhan beberapa bakteri dan mencegah pertumbuhan bakteri lainnya, atau mengalami perubahan warna sebagai respons terhadap bakteri tertentu dan bukan bakteri yang lain. Plat bakteriologis seperti ini biasanya digunakan dalam identifikasi klinis bakteri infeksius. Biakan mikrob juga dapat digunakan dalam identifikasi virus. Media yang digunakan untuk menumbuhkan virus adalah sel hidup yang dapat diinfeksi oleh virus yang dimaksud. Dalam proses identifikasi virus, akan tercipta suatu zona kematian sel, yang diakibatkan oleh pertumbuhan virus, yang disebut "plak". Parasit eukariotik juga dapat ditumbuhkan dalam kultur.
Apabila tidak ada teknik kultur plat yang sesuai, beberapa mikroorganisme membutuhkan hewan hidup sebagai media pertumbuhan. Bakteri seperti Mycobacterium leprae dan Treponema pallidum dapat tumbuh pada hewan, meskipun teknik serologis dan mikroskopis membuat penggunaan hewan hidup tidak diperlukan lagi. Virus juga biasanya diidentifikasi menggunakan media lain selain hewan hidup. Beberapa virus dapat tumbuh dalam telur berembrio. Metode identifikasi lain yang bermanfaat adalah xenodiagnosis, atau penggunaan vektor untuk mendukung pertumbuhan agen infeksi. Penyakit Chagas tidak mudah didiagnosis karena sulit untuk menunjukkan keberadaan agen penyebab penyakit ini, yaitu Trypanosoma cruzi, pada penderitanya. Oleh karena itu, diagnosis definitif sulit ditegakkan. Dalam kasus ini, xenodiagnosis melibatkan penggunaan vektor T. cruzi, yaitu Triatominae, serangga yang tidak terinfeksi, yang mengisap darah seseorang yang diduga terinfeksi. Serangga tersebut kemudian diperiksa untuk mendeteksi keberadaan T. cruzi dalam ususnya.
Mikroskopi[sunting | sunting sumber]
Alat utama lain untuk mendiagnosis penyakit infeksi adalah mikroskop. Hampir semua teknik kultur yang dibahas di atas bergantung, pada titik tertentu, pada pemeriksaan mikroskopis untuk mengidentifikasi agen infeksi secara definitif. Pemeriksaan mikroskopis dapat dilakukan dengan instrumen sederhana, seperti mikroskop cahaya majemuk, atau dengan instrumen serumit mikroskop elektron. Spesimen yang diperoleh dari penderita penyakit dapat dilihat langsung di bawah mikroskop cahaya, dan sering kali dapat membantu identifikasi dengan cepat. Mikroskop juga sering digunakan bersama dengan teknik pewarnaan biokimia, dan dapat bersifat sangat spesifik ketika dikombinasikan dengan teknik berbasis antibodi. Suatu antibodi dapat dilabel dengan teknik fluoresens sehingga dapat diarahkan untuk mengikat dan mengidentifikasi antigen spesifik yang ada pada patogen. Mikroskop fluoresens kemudian digunakan untuk mendeteksi antibodi tersebut, yang telah berikatan dengan antigen di dalam sampel klinis atau sel yang dikultur. Teknik ini sangat berguna untuk mendiagnosis penyakit virus, yang tidak mampu diidentifikasi oleh mikroskop cahaya.
Prosedur mikroskopis lainnya juga dapat membantu mengidentifikasi agen infeksi. Hampir semua sel mudah diwarnai dengan sejumlah bahan pewarna dasar akibat tarikan elektrostatik antara molekul seluler bermuatan negatif dengan muatan positif pada pewarna. Pada mikroskop, sel biasanya terlihat transparan dan pemberian warna akan meningkatkan kontras antara sel dengan latar belakangnya. Pewarnaan sel dengan zat warna seperti Giemsa atau kristal ungu memungkinkan seorang pengguna mikroskop untuk menggambarkan ukuran, bentuk, komponen internal dan eksternal sel, serta hubungannya dengan sel-sel lain. Perbedaan respons bakteri terhadap pewarnaan dapat dimanfaatkan untuk mengelompokkan mikroorganisme. Dua metode pewarnaan, yaitu pewarnaan Gram dan pewarnaan tahan asam, merupakan pendekatan standar yang digunakan untuk mengklasifikasikan bakteri dan untuk mendiagnosis penyakit. Pewarnaan Gram dapat mengidentifikasi kelompok bakteri Firmicutes dan Actinobacteria, yang berisi banyak bakteri patogenik penting. Sementara itu, prosedur pewarnaan asam-cepat dapat mengidentifikasi genus Mycobacterium dan Nocardia.
Uji biokimia[sunting | sunting sumber]
Identifikasi agen infeksi juga bisa menggunakan uji biokimia untuk mengetahui karakter produk metabolik atau enzimatik dari agen infeksi tertentu. Karena bakteri memfermentasi karbohidrat dengan pola tertentu sesuai dengan karakteristik genus dan spesiesnya, deteksi produk fermentasi biasanya untuk mengidentifikasi bakteri. Asam, alkohol, dan gas juga biasanya dideteksi dalam uji ini ketika bakteri ditumbuhkan dalam media cair atau padat.
Isolasi enzim dari jaringan yang terinfeksi juga membantu diagnosis penyakit infeksi. Sebagai contoh, manusia tidak dapat membuat enzim replikase RNA atau transkriptase balik, dan keberadaan enzim-enzim ini merupakan tanda infeksi virus tertentu. Kemampuan protein hemaglutinin yang dimiliki virus untuk mengikat sel-sel darah merah hingga dapat dideteksi juga merupakan uji biokimia untuk mengetahui infeksi virus, walaupun hemaglutinin bukanlah suatu enzim dan tidak memiliki fungsi metabolik.
Uji serologis merupakan metode pengujian yang sangat sensitif, spesifik, dan sering kali sangat cepat untuk mengidentifikasi mikroorganisme tertentu. Pengujian ini didasarkan pada kemampuan suatu antibodi untuk berikatan secara khusus pada suatu antigen. Antigen ini biasanya berupa protein atau karbohidrat yang dihasilkan atau dimiliki oleh agen infeksi. Ikatan ini kemudian memicu serangkaian peristiwa yang dapat diamati dengan jelas dalam berbagai cara, tergantung pada jenis pengujiannya. Misalnya, "sakit tenggorokan" biasanya didiagnosis dalam beberapa menit, dengan mendeteksi antigen yang dibuat oleh bakteri penyebabnya, Streptococcus pyogenes, yang diambil dari tenggorokan pasien dengan kapas. Uji serologis, jika tersedia, biasanya merupakan rute identifikasi yang disukai. Meskipun demikian, uji serologis butuh biaya pengembangan yang mahal dan reagen yang digunakan dalam tes sering kali harus disimpan dalam kondisi dingin. Beberapa uji serologis bisa berbiaya sangat mahal, meskipun ketika digunakan secara luas, misalnya dengan "uji cepat", metode ini bisa menjadi murah.[16]
Teknik serologis telah dikembangkan secara kompleks menjadi imunoasai. Imunoasai dapat menggunakan ikatan antibodi–antigen sebagai dasar untuk menghasilkan sinyal radiasi partikel atau elektromagnetik, yang dapat dideteksi oleh beberapa instrumen. Sinyal yang sebelumnya tidak diketahui dapat dibandingkan dengan standar yang memungkinkan penghitungan jumlah antigen target. Imunoasai dapat mendeteksi atau mengukur antigen milik agen infeksi atau protein yang dihasilkan oleh inang terinfeksi sebagai respons terhadap agen asing. Sebagai contoh, imunoasai A dapat mendeteksi keberadaan protein permukaan dari partikel virus, sedangkan imunoasai B dapat mendeteksi atau mengukur antibodi yang dihasilkan oleh sistem imun organisme yang dibuat untuk menetralisir dan menghancurkan virus.
Suatu instrumen dapat digunakan untuk membaca sinyal yang sangat kecil yang dihasilkan oleh reaksi sekunder dari ikatan antigen–antibodi. Instrumen tersebut dapat mengontrol pengambilan sampel, penggunaan reagen, waktu reaksi, deteksi sinyal, penghitungan hasil, dan manajemen data untuk menghasilkan proses otomatis yang hemat biaya untuk mendiagnosis penyakit infeksi.
Diagnosis berbasis PCR[sunting | sunting sumber]
Reaksi berantai polimerase (PCR) merupakan metote yang mendeteksi keberadaan segmen asam nukleat dalam spesimen yang diuji. Teknologi yang didasarkan pada metode ini akan menjadi standar emas untuk berbagai diagnosis penyakit karena beberapa alasan. Pertama, pendataan agen infeksi telah berkembang sehingga hampir semua agen infeksi penting telah diidentifikasi. Kedua, agen infeksi harus memperbanyak diri (melipatgandakan asam nukleatnya) di dalam tubuh manusia untuk menimbulkan penyakit. Amplifikasi asam nukleat dalam jaringan yang terinfeksi ini memungkinkan deteksi agen infeksi dengan menggunakan PCR. Ketiga, unsur penting untuk melakukan PCR, yaitu primer, berasal dari genom agen infeksi, dan seiring waktu genom tersebut akan diketahui.
Dengan demikian, teknologi saat ini telah mampu mendeteksi agen infeksi dengan cepat dan spesifik. Satu-satunya kesulitan untuk menjadikan PCR sebagai alat diagnosis standar adalah biaya yang cukup tinggi dan penerapannya yang tidak mudah. Beberapa penyakit juga tidak cocok didiagnosis dengan PCR, contohnya adalah penyakit klostridial (tetanus dan botulisme). Penyakit-penyakit ini pada dasarnya adalah keracunan biologis oleh sejumlah kecil bakteri infeksius yang menghasilkan neurotoksin yang sangat kuat. Tidak terjadi perbanyakan agen infeksi yang signifikan, yang akan membatasi kemampuan PCR untuk mendeteksi keberadaan bakteri-bakteri tersebut.
Pengurutan metagenomika[sunting | sunting sumber]
Mengingat banyaknya bakteri, virus, dan patogen lain yang menyebabkan penyakit ganas dan mengancam jiwa, kemampuan untuk mengidentifikasi penyebab infeksi dengan cepat merupakan hal penting meskipun sering kali dijumpai tantangan. Sebagai contoh, lebih dari setengah kasus ensefalitis, penyakit berat yang memengaruhi otak, tidak terdiagnosis, meskipun telah dilakukan pengujian ekstensif menggunakan metode laboratorium klinis yang canggih. Metagenomika pun dikembangkan untuk penggunaan klinis untuk mendiagnosis infeksi dengan sensitif dan cepat menggunakan pengujian tunggal. Pengujian ini mirip dengan PCR; namun, amplifikasi materi genetik dilakukan dengan tidak bias dan tidak menggunakan primer untuk agen infeksi tertentu. Langkah amplifikasi ini diikuti oleh pengurutan dan penjajaran menggunakan basis data besar dari ribuan genom organisme dan virus.
Pengurutan metagenomika terbukti sangat berguna untuk mendiagnosis penderita yang mengalami imunodefisiensi. Lebih banyak lagi agen infeksi yang dapat mengakibatkan penyakit serius pada individu dengan imunosupresi, sehingga penapisan klinis harus dilakukan lebih luas. Selain itu, ekspresi gejala sering kali tidak khas sehingga diagnosis klinis yang didasarkan pada manifestasi klinis menjadi lebih sulit. Ditambah lagi, metode diagnostik yang mengandalkan deteksi antibodi cenderung tidak dapat diandalkan. Pengujian yang luas dan sensitif untuk mendeteksi keberadaan materi infeksius lebih diinginkan dibandingkan deteksi antibodi.
Indikasi pengujian[sunting | sunting sumber]
Identifikasi agen infeksi spesifik biasanya dilakukan ketika ia bisa membantu pengobatan atau pencegahan penyakit, atau untuk menambah pengetahuan tentang proses penyakit sebelum langkah-langkah terapi atau pencegahan yang efektif dikembangkan. Sebagai contoh, pada awal 1980-an, sebelum kemunculan zidovudin untuk pengobatan AIDS, perkembangan penyakit ini diikuti dengan memantau komposisi sampel darah penderitanya, walaupun hasilnya tidak menawarkan pilihan pengobatan lebih lanjut. Beberapa studi tentang kemunculan HIV di komunitas-komunitas tertentu memungkinkan pengembangan hipotesis mengenai jalur penularan virus. Dengan memahami bagaimana penyakit ini ditularkan, sumber daya dapat ditargetkan ke masyarakat dengan risiko terbesar untuk mengurangi jumlah infeksi baru. Identifikasi serologis, dan kemudian identifikasi genotipik atau molekuler, dari HIV juga memungkinkan pengembangan hipotesis mengenai asal-usul waktu dan lokasi virus, serta segudang hipotesis lainnya. [17] Perkembangan alat diagnostik molekuler telah memungkinkan dokter dan peneliti untuk memantau kemanjuran pengobatan dengan obat antiretrovirus. Diagnosis molekuler sekarang telah banyak digunakan untuk mengidentifikasi HIV pada orang sehat, jauh sebelum timbulnya penyakit, dan telah digunakan untuk menunjukkan adanya orang yang secara genetik kebal terhadap infeksi HIV. Meskipun untuk sementara masih belum ada obat untuk menyembuhkan AIDS, ada manfaat terapeutik dan prediktif yang besar untuk mengidentifikasi HIV dan memantau tingkat virus dalam darah orang yang terinfeksi, baik untuk penderita maupun masyarakat luas.
Pencegahan[sunting | sunting sumber]

Beberapa metode seperti mencuci tangan dan mengenakan alat pelindung diri seperti masker dapat membantu mencegah infeksi dari satu orang ke orang lain. Teknik aseptik diperkenalkan dalam kedokteran pada akhir abad ke-19 dan sangat mengurangi insiden infeksi yang disebabkan oleh pembedahan. Sering mencuci tangan tetap menjadi cara paling penting untuk mencegah penyebaran organisme yang tidak diinginkan.[33] Beberapa bentuk pencegahan lain seperti menerapkan pola hidup higienis, menjaga sanitasi, berolahraga dengan teratur, mengonsumsi diet seimbang, dan serta memasak makanan dengan baik juga penting untuk mencegah infeksi.
Zat antimikrob yang digunakan untuk mencegah penularan infeksi meliputi:
- antiseptik, yang diaplikasikan pada jaringan hidup, misalnya kulit.
- disinfektan, yang menghancurkan mikroorganisme pada benda mati.
- antibiotik, dalam konteks profilaksis bila diberikan sebagai pencegahan dan bukan sebagai pengobatan infeksi. Namun, penggunaan antibiotik jangka panjang mengakibatkan resistansi. Pemakaian antibiotik lebih banyak dari yang diperlukan, memungkinkan bakteri bermutasi sehingga menjadi kebal.
Salah satu cara untuk mencegah atau memperlambat penularan penyakit infeksi adalah mengenali perbedaan sifat berbagai penyakit.[34] Beberapa karakteristik penting yang harus diperhatikan di antaranya virulensi patogen, jarak yang ditempuh oleh penderitanya, dan tingkat penularan. Galur virus Ebola pada manusia, misalnya, membunuh penderitanya dengan cepat. Akibatnya, para penderita penyakit ini tidak punya kesempatan untuk bepergian jauh dari zona infeksi awal.[35] Selain itu, virus ini harus menyebar melalui lesi kulit atau membran permeabel seperti mata. Dengan demikian, tahap awal penyakit Ebola tidak terlalu menular karena korbannya hanya mengalami pendarahan internal. Sebagai hasil dari karakteristik di atas, penyebaran penyakit Ebola sangat cepat dan biasanya tetap dalam area geografis yang relatif terbatas. Sebaliknya, HIV membunuh korbannya dengan sangat lambat dengan menyerang sistem kekebalan tubuh mereka.[16] Akibatnya, banyak dari korbannya menularkan virus ke orang lain bahkan sebelum menyadari bahwa mereka membawa penyakit itu. Selain itu, virulensi yang relatif rendah memungkinkan para penderitanya untuk melakukan perjalanan jarak jauh, yang meningkatkan kemungkinan terjadinya epidemi.
Metode umum untuk mencegah penularan patogen yang ditularkan melalui vektor adalah pengendalian vektor tersebut. Pemutusan siklus hidup vektor akan memutus penyebaran agen infeksi yang dibawanya.
Jika infeksi hanya dicurigai dan belum dapat dipastikan, seorang individu dapat dikarantina sampai masa inkubasi selesai untuk menunggu manifestasi penyakit muncul atau memastikan orang yang dikarantina tetap sehat. Selain terhadap individu, karantina juga dapat diterapkan terhadap kelompok atau populasi. Dalam suatu komunitas, cordon sanitaire dapat dikenakan untuk mencegah infeksi menyebar di luar komunitas tersebut, atau sekuestrasi protektif untuk mencegah infeksi masuk ke dalam komunitas. Otoritas kesehatan masyarakat dapat menerapkan bentuk-bentuk pencegahan lain seperti pembatasan sosial dalam bentuk penutupan sekolah, untuk mengendalikan epidemi.
Imunitas[sunting | sunting sumber]
Sebagian besar patogen yang menginfeksi tidak mengakibatkan kematian inang dan patogen tersebut pada akhirnya akan hilang setelah gejala penyakit berkurang.[15] Proses ini membutuhkan sistem imun untuk membunuh atau menonaktifkan patogen. Kekebalan spesifik yang didapat dari penyakit infeksi dapat dimediasi oleh antibodi dan/atau limfosit T. Kekebalan yang dimediasi oleh dua faktor ini dapat dimanifestasikan oleh:
- efek langsung pada patogen, seperti bakteriolisis yang bergantung pada komplemen yang diprakarsai oleh antibodi, opsonisasi, fagositosis, dan pembunuhan, yang terjadi pada beberapa bakteri,
- netralisasi virus sehingga mereka ini tidak bisa memasuki sel, atau
- kinerja limfosit T, yang akan membunuh sel yang dimasuki oleh mikroorganisme.
Respons sistem imun terhadap mikroorganisme sering kali menyebabkan gejala seperti demam tinggi dan peradangan. Efek ini berpotensi lebih merusak dibandingkan kerusakan langsung yang disebabkan oleh mikrob.[16]
Seseorang dapat menjadi resistan atau kebal terhadap suatu penyakit dengan membawa patogen secara asimtomatik, membawa organisme yang strukturnya serupa (reaksi silang), atau melalui vaksinasi. Patogen primer memberi pengetahuan tentang antigen pelindung dan kekebalan adaptif yang lebih lengkap dibandingkan patogen oportunistik. Fenomena kekebalan kelompok juga bisa tercipta untuk melindungi mereka yang rentan ketika sebagian besar populasi telah kebal dari infeksi tertentu.
Sistem imun mampu melawan patogen apabila jumlah antibodi yang spesifik terhadap antigen dan/atau sel T mencapai tingkat tertentu. Sejumlah individu mengembangkan antibodi alami dalam serumnya meskipun mereka hanya sedikit terpapar atau bahkan sama sekali tidak terpapar antigen. Antibodi alami ini memberikan perlindungan khusus kepada individu dewasa dan secara pasif diturunkan ke bayinya yang baru lahir.
Faktor genetik inang[sunting | sunting sumber]
Organisme yang menjadi target infeksi disebut inang. Dalam parasitologi, mereka yang membawa patogen (khususnya parasit) dalam fase dewasa dan bereproduksi secara seksual disebut inang definitif. Sementara itu, inang perantara merupakan sebutan bagi inang yang menjadi tempat parasit hidup dalam fase larva atau bereproduksi secara aseksual.[36] Pembersihan patogen, baik akibat pengobatan atau terjadi secara spontan, dapat dipengaruhi oleh variasi genetik inang secara individual. Misalnya, infeksi virus hepatitis C genotipe 1 yang diobati dengan peginterferon alfa-2a atau peginterferon alfa-2b yang dikombinasikan dengan ribavirin menunjukkan bahwa polimorfisme genetik di dekat gen IL28B manusia, yang mengode interferon lambda 3, dikaitkan dengan perbedaan yang signifikan dalam pembersihan virus oleh pengobatan. Temuan ini, awalnya menunjukkan bahwa penderita hepatitis C genotipe 1 yang membawa alel varian genetik tertentu di dekat gen IL28B cenderung lebih merespons pengobatan virus dibandingkan orang lain.[37] Laporan berikutnya menunjukkan bahwa varian genetik yang sama juga dikaitkan dengan pembersihan alami untuk virus hepatitis C genotipe 1.[38]
Pengobatan[sunting | sunting sumber]
Obat antiinfeksi dapat menekan infeksi yang menyerang tubuh. Ada beberapa jenis obat antiinfeksi yang luas, tergantung pada jenis organisme yang ditargetkan; obat-obat ini meliputi antibakteri (antibiotik), antivirus, antijamur, dan antiparasitik (termasuk antiprotozoal dan antelmintik). Antibiotik dapat diberikan melalui mulut, injeksi, atau dioleskan, tergantung pada tingkat keparahan dan jenis infeksi. Infeksi berat pada otak biasanya diobati dengan antibiotik intravena. Kadang-kadang, sejumlah antibiotik digunakan bersamaan jika ada resistansi terhadap satu antibiotik. Antibiotik hanya bekerja melawan bakteri dan tidak berefek pada virus. Cara kerja antibiotik yaitu memperlambat multiplikasi bakteri atau membunuh bakteri.
Tidak semua infeksi memerlukan pengobatan. Untuk infeksi yang sembuh sendiri, pengobatan dapat menimbulkan lebih banyak efek samping dibandingkan manfaatnya. Penatalayanan antimikrob merupakan konsep bahwa penyedia layanan kesehatan harus mengobati infeksi dengan antimikrob yang bekerja dengan baik untuk patogen spesifik dalam waktu sesingkat mungkin dan hanya akan mengobati ketika patogen diketahui atau kemungkinan besar terpengaruh oleh pengobatan tersebut.[39]
Epidemiologi[sunting | sunting sumber]


Pada 2010, sekitar 10 juta orang meninggal karena penyakit menular.[41] Organisasi Kesehatan Dunia (WHO) mengumpulkan informasi kematian global berdasarkan kategori kode ICD. Tabel berikut mencantumkan penyakit infeksi teratas berdasarkan jumlah kematian pada tahun 2002. Data tahun 1993 juga ditampilkan sebagai perbandingan.
| Urutan | Penyebab kematian | Kematian pada 2002 (dalam juta) |
Persentase dari seluruh kematian |
Kematian pada 1993 (dalam juta) |
Urutan pada 1993 |
|---|---|---|---|---|---|
| N/A | Semua penyakit infeksi | 14.7 | 25.9% | 16.4 | 32.2% |
| 1 | Infeksi saluran pernapasan bawah[44] | 3,9 | 6,9% | 4,1 | 1 |
| 2 | HIV/AIDS | 2,8 | 4,9% | 0,7 | 7 |
| 3 | Gastroenteritis[45] | 1.8 | 3.2% | 3.0 | 2 |
| 4 | Tuberkulosis (TB) | 1,6 | 2,7% | 2,7 | 3 |
| 5 | Malaria | 1,3 | 2,2% | 2,0 | 4 |
| 6 | Campak | 0,6 | 1,1% | 1,1 | 5 |
| 7 | Batuk rejan | 0,29 | 0,5% | 0,36 | 7 |
| 8 | Tetanus | 0,21 | 0,4% | 0,15 | 12 |
| 9 | Meningitis | 0,17 | 0,3% | 0,25 | 8 |
| 10 | Sifilis | 0,16 | 0,3% | 0,19 | 11 |
| 11 | Hepatitis B | 0.10 | 0,2% | 0,93 | 6 |
| 12-17 | Penyakit tropis (6)[46] | 0.13 | 0.2% | 0.53 | 9, 10, 16–18 |
| Catatan: Penyebab kematian lainnya termasuk kondisi ibu dan perinatal (5,2%), kekurangan nutrisi (0,9%), kondisi tidak menular (58,8%), dan cedera (9,1%). | |||||
Tiga pembunuh teratas adalah HIV/AIDS, tuberkulosis, dan malaria. Meskipun jumlah kematian akibat hampir semua penyakit lain menurun, kematian karena HIV/AIDS telah meningkat empat kali lipat. Penyakit anak-anak termasuk batuk rejan, poliomielitis, difteri, campak, dan tetanus. Anak-anak juga menjadi bagian besar dari kematian saluran pernapasan bawah dan diare. Pada tahun 2012, sekitar 3,1 juta orang telah meninggal karena infeksi saluran pernapasan bawah, menjadikannya penyebab kematian nomor 4 di dunia.[47]
Riwayat pandemi[sunting | sunting sumber]
Pandemi (atau epidemi global) adalah penyakit yang menyerang orang di wilayah geografis yang luas. Beberapa pandemi penting sepanjang sejarah di antaranya:
- Wabah Yustinianus, dari tahun 541 hingga 542, yang menewaskan antara 50–60% populasi Eropa.[48]
- Maut hitam, antara tahun 1347 hingga 1352 yang menewaskan 25 juta penduduk di Eropa selama 5 tahun. Pandemi ini mengurangi populasi dunia lama dari sekitar 450 juta menjadi antara 350–375 juta pada abad ke-14.
- Masuknya variola (cacar), campak, dan tifus ke wilayah Amerika Tengah dan Selatan yang dibawa oleh para penjelajah Eropa sepanjang abad ke-15 dan ke-16 yang membunuh penduduk asli. Antara tahun 1518 hingga 1568, pandemi ini menyebabkan populasi Meksiko turun dari 20 juta menjadi 3 juta.[49]
- Epidemi influenza Eropa pertama yang terjadi antara 1556 hingga 1560, dengan perkiraan tingkat kematian 20%.[49]
- Variola menewaskan sekitar 60 juta penduduk Eropa selama abad ke-18[50] (sekitar 400.000 per tahun).[51] Hingga 30% orang yang terinfeksi (80% di antaranya anak-anak berusia di bawah 5 tahun) akan meninggal karena penyakit ini, dan sepertiga dari yang selamat menjadi buta.[52]
- Pada abad ke-19, tuberkulosis menewaskan sekitar seperempat dari populasi orang dewasa di Eropa;[53] pada tahun 1918, satu dari enam kematian di Prancis masih disebabkan oleh tuberkulosis.
- Pandemi influenza 1918 (flu Spanyol) yang menewaskan 25-50 juta orang (sekitar 2% dari populasi dunia 1,7 miliar).[54] Saat ini, influenza masih membunuh sekitar 250.000 hingga 500.000 di seluruh dunia setiap tahun.
- Pandemi koronavirus 2019–2020 yang masih berlangsung di seluruh dunia.
Penyakit infeksi baru[sunting | sunting sumber]
Pada kebanyakan kasus, mikroorganisme hidup dalam harmoni bersama inangnya dengan hubungan timbal balik atau komensal. Penyakit dapat muncul ketika entitas biologi yang telah lama ada berubah menjadi patogenik atau ketika agen patogenik baru memasuki inang baru. Hal ini diakibatkan oleh dua hal: (1) koevolusi antara parasit dan inang sehingga inang menjadi resistan terhadap parasit atau parasit mengalami peningkatan virulensi yang mengarah ke penyakit imunopatologis, atau (2) pengaruh aktivitas manusia yang memicu perubahan lingkungan dan memunculkan penyakit infeksi baru sehingga patogen menempati relung yang baru. Ketika ini terjadi, jangkauan distribusi patogen yang sebelumnya terbatas akan menjadi semakin luas dan mungkin dapat menginfeksi jenis inang yang baru.[55]
Patogen yang berpindah dari hewan vertebrata ke manusia menimbulkan zoonosis. Sejumlah kegiatan manusia memungkinkan menyebarnya penyakit zoonotik[61] dan penyakit yang ditularkan melalui vektor.[55] Kegiatan tersebut meliputi:
- Perambahan di habitat satwa liar. Pembangunan desa-desa baru dan perumahan di daerah pedesaan memaksa hewan untuk hidup dalam populasi yang padat, dan menciptakan peluang bagi mikrob untuk bermutasi dan muncul di tengah populasi manusia.[56]
- Perubahan dalam pertanian. Pemasukan tumbuhan baru ke suatu wilayah akan menarik hama penyakit baru dan mikrob yang mereka bawa ke komunitas pertanian membuat orang terkena penyakit asing.
- Perusakan hutan hujan. Ketika suatu negara memanfaatkan hutan hujannya dengan membangun jalan melintasi hutan dan membuka lahan untuk permukiman atau usaha komersial, orang-orang bertemu dengan serangga dan hewan lain yang membaawa mikroorganisme yang sebelumnya tidak dikenal.
- Urbanisasi yang tidak terkendali. Pesatnya pertumbuhan kota di banyak negara berkembang cenderung memusatkan sejumlah besar orang ke daerah padat dengan sanitasi yang buruk. Kondisi ini mendorong penularan penyakit infeksi.
- Transportasi modern. Kapal pemumpang dan kapal pengangkut barang sering kali membawa patogen yang tidak diinginkan, yang dapat menyebarkan penyakit ke lokasi yang jauh. Sementara itu, pesawat jet internasional dapat mengantarkan orang yang terinfeksi penyakit ke tempat yang jauh, atau pulang kembali ke rumah mereka, sebelum munculnya gejala penyakit untuk pertama kali.
Teori kuman penyakit[sunting | sunting sumber]
Pada Zaman Klasik, sejarawan Yunani Thukidides (c. 460 - c. 400 SM) adalah orang pertama yang menulis tentang wabah Athena, bahwa penyakit dapat menyebar dari orang yang terinfeksi ke orang lain.[57][58] Dalam bukunya On the Different Types of Fever (c. 175 M), tabib Yunani-Romawi Galen berspekulasi bahwa wabah disebarkan oleh "benih wabah tertentu", yang ada di udara.[59] Dalam teks Sushruta Samhita, dokter India kuno Sushruta berteori: "Kusta, demam, konsumsi, penyakit mata, dan penyakit menular lainnya menyebar dari satu orang ke orang lain melalui penyatuan seksual, kontak fisik, makan bersama, tidur bersama, duduk bersama, dan menggunakan pakaian, karangan bunga, dan pasta yang sama."[60][61] Buku ini ditulis pada sekitar abad keenam SM.[62]
Teori dasar penularan penyakit diajukan oleh dokter Persia Ibnu Sina (dikenal sebagai Avicenna di Eropa) dalam Qanun Kedokteran (1025), yang kemudian menjadi buku teks medis paling otoritatif di Eropa hingga abad ke-16. Dalam Buku IV Qanun tersebut, Ibnu Sina membahas epidemi, menguraikan teori miasma klasik dan berusaha mencampurnya dengan teori penularan awal miliknya sendiri. Ia menyebutkan bahwa seseorang dapat menularkan penyakit kepada orang lain melalui napas, setelah mencatat penularan tuberkulosis, dan menjelaskan metode penularan penyakit melalui air dan debu.[63] Konsep penularan tak kasatmata kemudian dibahas oleh beberapa cendekiawan Islam pada Dinasti Ayyubiyah yang menyebutnya sebagai najis ("zat tidak murni"). Sarjana fikih Ibnu al-Haj al-Abdari (c. 1250–1336), saat membahas makanan dan kebersihan Islam, memberi peringatan tentang bagaimana penyakit dapat mencemari air, makanan, dan pakaian, dan dapat menyebar melalui pasokan air, dan menyiratkan bahwa mungkin penularan diakibatkan oleh partikel yang tak terlihat.[64]
Ketika Maut Hitam mencapai Al-Andalus pada abad ke-14, tabib Arab Ibnu Khatima (c. 1369) dan Ibnu al-Khatib (1313–1374) berhipotesis bahwa penyakit menular disebabkan oleh "tubuh kecil" dan menjelaskan bagaimana mereka dapat ditularkan melalui pakaian, bejana, dan anting-anting.[65] Gagasan penularan menjadi lebih populer di Eropa selama Renaisans, terutama melalui tulisan dokter Italia Girolamo Fracastoro.[66] Antony van Leeuwenhoek (1632–1723) memajukan ilmu mikroskop dengan menjadi orang pertama yang mengamati mikroorganisme dan memungkinkan visualisasi bakteri dengan mudah.
Pada pertengahan abad ke-19, John Snow dan William Budd melakukan pekerjaan penting, yaitu menunjukkan penularan tipus dan kolera melalui air yang terkontaminasi. Keduanya mendapat nama seiring dengan menurunnya epidemi kolera di kota-kota mereka setelah menerapkan langkah-langkah pencegahan kontaminasi air.[67] Louis Pasteur membuktikan tanpa keraguan bahwa penyakit tertentu disebabkan oleh agen infeksi, dan mengembangkan vaksin untuk rabies. Robert Koch menyajikan studi ilmiah tentang penyakit menular dengan dasar ilmiah yang dikenal sebagai postulat Koch. Edward Jenner, Jonas Salk, dan Albert Sabin mengembangkan vaksin yang efektif untuk cacar dan polio. Alexander Fleming menemukan antibiotik pertama di dunia, penisilin, yang kemudian dikembangkan oleh Florey dan Chain. Gerhard Domagk mengembangkan sulfonamida, obat antibakteri sintetis berspektrum luas yang pertama.
Referensi[sunting | sunting sumber]
- ^ Definition of "infection" from several medical dictionaries – Retrieved on 2012-04-03
- ^ Alberto Signore (2013). "About inflammation and infection" (PDF). EJNMMI Research. 8 (3).
- ^ GBD 2013 Mortality and Causes of Death, Collaborators (17 December 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990-2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. 385 (9963): 117–71. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604
 . PMID 25530442.
. PMID 25530442.
- ^ "Infectious Disease, Internal Medicine". Association of American Medical Colleges. Diarsipkan dari versi asli tanggal 2015-02-06. Diakses tanggal 2015-08-20.
Infectious disease is the subspecialty of internal medicine dealing with the diagnosis and treatment of communicable diseases of all types, in all organs, and in all ages of patients.
- ^ Kotra, Lakshmi P. (2007). "Infectious Diseases". xPharm: The Comprehensive Pharmacology Reference (dalam bahasa Inggris). Elsevier. hlm. 1–2. doi:10.1016/b978-008055232-3.60849-9. ISBN 978-0-08-055232-3. PMC 7152327
 .
.
- ^ Bush, Larry M. (Februari 2019). "Overview of Infectious Disease". Merck Manuals Consumer Version. Diakses tanggal 23 April 2020.
- ^ Pearson, Richard D. (Mei 2019). "Overview of Parasitic Infections". Merck Manuals Consumer Version. Diakses tanggal 23 April 2020.
- ^ da Silva, Luiz Jacintho (Desember 1997). "The Etymology of Infection and Infestation". The Pediatric Infectious Disease Journal. 16 (12): 1188. ISSN 0891-3668.
- ^ Kayser, Fritz H; Kurt A Bienz; Johannes Eckert; Rolf M Zinkernagel (2005). Medical microbiology. Stuttgart: Georg Thieme Verlag. hlm. 398. ISBN 978-3-13-131991-3.
- ^ Grinde, Bjørn (2013-10-25). "Herpesviruses: latency and reactivation – viral strategies and host response". Journal of Oral Microbiology. 5: 22766. doi:10.3402/jom.v5i0.22766. ISSN 0901-8328. PMC 3809354
 . PMID 24167660.
. PMID 24167660.
- ^ Elsevier, Dorland's Illustrated Medical Dictionary, Elsevier.
- ^ "Acute infections (MPKB)". mpkb.org. Diakses tanggal 2019-12-09.
- ^ Boldogh, Istvan; Albrecht, Thomas; Porter, David D. (1996), Baron, Samuel, ed., "Persistent Viral Infections", Medical Microbiology (edisi ke-4th), University of Texas Medical Branch at Galveston, ISBN 978-0-9631172-1-2, PMID 21413348, diakses tanggal 2020-01-23
- ^ a b Foster, John (2018). Microbiology. New York: Norton. hlm. 39. ISBN 978-0-393-60257-9.
- ^ a b This section incorporates public domain materials included in the text: Medical Microbiology Fourth Edition: Chapter 8 (1996). Baron, Samuel MD. The University of Texas Medical Branch at Galveston. Medical Microbiology. University of Texas Medical Branch at Galveston. 1996. ISBN 9780963117212. Diarsipkan dari versi asli tanggal June 29, 2009. Diakses tanggal 2013-11-27.
- ^ a b c d e Ryan KJ, Ray CG, ed. (2004). Sherris Medical Microbiology (edisi ke-4th). McGraw Hill. ISBN 978-0-8385-8529-0.
- ^ (Higurea & Pietrangelo 2016)
- ^ Infection Cycle – Retrieved on 2010-01-21 Diarsipkan May 17, 2014, di Wayback Machine.
- ^ Understanding Infectious Diseases Diarsipkan 2009-09-24 di Wayback Machine. Science.Education.Nih.Gov article – Retrieved on 2010-01-21
- ^ Negut, Irina; Grumezescu, Valentina; Grumezescu, Alexandru Mihai (2018-09-18). "Treatment Strategies for Infected Wounds". Molecules : A Journal of Synthetic Chemistry and Natural Product Chemistry. 23 (9): 2392. doi:10.3390/molecules23092392. ISSN 1420-3049. PMC 6225154
 . PMID 30231567.
. PMID 30231567.
- ^ Duerkop, Breck A; Hooper, Lora V (2013-07-01). "Resident viruses and their interactions with the immune system". Nature Immunology (dalam bahasa Inggris). 14 (7): 654–59. doi:10.1038/ni.2614. PMC 3760236
 . PMID 23778792.
. PMID 23778792.
- ^ "Bacterial Pathogenesis at Washington University". StudyBlue. St. Louis. Diakses tanggal 2016-12-02.
- ^ "Print Friendly". www.lifeextension.com. Diarsipkan dari versi asli tanggal 2016-12-02. Diakses tanggal 2016-12-02.
- ^ Reddy M, Gill SS, Wu W, et al. (Feb 2012). "Does this patient have an infection of a chronic wound?". JAMA. 307 (6): 605–11. doi:10.1001/jama.2012.98. PMID 22318282.
- ^ http://www.immunize.org/catg.d/p4215.pdf
- ^ Chronic Infection Information Retrieved on 2010-01-14 Diarsipkan July 22, 2015, di Wayback Machine.
- ^ Intestinal Parasites and Infection Diarsipkan 2010-10-28 di Wayback Machine. fungusfocus.com – Retrieved on 2010-01-21
- ^ "Clinical Infectious Disease – Introduction". www.microbiologybook.org. Diakses tanggal 2017-04-19.
- ^ Pathogens and vectors Diarsipkan 2017-10-05 di Wayback Machine.. MetaPathogen.com.
- ^ Ljubin-Sternak, Suncanica; Mestrovic, Tomislav (2014). "Review: Clamydia trachonmatis and Genital Mycoplasmias: Pathogens with an Impact on Human Reproductive Health". Journal of Pathogens. 2014 (183167): 3. doi:10.1155/2014/183167. PMC 4295611
 . PMID 25614838.
. PMID 25614838.
- ^ Van den Bruel A, Haj-Hassan T, Thompson M, Buntinx F, Mant D (March 2010). "Diagnostic value of clinical features at presentation to identify serious infection in children in developed countries: a systematic review". Lancet. 375 (9717): 834–45. doi:10.1016/S0140-6736(09)62000-6. PMID 20132979.
- ^ Bloomfield SF, Aiello AE, Cookson B, O'Boyle C, Larson EL (2007). "The effectiveness of hand hygiene procedures including hand-washing and alcohol-based hand sanitizers in reducing the risks of infections in home and community settings". American Journal of Infection Control. 35 (10): S27–S64. doi:10.1016/j.ajic.2007.07.001. PMC 7115270
 .
.
- ^ ""Generalized Infectious Cycle" Diagram Illustration". science.education.nih.gov. Diarsipkan dari versi asli tanggal 2009-09-24. Diakses tanggal 2010-01-21.
- ^ Watts, Duncan (2003). Six degrees: the science of a connected age
 . London: William Heinemann. ISBN 978-0-393-04142-2.
. London: William Heinemann. ISBN 978-0-393-04142-2.
- ^ Preston, Richard (1995). The hot zone. Garden City, N.Y.: Anchor Books. ISBN 978-0-385-49522-6.
- ^ Barreto ML, Teixeira MG, Carmo EH (2006). "Infectious diseases epidemiology". Journal of Epidemiology and Community Health. 60 (3): 192–95. doi:10.1136/jech.2003.011593. PMC 2465549
 . PMID 16476746.
. PMID 16476746.
- ^ Ge D, Fellay J, Thompson AJ, Simon JS, Shianna KV, Urban TJ, Heinzen EL, Qiu P, Bertelsen AH, Muir AJ, Sulkowski M, McHutchison JG, Goldstein DB (2009). "Genetic variation in IL28B predicts hepatitis C treatment-induced viral clearance". Nature. 461 (7262): 399–401. Bibcode:2009Natur.461..399G. doi:10.1038/nature08309. PMID 19684573.
- ^ Thomas DL, Thio CL, Martin MP, Qi Y, Ge D, O'Huigin C, Kidd J, Kidd K, Khakoo SI, Alexander G, Goedert JJ, Kirk GD, Donfield SM, Rosen HR, Tobler LH, Busch MP, McHutchison JG, Goldstein DB, Carrington M (2009). "Genetic variation in IL28B and spontaneous clearance of hepatitis C virus". Nature. 461 (7265): 798–801. Bibcode:2009Natur.461..798T. doi:10.1038/nature08463. PMC 3172006
 . PMID 19759533.
. PMID 19759533.
- ^ O'Brien, Deirdre J.; Gould, Ian M. (August 2013). "Maximizing the impact of antimicrobial stewardship". Current Opinion in Infectious Diseases. 26 (4): 352–58. doi:10.1097/QCO.0b013e3283631046. PMID 23806898.
- ^ World Health Organization (February 2009). "Age-standardized DALYs per 100,000 by cause, and Member State, 2004".
- ^ "Could Ebola rank among the deadliest communicable diseases?". CBC News. 20 October 2014.
- ^ "The World Health Report (Annex Table 2)" (PDF). 2004.
- ^ "Table 5" (PDF). 1995.
- ^ Infeksi saluran pernapasan bawah meliputi berbagai pneumonia, influenza, dan bronkitis akut.
- ^ Gastroenteritis atau diare diakibatkan oleh berbagai organisme yang berbeda, seperti kolera, botulisme, dan E. coli.
- ^ Penyakit tropis di antaranya penyakit Chagas, demam berdarah, filariasis limfatik, leismaniasis, onchocerciasis, schistosomiasis dan tripanosomiasis.
- ^ "WHO | The top 10 causes of death". WHO. Diakses tanggal 2015-09-24.
- ^ "Infectious and Epidemic Disease in History" Diarsipkan July 12, 2012, di Archive.is
- ^ a b Dobson AP, Carter ER (1996). "Infectious Diseases and Human Population History" (PDF). BioScience. 46 (2): 115–26. doi:10.2307/1312814. JSTOR 1312814.
- ^ "Smallpox". North Carolina Digital History.
- ^ Smallpox and Vaccinia. National Center for Biotechnology Information. Diarsipkan June 1, 2009, di Wayback Machine.
- ^ Barquet, Nicolau (15 October 1997). "Smallpox: The Triumph over the Most Terrible of the Ministers of Death". Annals of Internal Medicine. 127 (8_Part_1): 635–42. doi:10.7326/0003-4819-127-8_Part_1-199710150-00010. PMID 9341063.
- ^ Multidrug-Resistant "Tuberculosis". Centers for Disease Control and Prevention. Diarsipkan March 9, 2010, di Wayback Machine.
- ^ "Influenza of 1918 (Spanish Flu) and the US Navy". 20 February 2006. Diarsipkan dari versi asli tanggal 20 February 2006.
- ^ a b Krauss H, Weber A, Appel M (2003). Zoonoses: Infectious Diseases Transmissible from Animals to Humans (edisi ke-3rd). Washington, D.C.: ASM Press. ISBN 978-1-55581-236-2.
- ^ Peter Daszak; Andrew A. Cunningham; Alex D. Hyatt (27 January 2000). "Emerging Infectious Diseases of Wildlife—Threats to Biodiversity and Human Health". Science. 287 (5452): 443–49. Bibcode:2000Sci...287..443D. doi:10.1126/science.287.5452.443. PMID 10642539.
- ^ Singer, Charles and Dorothea (1917) "The scientific position of Girolamo Fracastoro [1478?–1553] with especial reference to the source, character and influence of his theory of infection," Annals of Medical History, 1 : 1–34; see p. 14.
- ^ Thucydides with Richard Crawley, trans., History of the Peloponnesian War (London, England: J.M. Dent & Sons, Ltd., 1910), Book III, § 51, pp. 131–32. From pp. 131–32.
- ^ Nutton, Vivian (1983) "The seeds of disease: an explanation of contagion and infection from the Greeks to the Renaissance," Medical History, 27 (1) : 1–34; see p. 10. Available at: U.S. National Library of Medicine, National Institutes of Health
- ^ Rastogi, Nalin; Rastogi, R (1985-01-01). "Leprosy in ancient India". International journal of leprosy and other mycobacterial diseases : official organ of the International Leprosy Association. 52: 541–3.
- ^ Susruta; Bhishagratna, Kunja Lal (1907–1916). An English translation of the Sushruta samhita, based on original Sanskrit text. Edited and published by Kaviraj Kunja Lal Bhishagratna. With a full and comprehensive introd., translation of different readings, notes, comperative views, index, glossary and plates. Gerstein - University of Toronto. Calcutta.
- ^ Hoernle, A. F. Rudolf (August Friedrich Rudolf) (1907). Studies in the medicine of ancient India. Gerstein - University of Toronto. Oxford : At the Clarendon Press.
- ^ Byrne, Joseph Patrick (2012). Encyclopedia of the Black Death. ABC-CLIO. hlm. 29. ISBN 9781598842531.
- ^ Reid, Megan H. (2013). Law and Piety in Medieval Islam. Cambridge University Press. hlm. 106, 114, 189–190. ISBN 9781107067110.
- ^ Majeed, Azeem (22 December 2005). "How Islam changed medicine". BMJ. 331 (7531): 1486–1487. doi:10.1136/bmj.331.7531.1486. ISSN 0959-8138. PMC 1322233
 . PMID 16373721.
. PMID 16373721.
- ^ Beretta M (2003). "The revival of Lucretian atomism and contagious diseases during the renaissance". Medicina Nei Secoli. 15 (2): 129–54. PMID 15309812.
- ^ Moorhead Robert (November 2002). "William Budd and typhoid fever". J R Soc Med. 95 (11): 561–64. doi:10.1258/jrsm.95.11.561. PMC 1279260
 . PMID 12411628.
. PMID 12411628.
Pranala luar[sunting | sunting sumber]
| Klasifikasi |
|---|
- European Center for Disease Prevention and Control
- U.S. Centers for Disease Control and Prevention,
- Infectious Disease Society of America (IDSA)
- Infectious Disease Index of the Public Health Agency of Canada (PHAC)
- Vaccine Research Center Information concerning vaccine research clinical trials for Emerging and re-Emerging Infectious Diseases.
- Infection Information Resource
- Microbes & Infection (journal)
- Knowledge source for Health Care Professionals involved in Wound management[pranala nonaktif permanen] www.woundsite.info
- Table: Global deaths from communicable diseases, 2010 – Canadian Broadcasting Corp.
