Tuberkulosis
Artikel ini memberikan informasi dasar tentang topik kesehatan. |
| Tuberkulosis | |
|---|---|
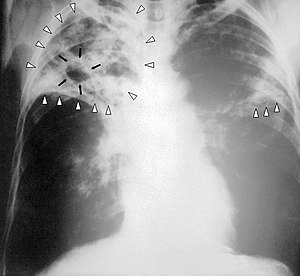 | |
| Hasil Sinar-X dada seorang penderita Tuberkulosis tingkat lanjut. Panah putih menunjukkan adanya infeksi pada kedua belah paru-paru. Panah hitam menunjukkan adanya lubang yang sudah terbentuk. | |
| Informasi umum | |
| Spesialisasi | Penyakit menular, Pulmonologi |
| Penyebab | Mycobacterium tuberculosis[1] |
| Faktor risiko | Merokok, HIV/AIDS[1] |
| Aspek klinis | |
| Gejala dan tanda | Batuk kronis, demam, hemoptisis, berat badan turun[1] |
| Diagnosis | Radiograf dada, kultur, tes Mantoux, IGRA[1] |
| Kondisi serupa | Pneumonia, histoplasmosis, sarcoidosis, kokidioidomikosis[2] |
| Tata laksana | |
| Pencegahan | Skrining bagi orang-orang dengan risiko tinggi TB, pengobatan pasien-pasien TB, vaksinasi dengan basil Calmette-Guérin (BCG)[3][4][5] |
| Perawatan | Antibiotik[1] |
| Distribusi dan frekuensi | |
| Prevalensi | 25% populasi dunia (TB laten)[6] |
| Kematian | 1.3 juta orang (2022)[6] |
Tuberkulosis (Tuberculosis, disingkat Tbc), atau Tb (singkatan dari "Tubercle bacillus") atau kematus[7]merupakan penyakit menular yang umum, dan dalam banyak kasus bersifat mematikan. Penyakit ini disebabkan oleh berbagai strain mikobakteria, umumnya Mycobacterium tuberculosis (disingkat "MTb" atau "MTbc").[8] Tuberkulosis biasanya menyerang paru-paru, tetapi juga bisa berdampak pada bagian tubuh lainnya. Tuberkulosis menyebar melalui udara ketika seseorang dengan infeksi TB aktif batuk, bersin, atau menyebarkan butiran ludah mereka melalui udara.[9]
Infeksi TB sebagian besar bersifat tanpa gejala dan laten (sering disebut TB laten). Namun, satu dari sepuluh kasus infeksi laten berkembang menjadi penyakit aktif (TB aktif). Bila tuberkulosis tidak diobati, maka lebih dari 50% orang yang terinfeksi bisa meninggal. Sebelum ditemukannya antibiotik yang ampuh untuk menangani TB (sekitar tahun 1900 awal) diperkirakan 1 dari 7 orang di dunia meninggal karena penyakit ini.
Gejala klasik infeksi TB aktif yaitu batuk kronis dengan bercak darah pada sputum atau dahak, demam, berkeringat di malam hari, dan berat badan turun. (dahulu TB disebut penyakit "konsumsi" karena orang-orang yang terinfeksi biasanya mengalami kemerosotan berat badan). Infeksi pada organ lain menimbulkan gejala yang bermacam-macam. Diagnosis TB aktif bergantung pada hasil radiologi (biasanya melalui rontgen dada) serta pemeriksaan fisik dan dilakukan kultur mikrobiologis. Sementara itu, diagnosis TB laten bergantung pada tes tuberkulin kulit/tuberculin skin test (TST) dan tes darah (IGRA). Pengobatan TB aktif memerlukan pemberian beberapa antibiotik secara teratur dalam jangka waktu 6 sampai 12 bulan. Orang-orang yang melakukan kontak juga harus menjalani tes penapisan dan diobati bila perlu. Dengan perkembangan antibiotik yang ada saat ini pengobatan TB yang dilakukan dengan baik akan memberkan tingkat kesembuhan diatas 90 %.
Namun, apabila pengobatan tidak dilakukan dengan teratur dan dengan jangka waktu yang diperlukan, bakteri TB tersebut bisa kembali kambuh dan beradaptasi menjadi resisten terhadap antibiotik. Resistansi antibiotik merupakan masalah yang besar pada penanganan epidemi TB. Infeksi tuberkulosis resisten multi-obat (atau sering disebut TB MDR) memerlukan pengobatan yang jauh lebih berat dengan dosis obat yang jauh lebih tinggi dan tingkat kesembuhan yang jauh lebih rendah. Untuk mencegah TB, semua orang harus menjalani tes penapisan penyakit tersebut dan mendapatkan vaksinasi basil Calmette–Guérin.
Epidemiologi[sunting | sunting sumber]
TB kini menjadi penyebab kematian nomor dua setelah pandemi Covid-19 akibat penyakit menular pada tahun 2022. Setelah terjadi tren penurunan angka orang yang menderita TB secara global dari tahun 2010, angka ini kembali menaik sejak tahun 2020 ketika pandemi Covid-19 dimulai. Sekitar 10,6 juta orang menderita TB dengan angka kasus TB baru yang dilaporkan adalah sebesar 7,5 juta pada tahun 2022. Angka ini merupakan angka terbesar sejak 1995 yang kemungkinan berasal dari orang-orang yang memiliki TB di tahun-tahun sebelumnya selama pandemi Covid-19 yang menyebabkan terhambatnya penemuan kasus, diagnosis, dan pengobatan TB.
Walaupun demikian, dampak lain dari adanya pandemi Covid-19 adalah penurunan angka kematian TB dengan adanya PPKM yang membatasi transmisi TB pada tahun 2020 dan 2021. Pada tahun 2022, angka kematian global akibat TB (termasuk orang dengan HIV) adalah sebesar 1,30 juta yang dikatakan menurun dibandingkan tahun 2020 dan 2021. Mayoritas orang yang meninggal akibat TB adalah orang yang negatif-HIV (sekitar 1,13 juta), sementara diperkirakan terdapat 167.000 kematian pada ODHA dengan TB.
Di samping itu, diperkirakan sebanyak 410.000 orang yang terinfeksi TB termasuk ke dalam golongan TB resisten multiobat (TB-MDR) atau TB resisten rifampisin (TB-RR) pada tahun 2022. Sementara orang yang menerima pengobatan jauh lebih kecil, yaitu sekitar 175.650 orang.
Dari segi geografis, daerah dengan kasus TB paling tinggi berada di Asia Tenggara (46%) diikuti Afrika (23%), Pasifik Barat (18%), diikuti Mediterania Timur (8,1%), Amerika (3,1%), dan Eropa (2,2%). Tingginya angka kasus TB di Asia Tenggara kemungkinan disebabkan oleh tiga negara yang tergolong ke dalam tiga puluh negara dengan beban kasus TB tertinggi, yaitu Indonesia (beban kasus TB tertinggi kedua, sebesar 10% kasus global), Filipina (beban kasus TB tertinggi keempat, sebesar 7,0% kasus), dan Myanmar. Selain itu, ketiga negara ini juga berperan dalam peningkatan kasus TB global tertinggi dengan penambahan 0,4 juta kasus pada tahun 2022.[10]
Situasi Tuberkulosis di Indonesia[sunting | sunting sumber]
Indonesia (10%) termasuk ke dalam negara kedua dari tiga puluh negara dengan beban kasus TB global tertinggi didahului India (27%) dan diikuti Tiongkok (7,1%), Filipina (7,0%), Pakistan (5,7%), Nigeria (4,5%), Bangladesh (3,6%), dan Republik Demokratik Kongo (3,0%).[10]
Berdasarkan Profil Kesehatan Indonesia tahun 2022, jumlah semua kasus TB yang ditemukan adalah sebanyak 677.464 kasus. Angka ini meningkat dengan cukup tinggi bila dibandingkan dengan laporan pada Profil Kesehatan Indonesia tahun 2022 dan 2020 berturut-turut, dengan temuan sebanyak 397.377 dan 351.936 kasus.[11]
Di Indonesia, kasus tuberkulosis tertinggi ditemukan di daerah-daerah dengan jumlah penduduk yang banyak, yaitu Jawa Barat, Jawa Timur, dan Jawa Tengah. Jumlah kasus tuberkulosis dari ketiga provinsi tersebut mencapai 44% dari seluruh kasus yang ditemukan di Indonesia.[12]
Jika ditinjau dari jenis kelamin, kasus tuberkulosis lebih banyak ditemukan pada laki-laki dibandingkan dengan perempuan yaitu 58,0% laki-laki dan 42,0% perempuan. Sedangkan, jika dilihat dari usia, pada tahun 2021 kasus tuberkulosis banyak ditemukan pada usia produktif, yaitu rentang usia 45—54 tahun sebanyak 16,8% diikuti rentang usia 25—34 tahun dan 55—64 tahun dengan masing-masing sebanyak 15%.[11]
Tanda dan gejala[sunting | sunting sumber]
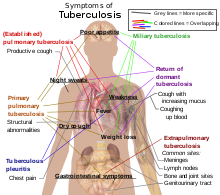
Dari kelompok yang bukan pengidap HIV namun kemudian terinfeksi tuberkulosis, 5-10% di antaranya menunjukkan perkembangan penyakit aktif selama masa hidup mereka.[14] Sebaliknya, dari kelompok yang terinfeksi HIV dan juga terinfeksi tuberkulosis, ada 30% yang menunjukkan perkembangan penyakit aktif.[14] Tuberkulosis dapat menginfeksi bagian tubuh mana saja, tapi paling sering menginfeksi paru-paru (dikenal sebagai tuberkulosis paru).[15] Bila tuberkulosis berkembang di luar paru-paru, maka disebut TB ekstra paru. TB ekstra paru juga bisa timbul bersamaan dengan TB paru.[15] Tanda dan gejala umumnya antara lain demam, menggigil, berkeringat di malam hari, hilangnya nafsu makan, berat badan turun, dan lesu.[15] Dapat pula terjadi jari tabuh yang signifikan.[14]
Tuberkulosis paru[sunting | sunting sumber]
Bila infeksi tuberkulosis yang timbul menjadi aktif, sekitar 90%-nya selalu melibatkan paru-paru.[16][17] Gejala-gejalanya antara lain berupa nyeri dada dan batuk berdahak yang berkepanjangan. Sekitar 25% penderita tidak menunjukkan gejala apapun (yang demikian disebut "asimptomatik").[16] Kadang kala, penderita mengalami sedikit batuk darah. Dalam kasus-kasus tertentu yang jarang terjadi, infeksi bisa mengikis ke dalam arteri pulmonalis, dan menyebabkan pendarahan parah yang disebut aneurisma Rasmussen. Tuberkulosis juga bisa berkembang menjadi penyakit kronis dan menyebabkan luka parut luas di bagian lobus atas paru-paru. Paru-paru atas paling sering terinfeksi.[15] Alasannya belum begitu jelas.[8] Kemungkinan karena paru-paru atas lebih banyak mendapatkan aliran udara[8] atau bisa juga karena drainase limfa yang kurang baik pada paru bagian atas.[15]
Tuberkulosis ekstra paru[sunting | sunting sumber]
Dalam 15–20% kasus aktif, terjadi penyebaran infeksi hingga ke luar organ pernapasan dan menyebabkan tuberkulosis jenis lainnya.[18] Tuberkulosis yang terjadi di luar organ pernapasan disebut "tuberkulosis ekstra paru".[19] TB ekstra paru umumnya terjadi pada orang dewasa dengan imunosupresi dan anak-anak. TB ekstra paru muncul pada 50% lebih kelompok pengidap HIV.[19] Lokasi TB ekstra paru yang bermakna termasuk: pleura (pada TB pleuritis), sistem saraf pusat (pada meningitisTB), dan sistem kelenjar getah bening (pada skrofuloderma leher). TB ekstra paru juga dapat terjadi di sistem urogenital (yaitu pada tuberkulosis urogenital) dan pada tulang dan persendian (yaitu pada penyakit Pott tulang belakang). Bila TB menyebar ke tulang maka dapat disebut "TB tulang",[20] yang merupakan salah satu bentuk osteomielitis.[8] Ada lagi TB yang lebih serius yaitu TB yang menyebar luas dan disebut sebagai TB diseminata, atau biasanya dikenal dengan nama tuberkulosis milier.[15] Di antara kasus TB ekstra paru, 10%-nya biasanya merupakan TB milier.[21]
Etiologi (penyebab) dan Faktor Risiko[sunting | sunting sumber]
Mikobakteria[sunting | sunting sumber]

Penyebab utama penyakit TB adalah Mycobacterium tuberculosis, yaitu sejenis basil aerobik kecil yang non-motil.[15] Berbagai karakter klinis unik patogen ini disebabkan oleh tingginya kandungan lipid yang dimilikinya.[22] Sel-selnya membelah setiap 16 –20 jam. Kecepatan pembelahan ini termasuk lambat bila dibandingkan dengan jenis bakteri lain yang umumnya membelah setiap kurang dari satu jam.[23] Mikobakteria memiliki lapisan ganda membran luar lipid.[24] Bila dilakukan uji pewarnaan Gram, maka MTB akan menunjukkan pewarnaan "Gram-positif" yang lemah atau tidak menunjukkan warna sama sekali karena kandungan lemak dan asam mikolat yang tinggi pada dinding selnya.[25] MTB bisa tahan terhadap berbagai disinfektan lemah dan dapat bertahan hidup dalam kondisi kering selama berminggu-minggu. Di alam, bakteri hanya dapat berkembang dalam sel inang organisme tertentu, tetapi M. tuberculosis bisa dikultur di laboratorium.[26]
Dengan menggunakan pewarnaan histologis pada sampel dahak yang diekspektorat, peneliti dapat mengidentifikasi MTB melalui mikroskop (dengan pencahayaan) biasa. (Dahak juga disebut "sputum"). MTB mempertahankan warna meskipun sudah diberi perlakukan larutan asam, sehingga dapat digolongkan sebagai Basil Tahan Asam (BTA).[8][25] Dua jenis teknik pewarnaan asam yang paling umum yaitu: teknik pewarnaan Ziehl-Neelsen, yang akan memberi warna merah terang pada bakteri BTA bila diletakkan pada latar biru,[27] dan teknik pewarnaan auramin-rhodamin lalu dilihat dengan mikroskop fluoresen.[28]
Kompleks M. tuberculosis (KMTB) juga termasuk mikobakteria lain yang juga menjadi penyebab TB: M. bovis, M. africanum, M. canetti, dan M. microti.[29] M. africanum tidak menyebar luas, tetapi merupakan penyebab penting Tuberkulosis di sebagian wilayah Afrika.[30][31] M. bovis merupakan penyebab umum Tuberkulosis, tetapi pengenalan susu pasteurisasi telah berhasil memusnahkan jenis mikobakterium yang selama ini menjadi masalah kesehatan masyarakat di negara-negara berkembang ini.[8][32] M. canetti merupakan jenis langka dan sepertinya hanya ada di kawasan Tanduk Afrika, meskipun beberapa kasus pernah ditemukan pada kelompok emigran Afrika.[33][34] M. microti juga merupakan jenis langka dan sering kali ditemukan pada penderita yang mengalami imunodefisiensi, meski demikian, patogen ini kemungkinan bisa bersifat lebih umum dari yang kita bayangkan.[35]
Mikobakteria patogen lain yang juga sudah dikenal antara lain M. leprae, M. avium, dan M. kansasii. Dua jenis terakhir masuk dalam klasifikasi "Mikobakteria non-tuberkulosis" (MNT). MNT tidak menyebabkan TB atau lepra, tetapi menyebabkan penyakit paru-paru lain yang mirip TB.[36]
Faktor risiko[sunting | sunting sumber]
Ada beberapa faktor yang menjadi penyebab mengapa orang lebih rentan terhadap infeksi TB. Di tingkat global, faktor risiko paling penting adalah HIV; 13% dari seluruh kasus TB ternyata terinfeksi juga oleh virus HIV.[37] Masalah ini umum ditemukan di kawasan sub-Sahara Afrika, yang angka HIV-nya tinggi.[38][39] Tuberkulosis terkait erat dengan kepadatan penduduk yang berlebihan serta gizi buruk. Keterkaitan ini menjadikan TB sebagai salah satu penyakit kemiskinan utama.[16] Orang-orang yang memiliki risiko tinggi terinfeksi TB antara lain: orang yang menyuntik obat terlarang, penghuni dan karyawan tempat-tempat berkumpulnya orang-orang rentan (misalnya, penjara dan tempat penampungan gelandangan), orang-orang miskin yang tidak memiliki akses perawatan kesehatan yang memadai, minoritas suku yang berisiko tinggi, dan para pekerja kesehatan yang melayani orang-orang tersebut.[40] Penyakit paru-paru kronis adalah faktor risiko penting lainnya. Silikosis meningkatkan risiko hingga 30 kali lebih besar.[41] Orang-orang yang merokok memiliki risiko dua kali lebih besar terkena TB dibandingkan yang tidak merokok.[42] Adanya penyakit tertentu juga dapat meningkatkan risiko berkembangnya Tuberkulosis, antara lain alkoholisme[16] dan diabetes mellitus (risikonya tiga kali lipat).[43] Obat-obatan tertentu, seperti kortikosteroid dan infliximab (antibodi monoklonal anti-αTNF) juga merupakan faktor risiko yang semakin penting, terutama di kawasan dunia berkembang.[16] Meskipun kerentanan genetik[44] juga bisa berpengaruh, tetapi para peneliti belum menjelaskan sampai sejauh mana peranannya.[16]
Mekanisme[sunting | sunting sumber]

Penularan[sunting | sunting sumber]
Ketika seseorang yang mengidap TB paru aktif batuk, bersin, bicara, menyanyi, atau meludah, mereka sedang menyemprotkan titis-titis aerosol infeksius dengan diameter 0.5 hingga 5 µm. Bersin dapat melepaskan partikel kecil-kecil hingga 40,000 titis.[45] Tiap titis bisa menularkan penyakit Tuberkulosis karena dosis infeksius penyakit ini sangat rendah. (Seseorang yang menghirup kurang dari 10 bakteri saja bisa langsung terinfeksi).[46]
Orang-orang yang melakukan kontak dalam waktu lama, dalam frekuensi sering, atau selalu berdekatan dengan penderita TB, berisiko tinggi ikut terinfeksi, dengan perkiraan angka infeksi sekitar 22%.[47] Seseorang dengan Tuberkulosis aktif dan tidak mendapatkan perawatan dapat menginfeksi 10-15 (atau lebih) orang lain setiap tahun.[48] Biasanya, hanya mereka yang menderita TB aktif yang dapat menularkan penyakit ini. Orang-orang dengan infeksi laten diyakini tidak menularkan penyakitnya.[8] Kemungkinan penyakit ini menular dari satu orang ke orang lain tergantung pada beberapa faktor. Faktor-faktor tersebut antara lain jumlah titis infeksius yang disemprotkan oleh pembawa, efektivitas ventilasi lingkungan tempat tinggal, jangka waktu paparan, tingkat virulensi strain M. tuberculosis, dan tingkat kekebalan tubuh orang yang tidak terinfeksi.[49] Untuk mencegah penyebaran berlapis dari satu orang ke orang lainnya, pisahkan orang-orang dengan TB aktif ("nyata") dan masukkan mereka dalam rejimen obat anti-TB. Setelah kira-kira dua minggu perawatan efektif, orang-orang dengan infeksi aktif yang non-resisten biasanya sudah tidak menularkan penyakitnya ke orang lain.[47] Bila ternyata kemudian ada yang terinfeksi, biasanya perlu waktu tiga sampai empat minggu hingga orang yang baru terinfeksi itu menjadi cukup infeksius untuk menularkan penyakit tersebut ke orang lain.[50]
Patogenesis[sunting | sunting sumber]
Sekitar 90% orang yang terinfeksi M. tuberculosis mengidap infeksi TB laten yang bersifat asimtomatik, (kadang disebut LTBI/Latent TB Infections).[51] Seumur hidup, orang-orang ini hanya memiliki 10% peluang infeksi latennya berkembang menjadi penyakit Tuberkulosis aktif yang nyata.[52] Risiko TB pada pengidap HIV untuk berkembang menjadi penyakit aktif meningkat sekitar 10% setiap tahunnya.[52] Bila tidak diberi pengobatan yang efektif, maka angka kematian TB aktif bisa mencapai lebih dari 66%.[48]
Infeksi TB bermula ketika mikobakteria masuk ke dalam alveoli paru, lalu menginvasi dan bereplikasi di dalam endosom makrofag alveolus.[8][53] Lokasi primer infeksi di dalam paru-paru yang dikenal dengan nama "fokus Ghon", terletak di bagian atas lobus bawah, atau di bagian bawah lobus atas.[8] Tuberkulosis paru dapat juga terjadi melalui infeksi aliran darah yang dikenal dengan nama fokus Simon. Infeksi fokus Simon biasanya ditemukan di bagian atas paru-paru.[54] Penularan hematogen (melalui pembuluh darah) ini juga dapat menyebar ke lokasi-lokasi lain seperti nodus limfa perifer, ginjal, otak dan tulang.[8][55] Tuberkulosis berdampak pada seluruh bagian tubuh, meskipun belum diketahui kenapa penyakit ini jarang sekali menyerang jantung, otot skeletal, pankreas, atau tiroid.[56]
Tuberkulosis digolongkan sebagai salah satu penyakit yang menyebabkan radang granulomatosa. Sel-sel seperti makrofag, limfosit T, limfosit B, dan fibroblast saling bergabung membentuk granuloma. Limfosit mengepung makrofag-makrofag yang terinfeksi. Granuloma mencegah penyebaran mikobakteria dan menyediakan lingkungan khusus bagi interaksi sel-sel lokal di dalam sistem kekebalan tubuh. Bakteri yang berada di dalam granuloma menjadi dorman lalu menjadi sumber infeksi laten. Ciri khas lain granuloma adalah membentuk kematian sel abnormal (nekrosis) di pusat tuberkel. Dilihat dengan mata telanjang, nekrosis memiliki tekstur halus, berwarna putih keju dan disebut nekrosis kaseosa.[57]
Bakteri TB bisa masuk ke dalam aliran darah dari area jaringan yang rusak itu. Bakteri-bakteri tersebut kemudian menyebar ke seluruh tubuh dan membentuk banyak fokus-fokus infeksi, yang tampak sebagai tuberkel kecil berwarna putih di dalam jaringan.[58] Penyakit TB yang sangat parah ini disebut tuberkulosis milier. Jenis TB ini paling umum terjadi pada anak-anak dan penderita HIV.[59] Angka fatalitas orang yang mengidap TB diseminata seperti ini cukup tinggi meskipun sudah mendapatkan pengobatan (sekitar 30%).[21][60]
Pada banyak orang, infeksi ini sering hilang timbul. Perusakan jaringan dan nekrosis sering kali seimbang dengan kecepatan penyembuhan dan fibrosis.[57] Jaringan yang terinfeksi berubah menjadi parut dan lubang-lubangnya terisi dengan material nekrotik kaseosa tersebut. Selama masa aktif penyakit, beberapa lubang ini ikut masuk ke dalam saluran udara bronkus dan material nekrosis tadi bisa terbatukkan. Material ini mengandung bakteri hidup dan dapat menyebarkan infeksi. Pengobatan menggunakan antibiotik yang sesuai dapat membunuh bakteri-bekteri tersebut dan memberi jalan bagi proses penyembuhan. Saat penyakit sudah sembuh, area yang terinfeksi berubah menjadi jaringan parut.[57]
Diagnosis[sunting | sunting sumber]
Tuberkulosis aktif[sunting | sunting sumber]
Sangat sulit mendiagnosis Tuberkulosis aktif hanya berdasarkan tanda-tanda dan gejala saja.[61] Sulit juga mendiagnosis penyakit ini pada orang-orang dengan imunosupresi.[62] Meski demikian, orang-orang yang menunjukkan tanda-tanda bahwa mereka memiliki penyakit paru-paru atau gejala konstitusional yang berlangsung lebih dari dua minggu maka bisa jadi orang tersebut tertular TB.[62] Gambar sinar-X dada dan pembuatan beberapa kultur sputum untuk basil tahan asam biasanya menjadi salah satu bagian evaluasi awal.[62] Uji pelepasan interferon-γ (IGRAs) dan tes kulit tuberkulin tidak optimal diterapkan di dunia berkembang.[63][64] IGRA memiliki kelemahan yang serupa bila diterapkan pada penderita HIV.[64][65]
Diagnosis yang tepat untuk TB dilakukan ketika bakteri “M. tuberculosis” ditemukan dalam sampel klinis (misalnya, dahak, nanah, atau biopsi jaringan). Namun, proses kultur organisme yang lambat pertumbuhannya ini membutuhkan waktu dua hingga enam minggu untuk kultur darah dan dahak saja.[66] Oleh karena itu, pengobatan sering kali dilakukan sebelum hasil kultur selesai.[67]
Tes amplifikasi asam nukleat dan uji adenosin deaminase dapat lebih cepat mendiagnosis TB.[61] Meski demikian, tes ini tidak direkomendasikan secara rutin karena jarang sekali mengubah cara pengobatan penderita.[67] Tes darah untuk mendeteksi antibodi tidak begitu spesifik atau sensitif, sehingga tes ini juga tidak direkomendasikan.[68]
Tuberkulosis laten[sunting | sunting sumber]

Tes kulit tuberkulin Mantoux sering digunakan sebagai penapisan bagi seseorang dengan risiko TB tinggi.[62] Orang yang pernah diimunisasi sebelumnya dapat memberikan hasil tes positif yang palsu.[69] Hasil tes dapat memberikan negatif palsu pada orang yang menderita sarkoidosis, Limfoma Hodgkin, dan malagizi. Yang terpenting, hasil tes dapat negatif palsu pada orang yang menderita tuberkulosis aktif.[8] Interferon gamma release assays (IGRAs) untuk sampel darah direkomendasikan pada orang dengan hasil tes Mantoux positif.[67] IGRAs tidak dipengaruhi oleh imunisasi ataupun sebagian besar mikobakteri dari lingkungan, sehingga mereka memunculkan hasil tes positif palsu yang lebih sedikit.[70] Bagaimanapun mereka dipengaruhi oleh “M. szulgai,” “M. marinum,” and “M. kansasii.”[71] IGRAs dapat meningkatkan sensitivitas bila digunakan sebagai tes tambahan selain tes kulit. Tetapi IGRAs menjadi kurang sensitif dibandingkan tes kulit apabila digunakan sendirian.[72]
Pencegahan[sunting | sunting sumber]
Usaha untuk mencegah dan mengontrol tuberkulosis bergantung pada vaksinasi bayi dan deteksi serta perawatan untuk kasus aktif.[16] The World Health Organization (WHO) telah berhasil mencapai sejumlah keberhasilan dengan regimen pengobatan yang dimprovisasi, dan sudah terdapat penurunan kecil dalam jumlah kasus.[16]
Vaksin[sunting | sunting sumber]
Sejak tahun 2011, satu-satunya vaksin yang tersedia adalah basil Calmette–Guérin (BCG). Walaupun BCG efektif melawan penyakit yang menyebar pada masa kanak-kanak, masih terdapat perlindungan yang inkonsisten terhadap TB paru.[73] Namun, ini adalah vaksin yang paling umum digunakan di dunia, dengan lebih dari 90% anak-anak yang mendapat vaksinasi.[16] Bagaimanapun, imunitas yang ditimbulkan akan berkurang setelah kurang lebih sepuluh tahun.[16] Tuberkulosis tidak umum di sebagian besar Kanada, Inggris Raya, dan Amerika Serikat, jadi BCG hanya diberikan kepada orang dengan risiko tinggi.[74][75][76] Satu alasan vaksin ini tidak digunakan adalah karena vaksin ini menyebabkan tes kulit tuberkulin memberikan positif palsu, sehingga tes ini tidak membantu dalam penyaringan penyakit.[76] Jenis vaksin baru masih sedang dikembangkan.[16]
Kesehatan masyarakat[sunting | sunting sumber]
World Health Organization (WHO) mendeklarasikan TB sebagai "emergensi kesehatan global pada tahun 1993.[16] Tahun 2006, Kemitraan Stop TB mengembangkan gerakan Rencana Global Stop Tuberkulosis yang ditujukan untuk menyelamatkan 14 juta orang pada tahun 2015.[77] Jumlah yang telah ditargetkan ini sepertinya tidak akan tercapai pada tahun 2015, sebagian besar disebabkan oleh kenaikan penderita HIV dengan tuberkulosis dan munculnya resistansi tuberkulosis multi-obat (multiple drug-resistant tuberculosis, MDR-TB).[16] Klasifikasi tuberkulosis yang dikembangkan oleh American Thoracic Society pada umumnya digunakan dalam program kesehatan masyarakat.[78]
Karena kuman TB ada di mana-mana termasuk di Mal, Kantor dan tentunya juga di Rumah Sakit, maka pencegahan yang paling efektif adalah Gaya Hidup untuk menunjang Ketahanan Tubuh kita:
- Cukup gizi, jangan telat makan
- Cukup istirahat, jika lelah istirahat dulu
- Jangan Stres Fisik, lelah berlebihan
- Jangan Stres Mental, berusahalah berpikir positif dan legowo (bisa menerima)
Penanganan[sunting | sunting sumber]
Pengobatan TB menggunakan antibiotik untuk membunuh bakterinya. Pengobatan TB yang efektif ternyata sulit karena struktur dan komposisi kimia dinding sel mikobakteri yang tidak biasa. Dinding sel menahan obat masuk sehingga menyebabkan antibiotik tidak efektif.[79] Dua jenis antibiotik yang umum digunakan adalah isoniazid dan rifampisin, dan pengbatan dapat berlangsung berbulan-bulan.[49] Pengobatan TB laten biasanya menggunakan antibiotik tunggal.[80] Penyakit TB aktif sebaiknya diobati dengan kombinasi beberapa antibiotik untuk menurunkan risiko berkembangnya bakteri yang resisten terhadap antibiotik.[16] Pasien dengan infeksi laten juga diobati untuk mencegah munculnya TB aktif di kehidupan selanjutnya.[80] WHO merekomendasikan terapi pengawasan langsung (Inggris: directly-observed therapy), yaitu seorang pengawas kesehatan mengawasi penderita meminum obatnya. Tujuannya adalah untuk mengurangi jumlah penderita yang tidak meminum obat antibiotiknya dengan benar.[81] Bukti yang mendukung terapi pengawasan langsung secara independen kurang baik.[82] Namun, metode dengan cara mengingatkan penderita bahwa pengobatan itu penting ternyata efektif.[83]
Kasus baru[sunting | sunting sumber]
Rekomendasi tahun 2010 untuk pengobatan kasus baru tuberkulosis paru adalah kombinasi antibiotik selama enam bulan. Rifampicin, isoniazid, pirazinamide, dan etambutol untuk dua bulan pertama, dan hanya rifampicin dan isoniazid untuk empat bulan selanjutnya.[16] Apabila resistansi terhadap isoniazid tinggi, ethambutol dapat ditambahkan untuk empat bulan terakhir sebagai alternatif.[16]
Penyakit kambuh[sunting | sunting sumber]
Bila tuberkulosis kambuh, lakukan tes untuk menentukan jenis antibiotik yang sensitif sebelum menentukan pengobatan.[16] Jika multiple drug-resistant TB (MDR-TB) terdeteksi, direkomdendasikan pengobatan dengan paling tidak empat jenis antibiotik efektif selama 8–24 bulan.[16]
Resistansi obat[sunting | sunting sumber]
Resistansi primer muncul saat seseorang terinfeksi jenis TB resisten. Seorang dengan TB yang rentan dapat mengalami resistansi sekunder (didapat) pada saat terapi. Seseorang juga dapat mengalami perkembangan resistansi karena pengobatan yang tidak adekuat, jika obat yang diresepkan tidak dipakai dengan sesuai (karena tidak patuh), atau karena obat yang digunakan berkualitas rendah.[84] TB dengan resistansi obat merupakan masalah kesehatan masyarakat yang serius di negara yang sedang berkembang. Pengobatan untuk TB yang resisten terhadap obat akan berlangsung lebih lama dan memerlukan obat yang lebih mahal. MDR-TB (Mulitple Drugs Resistance-TB) sering didefinisikan sebagai resistansi terhadap dua obat yang paling efektif dalam lini pertama pengobatan TB, yaitu rifampisin and isoniazid. Extensively drug-resistant TB juga resisten terhadap tiga atau lebih dari enam kelas pengobatan lini kedua.[85] TB resisten obat total adalah resistansi terhadap semua jenis obat yang selama ini digunakan. TB dengan resisten total terhadap obat pertama kali ditemukan pada tahun 2003 di Italia, tetapi hal ini tidak pernah dilaporkan hingga tahun 2012.[86] Sekarang ini ada kecenderungan untuk mengetahui terlebih dahulu apa betul yang menginfeksi adalah bakteri TB atau bakteri lainnya dan obat apa saja yang masih mempan, oleh karenanya perlu dilakukan kultur bakteri terlebih dulu sebelum dilakukan pengobatan. Pada tahun 2007, WHO merekomendasikan penggunaan media cair untuk kultur bakteri TB agar lebih akurat dan membutuhkan waktu hingga 40 hari.[87]
Prognosis[sunting | sunting sumber]
Perkembangan dari infeksi TB menjadi penyakit TB yang nyata muncul saat basil mengalahkan pertahanan sistem imun dan mulai memperbanyak diri. Pada penyakit TB primer (sejumlah 1–5% dari kasus), perkembangan ini muncul segera setelah infeksi awal.[8] Namun, pada kebanyakan kasus, suatu infeksi laten muncul tanpa gejalan yang nyata.[8] Kuman yang dorman ini menghasilkan tuberkulosis aktif pada 5–10% dari kasus laten ini, dan pada umumnya baru akan muncul bertahun-tahun setelah infeksi.[14]
Risiko reaktivasi meningkat sebagai akibat imunosupresi, seperti misalnya disebabkan oleh infeksi HIV. Pada orang yang juga terinfeksi oleh “M. tuberculosis” dan HIV, risiko adanya reaktivasi meningkat hingga 10% per tahun.[8] Studi yang menggunakan sidik DNA dari galur “M. tuberculosis”menunjukkan bahwa infeksi kembali menyebabkan kambuhnya TB lebih sering dari yang diperkirakan.[88] Infeksi kembali dapat dihitung lebih dari 50% kasus dimana TB biasa ditemukan.[89] Peluang terjadinya kematian karena tuberkulosis adalah kurang lebih 4% pada tahun 2008, turun dari 8% pada tahun 1995.[16]
Sejarah[sunting | sunting sumber]

Tuberculosis sudah ada dalam kehidupan manusia sejak zaman kuno.[16] Deteksi paling awal “M. tuberculosis” terdapat pada bukti adanya penyakit tersebut di dalam bangkai bison yang berasal dari sekira 17.000 tahun lalu.[90] Namun, tidak ada kepastian apakah tuberkulosis berasal dari sapi (bovin), yang kemudian ditularkan ke manusia, atau apakah tuberkulosis tersebut bercabang dari nenek moyang yang sama.[91] Para ilmuwan yakin bahwa manusia terkena MTBC dari binatang selama proses penjinakan. Namun, gen “Micobacterium tuberculosis” complex (MTbC) pada manusia telah dibandingkan dengan MTbC pada binatang, dan teori tersebut telah terbukti salah. Galur bakteri tuberkulosis memiliki nenek moyang yang sama, yang sebenarnya bisa menginfeksi manusia sejak Revolusi Neolitik.[92] Sisa kerangka menunjukkan bahwa manusia prasejarah (4000 Sebelum Masehi) mengidap TB. Para peneliti menemukan pembusukan tuberkulosis di dalam tulang spina mumi-mumi Mesir dari tahun 3000–2400 SM.[93] "Phthisis" berasal dari bahasa Yunani yang artinya “konsumsi,” yakni istilah kuno untuk tuberkulosis paru.[94] Sekira 460 SM, Hippocrates mengidentifikasi bahwa phthisis adalah penyakit yang paling mudah menular pada saat itu. Orang dengan phthisis mengalami demam dan batuk darah. Phthisis hampir selalu berakibat fatal.[95] Penelitian gen menunjukkan bahwa TB telah ada di Amerika dari sekira tahun 100 AD.[96]
Sebelum Revolusi Industri, cerita rakyat sering kali menghubungkan tuberkulosis dengan vampir. Jika seorang anggota keluarga meninggal karena TB, kesehatan anggota keluarga lainnya dari orang yang terinfeksi tersebut perlahan-lahan menurun. Masyarakat percaya bahwa orang pertama yang terkena TB menguras jiwa anggota keluarga lainnya.[97]
Jenis TB paru yang dikaitkan dengan tuberkel ditetapkan sebagai patologi oleh Dr Richard Morton pada 1689.[98][99] Namun, TB memiliki berbagai gejala, sehingga TB tidak diidentifikasi sebagai satu jenis penyakit hingga akhir 1820-an. TB belum dinamakan tuberkulosis hingga 1839 oleh J. L. Schönlein.[100] Selama tahun 1838–1845, Dr. John Croghan, pemilik Gua Mammoth, membawa mereka yang terkena TB ke dalam gua dengan harapan menyembuhkan penyakit tersebut dengan suhu konstan dan kemurnian udara di dalam gua: mereka meninggal setelah satu tahun di dalam gua.[101] Hermann Brehmer membuka sanatorium pertama pada 1859 di Sokołowsko, Polandia.[102]

Basilus yang menyebabkan tuberkulosis, “Mycobacterium tuberculosis,” diidentifikasi dan dijelaskan pada 24 Maret 1882 oleh Robert Koch. Dia menerima Penghargaan Nobel Fisiologi atau Kedokteran pada 1905 atas penemuan ini.[103] Koch tidak percaya bahwa penyakit tuberkulosis pada sapi (ternak) dan manusia adalah penyakit yang serupa. Keyakinan ini menunda pengakuan bahwa susu yang terinfeksi menjadi sumber infeksi. Kemudian, risiko penularan dari sumber ini sangat jauh berkurang karena penemuan proses pasteurisasi. Koch mengumumkan ekstrak gliserin dari basil tuberkulosis sebagai "obat" untuk tuberkulosis pada 1890. Dia menamakannya “tuberkulin.” Meskipun “tuberkulin” tidak efektif, tuberkulin diadaptasi sebagai tes penapisan untuk mengetahui adanya tuberkulosis prasimtomatik.[104]
Albert Calmette dan Camille Guérin menerima kesuksesan pertama dalam imunisasi anti tuberkulosis pada 1906. Mereka menggunakan tuberkulosis galur bovin di-atenuasi, dan vaksin tersebut dinamakan BCG (basil Calmette dan Guérin). Vaksin BCG pertama kali digunakan pada manusia pada 1921 di Prancis.[105] Namun, vaksin BCG baru diterima secara luas di AS, Inggris, dan Jerman setelah Perang Dunia II.[106]
Tuberkulosis menimbulkan kekhawatiran masyarakat pada abad ke-19 dan pada awal abad ke-20 sebagai penyakit endemik masyarakat miskin di perkotaan. Pada 1815, satu di antara empat kematian di Inggris disebabkan oleh "konsumsi." Pada 1918, satu di antara enam kematian di Prancis disebabkan oleh TB. Setelah para ilmuwan menetapkan bahwa penyakit tersebut menular pada 1880-an, TB dimasukkan ke penyakit wajib lapor di Inggris. Kampanye dimulai agar orang-orang berhenti meludah di tempat umum dan orang miskin yang terinfeksi penyakit tersebut ‘didorong’ untuk masuk sanatorium yang menyerupai rumah tahanan. (Sanatorium untuk kelas menengah ke atas menawarkan perawatan yang luar biasa dan pemeriksaan medis terus-menerus.) [102] Sanatorium tersebut seharusnya memberi manfaat "udara bersih" dan pekerjaan. Namun bahkan dalam kondisi terbaik, 50% pasien di dalamnya meninggal setelah lima tahun (“ca.” 1916).[102]
Di Eropa, angka tuberkulosis mulai meningkat pada awal 1600-an. Angka kasus TB mencapai puncak tertingginya di Eropa pada 1800-an ketika penyakit ini menyebabkan hampir 25% dari keseluruhan kasus kematian.[107] Angka kematian kemudian menurun hingga hampir mencapai 90% pada 1950-an.[108] Peningkatan kesehatan masyarakat secara signifikan mengurangi angka tuberkulosis bahkan sebelum streptomisin dan antibiotik lainnya digunakan. Namun, penyakit tersebut masih merupakan ancaman yang serius bagi kesehatan masyarakat. Ketika Konsil Penelitian Medis dibentuk di Inggris pada 1913, fokus awalnya adalah penelitian tuberkulosis.[109]
Pada 1946, pengembangan antibiotik streptomisin mewujudkan pengobatan dan penyembuhan efektif untuk TB. Sebelum obat ini diperkenalkan, pengobatan satu-satunya (kecuali sanatorium) adalah intervensi bedah. “Teknik pneumotoraks" membuat paru-paru yang terinfeksi kolaps dan memberikan "jeda" sehingga lesi akibat tuberkulosis mulai sembuh.[110] Kemunculan MDR-TB kembali menjadikan pembedahan sebagai opsi dalam standar tatalaksana untuk perawatan infeksi TB. Intervensi bedah saat ini meliputi pengangkatan kavitasi ("bula") patologis di dalam paru-paru untuk mengurangi jumlah bakteri dan meningkatkan pajanan obat bagi bakteri yang masih ada di dalam aliran darah. Intervensi ini secara bersamaan mengurangi jumlah bakteri total dan meningkatkan efektivitas terapi antibiotik sistemik.[111] Meskipun para ahli mengharapkan agar TB dapat diberantas sepenuhnya (bandingkan cacar), munculnya galur resistansi obat pada 1980-an membuat pemberantasan TB menjadi sulit. Kemunculan kembali tuberkulosis mendorong deklarasi emergensi kesehatan global yang dibuat oleh WHO pada 1993.[112]
Masyarakat dan budaya[sunting | sunting sumber]
Organisasi Kesehatan Dunia dan Yayasan Bill & Melinda Gates memberi subsidi untuk tes diagnosis cepat yang baru (fast-acting diagnostic test) untuk digunakan di negara berpendapatan rendah dan menengah.[113][114] Sejak 2011, banyak tempat miskin yang hanya memiliki akses ke mikroskopi sputum (pemeriksaan dahak menggunakan mikroskop).[115]
Pada 2010, India memiliki jumlah kasus TB tertinggi di dunia. Satu penyebabnya adalah karena pengelolaan penyakit yang buruk oleh sektor pelayanan kesehatan swasta. Program-program seperti Program kontrol TB nasional terevisi membantu untuk mengurangi jumlah TB di antara orang-orang yang menerima layanan kesehatan masyarakat.[116][117]
Riset[sunting | sunting sumber]
Vaksin BCG memiliki keterbatasan, dan riset untuk mengembangkan vaksin TB baru masih berjalan.[118] Sejumlah calon potensial saat ini dalam uji klinis fase I dan II.[118] Dua pendekatan utama dalam uji klinis berusaha untuk memperbaiki kemanjuran efikasi vaksin yang ada. Satu pendekatan melibatkan penambahan vaksin sub-unit ke BCG. Strategi lainnya mencoba untuk menciptakan vaksin baru dan vaksin hidup yang lebih baik.[118]MVA85A adalah contoh dari vaksin sub-unit yang sedang diuji-cobakan di Afrika Selatan. MVA85A didasarkan pada virus vaccinia yang dimodifikasi secara genetik.[119] Harapannya vaksin akan berperan secara signifikan dalam perawatan penyakit laten dan aktif.[120]
Untuk mendorong penemuan lebih lanjut, para peneliti dan pembuat kebijakan memperkenalkan model baru yang lebih murah untuk pegembangan vaksin, termasuk hadiah, insentif pajak, dan komitmen pasar lanjutan.[121][122] Beberapa kelompok dilibatkan dalam riset, termasuk Kemitraan Stop TB,[123] the South African Tuberculosis Vaccine Initiative, and the Aeras Global TB Vaccine Foundation.[124] Aeras Global TB Vaccine Foundation menerima hibah lebih dari $280 juta (AS) dari Bill and Melinda Gates Foundation untuk mengembangkan dan melisensi vaksin yang lebih baik untuk melawan tuberkulosis agar dapat digunakan di negara-negara dengan beban yang tinggi.[125][126]
Penyakit pada hewan[sunting | sunting sumber]
Mikrobakteria menginfeksi berbagai hewan, termasuk unggas,[127] binatang pengerat,[128] dan reptil.[129] Subspesies Mycobacterium tuberculosis jarang muncul pada hewan liar.[130] Penyakit tuberkulosis pada hewan di antaranya yaitu tuberkulosis unggas yang disebabkan Mycobacterium avium, tuberkulosis sapi yang disebabkan oleh Mycobacterium bovis, serta penyakit Johne yang disebabkan oleh Mycobacterium avium subspesies paratuberculosis.
Referensi[sunting | sunting sumber]
- ^ a b c d e "Tuberculosis (TB)". who.int (dalam bahasa Inggris). Diarsipkan dari versi asli tanggal 30 July 2020. Diakses tanggal 8 May 2020.
- ^ Ferri FF (2010). Ferri's differential diagnosis : a practical guide to the differential diagnosis of symptoms, signs, and clinical disorders (edisi ke-2nd). Philadelphia, PA: Elsevier/Mosby. hlm. Chapter T. ISBN 978-0-323-07699-9.
- ^ Hawn TR, Day TA, Scriba TJ, Hatherill M, Hanekom WA, Evans TG, et al. (December 2014). "Tuberculosis vaccines and prevention of infection". Microbiology and Molecular Biology Reviews. 78 (4): 650–71. doi:10.1128/MMBR.00021-14. PMC 4248657
 . PMID 25428938.
. PMID 25428938.
- ^ Implementing the WHO Stop TB Strategy: a handbook for national TB control programmes. Geneva: World Health Organization (WHO). 2008. hlm. 179. ISBN 978-92-4-154667-6. Diarsipkan dari versi asli tanggal 2 June 2021. Diakses tanggal 17 September 2017.
- ^ Implementing the WHO Stop TB Strategy: a handbook for national TB control programmes. Geneva: World Health Organization (WHO). 2008. hlm. 179. ISBN 978-92-4-154667-6. Diarsipkan dari versi asli tanggal 2 June 2021. Diakses tanggal 17 September 2017.
- ^ a b "Tuberculosis (TB)". World Health Organization (WHO). 16 February 2018. Diarsipkan dari versi asli tanggal 30 December 2013. Diakses tanggal 15 September 2018.
- ^ Stevens, Alan M.; Tellings, A. Ed Schmidgall (2004). A Comprehensive Indonesian-English Dictionary (dalam bahasa Inggris). Ohio University Press. ISBN 978-0-8214-1584-9.
- ^ a b c d e f g h i j k l m n Kumar V, Abbas AK, Fausto N, Mitchell RN (2007). Robbins Basic Pathology (edisi ke-8th). Saunders Elsevier. hlm. 516–522. ISBN 978-1-4160-2973-1.
- ^ Konstantinos A (2010). "Testing for tuberculosis". Australian Prescriber. 33 (1): 12–18.
- ^ a b Global Tuberculosis Report 2023 (PDF). Jenewa: World Health Organization. 2023. ISBN 978-92-4-008385-1.
- ^ a b Kementerian Kesehatan Republik Indonesia (2022). Profil Kesehatan Indonesia 2022. Jakarta: Kementerian Kesehatan Republik Indonesia.
- ^ Kementerian Kesehatan Republik Indonesia (2021). Profil Kesehatan Indonesia 2021. Jakarta: Kementerian Kesehatan Republik Indonesia.
- ^ Schiffman G (15 January 2009). "Tuberculosis Symptoms". eMedicineHealth.
- ^ a b c d al.], edited by Peter G. Gibson ; section editors, Michael Abramson ... [et (2005). Evidence-based respiratory medicine (edisi ke-1. publ.). Oxford: Blackwell. hlm. 321. ISBN 978-0-7279-1605-1.
- ^ a b c d e f g Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (2010). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (edisi ke-7th). Philadelphia, PA: Churchill Livingstone/Elsevier. hlm. Chapter 250. ISBN 978-0-443-06839-3.
- ^ a b c d e f g h i j k l m n o p q r s t Lawn, SD (2 July 2011). "Tuberculosis". Lancet. 378 (9785): 57–72. doi:10.1016/S0140-6736(10)62173-3. PMID 21420161.
- ^ Behera, D. (2010). Textbook of pulmonary medicine (edisi ke-2nd ed.). New Delhi: Jaypee Brothers Medical Pub. hlm. 457. ISBN 978-81-8448-749-7.
- ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. hlm. 549. ISBN 978-93-5025-073-0.
- ^ a b Golden MP, Vikram HR (2005). "Extrapulmonary tuberculosis: an overview". American family physician. 72 (9): 1761–8. PMID 16300038.
- ^ Kabra, [edited by] Vimlesh Seth, S.K. (2006). Essentials of tuberculosis in children (edisi ke-3rd ed.). New Delhi: Jaypee Bros. Medical Publishers. hlm. 249. ISBN 978-81-8061-709-6.
- ^ a b Ghosh, editors-in-chief, Thomas M. Habermann, Amit K. (2008). Mayo Clinic internal medicine : concise textbook. Rochester, MN: Mayo Clinic Scientific Press. hlm. 789. ISBN 978-1-4200-6749-1.
- ^ Southwick F (10 December 2007). "Chapter 4: Pulmonary Infections". Infectious Diseases: A Clinical Short Course, 2nd ed. McGraw-Hill Medical Publishing Division. hlm. 104. ISBN 0-07-147722-5. Diarsipkan dari versi asli tanggal 2009-05-13. Diakses tanggal 2013-08-13.
- ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. hlm. 525. ISBN 978-93-5025-073-0.
- ^ Niederweis M, Danilchanka O, Huff J, Hoffmann C, Engelhardt H (2010). "Mycobacterial outer membranes: in search of proteins". Trends in Microbiology. 18 (3): 109–16. doi:10.1016/j.tim.2009.12.005. PMC 2931330
 . PMID 20060722.
. PMID 20060722.
- ^ a b Madison B (2001). "Application of stains in clinical microbiology". Biotech Histochem. 76 (3): 119–25. doi:10.1080/714028138. PMID 11475314.
- ^ Parish T, Stoker N (1999). "Mycobacteria: bugs and bugbears (two steps forward and one step back)". Molecular Biotechnology. 13 (3): 191–200. doi:10.1385/MB:13:3:191. PMID 10934532.
- ^ Medical Laboratory Science: Theory and Practice. New Delhi: Tata McGraw-Hill. 2000. hlm. 473. ISBN 0-07-463223-X.
- ^ Piot, editors, Richard D. Semba, Martin W. Bloem; foreword by Peter (2008). Nutrition and health in developing countries (edisi ke-2nd ed.). Totowa, NJ: Humana Press. hlm. 291. ISBN 978-1-934115-24-4.
- ^ van Soolingen D; et al. (1997). "A novel pathogenic taxon of the Mycobacterium tuberculosis complex, Canetti: characterization of an exceptional isolate from Africa". International Journal of Systematic Bacteriology. 47 (4): 1236–45. doi:10.1099/00207713-47-4-1236. PMID 9336935.
- ^ Niemann S; et al. (2002). "Mycobacterium africanum Subtype II Is Associated with Two Distinct Genotypes and Is a Major Cause of Human Tuberculosis in Kampala, Uganda". J. Clin. Microbiol. 40 (9): 3398–405. doi:10.1128/JCM.40.9.3398-3405.2002. PMC 130701
 . PMID 12202584.
. PMID 12202584.
- ^ Niobe-Eyangoh SN; et al. (2003). "Genetic Biodiversity of Mycobacterium tuberculosis Complex Strains from Patients with Pulmonary Tuberculosis in Cameroon". J. Clin. Microbiol. 41 (6): 2547–53. doi:10.1128/JCM.41.6.2547-2553.2003. PMC 156567
 . PMID 12791879.
. PMID 12791879.
- ^ Thoen C, Lobue P, de Kantor I (2006). "The importance of Mycobacterium bovis as a zoonosis". Vet. Microbiol. 112 (2–4): 339–45. doi:10.1016/j.vetmic.2005.11.047. PMID 16387455.
- ^ Acton, Q. Ashton (2011). Mycobacterium Infections: New Insights for the Healthcare Professional. ScholarlyEditions. hlm. 1968. ISBN 978-1-4649-0122-5.
- ^ Pfyffer, GE (1998 Oct-Dec). "Mycobacterium canettii, the smooth variant of M. tuberculosis, isolated from a Swiss patient exposed in Africa". Emerging infectious diseases. 4 (4): 631–4. PMID 9866740.
- ^ Panteix, G (2010 Aug). "Pulmonary tuberculosis due to Mycobacterium microti: a study of six recent cases in France". Journal of medical microbiology. 59 (Pt 8): 984–9. PMID 20488936.
- ^ American Thoracic Society (1997). "Diagnosis and treatment of disease caused by nontuberculous mycobacteria. This official statement of the American Thoracic Society was approved by the Board of Directors, March 1997. Medical Section of the American Lung Association". Am J Respir Crit Care Med. 156 (2 Pt 2): S1–25. PMID 9279284.
- ^ World Health Organization (2011). "The sixteenth global report on tuberculosis" (PDF).
- ^ World Health Organization. "Global tuberculosis control–surveillance, planning, financing WHO Report 2006". Diakses tanggal 13 October 2006.
- ^ Chaisson, RE (13 March 2008). "Tuberculosis in Africa--combating an HIV-driven crisis". The New England Journal of Medicine. 358 (11): 1089–92. doi:10.1056/NEJMp0800809. PMID 18337598.
- ^ Griffith D, Kerr C (1996). "Tuberculosis: disease of the past, disease of the present". J Perianesth Nurs. 11 (4): 240–5. doi:10.1016/S1089-9472(96)80023-2. PMID 8964016.
- ^ ATS/CDC Statement Committee on Latent Tuberculosis Infection (200). "Targeted tuberculin testing and treatment of latent tuberculosis infection. American Thoracic Society". MMWR Recomm Rep. 49 (RR–6): 1–51. PMID 10881762.
- ^ van Zyl Smit, RN (2010 Jan). "Global lung health: the colliding epidemics of tuberculosis, tobacco smoking, HIV and COPD". The European respiratory journal : official journal of the European Society for Clinical Respiratory Physiology. 35 (1): 27–33. PMID 20044459.
These analyses indicate that smokers are almost twice as likely to be infected with TB and to progress to active disease (RR of ∼1.5 for latent TB infection (LTBI) and RR of ∼2.0 for TB disease). Perokok juga memiliki peluang meninggal karena TB yang lebih besar (Risiko Relatif ∼2.0 dari seluruh angka kematian akibat TB), namun data yang ada sulit diinterpretasikan karena keberagaman/heterogenitas hasil yang didapatkan dari berbagai penelitian berbeda.
- ^ Restrepo, BI (15 August 2007). "Convergence of the tuberculosis and diabetes epidemics: renewal of old acquaintances". Clinical infectious diseases : an official publication of the Infectious Diseases Society of America. 45 (4): 436–8. doi:10.1086/519939. PMC 2900315
 . PMID 17638190.
. PMID 17638190.
- ^ Möller, M (2010 Mar). "Current findings, challenges and novel approaches in human genetic susceptibility to tuberculosis". Tuberculosis (Edinburgh, Scotland). 90 (2): 71–83. doi:10.1016/j.tube.2010.02.002. PMID 20206579.
- ^ Cole E, Cook C (1998). "Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies". Am J Infect Control. 26 (4): 453–64. doi:10.1016/S0196-6553(98)70046-X. PMID 9721404.
- ^ Nicas M, Nazaroff WW, Hubbard A (2005). "Toward understanding the risk of secondary airborne infection: emission of respirable pathogens". J Occup Environ Hyg. 2 (3): 143–54. doi:10.1080/15459620590918466. PMID 15764538.
- ^ a b Ahmed N, Hasnain S (2011). "Molecular epidemiology of tuberculosis in India: Moving forward with a systems biology approach". Tuberculosis. 91 (5): 407–3. doi:10.1016/j.tube.2011.03.006. PMID 21514230.
- ^ a b "Tuberculosis Fact sheet N°104". World Health Organization. November 2010. Diakses tanggal 26 July 2011.
- ^ a b "Core Curriculum on Tuberculosis: What the Clinician Should Know" (PDF) (edisi ke-5th). Centers for Disease Control and Prevention (CDC), Division of Tuberculosis Elimination. 2011.
- ^ "Causes of Tuberculosis". Mayo Clinic. 21 December 2006. Diakses tanggal 19 October 2007.
- ^ Skolnik, Richard (2011). Global health 101 (edisi ke-2nd ed.). Burlington, MA: Jones & Bartlett Learning. hlm. 253. ISBN 978-0-7637-9751-5.
- ^ a b editors, Arch G. Mainous III, Claire Pomeroy, (2009). Management of antimicrobials in infectious diseases : impact of antibiotic resistance (edisi ke-2nd rev. ed.). Totowa, N.J.: Humana. hlm. 74. ISBN 978-1-60327-238-4.
- ^ Houben E, Nguyen L, Pieters J (2006). "Interaction of pathogenic mycobacteria with the host immune system". Curr Opin Microbiol. 9 (1): 76–85. doi:10.1016/j.mib.2005.12.014. PMID 16406837.
- ^ Khan (2011). Essence Of Paediatrics. Elsevier India. hlm. 401. ISBN 978-81-312-2804-3.
- ^ Herrmann J, Lagrange P (2005). "Dendritic cells and Mycobacterium tuberculosis: which is the Trojan horse?". Pathol Biol (Paris). 53 (1): 35–40. doi:10.1016/j.patbio.2004.01.004. PMID 15620608.
- ^ Agarwal R, Malhotra P, Awasthi A, Kakkar N, Gupta D (2005). "Tuberculous dilated cardiomyopathy: an under-recognized entity?". BMC Infect Dis. 5 (1): 29. doi:10.1186/1471-2334-5-29. PMC 1090580
 . PMID 15857515.
. PMID 15857515.
- ^ a b c Grosset J (2003). "Mycobacterium tuberculosis in the Extracellular Compartment: an Underestimated Adversary". Antimicrob Agents Chemother. 47 (3): 833–6. doi:10.1128/AAC.47.3.833-836.2003. PMC 149338
 . PMID 12604509.
. PMID 12604509.
- ^ Crowley, Leonard V. (2010). An introduction to human disease : pathology and pathophysiology correlations (edisi ke-8th ed.). Sudbury, Mass.: Jones and Bartlett. hlm. 374. ISBN 978-0-7637-6591-0.
- ^ Anthony, Harries (2005). TB/HIV a Clinical Manual (edisi ke-2nd). Geneva: World Health Organization. hlm. 75. ISBN 978-92-4-154634-8.
- ^ Jacob, JT (2009 Jan). "Acute forms of tuberculosis in adults". The American journal of medicine. 122 (1): 12–7. PMID 19114163.
- ^ a b Bento, J (2011 Jan-Feb). "[Diagnostic tools in tuberculosis]". Acta medica portuguesa. 24 (1): 145–54. PMID 21672452.
- ^ a b c d Escalante, P (2009 Jun 2). "In the clinic. Tuberculosis". Annals of internal medicine. 150 (11): ITC61–614; quiz ITV616. PMID 19487708.
- ^ Metcalfe, JZ (2011 Nov 15). "Interferon-γ release assays for active pulmonary tuberculosis diagnosis in adults in low- and middle-income countries: systematic review and meta-analysis". The Journal of infectious diseases. 204 Suppl 4: S1120–9. PMID 21996694.
- ^ a b Sester, M (2011 Jan). "Interferon-γ release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis". The European respiratory journal : official journal of the European Society for Clinical Respiratory Physiology. 37 (1): 100–11. PMID 20847080.
- ^ Chen, J (2011). "Interferon-gamma release assays for the diagnosis of active tuberculosis in HIV-infected patients: a systematic review and meta-analysis". PloS one. 6 (11): e26827. PMID 22069472.
- ^ Diseases, Special Programme for Research & Training in Tropical (2006). Diagnostics for tuberculosis : global demand and market potential. Geneva: World Health Organization on behalf of the Special Programme for Research and Training in Tropical Diseases. hlm. 36. ISBN 978-92-4-156330-7.
- ^ a b c National Institute for Health and Clinical Excellence. Clinical guideline 117: Tuberculosis. London, 2011.
- ^ Steingart, KR (2011 Aug). "Commercial serological tests for the diagnosis of active pulmonary and extrapulmonary tuberculosis: an updated systematic review and meta-analysis". PLoS medicine. 8 (8): e1001062. doi:10.1371/journal.pmed.1001062. PMC 3153457
 . PMID 21857806.
. PMID 21857806.
- ^ Rothel J, Andersen P (2005). "Diagnosis of latent Mycobacterium tuberculosis infection: is the demise of the Mantoux test imminent?". Expert Rev Anti Infect Ther. 3 (6): 981–93. doi:10.1586/14787210.3.6.981. PMID 16307510.
- ^ Pai M, Zwerling A, Menzies D (2008). "Systematic Review: T-Cell–based Assays for the Diagnosis of Latent Tuberculosis Infection: An Update". Ann. Intern. Med. 149 (3): 1–9. PMC 2951987
 . PMID 18593687.
. PMID 18593687.
- ^ Jindal, editor-in-chief SK. Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. hlm. 544. ISBN 978-93-5025-073-0.
- ^ Amicosante, M (2010 Apr). "Rational use of immunodiagnostic tools for tuberculosis infection: guidelines and cost effectiveness studies". The new microbiologica. 33 (2): 93–107. PMID 20518271.
- ^ McShane, H (12 October 2011). "Tuberculosis vaccines: beyond bacille Calmette–Guérin". Philosophical transactions of the Royal Society of London. Series B, Biological sciences. 366 (1579): 2782–9. doi:10.1098/rstb.2011.0097. PMC 3146779
 . PMID 21893541.
. PMID 21893541.
- ^ "Vaccine and Immunizations: TB Vaccine (BCG)". Centers for Disease Control and Prevention. 2011. Diakses tanggal 26 July 2011.
- ^ "BCG Vaccine Usage in Canada -Current and Historical". Public Health Agency of Canada. 2010. Diarsipkan dari versi asli tanggal 2012-03-30. Diakses tanggal 30 December 2011.
- ^ a b Teo, SS (2006 Jun). "Does BCG have a role in tuberculosis control and prevention in the United Kingdom?". Archives of Disease in Childhood. 91 (6): 529–31. doi:10.1136/adc.2005.085043. PMC 2082765
 . PMID 16714729.
. PMID 16714729.
- ^ "The Global Plan to Stop TB". World Health Organization. 2011. Diakses tanggal 13 June 2011.
- ^ Warrell, ed. by D. J. Weatherall ... [4. + 5. ed.] ed. by David A. (2005). Sections 1 - 10 (edisi ke-4. ed., paperback.). Oxford [u.a.]: Oxford Univ. Press. hlm. 560. ISBN 978-0-19-857014-1.
- ^ Brennan PJ, Nikaido H (1995). "The envelope of mycobacteria". Annu. Rev. Biochem. 64: 29–63. doi:10.1146/annurev.bi.64.070195.000333. PMID 7574484.
- ^ a b Menzies, D (2011 Mar). "Recent developments in treatment of latent tuberculosis infection". The Indian journal of medical research. 133: 257–66. PMID 21441678.
- ^ Arch G., III Mainous (2010). Management of Antimicrobials in Infectious Diseases: Impact of Antibiotic Resistance. Humana Pr. hlm. 69. ISBN 1-60327-238-0.
- ^ Volmink J, Garner P (2007). "Directly observed therapy for treating tuberculosis". Cochrane Database Syst Rev (4): CD003343. doi:10.1002/14651858.CD003343.pub3. PMID 17943789.
- ^ Liu, Q (2008 Oct 8). "Reminder systems and late patient tracers in the diagnosis and management of tuberculosis". Cochrane database of systematic reviews (Online) (4): CD006594. PMID 18843723.
- ^ O'Brien R (1994). "Drug-resistant tuberculosis: etiology, management and prevention". Semin Respir Infect. 9 (2): 104–12. PMID 7973169.
- ^ Centers for Disease Control and Prevention (CDC) (2006). "Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs—worldwide, 2000–2004". MMWR Morb Mortal Wkly Rep. 55 (11): 301–5. PMID 16557213.
- ^ Maryn McKenna (12 January 2012). "Totally Resistant TB: Earliest Cases in Italy". Wired. Diakses tanggal 12 January 2012.
- ^ Ricky Reynald Yulman (1 April 2015). "TB, Bakteri Lebih Cepat Terdeteksi". Diarsipkan dari versi asli tanggal 2015-04-02. Diakses tanggal 2015-04-01.
- ^ Lambert M; et al. (2003). "Recurrence in tuberculosis: relapse or reinfection?". Lancet Infect Dis. 3 (5): 282. doi:10.1016/S1473-3099(03)00607-8. PMID 12726976.
- ^ Wang, JY (15 July 2007). "Prediction of the tuberculosis reinfection proportion from the local incidence". The Journal of infectious diseases. 196 (2): 281–8. doi:10.1086/518898. PMID 17570116.
- ^ Rothschild BM; Martin LD; Lev G; et al. (2001). "Mycobacterium tuberculosis complex DNA from an extinct bison dated 17,000 years before the present". Clin. Infect. Dis. 33 (3): 305–11. doi:10.1086/321886. PMID 11438894.
- ^ Pearce-Duvet J (2006). "The origin of human pathogens: evaluating the role of agriculture and domestic animals in the evolution of human disease". Biol Rev Camb Philos Soc. 81 (3): 369–82. doi:10.1017/S1464793106007020. PMID 16672105.
- ^ Comas, I (2009 Oct). "The past and future of tuberculosis research". PLoS pathogens. 5 (10): e1000600. PMID 19855821.
- ^ Zink A, Sola C, Reischl U, Grabner W, Rastogi N, Wolf H, Nerlich A (2003). "Characterization of Mycobacterium tuberculosis Complex DNAs from Egyptian Mummies by Spoligotyping". J Clin Microbiol. 41 (1): 359–67. doi:10.1128/JCM.41.1.359-367.2003. PMC 149558
 . PMID 12517873.
. PMID 12517873.
- ^ The Chambers Dictionary. New Delhi: Allied Chambers India Ltd. 1998. hlm. 352. ISBN 978-81-86062-25-8.
- ^ Hippocrates.Aphorisms. Accessed 7 October 2006.
- ^ Konomi N, Lebwohl E, Mowbray K, Tattersall I, Zhang D (2002). "Detection of Mycobacterial DNA in Andean Mummies". J Clin Microbiol. 40 (12): 4738–40. doi:10.1128/JCM.40.12.4738-4740.2002. PMC 154635
 . PMID 12454182.
. PMID 12454182.
- ^ Sledzik, Paul S. (1994). "Bioarcheological and biocultural evidence for the New England vampire folk belief" (PDF). American Journal of Physical Anthropology. 94 (2): 269–274. doi:10.1002/ajpa.1330940210. ISSN 0002-9483. PMID 8085617.
- ^ Léon Charles Albert Calmette di Who Named It
- ^ Trail RR (1970). "Richard Morton (1637-1698)". Med Hist. 14 (2): 166–74. PMC 1034037
 . PMID 4914685.
. PMID 4914685.
- ^ Zur Pathogenie der Impetigines. Auszug aus einer brieflichen Mitteilung an den Herausgeber. [Müller’s] Archiv für Anatomie, Physiologie und wissenschaftliche Medicin. 1839, page 82.
- ^ Kentucky: Mammoth Cave long on history. Diarsipkan 2006-08-13 di Wayback Machine. CNN. 27 February 2004. Accessed 8 October 2006.
- ^ a b c McCarthy OR (2001). "The key to the sanatoria". J R Soc Med. 94 (8): 413–7. PMC 1281640
 . PMID 11461990.
. PMID 11461990.
- ^ Nobel Foundation. The Nobel Prize in Physiology or Medicine 1905. Accessed 7 October 2006.
- ^ Waddington K (2004). "To stamp out "So Terrible a Malady": bovine tuberculosis and tuberculin testing in Britain, 1890–1939". Med Hist. 48 (1): 29–48. PMC 546294
 . PMID 14968644.
. PMID 14968644.
- ^ Bonah C (2005). "The 'experimental stable' of the BCG vaccine: safety, efficacy, proof, and standards, 1921–1933". Stud Hist Philos Biol Biomed Sci. 36 (4): 696–721. doi:10.1016/j.shpsc.2005.09.003. PMID 16337557.
- ^ Comstock G (1994). "The International Tuberculosis Campaign: a pioneering venture in mass vaccination and research". Clin Infect Dis. 19 (3): 528–40. doi:10.1093/clinids/19.3.528. PMID 7811874.
- ^ Bloom, editor, Barry R. (1994). Tuberculosis : pathogenesis, protection, and control. Washington, D.C.: ASM Press. ISBN 978-1-55581-072-6.
- ^ Persson, Sheryl (2010). Smallpox, Syphilis and Salvation: Medical Breakthroughs That Changed the World. ReadHowYouWant.com. hlm. 141. ISBN 978-1-4587-6712-7.
- ^ editor, Caroline Hannaway, (2008). Biomedicine in the twentieth century: practices, policies, and politics. Amsterdam: IOS Press. hlm. 233. ISBN 978-1-58603-832-8.
- ^ Shields, Thomas (2009). General thoracic surgery (edisi ke-7th ed.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. hlm. 792. ISBN 978-0-7817-7982-1.
- ^ Lalloo UG, Naidoo R, Ambaram A (2006). "Recent advances in the medical and surgical treatment of multi-drug resistant tuberculosis". Curr Opin Pulm Med. 12 (3): 179–85. doi:10.1097/01.mcp.0000219266.27439.52. PMID 16582672. Diarsipkan dari versi asli tanggal 2013-05-10. Diakses tanggal 2013-08-13.
- ^ "Frequently asked questions about TB and HIV". World Health Organization. Diakses tanggal 15 April 2012.
- ^ Lawn, SD (2011 Sep). "Xpert® MTB/RIF assay: development, evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance". Future microbiology. 6 (9): 1067–82. PMID 21958145.
- ^ "WHO says Cepheid rapid test will transform TB care". Reuters. 8 December 2010.
- ^ Lienhardt, C (2011 Nov). "What research is needed to stop TB? Introducing the TB Research Movement". PLoS medicine. 8 (11): e1001135. doi:10.1371/journal.pmed.1001135. PMC 3226454
 . PMID 22140369.
. PMID 22140369.
- ^ Anurag Bhargava, Lancelot Pinto, Madhukar Pai (2011). "Mismanagement of tuberculosis in India: Causes, consequences, and the way forward". Hypothesis. 9 (1): e7. Diarsipkan dari versi asli tanggal 2020-01-12. Diakses tanggal 2013-08-13.
- ^ Amdekar, Y (2009 Jul). "Changes in the management of tuberculosis". Indian journal of pediatrics. 76 (7): 739–42. PMID 19693453.
- ^ a b c Martín Montañés, C (2011 Mar). "New tuberculosis vaccines". Enfermedades infecciosas y microbiologia clinica. 29 Suppl 1: 57–62. doi:10.1016/S0213-005X(11)70019-2. PMID 21420568.
- ^ Ibanga H, Brookes R, Hill P, Owiafe P, Fletcher H, Lienhardt C, Hill A, Adegbola R, McShane H (2006). "Early clinical trials with a new tuberculosis vaccine, MVA85A, in tuberculosis-endemic countries: issues in study design". Lancet Infect Dis. 6 (8): 522–8. doi:10.1016/S1473-3099(06)70552-7. PMID 16870530.
- ^ Kaufmann SH (2010). "Future vaccination strategies against tuberculosis: Thinking outside the box". Immunity. 33 (4): 567–77. doi:10.1016/j.immuni.2010.09.015. PMID 21029966.
- ^ Webber D, Kremer M (2001). "Stimulating Industrial R&D for Neglected Infectious Diseases: Economic Perspectives" (PDF). Bulletin of the World Health Organization. 79 (8): 693–801.
- ^ Barder O, Kremer M, Williams H (2006). "Advance Market Commitments: A Policy to Stimulate Investment in Vaccines for Neglected Diseases". The Economists' Voice. 3 (3). doi:10.2202/1553-3832.1144. Diarsipkan dari versi asli tanggal 2006-11-05. Diakses tanggal 2013-08-13.
- ^ Economic, Department of (2009). Achieving the global public health agenda : dialogues at the Economic and Social Council. New York: United Nations. hlm. 103. ISBN 978-92-1-104596-3.
- ^ Jong, [edited by] Jane N. Zuckerman, Elaine C. (2010). Travelers' vaccines (edisi ke-2nd ed.). Shelton, CT: People's Medical Pub. House. hlm. 319. ISBN 978-1-60795-045-5.
- ^ Bill and Melinda Gates Foundation Announcement (2004-02-12). "Gates Foundation Commits $82.9 Million to Develop New Tuberculosis Vaccines". Diarsipkan dari versi asli tanggal 2009-10-10. Diakses tanggal 2013-08-13.
- ^ Nightingale, Katherine (2007-09-19). "Gates foundation gives US$280 million to fight TB".
- ^ Shivaprasad, HL (2012 Jan). "Pathology of mycobacteriosis in birds". The veterinary clinics of North America. Exotic animal practice. 15 (1): 41–55, v–vi. PMID 22244112.
- ^ Reavill, DR (2012 Jan). "Mycobacterial lesions in fish, amphibians, reptiles, rodents, lagomorphs, and ferrets with reference to animal models". The veterinary clinics of North America. Exotic animal practice. 15 (1): 25–40, v. PMID 22244111.
- ^ Mitchell, MA (2012 Jan). "Mycobacterial infections in reptiles". The veterinary clinics of North America. Exotic animal practice. 15 (1): 101–11, vii. PMID 22244116.
- ^ Wobeser, Gary A. (2006). Essentials of disease in wild animals (edisi ke-1st ed.). Ames, Iowa [u.a.]: Blackwell Publ. hlm. 170. ISBN 978-0-8138-0589-4.
