Metabolisme: Perbedaan antara revisi
→Koenzim: Penamabahan konten |
|||
| Baris 66: | Baris 66: | ||
Dua jenis asam nukleat , yaitu DNA dan RNA merupakan polimer dari nukleotida. Tiap nukleotida disusun atas fosfat yang menempel pada gugus gula [[ribosa]] atau [[deoksiribosa]] yang menempel pada [[Basa nukleotida|basa nitrogen]]. Asam nukleat memiliki fungsi penting sebagai penyimpanan dan penggunaan informasi genetik yang akan dinterpretasi melalui proses [[Transkripsi (genetik)|transkripsi]] dan [[Translasi (genetik)|translasi]] dalam proses [[Sintesis protein|biosintesis protein]].{{Sfn|Nelson|Cox|2017|p=717-752}} Informasi genetik yang terkandung di dalam asam nukleat dilindungi oleh mekanisme [[perbaikan DNA]] dan diperbanyak pada proses [[replikasi DNA]]. Banyak [[virus]] memiliki [[Virus RNA|genom RNA]] seperti [[HIV]], yang menggunakan proses [[Transkriptase balik|transkripsi balik]] untuk membuat templat DNA dari genom virus RNAnya. <ref>{{Cite journal|last=Sierra|first=Saleta|last2=Kupfer|first2=Bernd|last3=Kaiser|first3=Rolf|date=2005-12-01|title=Basics of the virology of HIV-1 and its replication|url=http://www.sciencedirect.com/science/article/pii/S1386653205002374|journal=Journal of Clinical Virology|series=Focus on HIV|language=en|volume=34|issue=4|pages=233–244|doi=10.1016/j.jcv.2005.09.004|issn=1386-6532}}</ref> Molekul RNA yang berada di dalam [[ribozim]], seperti [[spliosom]] atau ribosom mirip dengan enzim yang mampu mengkatalisis reaksi kimia. [[Nukleosida]] adalah penyusun nukleotida yang merupakan [[Basa nukleotida|nukleobasa]] yang menempel pada gula [[ribosa]]. Basa nukleotida memiliki bentuk cincin [[Senyawa heterosiklik|heterosiklik]] yang mengandung nitrogen yang diklasifisikasikan menjadi dua macam, yaitu [[purina]] atau [[pirimidina]]. Nukleotida juga dapat berfungsi sebagai [[Kofaktor (biokimia)|koenzim]] pada reaksi transfer gugus metabolis.<ref name="Wimmer">{{cite journal|year=1978|title=Mechanisms of enzyme-catalyzed group transfer reactions|journal=Annu Rev Biochem|volume=47|issue=|pages=1031–78|doi=10.1146/annurev.bi.47.070178.005123|pmid=354490|vauthors=Wimmer M, Rose I}}</ref> |
Dua jenis asam nukleat , yaitu DNA dan RNA merupakan polimer dari nukleotida. Tiap nukleotida disusun atas fosfat yang menempel pada gugus gula [[ribosa]] atau [[deoksiribosa]] yang menempel pada [[Basa nukleotida|basa nitrogen]]. Asam nukleat memiliki fungsi penting sebagai penyimpanan dan penggunaan informasi genetik yang akan dinterpretasi melalui proses [[Transkripsi (genetik)|transkripsi]] dan [[Translasi (genetik)|translasi]] dalam proses [[Sintesis protein|biosintesis protein]].{{Sfn|Nelson|Cox|2017|p=717-752}} Informasi genetik yang terkandung di dalam asam nukleat dilindungi oleh mekanisme [[perbaikan DNA]] dan diperbanyak pada proses [[replikasi DNA]]. Banyak [[virus]] memiliki [[Virus RNA|genom RNA]] seperti [[HIV]], yang menggunakan proses [[Transkriptase balik|transkripsi balik]] untuk membuat templat DNA dari genom virus RNAnya. <ref>{{Cite journal|last=Sierra|first=Saleta|last2=Kupfer|first2=Bernd|last3=Kaiser|first3=Rolf|date=2005-12-01|title=Basics of the virology of HIV-1 and its replication|url=http://www.sciencedirect.com/science/article/pii/S1386653205002374|journal=Journal of Clinical Virology|series=Focus on HIV|language=en|volume=34|issue=4|pages=233–244|doi=10.1016/j.jcv.2005.09.004|issn=1386-6532}}</ref> Molekul RNA yang berada di dalam [[ribozim]], seperti [[spliosom]] atau ribosom mirip dengan enzim yang mampu mengkatalisis reaksi kimia. [[Nukleosida]] adalah penyusun nukleotida yang merupakan [[Basa nukleotida|nukleobasa]] yang menempel pada gula [[ribosa]]. Basa nukleotida memiliki bentuk cincin [[Senyawa heterosiklik|heterosiklik]] yang mengandung nitrogen yang diklasifisikasikan menjadi dua macam, yaitu [[purina]] atau [[pirimidina]]. Nukleotida juga dapat berfungsi sebagai [[Kofaktor (biokimia)|koenzim]] pada reaksi transfer gugus metabolis.<ref name="Wimmer">{{cite journal|year=1978|title=Mechanisms of enzyme-catalyzed group transfer reactions|journal=Annu Rev Biochem|volume=47|issue=|pages=1031–78|doi=10.1146/annurev.bi.47.070178.005123|pmid=354490|vauthors=Wimmer M, Rose I}}</ref> |
||
[[File:Acetyl-CoA-2D.svg|pra=https://en.wikipedia.org/wiki/File:Acetyl-CoA-2D.svg|al=|jmpl|Struktur koenzim [[Asetil-KoA|Asetil-Koa]].[[Gugus asetil]] yang dapat ditransfer terikat dengan atom sulfur yang ada di ujung kiri ]] |
|||
===Koenzim=== |
===Koenzim=== |
||
{{main|Koenzim}}Metabolisme melibatkan banyak reaksi kimia, tetapi sebagian besar reaksi tersebut dikategorikan ke dalam jenis reaksi sederhana yang melibatkan perpindahan [[gugus fungsional]] suatu atom serta ikatannya di dalam suatu molekul.<ref>{{Cite journal|last=Mitchell|first=Peter|date=Maret 1979|year=1979|title=Compartmentation and Communication in Living Systems. Ligand Conduction: a General Catalytic Principle in Chemical, Osmotic and Chemiosmotic Reaction Systems|url=https://febs.onlinelibrary.wiley.com/doi/abs/10.1111/j.1432-1033.1979.tb12934.x|journal=European Journal of Biochemistry|language=en|volume=95|issue=1|pages=1–20|doi=10.1111/j.1432-1033.1979.tb12934.x|issn=1432-1033}}</ref> Kimia sederhana ini memungkinkan pengunaaan kelompok senyawa intermediat untuk membawa gugus senyawa kimia ini berpindah diantara reaksi-reaksi yang berbeda.<ref>{{Cite journal|last=Wimmer|first=Mary J.|last2=Rose|first2=Irwin A.|date=1 Juni 1978|year=1978|title=Mechanisms of Enzyme-Catalyzed Group Transfer Reactions|url=https://www.annualreviews.org/doi/10.1146/annurev.bi.47.070178.005123|journal=Annual Review of Biochemistry|volume=47|issue=1|pages=1031–1078|doi=10.1146/annurev.bi.47.070178.005123|issn=0066-4154}}</ref>Kelompok senyawa intermediat yang berfungsi untuk memindahkan gugus tersebut, dikenal dengan nama koenzim. Tiap kelompok reaksi dikendalikan oleh suatu koenzim tertentu, yang menjadi [[Substrat (kimia)|substrat]] untuk kelompok enzim yang memproduksinya sekaligus enzim yang memakainya. Koenzim ini terus-menerus dibuat, dipakai dan didaur ulang<ref name="Dimroth">{{cite journal|date=March 2006|title=Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series|journal=EMBO Rep|volume=7|issue=3|pages=276–82|doi=10.1038/sj.embor.7400646|pmc=1456893|pmid=16607397|vauthors=Dimroth P, von Ballmoos C, Meier T}}</ref> |
|||
Salah satu koenzim utama yang ada didalam tubuh ialah ATP ([[Adenosina trifosfat|Adenosina Trifosfat]]) yang merupakan sumber energi universal di dalam sel. Jenis nukleotida ini digunakan untuk memindahkan energi kimiawi diantara reaksi kimia berbeda. Hanya ada sedikit ATP di dalam tubuh, namun ATP terus menerus diregenerasi sehingga tubuh manusia dapat menggunakan ATP dengan jumlah yang setara dengan berat badan tubuhnya. <ref name="Dimroth2">{{cite journal|date=March 2006|title=Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series|journal=EMBO Rep|volume=7|issue=3|pages=276–82|doi=10.1038/sj.embor.7400646|pmc=1456893|pmid=16607397|vauthors=Dimroth P, von Ballmoos C, Meier T}}</ref> <ref>{{Cite journal|last=Dimroth|first=Peter|last2=von Ballmoos|first2=Christoph|last3=Meier|first3=T|date=1 Maret 2006|year=|title=Catalytic and mechanical cycles in F-ATP synthases|url=https://www.embopress.org/doi/full/10.1038/sj.embor.7400646|journal=EMBO reports|volume=7|issue=3|pages=276–282|doi=10.1038/sj.embor.7400646|issn=1469-221X|pmc=PMC1456893|pmid=16607397}}</ref>ATP bertindak sebagai jembatan penghubung katabolisme dan anabolisme. Katabolisme menguraikan molekul dan katabolisme menyatukannya kembali. Reaksi katabolisme menghasilkan ATP dan reaksi anabolis memakainya. ATP juga berfungsi sebagai pembawa gugus fosfat dalam reaksi [[Fosforilasi oksidatif|fosforilasi]] <ref>{{Cite journal|last=Bonora|first=Massimo|last2=Patergnani|first2=Simone|last3=Rimessi|first3=Alessandro|last4=De Marchi|first4=Elena|last5=Suski|first5=Jan M.|last6=Bononi|first6=Angela|last7=Giorgi|first7=Carlotta|last8=Marchi|first8=Saverio|last9=Missiroli|first9=Sonia|date=12 September 2012|year=|title=ATP synthesis and storage|url=http://link.springer.com/10.1007/s11302-012-9305-8|journal=Purinergic Signalling|language=en|volume=8|issue=3|pages=343–357|doi=10.1007/s11302-012-9305-8|issn=1573-9538|pmc=PMC3360099|pmid=22528680}}</ref> |
|||
| ⚫ | |||
[[Vitamin]] merupakan senyawa organik yang dibutuhkan dalam jumlah yang sedikit yang tidak dapat diproduksi oleh sel di dalam tubuh manusia. Pada [[Nutrisi|nutris]]<nowiki/>i manusia, vitamin berfungsi sebagai koenzim, setelah mengalami modifikasi. Misalnya, vitamin larut air akan mengalami fosforilasi dan berpasangan dengan nukleotida ketika dipakai oleh sel.<ref>{{Cite journal|last=Berg|first=Jeremy M.|last2=Tymoczko|first2=John L.|last3=Stryer|first3=Lubert|date=2002|title=Vitamins Are Often Precursors to Coenzymes|url=https://www.ncbi.nlm.nih.gov/books/NBK22549/|journal=Biochemistry. 5th edition|language=en}}</ref> [[Nikotinamida adenina dinukleotida]] (NAD<sup>+</sup>) adalah senyawa turunan vitamin B<sub>3</sub>([[niasin]]) yang merupakan koenzim penting yang bertindak sebagai reseptor molekul hidrogen. Ratusan jenis enzim [[Dehidrogenases|dehidrogenase]] melepas elektron dari substrat dan mereduksi NAD<sup>+</sup> menjadi NADH. Koenzim yang telah direduksi ini kemudian menjadi substrat bagi enzim [[reduktase]] di dalam sel untuk mereduksi substrat.<ref>{{Cite journal|last=Pollak|first=Nadine|last2=Dölle|first2=Christian|last3=Ziegler|first3=Mathias|date=1 Maret 2007|year=2007|title=The power to reduce: pyridine nucleotides – small molecules with a multitude of functions|url=https://portlandpress.com/biochemj/article/402/2/205/41836/The-power-to-reduce-pyridine-nucleotides-small|journal=Biochemical Journal|language=en|volume=402|issue=2|pages=205–218|doi=10.1042/BJ20061638|issn=0264-6021|pmc=PMC1798440|pmid=17295611}}</ref> [[Nikotinamida adenina dinukleotida]] eksis dalam bentuk yang saling berhubungan di dalam sel, yaitu NADH dan NADPH. Bentuk NAD<sup>+</sup>/NADH lebih penting pada reaksi katabolis , sedangkan NADP<sup>+</sup>/NADPH dipakai pada reaksi anabolik.<ref>{{Cite book|url=https://www.worldcat.org/oclc/607553259|title=Advances in food biochemistry|last=Fatih|first=Yildiz|date=|publisher=CRC Press|others=|year=2009|isbn=978-1-4200-0769-5|location=Boca Raton|pages=228|oclc=607553259}}</ref> |
|||
| ⚫ | |||
== Katabolisme == |
== Katabolisme == |
||
Revisi per 9 Juni 2020 01.47
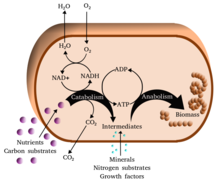

Metabolisme (Yunani: μεταβολισμος, metabolismos, perubahan) adalah seluruh reaksi kimia yang bertujuan untuk mempertahankan kehidupan yang terjadi di dalam suatu organisme
Tiga tujuan utama metabolisme yaitu:
- Konversi makanan menjadi energi untuk menjalankan proses pada tingkat seluler.
- Konversi makanan/bahan bakar menjadi bahan baku penyusun protein, lipid, asam nukleat dan beberapa jenis karbohidrat.
- Eliminasi limbah metabolis.
Reaksi-reaksi yang dikatalisis enzim ini memungkinkan organisme untuk tumbuh, bereproduksi,mempertahankan struktur, dan merespon lingkungannya.( kata metabolisme dapat diartikan sebagai semua reaksi kimia yang terjadi pada organisme hidup yang termasuk diantaranya pencernaan dan perpindahan zat di dalam dan di antara sel yang berbeda. Kelompok reaksi di atas yang terjadi pada tingkat sel dapat dikenal dengan nama metabolisme perantara atau metabolisme intermediat).
Reaksi kimia pada proses metabolisme terbagi atas beberapa lintasan metabolis, di mana satu senyawa dapat berubah melalui beberapa proses menjadi senyawa lain. Tiap proses difasilitasi dengan enzim yang bersifat spesifik
Secara umum, metabolisme memiliki dua arah lintasan reaksi kimia organik:
- Katabolisme, yaitu reaksi untuk menghasilkan energi dengan cara mengurai senyawa organik, seperti pemecahan glukosa menjadi piruvat oleh proses respirasi seluler.
- Anabolisme, yaitu reaksi yang memerlukan energi untuk menyusun (sintesis) senyawa organik seperti protein, karbohidrat, lipid, dan asam nukleat dari molekul-molekul tertentu.[1]
Kedua arah lintasan metabolisme diperlukan setiap organisme untuk dapat bertahan hidup. Arah lintasan metabolisme ditentukan oleh suatu senyawa yang disebut sebagai hormon, dan dipercepat (dikatalisis) oleh enzim. Pada senyawa organik, penentu arah reaksi kimia disebut promoter dan penentu percepatan reaksi kimia disebut katalis.
Pada setiap arah metabolisme, reaksi kimiawi melibatkan sejumlah substrat yang bereaksi dengan enzim sebagai katalis pada jenjang-jenjang reaksi guna menghasilkan senyawa intermediat, yang menjadi substrat pada jenjang reaksi berikutnya. Keseluruhan pereaksi kimia yang terlibat pada suatu jenjang reaksi disebut metabolom. Semua ini dipelajari pada suatu cabang ilmu biologi yang disebut metabolomika.
Enzim sangat krusial bagi proses metabolisme karena enzim memungkinkan suatu organisme mengatur reaksi yang diinginkan yang membutuhkan energi untuk tidak terjadi dengan sendirinya dengan cara memasangkan mereka . Pemasanan ini akan menghasilkan suatu reaksi spontan yang akan menghasilkan energi. Enzim yang berfungsi sebagai katalis akan memungkinkan suatu reaksi berjalan lebih cepat sekaligus mengatur laju suatu reaksi metabolis, misalnya sebagai respon terhadap perubahan lingkungan yang dialami sel atau sinyal dari sel lain. Laju metabolisme basal suatu organisme adalah ukuran jumlah energi yang dikonsumsi oleh semua reaksi kimia yang terjadi.
Sistem metabolisme suatu organisme menentukan senyawa mana yang merupakan nutrisi bagi tubuh atau bersifat racun. Misalnya, beberapa jenis prokariota memakai hidrogen sulfida sebagai nutrien, walaupun gas ini bersifat racun bagi hewan. Namun, ciri khusus metabolisme memiliki kesamaan pada hampir seluruh spesies yang berbeda. Misalnya, gugus asam karboksilat yang diketahui merupakan sebagai zat antara pada siklus asam sitrat, muncul pada semua organisme yang dikenal. Senyawa ini juga ditemukan pada spesies yang sangat berbeda seperti bakteri uniseluler Eschirichia coli dan organisme multiseluler berukuran besar seperti gajah .Kesamaan yang terdapat pada jalur metabolisme ini mungkin terjadi akibat keberadaanya pada sejarah evolusi awal dan retensinya karena efikasi yang ditimbulkan. Metabolisme sel kanker sangat berbeda dengan sel normal dan perbedaanya ini dapat digunakan sebagai intervensi terapeutik pada penyakit kanker
Senyawa biokimia kunci
Sebagian besar struktur yang menyusun hewan, tumbuhan dan mikroba tersusun atas empat gugus molekul dasar: asam amino, karbohidrat, asam nukleat, dan lipid (biasa dikenal dengan sebutan lemak). Makromolekul ini sangat vital bagi kehidupan, reaksi metabolis, baik yang bertujuan untuk membentuk molekul selama konstruksi sel dan jaringan atau menguraikannya dan menggunakannya sebagai sumber energi melalui proses pencernaan. Senyawa biokimia ini dapat digabungkan untuk membentuk polimer seperti DNA dan protein yang merupakan makromolekul esensial bagi kehidupan.
| Jenis molekul | Nama monomer | Nama polimer | Contoh bentuk polimer |
|---|---|---|---|
| Asam Amino | Asam amino | Protein (tersusun atas polipeptida) | Protein serabut dan protein globular |
| Karbohidrat | Monosakarida | Polisakarida | Amilum, glikogen dan selulosa |
| Asam nukleat | Nukleotida | Polinukleotida | DNA dan RNA |
Asam amino dan protein
Protein terdiri dari asam amino yang disusun menjadi sebuah rantai linier yang disatukan oleh ikatan peptida. Mayoritas protein berfungsi sebagai enzim yang dapat mengkatalisis reaksi kimia pada proses metabolisme. Selain enzim, protein memiliki fungsi struktural atau mekanik seperti sebagai penyusun sitoskeleton, suatu sistem perancah yang berfungsi untuk mempertahankan bentuk sel.[2] Protein memiliki beberapa fungsi seperti memproduksi cahaya pada kunang-kunang,membantu transpor oksigen dalam darah serta sebagai komponen penyusun keratin .[3] Asam amino berkontribusi dalam proses metabolisme energi seluler sebagai penyedia sumber karbon untuk memulai siklus asam sitrat, terutama ketika sumber energi utama, seperti glukosa menipis atau ketika sel mengalami keadaan represi katabolit kembali (Misalnya akibat stres metabolis).[4]
Lipid
Lipid adalah gugus senyawa biokimia yang paling beragam. Fungsi struktural utamanya adalah sebagai bagian membran biologis, baik sebagai membran internal dan membran eksternal, seperti membran sel atau sebagai sumber energi dan tempat penyimpanan energi.[5]Lipid didefinisikan sebagai molekul biologis yang bersifat hidrofobik atau amfifatik, tetapi dapat terlarut pada pelarut lipid, seperti eter, benzena, aseton atau kloroform.[6]. Lemak adalah gugus besar senyawa yang mengandung asam lemak dan gliserol; gliserol melekat pada asam lemak ester yang dikenal dengan nama triasilgliserida[7] Variasi dari lemak terdiri atas banyak variasi bentuk, misalnya spingosin yang merupakan rantai utama spingomielin , dan gugus hidrofilik , seperti fosfat yang ada di fosfolipid.. Steroid,seperti sterol adalah salah satu kelompok utama dari lipid[8]
Karbohidrat

Karbohidrat adalah senyawa aldehida dan keton dengan banyak gugus hidroksil yang menempel dalam bentuk rantai lurus atau cincin. Karbohidrat adalah molekul biologis paling berlimpah dan memiliki banyak fungsi, seperti tempat penyimpanan atau transpor energi( (amilum dan glikogen) dan juga merupakan komponen penyusun dari suatu senyawa pada organisme (selulosa pada tumbuhan dan kitin pada hewan [9]. Unit paling sederhana dari karbohidrat dikenal dengan nama monosakarida yang terdiri atas galaktosa, fruktosa dan yang senyawa yang paling penting bagi organisme, yaitu glukosa. Monosakarida akan saling terikat dengan monoskarida lain dan membentuk polisakarida dalam pelbagai bentuk yang tak terhitung jumlahnya. [10]
Nukleotida
Dua jenis asam nukleat , yaitu DNA dan RNA merupakan polimer dari nukleotida. Tiap nukleotida disusun atas fosfat yang menempel pada gugus gula ribosa atau deoksiribosa yang menempel pada basa nitrogen. Asam nukleat memiliki fungsi penting sebagai penyimpanan dan penggunaan informasi genetik yang akan dinterpretasi melalui proses transkripsi dan translasi dalam proses biosintesis protein.[11] Informasi genetik yang terkandung di dalam asam nukleat dilindungi oleh mekanisme perbaikan DNA dan diperbanyak pada proses replikasi DNA. Banyak virus memiliki genom RNA seperti HIV, yang menggunakan proses transkripsi balik untuk membuat templat DNA dari genom virus RNAnya. [12] Molekul RNA yang berada di dalam ribozim, seperti spliosom atau ribosom mirip dengan enzim yang mampu mengkatalisis reaksi kimia. Nukleosida adalah penyusun nukleotida yang merupakan nukleobasa yang menempel pada gula ribosa. Basa nukleotida memiliki bentuk cincin heterosiklik yang mengandung nitrogen yang diklasifisikasikan menjadi dua macam, yaitu purina atau pirimidina. Nukleotida juga dapat berfungsi sebagai koenzim pada reaksi transfer gugus metabolis.[13]

Koenzim
Metabolisme melibatkan banyak reaksi kimia, tetapi sebagian besar reaksi tersebut dikategorikan ke dalam jenis reaksi sederhana yang melibatkan perpindahan gugus fungsional suatu atom serta ikatannya di dalam suatu molekul.[14] Kimia sederhana ini memungkinkan pengunaaan kelompok senyawa intermediat untuk membawa gugus senyawa kimia ini berpindah diantara reaksi-reaksi yang berbeda.[15]Kelompok senyawa intermediat yang berfungsi untuk memindahkan gugus tersebut, dikenal dengan nama koenzim. Tiap kelompok reaksi dikendalikan oleh suatu koenzim tertentu, yang menjadi substrat untuk kelompok enzim yang memproduksinya sekaligus enzim yang memakainya. Koenzim ini terus-menerus dibuat, dipakai dan didaur ulang[16]
Salah satu koenzim utama yang ada didalam tubuh ialah ATP (Adenosina Trifosfat) yang merupakan sumber energi universal di dalam sel. Jenis nukleotida ini digunakan untuk memindahkan energi kimiawi diantara reaksi kimia berbeda. Hanya ada sedikit ATP di dalam tubuh, namun ATP terus menerus diregenerasi sehingga tubuh manusia dapat menggunakan ATP dengan jumlah yang setara dengan berat badan tubuhnya. [17] [18]ATP bertindak sebagai jembatan penghubung katabolisme dan anabolisme. Katabolisme menguraikan molekul dan katabolisme menyatukannya kembali. Reaksi katabolisme menghasilkan ATP dan reaksi anabolis memakainya. ATP juga berfungsi sebagai pembawa gugus fosfat dalam reaksi fosforilasi [19]
Vitamin merupakan senyawa organik yang dibutuhkan dalam jumlah yang sedikit yang tidak dapat diproduksi oleh sel di dalam tubuh manusia. Pada nutrisi manusia, vitamin berfungsi sebagai koenzim, setelah mengalami modifikasi. Misalnya, vitamin larut air akan mengalami fosforilasi dan berpasangan dengan nukleotida ketika dipakai oleh sel.[20] Nikotinamida adenina dinukleotida (NAD+) adalah senyawa turunan vitamin B3(niasin) yang merupakan koenzim penting yang bertindak sebagai reseptor molekul hidrogen. Ratusan jenis enzim dehidrogenase melepas elektron dari substrat dan mereduksi NAD+ menjadi NADH. Koenzim yang telah direduksi ini kemudian menjadi substrat bagi enzim reduktase di dalam sel untuk mereduksi substrat.[21] Nikotinamida adenina dinukleotida eksis dalam bentuk yang saling berhubungan di dalam sel, yaitu NADH dan NADPH. Bentuk NAD+/NADH lebih penting pada reaksi katabolis , sedangkan NADP+/NADPH dipakai pada reaksi anabolik.[22]
Katabolisme
Katabolisme adalah serangkaian proses metabolisme yang memecah molekul-molekul besar, termasuk juga memecah dan mengoksidasi molekul makanan. Tujuan dari reaksi katabolik adalah untuk menyediakan energi dan komponen yang dibutuhkan oleh reaksi anabolik dalam rangka membangun molekul.
Katabolisme karbohidrat
Glikolisis
Glikolisis adalah proses metabolisme yang mengubah glukosa menjadi piruvat, menghasilkan dua mol ATP, dua mol NADH, dan dua mol piruvat per mol glukosa.[1] Glikolisis dimulai dengan pengambilan glukosa ekstraseluler dan pengolahan glukosa intraseluler berikutnya dalam sitosol untuk akhirnya menghasilkan piruvat bersama dengan berbagai produk lainnya. Metabolisme glikolitik merupakan jalur yang relatif tidak efisien untuk pembentukan ATP seluler, hanya menerima bersih dua molekul ATP per unit glukosa. Namun, metabolisme glikolitik memberikan manfaat utama bagi sel karena juga memungkinkan untuk reduksi NAD+ menjadi NADH, yang digunakan oleh banyak enzim sebagai kofaktor, serta memungkinkan pengalihan produk antara pada lintasan biosintesis untuk mendukung proses anabolik.
Nasib piruvat tergantung pada banyak faktor di antaranya ketersediaan oksigen, yang merupakan salah satu yang paling penting. Dalam kondisi anaerob, piruvat direduksi menjadi laktat oleh laktat dehidrogenase. Dengan adanya oksigen, mitokondria dapat sepenuhnya mengoksidasi piruvat dan NADH dari glikolisis, menghasilkan hingga 36 mol ATP per mol glukosa menggunakan fosforilasi oksidasi.[23]
Jalur pentosa fosfat
Jalur pentosa fosfat atau jalur fosfoglukonat, terjadi di sitosol dan menyediakan beberapa tujuan utama yang mendukung proliferasi dan kelangsungan hidup sel. Pertama, dan yang paling terkenal, jalur pentosa fosfat memungkinkan pengalihan senyawa antara dari jalur glikolitik menuju produksi prekursor nukleotida dan asam amino yang diperlukan untuk pertumbuhan dan proliferasi sel. Jalur ini melibatkan cabang non-oksidatif dari jalur pentosa fosfat. Fungsi kunci kedua dari jalur pentosa fosfat yaitu menghasilkan reduksi ekuivalen NADPH, yang memiliki peran penting dalam pemeliharaan lingkungan redoks seluler yang menguntungkan dan juga diperlukan untuk sintesis asam lemak. Jalur ini melibatkan cabang oksidatif dari cabang pentosa fosfat.[24]
Pemecahan glikogen menjadi glukosa
Glikogen adalah bentuk penyimpanan polimer glukosa. Glikogenolisis yaitu proses pemecahan glikogen, yang terjadi di sel otot dan sel liver dalam merespon hormon epinefrin dan glukagon. Dalam suatu kondisi kelaparan, butuh glukosa tinggi, atau dalam keadaan bahaya, maka sel alpha pankreas akan merilis glukagon, sementara itu kelenjar adrenal akan merilis epinefrin. Di dalam liver, glukagon dan epinefrin berikatan pada GPCR yang berbeda, namun keduanya berinteraksi dan mengaktifkan protein Galpha s yang sama. Karena itu, kedua hormon menghasilkan respon metabolisme yang sama, yaitu aktivasi adenilat siklase dan peningkatan level cAMP.[25]
Glikogenolisis melibatkan proses pembuangan residu glukosa dari satu ujung polimer dengan reaksi fosforolisis, yang dikatalisis oleh glikogen fosforilase (GP) menghasilkan glukosa-1-fosfat. Glukosa-1-fosfat selanjutnya dikonversi menjadi glukosa-6-fosfat. Proses ini terjadi baik di sel otot maupun sel liver. Pada sel otot, glukosa-6-fosfat masuk ke siklus glikolisis dan dimetabolisme mejadi ATP yang digunakan untuk kontraksi otot. Sedangkan di sel liver, glukosa-6-fosfat diubah menjadi glukosa. Ini karena di sel liver ada enzim bernama fosfatase, yang mampu menghidrolisis glukosa-6-fosfat menjadi glukosa. Sehingga di liver, penyimpanan glikogen dibongkar menjadi glukosa, lalu dengan cepat dikeluarkan ke darah disebar ke jaringan lain misal otot dan otak, untuk memberi makan sel-sel tersebut.[25]
PKA aktif mendorong konversi glikogen menjadi glukosa-1-fosfat melalui dua cara yaitu menghambat sintesis glikogen dan menstimulasi degradasi glikogen. Untuk cara pertama, PKA memfosforilasi enzim penting dalam sintesis glikogen yaitu glikogen sintase (GS), dimana jika enzim ini difosforilasi (dikasih fosfat) membuat dia tidak aktif. Untuk cara kedua, PKA memfosforilasi enzim perantara penting yaitu glikogen fosforilase kinase (GPK). Bedanya dengan enzim GS, fosforilasi justru membuat GPK aktif. GPK yang aktif ini kemudian memfosforilasi enzim berikutnya yaitu glikogen fosforilase (GP) pada residu serin14 yang selanjutnya mendegradasi glikogen menjadi glukosa-1-fosfat.[25]
Katabolisme lipid
Oksidasi asam lemak
Jalur oksidasi asam lemak memungkinkan konversi asam lemak mitokondria menjadi banyak produk yang selanjutnya dapat digunakan sel untuk menghasilkan energi, termasuk asetil-KoA, NADH dan FADH2. Langkah awal oksidasi asam lemak adalah 'aktivasi' asam lemak dalam sitosol melalui reaksi yang diperantarai enzim dengan ATP untuk akhirnya menghasilkan asam lemak asil-KoA. Mekanisme oksidasi asam lemak selanjutnya tergantung pada panjang ekor alifatik dalam asam lemak.[24]
Asam lemak rantai pendek, yang didefinisikan memiliki kurang dari enam karbon di ekor alifatik, hanya mampu berdifusi menjadi mitokondria secara pasif. Asam lemak rantai panjang dan rantai panjang pertama-tama harus terkonjugasi ke karnitin melalui karnitin palmitoil transferase I (CPT1). Setelah ini, asam lemak rantai panjang terkonjugasi karnitin kemudian dipindahkan ke mitokondria di mana ia diubah kembali menjadi asam lemak asil-KoA melalui penghilangan karnitin oleh karnitin palmitoyl transferase II (CPT2). Pada tahap ini, β-oksidasi asam lemak asil-CoA dimulai, menghasilkan sejumlah besar asetil-KoA, NADH dan FADH2 yang selanjutnya digunakan dalam siklus TCA dan rantai transpor elektron untuk menghasilkan ATP. [24]
CPT1A bertindak sebagai langkah pengaturan utama dalam oksidasi asam lemak, karena membatasi laju dan dihambat oleh zat antara sintesis lipid malonyl-CoA, sehingga mencegah oksidasi lipid ketika sel secara aktif mensintesis lipid. Secara keseluruhan, oksidasi asam lemak dapat memungkinkan produksi ATP dalam jumlah yang luar biasa, dengan oksidasi β lengkap dari molekul palmitat tunggal (asam lemak utama dalam sel mamalia) akhirnya memiliki potensi untuk menghasilkan lebih dari 100 molekul ATP.[24]
Pemecahan kolesterol
Pada orang dewasa, banyak jaringan mampu menyintesis kolesterol. Produk hewani merupakan sumber kolesterol, sedangkan tumbuhan tidak memiliki kolesterol. Namun membran pada sel tumbuhan mengandung fitosterol, yang secara struktural mirip dengan kolesterol dan berguna dalam pengobatan diet hiperkolesterolemia karena mereka bersaing saat penyerapan kolesterol. Hati dan usus merupakan situs kuantitatif yang paling penting untuk metabolisme kolesterol pada manusia, meskipun sejumlah kecil kolesterol juga hilang melalui pergantian kulit yang normal.[26]
Anabolisme
Jalur anabolisme yang membentuk senyawa-senyawa dari prekursor sederhana mencakup:
- Glikogenesis, pembentukan glikogen dari glukosa.
- Glukoneogenesis, pembentukan glukosa dari senyawa organik lain.
- Jalur sintesis porfirin
- Jalur HMG-CoA reduktase, mengawali pembentukan kolesterol dan isoprenoid.
- Metabolisme sekunder, jalur-jalur metabolisme yang tidak esensial bagi pertumbuhan, perkembangan, maupun reproduksi, namun biasanya berfungsi secara ekologis, misalnya pembentukan alkaloid dan terpenoid.
- Fotosintesis
- Siklus Calvin dan fiksasi karbon
Sintesis komponen pembangun
Komponen lipid
Lipid dalam sel ditemukan dalam lemak penyimpanan, dalam lipoprotein (kombinasi lipid dan protein), dan dalam membran sel dan organel. Komponen pembangun lipid yaitu gliserol, asam lemak, dan sejumlah senyawa lain (misalnya serin, inositol, etanolamin).
Gliserol. Gliserol berasal dari zat antara glikolisis yaitu dihidroksiaseton fosfat, yang kemudian direduksi menjadi gliserol 1-fosfat dengan bantuan katalisis oleh gliserol 1-fosfat dehidrogenase.[27]
Asam lemak. Jalur sintesis asam lemak memungkinkan sel untuk menghasilkan lipid yang diperlukan untuk pertumbuhan sel dan proliferasi dari prekursor yang berasal dari jalur metabolisme intrinsik lainnya. Aktivitas jalur sintesis asam lemak sangat terkait dengan pensinyalan mTOR, yang telah terbukti mendorong sintesis asam lemak melalui regulasi banyak enzim utama yang bertanggung jawab untuk sintesis lipid de novo, termasuk SREBP (protein pengikat elemen pengatur sterol), FASN (asam lemak sintase) dan ACC (asetil CoA karboksilase), di mana keduanya diinduksi oleh SREBP. [24]
Sintesis asam lemak menggunakan produk yang berasal dari beberapa jalur metabolisme lainnya, terutama glikolisis, siklus TCA, dan jalur pentosa fosfat. Untuk sintesis asam lemak rantai lurus, sitrat yang berasal dari siklus TCA dapat diekspor dari mitokondria ke sitosol melalui pembawa sitrat, di mana ATP sitrat lyase mengubahnya menjadi asetil-koA, bersama dengan oksaloasetat. Asetil-KoA yang berasal dari proses ini kemudian dapat dikarboksilasi oleh ACC untuk menghasilkan malonil-KoA. Selanjutnya, FASN bertindak dalam cara yang tergantung pada NADPH untuk memperpanjang rantai asam lemak yang baru terbentuk sampai produk seperti asam palmitat disintesis. Asam lemak dengan panjang rantai alternatif dapat disintesis menggunakan asam palmitat sebagai substrat untuk pemanjangan, sementara reaksi desaturasi dapat dilakukan untuk menghasilkan asam lemak tak jenuh.[24]
Sintesis asam lemak rantai cabang berbeda dengan sintesis asam lemak lurus, yaitu membutuhkan asam amino rantai cabang seperti valin dan leusin sebagai substrat untuk perpanjangan. Lebih lanjut, asam lemak dapat dikondensasikan dengan gliserol produk dari glikolisis untuk menghasilkan banyak kemungkinan kombinasi triasilgliserol dan fosfolipid, yang merupakan komponen kunci dari banyak struktur seluler.[24]
Fosfatidilkolin. Pada sebagian besar sel, fosfatidilkolin disintesis melalui jalur sitidin 5-difosfat (CDP)-kolin, di mana kolin difosforilasi menjadi fosfokolin oleh kolin kinase kemudian dikonversi menjadi CDP-kolin oleh CPT:fosfokolin sitidiltransferase. Selanjutnya, CDP-kolin dikombinasikan dengan diasilgliserol oleh dua enzim yang terintegrasi ke retikulum endoplasma: CDP-kolin:1,2-diasilgliserol kolinfosfotransferase (CPT) dan CDP-kolin: 1,2-diasilgliserol kolin/etanolamin fosfotransferase (CEPT). Jalur CDP-kolin terdapat di semua sel mamalia berinti. Namun, di hati, hingga 30% fosfatidilkolin dihasilkan oleh konversi fosfatidletanolamin menjadi fosfatidilkolin oleh fosfatidiletanolamin N-metiltransferase (PEMT).[28]
Fosfatidiletanolamin. Fosfatidiletanolamin dapat disintesis oleh dua jalur utama: jalur CDP-etanolamin di retikulum endoplasma dan jalur fosfatidilserin dekarboksilase (PSD) di mitokondria. Jalur CDP-etanolamin mirip dengan sintesis fosfatidilkolin. Fosfoetanolamin diubah menjadi CDP-etanolamin oleh CTP:fosfoetanolamin sitidiltransferase kemudian ditambahkan ke diasilgliserol oleh CEPT untuk membentuk fosfatidiletanolamin. Jalur PSD terjadi secara eksklusif di mitokondria, di mana fosfatidilserin didekarboksilasi oleh PSD untuk membentuk fosfatidiletanolamin. Sintesis fosfatidilserin, yang dikendalikan oleh dua sintase fosfatidilserin, merupakan langkah pembatas laju untuk sintesis fosfatidiletanolamin pada jalur PSD.[28]
Asam amino
Sintesis makomolekul
Xenobiotika dan metabolisme redoks
Metabolisme obat
Jalur metabolisme obat, yaitu modifikasi dan penguraian obat-obatan dan senyawa ksenobiotik lainnya melalui sistem enzim khusus mencakup:
Regulasi dan kontrol
Karena lingkungan sebagian besar organisme terus berubah, reaksi metabolisme harus diatur dengan baik untuk mempertahankan serangkaian kondisi konstan dalam sel, suatu kondisi yang disebut homeostasis.[29][30] Regulasi metabolik juga memungkinkan organisme untuk merespons sinyal dan berinteraksi aktif dengan lingkungannya.[31]
Sejarah

Eksperimen terkontrol atas metabolisme manusia pertama kali diterbitkan oleh Santorio Santorio pada tahun 1614 di dalam bukunya, Ars de statica medecina yang membuatnya terkenal di Eropa. Dia mendeskripsikan rangkaian percobaan yang dilakukannya, yang melibatkan penimbangan dirinya sendiri pada sebuah kursi yang digantung pada sebuah timbangan besar (lihat gambar) sebelum dan sesudah makan, tidur, bekerja, berhubungan seksual, berpuasa makan atau minum, dan buang air besar. Dia menemukan bahwa bagian terbesar makanan yang dimakannnya hilang dari tubuh melalui perspiratio insensibilis (mungkin dapat diterjemahkan sebagai "keringatan yang tidak tampak").
Lihat pula
Referensi
- ^ a b (Inggris) "Overview of Metabolism". ElmHurst College. Diakses tanggal 2010-06-23.
- ^ Michie, Katharine A.; Löwe, Jan (2006-06). "Dynamic Filaments of the Bacterial Cytoskeleton". Annual Review of Biochemistry (dalam bahasa Inggris). 75 (1): 467–492. doi:10.1146/annurev.biochem.75.103004.142452. ISSN 0066-4154.
- ^ Nelson & Cox 2017, hlm. 187.
- ^ Hothersall, John S.; Ahmed, Aamir (2013-02-04). "Metabolic Fate of the Increased Yeast Amino Acid Uptake Subsequent to Catabolite Derepression". Journal of Amino Acids (dalam bahasa Inggris). doi:10.1155/2013/461901. PMC 3575661
 . PMID 23431419. Diakses tanggal 2020-06-06.
. PMID 23431419. Diakses tanggal 2020-06-06.
- ^ Nelson & Cox 2017, hlm. 225.
- ^ Attwood T K, Campbell P N, Parish J H, Smith A D, Stirling J L, Vella F (2006). Oxford dictionary of biochemistry and molecular biology. Cammack, Richard, Ph. D. (edisi ke-Rev. ed). Oxford: Oxford University Press. hlm. 388. ISBN 978-0-19-852917-0. OCLC 65467611.
- ^ "Lipid nomenclature Lip-1 & Lip-2". www.qmul.ac.uk. Diakses tanggal 2020-06-06.
- ^ Berg JM, Tymoczko, JL, Gatto GJ Jr , Stryer L. (8 April 2015). Biochemistry (edisi ke-8). New York: W. H. Freeman. hlm. 362. ISBN 978-1-4641-2610-9. OCLC 913469736.
- ^ Nelson & Cox 2017, hlm. 324-336.
- ^ Raman, Rahul; Raguram, S.; Venkataraman, Ganesh; Paulson, James C.; Sasisekharan, Ram (21 Oktober 2005). "Glycomics: an integrated systems approach to structure-function relationships of glycans". Nature Methods (dalam bahasa Inggris). 2 (11): 817–824. doi:10.1038/nmeth807. ISSN 1548-7105.
- ^ Nelson & Cox 2017, hlm. 717-752.
- ^ Sierra, Saleta; Kupfer, Bernd; Kaiser, Rolf (2005-12-01). "Basics of the virology of HIV-1 and its replication". Journal of Clinical Virology. Focus on HIV (dalam bahasa Inggris). 34 (4): 233–244. doi:10.1016/j.jcv.2005.09.004. ISSN 1386-6532.
- ^ Wimmer M, Rose I (1978). "Mechanisms of enzyme-catalyzed group transfer reactions". Annu Rev Biochem. 47: 1031–78. doi:10.1146/annurev.bi.47.070178.005123. PMID 354490.
- ^ Mitchell, Peter (Maret 1979). "Compartmentation and Communication in Living Systems. Ligand Conduction: a General Catalytic Principle in Chemical, Osmotic and Chemiosmotic Reaction Systems". European Journal of Biochemistry (dalam bahasa Inggris). 95 (1): 1–20. doi:10.1111/j.1432-1033.1979.tb12934.x. ISSN 1432-1033.
- ^ Wimmer, Mary J.; Rose, Irwin A. (1 Juni 1978). "Mechanisms of Enzyme-Catalyzed Group Transfer Reactions". Annual Review of Biochemistry. 47 (1): 1031–1078. doi:10.1146/annurev.bi.47.070178.005123. ISSN 0066-4154.
- ^ Dimroth P, von Ballmoos C, Meier T (March 2006). "Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series". EMBO Rep. 7 (3): 276–82. doi:10.1038/sj.embor.7400646. PMC 1456893
 . PMID 16607397.
. PMID 16607397.
- ^ Dimroth P, von Ballmoos C, Meier T (March 2006). "Catalytic and mechanical cycles in F-ATP synthases: Fourth in the Cycles Review Series". EMBO Rep. 7 (3): 276–82. doi:10.1038/sj.embor.7400646. PMC 1456893
 . PMID 16607397.
. PMID 16607397.
- ^ Dimroth, Peter; von Ballmoos, Christoph; Meier, T (1 Maret 2006). "Catalytic and mechanical cycles in F-ATP synthases". EMBO reports. 7 (3): 276–282. doi:10.1038/sj.embor.7400646. ISSN 1469-221X. PMC 1456893
 . PMID 16607397.
. PMID 16607397.
- ^ Bonora, Massimo; Patergnani, Simone; Rimessi, Alessandro; De Marchi, Elena; Suski, Jan M.; Bononi, Angela; Giorgi, Carlotta; Marchi, Saverio; Missiroli, Sonia (12 September 2012). "ATP synthesis and storage". Purinergic Signalling (dalam bahasa Inggris). 8 (3): 343–357. doi:10.1007/s11302-012-9305-8. ISSN 1573-9538. PMC 3360099
 . PMID 22528680.
. PMID 22528680.
- ^ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). "Vitamins Are Often Precursors to Coenzymes". Biochemistry. 5th edition (dalam bahasa Inggris).
- ^ Pollak, Nadine; Dölle, Christian; Ziegler, Mathias (1 Maret 2007). "The power to reduce: pyridine nucleotides – small molecules with a multitude of functions". Biochemical Journal (dalam bahasa Inggris). 402 (2): 205–218. doi:10.1042/BJ20061638. ISSN 0264-6021. PMC 1798440
 . PMID 17295611.
. PMID 17295611.
- ^ Fatih, Yildiz (2009). Advances in food biochemistry. Boca Raton: CRC Press. hlm. 228. ISBN 978-1-4200-0769-5. OCLC 607553259.
- ^ Salway, J. G. Metabolism at a Glance 20–21 (Blackwell Publishing, Oxford, UK, 2004).
- ^ a b c d e f g O'Neill, Luke A. J.; Kishton, Rigel J.; Rathmell, Jeff (09 2016). "A guide to immunometabolism for immunologists". Nature Reviews. Immunology. 16 (9): 553–565. doi:10.1038/nri.2016.70. ISSN 1474-1741. PMC 5001910
 . PMID 27396447.
. PMID 27396447.
- ^ a b c Lodish, Harvey; Berk, Arnold; Kaiser, Chris A.; Krieger, Monty; Bretscher, Anthony; Ploegh, HIddle; Amon, Angelika (2016). Molecular cell biology (edisi ke-Eighth edition). New York: WH Freeman and Company. hlm. 705. ISBN 9781464183393. OCLC 949909675.
- ^ Shlomo,, Melmed,; S.,, Polonsky, Kenneth; Reed,, Larsen, P.; Henry,, Kronenberg,. Williams textbook of endocrinology (edisi ke-Thirteenth edition). Philadelphia, PA. ISBN 0323341578. OCLC 932080537.p1664
- ^ "Metabolism - Anaplerotic routes". Encyclopedia Britannica (dalam bahasa Inggris). Diakses tanggal 2019-02-01.
- ^ a b Yang, Qin; Vijayakumar, Archana; Kahn, Barbara B. (2018-10). "Metabolites as regulators of insulin sensitivity and metabolism". Nature Reviews. Molecular Cell Biology. 19 (10): 654–672. doi:10.1038/s41580-018-0044-8. ISSN 1471-0080. PMID 30104701.
- ^ Albert R (2005). "Scale-free networks in cell biology". J Cell Sci. 118 (Pt 21): 4947–57. arXiv:q-bio/0510054
 . doi:10.1242/jcs.02714. PMID 16254242.
. doi:10.1242/jcs.02714. PMID 16254242.
- ^ Brand M (1997). "Regulation analysis of energy metabolism". J Exp Biol. 200 (Pt 2): 193–202. PMID 9050227.
- ^ Soyer O, Salathé M, Bonhoeffer S (2006). "Signal transduction networks: topology, response and biochemical processes". J Theor Biol. 238 (2): 416–25. doi:10.1016/j.jtbi.2005.05.030. PMID 16045939.
Bacaan lebih lanjut
- Aryulina, Diah (2007). Biologi 3 SMA dan MA Untuk Kelas XII. Jakarta: Esis/Erlangga. ISBN 974-734-551-3. (Indonesia)

