Penyakit seliak
| Penyakit seliak | |
|---|---|
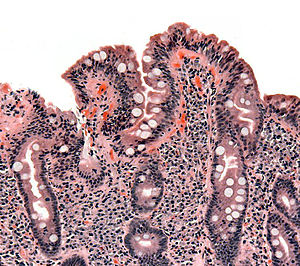 | |
| Biopsi dari usus halus yang menunjukkan penyakit seliak yang dapat dilihat dengan menumpulkan villus usus,hipertrofi crypt, dan limfosit infiltrasi crypts | |
| Informasi umum | |
| Pelafalan | |
| Spesialisasi | Gastroenterologi, obat penyakit dalam |
| Penyebab | Reaksi terhadap gluten[1] |
| Aspek klinis | |
| Gejala dan tanda | Tidak ada atau non-specific, distensi abdomen, diare, konstipasi, malabsorption, penurunan berat badan, dermatitis herpetiformis[2][3] |
| Komplikasi | Anemia, osteoporosis, mandul, kanker, masalah neurologis, lainnya penyakit autoimun[4][5][6][7] |
| Awal muncul | Seua umur [2][8] |
| Durasi | Seumur hidup [9] |
| Diagnosis | Riwayat keluarga, tes darah antibodi, usus biopsi, pengujian genetik, respon pada penarikan gluten [10][10][11] |
| Kondisi serupa | Penyakit Inflamasi usus, parasit usus, sindrom iritasi usus, fibrosis kistik[12] |
| Perawatan | Diet bebas Gluten[13] |
| Prevalensi | ~1 dari 135[14] |
Penyakit seliak adalah gangguan autoimun jangka panjang yang mempengaruhi usus kecil.[10] Gejala klasik termasuk masalah gastrointestinal seperti diare kronis, distensi abdomen, malabsorpsi, hilangnya nafsu makan dan diantara anak-anak gagal untuk tumbuh secara normal.[2] Penyakit ini biasanya dimulai pada usia enam bulan dan dua tahun.[2] Gejala non-klasik lebih umum, terutama pada orang yang lebih tua.[8][15][16][17] Mungkin ada beberapa gejala.[2] Penyakit seliak pertama kali dijelaskan pada anak-anak;[8][9] namun, dapat menjangkit segala usia.[2][8] Hal ini terkait dengan penyakit autoimun lainnya, seperti diabetes mellitus tipe 1 dan tiroiditis.[9]
Penyakit seliak disebabkan oleh reaksi terhadap gluten, yang sama seperti butiran gandum dan rye.[1][18][19] Jumlah oat yang moderat, bebas kontaminasi dengan biji-bijian lain yang mengandung gluten, biasanya ditoleransi.[18][20] Terjadinya penyakit ini mungkin tergantung pada jenis oat yang dikonsumsi.[18][20] Penyakit ini terjadi pada orang yang secara genetis memiliki kecenderungan.[10] Setelah terpapar oleh gluten, respons imun abnormal dapat menyebabkan produksi beberapa autoantibodi yang berbeda yang dapat mempengaruhi sejumlah organ yang berbeda.[5][21] Dalam usus kecil, ini menyebabkan reaksi peradangan dan dapat memendekkan vili yang melapisi usus kecil (vili atrofi).[10][11] Hal ini mempengaruhi penyerapan nutrisi, yang sering menyebabkan anemia.[10][19]
Diagnosis biasanya dibuat oleh kombinasi tes antibodi darah dan biopsi usus, dibantu oleh uji genetik secara spesifik.[10] Membuat diagnosis tidak selalu mudah.[22] Seringkali, autoantibodi dalam darah negatif,[23][24] dan banyak orang hanya mengalami perubahan usus kecil dengan vili yang normal.[16][25] Orang-orang mungkin memiliki gejala berat dan diteliti selama bertahun-tahun sebelum diagnosis tercapai.[26] Semakin banyak, diagnosis dibuat pada orang tanpa gejala, sebagai akibat dari skrining.[27] Bukti dari efek penyaringan, tidak akan cukup untuk menentukan kegunaannya.[28] Sementara penyakit ini disebabkan oleh intoleransi permanen terhadap protein gandum, dan itu bukan bentuk dari alergi gandum.[10]
Satu-satunya pengobatan yang dikenal paling efektif sejauh ini adalah diet bebas gluten seumur hidup, yang mengarah pada pemulihan mukosa usus, mengurangi gejala dan mengurangi risiko adanya komplikasi pada kebanyakan orang.[13] Jika penyakit ini tidak diobati, dapat menyebabkan kanker seperti limfoma usus dan risiko kematian dini yang meningkat.[4] Angkanya bervariasi di berbagai wilayah di dunia, mulai dari 1 dari 300 hingga 1 dari 40, dengan rata-rata antara 1 dari 100 dan 1 dari 170 orang.[14] Di negara-negara maju, diperkirakan bahwa 80% kasus tidak terdiagnosis, biasanya karena sedikitnya keluhan gastrointestinal atau karena kurangnya kesadaran akan kondisi ini.[6][29] Penyakit seliak lebih sering terjadi pada wanita dibandingkan pada pria.[30] Istilah "seliak" berasal dari bahasa Yunani κοιλιακός (koiliakó, "perut") dan disahkan oleh Aretaeus dari Kapadokia.[31][32]
Tanda dan gejala
[sunting | sunting sumber]Pucat, tinja atau kotoran yang berminyak (steatorrhoea) dan penurunan berat badan atau sulit untuk menambahkan berat badan merupakan gejala klasik penyakit ini. Gejala lainnya yang lebih umum biasanya tidak terlihat yang terutama terjadi pada organ selain dari usus itu sendiri.[33] Juga memungkinkan untuk menderita penyakit celiac tanpa gejala klasik apapun.[34] Inilah yang mewakili 43% kasus pada anak-anak.[35] Banyak orang dewasa dengan penyakit ini hanya mengalami kelelahan atau anemia.[36] Kebanyakan yang tidak terdiagnosis dianggap tidak bergejala namun sebenarnya tidak, tetapi karena mereka telah terbiasa hidup dengan status kesehatan yang buruk menjadikan seolah-olah itu normal atau hal biasa, dan mereka sebenarnya dapat mengenali bahwa mereka memiliki gejala yang berkaitan dengan penyakit seliak setelah memulai diet bebas gluten dan perbaikan yang terlihat jelas, dan berbeda dengan situasi sebelum dimulainya diet bebas gluten.[37][38][39]
Penyebab
[sunting | sunting sumber]Penyakit seliak disebabkan oleh reaksi pada gliadin dan glutenin (protein gluten) [40] yang ditemukan dalam gandum, dan protein serupa yang ditemukan pada tanaman dari suku Triticeae (yang termasuk biji-bijian umum lainnya seperti barley dan rye) [34] dan suku Aveneae (oats).[41] Subspesies gandum (yang dieja, durum dan Kamut) dan hibrida gandum (seperti triticale) juga menginduksi gejala penyakit seliak.[42][43]
Sejumlah orang yang menderita seliak bereaksi terhadap oat.[34] Pengaruh oat pada orang yang menderita seliak tergantung pada oat yang dikonsumsi kultivar karena adanya gen prolamin, sekuens asam amino protein, dan immunoreactivities dari prolamin beracun, yang berbeda di antara varietas oat itu sendiri.[44][45] Juga, oat sering terkontaminasi silang dengan biji-bijian lain yang mengandung gluten.[44][46][47] "Oat murni" berarti gandum yang tidak terkontaminasi dengan sereal yang mengandung gluten lainnya.[44] Efek jangka panjang dari konsumsi gandum murni masih belum jelas [48] dan penelitian lebih lanjut mengidentifikasi kultivar yang diperlukan sebelum membuat rekomendasi pada inklusi mereka dalam program diet bebas gluten.[49] Orang yang menderita penyakit seliak dan lebih memilih untuk mengkonsumsi gandum membutuhkan tindak lanjut yang lebih ketat, termasuk kinerja periodik dari biopsi usus.[50]
Diagnosa
[sunting | sunting sumber]Diagnosa sering kali sangat sulit sehingga kebanyakan kasus didiagnosa dengan tingkat penundaan yang besar.[51] Ada beberapa tes yang bisa dilalukan. Tingkatan gejala dapat menentukan urutan dari tes, tetapi semua tes kehilangan kegunaannya apabila orang tersebut sudah melakukan diet bebas gluten. Kerusakan usus mulai sembuh dalam beberapa minggu setelah diet dilakukan, dan tingkat antibodi akan menurun selama berbulan-bulan. Bagi mereka yang sudah menjalankan diet bebas gluten, mungkin perlu menghindari beberapa makanan yang mengandung gluten dalam satu kali makan dalam sehari selama 6 minggu sebelum mengulangi penyelidikan.[52]
Referensi
[sunting | sunting sumber]- ^ a b Tovoli F, Masi C, Guidetti E, Negrini G, Paterini P, Bolondi L (March 2015). "Clinical and diagnostic aspects of gluten related disorders". World Journal of Clinical Cases (Review). 3 (3): 275–84. doi:10.12998/wjcc.v3.i3.275. PMC 4360499
 . PMID 25789300.
. PMID 25789300.
- ^ a b c d e f Fasano A (Apr 2005). "Clinical presentation of celiac disease in the pediatric population". Gastroenterology (Review). 128 (4 Suppl 1): S68–73. doi:10.1053/j.gastro.2005.02.015. PMID 15825129.
- ^ "Symptoms & Causes of Celiac Disease | NIDDK". National Institute of Diabetes and Digestive and Kidney Diseases. June 2016. Diarsipkan dari versi asli tanggal 24 April 2017. Diakses tanggal 24 April 2017.
- ^ a b Lebwohl B, Ludvigsson JF, Green PH (October 2015). "Celiac disease and non-celiac gluten sensitivity". BMJ (Review). 351: h4347. doi:10.1136/bmj.h4347. PMC 4596973
 . PMID 26438584.
. PMID 26438584. Celiac disease occurs in about 1% of the population worldwide, although most people with the condition are undiagnosed. It can cause a wide variety of symptoms, both intestinal and extra-intestinal because it is a systemic autoimmune disease that is triggered by dietary gluten. Patients with coeliac disease are at increased risk of cancer, including a twofold to fourfold increased risk of non-Hodgkin’s lymphoma and a more than 30-fold increased risk of small intestinal adenocarcinoma, and they have a 1.4-fold increased risk of death.
- ^ a b Lundin KE, Wijmenga C (September 2015). "Coeliac disease and autoimmune disease-genetic overlap and screening". Nature Reviews. Gastroenterology & Hepatology (Review). 12 (9): 507–15. doi:10.1038/nrgastro.2015.136. PMID 26303674.
The abnormal immunological response elicited by gluten-derived proteins can lead to the production of several different autoantibodies, which affect different systems.
- ^ a b "Celiac disease". World Gastroenterology Organisation Global Guidelines. July 2016. Diarsipkan dari versi asli tanggal 17 March 2017. Diakses tanggal 23 April 2017.
- ^ Lionetti E, Francavilla R, Pavone P, Pavone L, Francavilla T, Pulvirenti A, Giugno R, Ruggieri M (August 2010). "The neurology of coeliac disease in childhood: what is the evidence? A systematic review and meta-analysis". Developmental Medicine and Child Neurology. 52 (8): 700–7. doi:10.1111/j.1469-8749.2010.03647.x. PMID 20345955.

- ^ a b c d Husby S, Koletzko S, Korponay-Szabó IR, Mearin ML, Phillips A, Shamir R, Troncone R, Giersiepen K, Branski D, Catassi C, Lelgeman M, Mäki M, Ribes-Koninckx C, Ventura A, Zimmer KP, ESPGHAN Working Group on Coeliac Disease Diagnosis; ESPGHAN Gastroenterology Committee; European Society for Pediatric Gastroenterology, Hepatology, and Nutrition (Jan 2012). "European Society for Pediatric Gastroenterology, Hepatology, and Nutrition guidelines for the diagnosis of coeliac disease" (PDF). J Pediatr Gastroenterol Nutr (Practice Guideline). 54 (1): 136–60. doi:10.1097/MPG.0b013e31821a23d0. PMID 22197856. Diarsipkan (PDF) dari versi asli tanggal 3 April 2016.
Since 1990, the understanding of the pathological processes of CD has increased enormously, leading to a change in the clinical paradigm of CD from a chronic, gluten-dependent enteropathy of childhood to a systemic disease with chronic immune features affecting different organ systems. (...) atypical symptoms may be considerably more common than classic symptoms
- ^ a b c Ciccocioppo R, Kruzliak P, Cangemi GC, Pohanka M, Betti E, Lauret E, Rodrigo L (Oct 22, 2015). "The Spectrum of Differences between Childhood and Adulthood Celiac Disease". Nutrients (Review). 7 (10): 8733–51. doi:10.3390/nu7105426. PMC 4632446
 . PMID 26506381.
. PMID 26506381. Several additional studies in extensive series of coeliac patients have clearly shown that TG2A sensitivity varies depending on the severity of duodenal damage, and reaches almost 100% in the presence of complete villous atrophy (more common in children under three years), 70% for subtotal atrophy, and up to 30% when only an increase in IELs is present. (IELs: intraepithelial lymphocytes)
- ^ a b c d e f g h "Celiac Disease". NIDDKD. June 2015. Diarsipkan dari versi asli tanggal 13 March 2016. Diakses tanggal 17 March 2016.
- ^ a b Vivas S, Vaquero L, Rodríguez-Martín L, Caminero A (November 2015). "Age-related differences in celiac disease: Specific characteristics of adult presentation". World Journal of Gastrointestinal Pharmacology and Therapeutics (Review). 6 (4): 207–12. doi:10.4292/wjgpt.v6.i4.207. PMC 4635160
 . PMID 26558154.
. PMID 26558154. In addition, the presence of intraepithelial lymphocytosis and/or villous atrophy and crypt hyperplasia of small-bowel mucosa, and clinical remission after withdrawal of gluten from the diet, are also used for diagnosis antitransglutaminase antibody (tTGA) titers and the degree of histological lesions inversely correlate with age. Thus, as the age of diagnosis increases antibody titers decrease and histological damage is less marked. It is common to find adults without villous atrophy showing only an inflammatory pattern in duodenal mucosa biopsies: Lymphocytic enteritis (Marsh I) or added crypt hyperplasia (Marsh II)
- ^ Ferri, Fred F. (2010). Ferri's differential diagnosis : a practical guide to the differential diagnosis of symptoms, signs, and clinical disorders (edisi ke-2nd). Philadelphia, PA: Elsevier/Mosby. hlm. Chapter C. ISBN 0323076998.
- ^ a b See JA, Kaukinen K, Makharia GK, Gibson PR, Murray JA (October 2015). "Practical insights into gluten-free diets". Nature Reviews. Gastroenterology & Hepatology (Review). 12 (10): 580–91. doi:10.1038/nrgastro.2015.156. PMID 26392070.
A lack of symptoms and/or negative serological markers are not reliable indicators of mucosal response to the diet. Furthermore, up to 30% of patients continue to have gastrointestinal symptoms despite a strict GFD.122,124 If adherence is questioned, a structured interview by a qualified dietitian can help to identify both intentional and inadvertent sources of gluten.
- ^ a b Fasano A, Catassi C (December 2012). "Clinical practice. Celiac disease". The New England Journal of Medicine (Review). 367 (25): 2419–26. doi:10.1056/NEJMcp1113994. PMID 23252527.
- ^ Newnham, Evan D (2017). "Coeliac disease in the 21st century: Paradigm shifts in the modern age". Journal of Gastroenterology and Hepatology. 32: 82–85. doi:10.1111/jgh.13704. PMID 28244672.
Presentation of CD with malabsorptive symptoms or malnutrition is now the exception rather than the rule.

- ^ a b Rostami Nejad M, Hogg-Kollars S, Ishaq S, Rostami K (2011). "Subclinical celiac disease and gluten sensitivity". Gastroenterol Hepatol Bed Bench (Review). 4 (3): 102–8. PMC 4017418
 . PMID 24834166.
. PMID 24834166.
- ^ Tonutti E, Bizzaro N (2014). "Diagnosis and classification of celiac disease and gluten sensitivity". Autoimmun Rev (Review). 13 (4–5): 472–6. doi:10.1016/j.autrev.2014.01.043. PMID 24440147.
- ^ a b c Penagini F, Dilillo D, Meneghin F, Mameli C, Fabiano V, Zuccotti GV (November 2013). "Gluten-free diet in children: an approach to a nutritionally adequate and balanced diet". Nutrients (Review). 5 (11): 4553–65. doi:10.3390/nu5114553. PMC 3847748
 . PMID 24253052.
. PMID 24253052.
- ^ a b Di Sabatino A, Corazza GR (April 2009). "Coeliac disease". Lancet. 373 (9673): 1480–93. doi:10.1016/S0140-6736(09)60254-3. PMID 19394538.
- ^ a b Pinto-Sánchez MI, Causada-Calo N, Bercik P, Ford AC, Murray JA, Armstrong D, Semrad C, Kupfer SS, Alaedini A, Moayyedi P, Leffler DA, Verdú EF, Green P (August 2017). "Safety of Adding Oats to a Gluten-Free Diet for Patients With Celiac Disease: Systematic Review and Meta-analysis of Clinical and Observational Studies". Gastroenterology. 153 (2): 395–409.e3. doi:10.1053/j.gastro.2017.04.009. PMID 28431885.
- ^ National Institute for Health and Clinical Excellence. Clinical guideline 86: Recognition and assessment of coeliac disease. London, 2015.
- ^ Matthias T, Pfeiffer S, Selmi C, Eric Gershwin M (Apr 2010). "Diagnostic challenges in celiac disease and the role of the tissue transglutaminase-neo-epitope". Clin Rev Allergy Immunol (Review). 38 (2–3): 298–301. doi:10.1007/s12016-009-8160-z. PMID 19629760.
- ^ Lewis NR, Scott BB (July 2006). "Systematic review: the use of serology to exclude or diagnose coeliac disease (a comparison of the endomysial and tissue transglutaminase antibody tests)". Alimentary Pharmacology & Therapeutics. 24 (1): 47–54. doi:10.1111/j.1365-2036.2006.02967.x. PMID 16803602.
- ^ Rostom A, Murray JA, Kagnoff MF (Dec 2006). "American Gastroenterological Association (AGA) Institute technical review on the diagnosis and management of celiac disease". Gastroenterology (Review). 131 (6): 1981–2002. doi:10.1053/j.gastro.2006.10.004. PMID 17087937.
- ^ Molina-Infante J, Santolaria S, Sanders DS, Fernández-Bañares F (May 2015). "Systematic review: noncoeliac gluten sensitivity". Alimentary Pharmacology & Therapeutics (Review). 41 (9): 807–20. doi:10.1111/apt.13155. PMID 25753138.
Furthermore, seronegativity is more common in coeliac disease patients without villous atrophy (Marsh 1-2 lesions), but these ‘minor’ forms of coeliac disease may have similar clinical manifestations to those with villous atrophy and may show similar clinical–histological remission with reversal of haematological or biochemical disturbances on a gluten-free diet (GFD).
- ^ Ludvigsson JF, Card T, Ciclitira PJ, Swift GL, Nasr I, Sanders DS, Ciacci C (April 2015). "Support for patients with celiac disease: A literature review". United European Gastroenterology Journal (Review). 3 (2): 146–59. doi:10.1177/2050640614562599. PMC 4406900
 . PMID 25922674.
. PMID 25922674.
- ^ van Heel DA, West J (July 2006). "Recent advances in coeliac disease". Gut (Review). 55 (7): 1037–46. doi:10.1136/gut.2005.075119. PMC 1856316
 . PMID 16766754.
. PMID 16766754.
- ^ Bibbins-Domingo K, Grossman DC, Curry SJ, Barry MJ, Davidson KW, Doubeni CA, Ebell M, Epling JW, Herzstein J, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Phipps MG, Silverstein M, Simon MA, Tseng CW (March 2017). "Screening for Celiac Disease: US Preventive Services Task Force Recommendation Statement". JAMA. 317 (12): 1252–1257. doi:10.1001/jama.2017.1462. PMID 28350936.
- ^ Lionetti E, Gatti S, Pulvirenti A, Catassi C (June 2015). "Celiac disease from a global perspective". Best Practice & Research. Clinical Gastroenterology (Review). 29 (3): 365–79. doi:10.1016/j.bpg.2015.05.004. PMID 26060103.
- ^ Hischenhuber C, Crevel R, Jarry B, Mäki M, Moneret-Vautrin DA, Romano A, Troncone R, Ward R (March 2006). "Review article: safe amounts of gluten for patients with wheat allergy or coeliac disease". Alimentary Pharmacology & Therapeutics. 23 (5): 559–75. doi:10.1111/j.1365-2036.2006.02768.x. PMID 16480395.
- ^ Adams F, translator (1856). "On The Cœliac Affection". The extant works of Aretaeus, The Cappadocian. London: Sydenham Society. hlm. 350–1. Diakses tanggal 12 December 2009.
- ^ Losowsky MS (2008). "A history of coeliac disease". Digestive Diseases. 26 (2): 112–20. doi:10.1159/000116768. PMID 18431060.
- ^ Schuppan D, Zimmer KP (December 2013). "The diagnosis and treatment of celiac disease". Deutsches Arzteblatt International. 110 (49): 835–46. doi:10.3238/arztebl.2013.0835. PMC 3884535
 . PMID 24355936.
. PMID 24355936.
- ^ a b c name=Lancet2009
- ^ name=VriezingaSchweizer2015>Vriezinga SL, Schweizer JJ, Koning F, Mearin ML (September 2015). "Coeliac disease and gluten-related disorders in childhood". Nature Reviews. Gastroenterology & Hepatology (Review). 12 (9): 527–36. doi:10.1038/nrgastro.2015.98. PMID 26100369.
- ^ name=VanHeelWest
- ^ name=WGO2016
- ^ name=LudvigssonCard2015
- ^ name=LionettiGatti2015
- ^ name=KupferJabri2012>Kupfer SS, Jabri B (2012). "Pathophysiology of celiac disease". Gastrointest Endosc Clin N Am (Review). 22 (4): 639–60. doi:10.1016/j.giec.2012.07.003. PMC 3872820
 . PMID 23083984.
. PMID 23083984. Gluten comprises two different protein types, gliadins and glutenins, capable of triggering disease.
- ^ name=Biesiekierski2017>Biesiekierski, Jessica R (2017). "What is gluten?". Journal of Gastroenterology and Hepatology. 32: 78–81. doi:10.1111/jgh.13703. PMID 28244676.
Similar proteins to the gliadin found in wheat exist as secalin in rye, hordein in barley, and avenins in oats and are collectively referred to as “gluten.” Derivatives of these grains such as triticale and malt and other ancient wheat varieties such as spelt and kamut also contain gluten. The gluten found in all of these grains has been identified as the component capable of triggering the immune-mediated disorder, coeliac disease.

- ^ name=Biesiekierski2017
- ^ name=Kupper>Kupper C (2005). "Dietary guidelines and implementation for celiac disease". Gastroenterology. 128 (4 Suppl 1): S121–7. doi:10.1053/j.gastro.2005.02.024. PMID 15825119.
- ^ a b c name=CominoMoreno2015
- ^ name=PenaginiDilillo>Penagini F, Dilillo D, Meneghin F, Mameli C, Fabiano V, Zuccotti GV (Nov 18, 2013). "Gluten-free diet in children: an approach to a nutritionally adequate and balanced diet". Nutrients. 5 (11): 4553–65. doi:10.3390/nu5114553. PMC 3847748
 . PMID 24253052.
. PMID 24253052.
- ^ name=PenaginiDilillo
- ^ name=DeSouzaDeschenes2016>de Souza MC, Deschênes ME, Laurencelle S, Godet P, Roy CC, Djilali-Saiah I (2016). "Pure Oats as Part of the Canadian Gluten-Free Diet in Celiac Disease: The Need to Revisit the Issue". Can J Gastroenterol Hepatol (Review). 2016: 1576360. doi:10.1155/2016/1576360. PMC 4904650
 . PMID 27446824.
. PMID 27446824.
- ^ name=HaboubiTaylor2006>Haboubi NY, Taylor S, Jones S (Oct 2006). "Coeliac disease and oats: a systematic review". Postgrad Med J (Review). 82 (972): 672–8. doi:10.1136/pgmj.2006.045443. PMC 2653911
 . PMID 17068278.
. PMID 17068278.
- ^ name=DeSouzaDeschenes2016
- ^ name=HaboubiTaylor2006
- ^ name=MatthiasPfeiffer2010>Matthias T, Pfeiffer S, Selmi C, Eric Gershwin M (Apr 2010). "Diagnostic challenges in celiac disease and the role of the tissue transglutaminase-neo-epitope". Clin Rev Allergy Immunol (Review). 38 (2–3): 298–301. doi:10.1007/s12016-009-8160-z. PMID 19629760.
- ^ name="NICEcoeliac"
