Pirazina
| |||
| |||
| Nama | |||
|---|---|---|---|
| Nama IUPAC
Pyrazine
| |||
| Nama lain
1,4-Diazabenzene, p-Diazine, 1,4-Diazine, Paradiazine, Piazine, UN 1325
| |||
| Penanda | |||
Model 3D (JSmol)
|
|||
| 3DMet | {{{3DMet}}} | ||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| Nomor EC | |||
PubChem CID
|
|||
| Nomor RTECS | {{{value}}} | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sifat | |||
| C4H4N2 | |||
| Massa molar | 80.09 g/mol | ||
| Penampilan | White crystals | ||
| Densitas | 1.031 g/cm3 | ||
| Titik lebur | 52 °C (126 °F; 325 K) | ||
| Titik didih | 115 °C (239 °F; 388 K) | ||
| Soluble | |||
| Keasaman (pKa) | 0.37[1] (protonated pyrazine) | ||
| Bahaya | |||
| Frasa-R | R11, R36/37/38 | ||
| Frasa-S | S16, S26, S36 | ||
| Titik nyala | 55 °C (131 °F; 328 K) | ||
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |||
| Referensi | |||
Pirazina (Inggris: Pyrazine) adalah senyawa organik aromatik heterosiklik dengan formula kimia C4H4N2.
Pirazina adalah molekul simetri dengan point group D2h. Derivatif seperti phenazina terkenal karena aktivitas antitumor, antibiotika dan diuretik. Pirazina bersifat kurang basa dibandingkan dengan piridina, piridazina dan pirimidina. Tetramethylpyrazine (juga dikenal sebagai "ligustrazine") dilaporkan dapat melakukan memburu anion superoksida dan menurunkan produksi nitrogen monoksida pada leukosit polimorfonuklear manusia,[2] dan merupakan sebuah komponen sejumlah ramuan obat tradisional Tiongkok.[3]
Sintesis[sunting | sunting sumber]
Ada banyak metode sintesis organik pirazina dan derivatifnya. Beberapa di antaranya merupakan reaksi sintesis tertua yang masih dipakai.
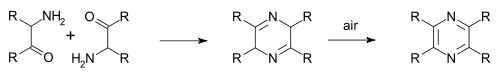
Dalam Staedel–Rugheimer pyrazine synthesis (1876) 2-chloroacetophenone direaksikan dengan amonia menjadi amino keton, kemudian dikondensasi dan dioksidasi menjadi suatu pirazina.[4] Variasi lain adalah Sintesis pirazina Gutknecht (1879) juga berdasarkan kondensasi sendiri, tetapi berbeda dalam cara sintesis alfa-ketoamina[5][6]
Sintesis Gastaldi (1921) merupakan variasi lain:[7][8]
Lihat pula[sunting | sunting sumber]
- Pirimidina, analog dengan atom nitrogen kedua pada posisi 3
- Piridazina, analog dengan atom nitrogen kedua pada posisi 2
- Piridina, analog hanya dengan satu atom nitrogen
- Benzena, analog tanpa atom nitrogen
- Cincin aromatik sederhana
- Metokspirazina
- Alkilpirazina
Pranala luar[sunting | sunting sumber]
- Safety MSDS data Diarsipkan 2007-10-11 di Wayback Machine.
- Safety evaluation of food additives – pyrazine derivatives
Referensi[sunting | sunting sumber]
- ^ Brown, H.C., et al., in Baude, E.A. and Nachod, F.C., Determination of Organic Structures by Physical Methods, Academic Press, New York, 1955.
- ^ Zhang, Zhaohui (2003). "Tetramethylpyrazine scavenges superoxide anion and decreases nitric oxide production in human polymorphonuclear leukocytes". Life Sciences. 72 (22): 2465–2472. doi:10.1016/S0024-3205(03)00139-5.
- ^ http://www.itmonline.org/arts/ligustrazine.htm
- ^ Ueber die Einwirkung von Ammoniak auf Chloracetylbenzol (pp. 563–564) W. Staedel, L. Rügheimer doi:10.1002/cber.187600901174 Berichte der deutschen chemischen Gesellschaft Volume 9, Issue 1, pp. 563–564, 1876
- ^ Mittheilungen Ueber Nitrosoäthylmethylketon H. Gutknecht Berichte der deutschen chemischen Gesellschaft Volume 12, Issue 2 , pp. 2290–2292, 1879 doi:10.1002/cber.187901202284
- ^ Heterocyclic chemistry T.L. Gilchrist ISBN 0-582-01421-2
- ^ G. Gastaldi, Gazz. Chim. Ital. 51, (1921) 233
- ^ Amines: Synthesis, Properties and Applications Stephen A. Lawrence 2004 Cambridge University Press ISBN 0-521-78284-8