Bismut pentafluorida

| |

| |
| Nama | |
|---|---|
| Nama lain
bismut(V) fluorida
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| BiF5 | |
| Massa molar | 303.97 g mol−1 |
| Penampilan | jarum putih panjang,[1] padat kristalin tidak berwarna[2] |
| Densitas | 5.40 g cm−3[1] |
| Titik lebur | 1.514 °C (2.757 °F; 1.787 K) ,[2] 154.4 °C[1] |
| Titik didih | 230 °C (446 °F; 503 K)[1][2] |
| Struktur | |
| oktahedral Bi | |
| Bahaya | |
| Senyawa terkait | |
Anion lain
|
bismut triklorida, bismut tribromida, bismut triiodida, pentametilbismut |
Kation lainnya
|
fosfor pentafluorida, arsen pentafluorida, antimon pentafluorida |
Senyawa terkait
|
bismut trifluorida |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Bismut pentafluorida adalah senyawa anorganik dengan rumus BiF5. Senyawa ini merupakan senyawa padat berwarna putih yang sangat reaktif.
Struktur[sunting | sunting sumber]
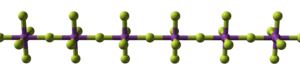  |
  |
| Gugusan |
Pembuatan[sunting | sunting sumber]
BiF5 dapat dibuat dari reaksi BiF3 dengan F2 pada suhu 500 °C.[2]
- BiF3 + F2 → BiF5
Cara lain adalah dengan menggunakan ClF3 sebagai agen fluorinasi pada suhu 350 °C.[3]
- BiF3 + ClF3 → BiF5 + ClF
Referensi[sunting | sunting sumber]
- ^ a b c d Greenwood, Norman N.; Earnshaw, A. (1997), Chemistry of the Elements (edisi ke-2), Oxford: Butterworth-Heinemann, hlm. 561–563, ISBN 0-7506-3365-4
- ^ a b c d Holleman, A. F.; Wiberg, E. (2001), Inorganic Chemistry, San Diego: Academic Press, hlm. 769–770, ISBN 0-12-352651-5
- ^ A. I. Popov; A. V. Scharabarin; V. F. Sukhoverkhov; N. A. Tchumaevsky (1989). "Synthesis and properties of pentavalent antimony and bismuth fluorides". Z. anorg. allg. Chem. 576 (1): 242–254. doi:10.1002/zaac.19895760128.
