Kanker paru-paru
Artikel ini memberikan informasi dasar tentang topik kesehatan. |
| Kanker Paru-paru | |
|---|---|
 | |
| Sebuah Radiograf dada menunjukkan tumor di paru-paru (ditandai dengan panah) | |
| Informasi umum | |
| Nama lain | Karsinoma Paru-paru |
| Spesialisasi | Onkologi, Pulmonologi |
| Tipe | Karsinoma sel kecil (SCLC), Kanker paru-paru bukan sel kecil (NSCLC) |
| Faktor risiko |
|
| Aspek klinis | |
| Gejala dan tanda | Batuk (termasuk Batuk darah), Dispnea, Nyeri dada |
| Awal muncul | Setelah usia 40;[1] Rata-rata 70 Tahun[2] |
| Diagnosis | Pencitraan medis, Biopsi |
| Tata laksana | |
| Pencegahan | Hindari merokok dan mutagen lingkungan lainnya |
| Perawatan | Operasi, Kemoterapi, Radioterapi, Terapi molekuler, Imunoterapi kanker |
| Prognosis | Kelangsungan hidup lima tahun: 10 to 20% (sebagian besar negara)[3] |
| Distribusi dan frekuensi | |
| Prevalensi | 2.2 juta (2020)[3] |
| Kematian | 1.8 juta (2020)[3] |
Kanker paru-paru merupakan penyakit dengan ciri khas adanya pertumbuhan sel yang tidak terkontrol pada jaringan paru-paru. Bila tidak dirawat, pertumbuhan sel ini dapat menyebar ke luar dari paru-paru melalui suatu proses yang disebut metastasis ke jaringan yang terdekat atau bagian tubuh yang lainnya. Sebagian besar kanker yang mulai di paru-paru, yang dikenal sebagai kanker paru primer, adalah karsinoma yang berasal dari sel epitelium. Jenis kanker paru yang utama adalah SCLC (kanker paru sel kecil), atau disebut juga kanker sel gandum, dan NSCLC (kanker paru non-sel-kecil). Gejala paling umum adalah batuk (termasuk batuk darah), berat badan turun dan sesak napas.[4]
Penyebab paling umum kanker paru adalah paparan dalam jangka waktu yang lama terhadap asap tembakau,[5] yang menyebabkan 80–90% kanker paru.[4] Bukan perokok mencapai angka 10–15% dari kasus kanker paru,[6] dan kasus ini biasanya disebabkan oleh kombinasi antara faktor genetik,[7] gas radon,[7] asbestos,[8] dan polusi udara[7] termasuk asap rokok pasif.[9][10] Kanker paru dapat dilihat melalui foto rontgen dada dan tomografi komputer (CT scan). diagnosis dapat dipastikan dengan biopsi[11] yang biasanya dilakukan melalui prosedur bronkoskopi atau dipandu dengan CT. Perawatan dan hasil dalam jangka panjang tergantung pada tipe kanker, stadium (tingkat penyebaran), dan keadaan kesehatan pasien secara keseluruhan, diukur berdasarkan kondisi umum.
Perawatan biasanya meliputi pembedahan, kemoterapi, dan radioterapi. NSCLC biasanya ditangani melalui pembedahan, sedangkan SCLC umumnya memberikan respons yang lebih baik terhadap kemoterapi dan radioterapi.[12] Secara keseluruhan, 15% dari penduduk di Amerika Serikat terdiagnosis kanker paru mencapai harapan hidup lima tahun setelah diagnosis.[13] Secara global, kanker paru merupakan penyebab utama kematian karena kanker pada laki-laki dan perempuan, dan bertanggung jawab untuk 1,38 juta kematian setiap tahunnya, hingga tahun 2008.[14]
Tanda-tanda dan gejala[sunting | sunting sumber]
Tanda-tanda dan gejala yang menunjukkan adanya kanker paru adalah:[4]
- gejala pada saluran napas: batuk, batuk darah, mengi atau napas pendek
- gejala sistemik: berat badan turun, demam, gada pada kuku jari, atau kelelahan
- gejala karena tekanan di daerah lokal: nyeri dada, nyeri tulang, obstruksi vena cava superior, kesulitan menelan
Bila kanker tumbuh di sekitar saluran napas, keadaan ini dapat menghambat aliran udara, menyebabkan sesak napas. Hambatan ini dapat menyebabkan adanya akumulasi sekret di belakang sumbatan, dan menyebabkan terjadinya pneumonia.[4]
Bergantung pada jenis tumornya, fenomena paraneoplastik mungkin adalah yang pertama kali menarik perhatian mengenai adanya penyakit ini.[15] Pada kanker paru, fenomena ini dapat meliputi Sindrom Lambert–Eaton myastenik (lemah otot yang disebabkan oleh autoantibodi), hiperkalsemia, atau sindrom dari ketidakstabilan hormon antidiuretik (SIADH). Tumor pada bagian pucuk paru, dikenal sebagai Tumor Pancoast, dapat menginvasi bagian lokal dari sistem saraf simpatik, sehingga menyebabkan Sindrom Horner (jatuhnya kelopak mata dan pupil kecil pada sisi tersebut), dan juga menyebabkan kerusakan pada pleksus brakhialis.[4]
Kebanyakan gejala kanker paru (hilang nafsu makan, berat badan turun, demam, kelelahan) tidak spesifik.[11] Pada kebanyakan orang, kanker telah menyebar dari lokasi awalnya saat timbul gejala dan datang ke dokter. Lokasi umum penyebarannya termasuk otak, tulang, kelenjar adrenal, paru sebelahnya, hati, perikardium, dan ginjal.[16] Sekitar 10% dari penderita kanker paru tidak mengalami gejala saat diagnosis; kanker ini ditemukan secara tidak sengaja pada pemeriksaan foto rontgen dada.[13]
Penyebab[sunting | sunting sumber]
Kanker berkembang mengikuti kerusakan genetik pada DNA. Kerusakan genetik ini mempengaruhi fungsi normal sel, termasuk proliferasi sel, pemrograman kematian sel (apoptosis), dan perbaikan DNA. Ketika lebih banyak kerusakan terakumulasi, risiko terhadap kanker makin bertambah.[17]
Merokok[sunting | sunting sumber]

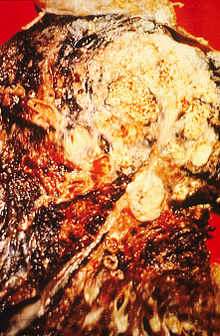
Merokok, khususnya sigaret, secara umum merupakan penyumbang utama kanker paru.[18] Rokok sigaret mengandung lebih dari 60 jenis karsinogen,[19] termasuk di antaranya radioisotop dari peluruhan sekuens radon, nitrosamin, dan benzopiren. Selain itu, nikotin menekan respons imun terhadap pertumbuhan kanker pada jaringan yang terpapar.[20] Di seluruh negara maju, 90% dari kematian karena kanker paru pada laki-laki selama tahun 2000 disebabkan oleh merokok (70% untuk perempuan).[21] Merokok bertanggung jawab terhadap 80–90% kasus kanker paru.[4]
Merokok pasif—proses inhalasi asap dari perokok lain—merupakan penyebab kanker paru pada bukan perokok. Perokok pasif dapat digolongkan sebagai seseorang yang hidup atau bekerja bersama perokok. Penelitian dari AS,[22][23] Eropa,[24] Inggris,[25] dan Australia[26] telah secara konsisten menunjukkan adanya peningkatan risiko yang signifikan di antara mereka yang terpapar asap rokok pasif.[27] Mereka yang hidup dengan perokok memiliki risiko yang lebih tinggi sebesar 20–30% sedangkan mereka yang bekerja pada lingkungan perokok mempunyai risiko 16–19% lebih tinggi.[28] Penelitian asap aliran sisi menunjukkan bahwa hal ini lebih berbahaya dari merokok langsung.[29] Merokok pasif menyebabkan 3, 400 kematian karena kanker paru setiap tahun di AS.[23]
Gas radon[sunting | sunting sumber]
Radon adalah gas yang tidak berwarna dan tidak berbau dihasilkan dari penguraian radioaktif radium, yang merupakan produk dari peluruhan uranium, yang ditemukan di lapisan kerak bumi. Produk peluruhan radiasi meng ion kan materi genetika, sehingga menyebabkan mutasi yang kadang menjadi bersifat kanker. Radon merupakan penyebab kanker paru paling banyak kedua di AS, setelah rokok.[23] Risikonya meningkat hinggga 8–16% untuk setiap peningkatan konsentrasi radon sebesar 100 Bq/m³.[30] Tingkat gas radon bervariasi tergantung pada lokasi dan komposisi tanah dan batuan di bawahnya. Sebagai contoh, di wilayah seperti Cornwall di Inggris (yang mengandung granit sebagai substrata), gas radon merupakan masalah utama, dan bangunan harus memiliki ventilasi aktif dengan kipas untuk menurunkan konsentrasi gas radon. United States Environmental Protection Agency (EPA) memperkirakan satu dari 15 rumah di AS memiliki tingkat radon lebih tinggi dari tingkat rekomendasi 4 picocurie per liter (pCi/l) (148 Bq/m³).[31]
Asbestos[sunting | sunting sumber]
Asbestos dapat menyebabkan berbagai penyakit paru-paru, termasuk kanker paru. Merokok tembakau dan asbestos memberikan efek sinergis dalam pembentukan kanker paru.[8] Asbestos juga dapat menyebabkan kanker pada pleura, yang disebut mesotelioma (yang berbeda dari kanker paru).[32]
Polusi udara[sunting | sunting sumber]
Polusi udara di luar rumah hanya memberikan efek yang kecil dalam meningkatkan risiko kanker paru.[7] Bahan partikulat atmosfer (PM2.5) halus dan aerosol sulfat, yang berasal dari pelepasan asap kendaraan bermotor di jalanan, dihubungkan sedikit meningkatkan risiko.[7][33] Untuk nitrogen dioksida, kenaikan bertahan hingga 10 bagian per miliar meningkatkan risiko kanker paru hingga 14%.[34] Polusi udara luar diperkirakan bertanggung jawab terhadap 1–2% kejadian kanker paru.[7]
Bukti tentatif mendukung adanya kenaikan risiko kanker paru dari polusi dalam ruang yang berhubungan dengan pembakaran kayu, batubara, residu bahan bakar kotoran dan sisa sampah yang dipakai untuk memasak dan pemanas ruang.[35] Wanita yang terpapar asap pembakaran batubara memiliki risiko dua kali lebih tinggi dan sejumlah produk sampingan dari pembakaran tanaman organik diketahui atau dicurigai bersifat karsinogen.[36] Risiko ini memengaruhi kurang lebih 2.4 miliar orang di seluruh dunia,[35] dan dipercaya menyebabkan 1.5% kematian karena kanker paru.[36]
Genetik[sunting | sunting sumber]
Diperkirakan bahwa 8 hingga 14% dari kanker paru disebabkan oleh faktor diturunkan.[37] Pada orang dengan saudara yang terkena kanker paru, risiko meningkat hingga 2.4 kali. Hal ini disebabkan oleh adanya kombinasi gen.[38]
Penyebab lain[sunting | sunting sumber]
Sejumlah zat, pekerjaan, dan paparan lingkungan lain juga dihubungkan dengan kanker paru. Badan Penelitian Kanker Internasional (IARC) menyatakan ada "bukti yang cukup" untuk menunjukkan bahwa sejumlah hal berikut karsinogenik untuk paru-paru:[39]
- Sejumlah jenis logam (produk aluminium, kadmium dan senyawa kadmium, senyawa kromium(VI), berilium dan senyawa berilium, peleburan besi dan baja, senyawa nikel, arsenik dan senyawa arsenik inorganik, tambang hematit bawah tanah)
- Sejumlah produk pembakaran (pembakaran tidak sempurna), arang batu (emisi dalam ruangan dari pembakaran arang batu rumah tangga), gasifikasi batu bara, aspal, produk kokas, jelaga, gas buang mesin disel)
- Radiasi ionisasi (radiasi sinar-X, radon-222 dan produk peluruhannya, radiasi gamma, plutonium)
- Sejumlah gas beracun (metil eter (kadar teknis), Bis-(klorometil) eter, sulfur mustard, MOPP (campuran vinkristina-prednison-nitrogen mustard-procarbazin), uap pengecatan)
- Produk karet dan kristalin debu silika
Patogenesis[sunting | sunting sumber]
Seperti jenis kanker lainnya, kanker paru diinisiasi oleh aktivasi onkogen atau inaktivasi gen supresor tumor.[40] Onkogen diyakini menjadikan orang lebih rentan terhadap kanker. Proto-onkogen diyakini berubah menjadi onkogen ketika terpapar karsinogen tertentu.[41] Mutasi pada proto-onkogen K-ras bertanggung jawab atas 10–30% adenokarsinoma paru.[42][43] Reseptor faktor pertumbuhan epidermal (EGFR) mengatur proliferasi sel, apoptosis, angiogenesis, dan invasi tumor.[42] Mutasi dan amplifikasi EGFR biasa ditemukan pada kanker paru bukan-sel-kecil dan memberikan dasar pengobatan menggunakan inhibitor-EGFR. Her2/neu lebih jarang terpengaruh.[42] Kerusakan kromosomal bisa menyebabkan hilangnya heterozigositas. Hal ini bisa menyebabkan inaktivasi gen supresor tumor. Kerusakan pada kromosom 3p, 5q, 13q, dan 17p secara spesifik ditemukan pada kanker bukan-sel-kecil. Gen supresor tumor p53, yang terdapat di kromosom 17p, terpengaruh pada 60-75% kasus. Gen-gen lain yang sering dimutasi atau dikuatkan adalah c-MET, NKX2-1, LKB1, PIK3CA, dan BRAF.[42]
Diagnosis[sunting | sunting sumber]

Melakukan foto rontgen dada adalah salah satu langkah pemeriksaan awal jika seseorang melaporkan gejala-gejala yang mengarah pada kanker paru. Upaya ini bisa menunjukkan adanya massa yang jelas, pelebaran mediastinum (yang menunjukkan penyebaran ke nodus limfatik), atelektasis (kolaps), konsolidasi (pneumonia), atau efusi pleura.[5] Pencitraan CT umumnya digunakan untuk memberi informasi tambahan tentang jenis dan perluasan penyakit. Bronkoskopi atau biopsi dipandu-CT kerap dipakai dalam pengambilan sampel tumor untuk pemeriksaan histopatologi.[13]
Kanker paru sering tampak sebagai nodul paru soliter dalam foto rontgen dada. Tetapi, diagnosis diferensialnya luas. Banyak penyakit lain yang menunjukkan tampilan seperti itu, termasuk tuberkulosis, infeksi jamur, kanker metastatik, atau pneumonia terkelompok. Penyebab nodul paru soliter yang lebih jarang ditemukan termasuk hamartoma, kista bronkogenik, adenoma, malformasi arteriovena, sekuestrasi paru, nodul reumatoid, granulomatosis Wegener, atau limfoma.[44] Kanker paru juga bisa berupa temuan insidental, sebagai nodul paru soliter dalam sebuah foto rontgen dada atau CT scan yang dilakukan untuk tujuan yang tidak berkaitan.[45] Diagnosis definitif kanker paru didasarkan pada pemeriksaan histologi jaringan yang meragukan dalam konteks ciri klinis dan radiologi.[4]
Klasifikasi[sunting | sunting sumber]
| Tipe histologi | Kejadian per 100, 000 per tahun |
|---|---|
| Semua jenis | 66.9 |
| Adenokarsinoma | 22.1 |
| Karsinoma skuamosa | 14.4 |
| Karsinoma sel kecil | 9.8 |
Kanker paru diklasifikasikan berdasarkan tipe histologi.[11] Klasifikasi ini penting untuk menentukan manajemen dan memprediksi keluaran penyakit. Mayoritas besar kanker paru adalah karsinoma—keganasan yang timbul dari sel epitelial. Kanker paru dikategorikan menurut ukuran dan tampakan sel-sel ganas yang dilihat oleh ahli histopatologi melalui mikroskop. Dua kelas besarnya adalah kanker paru bukan-sel-kecil dan sel kecil.[46]
Kanker paru bukan-sel-kecil[sunting | sunting sumber]

Tiga subtipe utama NSCLC adalah adenokarsinoma, karsinoma paru sel skuamosa, dan karsinoma paru sel besar.[4]
Hampir 40% kanker paru adalah adenokarsinoma, yang biasanya bermula di jaringan paru perifer.[11] Kebanyakan kasus adenokarsinoma dihubungkan dengan kebiasaan merokok; namun, di antara orang-orang yang merokok kurang dari 100 rokok sepanjang hidup mereka ("tidak pernah merokok"),[4] adenokarsinoma merupakan jenis kanker paru yang paling umum.[47] Satu subtipe adenokarsinoma, karsinoma bronkioloalveolar, lebih umum ditemukan pada wanita yang tidak pernah merokok, dan penderitanya dapat memiliki daya tahan hidup yang lebih baik.
Karsinoma sel skuamosa menjadi penyebab sekitar 30% kanker paru. Jenis ini khususnya timbul di saluran napas besar. Rongga berlubang dan kematian sel yang berkaitan umumnya ditemukan di pusat tumor. Sekitar 9% kanker paru adalah karsinoma sel besar. Disebut demikian karena sel-sel kanker tersebut besar, memiliki sitoplasma berlebihan, nuklei besar dan nukleoli kelihatan jelas.
Kanker paru sel kecil[sunting | sunting sumber]

Pada karsinoma paru sel kecil (SCLC), sel kanker mengandung granul neurosekretori padat (vesikel yang mengandung hormon neuroendokrin), yang memberi tumor ini suatu asosiasi endokrin/sindrom paraneoplastik.[48] Sebagian besar kasus muncul di saluran napas besar (bronki primer dan sekunder).[13] Kanker ini berkembang cepat dan menyebar di tahap awal perkembangan penyakit. Enam puluh sampai tujuh puluh persen memiliki penyakit metastatik pada saat penyakit mulai memberikan gejala. Kanker paru jenis ini sangat berkaitan dengan kebiasaan merokok.[4]
Lain-lain[sunting | sunting sumber]
Empat subtipe histologi utama telah diketahui, meskipun sejumlah kanker mungkin mengandung kombinasi beberapa subtipe yang berbeda.[46] Subtipe yang jarang termasuk tumor kelenjar, tumor karsinoid, dan karsinoma tak terdiferensiasi.[4]
Metastasis[sunting | sunting sumber]
| Tipe histologi | Immunostain (pewarnaan imunologi) |
|---|---|
| Karsinoma sel skuamosa | CK5/6 positif CK7 negatif |
| Adenokarsinoma | CK7 positif TTF-1 positif |
| Karsinoma sel besar | TTF-1 negatif |
| Kanker sel kecil | TTF-1 positif CD56 positif Kromogranin positif Sinaptofisin positif |
Paru-paru merupakan tempat yang umum untuk persebaran tumor dari bagian tubuh yang lain. Kanker sekunder diklasifikasikan menurut tempat asalnya, misalnya kanker payudara yang telah menyebar ke paru-paru disebut kanker payudara metastatik. Metastasis kerapkali mempunyai tampilan bulat yang khas dalam foto rontgen dada.[49]
Kanker paru primer sendiri kerapkali bermetastasis ke otak, tulang, hati dan kelenjar adrenal.[11] Metode biopsi immunostain (pewarnaan imunologi) sering kali bermanfaat untuk menentukan sumber kanker.[50]
Stadium[sunting | sunting sumber]
Stadium kanker paru adalah pengkajian tingkat penyebaran kanker dari sumber asalnya. Langkah ini merupakan salah satu faktor yang mempengaruhi prognosis dan penanganan potensial kanker paru.[4]
Evaluasi awal dari pentahapan kanker paru bukan-sel-kecil (NSCLC) menggunakan klasifikasi TNM. Cara ini didasarkan pada ukuran tumor primer, keterlibatan nodus limfatik, dan metastasis jauh. Setelah ini, dengan menggunakan deskriptor TNM, ditentukan satu grup, berkisar mulai dari kanker yang tersembunyi, sampai stadium 0, IA (satu-A), IB, IIA, IIB, IIIA, IIIB dan IV (empat). Kelompok stadium ini membantu pemilihan metode penangangan dan estimasi prognosis.[51] Kanker paru sel kecil (SCLC) umumnya diklasifikasikan sebagai 'stadium terbatas' (terbatas pada separuh dada dan dalam cakupan satu bidang radioterapi yang dapat ditoleransi) atau 'stadium ekstensif' (penyakit lebih meluas).[4] Namun, klasifikasi TNM dan pengelompokan bermanfaat untuk estimasi prognosis.[51]
Baik untuk NSCLC maupun SCLC, dua jenis evaluasi penentuan stadium adalah stadium klinis dan stadium bedah. Stadium klinis dilakukan sebelum pembedahan definitif. Tindakan ini didasarkan pada hasil kajian pencitraan (seperti CT scan dan PET scan) dan hasil biopsi. Stadium bedah dievaluasi baik selama maupun setelah operasi, dan didasarkan atas gabungan hasil-hasil temuan dalam pembedahan dan klinis, termasuk contoh sampel nodus limfatik dada yang diambil dalam pembedahan.[11]
Pencegahan[sunting | sunting sumber]
Pencegahan adalah cara paling murah untuk mengurangi perkembangan kanker paru. Meskipun di berbagai negara, karsinogen industri dan rumah tangga telah diidentifikasi dan dilarang, kebiasaan merokok masih dilakukan secara luas. Menghilangkan kebiasaan merokok adalah tujuan utama langkah pencegahan kanker paru, dan berhenti merokok merupakan salah satu pencegahan yang penting dalam proses ini.[52]
Intervensi kebijakan pengurangan dampak merokok pasif di ruang publik seperti restoran dan tempat kerja semakin banyak dilakukan di sejumlah negara barat.[53] Bhutan telah menerapkan larangan merokok sejak 2005[54] dan India mengeluarkan larangan merokok di area publik pada Oktober 2008.[55] Organisasi Kesehatan Dunia (WHO) telah menyerukan kepada pemerintah untuk menerapkan larangan penuh pada iklan rokok dalam upaya mencegah kaum muda mencoba merokok. Mereka menilai bahwa larangan tersebut mampu mengurangi konsumsi tembakau sampai sekitar 16% jika larangan tersebut diberlakukan.[56]
Penggunaan jangka panjang suplemen vitamin A,[57][58] vitamin C,[57] vitamin D,[59] atau vitamin E[57] tidak mengurangi risiko kanker paru. Beberapa penelitian mengindikasikan bahwa orang yang mengonsumsi makanan dengan proporsi sayur dan buah lebih tinggi cenderung memiliki risiko yang lebih rendah,[23][60] namun hal ini kemungkinan karena adanya kerancuan. Penelitian yang lebih cermat belum menunjukkan hubungan yang jelas.[60]
Selain itu, penggunaan produk tembakau alternatif sebagai upaya untuk mengurangi risiko kesehatan akibat rokok telah lama menjadi pembahasan. Penelitian dari Public Health England (PHE) mengungkapkan bahwa produk tembakau alternatif seperti produk tembakau yang dipanaskan bukan dibakar dan rokok elektrik memiliki potensi risiko kesehatan 95 persen lebih rendah dibandingkan rokok. Sudah ada beberapa penelitian, salah satunya yakni dari American Cancer Society yang mengatakan bahwa perokok yang mengalami kesulitan atau tidak mau berhenti harus didorong untuk beralih ke produk tembakau alternatif dengan potensi risiko kesehatan yang lebih rendah. Namun, tentu masih diperlukan penelitian yang lebih dalam dan komprehensif untuk meyakinkan dampak produk ini dalam jangka panjang.[61]
Penapisan[sunting | sunting sumber]
Penapisan merujuk pada penggunaan tes kesehatan untuk mendeteksi penyakit pada orang tanpa gejala. Tes penapisan yang mungkin untuk kanker paru meliputi sitologi dahak, foto rontgen dada (CXR), dan tomografi komputer (CT). Program penapisan yang menggunakan CXR atau sitologi belum menunjukkan adanya manfaat.[62] Melakukan penapisan pada orang-orang dengan risiko tinggi (misal, orang berusia 55-79 tahun yang sudah merokok lebih dari 30 pak tiap tahun atau mereka yang sebelumnya memiliki kanker paru) setiap tahun dengan pindai tomografi komputer (CT) dosis rendah dapat mengurangi peluang kematian akibat kanker paru dengan nilai mutlak sebesar 0, 3% (nilai relatif sebesar 20%).[63][64] Akan tetapi, ada sejumlah besar pindai positif palsu yang dapat menyebabkan prosedur invasif yang tidak diperlukan maupun biaya yang cukup besar.[65] Untuk setiap pindai positif yang sejati, ada lebih dari 19 positif palsu.[66] Pajanan radiasi merupakan potensi bahaya lain dari penapisan menggunakan X-Ray dan CT-Scan.[67]
Foto rontgen terkadang tidak mendapatkan hasil sama sekali, karena untuk jenis kanker sel kecil (small cells) yang masih sedikit dan tersebar, maka foto rontgen tidak akan menampakkannya. Menggunakan CT Scan biayanya mahal, dan radiatif. Penapis tumor untuk kanker paru-paru yang biasanya digunakan adalah NSE, SCC dan Cyfra 21.1; biasanya dilakukan sekaligus, karena hampir semua penapis tumor tidak memiliki spesifitas dan sensitivitas yang tinggi, oleh karenanya dengan melakukan beberapa penapis tumor sekaligus akan didapat perpotongan (intersection) yang meyakinkan dugaan adanya tumor tertentu pada area tertentu (bukan diagnosis, diagnosis hanya dengan biopsi). Yang terakhir masuk ke Indonesia adalah penapis tumor M2-PK, di mana sebenarnya penapis tumor ini tadinya diperuntukkan untuk menapis kanker usus besar, dapat mendeteksi polip yang belum menjadi tumor atau kanker dengan tingkat spesifisitas di atas 90 persen dan tingkat sensitivitas yang tinggi juga. Tidak memiliki negatip palsu dan berarti, jika negatip pasti negatip. Pada penelitian lebih lanjut, ternyata penapis tumor M2-PK juga dapat digunakan untuk menapis kanker paru-paru, bahkan lebih baik daripada NSE dan SCC, yang berarti lebih murah untuk digunakan.
Penanganan[sunting | sunting sumber]
Pengobatan untuk kanker paru tergantung pada jenis sel khusus kanker tersebut, seberapa jauh sel tersebut menyebar, dan kondisi umum orang tersebut. Pengobatan umum meliputi perawatan paliatif,[68] pembedahan, kemoterapi, dan terapi radiasi.[4]
Pembedahan[sunting | sunting sumber]

Jika pemeriksaan mengonfirmasi adanya kanker paru bukan-sel-kecil (NSCLC), penilaian stadium dilakukan untuk menentukan apakah penyakit tersebut termasuk lokal dan dapat dilakukan pembedahan atau jika sel tersebut telah menyebar ke titik di mana tidak dapat ditangani dengan jalan pembedahan. Pindai tomografi komputer (CT scan) dan tomografi emisi positron digunakan untuk penentuan ini.[4] Jika dicurigai adanya keterlibatan kelenjar limfa mediastinum, mediastinoskopi dapat digunakan untuk mengambil sampel nodus dan membantu penentuan stadium.[69] Tes darah dan uji fungsi paru digunakan untuk menilai apakah seseorang cukup sehat untuk melakukan pembedahan.[13] Jika uji fungsi paru menunjukkan cadangan pernapasan yang rendah, pembedahan tidak mungkin dilakukan.[4]
Pada sebagian besar kasus kanker paru bukan-sel-kecil (NSCLC) stadium awal, pembuangan lobus paru (lobektomi) merupakan penanganan bedah pilihan. Pada orang-orang yang tidak siap untuk lobektomi total, eksisi sublobar yang lebih kecil (eksisi baji) dapat dilakukan. Akan tetapi, eksisi baji memiliki risiko kambuh yang lebih besar daripada lobektomi.[70] Brakiterapi iodin radioaktif di bagian tepi eksisi baji dapat mengurangi risiko kambuh.[71] Jarang sekali dilakukan pembuangan semua paru-paru (pneumonektomi).[70] Pembedahan torakoskopi berbantu video (VATS) dan lobektomi VATS menggunakan pendekatan invasif yang minimal pada pembedahan kanker paru.[72] Lobektomi VATS sama efektifnya jika dibandingkan dengan lobektomi terbuka konvensional, dengan rasa sakit pascabedah yang lebih ringan.[73]
Penanganan kanker paru sel kecil (SCLC), biasanya menggunakan kemoterapi dan/atau radioterapi.[74] Akan tetapi, peran pembedahan dalam kanker paru sel kecil (SCLC) perlu dipertimbangkan kembali. Pembedahan mungkin meningkatkan keberhasilan jika ditambahkan pada kemoterapi dan radiasi dalam kanker paru sel kecil (SCLC) tahap awal.[75]
Radioterapi[sunting | sunting sumber]
Radioterapi sering diberikan bersama dengan kemoterapi, dan dapat digunakan dengan maksud pengobatan pada orang dengan kanker paru bukan-sel-kecil (NSCLC) yang tidak memenuhi syarat untuk pembedahan. Bentuk radioterapi berintensitas tinggi ini disebut radioterapi radikal.[76] Penyempurnaan teknik ini berupa radioterapi yang dipercepat dan dengan hiperfraksinasi berkelanjutan (continuous hyperfractionated accelerated radiotherapy/CHART), yaitu saat dosis tinggi radioterapi diberikan dalam jangka waktu pendek.[77] Biasanya radioterapi dada pascabedah tidak digunakan setelah pembedahan yang bertujuan pengobatan untuk NSCLC.[78] Beberapa orang dengan keterlibatan kelenjar limfa mediastinum N2 mendapatkan manfaat setelah radioterapi pascabedah.[79]
Untuk kasus SCLC yang berpotensi dapat disembuhkan, radioterapi dada sering disarankan selain kemoterapi.[11]
Jika pertumbuhan kanker menyumbat bagian pendek bronkus, brakiterapi (radioterapi lokal) dapat diberikan langsung di dalam saluran napas untuk membuka saluran tersebut.[80] Dibandingkan dengan radioterapi pancaran eksternal, brakiterapi memungkinkan pengurangan waktu pengobatan dan mengurangi pajanan radiasi pada staf kesehatan.[81]
Iradiasi kranial profilaktik (Prophylactic cranial irradiation/PCI) adalah jenis radioterapi untuk otak, yang digunakan untuk mengurangi risiko metastasis. PCI sangat berguna dalam SCLC. Pada penyakit stadium-terbatas, PCI meningkatkan tiga tahun masa kelangsungan hidup mulai dari 15% hingga 20%; pada penyakit ekstensif, satu tahun masa kelangsungan hidup meningkat mulai dari 13% hingga 27%.[82]
Kemajuan terbaru dalam menjangkau sasaran dan membuat pencitraan telah mengarah pada pengembangan radiasi stereotaktik dalam pengobatan kanker paru stadium awal. Pada radioterapi dalam bentuk ini, dosis tinggi diberikan dalam sejumlah kecil sesi menggunakan teknik penargetan stereotaktik. Penggunaan teknik ini terutama diberikan pada pasien yang bukan calon pasien bedah karena komorbiditas medis.[83]
Untuk kedua jenis pasien NSCLC dan SCLC, dosis radiasi yang lebih kecil pada dada dapat digunakan untuk kontrol gejala (radioterapi paliatif).[84]
Kemoterapi[sunting | sunting sumber]
Panduan kemoterapi tergantung pada jenis tumor.[11] Kanker paru sel kecil (SCLC), meski penyakit relatif pada stadium awal, penting ditangani dengan kemoterapi dan radiasi.[85] Pada SCLC, kemoterapi yang paling sering digunakan yaitu sisplatin dan etoposid.[86] Kombinasi antara karboplatin, gemsitabin, paklitaksel, vinorelbin, topotekan, dan irinotecan juga digunakan.[87][88]
Pada kanker paru bukan-sel-kecil (NSCLC) tahap lanjut, kemoterapi meningkatkan masa hidup dan digunakan sebagai pengobatan urutan pertama, yang diberikan jika seseorang cukup kuat untuk pengobatan tersebut.[89] Biasanya, pengobatan ini menggunakan dua obat, yang salah satunya sering berupa obat berbasis platina (baik cisplatin atau karboplatin). Obat lain yang biasa digunakan adalah gemsitabin, paklitaksel, doksetaksel,[90][91] pemetreksed,[92] etoposid, atau vinorelbin.[91]
Kemoterapi adjuvan merujuk pada penggunaan kemoterapi setelah melakukan pembedahan kuratif untuk menyempurnakan hasilnya. Dalam NSCLC, sampel diambil di dekat nodus limfatik selama pembedahan untuk membantu penentuan stadium. Jika terkonfirmasi penyakit stadium II atau III, kemoterapi adjuvan meningkatkan tingkat kelangsungan hidup sebesar 5% pada lima tahun.[93][94] Kombinasi vinorelbin dan cisplatin lebih efektif daripada pengobatan lama.[94] Kemoterapi adjuvan untuk penderita kanker stadium IB mengundang kontroversi, karena uji coba klinis belum menunjukkan manfaat yang jelas terhadap kelangsungan hidup.[95][96] Uji coba pra-operasi kemoterapi (kemoterapi neo-adjuvan) dalam NSCLC yang dapat diangkat belum mencapai suatu kesimpulan.[97]
Perawatan paliatif[sunting | sunting sumber]
Pada penderita dengan penyakit terminal, perawatan paliatif atau pengelolaan rawat akhir mungkin lebih tepat.[13] Pendekatan ini memungkinkan diskusi tambahan tentang pilihan perawatan dan membuka kesempatan didapatkannya keputusan dari pertimbangan yang matang [98][99] dan dapat menghindarkan perawatan yang tidak menolong tetapi mahal di akhir kehidupan.[99]
Kemoterapi dapat digabungkan dengan perawatan paliatif dalam merawat NSCLC. Dalam kasus lanjut, kemoterapi yang tepat meningkatkan rerata kelangsungan hidup melampaui perawatan dukungan saja, serta meningkatkan kualitas hidup.[100] Dengan kebugaran fisik yang cukup, mempertahankan kemoterapi dalam meringankan kanker paru memberikan perpanjangan hidup 1,5 hingga 3 bulan, mengurangi gejala, dan peningkatan kualitas hidup, dengan hasil yang lebih baik tampak pada obat-obatan yang lebih baru.[101][102] NSCLC Meta-Analyses Collaborative Group menyarankan jika penderita menginginkan dan dapat menerima perawatan ini, maka kemoterapi harus dipertimbangkan pada kasus NSCLC lanjut.[89][103]
Prognosis[sunting | sunting sumber]
| Stadium klinis | Kelangsungan hidup lima tahun (%) | |
|---|---|---|
| Kanker paru bukan-sel-kecil | Kanker paru sel kecil | |
| IA | 50 | 38 |
| IB | 47 | 21 |
| IIA | 36 | 38 |
| IIB | 26 | 18 |
| IIIA | 19 | 13 |
| IIIB | 7 | 9 |
| IV | 2 | 1 |
Prognosis umumnya buruk. Dari semua penderita kanker paru, 15% bertahan selama 5 tahun setelah prognosis.[5] Sering terjadi stadium sudah lanjut pada saat diagnosis. Pada presentasi, 30–40% kasus NSCLC ada pada stadium IV, dan 60% SCLC ditemukan pada stadium IV.[11]
Faktor prognostik dalam NSCLC termasuk ada atau tidak adanya gejala paru, ukuran tumor, (histologi) jenis sel, derajat penyebaran (stadium), dan metastasis ke beberapa nodus limfatik, serta invasi pembuluh darah. Untuk penderita dengan penyakit yang tidak dapat dioperasi, hasilnya lebih buruk bagi yang memiliki kondisi umum buruk dan kehilangan berat badan lebih dari 10%.[104] Faktor prognostik dalam kanker paru sel kecil termasuk kondisi umum, jenis kelamin, stadium penyakit, dan keterlibatan sistem saraf pusat atau organ hati pada saat diagnosis.[105]
Untuk NSCLC, prognosis terbaik didapatkan dengan reseksi bedah lengkap penyakit stadium IA, dengan tingkat kelangsungan hidup lima tahun sebesar 70%.[106] Untuk SCLC, keseluruhan tingkat kelangsungan hidup lima tahunnya sekitar 5%.[4] Penderita SCLC tingkat ekstensif mempunyai rerata tingkat kelangsungan hidup lima tahun kurang dari 1%. Rerata waktu kelangsungan hidup untuk penyakit stadium terbatas adalah 20 tahun, dengan tingkat kelangsungan hidup lima tahun sebesar 20%.[5]
Menurut data yang disediakan oleh National Cancer Institute, usia median pada diagnosis kanker paru di Amerika Serikat adalah 70 tahun,[107] dan usia median saat kematian adalah 72 tahun.[108] Di AS, orang yang memiliki asuransi kesehatan cenderung mempunyai hasil yang lebih baik.[109]
Epidemiologi[sunting | sunting sumber]

no data ≤ 5 5-10 10-15 15-20 20-25 25-30 | 30-35 35-40 40-45 45-50 50-55 ≥ 55 |

Di seluruh dunia, kanker paru merupakan kanker paling umum dari segi insiden dan mortalitas. Pada 2008, terdapat 1,61 juta kasus baru, dan 1,38 juta kematian akibat kanker paru. Tingkat tertinggi ada di Eropa dan Amerika Utara.[14] Segmen populasi yang paling mungkin menderita kanker paru adalah orang berusia di atas 50 tahun yang mempunyai riwayat merokok. Berlawanan dengan tingkat mortalitas pria, yang mulai menurun lebih dari 20 tahun yang lalu, tingkat mortalitas kanker paru wanita telah meningkat dalam dekade terakhir, dan baru saja mulai stabil.[111] Di AS, risiko seumur hidup untuk terkena kanker paru adalah 8% pada pria dan 6% pada wanita.[4]
Untuk setiap 3–4 juta rokok yang diisap, akan terjadi satu kematian karena kanker paru.[4][112] Pengaruh dari "Big Tobacco" memainkan peranan penting dalam budaya merokok.[113] Orang muda bukan perokok yang melihat iklan tembakau punya kecenderungan untuk mulai merokok.[114] Peran dari merokok pasif makin diakui sebagai faktor risiko kanker paru,[27] yang memunculkan intervensi kebijakan untuk menurunkan paparan yang tidak dikehendaki para non-perokok terhadap asap tembakau orang lain.[115] Buangan dari mobil, pabrik, dan instalasi pembangkit listrik juga punya risiko potensial.[7]
Eropa Timur mempunyai angka mortalitas tertinggi di kalangan pria, sedangkan Eropa utara dan AS mempunyai angka mortalitas tertinggi di kalangan wanita. Di Amerika Serikat, pria dan wanita kulit hitam mempunyai insiden lebih tinggi.[116] Tingkat kanker paru saat ini lebih rendah pada negara berkembang.[117] Dengan meningkatnya kebiasaan merokok di negara berkembang, diduga tingkat kanker ini akan naik dalam beberapa tahun ke depan, khususnya di negara Cina[118] dan India.[119]
Sejak 1960-an, tingkat adenokarsinoma paru mulai meningkat relatif terhadap jenis kanker paru yang lain. Hal ini sebagian disebabkan karena munculnya sigaret filter. Penggunaan filter menghilangkan partikel-partikel besar dari asap tembakau, sehingga mengurangi deposisi pada saluran pernapasan besar. Namun, perokok harus menghisap lebih dalam untuk mendapatkan nikotin dalam jumlah yang sama, meningkatkan deposisi partikel dalam saluran pernapasan kecil tempat adenokarsinoma cenderung muncul.[120] Insiden adenokarsinoma paru terus meningkat.[121]
Sejarah[sunting | sunting sumber]
Kanker paru jarang dijumpai sebelum ditemukannya kebiasaan merokok; bahkan belum dikenali sebagai suatu penyakit khusus hingga tahun 1761.[122] Berbagai aspek berbeda dari kanker paru dijelaskan lebih jauh pada tahun 1810.[123] Jumlah kanker paru ganas hanya sebanyak 1% dari semua kanker yang ditemukan pada autopsi pada tahun 1878, tetapi telah meningkat 10–15% di awal 1900-an.[124] Laporan kasus dalam literatur kedokteran hanya sebanyak 374 di seluruh dunia pada tahun 1912,[125] tetapi kajian pada hasil autopsi menunjukkan bahwa insiden kanker paru telah meningkat dari 0, 3% pada 1852 menjadi 5, 66% pada 1952.[126] Di Jerman pada 1929, dokter Fritz Lickint menemukan hubungan antara kebiasaan merokok dengan kanker paru,[124] yang menjadi penyebab munculnya kampanye antirokok yang agresif.[127] British Doctors Study, yang dipublikasikan pada 1950-an, merupakan bukti kuat epidemiologis hubungan antara kanker paru dengan kebiasaan merokok.[128] Akibatnya, pada 1964 Surgeon General Amerika Serikat menyarankan para perokok untuk berhenti merokok.[129]
Hubungan dengan gas radon pertama kali dijumpai di kalangan penambang di Pegunungan Ore di dekat Schneeberg, Saxony. Perak telah ditambang di sana sejak 1470, dan tambang ini kaya dengan uranium, yang disertai radium, dan gas radon.[130] Para penambang menderita jumlah penyakit paru-paru yang tak sebanding, yang kemudian dikenali sebagai kanker paru pada 1870-an.[131] Walaupun ada penemuan ini, penambangan tetap berlanjut hingga 1950-an, karena adanya permintaan uranium dari Uni Republik Sosialis Soviet.[130] Radon dikonfirmasi sebagai penyebab kanker paru pada tahun 1960-an.[132]
Pneumonektomi pertama yang sukses untuk kanker paru dilakukan pada 1933.[133] Radioterapi paliatif telah digunakan sejak 1940-an.[134] Radioterapi radikal, yang mulai digunakan pada 1950-an, merupakan usaha untuk menggunakan dosis radiasi yang lebih besar pada pasien kanker paru dengan stadium yang relatif awal, tetapi yang tidak cocok untuk pembedahan.[135] Pada 1997, radioterapi dipercepat dengan hiperfraksionisasi dipandang sebagai perbaikan terhadap radioterapi radikal konvensional.[136] Untuk kanker paru sel kecil, upaya awal dilakukan pada 1960-an saat pembedahan[137] dan radioterapi radikal[138] tidak berhasil. Pada tahun 1970-an, dikembangkan perawatan kemoterapi yang sukses.[139]
Referensi[sunting | sunting sumber]
- ^ Horn & Iams 2022, "Epidemiology".
- ^ Bade & Dela Cruz 2020, "Age".
- ^ a b c Sung et al. 2021, "Lung cancer".
- ^ a b c d e f g h i j k l m n o p q r s t Horn, L (2012). "Chapter 89". Dalam Longo, DL; Kasper, DL; Jameson, JL; Fauci, AS; Hauser, SL; Loscalzo, J. Harrison's Principles of Internal Medicine (edisi ke-18th). McGraw-Hill. ISBN 0-07-174889-X.
- ^ a b c d "Lung Carcinoma: Tumors of the Lungs". Merck Manual Professional Edition, Online edition. Diakses tanggal 2007-08-15.
- ^ Thun, MJ (September 2008). "Lung cancer occurrence in never-smokers: an analysis of 13 cohorts and 22 cancer registry studies". PLoS Medicine. 5 (9): e185. doi:10.1371/journal.pmed.0050185. PMC 2531137
 . PMID 18788891.
. PMID 18788891.
- ^ a b c d e f g h Alberg AJ, Samet JM (2010). "Chapter 46". Murray & Nadel's Textbook of Respiratory Medicine (edisi ke-5th). Saunders Elsevier. ISBN 978-1-4160-4710-0.
- ^ a b O'Reilly, KM (March 2007). "Asbestos-related lung disease". American Family Physician. 75 (5): 683–688. PMID 17375514. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2014-01-30.
- ^ Carmona, RH (2006-06-27). "The Health Consequences of Involuntary Exposure to Tobacco Smoke: A Report of the Surgeon General". U.S. Department of Health and Human Services.
Secondhand smoke exposure causes disease and premature death in children and adults who do not smoke.
- ^ "Tobacco Smoke and Involuntary Smoking" (PDF). IARC Monographs on the Evaluation of Carcinogenic Risks to Humans. WHO International Agency for Research on Cancer. 83. 2002.
There is sufficient evidence that involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) causes lung cancer in humans. ... Involuntary smoking (exposure to secondhand or 'environmental' tobacco smoke) is carcinogenic to humans (Group 1).
- ^ a b c d e f g h i Lu, C (2010). "78: Cancer of the Lung". Holland-Frei Cancer Medicine (edisi ke-8th). People's Medical Publishing House. ISBN 9781607950141.
- ^ Chapman, S (2009). "Chapter 31". Oxford Handbook of Respiratory Medicine (edisi ke-2nd). Oxford University Press. ISBN 9-780199-545162.
- ^ a b c d e f Collins, LG (January 2007). "Lung cancer: diagnosis and management". American Family Physician. American Academy of Family Physicians. 75 (1): 56–63. PMID 17225705. Diarsipkan dari versi asli tanggal 2007-09-29. Diakses tanggal 2014-01-30.
- ^ a b Ferlay, J (December 2010). "Estimates of worldwide burden of cancer in 2008: GLOBOCAN 2008". International Journal of Cancer. 127 (12): 2893–2917. doi:10.1002/ijc.25516. PMID 21351269.
- ^ Honnorat, J (May 2007). "Paraneoplastic neurological syndromes". Orphanet Journal of Rare Diseases. BioMed Central. 2 (1): 22. doi:10.1186/1750-1172-2-22. PMC 1868710
 . PMID 17480225.
. PMID 17480225.
- ^ Greene, Frederick L. (2002). AJCC cancer staging manual. Berlin: Springer-Verlag. ISBN 0-387-95271-3.
- ^ Brown, KM (2010). "8". Holland-Frei Cancer Medicine (edisi ke-8th). People's Medical Publishing House USA. ISBN 978-1607950141.
- ^ Biesalski, HK (1998). "European Consensus Statement on Lung Cancer: risk factors and prevention. Lung Cancer Panel". CA Cancer J Clin. Smoking is the major risk factor, accounting for about 90% of lung cancer incidence. 48 (3): 167–176; discussion 164–166. doi:10.3322/canjclin.48.3.167. PMID 9594919.
- ^ Hecht, S (October 2003). "Tobacco carcinogens, their biomarkers and tobacco-induced cancer". Nature Reviews Cancer. Nature Publishing Group. 3 (10): 733–744. doi:10.1038/nrc1190. PMID 14570033.
- ^ Sopori, M (May 2002). "Effects of cigarette smoke on the immune system". Nature Reviews Immunology. 2 (5): 372–7. doi:10.1038/nri803. PMID 12033743.
- ^ Peto, R (2006). Mortality from smoking in developed countries 1950–2000: Indirect estimates from National Vital Statistics. Oxford University Press. ISBN 0-19-262535-7.
- ^ California Environmental Protection Agency (1997). "Health effects of exposure to environmental tobacco smoke. California Environmental Protection Agency". Tobacco Control. 6 (4): 346–353. doi:10.1136/tc.6.4.346. PMC 1759599
 . PMID 9583639.
. PMID 9583639.
* CDC (2001). "State-specific prevalence of current cigarette smoking among adults, and policies and attitudes about secondhand smoke—United States, 2000". Morbidity and Mortality Weekly Report. Atlanta, Georgia: CDC. 50 (49): 1101–1106. PMID 11794619. - ^ a b c d Alberg, AJ (2007). "Epidemiology of lung cancer". Chest. American College of Chest Physicians. 132 (S3): 29S–55S. doi:10.1378/chest.07-1347. PMID 17873159. Diarsipkan dari versi asli tanggal 2020-03-29. Diakses tanggal 2014-01-30.
- ^ Jaakkola, MS (2006). "Impact of smoke-free workplace legislation on exposures and health: possibilities for prevention". European Respiratory Journal. 28 (2): 397–408. doi:10.1183/09031936.06.00001306. PMID 16880370.
- ^ Parkin, DM (2011). "Tobacco—attributable cancer burden in the UK in 2010". British Journal of Cancer. 105 (Suppl. 2): S6–S13. doi:10.1038/bjc.2011.475. PMC 3252064
 . PMID 22158323.
. PMID 22158323.
- ^ National Health and Medical Research Council (April 1994). "The health effects and regulation of passive smoking". Australian Government Publishing Service. Diarsipkan dari versi asli tanggal September 29, 2007. Diakses tanggal 2007-08-10.
- ^ a b Taylor, R (2007). "Meta-analysis of studies of passive smoking and lung cancer: effects of study type and continent". International Journal of Epidemiology. 36 (5): 1048–1059. doi:10.1093/ije/dym158. PMID 17690135.
- ^ "Frequently asked questions about second hand smoke". World Health Organization. Diakses tanggal 25 July 2012.
- ^ Schick, S (December 2005). "Philip Morris toxicological experiments with fresh sidestream smoke: more toxic than mainstream smoke". Tobacco Control. 14 (6): 396–404. doi:10.1136/tc.2005.011288. PMC 1748121
 . PMID 16319363.
. PMID 16319363.
- ^ Schmid K, Kuwert T, Drexler H (2010). "Radon in Indoor Spaces: An Underestimated Risk Factor for Lung Cancer in Environmental Medicine". Dtsch Arztebl Int. 107 (11): 181–6. doi:10.3238/arztebl.2010.0181. PMC 2853156
 . PMID 20386676.
. PMID 20386676.
- ^ EPA (October 2006). "Radiation information: radon". EPA. Diakses tanggal 2007-08-11.
- ^ Davies, RJO (2010). "18.19.3". Oxford Textbook Medicine (edisi ke-5th). OUP Oxford. ISBN 978-0199204854.
- ^ Chen, H (2008). "A systematic review of the relation between long-term exposure to ambient air pollution and chronic diseases". Reviews on Environmental Health. 23 (4): 243–297. PMID 19235364.
- ^ Clapp, RW (2008). "Environmental and Occupational Causes of Cancer New Evidence, 2005–2007". Reviews on Environmental Health. 23 (1): 1–37. PMC 2791455
 . PMID 18557596.
. PMID 18557596.
- ^ a b Lim, WY (2012 Jan). "Biomass fuels and lung cancer". Respirology (Carlton, Vic.). 17 (1): 20–31. PMID 22008241.
- ^ a b Sood, A (2012 Dec). "Indoor fuel exposure and the lung in both developing and developed countries: an update". Clinics in chest medicine. 33 (4): 649–65. PMID 23153607.
- ^ Dudley, Joel (2013). Exploring Personal Genomics. Oxford University Press. hlm. 25. ISBN 9780199644483.
- ^ Kern JA, McLennan G (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 1802. ISBN 0-07-145739-9.
- ^ Cogliano, VJ (2011 Dec 21). "Preventable exposures associated with human cancers" (PDF). Journal of the National Cancer Institute. 103 (24): 1827–39. PMID 22158127. Diarsipkan dari versi asli (PDF) tanggal 2012-09-20. Diakses tanggal 2014-01-30.
- ^ Fong, KM (October 2003). "Lung cancer • 9: Molecular biology of lung cancer: clinical implications". Thorax. BMJ Publishing Group Ltd. 58 (10): 892–900. doi:10.1136/thorax.58.10.892. PMC 1746489
 . PMID 14514947.
. PMID 14514947.
- ^ Salgia, R (March 1998). "Molecular abnormalities in lung cancer". Journal of Clinical Oncology. 16 (3): 1207–1217. PMID 9508209.
- ^ a b c d Herbst, RS (September 2008). "Lung cancer". New England Journal of Medicine. 359 (13): 1367–1380. doi:10.1056/NEJMra0802714. PMID 18815398.
- ^ Aviel-Ronen, S (July 2006). "K-ras mutations in non-small-cell lung carcinoma: a review". Clinical Lung Cancer. Cancer Information Group. 8 (1): 30–38. doi:10.3816/CLC.2006.n.030. PMID 16870043.
- ^ Miller, WT (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 486. ISBN 0-07-145739-9.
- ^ Kaiser, LR (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 1815–1816. ISBN 0-07-145739-9.
- ^ a b Maitra, A (2007). Robbins Basic Pathology (edisi ke-8th). Saunders Elsevier. hlm. 528–529. ISBN 978-1-4160-2973-1.
- ^ Subramanian, J (2007). "Lung cancer in never smokers: a review". Journal of Clinical Oncology. American Society of Clinical Oncology. 25 (5): 561–570. doi:10.1200/JCO.2006.06.8015. PMID 17290066.
- ^ Rosti, G (March 2006). "Small cell lung cancer". Annals of Oncology. 17 (Suppl. 2): 5–10. doi:10.1093/annonc/mdj910. PMID 16608983.
- ^ Seo, JB (1 March 2001). "Atypical pulmonary metastases: spectrum of radiologic findings". Radiographics. 21 (2): 403–417. PMID 11259704.
- ^ Tan D, Zander DS (2008). "Immunohistochemistry for Assessment of Pulmonary and Pleural Neoplasms: A Review and Update". Int J Clin Exp Pathol. 1 (1): 19–31. PMC 2480532
 . PMID 18784820.
. PMID 18784820.
- ^ a b c Rami-Porta, R (2009). "The revised TNM staging system for lung cancer" (PDF). Annals of Thoracic and Cardiovascular Surgery. 15 (1): 4–9. PMID 19262443.
- ^ Goodman, GE (2002). "Lung cancer. 1: prevention of lung cancer" (PDF). Thorax. 57 (11): 994–999. PMC 1746232
 . PMID 12403886.
. PMID 12403886.
- ^ McNabola, A (2009). "The control of environmental tobacco smoke: a policy review". International Journal of Environmental Research and Public Health. 6 (2): 741–758. doi:10.3390/ijerph6020741. PMC 2672352
 . PMID 19440413.
. PMID 19440413.
- ^ Pandey, G (February 2005). "Bhutan's smokers face public ban". BBC. Diakses tanggal 2007-09-07.
- ^ Pandey, G (2 October 2008). "Indian ban on smoking in public". BBC. Diakses tanggal 2012-04-25.
- ^ "UN health agency calls for total ban on tobacco advertising to protect young" (Siaran pers). United Nations News service. 30 May 2008.
- ^ a b c Fabricius, P (2003). "Diet and lung cancer". Monaldi Archives for Chest Disease. 59 (3): 207–211. PMID 15065316.
- ^ Fritz, H (2011). "Vitamin A and Retinoid Derivatives for Lung Cancer: A Systematic Review and Meta Analysis". PLoS ONE. 6 (6): e21107. doi:10.1371/journal.pone.0021107. PMC 3124481
 . PMID 21738614.
. PMID 21738614.
- ^ Herr, C (2011). "The role of vitamin D in pulmonary disease: COPD, asthma, infection, and cancer". Respiratory Research. 12 (1): 31. doi:10.1186/1465-9921-12-31. PMC 3071319
 . PMID 21418564.
. PMID 21418564.
- ^ a b Key, TJ (2011). "Fruit and vegetables and cancer risk". British Journal of Cancer. 104 (1): 6–11. doi:10.1038/sj.bjc.6606032. PMC 3039795
 . PMID 21119663.
. PMID 21119663.
- ^ "Salinan arsip". Diarsipkan dari versi asli tanggal 2020-08-05. Diakses tanggal 2019-03-14.
- ^ Manser, RL (2004). "Screening for lung cancer". Cochrane Database of Systematic Reviews (1): CD001991. doi:10.1002/14651858.CD001991.pub2. PMID 14973979.
- ^ Jaklitsch, MT (2012). "The American Association for Thoracic Surgery guidelines for lung cancer screening using low-dose computed tomography scans for lung cancer survivors and other high-risk groups". Journal of Thoracic and Cardiovascular Surgery. 144 (1): 33–38. doi:10.1016/j.jtcvs.2012.05.060. PMID 22710039.
- ^ Bach, PB (2012). "Benefits and harms of CT screening for lung cancer: a systematic review". JAMA: the Journal of the American Medical Association. 307 (22): 2418–2429. doi:10.1001/jama.2012.5521. PMID 22610500.
- ^ Boiselle, PM (2013 Mar 20). "Computed tomography screening for lung cancer". JAMA : the journal of the American Medical Association. 309 (11): 1163–70. PMID 23512063.
- ^ Bach PB, Mirkin JN, Oliver TK; et al. (2012). "Benefits and harms of CT screening for lung cancer: a systematic review". JAMA. 307 (22): 2418–29. doi:10.1001/jama.2012.5521. PMID 22610500.
- ^ Aberle, DR (2013 Mar 10). "Computed tomography screening for lung cancer: has it finally arrived? Implications of the national lung screening trial". Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 31 (8): 1002–8. PMID 23401434.
- ^ Ferrell, B (2011). "Palliative care in lung cancer". Surgical Clinics of North America. 91 (2): 403–417. doi:10.1016/j.suc.2010.12.003. PMID 21419260.
- ^ Kaiser LR (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 1853–1854. ISBN 0-07-145739-9.
- ^ a b Kaiser LR (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 1855–1856. ISBN 0-07-145739-9.
- ^ Odell, DD (2010). "Sublobar resection with brachytherapy mesh for stage I non-small cell lung cancer". Seminars in Thoracic and Cardiovascular Surgery. 22 (1): 32–37. doi:10.1053/j.semtcvs.2010.04.003. PMID 20813314.
- ^ Alam, N (2007). "Video-assisted thoracic surgery (VATS) lobectomy: the evidence base". Journal of the Society of Laparoendoscopic Surgeons. 11 (3): 368–374. PMC 3015831
 . PMID 17931521.
. PMID 17931521.
- ^ Rueth, NM (2010). "Is VATS lobectomy better: perioperatively, biologically and oncologically?". Annals of Thoracic Surgery. 89 (6): S2107–S2111. doi:10.1016/j.athoracsur.2010.03.020. PMID 20493991.
- ^ Simon GR, Turrisi A (2007). "Management of small cell lung cancer: ACCP evidence-based clinical practice guidelines (2nd edition)". Chest. 132 (3 Suppl): 324S–339S. doi:10.1378/chest.07-1385. PMID 17873178.
- ^ Goldstein, SD (2011). "Role of surgery in small cell lung cancer". Surgical Oncology Clinics of North America. 20 (4): 769–777. doi:10.1016/j.soc.2011.08.001. PMID 21986271.
- ^ Arriagada, R (2002). Oxford Textbook of Oncology (edisi ke-2nd). Oxford University Press. hlm. 2094. ISBN 0-19-262926-3.
- ^ Hatton, MQ (2010). "Continuous hyperfractionated accelerated radiotherapy (CHART) and non-conventionally fractionated radiotherapy in the treatment of non-small cell lung cancer: a review and consideration of future directions". Clinical Oncology (Royal College of Radiologists). 22 (5): 356–364. doi:10.1016/j.clon.2010.03.010. PMID 20399629.
- ^ PORT Meta-analysis Trialists Group (2005). Rydzewska, Larysa, ed. "Postoperative radiotherapy for non-small cell lung cancer". Cochrane Database of Systematic Reviews (2): CD002142. doi:10.1002/14651858.CD002142.pub2. PMID 15846628.
- ^ Le Péchoux, C (2011). "Role of postoperative radiotherapy in resected non-small cell lung cancer: a reassessment based on new data". Oncologist. 16 (5): 672–681. doi:10.1634/theoncologist.2010-0150. PMC 3228187
 . PMID 21378080.
. PMID 21378080.
- ^ Cardona, AF (2008). "Palliative endobronchial brachytherapy for non-small cell lung cancer". Cochrane Database of Systematic Reviews (2): CD004284. doi:10.1002/14651858.CD004284.pub2. PMID 18425900.
- ^ Ikushima, H (2010). 2/1/_pdf "Radiation therapy: state of the art and the future" Periksa nilai
|url=(bantuan). Journal of Medical Investigation. 57 (1–2): 1–11. PMID 20299738. [pranala nonaktif permanen] - ^ Paumier, A (2011). "Prophylactic cranial irradiation in lung cancer". Cancer Treatment Reviews. 37 (4): 261–265. doi:10.1016/j.ctrv.2010.08.009. PMID 20934256.
- ^ Girard, N (2011). "Stereotactic radiotherapy for non-small cell lung cancer: From concept to clinical reality. 2011 update". Cancer Radiothérapie. 15 (6–7): 522–526. doi:10.1016/j.canrad.2011.07.241. PMID 21889901.
- ^ Fairchild, A (2008). "Palliative thoracic radiotherapy for lung cancer: a systematic review". Journal of Clinical Oncology. 26 (24): 4001–4011. doi:10.1200/JCO.2007.15.3312. PMID 18711191.
- ^ Hann CL, Rudin CM (2008-11-30). "Management of small-cell lung cancer: incremental changes but hope for the future". Oncology (Williston Park). 22 (13): 1486–92. PMID 19133604.
- ^ Murray, N (March 2006). "A review of first-line treatment for small-cell lung cancer". Journal of Thoracic Oncology. 1 (3): 270–278. PMID 17409868.
- ^ Azim, HA (March 2007). "Treatment options for relapsed small-cell lung cancer". Anticancer drugs. 18 (3): 255–261. doi:10.1097/CAD.0b013e328011a547. PMID 17264756.
- ^ MacCallum, C (July 2006). "Second-line treatment of small-cell lung cancer". Current Oncology Reports. 8 (4): 258–264. doi:10.1007/s11912-006-0030-8. PMID 17254525.
- ^ a b NSCLC Meta-Analyses Collaborative Group (2008). "Chemotherapy in Addition to Supportive Care Improves Survival in Advanced Non–Small-Cell Lung Cancer: A Systematic Review and Meta-Analysis of Individual Patient Data From 16 Randomized Controlled Trials". J. Clin. Oncol. 26 (28): 4617–25. doi:10.1200/JCO.2008.17.7162. PMC 2653127
 . PMID 18678835.
. PMID 18678835.
- ^ Mehra R, Treat J (2008). Fishman's Pulmonary Diseases and Disorders (edisi ke-4th). McGraw-Hill. hlm. 1876. ISBN 0-07-145739-9.
- ^ a b Clegg, A (January 2002). "Clinical and cost effectiveness of paclitaxel, docetaxel, gemcitabine, and vinorelbine in non-small cell lung cancer: a systematic review". Thorax. BMJ Publishing Group. 57 (1): 20–28. doi:10.1136/thorax.57.1.20. PMC 1746188
 . PMID 11809985.
. PMID 11809985.
- ^ Fuld AD, Dragnev KH, Rigas JR (2010). "Pemetrexed in advanced non-small-cell lung cancer". Expert Opin Pharmacother. 11 (8): 1387–402. doi:10.1517/14656566.2010.482560. PMID 20446853.
- ^ Carbone, DP (2011). "Adjuvant therapy in non-small cell lung cancer: future treatment prospects and paradigms". Clinical Lung Cancer. 12 (5): 261–271. doi:10.1016/j.cllc.2011.06.002. PMID 21831720.
- ^ a b Le Chevalier, T (2010). "Adjuvant chemotherapy for resectable non-small-cell lung cancer: where is it going?". Annals of Oncology. 21 (Suppl. 7): vii196–198. doi:10.1093/annonc/mdq376. PMID 20943614.
- ^ Horn, L (May 2007). "The rationale for adjuvant chemotherapy in stage I non-small cell lung cancer". Journal of Thoracic Oncology. 2 (5): 377–383. doi:10.1097/01.JTO.0000268669.64625.bb. PMID 17473651.
- ^ Wakelee, HA (July 2006). "Current status of adjuvant chemotherapy for stage IB non-small-cell lung cancer: implications for the New Intergroup Trial". Clinical Lung Cancer. Cancer Information Group. 8 (1): 18–21. doi:10.3816/CLC.2006.n.028. PMID 16870041.
- ^ Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamaClinical_evidence - ^ Kelley AS, Meier DE (2010). "Palliative care—a shifting paradigm". New England Journal of Medicine. 363 (8): 781–2. doi:10.1056/NEJMe1004139. PMID 20818881.
- ^ a b Prince-Paul M (2009). "When hospice is the best option: an opportunity to redefine goals". Oncology (Williston Park, N.Y.). 23 (4 Suppl Nurse Ed): 13–7. PMID 19856592.
- ^ Souquet PJ, Chauvin F, Boissel JP, Bernard JP (1995). "Meta-analysis of randomised trials of systemic chemotherapy versus supportive treatment in non-resectable non-small cell lung cancer". Lung Cancer. 12 Suppl 1: S147–54. doi:10.1016/0169-5002(95)00430-9. PMID 7551923.
- ^ Sörenson S, Glimelius B, Nygren P (2001). "A systematic overview of chemotherapy effects in non-small cell lung cancer". Acta Oncol. 40 (2–3): 327–39. PMID 11441939.
- ^ Clegg A, Scott DA, Sidhu M, Hewitson P, Waugh N (2001). "A rapid and systematic review of the clinical effectiveness and cost-effectiveness of paclitaxel, docetaxel, gemcitabine and vinorelbine in non-small-cell lung cancer". Health Technol Assess. 5 (32): 1–195. PMID 12065068.
- ^ Templat:Cite Cochrane
- ^ "Non-Small Cell Lung Cancer Treatment". PDQ for Health Professionals. National Cancer Institute. Diakses tanggal 2008-11-22.
- ^ "Small Cell Lung Cancer Treatment". PDQ for Health Professionals. National Cancer Institute. 2012. Diakses tanggal 2012-05-16.
- ^ Spiro, SG (2010). "18.19.1". Oxford Textbook Medicine (edisi ke-5th). OUP Oxford. ISBN 978-0199204854.
- ^ SEER data (SEER.cancer.gov)Median Age of Cancer Patients at Diagnosis 2002-2003
- ^ SEER data (SEER.cancer.gov)Median Age of Cancer Patients at Death 2002-2006
- ^ Slatore, CG (November 2010). "An official American Thoracic Society systematic review: insurance status and disparities in lung cancer practices and outcomes". American Journal of Respiratory and Critical Care Medicine. 182 (9): 1195–1205. doi:10.1164/rccm.2009-038ST. PMID 21041563.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. Diakses tanggal November 11, 2009.
- ^ Jemal A, Tiwari RC, Murray T; et al. (2004). "Cancer statistics, 2004". CA: a Cancer Journal for Clinicians. 54 (1): 8–29. doi:10.3322/canjclin.54.1.8. PMID 14974761.
- ^ Proctor, RN (2012). "The history of the discovery of the cigarette-lung cancer link: evidentiary traditions, corporate denial, global toll". Tobacco Control. 21 (2): 87–91. doi:10.1136/tobaccocontrol-2011-050338. PMID 22345227.
- ^ Lum, KL (October 2008). "Signed, sealed and delivered: "big tobacco" in Hollywood, 1927–1951". Tobacco Control. 17 (5): 313–323. doi:10.1136/tc.2008.025445. PMC 2602591
 . PMID 18818225.
. PMID 18818225.
- ^ Lovato, C (October 2011). "Impact of tobacco advertising and promotion on increasing adolescent smoking behaviours". Cochrane Database of Systematic Reviews (10): CD003439. doi:10.1002/14651858.CD003439.pub2. PMID 21975739.
- ^ Kemp, FB (2009). "Smoke free policies in Europe. An overview". Pneumologia. 58 (3): 155–158. PMID 19817310.
- ^ National Cancer Institute; SEER stat fact sheets: Lung and Bronchus. Surveillance Epidemiology and End Results. 2010 [1]
- ^ "Gender in lung cancer and smoking research" (PDF). World Health Organization. 2004. Diakses tanggal 2007-05-26.
- ^ Zhang, J (November 2011). "Tobacco smoking in China: prevalence, disease burden, challenges and future strategies". Respirology. 16 (8): 1165–1172. doi:10.1111/j.1440-1843.2011.02062.x. PMID 21910781.
- ^ Behera, D (2004). "Lung cancer in India" (PDF). Indian Journal of Chest Diseases and Allied Sciences. 46 (4): 269–281. PMID 15515828. Diarsipkan dari versi asli (PDF) tanggal 2008-12-17. Diakses tanggal 2014-01-30.
- ^ Charloux, A (February 1997). "The increasing incidence of lung adenocarcinoma: reality or artefact? A review of the epidemiology of lung adenocarcinoma". International Journal of Epidemiology. 26 (1): 14–23. doi:10.1093/ije/26.1.14. PMID 9126499.
- ^ Kadara, H (2012). "Pulmonary adenocarcinoma: a renewed entity in 2011". Respirology. 17 (1): 50–65. doi:10.1111/j.1440-1843.2011.02095.x. PMID 22040022.
- ^ Morgagni, Giovanni Battista (1761). De sedibus et causis morborum per anatomen indagatis. OL 24830495M.
- ^ Bayle, Gaspard-Laurent (1810). Recherches sur la phthisie pulmonaire (dalam bahasa French). Paris. OL 15355651W.
- ^ a b Witschi, H (November 2001). "A short history of lung cancer". Toxicological Sciences. 64 (1): 4–6. doi:10.1093/toxsci/64.1.4. PMID 11606795.
- ^ Adler, I (1912). Primary Malignant Growths of the Lungs and Bronchi. New York: Longmans, Green, and Company. OCLC 14783544. OL 24396062M., cited in Spiro SG, Silvestri GA (2005). "One hundred years of lung cancer". American Journal of Respiratory and Critical Care Medicine. 172 (5): 523–529. doi:10.1164/rccm.200504-531OE. PMID 15961694.
- ^ Grannis, FW. "History of cigarette smoking and lung cancer". smokinglungs.com. Diarsipkan dari versi asli tanggal July 18, 2007. Diakses tanggal 2007-08-06.
- ^ Proctor, R (2000). The Nazi War on Cancer. Princeton University Press. hlm. 173–246. ISBN 0-691-00196-0.
- ^ Doll, R (November 1956). "Lung Cancer and Other Causes of Death in Relation to Smoking". British Medical Journal. 2 (5001): 1071–1081. doi:10.1136/bmj.2.5001.1071. PMC 2035864
 . PMID 13364389.
. PMID 13364389.
- ^ US Department of Health Education and Welfare (1964). "Smoking and health: report of the advisory committee to the Surgeon General of the Public Health Service" (PDF). Washington, DC: US Government Printing Office.
- ^ a b Greaves, M (2000). Cancer: the Evolutionary Legacy. Oxford University Press. hlm. 196–197. ISBN 0-19-262835-6.
- ^ Greenberg, M (1993). "Lung cancer in the Schneeberg mines: a reappraisal of the data reported by Harting and Hesse in 1879". Annals of Occupational Hygiene. 37 (1): 5–14. PMID 8460878.
- ^ Samet, JM (2011). "Radiation and cancer risk: a continuing challenge for epidemiologists". Environmental Health. 10 (Suppl. 1): S4. doi:10.1186/1476-069X-10-S1-S4. PMC 3073196
 . PMID 21489214.
. PMID 21489214.
- ^ Horn, L (July 2008). "Evarts A. Graham and the first pneumonectomy for lung cancer". Journal of Clinical Oncology. 26 (19): 3268–3275. doi:10.1200/JCO.2008.16.8260. PMID 18591561. Diarsipkan dari versi asli tanggal 2020-03-17. Diakses tanggal 2014-01-30.
- ^ Edwards, AT (1946). "Carcinoma of the Bronchus". Thorax. 1 (1): 1–25. doi:10.1136/thx.1.1.1. PMC 1018207
 . PMID 20986395.
. PMID 20986395.
- ^ Kabela, M (1956). "Erfahrungen mit der radikalen Röntgenbestrahlung des Bronchienkrebses". Ceskoslovenská Onkológia (dalam bahasa German). 3 (2): 109–115. PMID 13383622.
- ^ Saunders, M (July 1997). "Continuous hyperfractionated accelerated radiotherapy (CHART) versus conventional radiotherapy in non-small-cell lung cancer: a randomised multicentre trial". Lancet. Elsevier. 350 (9072): 161–165. doi:10.1016/S0140-6736(97)06305-8. PMID 9250182.
- ^ Lennox, SC (November 1968). "Results of resection for oat-cell carcinoma of the lung". Lancet. Elsevier. 2 (7575): 925–927. doi:10.1016/S0140-6736(68)91163-X. PMID 4176258.
- ^ Miller, AB (September 1969). "Five-year follow-up of the Medical Research Council comparative trial of surgery and radiotherapy for the primary treatment of small-celled or oat-celled carcinoma of the bronchus". Lancet. Elsevier. 2 (7619): 501–505. doi:10.1016/S0140-6736(69)90212-8. PMID 4184834.
- ^ Cohen, M (1977). "Intensive chemotherapy of small cell bronchogenic carcinoma". Cancer Treatment Reports. 61 (3): 349–354. PMID 194691.
<ref> dengan nama "Clinical evidence" yang didefinisikan di <references> tidak digunakan pada teks sebelumnya.Pranala luar[sunting | sunting sumber]
- Kanker paru-paru di Curlie (dari DMOZ)
