Derajat kebebasan (fisika dan kimia)
Derajat kebebasan adalah suatu parameter fisika yang independen, biasa disebut dimensi, dalam deskripsi formal merupakan keadaan suatu sistem fisika. Himpunan semua dimensi dari suatu sistem dikenal sebagai ruang fasa.
Definisi[sunting | sunting sumber]
Dalam fisika, derajat kebebasan suatu sistem merupakan deskripsi formal dari parameter yang berkontribusi untuk keadaan dari sistem fisika. Juga bisa didefinisikan sebagai suatu angka minimum yang diperlukan untuk menentukan koordinat posisi suatu partikel atau sistem partikel. Dalam mekanika, partikel titik dapat bergerak secara bebas tiga arah dalam ruang. Dengan demikian, momentum suatu partikel terdiri atas tiga komponen, masing-masing disebut derajat kebebasan. Suatu sistem terdiri atas N partikel bebas sehingga memiliki total derajat kebebasan 3N. Demikian juga dalam mekanika statistik, derajat kebebasan adalah angka skalar tunggal yang menggambarkan keadaan mikro suatu sistem. Spesifikasi semua keadaan mikro sistem adalah suatu titik dalam ruang fasa sistem. Derajat kebebasan yang digunakan tidak bergantung pada variabel lain. Sebagai contoh, dalam model rantai ideal 3D, dua sudut yang diperlukan untuk menjelaskan masing-masing orientasi monomor.
Contoh: Gas diatomik[sunting | sunting sumber]
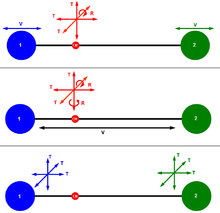
Dalam ruang tiga dimensi, tiga derajat kebebasan berkaitan dengan suatu mekanika partikel. Molekul gas diatomik memiliki 6 derajat kebebasan dalam bentuk translasi, rotasi, dan vibrasi molekul. Pergerakan massa inti menyumbang 3 derajat kebebasan dan molekul meiliki satu vibrasi dan dua rotasi sudut gerak. Rotasi terjadi disekitar dua sumbu yang saling tegak lurus di antara dua atom. Rotasi disekitar ikatan atom-ato tidak dihitung. Untuk molekul diatom menghasilkan:
- 3N = 6 = 3 + 1 + 2.
Untuk molekul dengan jumlah atom N > 2, dianggap memiliki 3 rotasi derajat kebebasan.
- 3 N = 3 + 3 + (3 N - 6)
dengan molekul N-atom memiliki 3 N - 6 vibrasi derajat kebebasan untuk N > 2.
Selain itu, menghitung derajat kebebasan dapat juga menggunakan nilai minimum koordinat yang diperlukan untuk menentukan posisi. Hal ini dilakukan sebagai berikut: 1. Untuk partikel tunggal diperlukan 2 koordinat pada bidang 2-D untuk menentukan posisinya dan derajat kaebebasan pada bidang 3-D adalah 3. 2. Untuk sistem yang terdiri atas 2 partikel (molekul diatomik) pada bidang 3-D dengan jarak konstan (d) memiliki derajat kebebasan 5. Satu partikel memiliki koordinat (x1,y1,z1) dan koordinat lainnya (x2) dan (y2). Persamaan untuk jarak antara 2 koordinat atom ( ) diperoleh nilai yang mengandung (z2). (Catatan:x1, x2, y1, y2, z1, atau z2 bisa aja tidak diketahui.) Berlawanan dengan teorema equipartisi klasik, pada gerak vibrasi molekul biasanya kapasitas suhu dapat diabaikan. Hal ini menyebabkan derajat kebebasan dibekukan karena jarak antara energi nilai eigen melebihi energi yang sesuai dengan suhu lingkungan (kT). Dalam tabel berikut derajat kebebasan diabaikan karena efeknya yang kecil terhadap energi total. Namun, pada suhu yang sangat tinggi derajat kebebasan tidak bisa diabaikan.
| Monatomik | Molekul linear | Non-Linear molekul | |
|---|---|---|---|
| Posisi (x, y and z) | 3 | 3 | 3 |
| Rotasi (x, y and z) | 0 | 2 | 3 |
| Vibrasi | 0 | 3N - 5 | 3N - 6 |
| Total | 3 | 3N | 3N |
Derajat kebebasan Independen[sunting | sunting sumber]
Derajat kebebasan terdiri atas suatu sistem yang independen jika energi assosiatif diatur bisa ditulis sebagai berikut: di mana adalah fungsi dengan variabel tunggal . example: jika and memiliki 2 derajat kebebasan, dan adalah energi assosiatif:
- Jika , dengan dua derajat kebebasan yang independen.
- Jika , dengan dua derajat kebebasan yang tidak independen. Istilah yang melibatkan produk dan adalah istilah kopling, yang menggambarkan interaksi antara dua derajat kebebasan.
Pada termodinamika equilibrium, semua statistik independen satu sama lain.
Untuk i dari 1 to N, dengan iderajat kebebasan didistribusikan berdasarkan distribusi Boltzmann. Probability fungsi kerapatan mengikuti:
- ,
Pada bagian ini, seluruh artikel dengan tanda kurung menunjukkan mean rata-rata jumlah.
Energi internal sistem merupakan jumlah dari rata-rata energi asosiatif untuk setiap derjat kebebasan:
Demonstrasi[sunting | sunting sumber]
Sebuah pertukaran energi sistem dalam bentuk panas dengan lingkungannya dan jumlah partikel dalam sistem tetap. Hal ini terkait dengan sistem dalam ansambel kanonik. Perhatikan bahwa dalam mekanika statistik, hasil yang ditunjukkan untuk sistem dalam ansambel tertentu tetap untuk sistem ini pada batas termodinamika dalam ansambel apapun. Dalam ansambel kanonik, kesetimbangan termodinamika, keadaan dari sistem didistribusikan di antara semua keadaan mikro berdasarkan distribusi Boltzmann. Jika suhu sistem dan konstanta Boltzmann, maka probabilitas fungsi kerapatan yang terkait untuk setiap keadaan mikro adalah sebagai berikut:
- ,
Penyebut pada persamaan di atas memiliki peranan penting. Dalam hal ini, terbentuk produk bergantung pada derajat kebebasan tunggal.
Gangguan dari multidimensional probabilitas fungsi kepadatan menjadi fungsi produk dengan satu variabel sudah cukup untuk menunjukkan bahwa X_1 adalah Konstanta Normalisasi, mengikuti bahwa adalah probabiliti fungsi kerapatan dari derajat kebebasan , untuk i dari 1 sampai N.
Sehingga energi internal dari sistem merupakan energi rata-rata. Energi dari derajat kebebasan adalah fungsi dari variabel tunggal . Jika adalah statistik independent satu sama lain, maka energi juga statistik independen satu sama lain. Total energi internal dari sistem bisa ditulis:
Derajat Kebebasan Kuadratik[sunting | sunting sumber]
Suatu derajat kebebasan adalah kuadratik apabila the energi terkait dengan derajat kebebasan, dapat ditulis sebagai
- ,
di mana adalah kombinasi linear dari setiap derajat kebebasan kuadratik.
contoh: jika dan adalah dua derajat kebebasan, dan adalah energi asosiatif:
- Jika , dengan dua derajat kebebasan yang tidak independen dan non-kuadratik.
- Jika , dengan dua derajat kebebasan yang independen and non-quadratik.
- Jika , dengan dua derajat kebebasan yang tidak independen dan kuadratik.
- Jika , dengan dua derajat kebebasan yang independen dan kuadratik.
Sebagai contoh, dalam Newtonian mechanics, dynamics suatu sistem dengan derajat kebebasan kuadratik diatur sehingga homogen persamaan differential linear dengan koefisien konstan.
Derajat Kebebasan Independen dan Kuadratik[sunting | sunting sumber]
adalah derajat kebebasan kuadratik dan independen apabila energi assosiatif untuk keadaan mikro suatu sistem bisa dipresentasikan sebagai berikut:
Teorema Equipartisi[sunting | sunting sumber]
Pada batasan klasik mekanika statisti, pada equilibrium termodinamika, energi internal dari suatu sistem N derajat kebebasan independen dan kuadratik adalah:
Disini, mean energi assosiatif dengan derajat kebebasan adalah:
Apabila derajat kebebasan independen, energi internal dari sistem setara dengan jumlah rata-rata energi assosiatif dengan setiap derajat kebebasan, yang dapat ditunjukkan pada hasil.
Rujukan[sunting | sunting sumber]
- [["Configuration integral (statistical mechanics)". http://clesm.mae.ufl.edu/wiki.pub/index.php/Configuration[pranala nonaktif permanen] integral (statistical mechanics)#Thermodynamic properties.]]



















![{\displaystyle \ ldotsX_{N}</math>adalah[[statistikindependen]]satusamalain.Setiapfungsi<math>p_{i}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/99d586875b8ed81e9709e66d8f39af43e458d27a)











