Rantai transpor elektron: Perbedaan antara revisi
Imamsyahid (bicara | kontrib) |
Imamsyahid (bicara | kontrib) sitasi |
||
| Baris 7: | Baris 7: | ||
Pada rantai transpor elektron, reaksi redoks yang terjadi didorong oleh keadaan [[energi bebas Gibbs]] pada komponen-komponen rantai ini. Energi bebas gibbs berhubungan dengan suatu besaran yang disebut potensial redoks (kecenderungan suatu senyawa untuk menangkap elektron, atau tereduksi, yang diukur dalam satuan Volt). |
Pada rantai transpor elektron, reaksi redoks yang terjadi didorong oleh keadaan [[energi bebas Gibbs]] pada komponen-komponen rantai ini. Energi bebas gibbs berhubungan dengan suatu besaran yang disebut potensial redoks (kecenderungan suatu senyawa untuk menangkap elektron, atau tereduksi, yang diukur dalam satuan Volt). |
||
Suatu elektron bergerak dari potensial redoks yang rendah menuju potensial redoks yang tinggi. Pada rantai transpor elektron, ketika elektron tersebut terdorong oleh potensialnya menuju potensial yang tinggi, maka elektron tersebut akan melepaskan energi. Energi inilah yang nantinya ditangkap oleh kompleks protein pada rantai transpor elektron. Protein kompleks akan menggunakan energi ini untuk melepaskan proton ke lumen dan menciptakan perbedaan konsentrasi (gradien) proton diantara membran. Gradien merupakan kondisi yang tidak stabil. Untuk stabil, proton diantara kedua sisi membran harus sama besar. Karena hal itulah proton yang tadi di pompa akan berusaha kembali ke dalam sisi membran lewat [[ATP sintase|ATP sintase.]]<ref>{{Cite |
Suatu elektron bergerak dari potensial redoks yang rendah menuju potensial redoks yang tinggi. Pada rantai transpor elektron, ketika elektron tersebut terdorong oleh potensialnya menuju potensial yang tinggi, maka elektron tersebut akan melepaskan energi. Energi inilah yang nantinya ditangkap oleh kompleks protein pada rantai transpor elektron. Protein kompleks akan menggunakan energi ini untuk melepaskan proton ke lumen dan menciptakan perbedaan konsentrasi (gradien) proton diantara membran. Gradien merupakan kondisi yang tidak stabil. Untuk stabil, proton diantara kedua sisi membran harus sama besar. Karena hal itulah proton yang tadi di pompa akan berusaha kembali ke dalam sisi membran lewat [[ATP sintase|ATP sintase.]]<ref>{{Cite book|last=Gerasimovskaya|first=Evgenia|last2=Kaczmarek|first2=Elzbieta|date=2010-04-26|url=https://books.google.co.id/books?id=UbTOMhtTYrwC|title=Extracellular ATP and adenosine as regulators of endothelial cell function: Implications for health and disease|location=|publisher=Springer Science & Business Media|isbn=978-90-481-3435-9|pages=139|language=en|url-status=live}}</ref> ATP sintase akan menggunakan energi perpindahan proton ini untuk menggerakkan sintesis ATP dengan [[fosforilasi oksidatif]] <ref>{{Cite journal|last=Anraku|first=Yasuhiro|date=1988-06-01|title=Bacterial electron transport chains|url=https://www.annualreviews.org/doi/10.1146/annurev.bi.57.070188.000533|journal=Annual Review of Biochemistry|volume=57|issue=1|pages=101–132|doi=10.1146/annurev.bi.57.070188.000533|issn=0066-4154}}</ref> |
||
Rantai transpor elektron dan fosforilasi oksidatif terdapat di [[Mitokondria|membran dalam mitokondria (''cristae).'']] Elektron-elektron ini berasal dari molekul-molekul yang sebelumnya tereduksi (ingat bahwa reduksi artinya menangkap elektron) seperti NADH dan FADH. Pada tumbuhan atau eukariot yang berfotosintesis, [[Foton|cahaya matahari]] akan menggerakkan elektron lewat [[fotosistem]] hingga pada akhirnya menghasilkan ATP. Pada [[Bakteri]], rantai transpor elektron sangat bervariasi. Namun pada makhluk hidup manapun intinya tetap sama, yaitu serangkaian reaksi redoks yang menciptakan gradien elektrokimia yang akan mensintesis ATP lewat fosforilasi oksidatif melalui ATP Sintase.<ref>{{Cite journal|last=Kracke|first=Frauke|last2=Vassilev|first2=Igor|last3=Krömer|first3=Jens O.|date=2015|title=Microbial electron transport and energy conservation – the foundation for optimizing bioelectrochemical systems|url=https://www.frontiersin.org/articles/10.3389/fmicb.2015.00575/full|journal=Frontiers in Microbiology|language=English|volume=6|doi=10.3389/fmicb.2015.00575|issn=1664-302X|pmc=PMC4463002|pmid=26124754}}</ref> |
Rantai transpor elektron dan fosforilasi oksidatif terdapat di [[Mitokondria|membran dalam mitokondria (''cristae).'']] Elektron-elektron ini berasal dari molekul-molekul yang sebelumnya tereduksi (ingat bahwa reduksi artinya menangkap elektron) seperti NADH dan FADH. Pada tumbuhan atau eukariot yang berfotosintesis, [[Foton|cahaya matahari]] akan menggerakkan elektron lewat [[fotosistem]] hingga pada akhirnya menghasilkan ATP. Pada [[Bakteri]], rantai transpor elektron sangat bervariasi. Namun pada makhluk hidup manapun intinya tetap sama, yaitu serangkaian reaksi redoks yang menciptakan gradien elektrokimia yang akan mensintesis ATP lewat fosforilasi oksidatif melalui ATP Sintase.<ref>{{Cite journal|last=Kracke|first=Frauke|last2=Vassilev|first2=Igor|last3=Krömer|first3=Jens O.|date=2015|title=Microbial electron transport and energy conservation – the foundation for optimizing bioelectrochemical systems|url=https://www.frontiersin.org/articles/10.3389/fmicb.2015.00575/full|journal=Frontiers in Microbiology|language=English|volume=6|doi=10.3389/fmicb.2015.00575|issn=1664-302X|pmc=PMC4463002|pmid=26124754}}</ref> |
||
| Baris 16: | Baris 16: | ||
Pergerakan elektron dari donor ke akseptor akan melepaskan energi, yang digunakan untuk menghasikan gradien proton diantara membran mitokondira dengan "memompa" proton menuju ruang antar-membran, menghasilkan kondisi termodinamika yang memiliki [[Potensial aksi|Potensial]] untuk melakukan kerja. Keseluruhan proses ini disebut [[Fosforilasi oksidatif]] karena ADP akan terfosforilasi menjadi ATP dalam suatu rangkaian transpor elektron yang membutuhkan oksigen. |
Pergerakan elektron dari donor ke akseptor akan melepaskan energi, yang digunakan untuk menghasikan gradien proton diantara membran mitokondira dengan "memompa" proton menuju ruang antar-membran, menghasilkan kondisi termodinamika yang memiliki [[Potensial aksi|Potensial]] untuk melakukan kerja. Keseluruhan proses ini disebut [[Fosforilasi oksidatif]] karena ADP akan terfosforilasi menjadi ATP dalam suatu rangkaian transpor elektron yang membutuhkan oksigen. |
||
Energi dihasilkan melalui transfer elekton yang menuruni rantai tranfer elektron. Energi ini digunakan untuk memompa proton dari matriks [[Mitokondria]] menuju ruang antar-membran, menciptakan gradien proton (ΔpH) diantara dua sisi membran dalam mitokondria. Gradien proton in menyebabkan adanya [[potensial membran]] (ΔΨ<sub>M</sub>)<ref>{{Cite journal|last=Zorova|first=Ljubava D.|last2=Popkov|first2=Vasily A.|last3=Plotnikov|first3=Egor Y.|last4=Silachev|first4=Denis N.|last5=Pevzner|first5=Irina B.|last6=Jankauskas|first6=Stanislovas S.|last7=Babenko|first7=Valentina A.|last8=Zorov|first8=Savva D.|last9=Balakireva|first9=Anastasia V.|date=2018-07-01|title=Mitochondrial membrane potential|url= |
Energi dihasilkan melalui transfer elekton yang menuruni rantai tranfer elektron. Energi ini digunakan untuk memompa proton dari matriks [[Mitokondria]] menuju ruang antar-membran, menciptakan gradien proton (ΔpH) diantara dua sisi membran dalam mitokondria. Gradien proton in menyebabkan adanya [[potensial membran]] (ΔΨ<sub>M</sub>)<ref>{{Cite journal|last=Zorova|first=Ljubava D.|last2=Popkov|first2=Vasily A.|last3=Plotnikov|first3=Egor Y.|last4=Silachev|first4=Denis N.|last5=Pevzner|first5=Irina B.|last6=Jankauskas|first6=Stanislovas S.|last7=Babenko|first7=Valentina A.|last8=Zorov|first8=Savva D.|last9=Balakireva|first9=Anastasia V.|date=2018-07-01|title=Mitochondrial membrane potential|url=|journal=Analytical Biochemistry|series=Mitochondrial Biochemistry and Bioenergenetics|language=en|volume=552|issue=|pages=50–59|doi=10.1016/j.ab.2017.07.009|issn=0003-2697|pmc=PMC5792320|pmid=28711444}}</ref> . Hal ini memungkinkan ATP sintase untuk menggunakan aliran H+ melalui enzim tersebut untuk memfosforilasi ATP dari ADP dan fosfat. |
||
=== Karier Redoks Mitokondria === |
=== Karier Redoks Mitokondria === |
||
| Baris 27: | Baris 27: | ||
[[Kemiosmosis|Hipotesis Penggandengan Kemiosmosis]] yang dicetuskan oleh pemenang [[Penghargaan Nobel Kimia]], [[Peter Mitchell (kimiawan)|Peter Mitchell]], mengusulkan bahwa rantai transpor elektron dan fosforilasi oksidatif digandeng dengan gradien proton yang melintasi membran dalam mitokondria. |
[[Kemiosmosis|Hipotesis Penggandengan Kemiosmosis]] yang dicetuskan oleh pemenang [[Penghargaan Nobel Kimia]], [[Peter Mitchell (kimiawan)|Peter Mitchell]], mengusulkan bahwa rantai transpor elektron dan fosforilasi oksidatif digandeng dengan gradien proton yang melintasi membran dalam mitokondria. |
||
Proton yang dipompa oleh kompleks protetin akan menghasilkan gradien elektrokimia. Gradien ini akan dingunakan oleh ATP sintase untuk membuat ATP lewat fosforilasi oksidatif. Komponen Fo dari ATP sintase berperan sebagai sebagai [[saluran ion]] yang akan dilintasi oleh proton untuk kembali ke matriks mitokondria. Komponen Fo terdiri dari subunit a,b, dan c. Proton pada ruang intra-membran akan memasuki ATP sintase lewat subunit a, lalu bergerak menuju subunit c<ref>{{Cite journal|last=Walsh|first=Edward J.|date=1997-02|title=Biochemistry (Garrett, Reginald H.; Grisham, Charles M.)|url=http://dx.doi.org/10.1021/ed074p189.2|journal=Journal of Chemical Education|volume=74|issue=2|pages=189|doi=10.1021/ed074p189.2|issn=0021-9584}}</ref>. Jumlah subunit c akan menentukan berapa banyak proton yang dibutuhkan untuk memutar Fo menjadi satu putaran penuh. Contohnya, pada manusia, terdapat 8 subunit c, sehingga dibutuhkan 8 proton <ref>{{Cite journal|last=Fillingame|first=Robert H.|last2=Angevine|first2=Christine M.|last3=Dmitriev|first3=Oleg Y.|date=2003|title=Mechanics of coupling proton movements to c-ring rotation in ATP synthase|url=https://febs.onlinelibrary.wiley.com/doi/abs/10.1016/S0014-5793%2803%2901101-3|journal=FEBS Letters|language=en|volume=555|issue=1|pages=29–34|doi=10.1016/S0014-5793(03)01101-3|issn=1873-3468}}</ref>. Setelah subunit c, proton akhirnya akan memasuki matriks mitokondira menggunakan subunit yang terbuka menuju matriks mitokondria. Aliran proton ini akan melepaskan [[energi bebas]] dalam bentuk karier elektron yang teroksidasi (NAD+ dan Q). Energi bebas ini akan digunakan untuk mendorong sintesis ATP, yang dikatalisis oleh komponen F1 dari kompleks ATP sinstase<ref>{{Cite journal|last=Berg|first=Jeremy M.|last2=Tymoczko|first2=John L.|last3=Stryer|first3=Lubert|date=2002|title=A Proton Gradient Powers the Synthesis of ATP|url=https:// |
Proton yang dipompa oleh kompleks protetin akan menghasilkan gradien elektrokimia. Gradien ini akan dingunakan oleh ATP sintase untuk membuat ATP lewat fosforilasi oksidatif. Komponen Fo dari ATP sintase berperan sebagai sebagai [[saluran ion]] yang akan dilintasi oleh proton untuk kembali ke matriks mitokondria. Komponen Fo terdiri dari subunit a,b, dan c. Proton pada ruang intra-membran akan memasuki ATP sintase lewat subunit a, lalu bergerak menuju subunit c<ref>{{Cite journal|last=Walsh|first=Edward J.|date=1997-02|title=Biochemistry (Garrett, Reginald H.; Grisham, Charles M.)|url=http://dx.doi.org/10.1021/ed074p189.2|journal=Journal of Chemical Education|volume=74|issue=2|pages=189|doi=10.1021/ed074p189.2|issn=0021-9584}}</ref>. Jumlah subunit c akan menentukan berapa banyak proton yang dibutuhkan untuk memutar Fo menjadi satu putaran penuh. Contohnya, pada manusia, terdapat 8 subunit c, sehingga dibutuhkan 8 proton <ref>{{Cite journal|last=Fillingame|first=Robert H.|last2=Angevine|first2=Christine M.|last3=Dmitriev|first3=Oleg Y.|date=2003|title=Mechanics of coupling proton movements to c-ring rotation in ATP synthase|url=https://febs.onlinelibrary.wiley.com/doi/abs/10.1016/S0014-5793%2803%2901101-3|journal=FEBS Letters|language=en|volume=555|issue=1|pages=29–34|doi=10.1016/S0014-5793(03)01101-3|issn=1873-3468}}</ref>. Setelah subunit c, proton akhirnya akan memasuki matriks mitokondira menggunakan subunit yang terbuka menuju matriks mitokondria. Aliran proton ini akan melepaskan [[energi bebas]] dalam bentuk karier elektron yang teroksidasi (NAD+ dan Q). Energi bebas ini akan digunakan untuk mendorong sintesis ATP, yang dikatalisis oleh komponen F1 dari kompleks ATP sinstase<ref>{{Cite journal|last=Berg|first=Jeremy M.|last2=Tymoczko|first2=John L.|last3=Stryer|first3=Lubert|date=2002|title=A Proton Gradient Powers the Synthesis of ATP|url=https://books.google.co.id/books?id=5k3OCwAAQBAJ|journal=Biochemistry. 5th edition|language=en|volume=|issue=|pages=356|doi=}}</ref>. Penggandengan dengan fosforilasi oksidatif sangatlah penting untuk produksi ATP. Namun, dalam kasus spesifik, memisahkan kedua proses ini menjadi dua proses yang berbeda mungkin dapat bermanfaat secara biologis. Salah satu protein yang disebut [[thermogenin]] menyediakan saluran alternatif proton untuk kembali ke matriks mitokondira. |
||
== Referensi == |
== Referensi == |
||
Revisi per 18 November 2020 09.31

Rantai transpor elektron (bahasa Inggris: electron transport chain, respiratory chain, ETC), merupakan rangkaian protein kompleks (kimia) yang mentransfer elektron dari donor elektron menuju akseptor elektron melalui reaksi redoks (reduksi dan oksidasi terjadi secara bersamaan). Transfer elektron ini akan mentransfer proton (H+) melintasi membran. Secara keseluruhan, rantai transpor elektron terdiri dari protein, enzim, dan molekul-molekul lainnya.
Elektron-elektron ini mengalir melintasi rantai elektron. Keseluruhan reaksi redoks yang terjadi pada rantai transpor elektron merupakan reaksi eksergonik,yaitu melepaskan energi. Energi ini akan digunakan untuk membuat gradien elektrokimia yang akan mendorong sintesis adenosina trifosfat (ATP). Pada akhirnya, aliran elektron ini akan berakhir pada oksigen sebagai akseptor elektron terkahir, mengasilkan H2O (Air). Pada respirasi anaerobik, ketidaktersediaan oksigen akan diganti dengan molekul lain, seperti Sulfat yang menghasilkan H2S (Asam sulfat), Nitrat, ataupun Sulfur. Hal ini merupakan salah satu adaptasi terhadap ketersediaan molekul pada habitat organisme tersebut.
Pada rantai transpor elektron, reaksi redoks yang terjadi didorong oleh keadaan energi bebas Gibbs pada komponen-komponen rantai ini. Energi bebas gibbs berhubungan dengan suatu besaran yang disebut potensial redoks (kecenderungan suatu senyawa untuk menangkap elektron, atau tereduksi, yang diukur dalam satuan Volt).
Suatu elektron bergerak dari potensial redoks yang rendah menuju potensial redoks yang tinggi. Pada rantai transpor elektron, ketika elektron tersebut terdorong oleh potensialnya menuju potensial yang tinggi, maka elektron tersebut akan melepaskan energi. Energi inilah yang nantinya ditangkap oleh kompleks protein pada rantai transpor elektron. Protein kompleks akan menggunakan energi ini untuk melepaskan proton ke lumen dan menciptakan perbedaan konsentrasi (gradien) proton diantara membran. Gradien merupakan kondisi yang tidak stabil. Untuk stabil, proton diantara kedua sisi membran harus sama besar. Karena hal itulah proton yang tadi di pompa akan berusaha kembali ke dalam sisi membran lewat ATP sintase.[1] ATP sintase akan menggunakan energi perpindahan proton ini untuk menggerakkan sintesis ATP dengan fosforilasi oksidatif [2]
Rantai transpor elektron dan fosforilasi oksidatif terdapat di membran dalam mitokondria (cristae). Elektron-elektron ini berasal dari molekul-molekul yang sebelumnya tereduksi (ingat bahwa reduksi artinya menangkap elektron) seperti NADH dan FADH. Pada tumbuhan atau eukariot yang berfotosintesis, cahaya matahari akan menggerakkan elektron lewat fotosistem hingga pada akhirnya menghasilkan ATP. Pada Bakteri, rantai transpor elektron sangat bervariasi. Namun pada makhluk hidup manapun intinya tetap sama, yaitu serangkaian reaksi redoks yang menciptakan gradien elektrokimia yang akan mensintesis ATP lewat fosforilasi oksidatif melalui ATP Sintase.[3]
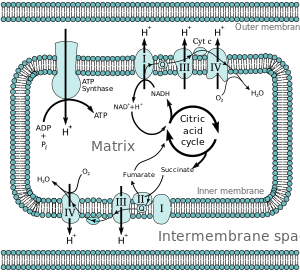
Rantai Transpor Elektron pada Mitokondria
Kebanyak sel Eukariota memiliki Mitokondria yang menghasilkan ATP dari produk hasil Siklus asam sitrat. Pada membran dalam mitokondria, NADH dan FADH akan melepaskan elektronnya, melintasi rantai transpor elektron, dan akan bertemu dengan oksigen, yang akan tereduksi menjadi air[4]. Rantai transpor elektron ini terdiri dari serangkaian enzim yang berfungsi sebagai donor dan akseptor elektron. Setiap donor elektron akan menggerakkan elektron tersebut kepada akseptor yang lebih Elektronegatif, yang selanjutnya akan kembali menggerakkan elektron tersebut ke akseptor lainnya. Proses ini terus berulang sampai elektron tersebut sampai ke oksigen, yang merupakan, molekul paling elektronegatif pada rantai tersebut.

Pergerakan elektron dari donor ke akseptor akan melepaskan energi, yang digunakan untuk menghasikan gradien proton diantara membran mitokondira dengan "memompa" proton menuju ruang antar-membran, menghasilkan kondisi termodinamika yang memiliki Potensial untuk melakukan kerja. Keseluruhan proses ini disebut Fosforilasi oksidatif karena ADP akan terfosforilasi menjadi ATP dalam suatu rangkaian transpor elektron yang membutuhkan oksigen.
Energi dihasilkan melalui transfer elekton yang menuruni rantai tranfer elektron. Energi ini digunakan untuk memompa proton dari matriks Mitokondria menuju ruang antar-membran, menciptakan gradien proton (ΔpH) diantara dua sisi membran dalam mitokondria. Gradien proton in menyebabkan adanya potensial membran (ΔΨM)[5] . Hal ini memungkinkan ATP sintase untuk menggunakan aliran H+ melalui enzim tersebut untuk memfosforilasi ATP dari ADP dan fosfat.
Karier Redoks Mitokondria
Rantai transpor elektron pada mitokondria terdiri dari serangkaian kompleks protein yang berperan dalam mengalirkan elektron. Terdapat empat kompleks yang sudah teridentifikasi pada mitokondria. Masing-masing merupakan struktur transmembran yang sangat kompleks dan tertanam pada membran dalam. Tiga diantaranya merupakan pompa proton. Struktur kompleks ini saling terhubung secara elektrostatis dengan karier elektron yang hidrofobik maupaun karier elektron yang hidrofilik.

Kompleks I (NADH ko-enzim Q Reduktase; ditulis I) menerima elektron dari NADH (karier elektron dari siklus krebs) dan akan meneruskannya ke Koenzim Q (Ubikuinon; ditulis Q). Selain dari kompleks I, Q juga menerima elektron dari kompleks II (Suksinat dehidrogenase; ditulis II). Selanjutnya, Q akan mengirimkan elektron tersebut menuju kompleks III (kompleks sitokrom bc1; ditulis III) yang akan melanjutkan elektron tersebut menuju Sitokrom c (ditulis Cyt c). Cyt c akan mengalirkan elektron menuju kompleks IV (sitokrom c oksidase; ditulis IV), yang akan menggunakan elektron dan ion hidrogen untuk mereduksi oksigen menjadi air.
Penggandengan dengan Fosforilasi Oksidatif
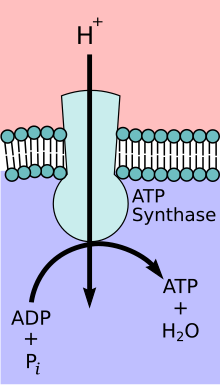
Hipotesis Penggandengan Kemiosmosis yang dicetuskan oleh pemenang Penghargaan Nobel Kimia, Peter Mitchell, mengusulkan bahwa rantai transpor elektron dan fosforilasi oksidatif digandeng dengan gradien proton yang melintasi membran dalam mitokondria.
Proton yang dipompa oleh kompleks protetin akan menghasilkan gradien elektrokimia. Gradien ini akan dingunakan oleh ATP sintase untuk membuat ATP lewat fosforilasi oksidatif. Komponen Fo dari ATP sintase berperan sebagai sebagai saluran ion yang akan dilintasi oleh proton untuk kembali ke matriks mitokondria. Komponen Fo terdiri dari subunit a,b, dan c. Proton pada ruang intra-membran akan memasuki ATP sintase lewat subunit a, lalu bergerak menuju subunit c[6]. Jumlah subunit c akan menentukan berapa banyak proton yang dibutuhkan untuk memutar Fo menjadi satu putaran penuh. Contohnya, pada manusia, terdapat 8 subunit c, sehingga dibutuhkan 8 proton [7]. Setelah subunit c, proton akhirnya akan memasuki matriks mitokondira menggunakan subunit yang terbuka menuju matriks mitokondria. Aliran proton ini akan melepaskan energi bebas dalam bentuk karier elektron yang teroksidasi (NAD+ dan Q). Energi bebas ini akan digunakan untuk mendorong sintesis ATP, yang dikatalisis oleh komponen F1 dari kompleks ATP sinstase[8]. Penggandengan dengan fosforilasi oksidatif sangatlah penting untuk produksi ATP. Namun, dalam kasus spesifik, memisahkan kedua proses ini menjadi dua proses yang berbeda mungkin dapat bermanfaat secara biologis. Salah satu protein yang disebut thermogenin menyediakan saluran alternatif proton untuk kembali ke matriks mitokondira.
Referensi
- ^ Gerasimovskaya, Evgenia; Kaczmarek, Elzbieta (2010-04-26). Extracellular ATP and adenosine as regulators of endothelial cell function: Implications for health and disease (dalam bahasa Inggris). Springer Science & Business Media. hlm. 139. ISBN 978-90-481-3435-9.
- ^ Anraku, Yasuhiro (1988-06-01). "Bacterial electron transport chains". Annual Review of Biochemistry. 57 (1): 101–132. doi:10.1146/annurev.bi.57.070188.000533. ISSN 0066-4154.
- ^ Kracke, Frauke; Vassilev, Igor; Krömer, Jens O. (2015). "Microbial electron transport and energy conservation – the foundation for optimizing bioelectrochemical systems". Frontiers in Microbiology (dalam bahasa English). 6. doi:10.3389/fmicb.2015.00575. ISSN 1664-302X. PMC 4463002
 . PMID 26124754.
. PMID 26124754.
- ^ Waldenström, Jan G. (1975). "Biochemistry. By Lubert Stryer". Acta Medica Scandinavica (dalam bahasa Inggris). 198 (1-6): 436–436. doi:10.1111/j.0954-6820.1975.tb19571.x. ISSN 0954-6820.
- ^ Zorova, Ljubava D.; Popkov, Vasily A.; Plotnikov, Egor Y.; Silachev, Denis N.; Pevzner, Irina B.; Jankauskas, Stanislovas S.; Babenko, Valentina A.; Zorov, Savva D.; Balakireva, Anastasia V. (2018-07-01). "Mitochondrial membrane potential". Analytical Biochemistry. Mitochondrial Biochemistry and Bioenergenetics (dalam bahasa Inggris). 552: 50–59. doi:10.1016/j.ab.2017.07.009. ISSN 0003-2697. PMC 5792320
 . PMID 28711444.
. PMID 28711444.
- ^ Walsh, Edward J. (1997-02). "Biochemistry (Garrett, Reginald H.; Grisham, Charles M.)". Journal of Chemical Education. 74 (2): 189. doi:10.1021/ed074p189.2. ISSN 0021-9584.
- ^ Fillingame, Robert H.; Angevine, Christine M.; Dmitriev, Oleg Y. (2003). "Mechanics of coupling proton movements to c-ring rotation in ATP synthase". FEBS Letters (dalam bahasa Inggris). 555 (1): 29–34. doi:10.1016/S0014-5793(03)01101-3. ISSN 1873-3468.
- ^ Berg, Jeremy M.; Tymoczko, John L.; Stryer, Lubert (2002). "A Proton Gradient Powers the Synthesis of ATP". Biochemistry. 5th edition (dalam bahasa Inggris): 356.
