Pengantar tentang virus: Perbedaan antara revisi
| Baris 56: | Baris 56: | ||
* '''Perakitan''' yaitu ketika protein-protein dan DNA atau RNA yang terbentuk di tahap sebelumnya menyusun diri membentuk ratusan partikel-partikel virus baru.<ref>Shors p. 137</ref> |
* '''Perakitan''' yaitu ketika protein-protein dan DNA atau RNA yang terbentuk di tahap sebelumnya menyusun diri membentuk ratusan partikel-partikel virus baru.<ref>Shors p. 137</ref> |
||
* '''Pelepasan''', yaitu ketika virus-virus baru keluar dari sel inangnya. Hal ini dicapai sebagian besar virus dengan cara memcahkan sel inang dalam proses yang disebut [[lisis]] (sehingga tahap ini juga disebut tahap '''lisis'''). Virus lain seperti HIV keluar dengan cara yang lebih halus yang disebut "pertunasan" (''budding'') yang tidak menghancurkan sel inang.<ref>Shors p. 141</ref> |
* '''Pelepasan''', yaitu ketika virus-virus baru keluar dari sel inangnya. Hal ini dicapai sebagian besar virus dengan cara memcahkan sel inang dalam proses yang disebut [[lisis]] (sehingga tahap ini juga disebut tahap '''lisis'''). Virus lain seperti HIV keluar dengan cara yang lebih halus yang disebut "pertunasan" (''budding'') yang tidak menghancurkan sel inang.<ref>Shors p. 141</ref> |
||
== Efek terhadap sel inang == |
|||
Virus mempunyai banyak efek terhadap struktur dan biokimia sel inang.<ref>Collier pp. 115–46</ref> Efek-efek ini disebut [[efek sitopatik]].<ref>Collier p. 115</ref> Sebagian besar infeksi virus berakhir dengan kematian sel inang. Sel inang mati dengan berbagai cara, di antaranya dengan pecah (mengalami lisis), perubahan membran sel, dan [[apoptosis]] (bunuh diri atau kematian sel terprogram.<ref name="pmid28846635">{{cite journal |vauthors=Okamoto T, Suzuki T, Kusakabe S, Tokunaga M, Hirano J, Miyata Y, Matsuura Y |title=Regulation of Apoptosis during Flavivirus Infection |journal=Viruses |volume=9 |issue=9 |pages= 243|year= 2017 |pmid=28846635 |pmc=5618009 |doi=10.3390/v9090243}}</ref> Sering kali sel mati karena aktivitas normalnya berhanti akibat protein-protein yang dihasilkan virus, termasuk protein yang bukan bagian dari partikel virus itu sendiri.<ref name="pmid18637511">{{cite book | vauthors = Alwine JC | title = Modulation of host cell stress responses by human cytomegalovirus | journal = Curr. Top. Microbiol. Immunol. | volume = 325 | issue = | pages = 263–79 | date = 2008 | pmid = 18637511 | doi = 10.1007/978-3-540-77349-8_15 | series = Current Topics in Microbiology and Immunology | isbn = 978-3-540-77348-1 }}</ref> |
|||
Sebagian virus tidak menyebabkan perubahan tampak kepada sel inang. Virus yang [[latensi virus|laten]] (tidak aktif) tidak banyak menunjukkan tanda infeksi dan sering berfungsi normal.<ref name="pmid18164651">{{cite journal | vauthors = Sinclair J | title = Human cytomegalovirus: Latency and reactivation in the myeloid lineage | journal = J. Clin. Virol. | volume = 41 | issue = 3 | pages = 180–85 | date = March 2008 | pmid = 18164651 | doi = 10.1016/j.jcv.2007.11.014 }}</ref> Hal ini menyebabkan infeksi yang tahan lama dan virus tersebut dapat tersembunyi selama bertahun-tahun. [[Virus herpes]] sering mengalami hal ini.<ref name="pmid6326635">{{cite journal | vauthors = Jordan MC, Jordan GW, Stevens JG, Miller G | title = Latent herpesviruses of humans | journal = Ann. Intern. Med. | volume = 100 | issue = 6 | pages = 866–80 | date = June 1984 | pmid = 6326635 | doi = 10.7326/0003-4819-100-6-866 }}</ref><ref name="pmid12076064">{{cite journal | vauthors = Sissons JG, Bain M, Wills MR | title = Latency and reactivation of human cytomegalovirus | journal = J. Infect. | volume = 44 | issue = 2 | pages = 73–77 | date = February 2002 | pmid = 12076064 | doi = 10.1053/jinf.2001.0948 | url = http://pdfs.semanticscholar.org/3c8d/108edcd6f47eed7dd3d2c15ba9ad72d6894d.pdf }}</ref> |
|||
Sebagian virus, seperti [[papilomavirus]], dapat menyebabkan sel memperbanyak diri tak terkendali dan menjadi penyebab [[kanker]],<ref name="pmid28798073">{{cite journal |vauthors=Graham SV |title=The human papillomavirus replication cycle, and its links to cancer progression: a comprehensive review |journal=Clinical Science |volume=131 |issue=17 |pages=2201–21 |year= 2017 |pmid=28798073 |doi=10.1042/CS20160786 }}</ref> sedangkan sebagian virus lainnya, seperti [[virus Epstein-Barr]], membuat sel memperbanyak tanpa menjadi [[maligna|ganas]].<ref name="pmid18035323">{{cite journal | vauthors = Barozzi P, Potenza L, Riva G, Vallerini D, Quadrelli C, Bosco R, Forghieri F, Torelli G, Luppi M | title = B cells and herpesviruses: a model of lymphoproliferation | journal = Autoimmun Rev | volume = 7 | issue = 2 | pages = 132–36 | date = December 2007 | pmid = 18035323 | doi = 10.1016/j.autrev.2007.02.018 }}</ref> Saat DNA sel terlalu rusak akibat serangan virus sehingga tidak dapat diperbaiki lagi, apoptosis sering terjadi. Salah satu akibatnya adalah penghancuran DNA oleh sel itu sendiri. Beberapa virus (misalnya, virus HIV) memiliki mekanisme untuk membatasi apoptosis sehingga sel inang tidak mati sebelum virus berhasil memperbanyak diri. <ref name="pmid10547702">{{cite journal | vauthors = Roulston A, Marcellus RC, Branton PE | title = Viruses and apoptosis | journal = Annu. Rev. Microbiol. | volume = 53 | issue = | pages = 577–628 | date = 1999 | pmid = 10547702 | doi = 10.1146/annurev.micro.53.1.577 }}</ref> |
|||
== Asal == |
== Asal == |
||
Revisi per 29 Maret 2020 00.40
Virus adalah agen infeksi berukuran kecil yang bereproduksi di dalam sel inang yang hidup. Ketika terinfeksi, sel inang dipaksa untuk menghasilkan ribuan salinan identik virus asli dengan cepat. Tidak seperti kebanyakan makhluk hidup, virus tidak memiliki sel; salinan virus yang baru terbentuk berkumpul dalam sel inang yang terinfeksi. Namun tidak seperti agen infeksi yang lebih sederhana seperti prion, virus memiliki materi genetik yang memungkinkan mereka untuk bermutasi dan berkembang. Hingga tahun 2018, lebih dari 4.800 spesies virus telah ditemukan.[1] Asal-usul virus belum jelas: beberapa di antaranya mungkin berevolusi dari plasmid (potongan DNA yang dapat bergerak di antara sel), sementara yang lain mungkin berevolusi dari bakteri.
Virus terdiri atas dua atau tiga bagian: materi genetik, kapsid (mantel protein), dan amplop. Semua virus memiliki materi genetik berupa DNA atau RNA, yaitu molekul panjang dengan banyak gen (pemberi instruksi pada sel). Semua virus juga ditutupi dengan mantel protein untuk melindungi gen. Sejumlah virus memiliki amplop berupa lipid yang menutupi lapisan protein, dan membuat virus tersebut rentan terhadap sabun. Virus menggunakan amplop ini—juga dengan reseptor spesifik—untuk memasuki sel inang baru.
Bentuk virus bervariasi, mulai dari heliks sederhana dan ikosahedral hingga struktur yang lebih kompleks. Ukuran virus berkisar dari 20 hingga 300 nanometer; diperlukan antara 33.000 hingga 500.000 virus yang disusun secara berdampingan untuk mencapai panjang 1 sentimeter (0,4 inci).
Virus menyebar melalui berbagai cara. Virus bersifat sangat spesifik dalam menentukan spesies inang atau jaringan yang mereka serang dan masing-masing spesies virus bergantung pada metode khusus untuk memperbanyak diri. Virus tumbuhan sering kali menyebar dari satu tumbuhan ke tumbuhan lain melalui serangga dan organisme lain, yang dikenal sebagai vektor. Beberapa virus manusia dan hewan disebarkan melalui paparan cairan tubuh yang terinfeksi. Virus influenza, misalnya, menyebar melalui udara melalui percikan saluran pernapasan ketika seseorang batuk atau bersin. Virus seperti norovirus ditularkan melalui transmisi fekal–oral, yang melibatkan tangan, makanan, dan air yang terkontaminasi. Rotavirus sering disebarkan melalui kontak langsung dengan anak-anak yang terinfeksi. Virus imunodefisiensi manusia, HIV, ditularkan oleh cairan tubuh yang ditransfer saat berhubungan seks. Virus lainnya, seperti virus dengue, disebarkan oleh serangga pengisap darah.
Virus, terutama yang memiliki RNA, dapat bermutasi dengan cepat dan memunculkan tipe baru yang tidak dapat diatasi dengan cepat oleh sistem imun inang mereka. Virus influenza, misalnya, sering kali bermutasi sehingga diperlukan vaksin baru setiap tahun. Perubahan besar dapat menyebabkan pandemi seperti pada tahun 2009 ketika flu menyebar ke sebagian besar negara. Mutasi ini sering terjadi ketika virus telah menginfeksi hewan lain seperti kelelawar dalam kasus koronavirus, serta babi dan burung dalam kasus influenza, sebelum mereka menyebar ke manusia.
Infeksi virus dapat mengakibatkan penyakit pada manusia, hewan, dan tumbuhan. Virus yang memyerang manusia dan hewan biasanya dihilangkan oleh sistem imun, yang memberikan kekebalan seumur hidup kepada inang virus tersebut. Pemberian antibiotika tidak efektif terhadap virus, tetapi obat antivirus dapat mengobati infeksi yang mengancam jiwa. Vaksin yang menghasilkan kekebalan seumur hidup dapat mencegah beberapa infeksi.
Penemuan

Pada tahun 1884, ahli mikrobiologi Prancis Charles Chamberland menemukan saringan Chamberland (atau saringan Chamberland—Pasteur), yang memiliki pori-pori yang lebih kecil dari bakteri. Dengan demikian, ia bisa melewatkan larutan yang mengandung bakteri melalui saringan tersebut sehingga larutan benar-benar bebas dari bakteri. Pada awal 1890-an, ahli biologi Rusia Dmitri Ivanovsky menggunakan metode ini untuk mempelajari suatu zat yang kemudian dikenal sebagai virus mosaik tembakau. Eksperimennya menunjukkan bahwa ekstrak dari daun tanaman tembakau terinfeksi yang telah dihancurkan tetap menular setelah penyaringan.[2]
Pada saat yang sama, beberapa ilmuwan lain menunjukkan bahwa, meskipun agen ini (yang kemudian disebut virus) berbeda dengan bakteri dan berukuran sekitar seratus kali lebih kecil, mereka masih dapat menimbulkan penyakit. Pada tahun 1899, ahli mikrobiologi Belanda Martinus Beijerinck mengamati bahwa agen tersebut berkembang biak hanya dalam sel yang membelah. Ia menyebutnya "cairan hidup menular" (bahasa Latin: contagium vivum fluidum)—atau "kuman hidup terlarut" karena ia tidak dapat menemukan partikel seperti kuman.[3] Pada awal abad ke-20, ahli bakteriologi Inggris Frederick Twort menemukan virus yang menginfeksi bakteri,[4] dan ahli mikrobiologi Prancis-Kanada Félix d'Herelle menggambarkan virus yang, ketika ditambahkan ke bakteri yang tumbuh pada agar, akan mengarah pada pembentukan area kematian bakteri. Penghitungan area kematian ini memungkinkan Félix untuk mengalkulasi jumlah virus dalam suspensi tersebut.[5]
Penemuan mikroskop elektron pada tahun 1931 memunculkan gambar virus untuk pertama kalinya.[6] Pada tahun 1935, ahli biokimia dan virologi Amerika Serikat Wendell Meredith Stanley memeriksa virus mosaik tembakau dan menemukan bahwa virus tersebut sebagian besar terbuat dari protein.[7] Tidak lama kemudian, virus ini dipisahkan menjadi bagian protein dan RNA.[8] Masalah bagi para penelti virus awal adalah bahwa mereka tidak tahu cara mengembangkan virus tanpa menggunakan hewan hidup. Sebuah terobosan terjadi pada tahun 1931, ketika ahli patologi Amerika Serikat Ernest William Goodpasture dan Alice Miles Woodruff menumbuhkan virus influenza dan beberapa virus lain pada telur ayam yang telah dibuahi.[9] Beberapa virus tidak dapat tumbuh dalam telur ayam, tetapi masalah ini diselesaikan pada tahun 1949 ketika John Franklin Enders, Thomas Huckle Weller, dan Frederick Chapman Robbins menumbuhkan virus polio dalam biakan sel hewan hidup.[10] Hingga tahun 2018, lebih dari 4.800 spesies virus telah ditemukan.[1]
Struktur

Partikel virus, disebut juga "virion", terdiri dari materi genetik yaitu DNA atau RNA yang dikelilingi lapisan protein pelindung yang disebut kapsid.[11] Kapsid terbentuk dari susunan molekul-molekul protein kecil identik yang disebut kapsomer. Kapsomer-kapsomer ini dapat tersusun dalam struktur ikosahedron (bangun ruang bersisi 20), heliks/spiral, atau bentuk-bentuk lain yang lebih kompleks. Di dalam kapsid terdapat selubung nukleokapsid, yang juga terdiri dari protein. Sebagian virus dikelilingi bagian luar yang terdiri dari lipid (lemak) dan disebut selubung virus (amplop). Selubung luar ini menyebabkan virus tersebut dapat dihancurkan sabun atau alkohol.[12]
Ukuran
Virus termasuk dalam makhluk terkecil yang dapat menyebabkan infeksi dan tidak dapat dilihat menggunakan mikroskop cahaya akibat ukurannya. Kebanyakan virus hanya dapat dilihat menggunakan mikroskop elektron. Ukuran virus berkisar antara 20 hingga 300 nanometer—artinya garis sepanjang 1 sentimeter dapat diisi 33.000 hingga 500.000 virus yang berbaris lurus.[11] Bakteri umumnya memiliki diameter 1000 nanometer (1 mikrometer), dan sel makhluk hidup yang lebih besar biasanya berukuran puluhan mikrometer. Terdapat juga golongan virus yang berukuran relatif besar dibandingkan virus biasa, seperti megavirus dan pandoravirus. Virus-virus ini menginfeksi ameba, dan ditemukan pada 2003 dan 2013 dengan ukuran sekitar 1000 nanometer.[13][14] Virus-virus ini sekitar sepuluh kali lebih panjang dari virus influenza (sehingga volumnya 1000 kali lebih besar), sehingga disebut virus "raksasa" dan penemuannya mengejutkan para ilmuwan.[15]
Bahan genetis
Gen virus terbuat dari DNA (asam deoksiribonukleat) atau RNA (asam ribonukleat), tergantung jenis virus. Gen menyimpan informasi biologi dari suatu organisme dalam bentuk kode. Sebagian besar organisme menggunakan DNA sebagai bahan genetis, tetapi sejumlah virus menggunakan RNA (golongan ini disebut virus RNA). DNA atau RNA virus dapat berbentuk satu untaian saja atau berbentuk heliks ganda.[16]
Virus dapat berkembang biak dengan cepat karena jumlah gennya sangat kecil. Virus influenza memiliki hanya delapan gen, sedangkan rotavirus memiliki sebelas gen (sebagai perbandingan, manusia memiliki 20.000 hingga 25.000). Gen-gen ini mengandung kode untuk menghasilkan protein, baik protein struktural yang membentuk tubuh virus itu sendiri, maupun protein nonstruktural yang hanya ditemukan dalam sel yang diinfeksi virus.
Seperti halnya sebuah sel, banyak virus menghasilkan protein enzim yang disebut DNA polimerase dan RNA polimerase, yang membuat salinan dari DNA atau RNA-nya. Enzim polimerase sebuah virus sering lebih efisien dalam menyalin DNA atau RNA dibandingkan enzim serupa dalam sel inangnya,[17] tetapi RNA polimerase dari virus lebih rentan mengalami kesalahan penyalinan. Hal ini menyebabkan virus RNA mudah bermutasi dan menghasilkan jenis-jenis (atau galur) baru.[18]
Beberapa virus RNA memiliki gen yang tidak menyatu dalam satu molekul RNA tunggal. Misalnya, virus influenza memiliki delapan gen terpisah yang masih-masing berupa molekul RNA tersendiri. Saat beberapa galur dari virus influenza menginfeksi sel yang sama, gen-gen ini dapat bercampur dan membentuk galur baru dalam sebuah proses yang disebut reassortment (pemilahan ulang).[19]
Sintesis protein

Protein adalah molekul yang mutlak diperlukan untuk kelangsungan hidup. Sebuah sel biasa membuat protein dengan merangkai asam-asam amino sesuai informasi yang ada dalam DNA. Sintesis (pembuatan) protein membutuhkan berbagai proses yang tidak dimiliki oleh virus.[20] Karena itu, virus memaksa sel inangnya untuk membuat protein-protein yang tidak dibutuhkan sel inang tetapi diperlukan oleh virus untuk memperbanyak diri.[21]
Dalam sebuah sel, sintesis protein terdiri dari dua tahap utama: transkripsi (penyalinan) dan translasi (penerjemahan).[22] Dalam transkripsi, informasi yang dikandung DNA (disebut kode genetik) digunakan untuk membuat salinan berupa RNA yang disebut RNA duta (disebut mRNA dari messenger-RNA). Molekul mRNA ini berpindah menuju ribosom tempat protein dibuat menggunakan informasi yang ada dalam mRNA. Tahap ini disebut translasi atau penerjemahan karena informasi mRNA yang formatnya adalah susunan asam nukleat diubah menjadi protein yang merupakan susunan asam amino, seolah dari suatu bahasa ke bahasa lain.[22]
Virus "membajak" proses dalam sel ini dengan berbagai cara. Sebagian virus RNA bekerja dengan menggunakan RNAnya secara langsung sebagai mRNA sel. Golongan virus seperti ini disebut virus RNA makna-positif (positive-sense).[23] Sebaliknya, dalam golongan virus RNA lainnya RNA virus harus diubah menjadi komplemennya terlebih dahulu agar berfungsi sebagai mRNA, sehingga harus dilakukan penyalinan komplemen menggunakan enzim milik sel inang atau milik virus itu sendiri. Golongan virus ini disebut virus RNA makna-negatif (negative-sense). Sebagian virus lainnya memiliki DNA alih-alih RNA; virus-virus ini membuat mRNA seprti halnya sebuah sel. Ada golongan virus lain, yaitu retrovirus, yang menggunakan mekanisme berbeda: golongan virus ini memiliki RNA, tetapi salinan berupa DNA dari RNA virus dibuat dalam sel inang dengan bantuan enzim transkriptase balik. DNA ini kemudian disisipkan ke dalam DNA sel inang, sehingga akan disalin menjadi mRNA dan dibuat proteinnya menggunakan proses biasa dalam sel.[24]
Siklus hidup
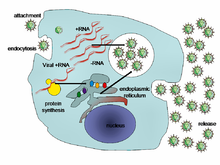
Saat sebuah virus menginfeksi sel, virus tersebut mengendalikan sel inangnya untuk memperbanyak virus itu, dengan membuat sel inang menyalin DNA dan RNA virus dan membuat protein yang kemudian bergabung untuk membentuk partikel virus baru.[25]
Pada dasarnya, ada enam tahap siklus hidup virus dalam sel makhluk hidup:[26]
- Adsorpsi, yaitu mengikatnya virus ke molekul tertentu pada permukaan sel. Setiap virus hanya bisa terikat pada molekul yang sesuai, alhasil virus hanya bisa menginfeksi jenis sel yang sangat terbatas. Fenomena ini disebut tropisme, dan kadang virus juga memiliki tropisme spesies yaitu hanya menginfeksi sel dari spesies atau golongan spesies tertentu. Misalnya, virus HIV hanya bisa menginfeksi sel T manusia, karena protein di permukaan virus ini, gp120, hanya bisa bereaksi dengan molekul CD4 dengan adanya koreseptor tertentu di permukaan sel T.[27]
- Penetrasi setelah terikat dalam tahap adsorpsi, virus memasuki sel inang melalui endositosis atau fusi dengan sel tersebut.[28]
- Pembukaan atau pembongkaran, yaitu saat kapsid yang melindungi virus terbuka dan dihancurkan oleh enzim virus atau enzim sel inang, sehingga bahan genetis yang dimiliki virus dapat memasuki sel.[29]
- Replikasi yaitu ketika sel inang menyintesis protein-protein yang dibutuhkan virus dan memperbanyak DNA atau RNA virus. Hal ini terjadi karena virus telah mengendalikan kemampuan sel untuk membuat protein dan memperbanyak bahan genetis.[30]
- Perakitan yaitu ketika protein-protein dan DNA atau RNA yang terbentuk di tahap sebelumnya menyusun diri membentuk ratusan partikel-partikel virus baru.[31]
- Pelepasan, yaitu ketika virus-virus baru keluar dari sel inangnya. Hal ini dicapai sebagian besar virus dengan cara memcahkan sel inang dalam proses yang disebut lisis (sehingga tahap ini juga disebut tahap lisis). Virus lain seperti HIV keluar dengan cara yang lebih halus yang disebut "pertunasan" (budding) yang tidak menghancurkan sel inang.[32]
Efek terhadap sel inang
Virus mempunyai banyak efek terhadap struktur dan biokimia sel inang.[33] Efek-efek ini disebut efek sitopatik.[34] Sebagian besar infeksi virus berakhir dengan kematian sel inang. Sel inang mati dengan berbagai cara, di antaranya dengan pecah (mengalami lisis), perubahan membran sel, dan apoptosis (bunuh diri atau kematian sel terprogram.[35] Sering kali sel mati karena aktivitas normalnya berhanti akibat protein-protein yang dihasilkan virus, termasuk protein yang bukan bagian dari partikel virus itu sendiri.[36]
Sebagian virus tidak menyebabkan perubahan tampak kepada sel inang. Virus yang laten (tidak aktif) tidak banyak menunjukkan tanda infeksi dan sering berfungsi normal.[37] Hal ini menyebabkan infeksi yang tahan lama dan virus tersebut dapat tersembunyi selama bertahun-tahun. Virus herpes sering mengalami hal ini.[38][39]
Sebagian virus, seperti papilomavirus, dapat menyebabkan sel memperbanyak diri tak terkendali dan menjadi penyebab kanker,[40] sedangkan sebagian virus lainnya, seperti virus Epstein-Barr, membuat sel memperbanyak tanpa menjadi ganas.[41] Saat DNA sel terlalu rusak akibat serangan virus sehingga tidak dapat diperbaiki lagi, apoptosis sering terjadi. Salah satu akibatnya adalah penghancuran DNA oleh sel itu sendiri. Beberapa virus (misalnya, virus HIV) memiliki mekanisme untuk membatasi apoptosis sehingga sel inang tidak mati sebelum virus berhasil memperbanyak diri. [42]
Asal
Virus selalu berdampingan dengan organisme. Mereka mungkin telah ada sejak sel hidup pertama kali berevolusi. Asal mereka belum jelas karena virus tidak membentuk fosil sehingga teknik molekuler merupakan cara terbaik untuk membuat hipotesis tentang asal mereka. Teknik ini bergantung pada ketersediaan DNA atau RNA virus yang terdahulu. Akan tetapi, sebagian besar virus yang diawetkan dan disimpan di laboratorium berusia kurang dari 90 tahun.[43][44] Metode molekuler hanya berhasil melacak nenek moyang virus yang berevolusi pada abad ke-20.[45]
Peranan dalam ekologi
Virus merupakan entitas biologis yang paling melimpah di lingkungan perairan;[46] satu sendok teh air laut mengandung sekitar sepuluh juta virus,[47] dan mereka berperan penting dalam pengaturan ekosistem air asin dan air tawar.[48] Sebagian besar virus dalam perairan tersebut merupakan bakteriofag,[49] yang tidak berbahaya bagi tumbuhan dan hewan. Mereka menginfeksi dan menghancurkan bakteri pada komunitas mikroba akuatik dan hal ini merupakan mekanisme daur ulang karbon yang paling penting dalam ekosistem laut. Molekul organik yang dilepaskan dari sel bakteri oleh virus merangsang pertumbuhan bakteri dan alga segar.[50]
Mikroorganisme menyusun lebih dari 90% biomassa di laut. Virus diperkirakan membunuh sekitar 20% dari biomassa ini setiap hari. Terdapat 15 kali lebih banyak virus di lautan dibandingkan bakteri dan arkea. Virus-virus ini terutama bertanggung jawab atas pengurangan populasi alga dengan cepat sehingga mencegah ledakan populasi alga,[51] yang sering kali membunuh kehidupan laut lainnya.[52] Jumlah virus di lautan semakin berkurang di lepas pantai dan lebih dalam ke dalam air karena jumlah organisme inang lebih sedikit.[53]
Peran virus di lautan sangat besar; dengan meningkatkan jumlah respirasi di lautan, virus secara tidak langsung berperan untuk mengurangi jumlah karbon dioksida di atmosfer sekitar 3 gigaton karbon per tahun.[53]
Mamalia laut juga rentan terhadap infeksi virus. Pada tahun 1988 dan 2002, ribuan anjing laut di Eropa mati akibat infeksi Phocine morbillivirus.[54] Banyak virus lain, termasuk calicivirus, herpesvirus, adenovirus, dan parvovirus, beredar pada populasi mamalia laut.[53]
Rujukan
Catatan kaki
- ^ a b King AM, Lefkowitz EJ, Mushegian AR, Adams MJ, Dutilh BE, Gorbalenya AE, Harrach B, Harrison RL, Junglen S, Knowles NJ, Kropinski AM, Krupovic M, Kuhn JH, Nibert ML, Rubino L, Sabanadzovic S, Sanfaçon H, Siddell SG, Simmonds P, Varsani A, Zerbini FM, Davison AJ (September 2018). "Changes to taxonomy and the International Code of Virus Classification and Nomenclature ratified by the International Committee Taxonomy of Viruses (2018)" (PDF). Archives of Virology. 163 (9): 2601–31. doi:10.1007/s00705-018-3847-1. PMID 29754305.
- ^ Shors, hlm. 6.
- ^ Collier, hlm. 3.
- ^ Shors, hlm. 827.
- ^ D'herelle F (2007). "On an invisible microbe antagonistic toward dysenteric bacilli: brief note by Mr. F. D'Herelle, presented by Mr. Roux. 1917". Research in Microbiology. 158 (7): 553–54. doi:10.1016/j.resmic.2007.07.005. PMID 17855060.
- ^ From Nobel Lectures, Physics 1981–1990, (1993) Editor-in-Charge Tore Frängsmyr, Editor Gösta Ekspång, World Scientific Publishing Co., Singapore
- ^ Stanley WM, Loring HS (1936). "The isolation of crystalline tobacco mosaic virus protein from diseased tomato plants". Science. 83 (2143): 85. Bibcode:1936Sci....83...85S. doi:10.1126/science.83.2143.85. PMID 17756690.
- ^ Stanley WM, Lauffer MA (1939). "Disintegration of tobacco mosaic virus in urea solutions". Science. 89 (2311): 345–47. Bibcode:1939Sci....89..345S. doi:10.1126/science.89.2311.345. PMID 17788438.
- ^ Goodpasture EW, Woodruff AM, Buddingh GJ (October 1931). "The Cultivation Of Vaccine and other Viruses In The Chorioallantoic Membrane of Chick Embryos". Science. 74 (1919): 371–72. Bibcode:1931Sci....74..371G. doi:10.1126/science.74.1919.371. PMID 17810781.
- ^ Rosen FS (October 2004). "Isolation of poliovirus – John Enders and the Nobel Prize". N. Engl. J. Med. 351 (15): 1481–83. doi:10.1056/NEJMp048202. PMID 15470207.
- ^ a b Collier pp. 33–55
- ^ Rotter ML (August 2001). "Arguments for alcoholic hand disinfection". The Journal of Hospital Infection. 48 Suppl A: S4–8. doi:10.1016/s0195-6701(01)90004-0. PMID 11759024.
- ^ Abergel C, Legendre M, Claverie JM (November 2015). "The rapidly expanding universe of giant viruses: Mimivirus, Pandoravirus, Pithovirus and Mollivirus". FEMS Microbiol. Rev. 39 (6): 779–96. doi:10.1093/femsre/fuv037. PMID 26391910.
- ^ Philippe N, Legendre M, Doutre G, Couté Y, Poirot O, Lescot M, Arslan D, Seltzer V, Bertaux L, Bruley C, Garin J, Claverie JM, Abergel C (July 2013). "Pandoraviruses: amoeba viruses with genomes up to 2.5 Mb reaching that of parasitic eukaryotes" (PDF). Science. 341 (6143): 281–86. Bibcode:2013Sci...341..281P. doi:10.1126/science.1239181. PMID 23869018.
- ^ Zimmer C (18 July 2013). "Changing View on Viruses: Not So Small After All". New York Times. Diakses tanggal 20 December 2014.
- ^ Shors p. 81
- ^ Shors pp. 129–31
- ^ Shors p. 652
- ^ Shors p. 654
- ^ Shors p. 113
- ^ Shors p. 104
- ^ a b de Klerk E, 't Hoen PA (March 2015). "Alternative mRNA transcription, processing, and translation: insights from RNA sequencing". Trends in Genetics : TIG. 31 (3): 128–39. doi:10.1016/j.tig.2015.01.001. PMID 25648499.
- ^ Collier pp. 75–82
- ^ Shors p. 698
- ^ Shors pp. 6–13
- ^ Shors p. 129
- ^ Shors pp. 124–125
- ^ Shors p. 125
- ^ Shors p. 127
- ^ Shors p. 129
- ^ Shors p. 137
- ^ Shors p. 141
- ^ Collier pp. 115–46
- ^ Collier p. 115
- ^ Okamoto T, Suzuki T, Kusakabe S, Tokunaga M, Hirano J, Miyata Y, Matsuura Y (2017). "Regulation of Apoptosis during Flavivirus Infection". Viruses. 9 (9): 243. doi:10.3390/v9090243. PMC 5618009
 . PMID 28846635.
. PMID 28846635.
- ^ Alwine JC (2008). Modulation of host cell stress responses by human cytomegalovirus. Curr. Top. Microbiol. Immunol. Current Topics in Microbiology and Immunology. 325. hlm. 263–79. doi:10.1007/978-3-540-77349-8_15. ISBN 978-3-540-77348-1. PMID 18637511.
- ^ Sinclair J (March 2008). "Human cytomegalovirus: Latency and reactivation in the myeloid lineage". J. Clin. Virol. 41 (3): 180–85. doi:10.1016/j.jcv.2007.11.014. PMID 18164651.
- ^ Jordan MC, Jordan GW, Stevens JG, Miller G (June 1984). "Latent herpesviruses of humans". Ann. Intern. Med. 100 (6): 866–80. doi:10.7326/0003-4819-100-6-866. PMID 6326635.
- ^ Sissons JG, Bain M, Wills MR (February 2002). "Latency and reactivation of human cytomegalovirus" (PDF). J. Infect. 44 (2): 73–77. doi:10.1053/jinf.2001.0948. PMID 12076064.
- ^ Graham SV (2017). "The human papillomavirus replication cycle, and its links to cancer progression: a comprehensive review". Clinical Science. 131 (17): 2201–21. doi:10.1042/CS20160786. PMID 28798073.
- ^ Barozzi P, Potenza L, Riva G, Vallerini D, Quadrelli C, Bosco R, Forghieri F, Torelli G, Luppi M (December 2007). "B cells and herpesviruses: a model of lymphoproliferation". Autoimmun Rev. 7 (2): 132–36. doi:10.1016/j.autrev.2007.02.018. PMID 18035323.
- ^ Roulston A, Marcellus RC, Branton PE (1999). "Viruses and apoptosis". Annu. Rev. Microbiol. 53: 577–628. doi:10.1146/annurev.micro.53.1.577. PMID 10547702.
- ^ Shors. p. 16
- ^ Collier pp. 18–19
- ^ Liu Y, Nickle DC, Shriner D, Jensen MA, Learn GH, Mittler JE, Mullins JI (November 2004). "Molecular clock-like evolution of human immunodeficiency virus type 1". Virology. 329 (1): 101–08. doi:10.1016/j.virol.2004.08.014. PMID 15476878.
- ^ Koonin EV, Senkevich TG, Dolja VV (September 2006). "The ancient Virus World and evolution of cells". Biol. Direct. 1: 29. doi:10.1186/1745-6150-1-29. PMC 1594570
 . PMID 16984643.
. PMID 16984643.
- ^ Dávila-Ramos S, Castelán-Sánchez HG, Martínez-Ávila L, Sánchez-Carbente MD, Peralta R, Hernández-Mendoza A, Dobson AD, Gonzalez RA, Pastor N, Batista-García RA (2019). "A Review on Viral Metagenomics in Extreme Environments". Frontiers in Microbiology. 10: 2403. doi:10.3389/fmicb.2019.02403. PMC 6842933
 . PMID 31749771.
. PMID 31749771.
- ^ Shors p. 5
- ^ Breitbart M, Bonnain C, Malki K, Sawaya NA (July 2018). "Phage puppet masters of the marine microbial realm". Nature Microbiology. 3 (7): 754–66. doi:10.1038/s41564-018-0166-y. PMID 29867096.
- ^ Shors pp. 25–26
- ^ Suttle CA (September 2005). "Viruses in the sea". Nature. 437 (7057): 356–61. Bibcode:2005Natur.437..356S. doi:10.1038/nature04160. PMID 16163346.
- ^ "Harmful Algal Blooms: Red Tide: Home | CDC HSB". www.cdc.gov. Diakses tanggal 23 August 2009.
- ^ a b c Suttle CA (October 2007). "Marine viruses – major players in the global ecosystem". Nat. Rev. Microbiol. 5 (10): 801–12. doi:10.1038/nrmicro1750. PMID 17853907.
- ^ Hall A, Jepson P, Goodman S, Harkonen T (2006). "Phocine distemper virus in the North and European Seas – Data and models, nature and nurture". Biological Conservation. 131 (2): 221–29. doi:10.1016/j.biocon.2006.04.008.
Daftar pustaka
- Collier, Leslie; Balows, Albert; Sussman Max, eds. (1998). Topley and Wilson's Microbiology and Microbial Infections. Volume 1, Virology (9th ed.). Arnold. ISBN 0-340-66316-2
- Shors, Teri (2017). Understanding Viruses. Jones and Bartlett Publishers. ISBN 978-1284025927

