Interaksi agostik
Interaksi agostik merupakan istilah dalam kimia organologam yang digunakan untuk merujuk pada interaksi antara logam transisi dengan ikatan karbon-hidrogen, dengan dua elektron yang terlibat pada ikatan C-H memasuki orbital d logam transisi yang kosong, menghasilkan ikatan tiga-pusat dua-elektron.[1] Banyak transformasi katalitik seperti adisi oksidatif dan eliminasi reduktif yang diajukan berjalan melalui zat antara yang memiliki interaksi agostik. Interaksi agostik terpantau pada kimia organik yang melibatkan ligan alkil, alkilidena, dan polienil.
Sejarah[sunting | sunting sumber]
Istilah agostik diciptakan oleh Maurice Brookhart dan Malcolm Green untuk mendeskripsikan interaksi antara logam transisi dengan ikatan karbon-hidrogen. Sering kali, interaksi agostik seperti ini melibatkan gugus alkil ataupun aril yang berada dekat dengan pusat logam melalui ikatan sigma tambahan.[2][3]
Interaksi pendek antara substituen hidrokarbon dengan kompleks logam yang secara koordinatif tak jenuh telah tercatat sejak tahun 1960-an. Sebagai contohnya, tris(trifenilfosfina) rutenium diklorida memiliki interaksi yang terpantau antara pusat Ru(II) dengan atom hidrogen pada posisi orto salah satu dari sembilan cincin fenil.[4]
Karakteristik ikatan agostik[sunting | sunting sumber]
Interaksi agostik dapat diperlihatkan dengan baik oleh kristalografi. Data difraksi neutron menunjukkan bahwa panjang ikat C-H dan M-H 5-20% lebih panjang daripada yang terdapat pada ikatan logam hidrida dan hidrokarbon biasanya. Panjang ikat antara logam dengan hidrogen umumnya adalah 1,8 - 2,3 Ǻ, dan sudut M-H-C berkisar antara 90 - 140°. Terdapat pula satu signal 1H NMR dari hidrogen aril atau alkana yang bergeser ke medan atas yang biasanya menandakan keberadaan ligan hidrida. Konstanta kopling 1JCH biasanya akan menurun menjadi 70–100 Hz dibandingkan dengan 125 Hz yang terpantau pada ikatan karbon hidrogen sp3 yang biasanya.
Kekuatan ikatan[sunting | sunting sumber]
Berdasarkan kajian eksperimental dan komputasional, stabilisasi yang dihasilkan dari interaksi agostik diperkirakan berkisar antara 10–15 kcal/mol. Oleh karena itu, interaksi agostik lebih kuat dari kebanyakan ikatan hidrogen. Ikatan agostik kadang-kadang berperan penting dalam katalisis dengan meningkatkan 'kekakuan' keadaan transisi. Sebagai contoh, pada katalisis Ziegler-Natta, pusat logam yang sangat elektrofilik memiliki interaksi agostik dengan rantai polimer yang memanjang. Peningkatan kekakuan ini memengaruhi stereoselektivitas proses polimerisasi.
Interaksi ikatan yang berkaitan[sunting | sunting sumber]
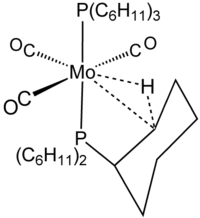
Istilah agostik biasanya hanya digunakan untuk merujuk pada interaksi tiga pusat dua elektron antara karbon, hidrogen, dan logam. Ikatan tiga-pusat dua-elektron secara jelas terlibat dalam kompleksasi H2, misalnya dalam in W(CO)3(PCy3)2H2, yang berhubungan dekat dengan kompleks agostik yang terdapat pada gambar di atas.[5] Silana sering berikatan dengan pusat logam melalui interaksi tiga pusat Si-H-M yang seperti interaksi agostik. Namun interaksi ini tidak diklasifikasikan sebagai agostik karena tidak melibatkan atom karbon.
Ikatan anagostik[sunting | sunting sumber]
Interaksi M---H-C tertentu tidak diklasifikasikan sebagai "agostik", tetapi diklasifikasikan sebagai "anagostik". Interaksi anagostik memiliki sifat-sifat yang lebih elektrostatik. Dalam hal strukturnya, jarak M---H dan sudut M-H-C berkisar antara 2,3-2,9 Ǻ dan 110-170° secara berturut-turut.[2][6]
Referensi[sunting | sunting sumber]
- ^ "Agostic Interaction". IUPAC Compendium of Chemical Terminology. 21 Jan 2008. http://www.iupac.org/goldbook/AT06984.pdf Diarsipkan 2007-06-10 di Wayback Machine.
- ^ a b Maurice Brookhart, Malcolm L. H. Green, Carbon-hydrogen-transition metal bonds. Journal of Organometallic Chemistry, 250(1), 395-408 (1983). DOI:10.1016/0022-328X(83)85065-7.
- ^ Maurice Brookhart, Malcolm L. H. Green, and Gerard Parkin "Agostic interactions in transition metal compounds" Proceeding of the U.S. National Academy of Sciences 2007, volume 104, 6908–6914.DOI:10.1073/pnas.0610747104
- ^ Sam J. La Placa and James A. Ibers "A Five-Coordinated d6 Complex: Structure of Dichlorotris(triphenylphosphine)ruthenium (II)" Inorganic Chemistry, 1965, volume 4, pp 778 - 783. DOI:10.1021/ic50028a002
- ^ Kubas, G. J., "Metal Dihydrogen and σ-Bond Complexes", Kluwer Academic/Plenum Publishers: New York, 2001
- ^ Braga D, Grepioni F, Tedesco E, Biradha K., Desiraju G. R. (1997). Organometallics 16, 1846-1856
Pranala luar[sunting | sunting sumber]
- IUPAC, Compendium of Chemical Terminology, edisi ke-2 ("Buku Emas") (1997). Versi koreksi daring: (2006–) "agostic".
- http://www.ilpi.com/organomet/agostic.html
