Magnesium sulfat: Perbedaan antara revisi
Tag: halaman dengan galat kutipan Suntingan visualeditor-wikitext |
Tag: Suntingan visualeditor-wikitext |
||
| Baris 118: | Baris 118: | ||
<ref name="fort2012">A. Dominic Fortes, Frank Browning, and Ian G. Wood (2012): "Cation substitution in synthetic meridianiite (MgSO<sub>4</sub>·11H<sub>2</sub>O) I: X-ray powder diffraction analysis of quenched polycrystalline aggregates". ''Physics and Chemistry of Minerals'', volume 39, issue, pages 419–441. {{doi|10.1007/s00269-012-0497-9}}</ref> |
<ref name="fort2012">A. Dominic Fortes, Frank Browning, and Ian G. Wood (2012): "Cation substitution in synthetic meridianiite (MgSO<sub>4</sub>·11H<sub>2</sub>O) I: X-ray powder diffraction analysis of quenched polycrystalline aggregates". ''Physics and Chemistry of Minerals'', volume 39, issue, pages 419–441. {{doi|10.1007/s00269-012-0497-9}}</ref> |
||
<ref name="pete2007">R. C. Peterson, W. Nelson, B. Madu, and H. F. Shurvell (2007): "Meridianiite: A new mineral species observed on Earth and predicted to exist on Mars". ''American Mineralogist'', volume 92, issue 10, pages 1756–1759. {{doi|10.2138/am.2007.2668}}</ref> |
<ref name="pete2007">R. C. Peterson, W. Nelson, B. Madu, and H. F. Shurvell (2007): "Meridianiite: A new mineral species observed on Earth and predicted to exist on Mars". ''American Mineralogist'', volume 92, issue 10, pages 1756–1759. {{doi|10.2138/am.2007.2668}}</ref> |
||
<ref name="pete2006">{{cite journal |title=Alpersite (Mg,Cu)SO<sub>4</sub>·7H<sub>2</sub>O, a new mineral of the melanterite group, and cuprian pentahydrite: Their occurrence within mine waste |first1=Ronald C. |last1=Peterson |first2=Jane M. |last2=Hammarstrom |first3=Robert R |last3=Seal, II |journal=American Mineralogist |date=Feb 2006 |volume=91 |pages=261–269 |doi=10.2138/am.2006.1911 |issue=2–3|s2cid=56431885 }}</ref> |
|||
</references> |
</references> |
||
Revisi per 19 Desember 2021 06.56
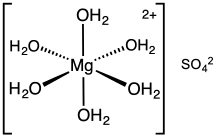 heksahidrat
| |
 Magnesium sulfat anhidrat
| |
 Epsomite (heptahidrat)
| |
| Nama | |
|---|---|
| Nama IUPAC
Magnesium sulfat
| |
| Nama lain
garam epsom (heptahidrat)
| |
| Penanda | |
| |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| MgSO4 | |
| Massa molar | 120.366 g/mol (anhidrat) 246.47 g/mol (heptahidrat) |
| Penampilan | padatan kristal putih |
| Bau | tak berbau |
| Densitas | 2.66 g/cm3 (anhidrat) 2.445 g/cm3 (monohidrat) 1.68 g/cm3 (heptahidrat) 1.512 g/cm3 (11-hidrat) |
| Titik lebur | anhidrat terdekomposisi pada 1124 °C monohidrat terdekomposisi pada 200 °C heptahidrat terdekomposisi pada 150 °C undekahidrat terdekomposisi pada 2 °C |
| anhidrat 26.9 g/100 mL (0 °C) 25.5 g/100 mL (20 °C) heptahidrat 71 g/100 mL (20 °C) | |
| Kelarutan | 1.16 g/100 mL (18 °C, eter) agak larut pada alkohol, gliserol tidak larut dalam aseton |
| Indeks bias (nD) | 1.523 (monohidrat) 1.433 (heptahidrat) |
| Struktur | |
| monoklinik (hidrat) | |
| Bahaya | |
| Senyawa terkait | |
Kation lainnya
|
Berilium sulfat Kalsium sulfat Stronsium sulfat Barium sulfat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Magnesium sulfat adalah senyawa kimia, suatu garam dengan rumus MgSO4, yang tersusun dari kation magnesium Mg2+ (20,19% b/b) dan anion sulfat SO2−4. Senyawa ini berbentuk kristal padat, yang larut dalam air tetapi tidak larut dalam etanol.
Magnesium sulfat biasanya dijumpai dalam bentuk terhidrasi MgSO4·nH2O, dengan nilai n yang beragam antara 1 dan 11. Bentuk terhidrasinya yang paling umum adalah magnesium sulfat heptahidrat MgSO4·7H2O, yang dikenal sebagai garam Epsom, yaitu bahan kimia rumah tangga multiguna, termasuk garam mandi.[1]
Penggunaan utama magnesium sulfat adalah pada bidang pertanian, untuk memperbaiki tanah yang kekurangan magnesium (suatu zat gizi tanaman esensial karena magnesium berperan penting dalam klorofil dan fotosintesis). Bentuk monohidratnya dipilih untuk penggunaan ini. Pada pertengahan tahun 1970an, produksi tahunannya mencapai 2,3 juta ton per tahun.[2] Bentuk anhidrat dan beberapa hidratnya terjadi di alam sebagai mineral, dan garamnya adalah komponen air yang penting dari beberapa mata air.
Hidrat
Magnesium sulfat dapat mengkristal sebagai hidratnya, antara lain:
- Anhidrat, MgSO4; tidak stabil di alam, terhidrasi membentuk epsomite.[3]
- Monohidrat, MgSO4·H2O; kieserite, monoklinik.[4]
- MgSO4·1.25H2O atau 8MgSO4·10H2O.[5]
- Dihidrat, MgSO4·2H2O; ortorombik.
- MgSO4·2.5H2O atau 2MgSO4·5H2O.[5]
- Trihidrat, MgSO4·3H2O.[5]
- Tetrahidrat, MgSO4·4H2O; starkeyite, monoklinik.[6]
- Pentahidrat, MgSO4·5H2O; pentahydrite, triklinik.[4]
- Heksahidrat, MgSO4·6H2O; hexahydrite, monoklinik.
- Heptahidrat, MgSO4·7H2O ("garam Epsom"); epsomite, ortorombik.[4]
- Eneahidrat, MgSO4·9H2O, monoklinik.[7]
- Dekahidrat, MgSO4·10H2O.[6]
- Undekahidrat, MgSO4·11H2O; meridianiite, triklinik.[6]
Hingga tahun 2017, keberadaan heksahidrat belum dikonfirmasi.[7]
Semua hidratnya akan membebaskan air kristalnya ketika dipanaskan. Di atas suhu 320 °C, hanya bentuk anhidratnya yang stabil. Ia terdekomposisi tanpa meleleh pada 1124 °C membentuk magnesium oksida (MgO) dan belerang trioksida (SO3).
Garam rangkap
Terdapat garam rangkap yang mengandung magnesium. Ada beberapa yang dikenal sebagai naterium magnesium sulfat dan kalium magnesium sulfat. Campuran tembaga-magnesium sulfat heptahidrat (Mg,Cu)SO4·7H2O baru-baru ini ditemukan terdapat pada tailing tambang dan mineral tersebut diberi nama alspersite.[8]
Lihat juga
Referensi
- ^ "Quick Cures/Quack Cures: Is Epsom Worth Its Salt?". The Wall Street Journal. 9 April 2012. Diarsipkan dari versi asli tanggal 12 April 2012. Diakses tanggal 15 June 2019.
- ^ Industrial Inorganic Chemistry, Karl Heinz Büchel, Hans-Heinrich Moretto, Dietmar Werner, John Wiley & Sons, 2d edition, 2000, ISBN 978-3-527-61333-5
- ^ "Unnamed (Mg Sulphate)".
- ^ a b c Odochian, Lucia (1995). "Study of the nature of the crystallization water in some magnesium hydrates by thermal methods". Journal of Thermal Analysis and Calorimetry. 45 (6): 1437–1448. doi:10.1007/BF02547437. Diarsipkan dari versi asli tanggal 26 August 2011. Diakses tanggal 7 August 2010.
- ^ a b c A. Dominic Fortes, Frank Browning, and Ian G. Wood (2012): "Cation substitution in synthetic meridianiite (MgSO4·11H2O) I: X-ray powder diffraction analysis of quenched polycrystalline aggregates". Physics and Chemistry of Minerals, volume 39, issue, pages 419–441. DOI:10.1007/s00269-012-0497-9
- ^ a b c R. C. Peterson, W. Nelson, B. Madu, and H. F. Shurvell (2007): "Meridianiite: A new mineral species observed on Earth and predicted to exist on Mars". American Mineralogist, volume 92, issue 10, pages 1756–1759. DOI:10.2138/am.2007.2668
- ^ a b Kesalahan pengutipan: Tag
<ref>tidak sah; tidak ditemukan teks untuk ref bernamafort2017 - ^ Peterson, Ronald C.; Hammarstrom, Jane M.; Seal, II, Robert R (Feb 2006). "Alpersite (Mg,Cu)SO4·7H2O, a new mineral of the melanterite group, and cuprian pentahydrite: Their occurrence within mine waste". American Mineralogist. 91 (2–3): 261–269. doi:10.2138/am.2006.1911.
