Nuklida stabil
Artikel ini membutuhkan rujukan tambahan agar kualitasnya dapat dipastikan. (Juli 2022) |
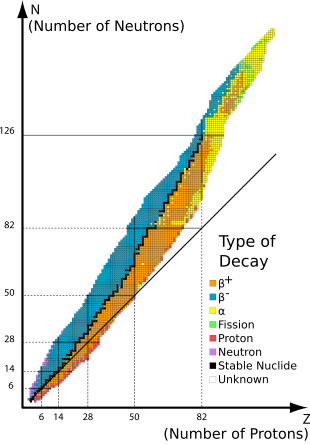
Nuklida stabil adalah nuklida yang tidak radioaktif sehingga (tidak seperti radionuklida) tidak mengalami peluruhan radioaktif secara spontan. Ketika nuklida tersebut dirujuk dalam kaitannya dengan unsur-unsur tertentu, mereka biasanya disebut isotop stabil.
80 unsur dengan satu atau lebih isotop stabil terdiri dari total 252 nuklida yang belum diketahui meluruh menggunakan peralatan saat ini (lihat daftar di akhir artikel ini). Dari unsur-unsur ini, 26 diataranya hanya memiliki satu isotop stabil; dengan demikian mereka disebut dengan monoisotop. Sisanya memiliki lebih dari satu isotop stabil. Timah memiliki 10 isotop stabil, jumlah isotop stabil terbanyak yang diketahui untuk suatu unsur.
Definisi mengenai stabilitas, dan nuklida yang terbentuk secara alami[sunting | sunting sumber]
Kebanyakan dari nuklida alami adalah stabil (sekitar 252 buah; lihat daftarnya di akhir artikel ini), dan sekitar 34 lagi (total 286) diketahui bersifat radioaktif dengan waktu paruh yang cukup panjang (juga diketahui) terjadi secara primordial. Jika waktu paruh suatu nuklida sebanding dengan, atau lebih besar dari, usia Bumi (4,5 miliar tahun), jumlah yang signifikan akan bertahan sejak pembentukan Tata Surya, dan kemudian ia dikatakan sebagai primordial. Ia kemudian akan berkontribusi dengan cara tersebut pada komposisi isotop alami dari unsur kimia. Radioisotop yang ada secara primordial mudah untuk dideteksi dengan waktu paruh sesingkat 700 juta tahun (misalnya, 235U). Ini adalah batas deteksi saat ini,[butuh rujukan] karena nuklida berumur pendek belum terdeteksi secara tidak terbantahkan di alam kecuali saat diproduksi baru-baru ini, seperti produk peluruhan atau spalasi sinar kosmik.
Banyak dari radioisotop alami (sekitar 53 atau lebih, dengan total sekitar 339) menunjukkan waktu paruh yang masih lebih pendek dari 700 juta tahun, tetapi mereka dibuat baru, sebagai produk anak dari proses peluruhan nuklida primordial (misalnya, radium dari uranium) atau dari reaksi energetik yang sedang berlangsung, seperti nuklida kosmogenik yang dihasilkan oleh pemborbardiran Bumi saat ini oleh sinar kosmik (misalnya, 14C yang terbuat dari nitrogen).
Beberapa isotop yang diklasifikasikan sebagai stabil (yaitu mereka yang tidak memiliki radioaktivitas yang teramati) diperkirakan memiliki waktu paruh yang sangat panjang (kadang-kadang setinggi 1018 tahun atau lebih).[1] Jika waktu paruh yang diprediksi jatuh ke dalam kisaran yang dapat diakses secara eksperimental, isotop tersebut memiliki peluang untuk berpindah dari daftar nuklida stabil ke kategori radioaktif, setelah aktivitasnya teramati. Misalnya, 209Bi dan 180W sebelumnya diklasifikasikan sebagai stabil, tetapi ditemukan menjadi alfa-aktif pada tahun 2003. Namun, suatu nuklida tidak mengubah statusnya sebagai primordial ketika ditemukan menjadi radioaktif.
Isotop paling stabil di Bumi diyakini telah terbentuk dalam proses nukleosintesis, baik dalam Ledakan Dahsyat, maupun dalam generasi bintang yang mendahului pembentukan Tata Surya. Namun, beberapa isotop stabil juga menunjukkan variasi kelimpahannya di Bumi sebagai akibat peluruhan dari nuklida radioaktif berumur panjang. Produk peluruhan ini disebut isotop radiogenik, untuk membedakannya dari kelompok isotop 'non-radiogenik' yang jauh lebih besar.
Isotop per unsur[sunting | sunting sumber]
Dari semua unsur kimia yang diketahui, 80 unsur memiliki setidaknya satu nuklida stabil. Mereka terdiri dari 82 unsur pertama, dari hidrogen hingga timbal, dengan dua pengecualian, yaitu teknesium (unsur 43) dan prometium (unsur 61), yang tidak memiliki satu pun nuklida stabil. Per Desember 2016, ada total 252 nuklida "stabil" yang diketahui. Dalam definisi ini, "stabil" berarti nuklida yang belum pernah teramati meluruh dengan latar belakang alami. Dengan demikian, unsur-unsur ini memiliki waktu paruh yang terlalu lama untuk diukur dengan cara apa pun, langsung atau tidak langsung.
Isotop stabil:
- 1 unsur (timah) memiliki 10 isotop stabil
- 5 unsur masing-masing memiliki 7 isotop stabil
- 7 unsur masing-masing memiliki 6 isotop stabil
- 11 unsur masing-masing memiliki 5 isotop stabil
- 9 unsur masing-masing memiliki 4 isotop stabil
- 5 unsur masing-masing memiliki 3 isotop stabil
- 16 unsur masing-masing memiliki 2 isotop stabil
- 26 unsur masing-masing memiliki 1 isotop stabil.
26 yang terakhir ini disebut unsur monoisotop.[2] Jumlah rata-rata isotop stabil untuk unsur-unsur yang memiliki setidaknya satu isotop stabil adalah 252/80 = 3,15.
Bilangan ajaib fisik dan jumlah proton dan neutron ganjil dan genap [sunting | sunting sumber]
Stabilitas isotop dipengaruhi oleh rasio proton terhadap neutron, dan juga oleh adanya bilangan ajaib tertentu dari neutron atau proton yang mewakili kulit kuantum tertutup dan terisi. Kulit kuantum ini sesuai dengan satu set tingkat energi dalam model kulit nukleus; kulit terisi, seperti kulit yang berisi 50 proton untuk timah, memberikan stabilitas yang tidak biasa pada nuklida. Seperti dalam kasus timah, bilangan ajaib untuk Z, nomor atom, cenderung meningkatkan jumlah isotop stabil untuk unsur tersebut.
Sama seperti dalam kasus elektron, yang memiliki tingkat energi terendah ketika mereka terjadi berpasangan dalam orbital tertentu, nukleon (proton dan neutron) menunjukkan keadaan energi yang lebih rendah ketika jumlahnya genap, daripada ganjil. Stabilitas ini cenderung mencegah peluruhan beta (dalam dua langkah) dari banyak nuklida genap–genap menjadi nuklida genap–genap lain dengan nomor massa yang sama tetapi dengan energi yang lebih rendah (dan tentu saja dengan dua proton lebih banyak dan dua neutron lebih sedikit), karena peluruhan berlangsung satu langkah pada suatu waktu harus melewati nuklida ganjil–ganjil dengan energi yang lebih tinggi. Inti seperti ini malah mengalami peluruhan beta ganda (atau diteorikan demikian) dengan waktu paruh beberapa kali lipat lebih besar dari usia alam semesta. Hal ini menghasilkan lebih banyak nuklida genap yang stabil, yang merupakan 151 dari total 252. Jumlah nuklida genap–genap yang stabil sebanyak tiga isobar untuk beberapa nomor massa, dan hingga tujuh isotop untuk beberapa nomor atom.
Sebaliknya, dari 252 nuklida stabil yang diketahui, hanya lima yang memiliki jumlah proton ganjil dan jumlah neutron ganjil: 2H (deuterium), 6Li, 10B, 14N, dan 180mTa. Juga, hanya ada empat nuklida ganjil–ganjil radioaktif alami yang memiliki waktu paruh lebih dari satu miliar tahun: 40K, 50V, 138La, dan 176Lu. Nuklida primordial ganjil–ganjil jarang terjadi karena sebagian besar inti ganjil–ganjil tidak stabil sehubungan dengan peluruhan beta, karena produk peluruhannya genap–genap, dan karena itu terikat lebih kuat, dikarenakan efek dari pasangan inti.[3]
Namun, efek lain dari ketidakstabilan jumlah ganjil dari kedua jenis nukleon adalah bahwa unsur-unsur bernomor ganjil cenderung memiliki lebih sedikit isotop stabil. Dari 26 unsur monoisotop (yang hanya memiliki satu isotop stabil), semua kecuali satu memiliki nomor atom ganjil, dan semua kecuali satu memiliki jumlah neutron genap—pengecualian tunggal untuk kedua aturan tersebut adalah berilium.
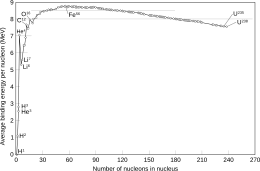
Akhir dari unsur-unsur stabil dalam tabel periodik terjadi setelah timbal, sebagian besar disebabkan oleh fakta bahwa inti dengan 128 neutron sangat tidak stabil dan segera melepaskan partikel alfa. Ini juga berkontribusi pada waktu paruh astatin, radon, dan fransium yang sangat singkat dibandingkan dengan unsur yang lebih berat. Ini juga dapat dilihat pada tingkat yang jauh lebih rendah dengan 84 neutron, yang menunjukkan sejumlah isotop dalam deret lantanida yang menunjukkan peluruhan alfa.
Isomer nuklir, termasuk yang "stabil"[sunting | sunting sumber]
Hitungan 252 nuklida stabil yang diketahui termasuk 180mTa, karena meskipun peluruhan dan ketidakstabilannya secara otomatis tersirat oleh notasi "metastabil", ini masih belum teramati. Semua isotop "stabil" (stabil dengan pengamatan, bukan teori) adalah keadaan dasar dari suatu inti, dengan pengecualian 180mTa, yang merupakan sebuah isomer nuklir atau keadaan tereksitasi. Keadaan dasar dari inti khusus ini, 180Ta, bersifat radioaktif dengan waktu paruh yang relatif pendek, yaitu 8 jam; sebaliknya, peluruhan isomer nuklir yang tereksitasi sangat dilarang oleh aturan pemilihan paritas spin. Telah dilaporkan secara eksperimental dengan pengamatan langsung bahwa waktu paruh 180mTa untuk peluruhan gama harus lebih dari 1015 tahun. Kemungkinan mode peluruhan 180mTa lainnya (peluruhan beta, penangkapan elektron, dan peluruhan alfa) juga tidak pernah teramati.
Peluruhan yang masih belum teramati[sunting | sunting sumber]
Diperkirakan bahwa beberapa perbaikan terus-menerus dari sensitivitas eksperimental akan memungkinkan penemuan radioaktivitas (ketidakstabilan) yang sangat ringan dari beberapa isotop yang dianggap stabil saat ini. Sebagai contoh penemuan baru-baru ini, pada tahun 2003, 209Bi (satu-satunya isotop primordial bismut) terbukti memiliki radioaktivitas yang sangat ringan,[4] mengonfirmasi prediksi teoretis dari fisika nuklir bahwa 209Bi akan meluruh dengan sangat lambat melalui emisi alfa.
Isotop-isotop yang secara teoretis diyakini tidak stabil tetapi belum pernah teramati meluruh disebut stabil secara pengamatan. Saat ini ada 162 isotop yang secara teoretis tidak stabil, 45 di antaranya telah teramati secara rinci tanpa tanda-tanda peluruhan, yang paling ringan adalah 36Ar.
Banyak nuklida "stabil" adalah "metastabil" karena mereka akan melepaskan energi jika peluruhan radioaktif terjadi,[5] dan pada kenyataannya, diperkirakan mengalami jenis peluruhan radioaktif yang sangat langka, termasuk emisi beta ganda.
90 nuklida dari 40 unsur dengan nomor atom dari 1 (hidrogen) hingga 40 secara teoretis stabil terhadap segala jenis peluruhan nuklir—kecuali untuk kemungkinan teoretis dari peluruhan proton - yang belum pernah teramati meskipun telah dilakukan pencarian secara ekstensif.[6]
Nuklida mulai dari isotop 93Nb dan meluas ke semua nomor massa atom yang lebih tinggi, secara teoretis dapat mengalami fisi spontan.[6]
Untuk proses selain fisi spontan, rute peluruhan teoretis lainnya untuk unsur-unsur yang lebih berat meliputi:[6]
- peluruhan alfa - 70 nuklida berat (dua yang paling ringan adalah 142Ce dan 143Nd)
- peluruhan beta ganda (termasuk konversi elektron-positron, dan peluruhan positron ganda) - 55 nuklida
- peluruhan beta - 180mTa
- penangkapan elektron - 123Te, 180mTa
- penangkapan elektron ganda
- transisi isomerik - 180mTa
- peluruhan gugus dan fisi spontan - 56 nuklida berat (dari 93Nb hingga 164Dy)
Mereka semua termasuk nuklida bermassa 165 dan lebih besar. 36Ar saat ini merupakan nuklida "stabil" namun secara teoritis tidak stabil paling ringan yang diketahui.[6]
Positivitas pelepasan energi dalam proses ini berarti bahwa mereka diizinkan secara kinematik (mereka tidak melanggar hukum kekekalan energi) dan dengan demikian, pada prinsipnya dapat terjadi.[6] Mereka tidak teramati karena penekanan yang kuat, tetapi tidak mutlak, oleh aturan pemilihan spin-paritas (untuk peluruhan beta dan transisi isomerik) atau oleh ketebalan penghalang potensial (untuk peluruhan alfa dan gugus serta fisi spontan).
Tabel ringkasan untuk jumlah dari setiap kelas nuklida[sunting | sunting sumber]
Ini adalah tabel ringkasan dari daftar nuklida. Perhatikan bahwa jumlahnya tidak tepat dan mungkin sedikit berubah di masa depan, karena nuklidanya teramati bersifat radioaktif, atau waktu paruh baru ditentukan dengan presisi tertentu.
| Jenis nuklida menurut kelas stabilitas | Jumlah nuklida di dalam kelas | Total berjalan dari nuklida di semua kelas hingga saat ini | Catatan |
|---|---|---|---|
| Secara teoretis stabil sesuai dengan Model Standar | 90 | 90 | Termasuk 40 unsur pertama. Jika proton dapat meluruh, maka tidak ada satu pun nuklida yang stabil. |
| Secara teoretis stabil terhadap peluruhan alfa, peluruhan beta, transisi isomerik, dan peluruhan beta ganda tetapi tidak terhadap fisi spontan, yang dimungkinkan untuk nuklida "stabil" ≥ 93Nb | 56 | 146 | Perhatikan bahwa fisi spontan tidak pernah teramati untuk nuklida dengan nomor massa < 230. |
| Secara energetik tidak stabil pada satu atau lebih mode peluruhan yang diketahui, tetapi belum ada peluruhan yang terlihat. Dianggap stabil sampai radioaktivitasnya dikonfirmasi. | 106 [butuh rujukan] |
252 | Total ini merupakan total nuklida yang stabil secara pengamatan. |
| Nuklida primordial yang radioaktif. | 34 | 286 | Termasuk Bi, Th, U |
| Nonprimordial yang radioaktif, tetapi terjadi secara alami di Bumi. | ~61 signifikan | ~347 signifikan | Nuklida kosmogenik dari sinar kosmik; anak dari nuklida primordial yang radioaktif, seperti fransium, dll. |
Daftar nuklida stabil[sunting | sunting sumber]
- Hidrogen-1
- Hidrogen-2
- Helium-3
- Helium-4
- tidak ada nomor massa 5
- Litium-6
- Litium-7
- tidak ada nomor massa 8
- Berilium-9
- Boron-10
- Boron-11
- Karbon-12
- Karbon-13
- Nitrogen-14
- Nitrogen-15
- Oksigen-16
- Oksigen-17
- Oksigen-18
- Fluorin-19
- Neon-20
- Neon-21
- Neon-22
- Natrium-23
- Magnesium-24
- Magnesium-25
- Magnesium-26
- Aluminium-27
- Silikon-28
- Silikon-29
- Silikon-30
- Fosforus-31
- Belerang-32
- Belerang-33
- Belerang-34
- Belerang-36
- Klorin-35
- Klorin-37
- Argon-36 (2E)
- Argon-38
- Argon-40
- Kalium-39
- Kalium-41
- Kalsium-40 (2E)*
- Kalsium-42
- Kalsium-43
- Kalsium-44
- Kalsium-46 (2B)*
- Skandium-45
- Titanium-46
- Titanium-47
- Titanium-48
- Titanium-49
- Titanium-50
- Vanadium-51
- Kromium-50 (2E)*
- Kromium-52
- Kromium-53
- Kromium-54
- Mangan-55
- Besi-54 (2E)*
- Besi-56
- Besi-57
- Besi-58
- Kobalt-59
- Nikel-58 (2E)*
- Nikel-60
- Nikel-61
- Nikel-62
- Nikel-64
- Tembaga-63
- Tembaga-65
- Seng-64 (2E)*
- Seng-66
- Seng-67
- Seng-68
- Seng-70 (2B)*
- Galium-69
- Galium-71
- Germanium-70
- Germanium-72
- Germanium-73
- Germanium-74
- Arsen-75
- Selenium-74 (2E)
- Selenium-76
- Selenium-77
- Selenium-78
- Selenium-80 (2B)
- Bromin-79
- Bromin-81
- Kripton-80
- Kripton-82
- Kripton-83
- Kripton-84
- Kripton-86 (2B)
- Rubidium-85
- Stronsium-84 (2E)
- Stronsium-86
- Stronsium-87
- Stronsium-88
- Itrium-89
- Zirkonium-90
- Zirkonium-91
- Zirkonium-92
- Zirkonium-94 (2B)*
- Niobium-93
- Molibdenum-92 (2E)*
- Molibdenum-94
- Molibdenum-95
- Molibdenum-96
- Molibdenum-97
- Molibdenum-98 (2B)*
- Teknesium - tidak memiliki isotop stabil
- Rutenium-96 (2E)*
- Rutenium-98
- Rutenium-99
- Rutenium-100
- Rutenium-101
- Rutenium-102
- Rutenium-104 (2B)
- Rodium-103
- Paladium-102 (2E)
- Paladium-104
- Paladium-105
- Paladium-106
- Paladium-108
- Paladium-110 (2B)*
- Perak-107
- Perak-109
- Kadmium-106 (2E)*
- Kadmium-108 (2E)*
- Kadmium-110
- Kadmium-111
- Kadmium-112
- Kadmium-114 (2B)*
- Indium-113
- Timah-112 (2E)
- Timah-114
- Timah-115
- Timah-116
- Timah-117
- Timah-118
- Timah-119
- Timah-120
- Timah-122 (2B)
- Timah-124 (2B)*
- Antimon-121
- Antimon-123
- Telurium-120 (2E)*
- Telurium-122
- Telurium-123 (E)*
- Telurium-124
- Telurium-125
- Telurium-126
- Iodin-127
- Xenon-126 (2E)
- Xenon-128
- Xenon-129
- Xenon-130
- Xenon-131
- Xenon-132
- Xenon-134 (2B)*
- Sesium-133
- Barium-132 (2E)*
- Barium-134
- Barium-135
- Barium-136
- Barium-137
- Barium-138
- Lantanum-139
- Serium-136 (2E)*
- Serium-138 (2E)*
- Serium-140
- Serium-142 (A, 2B)*
- Praseodimium-141
- Neodimium-142
- Neodimium-143 (A)
- Neodimium-145 (A)*
- Neodimium-146 (2B)
- tidak ada nomor massa 147
- Neodimium-148 (A, 2B)*
- Prometium - tidak memiliki isotop stabil
- Samarium-144 (2E)
- Samarium-149 (A)*
- Samarium-150 (A)
- tidak ada nomor massa 151
- Samarium-152 (A)
- Samarium-154 (2B)*
- Europium-153 (A)
- Gadolinium-154 (A)
- Gadolinium-155 (A)
- Gadolinium-156
- Gadolinium-157
- Gadolinium-158
- Gadolinium-160 (2B)*
- Terbium-159
- Disprosium-156 (A, 2E)*
- Disprosium-158 (A)
- Disprosium-160 (A)
- Disprosium-161 (A)
- Disprosium-162 (A)
- Disprosium-163
- Disprosium-164
- Holmium-165 (A)
- Erbium-162 (A, 2E)*
- Erbium-164 (A)
- Erbium-166 (A)
- Erbium-167 (A)
- Erbium-168 (A)
- Erbium-170 (A, 2B)*
- Tulium-169 (A)
- Iterbium-168 (A, 2E)*
- Iterbium-170 (A)
- Iterbium-171 (A)
- Iterbium-172 (A)
- Iterbium-173 (A)
- Iterbium-174 (A)
- Iterbium-176 (A, 2B)*
- Lutesium-175 (A)
- Hafnium-176 (A)
- Hafnium-177 (A)
- Hafnium-178 (A)
- Hafnium-179 (A)
- Hafnium-180 (A)
- Tantalum-180m (A, B, E, IT)* ^
- Tantalum-181 (A)
- Wolfram-182 (A)*
- Wolfram-183 (A)*
- Wolfram-184 (A)*
- Wolfram-186 (A, 2B)*
- Renium-185 (A)
- Osmium-184 (A, 2E)*
- Osmium-187 (A)
- Osmium-188 (A)
- Osmium-189 (A)
- Osmium-190 (A)
- Osmium-192 (A, 2B)*
- Iridium-191 (A)
- Iridium-193 (A)
- Platina-192 (A)*
- Platina-194 (A)
- Platina-195 (A)
- Platina-196 (A)
- Platina-198 (A, 2B)*
- Emas-197 (A)
- Raksa-196 (A, 2E)*
- Raksa-198 (A)
- Raksa-199 (A)
- Raksa-200 (A)
- Raksa-201 (A)
- Raksa-202 (A)
- Raksa-204 (2B)
- Talium-203 (A)
- Talium-205 (A)
- Timbal-204 (A)*
- Timbal-206 (A)
- Timbal-207 (A)
- Timbal-208 (A)*
- Bismut ^^ dan di atasnya –
- tidak memiliki isotop stabil
- tidak ada nomor massa 209 dan di atasnya
- Bismut ^^ dan di atasnya –
Singkatan dari prediksi peluruhan yang tak teramati[7][butuh sumber yang lebih baik]:
A untuk peluruhan alfa, B untuk peluruhan beta, 2B untuk peluruhan beta ganda, E untuk penangkapan elektron, 2E untuk penangkapan elektron ganda, IT untuk transisi isomerik, SF untuk fisi spontan, * untuk nuklida yang waktu paruhnya memiliki batas bawah.
^ 180mTa merupakan sebuah "isotop metastabil" yang berarti bahwa ia adalah isomer nuklir tereksitasi dari 180Ta. Lihat isotop tantalum. Namun, waktu paruh isomer nuklir ini begitu lama sehingga tidak pernah teramati meluruh, dan dengan demikian terjadi sebagai nuklida primordial "nonradioaktif secara pengamatan", sebagai isotop minor tantalum. Ini adalah satu-satunya kasus isomer nuklir yang memiliki waktu paruh begitu lama sehingga tidak pernah teramati meluruh. Dengan demikian ia termasuk dalam daftar ini.
^^ 209Bi telah lama diyakini stabil, karena waktu paruhnya yang luar biasa panjang, yaitu 2,01×1019 tahun, lebih dari satu miliar (1000 juta) kali usia alam semesta.
Lihat pula[sunting | sunting sumber]
- Geokimia isotop
- Daftar unsur menurut kestabilan isotop
- Daftar nuklida (991 nuklida dalam urutan stabilitas, semuanya dengan waktu paruh > satu jam)
- Unsur mononuklida
- Tabel periodik
- Nuklida primordial
- Radionuklida
- Rasio isotop stabil
- Tabel nuklida
Referensi[sunting | sunting sumber]
- ^ Belli, P.; Bernabei, R.; Danevich, F. A.; et al. (2019). "Experimental searches for rare alpha and beta decays". European Physical Journal A. 55 (8): 140–1–140–7. arXiv:1908.11458
 . Bibcode:2019EPJA...55..140B. doi:10.1140/epja/i2019-12823-2. ISSN 1434-601X.
. Bibcode:2019EPJA...55..140B. doi:10.1140/epja/i2019-12823-2. ISSN 1434-601X.
- ^ Sonzogni, Alejandro. "Interactive Chart of Nuclides". National Nuclear Data Center: Brook haven National Laboratory. Diarsipkan dari versi asli tanggal 10 Oktober 2018. Diakses tanggal 16 Juli 2022.
- ^ Various (2002). Lide, David R., ed. Handbook of Chemistry & Physics (edisi ke-88). CRC. ISBN 978-0-8493-0486-6. OCLC 179976746. Diarsipkan dari versi asli tanggal 24 Juli 2017. Diakses tanggal 16 Juli 2022.
- ^ "WWW Table of Radioactive Isotopes".[pranala nonaktif permanen]
- ^ "NNDC - Atomic Masses". www.nndc.bnl.gov. Diarsipkan dari versi asli tanggal 2019-01-11. Diakses tanggal 2022-07-16.
- ^ a b c d e http://www.nucleonica.net/unc.aspx
- ^ "Nucleonica :: Web driven nuclear science".
Referensi buku[sunting | sunting sumber]
- Various (2002). Lide, David R., ed. Handbook of Chemistry & Physics (edisi ke-88). CRC. ISBN 978-0-8493-0486-6. OCLC 179976746. Diarsipkan dari versi asli tanggal 24 Juli 2017. Diakses tanggal 16 Juli 2022.
Pranala luar[sunting | sunting sumber]
- The LIVEChart Nuklida - IAEA
- AlphaDelta: Kalkulator fraksinasi Isotop Stabil
- Pusat Pengembangan Isotop Nasional Informasi referensi mengenai isotop, serta koordinasi dan pengelolaan produksi, ketersediaan, dan distribusi isotop
- Pengembangan & Produksi Isotop untuk Penelitian dan Aplikasi (Isotope Development & Production for Research and Applications, IDPRA) Program Departemen Energi AS untuk produksi isotop serta produksi penelitian dan pengembangan
- Isosciences Diarsipkan 2021-01-18 di Wayback Machine. Penggunaan dan pengembangan label isotop stabil dalam molekul sintetik dan biologis
