Kimia organoarsen
Kimia organoarsen adalah kimia tentang senyawa-senyawa yang mengandung ikatan kimia antara arsen dan karbon. Beberapa senyawa organoarsen diproduksi secara industri untuk digunakan sebagai insektisida, herbisida, dan fungisida. Umumnya, penggunaan ini ditolak meningat dampaknya terhadap lingkungan dan kesehatan manusia. Senyawa induknya adalah arsina dan asam arsenat. Selain toksisitasnya, biomolekul organoarsen sudah sangat dikenal.
Sejarah[sunting | sunting sumber]
Kimia organoarsen memainkan peran penting dalam sejarah perkembangan ilmu kimia. Suatu hal yang mengejutkan mengingat bidang ilmu ini dahulu dianggap kurang penting. Senyawa organoarsen tertua yang diketahui yaitu cacodyl, yang berbau busuk, dilaporkan dalam "cacodyl" (1760) dan terkadang diklasifikasikan sebagai senyawa organologam yang pertama kali disintesis. Senyawa Salvarsan adalah produk farmasi pertama, dan membawa Paul Ehrlich sebagai pemenang Nobel. Beragam senyawa organoarsen pernah digunakan sebagai antibiotik (Solarson) atau kegunaan medis lainnya.[1]
Sintesis dan klasifikasi[sunting | sunting sumber]
Arsen umumnya berada pada tingkat oksidasi (III) dan (V), digambarkan sebagai halida AsX3 (X = F, Cl, Br, I) dan AsF5. Oleh karena itu, senyawa organoarsen juga jamak ditemukan pada kedua tingkat oksidasi tersebut.[2]
Kimia dan penggunaan organoarsen(V)[sunting | sunting sumber]
Senyawa arsen(V) biasanya membentuk gugus fungsional RAsO(OH)2 atau R2AsO(OH) (R = alkil atau aril). Asam kakodilat, dengan rumus (CH3)2AsO2H, menjelaskan gambaran utuh senyawa organoarsen. Sebaliknya, asam dimetilfosfonat kurang memberikan gambaran tentang kimia fosfor. Asam kakodilat terbentuk dari metilasi arsen(III) oksida. Asam fenilarsonat dapat diperoleh dari reaksi antara asam arsenat dengan anilin, yang dikenal dengan reaksi Bechamp.
Asam monometilnya, asam metanarsonat (CH3AsO(OH)2), adalah prekursor fungisida (nama dagang Neoasozin) pada penanaman beras dan kapas. Derivat asam fenilarsonat (C6H5AsO(OH)2) digunakan sebagai bahan tambahan pakan ternak, termasuk asam 4-hidroksi-3-nitrobenzenarsonat (3-NHPAA atau Roxarsone), asam ureidofenilarsonat, dan asam p-arsanilat. Aplikasi ini bersifat kontroversial karena mereka menambahkan arsen dalam bentuk terlarut ke dalam lingkungan.
Jarang ditemukan senyawa arsen(V) yang hanya mengandung ligan organik. Salah satu yang menonjol adalah derivat pentafenil As(C6H5)5.[3]
Kimia dan penggunaan organoarsen(III)[sunting | sunting sumber]
Kebanyakan senyawa ini dibuat dengan cara alkilasi AsCl3 dan derivatnya menggunakan organolitium dan pereaksi Grignard.[3] Misalnya, trimetilarsina ((CH3)3As), dimetilarsenat klorida ((CH3)2AsCl), dan metilarsenat diklorida (CH3AsCl2). Reduksi derivat klorida menggunakan pereduksi hidrida menghasilkan hidrida-hidrida seperti dimetilarsina ((CH3)2AsH) dan metilarsina (CH3AsH2). Perlakuan serupa dapat digunakan untuk senyawa klorida organoarsen lainnya.
Reaksi penting pembentukan senyawa dimetilarsenat dimulai dari reduksi asam kakodilat:
- (CH3)2AsO2H + 2 Zn + 4 HCl → (CH3)2AsH + 2 ZnCl2 + 2 H2O
- (CH3)2AsO2H + SO2 + HI → (CH3)2AsI + SO3 + H2O
Telah diketahui berbagai senyawa heterosiklik yang mengandung arsen(III). Antara lain: arsole senyawa organoarsen yang analog dengan pyrrole, dan arsabenzena, senyawa arsen yang analog dengan piridina.
Senyawa organoarsen(III) simetris, seperti trimetilarsina dan trifenilarsina, banyak digunakan sebagai ligan dalam kimia koordinasi. Mereka bertindak seperti ligan fosfin, tetapi kurang bersifat basa. Diarsin, C6H4(As(CH3)2)2, dikenal sebagai diar, suatu ligan khelat. Thorin adalah indikator untuk beberapa logam.
Senyawa organoarsen(I) dan penggunaannya[sunting | sunting sumber]
Spesies organoarsen yang jarang dimanfaatkan secara komersial adalah senyawa organoarsen(I). Obat anti sifilis Salvarsan dan Neosalvarsan mewakili kelompok ini. Senyawa ini biasanya memiliki tiga ikatan ke atom As, tetapi ikatan As-As adalah ikatan tunggal. Jarang ditemukan senyawa arsen(I) dengan ikatan rangkap As=As.
Perang kimia[sunting | sunting sumber]
Senyawa organoarsen, terutama yang mengandung ikatan As-Cl, telah digunakan sebagai senjata kimia, terutama selama Perang Dunia I. Contoh yang kurang populer antara lain "Lewisite" (klorovinil-2-arsenik diklorida) dan "Clark I" (klorodifenilarsina). Fenildikloroarsina adalah contoh lainnya.
Keberadaan di alam[sunting | sunting sumber]
Oleh karena arsen bersifat racun terhadap segala bentuk kehidupan dan peningkatan konsentrasinya di alam di beberapa area menunjukkan peningkatan, maka diperlukan strategi detoksifikasi yang memadai. Arsen anorganik dan senyawanya, begitu memasuki rantai makanan, akan dimetabolisme secara progresif menjadi bentuk yang kurang beracun melalui proses metilasi.[4] Senyawa organoarsen muncul melalui biometilasi senyawa arsen anorganik,[5] melalui proses yang dimediasi oleh enzim yang berhubungan dengan vitamin B12.[6] Sebagai contoh, jamur Scopulariopsis brevicaulis menghasilkan trimetilarsina dalam jumlah yang signifikan jika terdapat arsen anorganik.[7] Senyawa organik arsenobetain, suatu betain, juga ditemukan dalam bebeapa makanan laut seperti ikan dan alga, dan juga jamur dengan konsentrasi yang lebih besar. Rata-rata asupan per orang sekitar 10-50 µg/hari. Nilai sekitar 1000 µg tidak wajar dalam mengkonsumsi ikan atau jamur. Bahaya dari mengkonsumsi ikan adalah minimal, karena senyawa arsenobetain hampir tidak beracun.[8] Arsenobetain pertama kali diidentifikasi terdapat dalam lobster Panulirus cygnus.[9][10]
Arsen dapat mengikat karbohidrat, dikenal sebagai arsenogula, ditemukan terutama dalam rumput laut. Arsen yang mengandung lemak juga telah diketahui.[11] Meskipun arsen dan senyawanya bersifat racun terhadap manusia, satu dari antibiotik sintetis yaitu Salvarsan mengandung arsen. Penggunaan Salvarsan telah lama dihentikan.
Satu-satunya senyawa poliarsen yang diisolasi dari sumber alami adalah arsenicin A.[12]
Senyawa organoarsen dapat mempengaruhi kesehatan, bergantung pada spesiasinya. Rentang LD50 nya: mulai dari LD50 dengan rentang 5–6 mg/kg (sangat beracun) hingga 12 000–15 000 mg/kg (praktis tak beracun).
Contoh senyawa organoarsen[sunting | sunting sumber]
Ilustrasi beberapa senyawa organoarsen terdapat dalam tabel di bawah:
| Organoarsen | R | Massa molar | Nomor CAS | Sifat-sifat | |
| 10,10'-oxybis-10H-Phenoxarsine |  |
502.2318 | 58-36-6 | ||
| Trifenilarsina | Fenil |  |
306.23 | 603-32-7 | Titik leleh 58-61 °C |
| Fenildikloroarsina | fenil, klorin | 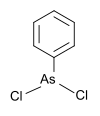 |
222.93 | 696-28-6 | |
| Roxarsone | 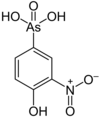 |
263.04 | 121-19-7 | ||
| Arsenobetain | 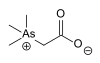 |
64436-13-1 | |||
| Contoh senyawa organoarsen [13] | |||||
Lihat juga[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ Singh, R. Synthetic Drugs. Mittal Publications (2002).ISBN 81-7099-831-X
- ^ Sabina C. Grund, Kunibert Hanusch, Hans Uwe Wolf "Arsenic and Arsenic Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, VCH-Wiley, 2008, Weinheim.
- ^ a b Elschenbroich, C. "Organometallics" (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ^ Reimer, K. J.; Koch, I.; Cullen, W. R. (2010). "Organoarsenicals. Distribution and transformation in the environment". Metal ions in life sciences (Cambridge: RSC publishing) 7: 165–229.doi:10.1039/9781849730822-00165. ISBN 978-1-84755-177-1. PMID 20877808.
- ^ Dopp, E.; Kligerman, A. D.; Diaz-Bone, R. A. (2010). "Organoarsenicals. Uptake, metabolism and toxicity". Metal ions in life sciences (Cambridge: RSC publishing) 7: 231–265.doi:10.1039/BK9781847551771-00231. ISBN 978-1-84755-177-1. PMID 20877809.
- ^ Toshikazu Kaise, Mitsuo Ogura, Takao Nozaki, Kazuhisa Saitoh, Teruaki Sakurai, Chiyo Matsubara, Chuichi Watanabe, Ken'ichi Hanaoka (1998). "Biomethylation of Arsenic in an Arsenic-rich Freshwater Environment". Applied Organometallic Chemistry 11: 297–304. doi:10.1002/(SICI)1099-0739(199704)11:4<297::AID-AOC584>3.0.CO;2-0.
- ^ Bentley, Ronald; Chasteen, Thomas G. (2002). "Microbial Methylation of Metalloids: Arsenic, Antimony, and Bismuth". Microbiology and Molecular Biology Reviews 66 (2): 250–271.doi:10.1128/MMBR.66.2.250-271.2002. PMC 120786. PMID 12040126.
- ^ Cullen, William R.; Reimer, Kenneth J. (1989). "Arsenic speciation in the environment". Chemical Reviews 89 (4): 713–764. doi:10.1021/cr00094a002.
- ^ Francesconi, Kevin A.; John S. Edmonds Croatian Chemica Acta (1998). "Arsenic Species in Marine Samples" Diarsipkan 2008-03-09 di Wayback Machine. (PDF) 71 (2). pp. 343–359.
- ^ John S. Edmonds, Kevin A. Francesconi, Jack R. Cannon, Colin L. Raston, Brian W. Skelton and Allan H. White (1977). "Isolation, crystal structure and synthesis of arsenobetaine, the arsenical constituent of the western rock lobster panulirus longipes cygnus George". Tetrahedron Letters 18 (18): 1543–1546. doi:10.1016/S0040-4039(01)93098-9.
- ^ Alice Rumpler, John S. Edmonds, Mariko Katsu, Kenneth B. Jensen, Walter Goessler, Georg Raber, Helga Gunnlaugsdottir, Kevin A. Francesconi (2008). "Arsenic-Containing Long-Chain Fatty Acids in Cod-Liver Oil: A Result of Biosynthetic Infidelity?". Angew. Chem. Int. Ed. 47: 2665–2667. doi:10.1002/anie.200705405. PMID 18306198.
- ^ Mancini, Ines; Guella, Graziano; Frostin, Maryvonne; Hnawia, Edouard; Laurent, Dominique; Debitus, Cecile; Pietra, Francesco (2006). "On the First Polyarsenic Organic Compound from Nature: Arsenicin a from the New Caledonian Marine SpongeEchinochalina bargibanti". Chemistry - A European Journal 12 (35): 8989–94. doi:10.1002/chem.200600783.PMID 17039560.
- ^ http://www.sigmaaldrich.com
