Peptida: Perbedaan antara revisi
Tidak ada ringkasan suntingan |
Tidak ada ringkasan suntingan |
||
| Baris 2: | Baris 2: | ||
[[Berkas:C-Peptide.svg|Kerangka Gambar Peptida|thumb|300px]] |
[[Berkas:C-Peptide.svg|Kerangka Gambar Peptida|thumb|300px]] |
||
'''Peptida''' merupakan molekul yang terbentuk dari dua atau lebih asam amino. Jika jumlah asam amino masih di bawah 50 molekul disebut peptide, namun jika lebih dari 50 molekul disebut dengan protein. Asam amino saling berikatan dengan ikatan peptida. Ikatan peptida terjadi jika atom nitrogen pada salah satu asam amino berikatan dengan gugus karboksil dari asam amino lain. |
'''Peptida''' merupakan molekul yang terbentuk dari dua atau lebih asam amino. Jika jumlah asam amino masih di bawah 50 molekul disebut peptide, namun jika lebih dari 50 molekul disebut dengan protein. Asam amino saling berikatan dengan ikatan peptida. Ikatan peptida terjadi jika atom nitrogen pada salah satu asam amino berikatan dengan gugus karboksil dari asam amino lain. |
||
Peptida terdapat pada setiap makhluk hidup dan berperan pada beberapa aktivitas biokimia. Peptida dapat berupa enzim, hormon, antibiotik, dan reseptor. <ref name="Oleg">Oleg |
Peptida terdapat pada setiap makhluk hidup dan berperan pada beberapa aktivitas biokimia. Peptida dapat berupa enzim, hormon, antibiotik, dan reseptor. <ref name="Oleg">Oleg L. 2010. Welcome to Peptide Guide. [terhubung berkala]. http://www.peptideguide.com/index.html [16 Mei 2010].</ref> |
||
== Sintesis Peptida == |
== Sintesis Peptida == |
||
Revisi per 17 Mei 2010 09.56
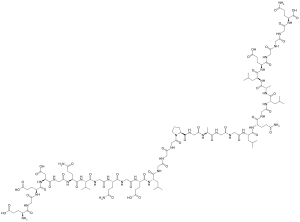
Peptida merupakan molekul yang terbentuk dari dua atau lebih asam amino. Jika jumlah asam amino masih di bawah 50 molekul disebut peptide, namun jika lebih dari 50 molekul disebut dengan protein. Asam amino saling berikatan dengan ikatan peptida. Ikatan peptida terjadi jika atom nitrogen pada salah satu asam amino berikatan dengan gugus karboksil dari asam amino lain. Peptida terdapat pada setiap makhluk hidup dan berperan pada beberapa aktivitas biokimia. Peptida dapat berupa enzim, hormon, antibiotik, dan reseptor. [1]
Sintesis Peptida

Sintesis peptida dilakukan dengan menggabungkan gugus karboksil salah satu asam amino dengan gugus amina dari asam amino yang lain. Sintesis peptida dimulai dari C-terminus (gugus karkobsil) ke N-terminus (gugus amin), seperti yang terjadi secara alami pada organisme. Namun, untuk mensintesis peptida, tidak semudah mencampurkan asam amino begitu saja. Seperti contohnya: mencampurkan glutamine (E) dan serine (S) dapat menghasilkan E-S, S-E, S-S, E-E, dan bahkan polipeptida seperti E-S-S-E-E. Untuk menghindari asam amino berikatan tidak terkendali, perlu dilakukan perlindungan dan kontrol terhadap ikatan peptida yang akan terjadis sehingga ikatan yang terbentuk sesuai dengan yang diinginkan. Langkah-langkah sintesis peptida adalah sebagai berikut: asam amino ditambahkan gugus proteksi. Kemudian asam amino yang diproteksi dilarutkan dalam pelarut seperti dimetyhlformamide (DMF) yand digabungkan dengan coupling reagents dipompa melalui kolom sintesis. Grup proteksi dihilangkan dari asam amino melalui reaksi deproteksi. Kemudian pereaksi deproteksi dihilangkan agar tercipta suasana penggabungan yang bersih. Coupling reagents, contohnya N,N'-dicyclohexylcarbodiimide (DCCI), membantu pembentukan ikatan peptida. Setelah reaksi coupling terbentuk, coupling reagents dicuci untuk menciptakan suasana deproteksi yang bersih. Proses proteksi, deproteksi, dan coupling ini terus dilakukan berulang-ulang hingga tercipta peptida yang diinginkan.[2]
Kelas Peptida
Peptida Ribosomal
Peptida ribosomal disintesis dari translasi mRNA. Peptida ini berfungsi sebagai hormon dan molekul signal pada organisme tingkat tinggi. Secara umum, peptida ini mempunyai strukstur linear.[3]
Peptida non-Ribosomal
Peptida non-Ribosomal disintesis dengan kompleks enzim. Peptida ini terdapat pada organisme uniselular, tanaman, dan fungi. Pada peptida ini terdapat struktur inti yang kompleks dan mengandung pengaturan yang berbeda-beda untuk melakukan manipulasi kimia untuk menghasilkan suatu produk. Secara umum, peptida ini berbentuk siklik, walaupun ada juga yang berbentuk linear.[4]
Peptida Hasil Digesti (Digested peptides)
Peptida ini terbentuk dari hasil proteolysis non-spesifik dalam siklus digesti. Peptida hasil digesti secara umum merupakan peptida ribosomal, akan tetapi tidak dibentuk dari translasi mRNA. Peptida ini juga dapat dibentuk dari protein yang didigesti dengan protease spesifik, seperti digesti trypsin yang sering dilakukan sebelum mass spectrometry peptide analysis.[5]
Referensi
- ^ Oleg L. 2010. Welcome to Peptide Guide. [terhubung berkala]. http://www.peptideguide.com/index.html [16 Mei 2010].
- ^ [Peptide Station]. 2006. Peptide Synthesis. [terhubung berkala]. http://www.peptidestation.com/peptide-synthesis/ [16 Mei 2010].
- ^ [Peptide Station]. 2006a. Ribosomal peptides. [terhubung berkala]. http://www.peptidestation.com/ribosomal-peptides/ [16 Mei 2010].
- ^ [Peptide Station]. 2006b. Non-ribosomal peptides. [terhubung berkala]. http://www.peptidestation.com/non-ribosomal-peptides/ [16 Mei 2010].
- ^ [Peptide Station]. 2006c. Digested peptides. [terhubung berkala]. http://www.peptidestation.com/digested-peptides/ [16 Mei 2010].
