Asam heksafluorosilikat
| |

| |
| Nama | |
|---|---|
| Nama IUPAC (preferensi)
Asam heksafluorosilikat | |
| Nama IUPAC (sistematis)
Dihidrogen heksafluorosilikat | |
| Nama lain
Asam fluorosilikat
| |
| Penanda | |
Model 3D (JSmol)
|
|
| 3DMet | {{{3DMet}}} |
| ChemSpider | |
| Nomor EC | |
PubChem CID
|
|
| Nomor RTECS | {{{value}}} |
| Nomor UN | 1778 |
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| F6H2Si | |
| Massa molar | 144,09 g·mol−1 |
| Penampilan | transparan, tidak berwarna, cairan menguap |
| Bau | asam, tajam |
| Densitas | 1.22 g/cm3 (25% soln.) 1.38 g/cm3 (35% soln.) 1.46 g/cm3 (larutan 61%) |
| Titik lebur | ca. 19 °C (66 °F; 292 K) (60–70% solution) < −30 °C (−22 °F; 243 K) (larutan 35%) |
| Titik didih | 1.085 °C (1.985 °F; 1.358 K) (berdekomposisi) |
| Dapat dicampur | |
| Indeks bias (nD) | 1.3465 |
| Struktur | |
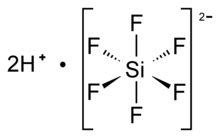
| Octahedral SiF62− | |
| Bahaya | |
| Lembar data keselamatan | External MSDS |
Klasifikasi UE (DSD) (usang)
|
|
| Frasa-R | R34, R25 |
| Frasa-S | (S1/2), S26, S27, S45 |
| Titik nyala | Tidak mudah terbakar |
| Dosis atau konsentrasi letal (LD, LC): | |
LD50 (dosis median)
|
430 mg/kg (mulut, tikus) |
| Senyawa terkait | |
Kation lainnya
|
Amonium heksafluorosilikat |
Senyawa terkait
|
Asam heksafluorofosfat asam fluoroborat |
Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). | |
| Referensi | |
Asam heksafluorosilikat adalah senyawa anorganik dengan rumus kimia (H3O)2SiF6 (juga ditulis (H3O)2[SiF6]). Asam ini merupakan cairan tak berwarna dengan bau yang tajam. Asam ini dihasilkan secara alami dalam jumlah besar di gunung berapi.[1][2] Asam ini diproduksi sebagai pendahulu aluminium trifluorida dan kriolit sintetik. Asam ini sering digunakan sebagai sumber fluorida dalam proses fluoridasi air.[3][4] Garam yang berasal dari asam heksafluorisilikat disebut "heksafluorosilikat".
Dalam larutan berair, kation hidronium (H3O+) biasanya disamakan dengan proton yang mengalami solvasi, sehingga senyawa ini juga dapat ditulis dengan rumus H2SiF6.
Keamanan[sunting | sunting sumber]
Asam heksafluorosilikat dapat mengeluarkan hidrogen fluorida saat mengalami penguapan, sehingga asam ini cukup berbahaya. Uapnya jika dihirup dapat memicu edema paru-paru. Seperti hidrogen fluorida, asam ini dapat mengkorosikan kaca dan alat keramik.[5]
Referensi[sunting | sunting sumber]
- ^ Palache, C., Berman, H., and Frondel, C. (1951) Dana’s System of Mineralogy, Volume II: Halides, Nitrates, Borates, Carbonates, Sulfates, Phosphates, Arsenates, Tungstates, Molybdates, etc. John Wiley and Sons, Inc., New York, 7th edition.
- ^ Anthony, J.W., Bideaux, R.A., Bladh, K.W., and Nichols, M.C. (1997) Handbook of Mineralogy, Volume III: Halides, Hydroxides, Oxides. Mineral Data Publishing, Tucson.
- link to bararite Diarsipkan 2016-04-01 di Wayback Machine.
- link to cryptohalite Diarsipkan 2021-12-02 di Wayback Machine.
- ^ "CDC - Water Fluoridation Additives - Engineering Fact Sheet - Community Water Fluoridation - Oral Health". Cdc.gov. Diakses tanggal 2015-03-10.
- ^ The New Zealand Institute of Chemistry (NZIC) - Hydrofluorosilic acid and water fluoridation hydrofluorosilic acid Diarsipkan 2018-01-27 di Wayback Machine..
- ^ "CDC – Fluorosilicic Acid – International Chemical Safety Cards - NIOSH". Cdc.gov. Diakses tanggal 2015-03-10.
