Cairan

Cairan adalah fluida tak termampatkan yang menyesuaikan dengan bentuk wadahnya tetapi mempertahankan volume yang (hampir) konstan tidak tergantung pada tekanan. Dengan demikian, ini adalah salah satu dari empat wujud dasar materi (yang lain adalah padat, gas, dan plasma), dan merupakan satu-satunya keadaan dengan volume yang pasti namun tidak memiliki bentuk yang tetap. Cairan terdiri dari partikel materi dengan vibrasi halus, seperti atom, yang disatukan oleh gaya antarmolekul. Air, sejauh ini, adalah cairan yang paling umum di Bumi. Seperti gas, cairan bisa mengalir dan berbentuk seperi wadahnya. Sebagian besar cairan tak dapat dimapatkan, meski yang lain bisa dimapatkan. Tidak seperti gas, cairan tidak menyebar untuk mengisi setiap ruang wadah, dan mempertahankan densitas dengan cukup konstan. Sifat khas dari wujud cairan adalah tegangan permukaan, yang mengarah pada fenomena pembasahan.
Densitas cairan biasanya mendekati padatan, dan jauh lebih tinggi daripada gas. Oleh karena itu, cair dan padat keduanya disebut benda terkondensasi. Di sisi lain, karena cairan dan gas berbagi kemampuan untuk mengalir, keduanya disebut fluida. Meskipun air berlimpah di Bumi, wujud materi ini sebenarnya adalah yang paling tidak umum di alam semesta yang diketahui, karena keberadaan cairan memerlukan rentang suhu/tekanan yang relatif sempit. Materi yang paling dikenal di alam semesta ada dalam bentuk gas (dengan jejak materi padat yang dapat dideteksi) sebagai awan antarbintang atau dalam bentuk plasma di dalam bintang.
Selayang pandang[sunting | sunting sumber]
Cairan adalah satu dari empat wujud utama materi, bersama dengan padat, gas dan plasma. Cairan adalah fluida. Tidak seperti benda padat, molekul dalam cairan memiliki kebebasan bergerak yang jauh lebih besar. Kekuatan yang mengikat molekul bersama dalam padatan hanya bersifat sementara dalam cairan, memungkinkan cairan mengalir sementara padatan tetap kaku.
Cairan, seperti gas, menampilkan sifat fluida. Cairan dapat mengalir, bayangkan bentuk wadah, dan jika ditempatkan dalam wadah tertutup, akan mendistribusikan tekanan secara merata ke setiap permukaan wadah. Jika cairan diletakkan di dalam kantong, bisa ditekan ke dalam bentuk apapun. Tidak seperti gas, cairan hampir tidak dapat dimampatkan. Ia memiliki volume yang hampir konstan dalam rentang tekanan yang lebar; ia tidak mengembang untuk memenuhi ruang kosong dalam suatu wadah tetapi membentuk permukaannya sendiri, dan tidak selalu mudah bercampur dengan cairan lainnya. Sifat ini membuat cairan cocok untuk aplikasi semacam hidrolik.
Partikel-partikel cairan terikat kokoh tetapi tidak kaku. Mereka mampu bergerak bebas, menghasilkan mobilitas partikel pada tingkat terbatas. Seiring dengan kenaikan suhu, vibrasi molekul meningkat menyebabkan jarak antar molekul bertambah. Ketika cairan mencapai titik didihnya, gaya kohesif yang menyatukan molekul menjadi terputus, dan cairan berubah menjadi gas (kecuali terjadi pemanasan super). Jika suhu turun, jarak antar molekul menjadi semakin dekat. Ketika cairan mencapai titik bekunya, molekul biasanya saling mengunci ke dalam orde spesifik, yang disbut mengkristal, dan ikatan antar mereka menjadi lebih kaku, mengubah cairan menjadi wujud padatnya (kecuali terjadi pendinginan super).
Contoh[sunting | sunting sumber]
Hanya ada dua unsur yang berwujud cairan pada suhu dan tekanan standar: raksa dan brom. Empat unsur lainnya memiliki titik leleh sedikit di atas suhu ruang: fransium, sesium, galium dan rubidium.[1] Paduan logam yang berwujud cairan pada suhu ruang antara lain NaK, logam paduan natrium-kalium, galinstan, dan beberapa amalgam (logam paduan yang melibatkan raksa).
Zat murni yang berwujud cair pada kondisi normal meliputi air, etanol dan banyak pelarut organik lainnya. Air adalah cairan vital dalam kimia dan biologi; ia diyakini merupakan kebutuhan vital untuk keberlangsungan hidup.
Cairan anorganik termasuk air, magma, pelarut tak berair anorganik dan beragam jenis asam.
Cairan sehari-hari yang penting termasuk larutan berair seperti pemutih rumah tangga, campuran lain dari berbagai zat seperti minyak mineral dan bensin, emulsi seperti vinaigrette atau mayones, suspensi seperti darah, dan koloid seperti cat dan susu.
Banyak gas dapat dicairkan dengan pendinginan, menghasilkan cairan seperti oksigen cair, nitrogen cair, hidrogen cair dan helium cair. Tidak semua gas dapat dicairkan pada tekanan atmosfer, misalnya karbon dioksida hanya dapat dicairkan pada tekanan di atas 5,1 atm.
Beberapa materi tidak dapat diklasifikasikan dalam tiga wujud materi klasik; mereka memiliki sifat seperti padat dan seperti cair. Contohnya termasuk kristal cair, yang digunakan pada layar LCD, dan membran biologis.
Sumber biofuel[sunting | sunting sumber]
Cairan memiliki beragam kegunaan, sebagai pelumas, pelarut, dan pendingin. Dalam sistem hidrolik, cairan berfungsi sebagai penghantar daya.
Dalam tribologi, cairan dipelajari tentang sifat-sifatnya sebagai pelumas. Pelumas seperti minyak dipilih karena viskositas dan karakteristik alirannya yang cocok untuk seluruh rentang suhu pengoperasian komponen. Minyak sering digunakan dalam mesin, bak persneling, karya logam, dan sistem hidrolik karena sifat lubrikasinya yang baik.[2]
Banyak cairan digunakan sebagai pelarut, untuk melarutkan padatan atau cairan lain. Larutan banyak digunakan untuk beragam aplikasi, termasuk cat, bahan segel (sealant), dan lem. Nafta dan aseton sering digunakan dalam industri untuk membersihkan minyak, gemuk, dan tar dari suku cadang dan mesin. Cairan tubuh adalah larutan berbasis air.
Surfaktan umum dijumpai dalam sabun dan deterjen. Pelarut seperti alkohol sering digunakan sebagai antimikroba. Mereka dijumpai dalam kosmetik, tinta, dan cairan pewarna laser. Mereka digunakan dalam industri pangan, untuk mengolah, misalnya ekstraksi, minyak sayur.[3]
Cairan cenderung memiliki konduktivitas termal yang lebih baik daripada gas, dan kemampuannya untuk mengalir menjadikan cairan cocok untuk menghilangkan kelebihan panas dari komponen mesin. Panas dapat dihilangkan dengan mengalirkan cairan melalui penukar panas, seperti radiator, atau panas dapat dihilangkan saat cairan menguap.[4] Pendingin air atau glikol digunakan untuk menjaga mesin agar tidak mengalami pemanasan berlebih (overheating).[5] Pendingin yang digunakan dalam reaktor nuklir termasuk air atau logam cair, seperti natrium atau bismut.[6] Lapisan tipis propelan cair digunakan untuk mendinginkan ruang gaya dorong (thrust chamber) roket.[7] Dalam permesinan, air dan minyak digunakan untuk menghilangkan kelebihan panas yang dihasilkan, yang bisa dengan cepat merusak bagian mesin dan perkakas. Selama perspirasi, keringat menghilangkan panas dari tubuh manusia melalui penguapan. Dalam industri pemanasan, ventilasi, dan AC (HVAC), cairan, misalnya air, digunakan untuk memindahkan panas dari satu bagian ke bagian lain.[8]
Cairan adalah komponen utama sistem hidrolik, yang memanfaatkan hukum Pascal untuk menghasilkan daya fluida. Piranti seperti pompa dan kincir air telah digunakan untuk mengubah gerak cairan menjadi kerja mekanis sejak zaman kuno. Minyak ditekan melalui pompa hidrolik, yang mengalirkan gaya ke tabung hidrolik. Hidrolik dapat dijumpai dalam banyak aplikasi, seperti rem dan transmisi kendaran, alat berat, dan sistem pengendali pesawat terbang. Beragam pengempa hidraulik digunakan secara luas dalam perbaikan dan manufakturing, untuk mengangkat, mengempa, menjepit dan membentuk.[9]
Cairan kadang-kadang digunakan dalam alat ukur. Termometer sering menggunakan ekspansi termal cairan, misalnya raksa, digabung dengan kemampuan mengalirnya untuk menunjukkan suhu. Manometer menggunakan berat cairan untuk mengukur tekanan udara.[10]
Sifat mekanis[sunting | sunting sumber]
Volume[sunting | sunting sumber]
Kuantitas cairan diukur dalam satuan volume. Ini meliputi satuan SI meter kubik (m3) beserta turunannya, terutama desimeter kubik, yang lebih umum disebut sebagai liter (1 dm3 = 1 L = 0,001m3), dan sentimeter kubik, yang juga disebut mililiter (1 cm3 = 1 mL = 0,001 L = 10−6 m3).
Volume cairan adalah fungsi dari suhu dan tekanan. Cairan biasanya memuai ketika dipanaskan, dan menyusut ketika didinginkan. Air pada suhu antara 0 °C dan 4 °C adalah pengecualian. Cairan memiliki sedikit kompresibilitas. Air, misalnya, hanya 46,4 bagian per jutanya yang akan terkompresi untuk setiap satuan kenaikan tekanan atmoser (bar).[11] Pada tekanan sekitar 4.000 bar (58.000 psi), pada suhu ruang, air hanya mengalami penurunan volume sebesar 11%.[12] Dalam studi dinamika fluida, cairan sering diperlakukan sebagai tak termampatkan, terutama ketika mempelajari aliran tak termampatkan. Sifat tak termampatkan membuat cairan cocok untuk menyalurkan daya hidrolik, karena sangat sedikit energi yang hilang dalam bentuk kompresi.[12] Namun, kompresibilitas yang sangat kecil memang menyebabkan fenomena lain. Benturan pada pipa, yang disebut palu air (water hammer), terjadi saat katup tiba-tiba ditutup, menciptakan lonjakan tekanan yang sangat besar pada katup yang bergerak berbalik arah melalui sedikit di bawah kecepatan suara. Fenomena lain yang disebabkan oleh ketaktermampatkan cairan adalah kavitasi. Oleh karena cairan memiliki sedikit elastisitas, mereka benar-benar dapat ditarik hingga terpisah di daerah dengan turbulensi tinggi atau perubahan arah yang dramatis, seperti tepi jejak baling-baling perahu atau sudut tajam pada pipa. Cairan di daerah bertekanan rendah (vakum) menguap dan membentuk gelembung, yang kemudian runtuh saat memasuki daerah bertekanan tinggi. Hal ini menyebabkan cairan mengisi rongga yang ditinggalkan oleh gelembung dengan kekuatan lokal yang luar biasa, mengikis permukaan padat yang berdekatan.[13]
Tekanan dan gaya apung[sunting | sunting sumber]
Dalam medan gravitasi, cairan memberikan tekanan pada sisi wadah dan juga pada apa pun di dalam cairan itu sendiri. Tekanan ini ditransmisikan ke segala arah dan meningkat seiring dengan kedalaman. Jika cairan diam di medan gravitasi yang seragam, tekanan, p, pada kedalaman apapun, z, diberikan oleh
dengan:
- adalah densitas cairan (diasumsikan konstan)
- adalah percepatan gravitasi.
Perhatikan bahwa rumus ini mengasumsikan bahwa tekanan pada permukaan bebas adalah nol, dan efek tegangan permukaan dapat diabaikan.
Benda yang direndam dalam cairan tunduk pada fenomena gaya apung (buoyancy). (Gaya apung juga teramati pada fluida lainnya, tetapi sangat kuat pada cairan karena densitasnya yang tinggi.)
Permukaan[sunting | sunting sumber]

Permukaan cairan, tempat munculnya tegangan permukaan, berperilaku seperti selaput elastis, sehingga memungkinkan pembentukan tetesan dan gelembung. Gelombang permukaan, aksi kapiler, pembasahan, dan riak adalah konsekuensi lain dari tegangan permukaan. Dalam cairan terkurung (confined liquid), yang didefinisikan berdasarkan batasan geometris pada skala nanoskopis, sebagian besar molekul merasakan beberapa efek permukaan, yang dapat mengakibatkan sifat fisik yang terlalu menyimpang dari cairan curah.
Permukaan bebas[sunting | sunting sumber]
Permukaan bebas adalah permukaan fluida yang terkena tekanan nol baik tegak lurus normal maupun geser paralel, seperti batas antara, misalnya, air dan udara di atmosfer bumi.
Muka cairan[sunting | sunting sumber]
Muka cairan (seperti pada, misalnya, muka air) adalah ketinggi permukaan bebas cairan, khususnya yaitu permukaan paling atas. Muka cairan dapat diukur menggunakan level sensor.
Aliran[sunting | sunting sumber]

Viskositas mengukur resistensi cairan terhadap deformasi akibat tekanan geser[14] maupun tekanan eksternal. Dengan kata lain, viskositas adalah resistensi cairan untuk mengalir.[15]
Ketika cairan mengalami pendinginan super menuju transisi kaca, viskositasnya mengalami peningkatan dramatis. Cairan kemudian menjadi medium viskoelastis yang menunjukkan elastisitas layaknya benda padat sekaligus fluiditas layaknya cairan, tergantung pada skala waktu pengamatan atau frekuensi perturbasi.
Perambatan bunyi[sunting | sunting sumber]
Kecepatan suara dalam fluida dinyatakan melalui persamaan
dengan K adalah modulus kompresi fluida, dan ρ adalah densitas. Dalam air tawar, c = 1497 m/s pada 25 °C
Termodinamika[sunting | sunting sumber]
Transisi fase[sunting | sunting sumber]

Pada suhu di bawah titik didih, sembarang materi berbentuk cairan akan menguap sampai kondensasi gas di atasnya mencapai kesetimbangan. Pada titik ini, gas akan terkondensasi dengan laju yang sama dengan laju penguapan cairannya. Jdi, cairan tidak dapat terus ada jika cairan yang menguap dihilangkan secara kontinu. Cairan pada titik didihnya akan menguap lebih cepat daripada kondensasi gasnya pada tekanan yang berlaku. Cairan pada atau di atas titik didihnya normalnya akan mendidih, meskipun pemanasan super dapat mencegah hal ini dalam situasi tertentu.
Pada suhu di bawah titik bekunya, cairan akan cenderung mengkristal, berubah bentuk menjadi padat. Tidak seperti transisi menjadi gas, tidak ada kesetimbangan pada transisi ini di bawah tekanan konstan, sehingga cairan akhirnya akan benar-benar mengkristal, kecuali terjadi pendinginan super. Perlu dicatat bahwa hal ini hanya benar di bawah tekanan konstan, jadi, seumpama air dan es yang berada di dalam wadah kuat yang tertutup rapat dapat mencapai kesetimbangan pada kedua fase yang terdapat bersamaan. Untuk transisi sebaliknya dari padat ke cair, lihat pencairan.
Cairan di ruang angkasa[sunting | sunting sumber]
Diagram fase menjelaskan alasan cairan tidak terdapat dalam ruang angkasa atau media vakum lainnya. Oleh karena tekanannya nol (kecuali pada permukaan atau bagian dalam planet dan bulan), air dan cairan lainnya yang terpapar ruang akan segera mendidih atau membeku bergantung pada suhunya. Di daerah ruang angkasa di dekat bumi, air akan membeku jika tidak terkena sinar matahari langsung dan menguap (menyublim) segera setelah terkena sinar matahari. Jika air berada sebagai es di bulan, ia hanya ada di lubang-lubang bayangan di mana matahari tidak pernah bersinar dan di tempat-tempat yang dikelilingi bebatuan yang tidak cukup untuk memanaskannya. Di beberapa titik di dekat orbit Saturnus, sinar matahari terlalu lemah untuk menyublimkan es menjadi uap air. Ini terbukti dari panjangnya umur es yang membentuk cincin Saturnus.
Larutan[sunting | sunting sumber]
Cairan dapat menunjukkan ketakcampuran. Campuran dua cairan yang tak saling campur, yang cukup akrab dalam keseharian kita, adalah minyak dan air[16] pada sup atau makanan berkuah lainnya. Sementara kita juga cukup akrab dengan campuran dua cairan yang saling campur seperti air dan alkohol.[16] Komponen cairan dalam campuran dapat dipisahkan satu sama lain melalui distilasi fraksional.
Sifat mikroskopik[sunting | sunting sumber]
Faktor struktur statik[sunting | sunting sumber]
Dalam cairan, atom-atom tidak membentuk kisi kristal maupun menunjukkan bentuk orde jangkau jauh. Hal ini dibuktikan dengan tidak adanya puncak Bragg pada difraksi sinar-X maupun neutron. Di bawah kondisi normal, pola difraksi memiliki simetri sirkular, menunjukkan isotropi cairan. Pada arah radial, intensitas difraksi berosilasi dengan lancar. Ini biasanya dijelaskan sebagai faktor struktur statis S(q), dengan bilangan gelombang
pada panjang gelombang λ dari kuar (probe) (foton atau neutron) dan sudut Bragg θ. Osilasi S(q) menyatakan orde dekat cairan, yaitu korelasi antara atom dan beberapa kelopak dari tetangga terdekat, kedua terdekat, ...
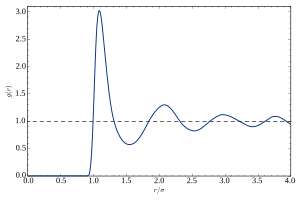
Penjelasan korelasi ini yang lebih intuitif diberikan oleh fungsi distribusi radial g(r), yang berdasarkan pada transformasi Fourier S(q). Ia menyajikan rata-rata spasial korelasi pasangan dalam cairan.
Dispersi suara dan relaksasi struktural[sunting | sunting sumber]
Persamaan di atas tentang kecepatan suara mengandung modulus kompresi K. Jika K tidak tergantung frekuensi maka cairan berperilaku seperti media linier, sehingga suara merambat tanpa disipasi dan tanpa penggandengan mode. Pada kenyataannya, cairan menunjukkan beberapa dispersi: dengan kenaikan frekuensi, K berpindah silang dari frekuensi rendah, (batas cairan, ) ke frekuensi tinggi (batas padat, ). Dalam cairan normal, sebagian besar pelintasan ini terjadi pada frekuensi antara GHz dan THz., kadang-kadang disebut hipersonik.
Pada frekuensi sub-GHz, cairan normal mempertahankan gelombang s: batas frekuensi 0 modulus geser adalah . Hal ini kadang-kadang dilihat sebagai sifat definitif cairan.[17][18] Namun, seperti modulus kompresi K, modulus geser G tergantung pada frekuensi, dan pada frekuensi hipersonik ia menunjukkan perpindahan silang yang mirip, dari batas seperti cairan ke batas seperti padatan, .
Menurut fungsi respon linier, transformasi Fourier K atau G menggambarkan cara sistem kembali ke kesetimbangan setelah perturbasi eksternal; untuk alasan ini, tahap dispersi dalam wilayah GHz...THz disebut relaksasi struktural. Menurut teorema fluktuasi-disipasi, relaksasi menuju kesetimbangan berhubungan erat dengan fluktuasi pada kesetimbangan. Fluktuasi densitas berkaitan dengan gelombang suara dapat diamati secara eksperimental melalui hamburan Brillouin.
Pada cairan superdingin menuju transisi kaca, pindah silang respon dari seperti cairan ke seperti padatan bergerak dari GHz ke MHz, kHz, Hz, ...; secara ekuivalen, waktu karakteristik relaksasi struktural meningkat dari μs, ms, s, ... Ini adalah penjelasan mikroskopis untuk perilaku viskoelastis cairan pembentuk kaca yang disebutkan di atas.
Lihat pula[sunting | sunting sumber]
Referensi[sunting | sunting sumber]
- ^ Theodore Gray, The Elements: A Visual Exploration of Every Known Atom in the Universe New York: Workman Publishing, 2009 p. 127 ISBN 1-57912-814-9
- ^ Theo Mang, Wilfried Dressel ’’Lubricants and lubrication’’, Wiley-VCH 2007 ISBN 3-527-31497-0
- ^ George Wypych ’’Handbook of solvents’’ William Andrew Publishing 2001 pp. 847–881 ISBN 1-895198-24-0
- ^ N. B. Vargaftik ’’Handbook of thermal conductivity of liquids and gases’’ CRC Press 1994 ISBN 0-8493-9345-0
- ^ Jack Erjavec ’’Automotive technology: a systems approach’’ Delmar Learning 2000 p. 309 ISBN 1-4018-4831-1
- ^ Gerald Wendt ’’The prospects of nuclear power and technology’’ D. Van Nostrand Company 1957 p. 266
- ^ ’’Modern engineering for design of liquid-propellant rocket engines’’ by Dieter K. Huzel, David H. Huang–American Institute of Aeronautics and Astronautics 1992 p. 99 ISBN 1-56347-013-6
- ^ Thomas E Mull ’’HVAC principles and applications manual’’ McGraw-Hill 1997 ISBN 0-07-044451-X
- ^ R. Keith Mobley Fluid power dynamics Butterworth-Heinemann 2000 p. vii ISBN 0-7506-7174-2
- ^ Bela G. Liptak ’’Instrument engineers’ handbook: process control’’ CRC Press 1999 p. 807 ISBN 0-8493-1081-4
- ^ Compressibility of Liquids
- ^ a b Wenwu Zhang (2011), Intelligent Energy Field Manufacturing: Interdisciplinary Process Innovations, CRC Press, hlm. 144
- ^ Gupta, S.C. (2006), Fluid Mechanics and Hydraulic Machines, Dorling-Kindersley, hlm. 85
- ^ Denton, Philip; Rostron, Chris (2013-07-25). Pharmaceutics: The Science of Medicine Design (dalam bahasa Inggris). OUP Oxford. ISBN 9780199655311.
- ^ Kulkarni, Vitthal S.; Shaw, Charles (2015-10-15). Essential Chemistry for Formulators of Semisolid and Liquid Dosages (dalam bahasa Inggris). Academic Press. ISBN 9780128010723.
- ^ a b Kelly, Theresa M. (2013-03-18). Quantum Psychics - Scientifically Understand, Control and Enhance Your Psychic Ability (dalam bahasa Inggris). Lulu.com. ISBN 9780557034031.
- ^ Born, Max (1940). "On the stability of crystal lattices". Mathematical Proceedings. Cambridge Philosophical Society. 36 (2): 160–172. Bibcode:1940PCPS...36..160B. doi:10.1017/S0305004100017138.
- ^ Born, Max (1939). "Thermodynamics of Crystals and Melting". Journal of Chemical Physics. 7 (8): 591–604. Bibcode:1939JChPh...7..591B. doi:10.1063/1.1750497. Diarsipkan dari versi asli tanggal 2016-05-15.











